Галогены и их соединения
реклама

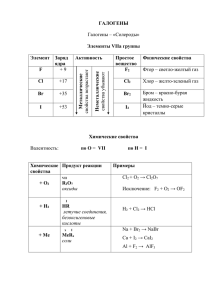
Галогены и их соединения. Задачи: 1.Выявить особенности строения атомов галогенов и их химических свойств. 2.Сформировать умение делать умозаключения. Ход урока Химически й символ Соединения галогенов Фтор - HF-плавиковая к-та CaF2-плавиковый шпат Na3AlF6-криолит CF2Cl2- фреон NaCl HClO-хлорноватистая HClO2-хлористая HClO3-хлорноватая HClO4- хлорная NaBr KBr LiBr KI Хлор - Бром - Иод - Состав ядра атома Р= е= n= Строение эл. Степень оболочки окисления галогенов Р= е= n= Р= е= n= Р= е= n= ПОЛУЧЕНИЕ: NaCl + H2SO4 = Химическая активность: F2 → Cl2 →Br2 →I2 HF CaF2 Na3AlF6 CF2Cl2 NaCl HClO HClO2 HClO3 HClO4 NaBr KBr LiBr KI Химические свойства Качественные реакции F2 + → F2 +H2 → 2F2 + 2H2O → 4HF + O2 NaF + AgNO3 → Cl2 + Fe → NaCl + AgNO3 → Cl2 + H2 → Br 2+ Cu → Br 2+ H2 → NaBr + AgNO3 → I2 + Al → I2 + H2 → NaI + AgNO3 → 4HCl + MnO 2 = MnCl2 + Cl2 + H2O