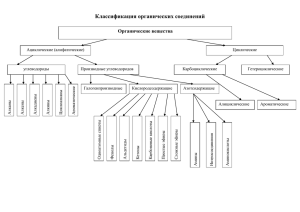
Производные п-аминобензойной килоты В медицинской практике в качестве местноанестезирующих средств широко применяются лекарственные средства производные п-аминобензойной кислоты, являющие по структуре сложными эфирами. Местоанестезирующие вещества поражают окончания чувствительных нервов и, в отличие от наркотических веществ, не действуют на ЦНС и не вызывают общего наркоза. Их применение приводит к потере чувствительности, а затем обезболиванию тканей в ограниченной части тела, в которую введено вещество. При этом сознание человека сохраняется, в отличие от наркоза, при котором наступает полная потеря сознания. Применение местноанестезирующих средств стало важным достижением фармакотерапии, так как позволило проводить хирургические вмешательства без применения общего наркоза. Это имеет важное значения при операциях, когда применение общего наркоза невозможно. Предпосылкой создания этой группы лекарственных средства явилась попытка найти аналоги алкалоида кокаина, обладающего местноанестезирущим эффектом, но вызывающего наркотическую зависимость. При изучении химической структуры производных кокаина и их фармакологического действия было установлено, что местноанестезирующий эффект обусловлен не всей молекулой кокаина, а отдельным структурным элементом – анестезиофорной группой (в структуре кокаина выделена овалом): O C O CH3 O N CH3 O C Общая формула производных сложных эфиров п-аминобензойной кислоты имеет следующий вид: O R NH C O К ним относятся бензокаин, прокаин и тетракаин. Бензокаин. Benzocainum. Анестезин. NH2 CH2 CH2 N R1 R2 Белый кристаллический порошок без запаха, слабо горькогоквуса. Вызывает на языке чувство онемения. Очень мало растворим в воде, легко растворим в спирте, эфире, хлороформе, умеренно растворим в жирных маслах и разведенной соляной кислоте. O C O C2H5 Этиловый эфир п-аминобензойной кислоты. С9H11NO2, М.м. 165,19 Прокаин. Procainum. Новокаин. NH2 . O C O CH2 CH2 N HCl Бесцветные кристаллы или белый кристаллический порошок, без запаха, горького вкуса. На языке вызывает чувство онемения. Очень легко растворим в воде, легко растворим в спирте, мало растворим в хлороформе, практически нерастворим в эфире. C2H5 C2H5 -диэтиламиноэтилового эфира паминобензойной кислоты гидрохлорид С13H20N2O2HCl, М.м. 272,78 Тетракаин. Tetracainum. Дикаин. Белый кристаллический порошок без запаха. NH Легко растворим в воде и спирте, умеренно растворим в хлороформе, практически нерастворим в эфире. C4H9 . HCl O C O CH2 CH3 N CH2 CH3 -диметиламиноэтилового эфира п-бутиламинобензойной кислоты гидрохлорид С15H24N2O2HCl, М.м. 300,83 Получение Исходным продуктом для синтеза сложных эфиров п-аминобензойной кислоты служит пнитробензойная кислота, которую получают окислением п-нитротолуола хромовой смесью. Для получения бензокаина п-нитробензойную кислоту ацелируют этанолом и затем восстанавливают нитрогруппу до аминогруппы: NO2 NH2 NO2 NH2 Fe C2H5OH K2Cr2O7 HCl H2SO4 O O CH3 O C C C O OH O C2H5 C2H5 Прокаин получают переэтерификацией бензокаина -диэтиламиноэтанолом в присутствии алкоголята натрия: NH2 HO CH2 CH2 N C2H5 O C2H5 HCl O O C C O . HCl C2H5 C2H5ONa O NH2 NH2 CH2 N CH2 C C2H5 O C2H5 CH2 CH2 N C2H5 C2H5 Синтез тетракаина проводится из п-аминобензоата натрия после алкилирования первичной аминогруппы бутилбромидом и этерефикации диметиламиноэтанолом: HO CH2 C4H9Br O C ONa NH C4H9 NH NH2 O C ONa CH2 N C4H9 CH3 HCl CH3 òåòðàêàèí C2H5ONa O C O CH2 CH2 N CH3 CH3 Качественный анализ Функциональные группы. Первичная и вторичная ароматические аминогруппы, третичный атом азота, сложноэфирная группа, связанная хлороводородная кислота. Химические свойства. Бензокаин и прокаин проявляют основные свойства за счет первичной ароматической аминогруппы, при этом основные свойства прокаина выражены сильнее за счет наличия третичного атома азота. Тетракаин также проявляет основные свойства, обусловленные третичным атомом азота и вторичной аминогруппой. Прокаин и тетракаин являются солью, образованной слабым основанием и сильной кислотой. В водной среде подвергаются гидролизу, реакция среды при этом изменяется в кислую сторону. Лекарственные вещества с первичной ароматической аминогруппой относительно легко окисляются с образованием окрашенных в различный цвет продуктов окисления. Ароматическая аминогруппа является ориентантом первого рода и в реакциях электрофильного замещения будет направлять вновь входящий заместитель в орто- и пара-положения. Наличие сложноэфирной группы обуславливает протекание реакции гидролитического разложения в кислой и щелочной средах. Физико-химические методы Подлинность лекарственных средств можно установить по температуре плавления, по идентичности ИК-спектров, снятых после прессования в таблетках калия бромида в области 4000-400 см1 и прилагаемых к ФС рисунков спектров стандартных образцов. УФ-спектры испытуемых лекарственных средств должны иметь полосы поглощения, приведенные в соответствующих ФС. Химические реакции подлинности 1. По ароматической аминогруппе: 1.1. Реакция образования азокрасителя. При действии на бензокаин и прокаин нитритом натрия в кислой среде образуется соль диазония, которая вступает в реакцию азосочетания с образованием азокрасителя (красное окрашивание). В качестве азосоставляющей применяются фенолы (фенол, резорцин, -нафтол) в слабощелочной среде или ароматические амины (анилин) в слабокислой среде. Процесс азосочетания обусловлен наличием в этих соединениях электронодонорных –OH и –NH2-групп, создающих частично отрицательные заряды в орто- и пара-положениях ароматического ядра. В этих положениях происходит электрофильное замещение водорода катионом диазония и образуется азосоединение.Азосочетание с фенолами протекает по схеме: + N NH2 NaNO2 OH N N ONa . Cl HCl R N NaOH R êðàñí î å î êðàø èâàí èå R Азосочетание с ароматическими аминами (анилин, N-(1-нафтил)этилендиамин) в кислой среде протекает по схеме: + N NH2 NaNO2 NH2 N N NH2 . Cl HCl R N R êðàñí î å î êðàø èâàí èå R 1.2. Образование оснований Шиффа с альдегидами (например, п-диметиламинобензальдегидом) в присутствии концентрированной серной кислоты с появлением желтого или оранжевого окрашивания: NH2 N O + C H R N CH3 CH N CH3 CH3 H2SO4 (ê) CH3 R æåëòî å èëè î ðàí æåâî å î êðàø èâàí èå î ñí î âàí èå Ø èô ô à Эта реакция лежит в основе лигниновой пробы, используемой для экспресс-анализа. Она выполняется на древесине или газетной бумаге, при нанесении на которую вещества с первичной ароматической аминогруппой и капли разведенной хлороводородной кислоты появляется оранжевожелтое окрашивание. Суть реакции заключается в том, что из лигнина, содержащегося в газетной бумаге, образуются ароматические альдегиды, которые и вступают в реакцию с образованием оснований Шиффа. 1.3. Реакция конденсации с 2,4-динитрохлорбензолом с образованием соединений (цвитттер-ионов) хиноидной структуры, окрашенных в желто-оранжевый цвет: NH2 _ N + NH NO2 Cl O , NaOH , t O2N O NO2 æåëòî -î ðàí æåâî å î êðàø èâàí èå R R 1.4. Реакция галогенирования (бромирования, йодирования). Реакция электрофильного замещения используется как для обнаружения, так и для количественного определения лекарственных средств с первичной ароматической аминогруппой, при этом выпадает белый осадокдибромпроизводного или желтоватый осадок дийодпроизводного (бром добавляется по каплям, т.к. при избытке брома возможно окисление первичной ароматической аминогруппы). NH2 NH2 Br Br + 2 Br2 _ 2 HBr R R 1.5. Реакции окисления. При действии на подкисленный разведенной хлороводородной кислотой растворбензокаина хлорамином и добавлении эфира, эфирный слой окрашивается в оранжевый цвет. При действии на подкисленный разведенной серной кислотой раствор прокаина перманганатом калия, фиолетовая окраска перманганата калия моментально исчезает. 1.6. Образование изонитрилов – веществ, имеющих тошнотворный запах, под действием хлороформа и спиртового раствора гидроксида натрия: NH2 N C CHCl3 , NaOH R R òî ø í î òâî ðí û é çàï àõ 2. Реакции на сложноэфирную группу. 2.1. Гидроксамовая проба. При взаимодействии с гидроксиламином в щелочной среде образуются гидроксамовые кислоты, после подкисления хлороводородной кислотой и прибавления раствора хлорида железа (III) образуются гидроксаматы железа, имеющие красное окрашивание: NH2 NH2 NH2 NH2OH FeCl3 NaOH C O O HCl C R O NH C OH O NH Fe 3 O красное окрашивание 2.2. Реакция гидролиза в кислой или щелочной среде. Образующие после гидролиза вещества открывают соответствующими реакциями. Так, образующийся при гидролизе бензокаина этиловый спирт открывают по реакции образования йодоформа: NH2 NH2 NaOH C2H5OH + O C COOH O C2H5 C2H5OH + 6NaOH + 4I2 CHI3 + HCOONa + 5NaI + 5H2O запах желтое окрашивание Наличие этоксильной групы в бензокаине можно также подтвердить, действуя уксусной и концентрированной серной кислотой. Образуется этилацетат, обнаруживаемый по характерному запаху: H2SO4 C2H5OH + CH3COOH O H3C C + OC2H5 H2O ô ðóêòî âû é çàï àõ 2.3. Идентифицируя продукты щелочного гидролиза можно также открыть тетракаин: NH NH C4H9 . HCl C4H9 CH2 N CH3 + NaCl CH3 O O C O HO CH2 + + 2 NaOH CH2 CH2 N C CH3 ONa CH3 При подкислении выпадает белый осадок п-бутиламинобензойной кислоты, который растворяется в избытке хлороводородной кислоты: NH NH C4H9 + C4H9 + HCl NaCl O O C C OH ONa Из полученного раствора п-бутиламинобензойной кислоты под действием нитрита натрия выпадает осадок N-нитрозосоединения этой кислоты: N NH O NH C4H9 C4H9 NaNO2 + H2O HCl O C OH O C OH 3. На третичный атом азота. Идентификацию можно провести с помощью общеалкалоидных (осадительных) реактивов: пикриновой кислоты (2,4,6-тринитрофенол) – желтый осадок, фосфорновольфрамовой кислоты (H3PO412WO32H2O – реактив Шейблера) – белый осадок, фосфорномолибденовой кислоты (H3PO412MoO32H2O – реактив Зонненштейна) – бурый или светложелтый осадок, хлорида ртути (II) (HgCl2 – сулема) – белый осадок и других реактивов. 4. Реакции по связанной хлороводородной кислоте в прокаине и тетракаине. 4.1. Хлорид-ион открывают нитратом серебра, при этом выпадает белый творожистый осадок: AgNO3+HCIAgCI + HNO3 белый 4.2. При нейтрализации связанной хлороводородной кислоты щелочью образуются бесцветные маслянистые капли (основание прокаина) или выпадает белый осадок (основание тетракаина), который можно идентифицировать по температуре плавления: NH2 NH2 . NaOH O O C O + NaCl HCl CH2 CH2 N C C2H5 O C2H5 CH2 CH2 N C2H5 C2H5 5. Тетракаин после нагревания досуха с концентрированной азотной кислотой и прибавления к остатку спиртового раствора гидроксида калия приобретает кроваво-красное окрашивание. Реакция основана на его нитровании и последующем образовании калиевой соли орто-хиноидного соединения: C4H9 C4H9 C4H9 NH O NH . HNO3 NO2 O2N KOH O N O O O C C R OK HCl O O + N C2H5OH C O NH + R O R êðî âàâî -êðàñí î å î êðàø èâàí èå Испытания на чистоту В прокаине идентифицируют примесь п-аминобензойной кислоты и бензокаина методом ТСХ. Пятна посторонних примесей на хроматограмме испытуемого раствора, находящиеся на уровне пятен 4аминобензойной кислоты и анестезина, по совокупности величины и интенсивности поглощения не должны превышать соответствующие пятна на хроматограмме раствора сравнения (не более 0,05% каждой примеси). Ввиду того, чтопрокаини тетракаин могутгидролизоваться с изменением рН среды в кислую сторону, то обязательным испытанием является определение рН: 1% раствор прокаина должен иметь рН от 6,0 до 7,5, 1% раствор тетракаина – от 4,5 до 6,0. Так как ароматическая аминогруппа может окисляться, при этом может изменяться не только окраска, но и растворимость, обязательным испытанием на чистоту бензокаина, прокаина и тетракаина является определение прозрачности и цветности их растворов. Количественное определение 1. Нитритометрия. При титровании нитритом натрия в кислой среде бензокаин и прокаин образуют диазосоединения, тетракаин – нитрозосоединение: + N NH2 N KBr . Cl + NaNO2 + 2 HCl R + NaCl + H2O R äèàçî ñî åäèí åí èå C4H9 C4H9 NH N N O KBr + NaNO2 + HCl + NaCl + R H2O R í èòðî çî ñî åäèí åí èå Титрование проводят в присутствии катализатора KBr при пониженной температуре и медленном прибавлении титранта. Точку эквивалентности определяют потенциометрическим методом либо с помощью внутреннего или внешнего индикатора. В качестве внутреннего индикатора используют смесь тропеолина 00 с метиленовым синим, конец титрования определяют по переходу окраски от фиолетовой до светло-голубой. В качестве внешнего индикатора используют йодкрахмальную бумагу, конец титрования определяют по посинению индикаторной бумаги при нанесении на нее капли титруемой смеси: 2NaNO2 + 2KI(крахмал) + 4HClI2(крахмал) + 2NaCl + 2KCl + 2NO + 2H2O Параллельно проводят контрольный опыт. Содержание лекарственного средства (Х,%) в пересчете на сухое вещество рассчитывают по формуле: o. X, áåí çî êàèí à , % = V NaNO ( 2 _ k.o. V NaNO ) K NaNO . T NaNO 2 2 2 . áåí çî êàèí ó 100 a (áåí çî êàèí à) T NaNO 2 áåí çî êàèí ó = Ñ ýêâ ( NaNO2 ) . M ýêâ . 100 100 _ W (áåí çî êàèí à) 1000 fэкв (бензокаина, прокаина, тетракаина) = 1. Мэкв (бензокаина, прокаина, тетракаина) = М (бензокаина, прокаина, тетракаина, соответственно). 2. Прямая броматометрия (бензокаин, прокаин). Титрант – раствор бромата калия. В анализируемый раствор перед его титрованием добавляют калия бромид, который при взаимодействии с калия броматом в кислой среде выделяет свободный бром: KBrO3 + 5KBr + 6HCl 3Br2 + 6KCl + 3H2O Образующийся бром вступает в реакцию электрофильного замещения с анализируемым веществом по первичной ароматической аминогруппе: NH2 NH2 Br Br + 2 Br2 _ 2 HBr R R Титрование ведут до обесцвечивания индикатора – метилового оранжевого. Параллельно проводят контрольный опыт. o. k.o. ( V KBrO3 _ V KBrO3 ) K KBrO3 . T KBrO3 áåí çî êàèí ó . 100 100 X, áåí çî êàèí à , % = T KBrO áåí çî êàèí ó 3 . a (áåí çî êàèí à) = 100 _ W Ñ ýêâ (1/6 KBrO3 ) . M ýêâ ( 1/4 áåí çî êàèí à ) 1000 fэкв (бензокаина, прокаина) = 1/4. Мэкв (1/4бензокаина, прокаина) = М (бензокаина, прокаина)/4. 3. Обратная йодхлорметрия. NH2 NH2 I I + 2 ICl èçáû òî ê + 2 HCl R R ICl +KI I2+ 2KCl I2+ Na2S2O3 2NaI + Na2S4O6 Индикатор – крахмал, добавляют в конце титрования. Параллельно проводят контрольный опыт. o. k.o. _ . . 100 ) ( X, áåí çî êàèí à , % = T Na S O 2 2 3 V Na S O 2 2 3 V Na S O K Na S O TNa S O 2 2 2 3 2 3 2 2 3 áåí çî êàèí ó a (áåí çî êàèí à) áåí çî êàèí ó = Ñ ýêâ ( Na2S 2O3 ) . 100 100 _ W . M ýêâ ( 1/4 áåí çî êàèí à ) 1000 fэкв (бензокаина, прокаина) = 1/4. Мэкв (бензокаина, прокаина) = М (бензокаина, прокаина)/4. 4. Алкалиметрия, аргентометрия, меркуриметрия – по связанной хлороводородной кислоте (прокаин, тетракаин). 5. Кислотно-основное титрование в неводных средах – прокаин, тетракаин. Титруют в ледяной уксусной кислоте в присутствии ацетата ртути по индикатору – кристаллическому фиолетовому. Параллельно проводят контрольный опыт. fэкв (бензокаина, прокаина) = 1. Мэкв (бензокаина, прокаина) = М (бензокаина, прокаина). Физико-химические методы 6. Высоко эффективная жидкостная хроматография (ВЭЖХ). Количественное определение проводят с использованием внешнего стандарта. Хроматографируют испытуемый и стандартный растворы, содержание лекарственного средства (X, %) в пересчете на сухое вещество рассчитывают по формуле: X, áåí çî êàèí à , % = S õ . à ñò . Ð S ñò . à õ . где Sxи Sст – площади пиков испытуемого и стандартного веществ, ах и аст – масса навески испытуемого и стандартного веществ, Р – содержание основного вещества в стандартном образце, W – потеря в массе при высушивании. 100 100 _ W 7. Спектрофотометрия (СПФ). При проведении количественного анализа с использованием стандартного образца расчеты проводят по формуле: X, áåí çî êàèí à , % = A õ . à ñò . Ð A ñò . à õ . 100 100 _ W где Axи Aст – оптическая плотность испытуемого и стандартного веществ, ах и аст – масса навески испытуемого и стандартного веществ, Р – содержание основного вещества в стандартном образце, W – потеря в массе при высушивании. Если количественное определение проводят с использованием удельного показателя поглощения, расчеты проводят по формуле: X, áåí çî êàèí à , % = Aõ . b . àõ E 1% 1 ñì . 100 100 _ W где Ax – оптическая плотность испытуемого вещества, ах – масса навески испытуемого вещества, b – разведение, W – потеря в массе при высушивании. Хранение Лекарственные средства хранят в хорошо укупоренной таре, предохраняющей от действия света, в банках из оранжевого стекла. При несоблюдении условий хранения возможно протекание процессов гидролиза, окисления. Применение Местноанестезирующие средства. Бензокаин мало всасывается с поверхности кожи и слизистых оболочек, используется для обезболивания наружных язв, при зуде, для анестезии слизистой оболочки желудка. Применяется чаще всего в сложных лекарственных формах, редко в таблетках по 0,3 г и 5% мази как однокомпонентные лекарственные формы.Прокаин применяется для спинномозговой и инфильрационной анестезии в виде 0,25% и 0,5% водных растворов. Тетракаин активнее прокаина, но и токсичнее его в 10 раз. Назначают главным образом для поверхностной анестезии в глазной и отоларингологической практике в виде 0,5-2% растворов, а также для перидуральной анестезии в виде 0,3% растворов. Производные амида п-аминобензойной кислоты Прокаинамид. Procainamidum. Новокаинамид. Белый или белый со слегка кремоватым оттенком кристаллический порошок, без запаха. Очень легко растворим в воде, легко растворим в спирте, мало растворим в хлороформе, практически нерастворим в эфире. NH2 . HCl O C NH CH2 CH2 N C2H5 C2H5 -диэтиламиноэтиламидап-аминобензойной кислоты гидрохлорид С13H21N3OHCl, М.м. 271,79 Метоклопрамид. Metoclopramidum.Церукал. Белый или белый с желтоватым или кремоватым оттенком кристаллический порошок без запаха или почти без запаха. Очень легко астворим в воде, лего растворим в спирте, умеренно растворим в хлороформе. NH2 Cl . HCl . H O 2 O O CH3 C NH CH2 CH2 N C2H5 C2H5 4-амино-N-[2-(диэтиламино)этил]-2-метокси-5хлорбензамида гидрохлорида моногидрат М.м. 299,80 Получение Прокаинамид получают по схеме: O Cl CH2 CH2 N NH3 C2H5 H2N C2H5 NO2 C2H5 N CH2 CH2 C O2N Cl C2H5 NH2 . H . HCl HCl Ni O O C NH CH2 CH2 N C C2H5 NH CH2 CH2 C2H5 N C2H5 C2H5 При получении метоклопрамида вместо хлорангидрида п-нитробензойной кислоты берут хлорангидрид 2-метокси-5-хлор-п-нитробензойной кислоты: Cl O O2N C Cl O CH3 Качественный анализ Химические свойства обусловлены наличием первичной ароматической аминогруппы, третичного атома азота, амидной группы, ковалентно связанного хлора, связанной хлороводородной кислоты. Идентификация физико-химическими методами проводится по температуре плавления, спектрофотометрически, ИК-спектроскопией, ВЭЖХ по времени удерживания пиков испытуемого и стандартного растворов. Химические реакции подлинности 1. По ароматической аминогруппе: реакции образования азокрасителя, оснований Шиффа, лигниновая проба, галогенирование, окисление ванадатом аммония в сернокислой среде – вишнево-красное окрашивание. 2. По третичному атому азота: реакции с общеалкалоидными реактивами. 3. По амидной группе: гидроксамовая проба, гидролитическое разложение: NH2 NH2 NH2 . NaOH , t HCl + H2N O O C NH CH2 CH2 N C2H5 C2H5 C ONa CH2 CH2 N C2H5 HCl C2H5 O C OH Òï ëàâë. 4. Метоклопрамид – по ковалетно связанному хлору. 4.1. Проба Бейльштейна. 4.2. Минерализация после предварительного отделения связанной хлороводородной кислоты. Минерализацию можно провести сжиганием в колбе с кислородом, нагреванием со смесью для спекания, сплавлением с металлическим натрием, нагреванием с цинковой пылью в кислой или щелочной среде. Образующиеся хлорид-ионы открывают нитратом серебра. Испытания на чистоту Наличие посторонних примесей устанавливают методом ТСХ (не более 1%), рН, прозрачность и цветность. Количественное определение 1. Нитритометрия. 2. Неводное титрование в ледяной уксусной кислоте в присутствии ацетата ртути. 3. Прокаинамид – броматометрия, обратная йодхлорметрия. 4. По связанной хлороводородной кислоте. 5. Прокаинамид – броматометрия, обратная йодхлорметрия. 6. Физико-химические методы: СПФ, ВЭЖХ. Хранение Хранят в хорошо укупоренной таре, в сухом, защищенном от света месте, чтобы не допустить гидролиза. Метоклопрамид хранят при температуре не выше 25 С. Применение Применяется прокаинамид как антиаритмическое средство, принимают внутрь, вводят внутривенно или внутримышечно. Выпускается в таблетках по 250 мг и в виде 10% раствора в ампулах. Метоклопрамид применяется внутрь или внутримышечно как противорвотное средство, снимает приступ икоты. Выпускается в виде таблеток по 5 мг, 10 мг или в виде 0,1% раствора дляприем внутрь и 0,5% раствора для инъекций