Руководство является фундаментальным тру­
дом, обобщающим современные достижения
в хирургии легких и плевры.
В книге изложены вопросы хирургической ана­
томии и клинической физиологии органов ды­
хания, знание которых необходимо в лечении
больных пульмонологического профиля. При­
ведены подробные данные об этиологии, пато­
генезе, клиническом течении заболеваний лег­
ких и плевры, рассмотрены показания и проти­
вопоказания к хирургическому лечению боль­
ных, наиболее существенные детали оператив­
ной техники. Особое внимание уделено острым
гнойно-деструктивным поражениям легких,
эмпиеме плевры, бронхоэктазиям, раку и дру­
гим опухолям, которые занимают в настоящее
время ведущее место в структуре хирургиче­
ских заболеваний дыхательной системы. До­
статочно полно приводятся также сведения
о других, менее часто встречающихся болез­
нях — врожденной патологии, паразитарных,
грибковых поражениях.
Существенное место отведено в руководстве
проблеме обеспечения безопасности оператив­
ных вмешательств на легких и плевре — предо­
перационной подготовке больных, анестезиоло­
гическому пособию, реаниматологии, профи­
лактике и лечению послеоперационных ослож­
нений. •
Руководство иллюстрировано оригинальными
рисунками и рентгенограммами.
Книга предназначена для хирургов, реанима­
тологов, терапевтов, рентгенологов и врачей
других специальностей, имеющих отношение
к диагностике и лечению больных хирурги­
ческими заболеваниями легких и плевры.
ХИРУРГИЯ
ЛЕГКИХ
И ПЛЕВРЫ
РУКОВОДСТВО ДЛЯ ВРАЧЕЙ
Под редакцией
академика АМН СССР И. С. Колесникова
и профессора М. И. Лыткина
Ленинград «Медицина» Ленинградское отделение 1988
ББК 54.5
Х50
УДК 616.24+616.25 [-089 (035)
Рецензент: академик АМН СССР зав. кафедрой хирургии I ЛМИ им. акад. И. П. Пав­
лова Углов Ф. Г.
Хирургия легких и плевры: Руководство для врачей / Под
Х50 ред. И. С. Колесникова, М. И. Лыткина.— Л.: Медицина, 1988.— 384 с.:
ил., [3] л. ил.
ISBN 5—225—01655—3
В руководстве освещены вопросы оперативной хирургии, топографической анатомии
легких и плевры, а также клинической физиологии легких. Рассмотрены клиника, течение,
диагностика хирургических заболеваний легких и плевры, показания к оперативному лечению,
степень оперативного риска.
4113000000-048
174-87
039(00-88
ISBN 5—225—01655—3
ББК 54.5
(g Издательство «Медицина», Москва, 1988 г.
ОГЛАВЛЕНИЕ
CONTENTS
Предисловие
.....................
......................................
Глава 1. Хирургическая анатомия легких (акад.
И. С. Колесников)................................................................
Глава 2. Клиническая физиология легких и плевры
(д-р мед. наук А. Л. Костюченко, канд. мед. наук
B. И. Буравцов)
.................................................................
56
Глава 3. Общие принципы обследования больных
заболеваниями легких и плевры (д-р мед. наук
C. А. Шалаев, д-р мед. наук А. Л. Костюченко, канд.
мед. наук Б. К. Савченко, канд. мед. наук Ю. А. По­
пов) ...........................................................................................
80
Глава 4. Подготовка больных к операции (д-р мед.
наук А. Л. Костюченко, д-р мед. наук С. А. Шалаев,
д-р мед. наук Л. С. Лесницкий)......................................
111
Глава 5. Аномалии развития легких (проф. М. И. Лыт­
кин, канд. мед. наук Ю. А. Попов, канд. мед. наук
Ю. Л. Шевченко)................................................................
119
Глава 6. Острые абсцессы и гангрена легких (акад.
И. С. Колесников, проф. М. И. Лыткин, д-р мед.
наук Л. С. Лесницкий, канд. мед. наук Б. К. Савченко)
Глава 7. Хронические абсцессы легких (акад.
И. С. Колесников , проф. М. И. Лыткин, д-р мед. наук
Л. С. Лесницкий) .................................................................
Глава 8. Острая эмпиема плевры и пиопневмоторакс (акад. И. С. Колесников, проф. М. И. Лыткин,
канд. мед. наук Г. С. Чепчерук, д-р мед. наук Л. С. Лес­
ницкий, С. В. Гришаков) ......
.
Глава 9. Хроническая эмпиема плевры и бронхиаль­
ные свищи (акад. И. С. Колесников, проф. М. И. Лыт­
кин, канд. мед. наук Г. С. Чепчерук)...........................
Глава 10. Опухоли плевры (проф. М. И. Лыткин, канд.
мед. наук Г. С. Чепчерук)................................................
Глава 11. Бронхоэктазии (акад. И. С. Колесников,
д-р мед. наук В. Т. Плешаков, д-р мед. наук Л. С. Лес­
ницкий)
................................................................................
Глава 12. Пневмомикозы (проф. М. И. Лыткин, канд.
мед. наук Ю. Л. Шевченко, канд. мед. наук И. А. Чалисов) ......................................................................................
7
141
172
186
210
228
234
255
Глава 13. Паразитарные заболевания легких (акад.
И. С. Колесников , д-р мед. наук С. А. Шалаев) . .
261
Глава 14. Рак легкого (акад. И. С. Колесников, проф.
М. И. Лыткин, д-р мед. наук С. А. Шалаев) ...
272
Глава 15. Саркома легких (проф. М. И. Лыткин)
.
Preface ......................................................................................
6
Chapter 1. Surgical anatomy of the lungs (Academician
/. 5. Kolesnikov)......................................................................
7
Chapter 2. Clinical physiology of the lungs and pleura
(Doctor of Medical Sciences A. L. Kostyuchenko, Can­
didate of Medical Sciences V. I. Buravtsov)
....
56
Chapter 3. General principles of examination of patients
suffering from the lung and pleura illnesses (Doctor
of Medical Sciences 5. A. Shalaev, Doctor of Medical
Sciences A. L. Kostyuchenko, Candidate of Medical
Sciences В. K. Savchenko, Candidate of Medical Sci­
ences Yu. A. Popov).................................................................. 80
Chapter 4. Preparation of the patients to operation
(Doctor of Medical Sciences A. L. Kostyuchenko, Doc­
tor of Medical Sciences 5. A. Shalaev, Doctor of Medi­
cal Sciences L. S. Lesnitsky)......................................................Ill
Chapter 5. Anomalies in development of the lungs (Pro­
fessor M. I. Lytkin, Candidate of Medical Sciences
Yu. A. Popov, Candidate of Medical Sciences Yu. L. Shev­
chenko)
..................................................................................... 119
Chapter 6. Acute abscesses and gangrene of the lungs
(Academician /. 5. Kolesnikov, Professor M. I. Lytkin,
Doctor of Medical Sciences L. S. Lesnitsky, Candidate of
Medical Sciences В. K. Savchenko)..................................... 141
Chapter 7. Chronic abscesses of the lungs (Academician
/. 5. Kolesnikov, Professor M. 1. Lytkin, Doctor of Me­
dical Sciences L. S. Lesnitsky)................................................172
Chapter 8. Acute empyema of the chest and pyopneu­
mothorax (Academician /. 5. Kolesnikov, Professor
M. I. Lytkin, Candidate of Medical Sciences G. 5. Chepcheruk. Doctor of Medical Sciences L. S. Lesnitsky,
S. V. Grishakov)........................................................................... 186
Chapter 9. Chronic empyema of the chest and bronchial
fistulas (Academician /. 5. Kolesnikov, Professor
M. I. Lytkin, Candidate of Medical Sciences G. 5. Chepcheruk)
..................................................................................... 210
Chapter 10. Tumors of the pleura (Professor M. 1. Lyt­
kin, Candidate of Medical Sciences G. 5. Chepcheruk) 228
Chapter 11. Bronchiectases (Academician /. S. Kolesni­
kov, Doctor of Medical Sciences V. T. Pleshakov, Doc­
tor of Medical Sciences L. S. Lesnitsky)................................234
Chapter 12. Pneumomycoses (Professor M. I. Lytkin,
Candidate of Medical Sciences Yu. L. Shevchenko,
Candidate of Medical Sciences /. A. Chalisov) . .
255
Chapter 13. Parasitogenic diseases of the lungs (Aca­
demician /. 5. Kolesnikov, Doctor of Medical Sciences
5. A. Shalaev).......................................................................... 261
Chapter 14. Cancer of the lungs (Academician /. S. Ko­
lesnikov, Professor M. I. Lytkin, Doctor of Medical
Sciences 5. A. Shalaev).......................................................... 272
Chapter 15. Sarcoma of the lungs (Professor M. I. Lyt­
kin)
........................................................................................... 303
Chapter 16. Benign neoplasms and cysts of the lungs
(Doctor of Medical Sciences 5. A. Shalaev, Candidate
of Medical Sciences 5. F. Malakhov, Candidate of Me­
dical Sciences В. K. Savchenko).......................................... 308
Chapter 17. Spontaneous pneumothorax (Academician
/. 5. Kolesnikov, Doctor of Medical Sciences V. T. Pleschakov. Doctor of Medical Sciences L. S. Lesnitsky) 320
Chapter 18. How to ensure safity of operations per­
formed in connection 'vith the lungs and pleura diseases
(Doctor of Medical Sciences G. A. Livanov, Doctor of
Medical Sciences A. L. Kostyuchenko, Doctor of Medi­
cal Sciences V. T. Pleshakov, Candidate of Medical
Sciences M. Ya. Matusevich, Candidate of Medical
Sciences О. I. Zhukov).................. _.........................................332
Chapter 19. Intensive therapy and local treatment of
patients after operations performed in the lungs and
pleura (Doctor of Medical Sciences A. L. Kostyuchenko,
Candidate of Medical Sciences V. I. Buravtsov, Candi­
date of Medical Sciences A. N. Tulupov................................350
Bibliography................................................................................ 373
6
.
303
Глава 16. Доброкачественные новообразования и
кисты легких (д-р мед. наук С. А. Шалаев, канд. мед.
наук С. Ф. Малахов, канд. мед. наук Б. К. Савченко)
Глава 17. Спонтанный пневмоторакс (акад. И. С. Ко­
лесников, д-р мед. наук В. Т. Плешаков, д-р мед.
наук Л. С. Лесницкий) . ... . ...........................
308
320
Глава 18. Обеспечение безопасности операций по
поводу заболеваний легких и плевры (д-р мед. наук
А. Л. Костюченко, д-р мед. наук Г. А. Ливанов, д-р
мед. наук В. Т. Плешаков, канд. мед. наук М. Я. Матусевич, канд. мед. наук О. И. Жуков)...........................
332
Глава 19. Интенсивная терапия и местное лечение
больных после операций на легких и плевре (д-р
мед. наук А. Л. Костюченко, канд. мед. наук В. И. Буровцов, канд. мед. наук А. Н. Тулупов)...........................
Список литературы...........................................................
350
373
5
ПРЕДИСЛОВИЕ
Хирургия легких и плевры в настоящее время перестала быть уделом
отдельных крупных клиник и все шире проникает в периферийные хирурги­
ческие стационары. Развитию ее в определяющей степени способствовали
прогресс в анестезиологии и реаниматологии, исследования в области
клинической физиологии дыхания и кровообращения, а также совершен­
ствование методов диагностики и лечения хирургических заболеваний
легких.
В основу настоящего руководства положен многолетний опыт коллек­
тива госпитальной хирургической клиники Военно-медицинской академии
им. С. М. Кирова в лечении заболеваний легких и плевры. Этот опыт убе­
дил авторов в необходимости прочных знаний хирургической анатомии
и физиологии легких и плевры в процессе как диагностики, так и лечения
больных пульмонологического профиля, что нашло отражение в структуре
и содержании предлагаемого руководства.
Читатель найдет в этой книге сведения об этиологии и патогенезе,
описание клинической картины и особенностей диагностики, предопера­
ционной подготовки и лечения хирургических заболеваний легких и плевры.
Особенно большое внимание уделено раку легкого, абсцессам и гангрене
легких, острой и хронической эмпиеме плевры. Достаточно подробно
изложены также сведения о грибковых и паразитарных заболеваниях,
бронхоэктазиях, спонтанном пневмотораксе, кистах легких и других более
редких болезнях. На основании большого опыта коллектива клиники под­
робно изложены вопросы анестезиологического и реаниматологического
обеспечения при операциях на легких.
При описании осложнений особое внимание уделялось анализу тех
из них, которые служат наиболее частой причиной тревог и грустных раз­
мышлений хирурга и реаниматолога в послеоперационном периоде. К ним
относ ятся недостаточность основных систем жизнеобеспечения — дыхания
и кровообращения, тромбозы и тромбоэмболии, перфузионные и вентиля­
ционные нарушения в оставшейся части легкого, несостоятельность культи
бронха и тяжелые инфекционные осложнения.
В предлагаемом руководстве сознательно опущены главы, касаю­
щиеся травмы груди и легочных кровотечений, так как ограниченный объем
издания не позволяет изложить этот раздел с должной степенью детали­
зации. Не включено также и хирургическое лечение туберкулеза легких,
ныне выделившееся в отдельную специальность — фтизиохирургию.
В изложении материала авторы стремились не только представить свой
личный опыт, но и сообщить все новое и полезное из доступной им отече­
ственной и иностранной литературы. Мы отчетливо сознаем, что не все
получилось одинаково удачно и, вероятно, не все разделы представлены
с такой степенью детализации, какую хотелось бы видеть читателю. Поэтому
авторы будут искренне признательны за все критические замечания, кото­
рые послужат делу дальнейшего укрепления здоровья населения нашей
страны.
сосудами ткани легкого, но и вне ее, в средо­
стении. Это — четвертая закономерность.
Меньше внимания уделено системе бронхи­
альных (питательных) сосудов и еще меньше—
иннервации. В частности, значение тех или иных
нервов для функции отдельных структурных
анатомических элементов легкого остается еще
малоизвестным.
При изучении межсегментарных плоскостей
в легком установлено, что у эмбриона легкое
разделено на сегменты. При дальнейшем раз­
витии плода они сливаются, остаются разде­
ленными лишь доли. Этим объясняется нередко
встречающееся у взрослых сохранение щелей и
их зачатков между сегментами, которых в нор­
ме нет (например, щель между Se и пирамидой).
В то же время этим процессом воссоединения
следует объяснить не выраженность и даже пол­
ное отсутствие междолевых щелей (например,
отсутствие главной междолевой щели в левом
легком, которое нам пришлось наблюдать).
Практика показывает, что разъединение меж­
долевых пространств при хирургических вме­
шательствах, как бы анатомично оно сделано
ни было, для легкого (а следовательно, и для
больного) — ущерб, рана. Поэтому пироговское
понятие сберегательных действий не всегда бу­
дет относиться к сегментэктомиям, а тем более
к субсегментэктомиям. Это следует понимать
с точки зрения не только характера и распро­
страненности патологического процесса, но и
последующей реакции травмированных тканей
легкого. Удаление хорошо отделенной щеля­
ми доли может быть менее травматичной опе­
рацией, чем резекция одного какого-либо
сегмента, окруженного со всех сторон другими
сегментами.
В результате подробного изучения строения
бронхов легкого различными исследователями
было предложено около 30 схем их системати­
зации. Однако большинство хирургов в настоя­
щее время придерживаются номенклатуры,
утвержденной международным конгрессом ана­
томов и гистологов в Париже (1955), согласно
которой бронхи делятся дихотомически, опре­
деляя сегментарное строение легкого. Однако
ряд сегментов имеет три субсегмента (рис. 1).
По этой номенклатуре бронхи долей и сег­
ментов легкого обозначаются следующим об­
разом:
Глава ± ХИРУРГИЧЕСКАЯ
АНАТОМИЯ ЛЕГКИХ
Лечение различных заболеваний легких
хирургическими методами получило в настоя­
щее время широкое распространение. Это яви­
лось толчком к детальному изучению анатомии
легких. Появился ряд фундаментальных иссле­
дований в этом направлении и, прежде eceio,
работы В. М. Сергеева (1956), Е. Boyden (1947,
1958), G. Heberer (1953), G. Cordie, C. Cabrol
(1955), Д. Надь, И. Каласи (1959) и ряда других.
В этих работах, а также в нашем «Руководстве
по легочной хирургии» (1969) изложены систе­
матические данные о строении легкого. К ним
мы и отсылаем читателя. Нам же хотелось в
этой главе изложить анатомию легких в при­
кладном аспекте, избегая деталей, которые не
имеют большого практического значения.
Деление легкого на доли, сегменты, субсег­
менты и более ме/кие дольки известно. Аэра­
ция легких и кровообращение в них происхо­
дят довольно автономно.
Следует подчеркнуть определенную законо­
мерность, относящуюся как к бронхам, так и
к сосудам: чем периферичней располагается
структурная единица органа дыхания, тем боль­
ше отклонений в его строении от типичного,
чаще всего встречающегося. В корне легкого
этих отклонений мало, их больше в корнях
долей, еще больше в корнях сегментов и суб­
сегментов. Детальное изучение анатомии легко­
го показало, что в бронхах такого разнообра­
зия вариантов строения меньше, чем в арте­
риях, а в последних меньше, чем в венах. Это —
вторая закономерность. Бронхи никогда не ана­
стомозируют друг с другом, артерии — очень
редко и только самые мелкие, вены же ана­
стомозируют чаще, чем предыдущие две си­
стемы; это — третья закономерность.
В последнее время большое внимание уделе­
но изучению лимфатической системы легких
и средостения. Эта система так же, как и опи­
санные выше, автономна. Лимфоток идет по
пути, определяемому анатомическим строени­
ем легкого. Анастомозирование этой системы
еще выше, чем венозной. Имеется множество
анастомозов не только между лимфатическими
7
Правое легкое
Верхняя доля
Номенклатура артерий, как говорилось выше,
такая же, как бронхов.
Номенклатур вен много. В практическом отно­
шении наиболее удобна номенклатура Е. Boyden
(1947, 1948), предусматривающая сегментарное
строение легких:
Верхушечный (В|)
Задний (В2)
Передний (Вз)
Наружный (В4)
Внутренний (В5)
Верхний (В«)
Внутренний, паракардиальный
(В7)
Переднебазальный (В8)
Наружнобазальный (В9)
Заднебазальный (Вт)
Левое легкое
Средняя доля
Нижняя доля
Верхняя доля
Правое легкое
Центральная вена (Vla)
Межсегментарная вена между I
и III сегментами (Vlb)
Межсегментарная вена между I
Вены II сегмента (V2)
и II сегментами (V2a)
Центральная вена (V2b)
Межсегментарная вена между II
и III сегментами (V2c)
Центральная вена (V Ja)
Вены III сегмента (V3)
Межсегментарная вена между III
и V сегментами (V3b)
Вены IV сегмента (V4)
Центральная вена (V4a)
Межсегментарная вена между IV
и V сегментами (V4b)
Вена V сегмента (V6)
Центральная вена (V5a)
Межсегментарная вена между
Вены VI сегмента (Уб)
верхним и внутренним субсег­
ментами (V6a)
Межсегментарная вена между
внутренним и наружным суб­
сегментами (V6b)
Межсегментарная вена между VI
и X сегментами (V6c)
Вены VII сегмента (V7) Центральная вена (V7a), иногда
их несколько (V7a, V7b, V7c)
Вены VIII сегмента (Ve) Межсегментарная вена между
VII. VIII и IX сегментами
<V8a)
Центральные, впадающие в меж­
сегментарные (Vgb, V8c)
Центральная вена (V9a)
Вена IX сегмента (V9)
Центральная вена (V10a)
Вена X сегмента (Vm)
Вены I сегмента (V1)
Верхушечно-задний (Bi 2)
Передний (В3)
Верхнеязычковый (В4)
Нижнеязычковый (Bs)
Верхний (В«)
Переднебазальный (Be)
Наружнобазальный (В9)
Заднебазальный (Вт)
Нижняя доля
Номенклатура бронхов субсегментов париж­
ской конференции не предусмотрена. По дан­
ным литературы и нашему опыту, ее можно
представить в следующем виде:
Правое легкое
Верхушечный (В|а)
Передний (В,ь)
Задний (В2а)
Наружный (В2Ь)
Наружный (В3а)
Передний (Взь)
Задний (В4а)
Передний (В4Ь)
Верхний (В5а)
Нижний (В5Ь)
Внутренний (В6а)
Верхний (В6Ь)
Наружный (В^)
Верхушечный (В|)
Задний (В2)
Передний (Вз)
Наружный (В4)
Внутренний (В5)
Верхний (Вб)
Внутренний,
паракардиальный (В7)
Передний (EjJ
Левое легкое
Переднебазальный (Be)
Наружнобазальный (В9)
Заднебазальный (Вт)
Задний (В7Ь)
Наружный (В8а)
Базальный (В8Ь)
Наружный (В9а)
Базальный (В9Ь)
Наружный (В10а)
Внутренний (В1оь)
Вены I (верхушечного)
сегмента (V0
Вены III сегмента (V3)
Левое легкое
Верхушечный (Bi)
Задний (В2)
Передний (Вз)
Верхнеязычковый (В4)
Нижнеязычковый (Bs)
Верхний (Be)
Переднебазальный (Be)
Наружнобазальный (В9)
Заднебазальный (Вт)
Верхушечный (В1а)
Передний (В1Ь)
Верхушечный (В2а)
Задний (В2Р
Наружный (В3а)
Передний (Взь)
Задний (В4а)
Передний (В4Ь)
Верхний (В5а)
Нижний (В5Ь)
Внутренний (В6а)
Верхний (В6Ь)
Наружный (В6с)
Наружный (В8а)
Базальный (В8Ь)
Наружный (В9а)
Базальный (В9Ь)
Наружный (В1|)а)
Внутренний (В1оь)
Вены IV сегмента (V4)
Вена V сегмента (Vs)
Вены VI сегмента (V6)
Вена VIII сегмента (Vs)
Вена IX сегмента (V9)
Вена X сегмента (Vm)
8
Центральная вена (Vla)
Межсегментарная вена между I
и III сегментами (Vlb)
Межсегментарная вена между I
и II сегментами (Vic)
Центральная вена (V3a)
Межсегментарная вена между III
и IV сегментами (V3b)
Межсегментарная вена между IV
и V сегментами (V4a) (наруж­
ная)
Межсегментарная вена между IV
и V сегментами (внутренняя)
<v4b)
Центральная вена (V5a)
Межсегментарная вена между
верхним и внутренним субсег­
ментами (V6a)
Межсегментарная вена между
верхним и наружным субсег­
ментами (V6b)
Межсегментарная вена между
VI и X сегментами (V6c)
Центральная вена (Vs)
Центральная вена (V9)
Центральная вена (Vm)
Рис. 1. Сегментарное строение бронхиального дерева.
1 —верхушечный сегментарный бронх (Bt); 2 — задний сегмен­
тарный бронх (В2); 3 — передний сегментарный бронх (Вз); 4 —
наружный сегментарный бронх справа (В4) J 5 — внутренний сег­
ментарный бронх справа (В&); 6 — верхний сегментарный бронх
(Вь); 7 — медиобазальный сегментарный бронх (В?); 8 — перед­
небазальный сегментарный бронх (Вв); 9 — наружнобазальный
сегментарный бронх (В9); 10 — заднебазальный сегментарный
бронх (Bio); 11 —верхнеязычковый сегментарный бронх слева
(В4); 12 — нижнеязычковый сегментарный бронх слева (В5).
Вены базальных сегментов ввиду крайне ред­
ко возникающей необходимости в резекции их
по отдельности, не приводятся Е. Boyden (1947,
1958). Они подробно представлены у G. Cordie,
С. Cobrol (1955). Последними авторами пока­
зано, что венозная система сегментов средней
доли справа и язычка слева, а также базальных
сегментов обоих легких построена в основном
так же, как и в других сегментах, т. е. с постоян­
ством межсегментарных и субсегментарных вен
и непостоянством центральных. Однако порой
возникает нужда к удалению IV (наружного)
9
сегмента средней доли справа или V (нижнего)
сегмента язычка слева. В то же время изредка
требуется удалить VII сегмент.
Важной особенностью строения легкого яв­
ляется резкое уменьшение диаметра бронхов,
артерий и вен к периферии органа. Эта зона
мелких и мельчайших бронхов в различных
участках легкого неодинакова по расстоянию
от висцеральной плевры. В паракостальных и
диафрагмальных участках она достигает 3—4
и даже 5 см; в медиастинальных, междолевых
и ближе к корню толщина этой зоны может
уменьшаться до 1 см и даже менее. Знание
глубины зоны расположения мелких и мельчай­
ших бронхов, а также сосудов на тех или иных
участках легкого важно для проведения ати­
пичных краевых и клиновидных его резекций.
В отличие от артерий и вен малого круга кро­
вообращения, о которых говорилось выше, обес­
печивающих в основном функцию газообмена
при дыхании, в легких имеется самостоятель­
ная система сосудов большого круга кровообра­
щения, называемых бронхиальными сосудами.
Они несут в основном функцию «питания» и
обмена в тканях органа. Этой системе в послед­
ние годы придается большое значение, в частно­
сти потому, что после перевязки артерий малого
круга кровообращения наблюдается резкое уве­
личение бронхиальных артерий.
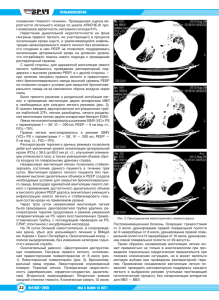
Примером может служить один из наших больных (В.),
обследованный через 27 лет после операции по поводу
гангренозного абсцесса верхней доли правого легкого, кото­
рому вначале была сделана пневмотомия. Через месяц пос­
ле этой операции из-за аррозионного кровотечения в крайне
тяжелом состоянии при экстренном повторном вмеша­
тельстве успели перевязать лишь общий ствол артерии лег­
кого. Больной выздоровел без дополнительных операций.
За все последующее время не болел, был работоспособ­
ным. В клинику приехал для очередного обследования. На
рентгенограмме видна ложная киста верхней доли правого
легкого. На ангиограмме легочной артерии отчетливо обоз­
начается культя главного ствола правой легочной артерии,
а ангиограмма бронхиальных артерий указывает на изви­
тость и резкое расширение бронхиальной артерии в зоне
этой кисты (рис. 2).
Подобные наблюдения указывают на тесную
связь обеих систем кровообращения в легком.
Более глубокое изучение функциональной зна­
чимости бронхиальных сосудов как анатомиче­
ской, так и функциональной — дело будущих
исследований.
Лимфатическая система легких представлена
поверхностными лимфатическими сосудами
плевры и глубокими, внутрилегочными лимфати­
ческими сосудами. Поверхностная лимфати­
ческая сеть состоит из крупных петель, соот­
ветствующих контурам оснований долек легкого
и мелких петель, располагающихся на поверх­
ности оснований долек. Степень развития по­
верхностной лимфатической сети, форма и раз­
меры лимфатических капилляров находятся в
прямой зависимости от функциональной актив­
ности различных отделов легкого. В области
менее вентилируемых сегментов легкого (верху­
шечного, заднего, верхнезадней части переднего
и латерального базальных сегментов) лимфа­
тические капилляры выражены слабее, а в об­
ласти нижних долей, на диафрагмальной по­
верхности легких, петлистость поверхностной
лимфатической сети всегда выражена хорошо,
представлена широкими, петлистыми сосудами.
Истоки глубокой лимфатической системы
легких представлены лимфатическими капилля­
рами, расположенными вокруг респираторных
и терминальных бронхиол, в межлобулярных
перегородках, слизистой оболочке бронхов.
Обе сети лимфатических капилляров (поверх­
ностная и глубокая) широко анастомозируют
между собой, и поэтому деление лимфатической
системы легких на поверхностную и глубокую
весьма условно. Связи между ними хорошо раз­
виты как на периферии, так и у корня легких.
Соединяясь между собой, лимфатические ка­
пилляры образуют лимфатические сосуды, на­
правляющиеся к корню легкого. Вместе с лимфа­
тическими узлами многочисленные лимфати­
ческие сосуды формируют основные лимфати­
ческие коллекторы легких, по которым проис­
ходит регионарный ток лимфы. Все лимфати­
ческие узлы, принимающие лимфу от различ­
ных отделов легких, условно распределяют в
несколько основных групп: внутрилегочные,
корневые, медиастинальные и надключичные;
последние являются завершающим этапом тока
лимфы от легких перед поступлением ее в ве­
нозную систему (рис. 3).
Внутрилегочные (бронхопульмональные) лим­
фатические узлы располагаются по ходу сег­
ментарных и долевых бронхов и сосудов, а так­
же под плеврой — между долями легких. Основ­
ная масса внутрилегочных лимфатических уз­
лов располагается у места деления главных,
долевых и сегментарных бронхов в клетчатке
между бронхами и ветвями легочной артерии
и вены. В практическом отношении важным
является выделение групп внутрилегочных лим­
фатических узлов в основании каждого из до­
левых бронхов, а также междолевых (верхних
и нижних — для правого легкого, междоле­
вых — в левом легком).
Корневые лимфатические узлы располага­
ются в области корней правого и левого легких.
Граница между внутрилегочными и корневыми
лимфатическими узлами регионарных лимфа­
тических коллекторов легких условна. Принято
считать, что ею является плоскость, мысленно
проведенная через ворота легкого. Другим приз­
наком такого разделения может являться отно­
шение лимфатических узлов к легочной ткани:
10
Рис. 2. Рентгенологическая картина через 27 лет после пере­
вязки легочной артерии справа.
а -— обзорная рентгенограмма; б — бронхограмма; в — ангиопульмонограмма; г — селективная ангиограмма бронхиальных арте­
рий.
Медиастинальные лимфатические узлы,
принимающие лимфу от легких, наиболее мно­
гочисленны и располагаются в клетчаточных
пространствах средостения. Здесь выделяют
передние, задние и трахеальные группы
лимфоузлов.
В свою очередь, в каждой из этих групп
различают лимфатические узлы, принимающие
лимфу преимущественно из правого или левого
легкого.
На передней поверхности верхней полой вены
и отчасти — правой плечеголовной вены рас-
если она со всех сторон окружает лимфатиче­
ский узел, то он относится к внутрилегочным,
если узел или группа узлов лишь частично при­
крыта легким, то к корневым. По отношению
к элементам корня легкого последние делят на
верхние, нижние, передние и задние. Обычно
лучше выражены и представлены большим чис­
лом передняя и верхняя корневые группы узлов
регионарных лимфатических коллекторов. Ниж­
ние корневые лимфатические узлы без четкой
границы переходят в лимфатические узлы ле­
гочных связок.
11
правые; 8 — левые; 9 — легочных связок. Медиастинальные:
10 — трахеобронхиальные; 11 — паратрахеальные; 12 — бифур­
кационные; 13 — претрахеальные; 14 — преаортокаротидные;
15 — превенозные;
16 — околопищеводные.
Надключичные:
17 — глубокие яремные (нижние, средние, верхние); 18 — по
ходу поперечной артерии шеи; 19 — по ходу добавочного нерва.
Рис. 3. Расположение основных групп узлов регионарных
лимфатических коллекторов легких.
Внутрилегочные: 1 — верхнедолевые; 2 — среднедолевые; 3 —
нижнедолевые; 4 — верхние междолевые правые; 5 — нижние
междолевые правые; 6 — междолевые левые. Корневые: 7 —
12
полагаются лимфатические узлы, объединяе­
мые в правую переднюю медиастинальную или
превенозную группу.
Слева, на передней поверхности дуги аорты,
начинаясь несколько ниже, близ артериальной
связки, и достигая основания левой сонной
артерии, группируются левые передние медиа­
стинальные или преаортокаротидные лимфати­
ческие узлы.
Среди них нередко выделяют один, наиболее
крупный лимфатический узел, именуемый «узлом
боталлова протока». Последний прилежит к ниж­
ней гортанной ветви левого блуждающего нерва,
восходящей вдоль трахеи к мышцам левой по­
ловины гортани.
Непостоянно выражены в переднем средосте­
нии лимфатические узлы поперечной цепи, рас­
полагающиеся вдоль левой плечеголовной вены,
и преперикардиальные — вдоль диафрагмаль­
ного нерва.
В заднем средостении основная масса лимфа­
тических узлов лежит вдоль пищевода — перед­
ней и боковых его поверхностей. Самые ниж­
ние из околопищеводных лимфатических узлов
могут достигать пищеводного отверстия диа­
фрагмы.
Трахеальная группа медиастинальных лимфа­
тических узлов наиболее многочисленна и рас­
положена у трахеи и начальных отделов пра­
вого и левого главных бронхов.
В клетчаточном пространстве, ограниченном
нижними полуокружностями правого и левого
главных бронхов, сзади — пищеводом, спере­
ди — перикардом левого предсердия, постоян­
но находятся бифуркационные лимфатические
узлы.
Как правило, они группируются вдоль право­
го главного бронха, располагаясь, в основном, на
его внутренней поверхности.
Выше, на передней поверхности трахеи, в виде
своеобразного «мостика» встречаются претрахеальные лимфатические узлы. Они связаны
многочисленными лимфатическими сосудами
с лимфатическими узлами боковых поверхно­
стей трахеи.
Вдоль задней поверхности трахеи, ее мембра­
нозной части, непостоянно выделяют ретротрахеальные лимфатические узлы. Правые трахео­
бронхиальные лимфатические узлы занимают
клетчаточное пространство, ограниченное углом
трахеи с правым главным бронхом и выше —
между боковой поверхностью трахеи и медиа­
стинальной плеврой. Условной границей между
ними и вышележащими правыми паратрахеальными лимфатическими узлами является место
впадения непарной вены в верхнюю полую. Не­
редко расположенный здесь один из крупных
лимфатических узлов именуют «узлом непарной
вены».
Верхней границей правых паратрахеальных
лимфатических узлов является проходящий
здесь плечеголовной артериальный ствол у места
отхождения правой подключичной артерии. Мно­
гочисленные лимфатические сосуды от правых
паратрахеальных лимфатических узлов направ­
ляются далее вверх — к надключичному отде­
лу регионарных коллекторов.
Левая трахеобронхиальная группа лимфати­
ческих узлов ограничена боковой поверхностью
трахеи и левым главным бронхом, сзади —
дугой аорты, снаружи — артериальной связкой.
По направлению вверх, вдоль трахеи они пере­
ходят в немногочисленную группу левых пара­
трахеальных лимфатических узлов, имеющих
связь с лимфатическими узлами, расположен­
ными в глубоких клетчаточных пространствах
левой половины шеи.
На шее передние пре- и паратрахеальные
лимфатические узлы прилежат непосредственно
к трахее. Глубокие боковые лимфатические
узлы шеи, принимающие часть лимфы от лег­
ких, наиболее многочисленны и занимают глав­
ным образом область надключичных клет­
чаточных пространств, органиченных фасциаль­
ными футлярами.
Глубокие лимфатические узлы боковых по­
верхностей шеи справа и слева подразделяются
на внутренние и наружные. Внутренние распо­
ложены вдоль яремной вены от уровня сосце­
видного отростка до места ее слияния с под­
ключичной веной. Эту группу узлов именуют
внутренними яремными. Нижние из них наибо­
лее многочисленны, являются связующим зве­
ном с лимфатическими коллекторами средосте­
ния и нередко называются надключичными.
Среди лимфатических узлов этой группы выде­
ляют один узел, именуемый «узлом Труазье»
[Troisier, 1889]. Он довольно крупный, занимает
место слияния внутренней яремной вены с под­
ключичной.
Наружные глубокие лимфатические узлы
менее многочисленны. Их подразделяют по
анатомическим образованиям этой области,
вдоль которых они группируются, и соответ­
ственно именуют лимфатическими узлами до­
бавочного нерва и поперечной артерии шеи.
Выносящие лимфатические сосуды принима­
ют участие в формировании правого лимфати­
ческого протока и грудного лимфатического
протока, впадающих в венозную систему.
Физиологическое состояние лимфатической
системы и отводящих лимфатических коллек­
торов легких определяет регионарный отток
лимфы. В нормальных условиях от различных
отделов легких лимфа направляется к регио­
нарным для них группам лимфатических уз­
лов, несмотря на существование обширных
связей в лимфатической системе этого органа.
13
По существующим представлениям, легочная
долька и сегмент не являются основными струк­
турными единицами для лимфатической систе­
мы легкого: от рядом расположенных сегментов
лимфа поступает в одни группы лимфатических
узлов и даже в отдельные лимфатические узлы.
Лишь в отношении каждой из долей легкого
наиболее полно и строго выдерживается прин­
цип регионарного оттока лимфы. Движение
лимфы в легких ориентировано в направлении
от дистальных отделов к корню. Пройдя эти
группы лимфатических узлов в пределах медиа­
стинальной части регионарных коллекторов,
лимфа движется главным образом по сосудам
одноименной правому или левому легкому сто­
роны в восходящем направлении. Ток лимфы
вниз, к забрюшинным лимфатическим узлам,
расценивается как дополнительный, встре­
чающийся менее чем в 10 % наблюдений [Hoff­
man A., Jiinemann L., 1968].
Следуя по регионарным коллекторам от каж­
дой из долей легкого, лимфа последовательно
проходит через внутрилегочные, корневые, ме­
диастинальные, надключичные группы лимфа­
тических узлов. Согласно «закону Москаньи»
[Moccagni R., 1787], все лимфатические сосуды
на пути от органа до венозной системы проходят
по крайней мере один лимфатический узел. Важ­
но, что для легкого такой лимфатический узел
или группа узлов могут располагаться на раз­
ном удалении от истоков: нередко лишь в пре­
делах средостения. Имеются сведения о том,
что отдельные лимфатические сосуды легких
на всем протяжении до кровеносной системы
не имеют ни одного лимфатического узла. По­
следнее может существенно влиять на распро­
странение патологического процесса в легком.
В общем виде ток лимфы от каждой из долей
легкого в нормальных условиях выглядит сле­
дующим образом.
Верхняя доля правого легкого.
Наиболее постоянны два пути:
1) переднемедиальный
(внутренний) —че­
рез внутрилегочные, междолевые верхние, кор­
невые, правые трахеобронхиальные, паратрахеальные, превенозные и правые надключичные
лимфатические узлы;
2) заднелатеральный
(наружный) — через
верхнедолевые, верхние междолевые к задней
и нижней группам корневых и далее вверх через
правые трахеобронхиальные или бифуркацион­
ные лимфатические узлы в надключичную об­
ласть.
Средняя доля правого легкого.
Лимфа поступает через среднедолевые и верх­
ние междолевые внутрилегочные лимфатиче­
ские узлы к корневым, правым трахеобронхи­
альным и бифуркационным лимфатическим
узлам.
Нижняя доля правого легкого.
Формируются два пути оттока лимфы:
1) верхний — через нижнедолевые, нижние
междолевые, корневые группы узлов — к тра­
хеобронхиальным и далее вверх;
2) нижний путь тока лимфы — через ниж­
недолевые, нижние корневые к бифуркацион­
ным, претрахеальным, правым трахеобронхи­
альным, правым паратрахеальным — к над­
ключичным.
Верхняя доля левого легкого.
Имеются два пути оттока лимфы:
1) верхний — через верхнедолевые, верх­
ние корневые к преаортокаротидным лимфати­
ческим узлам и далее в левые надключичные;
2) нижний — преимущественно от язычко­
вых сегментов — через верхнедолевые, междо­
левые, бифуркационные к левым трахеоброн­
хиальным, преаортокаротидным и далее вверх.
Нижняя доля левого легкого.
Известны три основных направления оттока
лимфы. Верхний и средний из них проходят
через нижнедолевые, междолевые, корневые
к преаортокаротидным и левым трахеоброн­
хиальным группам лимфатических узлов.
Нижний путь регионарного тока — через
нижнедолевые, междолевые (или их минуя),
нижние корневые, узлы левой легочной связ­
ки, к околопищеводным и бифуркационным, а
затем — через левые трахеобронхиальные и преаортокаротидные — в надключичные и далее
к грудному протоку.
Многочисленные связи в лимфатических кол­
лекторах средостения (в том числе — попереч­
ные), установленные методом наливок при про­
ведении морфологических исследований, равно
как и коллатерали, в нормальных условиях, при
отсутствии патологических изменений в лимфа­
тических коллекторах, находятся в состоянии
функционального покоя, «включаясь» лишь при
возникновении препятствия или особенно ин­
тенсивного движения лимфы, при которых
регионарные коллекторы не в состоянии обес­
печить отток лимфы от отдельных участков лег­
кого.
Легкие иннервируются из симпатических
нервных стволов и из блуждающего нерва. Нер­
вы проходят в корень легкого иидут сначала
позади главных бронхов, у их мембранозной
части и далее, сопровождая их, до мельчайших
разветвлений. Считается доказанным, что в нерв­
ных стволах как чревного нерва, так и симпа­
тической цепочки проходят смешанные волок­
на симпатического и парасимпатического дей­
ствия. Однако данных о влиянии тех или иных
нервных стволов на различное функциониро­
вание легочной ткани, бронхов, сосудов, по сути,
нет. Практическая зависимость пересечений их
неясна.
14
Рис. 4. Границы сегментов правого легкого (вид с внутренней
стороны).
Верхняя доля: 1 — верхушечный; 2 — задний; 3 — передний.
Средняя доля: 4 — наружный; 5 — внутренний. Нижняя доля:
6 — верхний; 7 — внутренний (паракардиальный); 8 — передне­
базальный; 9 — наружнобазальный; 10 — заднебазальный.
15
Рис. 5. Границы сегментов правого легкого (вид с наружной
стороны).
Верхняя доля: 1 — верхушечный; 2 — задний; 3 — передний. Сред­
няя доля: 4 — наружный; 5 — внутренний. Нижняя доля: 6 —
верхний; 7 — переднебазальный; 8 — наружнобазальный; 9 —
заднеб а зальн ый.
16
Рис. 6. Границы сегментов левого легкого (вид с наружной
стороны).
Верхняя доля: 1,2 — верхушечнозадний; 3 — передний; 4 — верх­
неязычковый; 5 — нижнеязычковый. Нижняя доля: 6 — верхний;
7 — переднебазальный; 8 — наружнобазальный; 9 — заднебазаль­
ный.
2 Зак. 0517
17
I
Рис. 7. Границы сегментов левого легкого (вид с внутренней
стороны).
Верхняя доля: 1,2 — верхушечнозадний; 3 — передний; 4 — верх­
неязычковый; 5 — иижнеязычковый. Нижняя доля: 6 — верх­
ний; 7 — переднебазальный; 8 — наружнобазальный; 9 — задне­
базальный.
что эти плоскости имеют довольно сложную
конфигурацию (рис. 4—7) и разделение их,
конечно, происходит довольно грубо. Чем луч­
ше знание границ сегментов, тем меньше ущерб
легкому при их разделении.
Хирурга прежде всего интересует строение
корней органа в целом, его долей и сегментов,
а также анатомические ориентиры, позволяю­
щие возможно точно разделить легкое по меж­
сегментарным плоскостям. Следует отметить,
18
ПРАВОЕ ЛЕГКОЕ
КОРЕНЬ ПРАВОГО ЛЕГКОГО
После вскрытия грудной полости по четвер­
тому или пятому межреберью, в зависимости
от намечаемого характера вмешательства, хи­
рург обнаруживает медиастинальную поверх­
ность легкого и средостения. Отчетливо видны
верхняя полая вена, латеральная поверхность
предсердия и желудочка, диафрагмальный нерв
с сосудами перикарда и диафрагма.
Дорсально и выше корня легкого справа в по­
лую вену впадает непарная вена, делящаяся
к периферии на1 две ветви: верхнюю и нижнюю.
Непарная вена собирает кровь из межреберных
вен правой стороны. Корень правого легкого
находится каудальнее непарной вены и прикры­
вается со всех сторон плеврой и корневой фас­
цией под ней. После вскрытия плевры и фасции,
что лучше делать на месте переходной складки
плевры корня с плеврой, покрывающей средо­
стение, первой обнаруживается верхняя легоч­
ная вена. Она нередко частично покрывает ле­
гочную артерию, лежащую дорсальнее и краниальнее вены. При препаровке вены следует пом­
нить, что на месте прохождения ее в полость
перикарда она «увлекает» его за собой, образуя
муфту. При неосторожных манипуляциях
хирурга эта муфта может быть повреждена и
полость перикарда напрасно вскрыта.
Нередко верхняя (краниальная) часть верх­
ней легочной вены довольно плотно сращена
с легочной артерией, и выделить ее, не повреж­
дая артерии, можно лишь препарируя вену с
нижней (каудальной) и задней ее поверхностей.
Сращения не всегда являются следствием вос­
палительного процесса, чаще — это вариант нор­
мального развития. Корневая фасция, переки­
дываясь с вены на артерии, довольно прочно
их спаивает. Не так редко вена заднего (II)
сегмента соединяется с общим стволом верхней
легочной вены у самого средостения, при так
называемом заднем типе венозного оттока.
В этих случаях выделение вены грозит повреж­
дением ее. Выделять верхнюю легочную вену
нужно, сдвинув медиально перикардиальную
муфту, т. е. как можно ближе к сердцу, а в труд­
ных условиях — даже внутриперикардиально.
Верхняя легочная вена образуется из трех
истоков: верхнего — вены III (переднего) сег­
мента и частично верхушечного, заднего — ве­
ны II сегмента и частично субсегментарной вет­
ви I сегмента и нижнего — среднедолевой вены.
Следует отметить, что среднедолевая вена
может не оказаться на месте, где она чаще
всего вливается в верхнюю легочную вену. В этих
случаях V4,5 впадает либо в нижнюю легоч­
2*
ную вену, либо самостоятельным стволом —
в левое предсердие. Это можно выяснить лишь
препаровкой корня легкого вниз (каудальнее).
Опаснее дистальное слияние средней долевой
вены с общим стволом верхней легочной. Пере­
вязка последней в таких случаях нарушает ве­
нозный отток из средней доли. При удалении
только верхней доли правого легкого перевязка
V4,5 в таких случаях может привести либо
к напрасному удалению средней доли (если
ошибка замечена во время операции), либо к
тяжелым осложнениям (болезни средней доли)
после операции.
Нижняя легочная вена собирает кровь из ниж­
ней доли. Иногда, как указывалось выше, в нее
вливается У4Л; тогда кровь собирается и из
средней доли.
Нижняя легочная вена расположена ниже и
кзади от верхней легочной вены. Кзади (дор­
сально) и медиальнее от нее проходят ниж­
няя ветвь непарной вены, блуждающий нерв и
еще медиальнее — пищевод.
Выделение нижней легочной вены не пред­
ставляет большой трудности. Исключение уча­
стия в ее формировании среднедолевой вены
обеспечивается прослеживанием основного
ствола к периферии.
Обычно нижняя легочная вена образуется
тремя истоками: Уб, идущей сзади и снаружи,
минуя среднюю долю, верхней базальной веной
(У7 и V8), идущей спереди вниз и латеральней
этой последней, и нижней базальной веной (V9
и Vio), идущей снизу и снаружи. Отклонения
от этого типичного расположения легочных
вен встречаются очень редко. Все же следует
указать на одно из них: раннее слияние вен
в один мощный ствол. Препаровка такой общей
вены к периферии позволяет установить эту
особенность и избежать ошибки.
Ниже (каудальнее) вен легкое связано со
средостением легочной связкой, представляю­
щей два листка плевры с клетчаткой между
ними и лимфатическими узлами, лежащими по
наружной поверхности пищевода. Эта связка
должна быть разъединена тупо или остро (с пе­
ревязкой ее элементов). При врожденной
аномалии развития и образовании участков
нижней или средней доли, снабжаемых кровью
из большого круга кровообращения, в легочной
связке могут проходить довольно крупные арте­
риальные стволы, идущие непосредственно от
аорты. При неосторожном рассечении легочной
связки эти артерии могут быть пересечены, и их
центральные концы тогда уходят глубоко в сре­
достение, давая большое кровотечение.
Легочная артерия лежит выше и кзади от верх­
ней легочной вены. Спереди артерия прикрыта
верхней полой веной, частично, как указывалось,
верхней легочной веной, а краниальнее ее, сни-
19
Рис. 8. Сосуды корня правого легкого из полости перикарда.
1 — легочная артерия; 2 — верхняя легочная вена; 3 — нижняя
легочная вена; 4 — ушко сердца; 5 — верхняя полая вена; 6 —
V. azygos.
зу вверх, идет непарная вена, впадающая в верх­
нюю полую вену. Тут же локализуется и лимфа­
тический узел, называемый «узлом непарной
вены». Нередко он резко увеличен (при мета­
стазе рака, гнойном лимфадените), плотно спаян
с артерией. Это затрудняет выделение артерии.
Кроме того, к нижней ее поверхности приле­
жит нередко плотно сращенный с ней верхний
междолевой лимфатический узел. В этих слу­
чаях выделение легочной артерии затруднено
не только из-за наличия сращения ее с патоло­
гически измененными лимфатическими узлами,
но и вследствие изменения стенки артерии. Эти
изменения в стенке артерии, как правило, боль­
ше выражены к периферии и меньше — к цент­
ральной части ее. Поэтому препарирование ле­
гочных артерий в подобных случаях следует ве­
сти ближе к средостению, сместив полую вену
медиально и отпрепарировав вначале перикард
внутрь, к сердцу.
Следует иметь в виду, что метастаз рака в тот
или иной лимфатический узел и сращение его
с легочной артерией не указывают еще на про­
растание ее раковой опухолью. В большинстве
случаев это свидетельствует лишь о развитии
параканкрозных воспалительйых и дегенератив­
ных изменений вокруг лимфатического узла.
Это подтверждается свободным отделением ар­
терии от измененных лимфатических узлов.
Главный бронх правого легкого, отойдя от
трахеи, направляется вниз, кнаружи и несколько
кзади, располагаясь кзади от легочной арте­
рии, плотно прилегая к ней. Он служит как бы
продолжением трахеи. Снизу (каудально) бронх
граничит с клетчаткой и бифуркационными
лимфатическими узлами, сзади (дорсально) —
с пищеводом; сверху его огибает непарная вена.
К периферии он делится на верхнедолевой и
промежуточный бронхи. Между ними находится
верхний междолевой лимфатический узел.
20
правило, к застою в верхней доле, что доказы­
вается достаточностью венозных анастомозов
между венами верхней доли с венами средней
(Vs) и нижней (Vc) долей.
При выделении верхней легочной вены сле­
дует, как указывалось выше, проследить за от­
хождением V•>, помня о том, что иногда она
вливается в общий ствол близко у перикарда.
В то же время тщательная препаровка истоков
верхней легочной вены может обнаружить осо­
бенности впадения в нее вены средней доли.
Это предупредит перевязку вен верхней и сред­
ней долей. Случаи впадения в верхнюю легоч­
ную вену V7 в хирургической практике встре­
чаются очень редко.
Для выделения артерий верхней доли следует
сначала отпрепарировать общий ствол правой
легочной артерии. Она, покинув полость пери­
карда, отдает ветвь в виде мощного ствола, от­
ходящего от передней поверхности ее и назы­
ваемого передним или верхним стволом легоч­
ной артерии. Этот ствол снабжает кровью вер­
хушечный (Si) и передний (S3) сегменты. Пос­
ле отхождения переднего ствола артерия уходит
вниз и кзади и называется междолевым ство­
лом. Задний сегмент снабжается кровью в боль­
шинстве случаев (80—90 %) по артерии, отходя­
щей от междолевого ствола и идущей позади
верхнедолевого бронха, на месте разделения
его на верхний и промежуточный бронхи. Эта
артерия может в сложных анатомических ус­
ловиях служить при выделении верхнедолевого
бронха ориентиром разделения бронхов. Здесь
же локализуется верхний междолевой лимфа­
тический узел.
Нередко верхушечный и передний сегменты
снабжаются кровью самостоятельными вет­
вями легочной артерии, т. е. вместо одного,
крупного, переднего ствола отходят две арте­
рии — А| и Аз, т. е., отпрепарировав артерию,
отходящую вперед от основного ствола, но име­
ющую диаметр, не соответствующий калибру
переднего ствола (0,8—1,2 см), следует искать
вторую артерию, обычно отходящую от боко­
вой поверхности основного ствола (А|). Если
оказывается, что этот последний имеет диаметр,
значительно больший, чем предыдущая артерия
(Аз), то это должно указывать хирургу, что
периферичней от нее и кзади будет отходить
ветвь к заднему сегменту или субсегменту. В этих
случаях рекуррентной артерии, отходящей от
междолевого ствола, либо не будет совсем, либо
она будет небольшой, субсегментарной.
В случаях, когда имеется особенность раз­
вития с отхождением сегментарного или суб­
сегментарного бронха от трахеи, его, как пра­
вило, сопровождает и артерия, отходящая от
ствола правой легочной артерии у выхода из
полости перикарда.
Выделение главного бронха правого легкого
не представляет обычно большой трудности.
Следует помнить одну особенность — от­
хождение сегментарного верхушечного брон­
ха (В|) выше места бифуркации, непосредствен­
но от трахеи. Таких случаев в практике клини­
ки встретилось два.
Внутриперикардиально препарировать эле­
менты корня легкого приходится в тех случаях,
когда вне перикарда имеются метастазы рака
или грубые воспалительные изменения в лимфа­
тических узлах корня, не позволяющие сво­
бодно выделить сосуды легкого без риска по­
вреждения их. В то же время характер пораже­
ния легкого дает возможность сделать предпо­
ложение об операбельности больного.
Вскрывается перикард кзади от диафрагмаль­
ного нерва, как можно ближе к передней по­
верхности верхней легочной вены. В полости
перикарда сверху обнаруживается легочная
артерия. Она направляется поперечно, чуть
вверх. Ниже нее строго поперечно идет верх­
няя легочная вена, а еще ниже — нижняя
(рис. 8). Все сосуды корня легкого в полости
перикарда лежат, как правило, мезоперикардиально, будучи окутаны перикардом неполно,
иногда образуя складку двух листков перикар­
да по задней поверхности сосудов (по типу
брыжейки). Выделение сосудов тупым спосо­
бом в случае полного окутывания их листками
перикарда не представляет больших затрудне­
ний. Если же сосуды расположены таким об­
разом, что 1 /4 или даже 1 /з их на задней поверх­
ности оказывается лежащей вне перикарда, то
разделение одного листка перикарда, прохожде­
ние инструментом по задней поверхности сосуда,
а затем — второго листка довольно затрудни­
тельны и опасны. О том, как обезопасить этот
этап препаровки сосудов, будет указано ниже.
Анатомической особенностью расположения
сосудов корня легкого в полости перикарда
является образование углублений его между
сосудами: верхнее и нижнее углубление (recessus) легочной артерии и такие же углубления
около вен.
ДОЛИ ПРАВОГО ЛЕГКОГО
ВЕРХНЯЯ ДОЛЯ
ПРАВОГО ЛЕГКОГО
Доступ к корню верхней доли правого лег­
кого — переднебоковой, через четвертое меж­
реберье. Первой видна верхняя легочная вена.
Для выделения и препаровки артерий верхней
доли вена может быть взята на провизорную
лигатуру (без вены средней доли) и смещена
книзу или перевязана и пересечена. Перевязка
вены без обработки артерии не приводит, как
21
Рис. 9. Центральная вена (V3a) является ориентиром между
передним (S3) и внутренним (Ss) сегментами правого лег­
кого.
Бронх верхней доли правого легкого лучше
всего препарируется после перевязки и пересе­
чения вен и артерий этой доли. При неболь­
ших патологических изменениях в корне доли
или паренхиме легкого выделение бронха не­
трудно. Однако чаще всего при удалении верх­
ней доли по поводу опухоли в ней, метастазов
в лимфатических узлах корня доли и легкого,
а также при воспалительных изменениях в тка­
нях вокруг бронха определение и выделение
его могут представить большие трудности. В оп­
ределении места отхождения верхнедолевого
бронха от главного может, как говорилось вы­
ше, помочь направление рекуррентной Аг. Вто­
рым важным признаком является прослежи­
вание пальцем сзади за ходом хрящевых колец:
если идти к периферии, отчетливо определяет­
ся место разделения главного бронха на верх­
недолевой и промежуточный. Наконец, третьим
признаком является место расположения верх­
него междолевого лимфатического узла.
Передний сегмент верхней доли имеет широ­
кую взаимосвязь с S5 средней доли. Разделение
их по межсегментарной плоскости возможно,
если ориентироваться на проходящую почти
под плеврой со стороны средостения V3c
(рис. 9) и на поперечную междолевую щель.
Поперечная междолевая щель никогда не отде­
ляет S3 от S5 полностью, но довольно часто
бывает недостаточно глубокой. При отсутствии
или при недоразвитии ее, т. е. при почти полном
слиянии S3 и S5, разделение их следует вести,
ориентируясь по ходу межсегментарной вены
(V3c). Однако в ряде случаев целесообразней
22
Рис. 10. Истоки верхней легочной вены правого легкого.
произвести верхнюю билобэктомию, чем разъ­
единять два сегмента, потеряв четкую границу
между ними. Разъединение легочной пере­
мычки между S2 и S6 не представляет трудно­
стей, так как в ней нет сколько-нибудь значи­
тельных сосудистых образований.
СРЕДНЯЯ ДОЛЯ
ПРАВОГО ЛЕГКОГО
При препаровке корня правого легкого спе­
реди, из переднебокового разреза, сделанного
по четвертому межреберью, из элементов корня
средней доли обнаруживается прежде всего сред­
недолевая вена. Она, как указывалось выше,
чаще впадает одним или двумя стволами в верх­
нюю легочную вену, реже — в нижнюю и совсем
редко — в левое предсердие самостоятельным
стволом. Иногда вена одного сегмента (Vs)
впадает в верхнюю легочную вену, а вена дру­
гого сегмента (V4) — в нижнюю.
Спереди от вены и ниже ее имеются неболь­
шое количество жировой клетчатки и один или
двд лимфатических узла, принимающих лимфу
как от средней, так и от верхней (S3) долей.
Их увеличение и особенно наличие метастазов
рака затрудняют препаровку вены, а иногда ука­
зывают на широкое распространение опухоле­
вого процесса, требующего удаления всего лег­
кого. Среднедолевая вена имеет своими исто­
ками две сегментарные вены (V4 и V5). V4 яв­
ляется межсегментарной веной между IV и V
сегментами, a V5 — центральной веной V сег­
мента (рис. 10).
23
Рис. 11. Раздельное отхождение артерий средней доли (А^
и As) от междолевого артериального ствола.
Вторым элементом, требующим препаровки
до разделения межсегментарной щели, является
среднедолевая артерия. Ее лучше всего препари­
ровать из главной междолевой щели. Плевра
вскрывается ближе к месту соединения косой
и поперечной щелей. Верхняя доля отводится
вверх, средняя — кпереди, задняя — книзу и
кнаружи. Препарируется междолевой ствол
легочной артерии (от Аг до А44.5). Первой вет­
вью, отходящей от передней поверхности меж­
долевого ствола, является А4 5. Она направляет­
ся вверх и кнаружи и вскоре делится на две вет­
ви. Иногда она отходит двумя стволами (рис. 11).
Другие варианты, которых не так много, боль­
шого практического значения не имеют.
Бронх средней доли отходит от промежуточ­
ного бронха, от передненаружной его поверх­
ности, и направляется вверх и наружу. Длина
его варьирует от 0,5 до 3 см. Далее он делится
на два сегментарных бронха: В4 и В5. В5 аэри­
рует внутренний (V) сегмент средней доли,
В4 — наружный (IV) сегмент. Его препарируют
спереди, после перевязки и пересечения V4, 5.
У места отхождения с редне до левого бронха
расположен нижний междолевой лимфатиче­
ский узел, собирающий лимфу как из средней,
так и из нижней долей. Увеличение его с раз­
витием в нем рубцовой ткани и карнификации
может вести к сдавлению мембранозной части
среднедолевого бронха и ателектазу доли.
24
Межсегментарная поверхность у средней до­
ли имеется лишь между S5 и S3. Ориентиром для
разделения ее, как это изложено выше, явля­
ется V3c. Ею же следует руководствоваться при
препаровке в случае рудиментарной поперечной
щели.
иногда — выше его. Для точного ориентирова­
ния при препаровке нижнедолевого бронха важ­
но найти вначале место отхождения средне­
долевого бронха, а затем Be. В дальнейшем,
препарируя базальный бронх к периферии,
находят отходящий от передней поверхности
базального бронха В7 и тем убеждаются в пол­
ноте выделения нижнедолевого бронха.
нижняя доля
ПРАВОГО ЛЕГКОГО
СЕГМЕНТЫ ПРАВОГО ЛЕГКОГО
Препаровку корня нижней доли правого лег­
кого следует вести из переднебокового досту­
па через пятое межреберье, со стороны сре­
достенной щели. Здесь обнаруживается ниж­
няя легочная вена, собирающая кровь только
из нижней доли (о случаях слияния ее со сред­
недолевой или только с V4 указывалось выше).
Препаровка вены связана с рассечением легоч­
ной связки и обнажением параэзофагеальных
лимфатических узлов и наружной стенки пище­
вода.
Артерия нижней доли является продолже­
нием междолевого ствола. Ее легче всего обна­
ружить в главной междолевой щели, сместив
верхнюю долю вверх, оттянув среднюю вперед
и медиально, а нижнюю оттеснив вниз и кнару­
жи. Под плеврой у места отхождения средне­
долевого бронха локализуется, как это уже со­
общалось, нижний междолевой лимфатический
узел. Здесь же отходит среднедолевая арте­
рия. После этого артерия считается нижнедо­
левой. Несколько периферичней в половине слу­
чаев отходит артерия верхнего (VI) сегмента
нижней доли. Не так уж редко Аб отходит на
одном уровне со среднедолевой артерией и даже
выше ее. Часто отпрепарировать эту развилку
артерий не позволяет увеличенный нижний меж­
долевой лимфатический узел. В этих случаях
следует сначала осторожно выделить узел и
только после этого препарировать артерию с
ее ветвями. Далее, при типичном делении арте­
рии, от ее передней поверхности отходит арте­
рия паракардиального сегмента (А7), а ниже —
переднебазальная артерия (А8); затем артерия
делится на два ствола: А9 и А)0 (рис. 12). Неред­
ко при рассыпном типе ветвления артерии после
отхождения Аб базальная артерия сразу делится
на все или почти на все свои сегментарные вет­
ви (А7, А8, А9 и Аю). При необходимости пере­
вязать нижнедолевую артерию приходится
перевязывать и пересекать все сегментарные
артерии по отдельности либо группами — Аб,
Aj, в и Ад ioБронх нижней доли правого легкого начина­
ется ниже отхождения от промежуточного ство­
ла среднедолевого бронха. Типично периферич­
ней кзади и кнаружи отходит бронх верхнего
(VI) сегмента (Вб). Во, как правило, отходит
на одном уровне со среднедолевым бронхом, а
В верхней доле правого легкого чаще всего
удаляются задний (II) и верхушечный (I) сег­
менты. Редко резецируется передний (III) сег­
мент. При туберкулезе легкого часто удаляются
I и II сегменты вместе, производится бисегментэктомия. Поэтому целесообразно рассмотреть
анатомию корней всех трех сегментов верхней
доли правого легкого.
ВЕРХУШЕЧНЫЙ (I) СЕГМЕНТ
ПРАВОГО ЛЕГКОГО
При переднебоковом доступе через четвер­
тое межреберье, препарируя легкое по медиа­
стинальной поверхности, первой, как и при пре­
паровке корня легкого, встречается верхняя
легочная вена с ее двумя истоками. Верхний
исток образуется центральной веной (Vi). Она
расположена в верхнем отделе верхней легоч­
ной вены и слагается из двух ветвей V,a и Vn
(рис. 13). Обе эти ветви межсегментарные, рас­
положенные между Si и S2; в межсегментарной
плоскости между S, и S3 проходит ветвь от
V3 — V3b. Часто, однако, верхний исток (Vi)
у места деления верхней легочной вены отсут­
ствует и Vi вливается в V2 позади бронха (зад­
ний отток). Этот вариант, с точки зрения хирур­
гической, неопасен, так как при удалении вер­
хушечного сегмента в этих случаях Vi выде­
ляется и перевязывается последней. Зон, ли­
шенных венозного оттока, не остается.
Редко встречающийся (5 %) передний тип
венозного оттока может быть опасным в хирур­
гическом отношении. В этих случаях V2 «ис­
чезает» со своего места. В нижней части легоч­
ной вены (адней сегментарной вены не обна­
руживается. Она вливается в верхушечную вену,
образуя необычно мощный ствол верхнего
истока (рис. 14). Перевязка ее при удалении
верхушечного сегмента грозит затруднением
оттока крови из заднего сегмента, его болезнью
в послеоперационном периоде.
Вариантом, требующим большого внимания
хирурга, являются также раннее слияние Vi и
V3 и впадение их общего ствола в верхнюю ле­
гочную вену. Перевязка и пересечение этого
общего ствола могут привести к затруднению
оттока крови из S3.
25
Рис. 12. Ветвление артерий и вен нижней доли правого
легкого.
26
Рис. 13. Вены верхушечного сегмента правого легкого спе­
реди.
1 —артерия верхушечного сегмента (Ai); 2 — артерия перед­
него сегмента (Аз); 3 — вена верхушечного сегмеита; 4 — цент­
ральная вена (Vla); 5 — межсегментарная вена между верху­
шечным и передним сегментами (VjB ); 6 — вена заднего сег­
мента (VO-
му сегменту или одному из субсегментов его.
Это, как правило, может быть распознано по
калибру этой артерии.
Обычно Ai и Аз, отходящие от переднего
ствола, одинаковы по диаметру. Имея в виду,
что Аз довольно стабильна, от нее очень редко
отходят ветви к другим сегментам, она может
считаться как бы эталоном определения диа­
метра и для других артерий. В случае слияния
Ai и Аг (или одной из субсегментарных арте­
рий заднего сегмента) верхушечная артерия
оказывается более мощной по сравнению с АзСледовательно, при удалении Si она должна
отпрепарироваться вглубь легочной паренхи-
Перевязка и пересечение Vi позволяют пе­
рейти к препаровке артерий сегмента.
Кзади и краниально от верхней легочной
вены локализуются артерии верхней доли, в том
числе и верхушечная (Ai).
Передний ствол в типичных случаях делится
на две ветви: Ai и Аз. Аг отходит от междо­
левого ствола легочной артерии в виде одной
или двух так называемых рекуррентных арте­
рий. Артерия верхушечного сегмента в даль­
нейшем делится на две ветви, которые и направ­
ляются к обоим субсегментам. Однако часто
этот верхний ствол (Ai) несет кровь не только
к верхушечному сегменту, но и ко всему задне­
27
ЗАДНИЙ (II) СЕГМЕНТ
ВЕРХНЕЙ ДОЛИ ПРАВОГО ЛЕГКОГО
Рис. 14. Вариант «полного» венозного оттока верхней доли
правого легкого.
мы на 0,5—1 см, и здесь обнаружится отходя­
щая от нее кзади ветвь А2. Перевязывать и пере­
секать А| в этих случаях надо периферичней
отхождения Аг- Следует указать, что ошибки,
т. е. перевязка AL 2 у ее устья, нарушают, ко­
нечно, функцию S2 или одного из его субсег­
ментов, но не приводят к каким-либо тяжелым
послеоперационным осложнениям.
После идентификации, перевязки и пере­
сечения артерии верхушечного сегмента кзади
от переднего ствола легочной артерии опре­
деляется верхнедолевой бронх. Он делится на
3 сегментарные ветви: В|, В2 и Вз. Верхушечный
сегментарный бронх (В,) находится кзади и
краниально от места отхождения переднего
сегментарного бронха, направляется вверх
и несколько кнаружи. В дальнейшем он делит­
ся на две субсегментарные ветви (В1а и Вц,).
Верхушечный сегмент (Si) широко взаимо­
связан с S2 и S3. Межсегментарные плоскости
между этими сегментами хотя неправильной
формы, но все совершенно четкие. Связь между
сегментами рыхлая, легко разъединяемая.
В межсегментарной плоек сти и между Si и S2
проходит V2a, а в плоскости между Si и S3 соби­
рает кровь Vib.
Корень заднего (II) сегмента как из передне­
бокового, так и бокового доступов отпрепари­
ровать труднее, чем корень Si. При препаровке
корня легкого верхняя легочная вена встреча­
ется и выделяется первой. Вена заднего про­
тока наибольшая из всех протоков верхней
легочной вены. Она собирает кровь порой не
только из So, но и из других сегментов верхней
доли и даже из S6. При типичном оттоке крови
из верхней доли задняя вена образуется из
слияния следующих венозных стволов: межсег­
ментарной вены между Si и So — V2a, централь­
ной вены S2 — V2b и межсегментарной вены
между So и S3 — V2c. Часто в нее впадают не­
большие вены из S3 (в 60 % случаев) и из Sfi
(в 5—10 %).
Межсегментарная вена V2a, собирающая кровь
из S, и So, расположена субплеврально спере­
ди и хорошо видна. Она служит ориентиром при
препаровке межсегментарной плоскости. V2
вливается в общий ствол задней вены позади
бронха II сегмента (рис. 15). Ее перевязывать
не следует из-за большого числа и довольно
значительных притоков к ней из переднего ос­
тающегося сегмента.
Центральная вена —
V2b — при типичном, наиболее частом ветвле­
нии проходит вдоль бронха и артерии и влива­
ется вблизи от устья V2a, т. е. позади долевого
бронха, вблизи и кпереди отхождения В2. Меж­
сегментарная вена — V2c — собирает кровь
из S2 и Si и вливается в уже объединенную
вену V2a и V2b медиальней их. После этого обра­
зуется общий ствол V2. Он впадает в этих случаях
в общий ствол верхней легочной вены по его
задней поверхности.
При другом варианте, так называемом зад­
нем типе ветвления, в верхнюю легочную вену
впадает вена двух сегментов — S, и S2. Только
после слияния этих вен в образовавшийся об­
щий ствол впадает межсегментарная вена
между Si и S2 — V2a. Через междолевую щель
также можно отпрепарировать основной ствол
V2. V2a и V2c, являясь межсегментарными вена­
ми, могут быть ориентиром при разделении сег­
ментов по их межсегментарным плоскостям.
Сверять правильность определения вариантов
ветвления вен при удалении заднего сегмента
возможно прежде всего выделением верхней
легочной вены, прослеживанием ее истоков
к периферии, а также распрепарировав корень
верхней доли через поперечную междолевую
щель.
Рис. 15. Истоки вены II сегмента (V2) верхней доли пра­
вого легкого.
28
29
Рис. 16. Частный вариант кровоснабжения заднего (S?)
сегмента общим отхождением передней (А,) и задней (Аз)
сегментарных артерий.
Рис. 17. Вариант раздельного отхождения артерий верху­
шечного (А|), заднего (Аг) и переднего (А3) сегментов.
Задний сегмент в большинстве случаев снаб­
жается кровью из малого круга кровообраще­
ния через артериальный ствол, выходящий из
междолевой артерии (так называемой рекур­
рентной артерии). Она обнаруживается путем
препаровки легочной артерии. Артерия, отдав
передний ствол, далее идет вниз и кнаружи.
Этот ствол называется междолевым. От перед­
него, или, как его называют, иногда, верхнего,
ствола отходят артерия переднего сегмента Аз,
идущая вверх и наружу, и артерия верхушеч­
ного сегмента А|. Иногда от А| и ее субсегмен­
тарной ветви отходит небольшой ствол ко вто­
рому сегменту S2.
Наряду с этим вариантом ветвления легоч­
ной артерии, существуют и другие.
Вторым вариантом по частоте является от­
хождение от переднего ствола крупной ар­
терии — до 1,2 см в диаметре, являющейся
объединенным стволом А| и Аг. От этого общего
ствола отходят сначала верхушечная артерия —
А| и две ее ветви — А1а и А1в, а затем кзади
и кнаружи — Аг. Реже Аг отходит от одной из
субсегментарных артерий S|. Направление и
диаметр могут подсказать, является ли это
стволом или часть крови идет в S2 через рекур­
рентную артерию (рис. 16).
Третьим и самым редким вариантом ветвле­
ния артерии является отхождение от переднего
(верхнего) ствола легочной артерии трех само­
стоятельных сегментарных артерий: Aj, Аг и Аз.
Тогда рекуррентной артерии нет (рис. 17). Хи­
рург при препаровке переднего ствола легочной
артерии, увидев ветвление его на две одинако­
вые артерии диаметром примерно около 0,5—
0,9 см, может с уверенностью утверждать, что
Sj снабжается кровью из междолевого ствола,
и найдет Аг отходящей от него вскоре (0,5—
1 см) от его начала. Аг имеет направление кза­
ди и кнаружи, под верхнедолевой бронх у ме­
ста отхождения от главного. Если же от перед­
него ствола отходит одна артерия диаметром
примерно 0,6—0,8 см, а вторая оказывается
калибром вдвое большим, это означает, что Аг
отходит от этого крупного ствола и рекуррент­
ной артерии либо нет. либо она очень малень­
кая. Когда от переднего ствола отходят три
почти равные по калибру артерии и одна из них
направляется книзу и кнаружи, это свидетель­
ствует, что она представляет собой часть Аг.
30
Наряду с этими методами идентификации
артерий, наиболее верными являются препа­
ровка того или иного ствола к периферии и про­
слеживание его направления.
В корне II сегмента при препаровке его из
переднебокового доступа бронх встречается
последним, т. е. он расположен кзади и несколь­
ко краниальней от вен и артерий. Верхнедоле­
вой бронх в большей части случаев делится на
три сегментарных бронха: В|, В2 и В3. Задний
сегментарный бронх отходит кзади и кнару­
жи, и, как у других сегментарных бронхов, ка­
либр его колеблется от 0,7 до 1,2 см, длина —
от 0,3 до 1,5 см. Далее он делится на две суб­
сегментарные ветви.
Однако, наряду с таким типичным делением
и отхождением В2, существуют и другие вариан­
ты деления. Долевой бронх иногда образует
не трифуркацию, а бифуркацию. Происходит
объединение сегментарных бронхов. Bi объе­
диняется с В2 или В2 — с В3. При этом объеди­
ненный бронх всегда имеет калибр, вдвое боль­
ший, чем обычный сегментарный бронх. Окон­
чательное определение варианта возможно
лишь при препаровке увеличенного в диаметре
бронха к периферии. Отходящий от него кзади и
кнаружи бронх и будет являться В2. Наконец,
в самых затруднительных случаях идентифика­
ция бронха может быть получена пережатием
его мягким зажимом и раздуванием легкого.
Ателектаз типичного для S2 участка легкого
будет служить несомненным доказательством
такого варианта строения.
S2 имеет широкую межсегментарную связь
с Si и S3. С верхним сегментом (Se) нижней
доли легочная перемычка сохраняется ближе
к корню легкого. Это соединение редко бывает
значительным, трудностей при разъединении
S2 и S6 обычно не бывает. В этой плоскости
иногда проходит небольшая вена Vx2a или
Vx6a.
Плоскость между S2 и S< довольно обширна.
Межсегментарная вена V2a проходит глубоко,
со стороны плевры она не видна. Поэтому пре­
паровку и прослеживание V2a можно проводить
только после перевязки и пересечения У2Ь, А2
и обработки бронха. Прослеживая V2a( препари­
руют тем самым межсегментарную плоскость.
То же самое следует сказать и про препаров­
ку V2c, идущей между S2h S3.
ПЕРЕДНИЙ (III) СЕГМЕНТ
ВЕРХНЕЙ ДОЛИ ПРАВОГО ЛЕГКОГО
Корень переднего сегмента лучше всего пре­
парируется спереди, из переднебокового доступа.
После обнаружения и препаровки верхней
легочной вены, как указывалось выше, видно
впадение в нее в типичных, чаще всего встречаю­
щихся случаях, вен всех трех сегментов. Вена
переднего сегмента наиболее стабильна. Она
находится ниже (каудальнее) от Vi и V2. Вена
верхушечного сегмента (Vi) находится выше
всех, a V2 — посредине между Vi и V3 (рис. 18).
Самым нижним истоком верхней легочной вены
является вена средней доли (V4 S). При препа­
ровке V3 к периферии вскоре обнаруживается
деление ее на две ветви: V3a и V3b. V3b является
межсегментарной между S3 и S5. Она расположе­
на на поверхности почти под плеврой. V,a явля­
ется центральной веной S3 и собирает кровь из
ткани переднего сегмента между его субсег­
ментами. Между S3 и S4, если существует легоч­
ная перемычка между ними (при невыражен­
ное™ поперечной щели), находится V3c, впа­
дающая либо в общий ствол V3, либо в субсег­
ментарную ветвь V]. Чаще же всего при доста­
точной выраженности поперечной щели этой
вены нет.
Для того, чтобы увидеть артерию переднего
сегмента (А3), следует отпрепарировать перед­
ний ствол легочной артерии и отодвинуть книзу
верхнюю легочную вену. Нижняя ветвь перед­
него ствола и является Аз. Она имеет длину при­
мерно 1,4 см, диаметр — 0,7 см (рис. 19) и де­
лится на две субсегментарные ветви: А3а и Азь,
как правило, сопутствующие соответствующим
бронхам.
Бронх переднего сегмента (В3) открывается
при препаровке спереди лишь после перевязки
и пересечения V3 и А3, смещения переднего
ствола вверх (краниально), а верхней легоч­
ной вены — вниз (каудально). При этом в глу­
бине виден верхнедолевой бронх с отходящим
от него бронхом переднего сегмента (рис. 20).
Он редко варьирует, делясь сразу на субсегмен­
тарные бронхи.
Варианты деления субсегментарных брон­
хов встречаются не так уж редко. Иногда от
одного из субсегментарных бронхов может от­
ходить субсегментарный бронх к Si, реже —
к S2. Выявление этих вариантов, очень важных
с хирургической точки зрения, возможно при
пережатии мягким зажимом В3 и раздувании
легкого. Зона ателектаза (при знании пример­
ных границ сегмента), распространяющаяся
на соседние сегменты, может указать на тот
или иной вариант ветвления. Это может быть
обнаружено и при препаровке субсегментарных
бронхов к периферии. Обычно отхождение
субсегментарных бронхов соседних сегментов
происходит не далее 0,5—1 см, максимум 1,5 см,
от места деления сегментарного бронха на суб­
сегментарные.
Межсегментарные плоскости между S3 и S5
обозначаются, кроме зоны ателектаза после
пересечения В3, часто видимой поверхностно
расположенной межсегментарной веной V3b.
31
Рис. 18. Формирование вены Ill сегмента.
исключая некоторые детали строения сегмен­
тов, которые излагались выше.
Обнажение корня двух сегментов при перед­
небоковом доступе начинается с препаровки
вен Si. При этом, изолируя Vi, нужно отпре­
парировать два ее истока — Vja и Vib- Vja может
быть перевязана и пересечена. Vib следует
иметь ориентиром при препаровке межсегмен­
тарной плоскости между Si и S3 (рис. 21).
После этого препарируются передний ствол
легочной артерии и ее верхняя ветвь — А|. Часто
(см. калибр ее) от нее отходит и Аг. В тех слу­
чаях, когда Ai имеет обычный для сегментарной
артерии диаметр (0,3—0,6 см), Аг следует искать
отходящей от междолевого ствола (рекуррент­
ная артерия).
Между Si и Sv межсегментарные вены (Vla
и V3c) находятся в глубине легочной ткани, и
их можно обнаружить только после отделения
сегментов, т. е. после полной обработки корня
легкого. Тогда делается видным направление
Vib и V3c. Препарируя их, постепенно обна­
руживают межсегментарную плоскость. Вены,
идущие из S3, перевязывают. Стволы Vib и V3c
по возможности оставляют не перевязанными.
ВЕРХУШЕЧНЫЙ (S1) И ЗАДНИЙ (S2)
СЕГМЕНТЫ ПРАВОГО ЛЕГКОГО
Удаление Si —|— S2 имеет ряд особенностей,
что заставляет изложить строение этих двух
сегментов отдельно. Повторение необходимо,
32
Рис. 19. Препаровка сосудов корня верхней доли правого
легкого.
Рис. 20. Препаровка переднего сегментарного бронха (Вз)
правого легкого.
3 Зак. 0517
33
Рис. 21- Вены верхней доли правого легкого.
34
Перевязка А, 2 и пересечение ее позволяют
легко отпрепарировать бронх. Первым стволом,
отходящим в верхней части верхнего долевого
бронха, является В,. Иногда от него вскоре от­
ходит и В2. Однако чаще всего В2 отходит само­
стоятельно. Его можно отпрепарировать спе­
реди, с медиастинальной плоскости, обработав
сначала В|. После пересечения В| снизу дела­
ется легкодоступным для препаровки и В2. Удоб­
но также препарировать В2 и В| в обратном
порядке из междолевой главной щели. Из меж­
долевой щели легко препарировать и V2. В нее
вливаются V2a — центральная вена заднего
сегмента — и V2b — вена между S2 и S3. Меж­
сегментарные плоскости между S, и S2 препари­
руются в соответствии с вышесказанным.
ВЕРХНИЙ (VI) СЕГМЕНТ
НИЖНЕЙ ДОЛИ ПРАВОГО ЛЕГКОГО
НАРУЖНЫЙ (IV) СЕГМЕНТ
СРЕДНЕЙ ДОЛИ ПРАВОГО ЛЕГКОГО
При препаровке корня S4 спереди первой об­
наруживается верхняя легочная вена, нижним
истоком которой является среднедолевая вена.
Обычно вблизи устья V2 определяются два ее
истока: V5 и V4. Вена внутреннего (V) сегмента
вливается в общий ствол V2 медиальней и выше,
а устье V4 расположено несколько ниже и кна­
ружи. Чтобы не ошибиться, следует V 4 взять
на провизорную лигатуру. Вена наружного сег­
мента является одновременно и межсегментар­
ной веной между S4 и S5.
Артерию IV сегмента (А4) лучше всего пре­
парировать из главной (косой) междолевой ще­
ли. После разведения ее, при поднятой вперед
и вверх средней доле, смещении верхней доли
краниально и оттягивании нижней доли книзу
и наружу следует рассечь плевру, удалить ниж­
ний междолевой лимфатический узел, выделить
первую нижнедолевую артерию. Кверху от нее
отходит среднедолевая артерия (А4 5). Вскоре
она делится на два ствола — А4 и А5. Направле­
ние А4 определяет ее принадлежность. Эта ветвь
артерии перевязывается и пересекается (рис.
22).
Здесь же обнаруживается и среднедолевой
бронх с делением его на В4 и В5. Иногда они
отходят двумя отдельными стволами. Выделе­
ние и обработка бронха наружного сегмента
средней доли возможны как со стороны междо­
левой щели, так и спереди, с медиастинальной
поверхности. При последнем методе требуется
сначала перевязать и пересечь V4, взятую ранее
на провизорную лигатуру, а затем обработать
В4. Он, так же как и V4, определяет направле­
ние к наружному сегменту. Препаровка эле­
ментов корня легкого к периферии позволяет
избежать ошибки и не нанести ущерб оставляе­
мому S5.
3*
35
Корень верхнего сегмента лучше всего об­
наруживается после широкого разведения глав­
ной (косой) междолевой щели. Для этого верх­
нюю и среднюю доли приподнимают вверх и
кпереди, а нижнюю — низводят вниз и кнаружи.
У места слияния косой и поперечной щелей
и находится корень VI сегмента. После рассе­
чения плевры и удаления нижнего междолевого
лимфатического узла первым обнаруживается
артериальный ствол с отходящей кзади и кнару­
жи Аб. Несколько выше отходит А4 s. Ниже
места отхождения А6 препарируются базаль­
ные сегментарные артерии. А(| довольно посто­
янна, диаметр ее колеблется от 1,1 до 2,2 мм,
длина до ветвления на субсегментарные арте­
рии равна 0,5—1,5 см. Варианты отхождения
ее от основного ствола по отношению к устью
среднедолевой артерии указаны выше.
Далее, как правило, Ас делится на три ветви:
Аба, Абь и Абе Они идут к внутреннему, верхнему
и наружному субсегментам.
Однако нужно отметить варианты, имеющие
хирургическое значение. Иногда от междолевого
ствола легочной артерии одной довольно мощ­
ной ветвью отходит А2+6. Вскоре он ветвится.
Одна из ветвей направляется вверх, в оттяну­
тую туда верхнюю долю, вторая — кзади и вниз,
к Sb. Перевязывать этот общий (А2 6) ствол
не следует.
Встречается вариант ветвления, когда субсег­
ментарные артерии Sb отходят самостоятельно,
без слияния в общий ствол Ав.
После выделения, идентификации артерий,
перевязки и пересечения их препарируется
бронх.
Вб постоянен, отходит от задненаружной
поверхности нижнедолевого бронха. Диаметр
его колеблется от 0,8 до 1,2 см. Длина до деле­
ния на субсегментарные бронхи равна 0,2—
1,2 см. Так же как и артерия, бронх может от­
ходить либо ниже отхождения В4 5, либо на
одном уровне и даже выше уровня среднедоле­
вого бронха.
Однако направление бронха книзу и кнаружи
и расположение под артерией указывают на
то, что препарируется именно Вв- Редким, но
в хирургическом отношении важным вариантом
является отхождение к VI сегменту от основ­
ного ствола нижнедолевого бронха раздельно
двух и даже трех бронхов. Обработка их долж­
на производиться раздельно.
Вена верхнего (VI) сегмента нижней доли
правого легкого может быть отпрепарирована
либо через междолевую щель, либо спереди через
медиастинальную плоскость. В первом случае
культю артерии (Ав) и бронха (BR) следует от-
Рис. 22. Выделение артерий средней доли (А< и As) и VI
сегмента (Ав) правого легкого.
1 —артерия наружного сегмента (А4); 2 — артерия внутреннего
сегмента (АО; 3 — бронх средней доли (В4 5).
При препарировании вен спереди находят сна­
чала нижнюю легочную вену. Она имеет три
истока: Уб, верхнюю базальную вену (V7, Ve)
и нижнюю базальную вену (Ve, V10). Уб пред­
ставляет собой самый верхний исток. При пре­
паровке ее к периферии выявляются все ее
ветви, в том числе У6с.
Препарируя V6c, разделяют межсегментар­
ную плоскость между Se и базальными сегмен­
тами. Вверху Se нередко имеет довольно широ­
кую легочную перемычку с S2, особенно в меди­
альной их части. В этих случаях кровь из обоих
сегментов собирает У2с. В редких случаях У6а
вести книзу и кнаружи, тогда откроется Уб,
вливающаяся верхним истоком в нижнюю ле­
гочную вену. Она вскоре делится на V6a, V6b
и V 6с. V6a — межсегментарная вена, располо­
женная между верхним и внутренним субсег­
ментами. V6b — также межсегментарная, распо­
ложенная между наружным и верхним субсег­
ментами. V6c — межсегментарная вена, соби­
рающая кровь из Se и базальных сегментов.
Первые две вены могут быть легко перевязаны
и пересечены. V6c нужно сохранить как ориен­
тир при препаровке межсегментарной плоско­
сти между Se и базальными сегментами.
36
Рис. 23. Выделение и обработка артерий и бронха VII сегмента.
и V6b впадают одним или двумя стволами через
легочную перемычку между S2 и Se во вторую
вену. В этих случаях разделение межсегментар­
ной плоскости должно производиться осторож­
но, чтобы не повредить или не перевязать мощ­
ный ствол V2. Это грозит застоем крови в S2.
базальный исток (V7 + Vg). Эта вена берется
на провизорную лигатуру, затем раскрывается
главная междолевая щель.
Так же как и при препаровке корня верхнего
(VI) сегмента, в верхней части щели рассека­
ется плевра, удаляется нижний междолевой
лимфатический узел (если он увеличен и меша­
ет препаровке артерии) и выделяется нижне­
долевая артерия у места ее ветвления на А4,
А5 и А6. Препарируя артериальный ствол далее,
к периферии, первой с медиальной поверхности
базальной артерии отходит А7. Ее длина равна
0,3—0,7 см, диаметр — 0,3—0,6 см. Эта артерия
вскоре делится на две субсегментарные арте­
рии.
ВНУТРЕННИЙ (ПАРАКАРДИАЛЬНЫЙ) СЕГМЕНТ
НИЖНЕЙ ДОЛИ ПРАВОГО ЛЕГКОГО
Корень паракардиального (внутреннего) сег­
мента следует препарировать спереди, через
переднебоковой доступ по пятому межреберью.
Парамедиастинально препарируется вначале
нижняя легочная вена. Выделяется ее верхний
37
Рис. 24. Ветвление базальной артерии правого легкого (Д7,
Ав, Ач и А[п).
1 — артерия средней доли; 2 — артерия верхнего сегмента (Аг,);
3 — медиобазальная сегментарная артерия (А7); 4 — передне­
базальная сегментарная артерия (Ак); 5 — наружнобазальная
сегментарная артерия (Ач): 6—заднебазальная сегментарная
артерия (А|0); 7 — бронх верхнего сегмента (В6); 8 — задне­
базальный бронх (Ви,); 9 — передне- и наружнобазальный сег­
ментарные бронхи (Be, 9).
Межсегментарной веной между S7 и базаль­
ными сегментами является V,o, т. е. все вены
VII сегмента могут быть без ущерба перевязаны
и пересечены.
Под артерией локализуется бронх паракардиального сегмента, выделение которого облег­
чается после перевязки и пересечения А7
(рис. 23).
В7 отходит от нижнедолевого бронха, отступя
на 0,5—1,2 см от места отхождения Be, и вскоре
делится на два субсегментарных бронха.
Обработка бронха и пересечение его откры­
вают доступ к вене сегмента. Вена VII сегмента
вливается в большинстве случаев в верхнеба­
зальный ствол. Однако нередко она двумя само­
стоятельными ветвями вливается и в верхнюю,
и в нижнюю базальные вены. Их легко иденти­
фицировать, прослеживая в направлении сег­
мента.
БАЗАЛЬНЫЕ СЕГМЕНТЫ
НИЖНЕЙ ДОЛИ ПРАВОГО ЛЕГКОГО
Корни базальных сегментов (S7, Sb, Sq и Sm)
препарируются так же, как и корни S6 и S?, т. е.
из переднебокового доступа по пятому межре­
берью.
Вначале целесообразно выделить нижнюю
легочную вену и ее притоки:
верхнюю и ниж­
нюю базальные вены.
38
Рис. 25. Отделение базальных сегментов от VI сегмента
правого легкого
1 —культя базального бронха (В7 8 д 10 ); 2 — культя арте­
риального ствола сегментов базальной пирамиды; 3 — вена меж­
ду верхним и внутренним субсегментами (V6a).
После этого широко раскрывается главная
(косая) междолевая щель. Препарируется
нижнедолевая артерия. Нужно обязательно
выделить А6 и А4 5. Периферичней этих арте­
рий открывается ствол базальных сегментов.
В этом можно убедиться также при препаровке
артерии. Первой внутрь и книзу отходит А?,
второй вперед и книзу — A«. Далее артериаль­
ный ствол делится на ветви, идущие к девятому
и десятому сегментам — Ад и Аю (рис. 24).
Для препаровки базальных вен в междолевой
щели необходимо не только перевязать и пере­
сечь базальную артерию и бронх, но и разде­
лить легочную связку. Тогда открываются ниж­
няя легочная вена и ее три истока — Ve, верх­
няя и нижняя базальные вены. Это можно сде­
лать и с медиастинальной стороны.
Межсегментарная поверхность между базаль­
ными сегментами и Se, как указывалось выше,
разделяется, ориентируясь на V6a (рис. 25).
39
ЛЕВОЕ ЛЕГКОЕ
Строение корня левого легкого отличается от
правого. Вблизи корня левого легкого распо­
ложены такие образования, как аорта, развет­
вление общей легочной артерии на правый и
левый ее стволы; нередко наблюдается раннее
слияние легочных вен. Редко, но все же встре­
чается незаращенный артериальный (боталлов)
проток. Под аорту уходит вблизи артериаль­
ного протока, ответвляясь от блуждающего нер­
ва, возвратная ветвь его, иннервирующая левую
половину гортани. Поэтому препаровка корня
левого легкого представляет ряд особенностей.
КОРЕНЬ ЛЕВОГО ЛЕГКОГО
При переднебоковом доступе по четвертому
межреберью на средостенной поверхности вид­
ны диафрагмальный нерв с перикардо-диафраг­
мальными сосудами и блуждающий нерв. Иног­
да видна возвратная его ветвь, отходящая от
него медиально и огибающая дугу аорты у аор­
тальной связки. Отчетливо видны дуга аорты
и отходящая от нее подключичная артерия,
корень легкого.
При препаровке корня следует рассечь плев­
ру, субплевральную фасцию и клетчатку под
ней. Первой обнажается верхняя легочная вена.
В нее сверху, почти у перикарда, впадает вена
верхушечного и заднего сегментов (Vj 2), иду­
щая вверх и несколько кнаружи, перекрывая
поперечно легочную артерию и ее ветви
(рис. 26—28). Вблизи устья V1>2 обнаруживают­
ся V3 и V4>5.
Краниально и несколько кзади от легочной
вены находится левая легочная артерия. Арте­
рия вскоре после выхода ее из полости пери­
карда отдает общий ствол Alt 2, идущий вверх
и несколько кнаружи. Второй артерией, отхо­
дящей здесь же, у устья А, 2, является артерия
переднего (III) сегмента (Аз). После этого так
называемый междолевой ствол направляется
назад, огибая левый главный бронх. При пре­
паровке легочной артерии в сторону средосте­
ния встречается прежде всего лимфатический
узел — первый узел корня легкого, собирающий
лимфу из верхней зоны его. За ним, медиальней, препарируется артериальная связка — за­
ращенный артериальный проток. Поэтому узел
получил название «узла боталловой связки»
(по аналогии с лимфатическим узлом непар­
ной вены справа). Важным элементом корня
легкого, требующим специальной препаровки,
является возвратная ветвь блуждающего нерва.
Для обнаружения ее необходимо рассечь плев­
ру средостения по ходу этого нерва. Препа­
рируя осторожно тупфером нерв, удается на
передней поверхности дуги аорты увидеть отхо­
дящий от него медиально ствол нижнего гор­
танного нерва. Он, как указывалось выше, оги­
бает аорту у аортальной связки и уходит вверх.
Повреждение его ведет к параличу левой голо­
совой складки, потере голоса и нарушению каш­
ля. При препаровке левой легочной артерии
к периферии обнаруживается первой А, 2. Она
уходит вверх и кнаружи и несколько дорсально,
направляясь к верхушечному сегменту. Часто
(в 80—90 %) вскоре от нее отходит ствол кзади
и кнаружи; это — А2.
Второй ветвью, отходящей от основного ство­
ла левой легочной артерии, является Аз. Она
направляется вперед и кнаружи, к переднему
сегменту. Изредка спереди от легочной артерии
отходит третий ствол и направляется вниз и
наружу к язычковым сегментам. Это А4 s (или
только А4). После этого легочная артерия, как
указывалось выше, направляется вниз, огибая
главный левый бронх.
Ниже и несколько кзади от верхней легочной
вены обнаруживается нижняя легочная вена
с ее истоками от сегментов нижней доли.
Под верхней легочной веной и ниже (каудальнее) артерии находится главный бронх левого
легкого. Он вскоре по выходе из средостения
делится на две ветви — верхнедолевой и ниж­
недолевой бронхи. Под бронхом, в клетчатке,
локализующейся на мембранозной части его,
проходят бронхиальные сосуды и нервы. Кзади
(дорсально) при препаровке по направлению
к средостению под бронхом сверху вниз идут
пищевод и блуждающий нерв по латеральной
поверхности последнего.
Часто, особенно при далеко зашедших фор­
мах рака легкого, с метастазами в лимфатиче­
ские узлы корня, для определения возможно­
сти удаления легкого, требуется ориентировать­
ся в полости перикарда.
Перикард вскрывается кзади (дорсально)
от диафрагмального нерва. В полости перикарда
видна левая легочная артерия, сливающаяся
с правым стволом. Верхняя легочная вена на­
ходится ниже, направляется поперечно и влива­
ется в левое предсердие. Еще ниже обнаружи­
вается нижняя легочная вена. Так же как и
справа, сосуды легкого располагаются мезоперикардиально. Здесь также имеются углубления
перикарда, отмеченные выше, при описании
правой стороны (рис. 29).
Такое расположение сосудов легкого слева
требует особой осторожности в выделении их.
Надо иметь в виду прежде всего близость обще­
го ствола легочной артерии. Поэтому при выде­
лении левой легочной артерии диссектором
может быть повреждено место отхождения пра­
вой легочной артерии или захвачен в лигатуру
общий ствол ее, т. е. центральней места отхож­
дения правой легочной артерии. При незара-
40
Рис. 26. Анатомическое взаимоотношение элементов корня
верхней доли правого легкого.
1 — бронх; 2 — артерия; 3 — вена.
41
Рис. 27. Вены верхней доли левого легкого.
1 — верхняя легочная вена; 2 — нижняя легочная вена; 3 — легоч­
ная артерия.
42
Рис. 28. Артерии левого легкого.
43
Рис. 29. Сосуды корня левого легкого из полости перикарда.
1 — легочная артерия; 2 — верхняя легочная вена; 3 — нижняя
легочная вена; 4 — ушко сердца.
щенном артериальном протоке, что встреча­
ется очень редко, имеется отчетливое увеличе­
ние диаметра левой легочной артерии, видно
усиление пульсации, прослеживается пульсиру­
ющий кровоток.
Верхняя легочная вена внутри полости пери­
карда проходит также мезоперикардиально.
Между артерией и веной в перикарде образу­
ется углубление (recessus) с заворотами выше
и ниже вены. У предсердия вена часто лежит
свободно. Здесь легче обойти ее инструментом
и лигировать.
Нижняя легочная вена в полости перикарда
находится почти на одном уровне с верхней,
располагаясь чуть ниже последней. Ее отно­
шение к перикарду такое же, как и верхней
легочной вены.
Иногда вены, прежде чем войти в левое пред­
сердие, сливаются вместе. Это происходит либо
в полости перикарда, либо вне его, что не только
создает трудности в выделении массивного об­
щего венозного ствола, но также опасно при
наложении лигатуры из-за прорезывания стен­
ки сосуда. Лучше в этих случаях общий веноз­
ный ствол обеих вен прошивать прошивателем
ушка сердца.
При внутриперикардиальном препарировании
сосудов левого легкого выделение бронха воз­
можно только после рассечения заднего листка
перикарда.
44
ДОЛИ ЛЕВОГО ЛЕГКОГО
ВЕРХНЯЯ ДОЛЯ
ЛЕВОГО ЛЕГКОГО
Доступ к корню верхней доли левого легкого—
переднебоковой через четвертое межреберье.
Первой, как и при препаровке корня лег­
кого, встречается верхняя легочная вена, соби­
рающая кровь из всей верхней доли. Первой
ветвью ее сверху является V1+2, второй ветвью,
находящейся несколько ниже первой,— вена
переднего сегмента (V3). Третьим истоком верх­
ней легочной вены является ствол, обнаружи­
ваемый наиболее каудально,— вены язычка
(V4,5).
Для препаровки артерии и ветвей ее к верх­
ней доле лучше всего перевязать и пересечь
верхнюю легочную вену. Главный ствол левой
легочной артерии может быть отпрепарирован
и после отведения верхней легочной вены книзу.
Препарируя артерию к периферии, первой
ветвью ее встречается артерия верхушечного
сегмента (А>). Это бывает в ’/з случаев. Чаще
же стволом, отходящим выше других, является
объединенный ствол I и II сегментов (Аг 2)
(рис. 30), а порой и переднего сегмента (А3).
Тогда этот общий ствол, так же как и справа,
целесообразно называть передним, или верхним,
стволом легочной артерии.
В 50 % случаев встречается ветвление арте­
рий с объединением А| и А2 — А,. 2, А3 отхо­
дит самостоятельно и лучше всего обнаружи­
вается после перевязки и пересечения верхней
легочной вены. Она направляется вверх, кна­
ружи и кпереди. Иногда ее (А3) лучше обнару­
жить в верхней части междолевой щели, когда
артерия отходит от наружной поверхности ар­
териального ствола.
Артерии язычка препарируют из междолевой
щели. Верхняя доля и язычок отводятся впе­
ред и вверх, нижняя доля и Se — вниз и кна­
ружи.
Препаровку проходящего в нижней части ще­
ли артериального ствола часто затрудняет уве­
личенный междолевой лимфатический узел.
Его нужно осторожно отпрепарировать и уда­
лить. От отпрепарированной артерии отходят А 4 5
и Аб. Вариантов отхождения язычковой артерии
и артерии верхнего сегмента нижней доли су­
ществует три: 1) А4> 5 отходит выше устья А6;
2) А4 5 отходит на одном уровне с А6 (рис. 31)
и 3) А4 5 отходит ниже устья Аб. Все это можно
наблюдать на протяжении 1—2 см.
А4_5, отойдя от общего ствола, направляется
к язычку. Идентификация ее труда не представ­
ляет. Она вскоре делится на две ветви — А4
и Аб. Нередко эти артерии отходят от основ­
ного ствола самостоятельно.
Рис. 30. Взаиморасположение сосудов и бронхов верхней
доли левого легкого.
Не так редко А4 и Аб отходят, как указыва­
лось выше, от передней поверхности легочной
артерии, после ответвления Ai, 2 и Аз. Направ­
ляются они книзу под веной верхушечного сег­
мента и кпереди от бронха (передний тип кро­
воснабжения). Иногда одна из артерий язычка
(А4) идет впереди бронха, другая (А5) — сзади.
Бронх верхней доли левого легкого лучше
всего препарировать спереди после перевязки
верхней легочной вены, артериальных ветвей,
идущих к сегментам верхней доли. При этом,
так же как и при препаровке корня легкого, об­
наруживается сначала главный бронх. При его
препаровке к периферии освобождается его
бифуркация, верхнедолевой и нижнедолевой
бронхи.
Со стороны междолевой щели обнаружить
верхнедолевой бронх можно только после
перевязки А4 5, если она отходит позади брон­
ха, а также А3 и А2, в случае их задней локали­
зации. Для идентификации верхнедолевого
бронха надо убедиться в отхождении нижне­
долевого.
От бронха верхней доли левого легкого, ниже
на 0,5—1,5 см, ответвляется Вь Слева, в отличие
от ветвления верхнедолевого бронха справа,
45
1
3
2
Рис. 31. Препаровка артерий наружного и внутреннего сег­
ментов в междолевой щели.
1 —артерия наружного сегмента (А4); 2 — артерия внутреннего
сегмента (As); 3 — артерия верхнего сегмента нижней доли (Ак).
Bi часто вскоре отдает ветвь к заднему (S2)
сегменту. Поэтому его обозначают Вь 2 (рис. 32).
Вторым бронхом, отходящим от верхнедолево­
го бронха, является Вз. Его устье расположено
рядом с устьем В, 2, несколько ниже и спереди
от него. Вз идет вверх и кнаружи, аэрируя пе­
редний сегмент верхней доли левого легкого.
Третьим бронхиальным стволом, отходящим от
верхнедолевого бронха, является В4 5. Он вско­
ре делится на два бронха — В4 и В5.
Межсегментарной поверхностью верхней доли
является легочная перемычка с S6- Она, как
правило, выражена слабо, сосуды в ней незна­
чительные, и разделить ее обычно не трудно.
46
Легочная связка разделяется частично тупо,
частично — остро с перевязкой сосудов в ней.
Вена выделяется без особого труда, препаровка
ее к периферии дает возможность увидеть ее
истоки: Уб, верхнюю и нижнюю базальные вены.
Вена перевязывается и пересекается.
Бронх лучше изолировать из междолевой
щели. После удаления нижнего междолевого
лимфатического узла, перевязки и пересечения
Аб и базальной артерии бронх нижней доли
легко определить, препарируя бифуркацию глав­
ного бронха. Надо иметь в виду вариант отхож­
дения бронха S6 от главного бронха вместе с
отхождением базального бронха, т. е. тогда,
когда главный бронх образует не бифуркацию,
а трифуркацию. Возможно также деление ба­
зального бронха сразу на сегментарные брон­
хи — Be, Bg и В io. В этих случаях стремление
наложить шов на базальный бронх (даже если
Вб прошивается отдельно) может привести к
сужению верхнедолевого бронха. Поэтому при­
ходится обрабатывать каждый сегментарный
бронх отдельно.
Межсегментарная поверхность доли описана
выше.
СЕГМЕНТЫ ЛЕВОГО ЛЕГКОГО
ВЕРХУШЕЧНЫЙ И ЗАДНИЙ СЕГМЕНТЫ
ЛЕВОГО ЛЕГКОГО
Рис. 32. Наиболее часто встречающееся строение бронха
верхней доли левого легкого.
Имея в виду особенность строения левого
легкого, считают, что типичного, как это имеет
место в правом легком, заднего сегмента слева
нет.
Поэтому практически, если есть необходи­
мость в удалении задних отделов верхней доли,
резецируется этот участок вместе с верхушеч­
ным сегментом. Это оправдывает себя в подав­
ляющем большинстве случаев и потому, что
патологический процесс в так называемом S2
или в заднем субсегменте верхушечного сег­
мента, как правило, захватывает и какие-то
участки Si.
Доступ к корню этого Sb 2—переднебоко­
вой, через четвертое межреберье. Первой обна­
руживается верхняя легочная вена. Препари­
руются истоки ее. Изолируется V, 2. Крайне
желательно, если позволяет патологический
процесс, найти ее ветвление и выделить Vlc. Она
является межсегментарной и может служить
хорошим ориентиром при разделении межсег­
ментарной плоскости между Si и S3. Vla сле­
дует перевязать и пересечь, так как она мешает
препарировать артерии к S1>2.
Препарировать артерии S, 2 можно из перед­
небокового доступа. После изоляции основного
ствола левой легочной артерии препарируют
ее ветви. Первой, отходящей вверх и кнаружи,
1 — верхушечный сегментарный бронх (В|); 2 — задний сег­
ментарный бронх <В-2>; 3 — передний сегментарный бронх (В3);
4 — верхнеязычковый сегментарный бронх (В*); 5 — нижне­
язычковый сегментарный бронх (Вб).
НИЖНЯЯ доля
ЛЕВОГО ЛЕГКОГО
Корень нижней доли левого легкого лучше
препарировать через переднебоковой доступ
по пятому межреберью или через боковой до­
ступ тоже по пятому межреберью. Бронх и ар­
терии хорошо доступны через междолевую
щель, а нижняя легочная вена — спереди, с ме­
диастинальной поверхности легкого.
Начинать препаровку следует с поиска и об­
нажения нижнедолевой артерии. Это делается
так же, как было описано при препаровке А4
Нужно иметь в виду (об этом указывалось
выше), что Ав может отходить не только ниже
места отхождения А4 5 (это типично), но и на
одном уровне с местом отхождения этой арте­
рии и даже выше ее. Изолирование, перевязка
и пересечение Аб у базальной артерии позволя­
ют перейти к препаровке нижней легочной вены.
Это лучше сделать с медиастинальной поверх­
ности легкого. Для этого легкое отводят кна­
ружи, а сердце осторожно смещают медиально.
47
является А, 2, второй, идущей вверх и кнару­
жи,— Аз. А,_ 2 перевязывается и пересекается.
Можно хорошо отпрепарировать А|>2 и со сто­
роны междолевой щели, вверху ее. После отделе­
ния от нижней доли, т. е. разделения легочной
перемычки между S2 и Sb, в щели прощупыва­
ется, а затем выделяется артериальный ствол.
Сдвигая верхушку легкого (Si) кпереди и кни­
зу, обнаруживают А, 2. Она изолируется и пере­
вязывается.
После перевязки и пересечения Vi (без Vlb)
и артерии (Аь 2) бронх легко обнаруживается.
Это нетрудно теперь сделать из любого доступа.
ПЕРЕДНИЙ (III) СЕГМЕНТ
ЛЕВОГО ЛЕГКОГО
Корень переднего сегмента лучше всего пред­
ставляется при переднебоковом доступе через
четвертое межреберье. При препаровке верх­
ней легочной вены средний коллектор ее и яв­
ляется веной переднего сегмента (V3). Она вско­
ре делится на три ветви: V3a, V3b и V3c. Самая
верхняя вена V3a — центральная вена сегмента.
Она может быть перевязана и пересечена. V3b
и V3c являются межсегментарными между S3
и S4. При этом V3b собирает кровь из двух сег­
ментов (S3 и S4) с медиальной стороны, a V3c—
с латеральной. Иначе говоря, ориентируясь по
V3bB можно довольно точно распрепарировать
межсегментарную плоскость с медиальной сто­
роны, т. е. со стороны средостения, а ориенти­
руясь на ход V3c,— со стороны междолевой ще­
ли (рис. 33). Кровь из Si и S3 по межсегмен­
тарной плоскости собирается в Vlb.
Артерия переднего сегмента может быть
отпрепарирована с медистинальной стороны,
при отведении прикрывающих ее вен, а также
и со стороны междолевой щели (рис. 34). Арте­
рия третьего сегмента (Аз) — довольно посто­
янная артерия. Случаи отхождения от нее
ветви к переднему субсегменту Si очень редки
и практического значения не имеют.
Между ветвями V3 и V, L 2, несколько глубже
их ветвления, находится бронх III сегмента.
Он далее разделяется на два ствола, аэрируя
наружный и задний субсегменты.
После перевязки и пересечения Аз и V3a про­
изводится обработка бронха переднего сегмен­
та. Межсегментарные плоскости можно рас­
препарировать, как говорилось выше, ориенти­
руясь с медистинальной поверхности легкого,
между S2 и S3, на вену I сегмента — V| а, а между
S3 и S4 — на вену III сегмента (V3b). Со стороны
междолевой щели, между Si и S3, ориентиром
является вена III сегмента — V3 с субсегмен­
тарной ветвью V3c, а между S3 и S4 — V3c
(рис. 35).
ВЕРХУШЕЧНЫЙ (ЗАДНИЙ) И ПЕРЕДНИЙ
СЕГМЕНТЫ ЛЕВОГО ЛЕГКОГО
Удаление трех сегментов верхней доли (SL 2>3)
предпринимается в тех случаях, когда длитель­
но текущий патологический процесс в них при­
водит к уменьшению их объема и компенса­
торно к увеличению объема S4 и S5. Сморщен­
ные, патологически измененные, потерявшие
свою функциональную ценность верхние сег­
менты требуют для успеха лечения заболева­
ния их удаления, а здоровый, увеличенный язы­
чок удалять нецелесообразно. Такая тактика
подкрепляется неполным развитием междоле­
вой щели, т. е. при наличии выраженной ле­
гочной перемычки между язычком и нижней
долей. Иногда этому способствует наличие в лег­
ком S7.
Отсюда естествен интерес к анатомическому
строению корня S, 2 и S3.
При переднебоковом доступе по четвертому
межреберью препарируется верхняя легочная
вена, перевязываются и пересекаются V( 2 и
ее ветви. Ветви вены III сегмента (V3b и V3c)
собирают кровь из межсегментарных поверх­
ностей между S3 и S4, a V3a является централь­
ной веной сегмента. Поэтому перевязать и пе­
ресечь целесообразно лишь V3ai препарируя
легкое по ходу V3b, разделяя тем самым меж­
сегментарную плоскость между S3 и S4.
Истоки V3 имеют вариант, при котором Уз
сливается полностью с Vi. Перевязка этого об­
щего ствола может вести к напрасной перевяз­
ке и пересечению V3b и V3c. Такая перевязка
ранее считалась очень опасной, нарушающей
венозный отток из S4. Опыт не подтвердил это­
го. Однако перевязывать без нужды вены остав­
ляемого участка легкого все же нежелательно.
Вторым вариантом, который может встре­
титься, является слияние V3c V4,» Этот вариант
не грозит перевязкой V3b и V3c.
Существует вариант ветвления У3, при кото­
ром одна субсегментарная вена впадает в Vi,
а другая — в У4 5. У казанные варианты можно
определить не только по ветвлению вен, но и
по калибру коллекторов, вливающихся в верх­
нюю легочную вену.
Следующим слоем корня SL 2> 3 является ар­
терия.
После перевязки и пересечения V i открывает­
ся легочная артерия с ее ветвями к S|, 2 и S3.
Однако, прежде чем приступить к их обра­
ботке, следует проследить ветвление их к пери­
ферии, поскольку и в артериальной системе воз­
можны различные варианты. Так, нередко Аз
сливается с А4 5, образуя вначале общий ниж­
ний ствол, до того, как легочная артерия про­
следует кзади, огибая бронх. Объединение А3
с Аг при удалении Sj 2 и S3 значения не имеет.
48
7
4
3
12
Рис. 33. Препаровка сосудов корня левого легкого. Выделена
вена переднего сегмента (Уз).
1 —легочная артерия; 2 — артерия верхушечного сегмента (А>);
3 — артерия переднего сегмента (А3); 4 — верхняя легочная вена:
5 — вена верхушечнозаднего сегмента (V>); 6 — вена переднего
сегмента (Уз); 1 — вена нижнеязычкового сегмента (V$).
В1С, т. е. образуется трифуркация. Однако иног­
да бронх переднего сегмента сливается с брон­
хом язычка, и тогда верхнедолевой бронх пред­
ставляет бифуркацию. Существуют и другие,
правда, очень редкие варианты отхождения
сегментарных и субсегментарных бронхов, не
имеющие большого практического значения.
Нужно указать, что ошибка в перевязке и
пересечении той или иной ветви артерии лишает
участок легкого его функции — газообмена. Пе­
ревязка и пересечение вены более опасны: раз­
вивается застой крови в участке, из которого
Однако и этот вариант следует иметь в виду.
Более важным является объединение А3 только
с А4. А5 отходит при этом самостоятельным
стволом дорсально от язычкового бронха. Толь­
ко после тщательного изучения ветвления ар­
терий А12 и А3 перевязываются и пересекают­
ся. Нередко А2 (А1с) лучше выделить из междо­
левой щели. После этого открываются бронхи.
Чаще всего верхнедолевой бронх ветвится на
три ствола: В, , 2, В3 и В4 5. В, 2 отходит самым
верхним стволом. Следующим от него отходит
и В2 или, как его называют некоторые авторы,
4 Зак. 0517
49
Рис. 34. Препаровка артерии левого легкого в междолевой
щели.
Перевязана артерия переднего сегмента (АЛ.
иного бронха ведут к спадению аэрируемой
этим бронхом участка легкого и нередко к раз
витию воспаления. Препаровка межсегментар
ных плоскостей представлена выше при описа
нии корня Si, 2 и S>2.
по этой вене происходит отток крови. Однако
с тем и другим дефектами техники организм
больного справляется. Общий газообмен не на­
рушается, кровообращение восстанавливается.
Ошибочная перевязка и пересечение того или
50
Рис. 35. Выделение переднего сегмента (S J. Видны V3b
V,.
дельными стволами. Иногда, как указывалось
выше, нижний язычковый венозный исток
сливается или со всей V3, или с одной из ее
ветвей, в том числе и межсегментарными —
между S3 и S4 или V3b и V3c.
Артерию язычковых сегментов лучше всего
препарировать из междолевой щели. At, 5 может
прослеживаться и спереди, после перевязки и
пересечения V4, 5 и обработки В4, 5.
Вариантов ветвления язычковой артерии
много. Чаще всего А4 и As отходят самостоя­
ЯЗЫЧКОВЫЕ СЕГМЕНТЫ
ЛЕВОГО ЛЕГКОГО
Доступ к корню язычка — переднебоковой,
через четвертое межреберье. Обнаруживается
верхняя легочная вена. V4, 5 вливается в нее
нижним стволом. В этих случаях ее следует
отпрепарировать и взять на провизорную лига­
туру. Длина ее — 0,5—1 см. Далее она ветвится,
образуя V4 и Vs. Часто обе эти вены вливаются
в нижний участок верхней легочной вены от­
4*
и
51
тельными стволами. Проследить этот вариант
большого труда не составляет. Труднее выявить
варианты различного рода слияний. Чаще всего
встречается слияние язычковой артерии с Аз.
Тогда они образуют один ствол диаметром до
0,8—1,2 см и делятся, обычно отойдя от общего
ствола легочной артерии на 2—3 см. Перевязка
и пересечение такого ствола ведут к лишению
функции газообмена S3. Иногда это слияние
происходит лишь с субсегментарной артерией
III сегмента (А3с).
Нередко встречается менее опасный вариант,
когда только А4 отходит от Аз. В этих случаях
А5 можно принять за общий ствол А4 5.
Язычковый бронх (В4> 5) отходит обычно об­
щим стволом от нижней части верхнедолевого
бронха. Препаровка его возможна спереди толь­
ко после перевязки и пересечения язычковой
вены. Выделение язычкового бронха можно
сделать и из междолевой щели после перевяз­
ки и пересечения язычковой артерии. Однако
этот последний метод имеет свой недостаток —
углубление раны и опасность повреждения ство­
ла междолевой артерии.
Спереди легче проследить варианты отхожде­
ния язычкового бронха. Из них следует отме­
тить три, чаще всего встречающиеся. Первый
из них — отхождение от верхнедолевого брон­
ха В4 и Вз раздельно. После перевязки сосудов
ко всему язычку можно ошибочно далее разде­
лить межсегментарную поверхность между
S4 и S5 и удалить только V сегмент, оставив без
снабжения кровью S4. Избежать этой ошибки
можно лишь проследив ход V3b и V3c — меж­
сегментарных вен между S3 и S4.
Второй вариант — отхождение В4 от Вз. Толь­
ко правильная препаровка по межсегментар­
ной плоскости между S3 и S4 обнаружит и эту
ошибку.
Более опасен третий вариант, когда с В41 5
сливается один из субсегментарных бронхов от
переднего сегмента или весь передний бронх
В3 отходит вместе с В4> 5. Тогда перевязка этого
бронха лишает аэрации часть или весь передний
сегмент и удаление язычка может превратить­
ся в удаление всей верхней доли.
Межсегментарная плоскость препарируется
так же, как и при удалении переднего (III)
сегмента.
Рис. 36. Выделение артерии V сегмента (As) левого легкого.
1—артерия заднего субсегмента (А2); 2 — артерии язычковых
сегментов (Ад 5 ); 3 — артерия верхнего сегмента (Аь); 4 —
артерия сегментов базальной пирамиды (Ag q ю )•
так как удаление его мало чем технически отли­
чается от экстирпации всего язычка.
Корень V сегмента лучше всего начать пре­
парировать спереди, с венозного слоя.
Препаровка и идентификация V5 произво­
дятся так же, как и препаровка корня всего
язычка. Надо иметь в виду, что межсегментар­
ной веной между S4 и S5 является V4 с ее вет­
вями V4a и V4b. При этом V4a собирает кровь из
S4 и S5, располагаясь по задней межсегментар­
ной поверхности, a V4b — по передней поверх­
ности ее.
Одна из ветвей V5 (V5a) является центральной,
a V5b—субплевральной. V5 может быть пере­
вязана и пересечена. Из вариантов, которые
заслуживают внимания, является вливание всей
язычковой вены или одной V5 в нижнюю легоч­
ную вену, а также слияние язычковой вены с
V2, о чем говорилось выше.
Для препаровки бронха V сегмента целесооб­
разно V5 перевязать и пересечь. В5 является
во всех вариантах самым последним из ветвей
верхнедолевого бронха, каудально располо­
женным. Он легко идентифицируется. Под ним
кзади (дорсально) обнаруживается артерия V
сегмента. Однако ее лучше найти из междоле­
вой щели (рис. 36).
Межсегментарную щель препарируют, ориен­
тируясь на границу спадения S5 при раздува­
нии легкого, а также на V4 в V4c.
ВЕРХНИЙ (VI) СЕГМЕНТ
НИЖНЕЙ ДОЛИ ЛЕВОГО ЛЕГКОГО
Корень VI сегмента, в отличие от сегментов
верхней доли, лучше препарировать из междо­
левой щели. Одинаково хорош как переднебоко­
вой, так и боковой доступ. При препаровке кор­
ня VI сегмента из переднебокового доступа
первой препарируется нижняя легочная вена.
Сердце при этом отводится несколько медиальнее. Препаровка с медиастинальной стороны
нижней легочной вены дает возможность в боль­
шинстве случаев обнаружить три или две ветви
ее. Верхняя, меньшая (0,3—0,8 см), является
веной VI сегмента, а нижняя, почти вдвое тол­
ще (0,6—1,4 см),—базальная вена. Дальней­
шее выделение вены представляет трудности.
V СЕГМЕНТ ВЕРХНЕЙ ДОЛИ
ЛЕВОГО ЛЕГКОГО
IV сегмент язычка отдельно не удаляется.
Удаляется, хотя и редко, один V сегмент. Его
поражение, не позволяющее ограничиться кра­
евой резекцией, и в то же время хорошее состоя­
ние IV сегмента могут потребовать резекции
лишь V сегмента. Это тем более оправдано,
Рис. 37. Этапы обработки корня верхнего сегмента нижней
доли левого легкого.
а — вена VI сегмента; б — перевязана артерия VI сегмента. 1 —
культя артерии VI сегмента (А6); 2 — VI сегментарный бронх
(Во); 3 — вены VI сегмента.
52
б
53
6
5
2
4
Рис. 38. Отделение VI сегмента (S6). Видна межсегмен­
тарная вена (V6b).
1 — культя бронха верхнего сегмента (В6 ); 2 — культя артерии
верхнего сегмента (А6); 3 — культи вен верхнего сегмента
(V6a 6в); 4 — артерия заднего субсегмента (А2); 5 — артерии
язычковых сегментов (А4 5 ); 6 — артерии сегментов базальной
пирамиды (Ag 9 |g).
Далее артерия отдает три ствола: Ав, А^и А<,с,
идущие к соответствующим субсегментам —
внутреннему, верхнему и наружному. Не так уж
редко Ав отходит двумя стволами (A^H-A^g и
Абс).
Бронх верхнего сегмента нижней доли отхо­
дит от нижненаружной поверхности нижнедо­
левого бронха и прослеживается либо рядом
с артерией, чуть глубже ее, либо под артерией.
В этом последнем случае бронх может быть
хорошо отпрепарирован только после перевяз­
ки и пересечения артерии (рис. 37). Бронх,
Поэтому целесообразно взять Уб на провизор­
ную лигатуру.
Препарирование следует предпринять из меж­
долевой щели. Это делается так же, как и при
препарировании корня язычка. Как указывалось
выше, артерия VI сегмента отходит от междо­
левого ствола легочной артерии от задненаруж­
ной ее поверхности, несколько дистальней от­
хождения язычковой артерии и направляется
кзади и кнаружи. Нередко она отходит на од­
ном уровне с язычковой или выше ее. Тогда по
сути дела междолевого ствола как такового нет.
54
так же как и артерия, делится на три ствола,
соответственно субсегментам, либо сначала на
два (В6а и Вьь), а затем отдает третий — Вь,,
Бронх может быть обработан и пересечен, так
как вариантов, угрожающих выключением со­
седних сегментов слева, не встречается.
Последней препарируется вена. Уб образу­
ется из трех истоков: V6a) V6b и V6c. Первые две
собирают кровь из субсегментов VI сегмента,
т. е. идут по межсегментарным плоскостям; они
могут быть перевязаны и пересечены. V6c явля­
ется межсегментарной веной между VI и базаль­
ным сегментом. Поэтому при препаровке меж­
сегментарной поверхности между Бб и базальным
сегментом V6c является хорошим ориентиром
(рис. 38).
БАЗАЛЬНЫЕ СЕГМЕНТЫ НИЖНЕЙ ДОЛИ
ЛЕВОГО ЛЕГКОГО
Корень базальных сегментов, как и VI, может
быть хорошо распрепарирован и из передне­
бокового, и из бокового доступов. Он препари­
руется так же, как и корень VI сегмента. При
этом на провизорную лигатуру берется ниж­
ний исток нижней легочной вены — базальная
вена.
Далее препаровка ведется через междолевую
щель. Вначале изолируется ствол легочной арте­
рии с ее ветвями: А4 5, Ав и А8 9 10. Последняя,
как правило, отходит одним стволом. Первой
от ее передней поверхности отходит артерия
переднебазального сегмента (Ав), а затем про­
должение ее делится в виде бифуркации на Ад,
отходящую вниз и кнаружи, и Ащ, идущую вниз
и кзади.
Иногда при рассыпном типе ветвления базаль­
ной артерии как таковой нет, а сегментарные
артерии отходят самостоятельными ветвями.
Так же как и у бронхов, у базальных артерий
связи с верхней артерией нет. Поэтому один
ствол базальной артерии или все сегментарные
артерии раздельно перевязываются и пересе­
каются.
После этого удается легко отпрепарировать
бронх, который представляет собой ствол, за­
ключенный между устьями верхнедолевого
бронха и верхнего сегментарного бронха нижней
доли (В6).
Длина его бывает от 0,6 до 1,4 см. Различия
в длине нижнедолевого бронха зависят чаще
всего от уровня отхождения Вб.
Как и справа, ветвление нижнедолевого бронха
подвержено индивидуальным различиям. В боль­
шинстве случаев после отхождения Be нижнедо­
левой бронх продолжается в базальный. Под
бронхиальным стволом базальной пирамиды сле­
ва следует понимать отрезок бронха нижней до­
ли, заключенный между устьем Вв и местом
деления базального бронха на сегментарные вет­
ви. Его длина колеблется от 0,7 до 2,1 см. Обычно
базальный бронх оканчивается ветвлением на
передневнутренний сегментарный (Be) и задне­
наружный бронхиальный ствол, который раз­
деляется на наружнобазальный (Вд) и задне­
базальный (Вю) сегментарные бронхи.
Бронх передневнутреннего сегмента (Вв) от­
ходит от передневнутренней поверхности базаль­
ного бронха и имеет направление книзу, кпереди
и немного кнутри. Иногда он отходит общим
стволом с В9 (4 %). Длина В8 колеблется в пре­
делах от 0,1 до 1,5 см.
Бронх верхнего сегмента нижней доли левого
легкого отходит от задней поверхности нижне­
долевого бронха, направляется кзади и несколько
книзу. Длина Be колеблется в пределах от 0,1 до
1,5 см. От наружной поверхности задненаруж­
ного бронхиального ствола отходит бронх наруж­
нобазального сегмента (Вд). Иногда он отходит
совместно с В8. Во всех случаях длина Вд не
превышает 1,5 см.
Бронх заднебазального сегмента (В 15) пред­
ставляет собой заднюю ветвь задненаружного
ствола базального бронха. Он направляется
кзади, книзу. Обычно длина его колеблется в пре­
делах от 0,1 до 2,5 см.
Обнажается нижняя легочная вена с ее вет­
вями: V6 и общий ствол V8, 9, ю.
Межсегментарной веной между V8 и V8> 9, )0
как указывалось выше, является Vec • Поэтому
перевязка и пересечение базальной вены не мо­
гут нанести ущерб оставляемому VI сегменту.
ЛДГз, при снижении активности МДГ [Соловь­
ев Г. М. и др., 1970]. Изменение биоэнергети­
ки легкого при возникновении в нем патологи­
ческого процесса или повреждении подтверж­
дается методикой суммарного определения про­
дуктов промежуточного обмена (вакат-кислорода) в смешанной венозной (притекающей)
и артериальной (оттекающей от легких) крови.
Избыточное поступление кислорода с вдыха­
емым воздухом (при гипербарической оксиге­
нации) приводит к образованию в легких ра­
дикалов О2, активирующих свободное окисле­
ние липидов, что при длительной экспозиции
ведет к накоплению токсических продуктов,
дестабилизации клеточных мембран и наруше­
нию окислительных процессов в митохондриях.
Отсутствие функционально отчетливого по­
вреждения легких при короткой экспозиции
гипербарической оксигенации [Буравцов В. И.
и др., 1983] определяется тем, что в клетках
респираторной зоны существует ферментная
система противоокислительной защиты, главную
роль в которой играет специфический фермент—
супероксиддисмутаза, превращающая анион
Ог в перекись водорода и воду, а также проис­
ходит активация гликолиза и пентозного шун­
та. Это предупреждает гипероксическое по­
вреждение респираторной зоны и способствует
поддержанию различных видов обмена, нару­
шенных операцией или травмой [Козлов И. А.
и др., 1983].
Углеводный обмен в легких по интенсивности
соответствует таковому в головном мозге и со­
кращающемся сердце fCristall N., 1976]. Для
утилизации глюкозы легкими инсулин не ну­
жен. Глюкоза здесь используется не только
в цикле Кребса, но и в биосинтезе аминокислот
и липидов (схема 2). Потребление глюкозы
легкими резко возрастает на фоне гипоксии
[Горовенко Г. Г. и др., 1969]. Около 20 % глю­
козы окисляется до углекислого газа, на что
затрачивается значительная часть потребляе­
мого легкими кислорода. Остальная часть обес­
печивает синтез АТФ путем анаэробного гли­
колиза, что важно именно для альвеолоцитов,
бедных митохондриями. Таким путем около
40 % всей потребленной глюкозы превращается
в лактат, что служит показателем активности
анаэробного метаболизма в легких, но не явля­
ется следствием дефицита кислорода в тканях
организма.
Глава
Zs КЛИНИЧЕСКАЯ
ФИЗИОЛОГИЯ ЛЕГКИХ
И ПЛЕВРЫ
Структурные особенности легких позволяют
выделить в нем две основные функциональные
зоны. В одной из них, воздухопроводящей,
осуществляется движение газов из окружаю­
щей среды к диффузионной или дыхательной
мембране и от нее. Она представлена в основ­
ном бронхиальным деревом с окружающей его
стромой. В другой, респираторной, зоне про­
исходит сам процесс газообмена через дыхатель­
ную мембрану. Она содержит как воздухонос­
ные пути, так и саму диффузионную мембрану.
Деление легкого на две зоны во многом опре­
деляет и особенности его патологии, и особен­
ности органного обмена.
ОБМЕН ВЕЩЕСТВ В ЛЕГКИХ
Биоэнергетика легких. Утилизация кислоро­
да самой легочной паренхимой происходит тре­
мя путями (схема 1). Основной — это мито­
хондриальная система дыхательных ферментов
(трансферрин и оксидазы), обеспечивающая
синтез АТФ. Менее 10 % потребляемого в лег­
ких кислорода идет на синтез биологически ак­
тивных веществ и на детоксикацию токсинов
и лекарственных препаратов. При различных
заболеваниях (воспалениях, опухолях, туберку­
лезе) поглощение кислорода паренхимой лег­
ких возрастает; на фоне острой кровопотери
оно увеличивается в 8—9 раз.
В обычных условиях кровоснабжения в лег­
ких представлены как аэробный, так и анаэроб­
ный пути синтеза макроэргических соедине­
ний; отмечается относительно низкая активность
ферментов цикла Кребса при высокой актив­
ности лактатдегидрогеназы (ЛДГ)
[Бубно­
ва Н. И., Узбекова Д. Г., 1964]. Процессы
аэробного окисления активируются при нару­
шении кровообращения в легких. При значи­
тельной тканевой гипоксии начинают преобла­
дать процессы анаэробного гликолиза, что вы­
ражается в повышении активности ЛДГ, в том
числе и органоспецифичного изофермента
56
До 5 % потребляемой легкими глюкозы вклю­
чается в синтез липидов, главным образом
фосфолипидов. И, наконец, 10—15 % глюкозы,
поступающей с кровью в респираторную зону,
идет на синтез аминокислот [Козлов И. А. и
ДР-, 1983].
Обмен белков в легких не менее активен,
чем углеводов. При острой гипоксии и падении
содержания кислорода в притекающей к легким
крови катаболизм белков и аминокислот (нео­
глюкогенез) усиливается [Александрович А. Г.
и др., 1972]. Наоборот, в адаптированном к ги­
поксии организме легкие значительно усили­
вают синтез нуклеиновых кислот и белков, что
облегчает регенерацию и ведет к гипертрофии
легочной ткани на фоне усиленного поступле­
ния аминокислот. Одновременно синтезируются
белки, которые составляют протеиновую основу
поверхностно-активных веществ легких, покры­
вающих всю диффузионную мембрану [Gacad G.
et al., 1972]. Эти данные могут послужить фи­
зиологическим обоснованием необходимости
усиленного белкового питания больных, пере­
несших вмешательства на легких.
Установлено, что легкие могут как захваты­
вать, так и секретировать в кровоток белки
(альбумины, иммуноглобулины, некоторые фер­
менты). В патологических условиях (при инток­
сикации, воспалении) белковый обмен извра­
щается и идет не в направлении избыточного
синтеза белков для восстановления клеточных
структур, а для формирования коллагена ме­
жуточного вещества с развитием интерстициаль­
ного фиброза.
Жировой обмен в легких идет по двум основ­
ным путям: утилизации жира как энергетиче­
ского субстрата и синтезу поверхностно-актив­
ных веществ. Как и в отношении углеводов,
интенсивность захвата жира из притекающей
к легким крови зависит от особенностей снаб­
жения кислородом респираторной зоны, осо­
бенностей кровообращения и концентрации ли­
пидов в крови. Захват повышается при введе­
нии инсулина, снижается при ваготомии и гиперсимпатикотонии [Никулина М. Н., 1956].
Кроме нейтральных жиров, легкие способны
захватывать холестерин и свободные или неэстерифицированные жирные кислоты (НЭЖК).
В обычном состоянии в легких происходят
гидролиз нейтральных жиров с образованием
НЭЖК как энергетического субстрата и рас­
щепление холестерина. Особенности обмена
НЭЖК (и нейтральных жиров) зависят от ха­
рактера питания: при голодании они активно
окисляются, а при избыточном введении (влива­
нии жировых эмульсий) резко возрастает син­
тез фосфолипидов (схема 3).
При избыточном введении жира паренте­
ральным путем синтез фосфолипидов в легких
Схема 1. Поступление и использование кислорода в легких.
Схема 2. Биоэнергетика легких.
Глюкоза
Свободные жирные кислоты
I
I
I
Триглицериды
Липаза
Глицерин + Свободные жирные кислоты
/
Ct—fi — Диглицериды + холин
Дипапьметил — лецитин
Схема 3. Синтез дипальмитиллецитина — основы
ностно-активных веществ легких.
поверх­
57
пространства которых представляют первич­
ную дольку — ацинус. Он начинается с дыха­
тельной бронхиолы и включает помимо по­
следней альвеолярные мешки, альвеолярные
ходы и собственно альвеолы. Этому элементу
дали название «респирон» [Шанин Ю. Н., Ко­
стюченко А. Л., 1969]. Выделение такой едини­
цы облегчает понимание физиологии легких и
основано на следующих особенностях этого
структурно-функционального элемента:
1) клеточное строение респирона резко
отличается от выстилки бронхиального дерева
и обладает рядом уникальных особенностей;
2) респирон имеет значительный собствен­
ный объем воздухоносных пространств (одни
альвеолярные ходы занимают более 30 % общего
объема легких);
3) обмен газов над диффузионной мембра­
ной происходит не в силу смешивания и вытес­
нения (конвекции), а в силу диффузии из дыха­
тельных бронхиол и альвеолярных ходов;
4) респирон снабжается кровью только из
легочной артерии, а соединения между большим
и малым кругом находятся за пределами респи­
раторной зоны;
5) респирон практически лишен иннерва­
ции, так как эффекторные нервные окончания
простираются не далее дыхательной бронхио­
лы и сопутствующей ей артериолы.
увеличивается в 3—4 раза, тогда как в печени—
не более чем в 2 раза. Этот процесс замедля­
ется при снижении легочного кровотока и отеке
легких, что можно объяснить нарушением пита­
ния респираторной зоны и снижением вслед­
ствие этого продукции энергии, необходимой
для такого высокоэнергетического процесса,
каким считается синтез липидов [Лейтес С. М.,
Лаптев Н. Н., 1967]. По-видимому, от регио­
нарных колебаний перфузии легких зависят
и эффекты, наблюдаемые при однолегочной вен­
тиляции: в выключенном, а особенно в намеренно
коллабированном легком синтез фосфолипи­
дов ингибируется и депонируется холестерин,
тогда как в вентилируемом легком процесс рас­
щепления жиров усиливается [Карнаухов И. Ф.
и др., 1978]. Из жирных кислот в таких обстоя­
тельствах и даже на фоне относительной гипо­
ксемии особенно интенсивно захватывается
пальмитат. Лишь продолжительное нарушение
перфузии паренхимы легкого (при эмболии,
тромбозе в сосудах малого круга) замедляет
синтез фосфолипидов, ограничивает восстанов­
ление поверхностно-активных веществ.
Естественно эмульгированный жир, посту­
пающий в кровоток по грудному лимфатиче­
скому протоку, под влиянием липопротеиновых
липаз почти полностью гидролизуется в лег­
ких, не проникая далее легочных капилляров.
Эти ферменты продуцируются клетками эндо­
телия легочных сосудов и являются главной
ферментной системой гидролиза. Липолитиче­
ская активность легких возрастает при гипок­
сии и гиперкате холами нем ии, при введении
экзогенного гепарина и тормозится адренолитиками, в частности фенотиазинами. Даже при
введении неэмульгированного жира блокада ка­
пиллярного русла респираторной зоны несуще­
ственна и быстро разрешается [Gold R. et al.,
1965]. В случаях ишемического или гипоксиче­
ского повреждения респираторной зоны актив­
ность липопротеиновых липаз снижается на­
столько, что функциональные и клинические
проявления жировой эмболии становятся отчет­
ливыми.
ВНЕШНЕЕ ДЫХАНИЕ
В процессе легочного газообмена выделяют
внешнее дыхание, или собственно вентиляцию
легких, и обмен газов через альвеолярно-ка ­
пиллярную диффузионную мембрану. Вентиля­
ция обеспечивается аппаратом внешнего дыха­
ния, включающим в себя не только воздухо­
проводящую зону легкого, но также костно­
мышечные структуры грудной клетки и диа­
фрагму.
Действие дыхательных мышц. В физиологи­
ческих условиях система грудная клетка —
легкие выводится из равновесия в фазе вдоха
сокращением дыхательной мускулатуры. Объем
грудной клетки увеличивается вследствие опу­
скания диафрагмы и подъема ребер. На изме­
нение объема грудной клетки оказывают влия­
ние изгиб позвоночника и положение головы.
Вдох происходит наиболее легко при выпрям­
ленном позвоночнике и несколько откинутой
голове и затруднен при кифозе, опущенном на
грудь подбородке. Такое положение весьма
опасно в послеоперационном периоде.
Во время вдоха нижняя часть грудной клетки
увеличивается в поперечнике больше, чем верх­
няя. Эта особенность биомеханики объясня­
ет значение уровня перелома ребра, при торако­
томии — разреза для нарушения внешнего ды­
ГАЗООБМЕННАЯ ФУНКЦИЯ ЛЕГКИХ
Выделяя легочный газообмен как специфи­
ческую функцию легких, понимают, что она
возможна благодаря происходящим в легких
процессам обновления газа над диффузионной
мембраной (вентиляции), диффузии газов в
кровь и перфузии органа газотранспортной
средой (кровью).
Диффузионная мембрана расположена в ви­
де громадного числа конечных структурно­
функциональных элементов, воздухоносные
58
хания: чем ниже уровень повреждения каркаса
грудной клетки, тем больше оснований для на­
рушения вентиляции.
Главной дыхательной мышцей считается диа­
фрагма. Сокращение диафрагмы и смещение
ее в сторону брюшной полости увеличивают
объем грудной клетки в вертикальном направ­
лении и расширяют ее нижнюю апертуру. Рас­
ширение нижней апертуры объясняют куполо­
образной формой диафрагмы: волокна диафраг­
мы начинаются от сухожильного центра и при­
крепляются к нижним ребрам. Поэтому ее со­
кращение, смещая. сухожильный центр книзу,
поднимает нижние ребра.
Кроме ритмического сокращения диафрагмы,
в биомеханике дыхания существенную роль
играет постоянная тоническая активность ее
мышечной части в течение выдоха. Если сокра­
щения обоих куполов диафрагмы определяют
величину нарастания отрицательного давления
в замкнутой полости плевры и растяжение лег­
кого, то ее тоническая активность противодей­
ствует силам выдоха, в результате чего чере­
дование отрицательного давления происходит
плавно.
Увеличение объема грудной клетки, вызывае­
мое сокращением диафрагмы, обеспечивает
2/з жизненной емкости легких, т. е. почти весь
объем максимального вдоха. Поэтому понятно,
как ухудшаются условия вентиляции при сла­
бости диафрагмы, парезе диафрагмального
нерва или увеличении внутрибрюшного давле­
ния (при метеоризме, асците), когда вентиля­
цию обеспечивают преимущественно межре­
берные мышцы. И, наоборот, при выраженной
эмфиземе легких, но сохраненной дееспособ­
ности диафрагмы наложение пневмоперитонеума восстанавливает ее куполообразную фор­
му и улучшает вентиляцию.
Функциональная роль диафрагмы не огра­
ничивается ее участием в вентиляции легких.
Кашель, чиханье, рвота, возврат крови из орга­
нов живота — вот далеко не полный перечень
физиологических актов, в большей или мень­
шей степени зависящих от сократительной спо­
собности диафрагмы. Благодаря ее иннерва­
ции из Сз—С5 сохраняются дыхательные дви­
жения даже при высоком повреждении спин­
ного мозга.
Активность межреберных мышц во время
вдоха зависит от величины дыхательного объ­
ема (ДО). При возрастании ДО до 80 % жиз­
ненной емкости легких (ЖЕЛ) активны все
мышцы. Включение их на вдохе происходит в
нисходящем порядке от I до XI (что увеличи­
вает выраженность эффекта диафрагмы), как
и выключение к моменту пассивного выдоха.
Форсированный выдох происходит с участием
всех межреберных мышц, и включение их про­
59
исходит в восходящем порядке. Нижний отдел
грудной клетки сужается раньше верхнего, че­
му способствует не только тяга тонически ак­
тивной диафрагмы, но и возрастание напряже­
ния мышц живота. Этот же механизм обеспе­
чивает и кашель [Зильбер А. П., 1977].
Вспомогательные дыхательные мышцы (мыш­
цы плечевого пояса) принимают участие лишь
при необходимости гипервентиляции и значи­
тельном сопротивлении дыханию у больных
с патологией легких или грудной клетки.
В дыхательной паузе мышцы вдоха практи­
чески расслаблены, возникает состояние равно­
весия, при котором проявляется действие эла­
стичности системы грудная клетка — легкие.
Эластические структуры легочной паренхимы
стремятся уменьшить объем легких и содер­
жащегося в них воздуха, а эластические струк­
туры грудной клетки — увеличить их. Эти силы
противоположно направлены и в потенциальной
плевральной полости создают результирую­
щее отрицательное давление, которое прижи­
мает легкое к париетальной плевре и расправ­
ляет его. Расправлению легкого способствуют
и силы сцепления жидкости в плевральной
щели, которые исчезают, как только нарушает­
ся ее герметичность и в нее попадает воздух.
При сокращении основных дыхательных мышц
грудной клетки соответственно увеличивается
действие сил, растягивающих легкие. Давление
в воздухоносных путях падает, и воздух из
атмосферы поступает в легкие по воздухонос­
ным путям, увеличивая содержание газа в них.
Основное изменение объема газовой среды
зависит от колебаний объема воздухоносных
пространств респиронов. Доказано, что при спо­
койном дыхании объем альвеол не изменяется,
однако расширяется вход в них и изменяется
их форма [Storey J., Staub Р., 1962]. Расправ­
ленное состояние альвеол определяется глав­
ным образом внутренними факторами, действие
которых зависит от состояния диффузионной
мембраны. Однако следует учитывать и состоя­
ние воздухопроводящей зоны легкого. Во вре­
мя вдоха трахея удлиняется, увеличиваются
длина и диаметр бронхов, причем наибольшее
удлинение происходит в дистальной части брон­
хиального дерева. Во время спокойного выдо­
ха объем воздухоносных пространств респиро­
нов уменьшается, размер бронхов возвраща­
ется к исходному. Уменьшению объема брон­
хиального дерева, составляющего воздухопро­
водящую зону легкого, при выдохе способству­
ет и укорочение бронхов за счет согласован­
ного с дыханием сокращения их собственных
мышц.
В процессе вентиляции силы, вызывающие
изменения объема грудной клетки и легких,
преодолевают неэластическое и эластическое
сопротивления дыханию, величина, которых
определяет механику дыхательного акта и осо­
бенности регуляции вентиляции.
Общее неэластическое сопротивление дыха­
нию складывается из аэродинамическо­
го сопротивления газотоку в дыхатель­
ных путях, динамического сопротивления тре­
ния всех перемещаемых во время дыхания тка­
ней легких и грудной клетки (его называют
деформационным, вязкостным или
фрик­
ционным), а также инерционного
сопротивления
перемещаемой ткане­
вой массы. Учитывая незначительную величину
инерционного сопротивления (не более 5 % не­
эластического сопротивления), обычно под
неэластическим подразумевают сумму аэро­
динамического и фрикционного сопротивле­
ний.
Аэродинамическое сопротивление является
важнейшим компонентом общего респиратор­
ного сопротивления. Оно определяется вели­
чиной трения как между молекулами движу­
щейся по бронхиальному дереву газовой сме­
си, так и между молекулами газа и стенкой
воздухоносных путей.
Аэродинамическое сопротивление создается
главным образом в зоне дыхательных бронхиол,
общее сечение которых в 400 раз повышает
сечение трахеи. На фоне спокойного дыхания
сопротивление воздухоносных путей слегка
уменьшается во время вдоха (возможно, за счет
расширения бронхиол под влиянием тракции
паренхимы легких) и слегка возрастает к концу
выдоха. К концу максимального выдоха аэро­
динамическое сопротивление возрастает зна­
чительно.
Фрикционное сопротивление дыханию на­
ибольшего значения достигает при максималь­
ной вентиляции; в конце вдоха и выдоха оно,
как и аэродинамическое, равно нулю.
Неэластическое сопротивление возрастает
при системном поражении стромы легкого
(диффузном легочном фиброзе, перибронхи­
те, интерстициальном отеке и др.). Однако на­
ибольшую роль в изменении неэластического
сопротивления играют нарушения бронхиальной
проходимости, которые, имея различный генез,
в конечном счете приводят к сужению просве­
та с изменением его конфигурации, нарушаю­
щей обычное для данного уровня поведение
газотока. В крайних случаях обструкция дости­
гает высокой степени, вплоть до полной заку­
порки (дистелектаз, ателектаз).
Эластическое сопротивление дыханию. Доста­
точные эластические свойства легких и груд­
ной клетки — непременное условие эффектив­
ности легочного газообмена. В целом под эла­
стичностью понимается способность сохра­
нять и восстанавливать прежние форму и раз­
меры вопреки деформации, совершаемой под
воздействием любой внешней силы (сокращение
дыхательных мышц, воздействие аппарата ИВЛ,
работающего по принципу вдувания, и др.).
Знание динамики вышеописанных сил по­
зволяет врачу понять положение грудной клетки
при различных патологических состояниях
(эмфизема, фиброз легких, ожирение, пневмо­
торакс, ателектаз) и оценить влияние различ­
ных факторов на отдельные компоненты всей
системы грудная клетка — легкие. Эластиче­
ские свойства этой системы определяют их
эластическое сопротивление к растяжению, что
чаще всего выражается через соотношение меж­
ду объемом и давлением газа в легких, когда
обе эти величины сравниваются с состоянием
покоя. Это соотношение можно обозначить
как растяжимость или податливость дыхатель­
ной системы грудная клетка — легкие.
Значение податливости грудной
клетки в создании эластического сопротив­
ления дыханию хотя и меньше, чем значение
податливости легких, но все же достаточно
существенно, особенно за пределами нормаль­
ного состояния организма. Так, при ожирении
податливость грудной клетки уменьшается
примерно в 2—3 раза. У таких людей опреде­
ленное значение имеет и инерционность груд­
ной клетки, которую можно не принимать во
внимание у худых больных. Кроме того, этот
функциональный показатель может изменять­
ся под влиянием других факторов, оказываю­
щих воздействие на эластичность грудной клет­
ки. В частности, имеют значение деформации
ее костно-суставного аппарата, повышение
внутрибрюшного давления,
затрудняющего
смещение диафрагмы.
Следует подчеркнуть, что податливость лег­
ких феноменологически обратно пропорцио­
нальна эластичности. Если легкое теряет свою
эластичность (например, при эмфиземе), то
оно становится более податливым для растяже­
ния. И, наоборот, при уплотнении легких (фиб­
розе, воспалении) легкие становятся менее
податливыми. Понятно, что в силу многих при­
чин величина податливости легких изменяется
с возрастом. В известной мере она может зави­
сеть от неэластического сопротивления, повы­
шение которого понижает податливость при
форсированном дыхании у больных с обструк­
тивными нарушениями вентиляции. Растяжи­
мость легких прежде всего определяется состоя­
нием эластических структур респиронов, а также
плевры, бронхов и кровеносных сосудов, тону­
сом гладкой мускулатуры бронхов и количеством
бронхиальной слизи, даже при отсутствии от­
четливой бронхообтурации. Однако более чем
наполовину эластичность легких зависит от
стремления к спадению влажной поверхности
60
циркуляции в респираторной зоне. Гиповоле­
мия и гипоциркуляция любого происхождения,
эмболия легочной артерии, отек легких замед­
ляют репродукцию, а может быть, способству­
ют разрушению сурфактантов. Этому же спо­
собствуют курение табака, длительное вдыха­
ние кислорода в высокой концентрации, вос­
палительные процессы в легочной паренхиме.
Несомненное влияние на продукцию и рас­
пад сурфактантов оказывают некоторые фак­
торы операции и анестезия. Прекращение кро­
воснабжения и вентиляции отдельных участ­
ков легких, травматизация легочной паренхи­
мы, чрезмерное растяжение легких снижают
активность сурфактантов. В коллабированном
легком синтез их падает, что может привести
к усилению процессов ателектазирования в
послеоперационном периоде [Карнаухов И. Ф.
и др., 1976]. Жирорастворимые анестетики
(фторотан, метоксифлуран) уменьщают актив­
ность сурфактанта и увеличивают поверхност­
ное натяжение бронхиального секрета [Scar­
pelli Е., 1977]. Даже небольшое количество
жидкости на поверхности диффузионной мемб­
раны или в терминальных бронхиолах блоки­
рует сурфактантную систему, вызывает повы­
шение поверхностного натяжения со спадением
респиронов, что ощущается сразу по измене­
нию податливости легкого, особенно при руч­
ном методе ИВЛ.
Статические и динамические легочные объ­
емы. При спокойном вдохе количество воздуха,
поступившего в воздухоносные пути, обычно не
превышает объема, при котором эластические
структуры грудной клетки полностью расслаб­
лены. Уровень максимального вдоха опреде­
ляется взаимодействием между усилиями ды­
хательных мышц и противоположно направ­
ленной тягой легких и грудной клетки, в
которой ведущим является эластическое со­
противление легких. Уровень максимального
выдоха ограничивается все возрастающим (по
мере уменьшения объема газа в легких) со­
противлением сжатию грудной клетки. Пере­
численные уровни разделяют весь объем газа,
находящийся в легких в положении макси­
мально возможного вдоха, общую емкость лег­
ких (ОЕ) на ряд статических легочных объе­
мов и емкостей (рис. 39).
Дыхательный объем (ДО) — объем воздуха,
вдыхаемый или выдыхаемый при каждом дыха­
тельном цикле. Резервный объем вдоха (РОВД) —
максимальное количество воздуха, которое
можно вдохнуть после обычного вдоха. Резерв­
ный объем выдоха (РОВЫД) — максимальный
объем воздуха, который можно выдохнуть пос­
ле обычного выдоха. Остаточный объем легких
(ОО) — количество воздуха, остающееся в
легких даже после максимального выдоха.
Альвеолярный воздух
Фосфолипиды
Воздушногипофазная
граница
<7//^ Фосфолипиды, коллоиды ТШЪШ
< Z7 (альбумин, иммуноглобулин
шбМ/угпъъым (глукопротеины)^42£
Углеводы, иммуноглобулин, ферменты
Гипофаза
Гипофазно-клеточная греница
Легочная паренхима
es£>
Схема 4. Строение сурфактантной системы легких.
диффузионной мембраны под действием силы
поверхностного натяжения.
Стремлению к спадению противодействуют
поверхности о-a ктивные вещества
легких — сурфактанты, вырабатываемые
клетками альвеолярного эпителия [Pattie R.,
Clement Y., 1957]. Они снижают поверхност­
ное натяжение влаги на диффузионной мемб­
ране более чем в 10 раз и поддерживают рес­
пираторную зону в расправленном состоянии
даже при отсутствии дыхательных движений,
в состоянии апноэ. Именно эти вещества обес­
печивают не только антиателектатический, но
и противоотечный эффект в легочной парен­
химе, лишенной практически интерстициаль­
ной ткани, а также стабилизируют форму
мелких воздухоносных путей вплоть до тер­
минальных бронхиол [MacLem Р. et al., 1970].
Толщина пленки поверхностно-активных ве­
ществ, покрывающих изнутри дыхательную
мембрану,— всего 0,02—0,04 мкм. Структура
ее неоднородна и представлена тремя слоями
[Scarpelli Е., 1977]. Внутренний, находящийся
на воздушно-гипофазной границе, состоит из
фосфолипидов, придающих всей мембране по­
верхностное натяжение, близкое к нулю. Гипо­
фаза — второй слой — содержит все компо­
ненты сурфактантной системы и служит ис­
точником восполнения внутреннего слоя (схе­
ма 4). Третий слой — гипофазно-клеточная
граница — состоит из углеводов и является
местом секреции иммуноглобулинов (IgA),
некоторых ферментов (фосфолипазы).
Дефицит поверхностно-активных веществ
вследствие диффузного повреждения сурфак­
тантной системы резко изменяет механические
свойства легких, нарушая возможность осу­
ществления легочного газообмена не только
при спонтанном дыхании, но даже и на фоне
ИВЛ методом вдувания. Эти изменения могут
возникать вследствие прямого повреждения
легкого (при травме, инфекции и т. п.), а также
в результате нарушения метаболизма и микро­
61
Рис. 39. Изменение объемов легких в различные фазы ды­
хательного цикла.
ДО — дыхательный объем; РОВД — резервный объем вдоха;
РОВЫД — резервный объем выдоха; ОО — остаточный объем;
ОЕЛ — общая емкость легких; ЖЕЛ — жизненнвя емкость лег­
ких; Евд — емкость вдоха; ФОЕ — функциональная остаточ­
ная емкость.
Наибольшее количество воздуха, которое мо­
жет быть выдохнуто после максимального вдо­
ха, достигаемого с помощью мышечного уси­
лия, представляет собой жизненную емкость
легких (ЖЕЛ). РОВЫД и ОО вместе составляют
функциональную остаточную емкость (ФОЕ), а
часть общей емкости легких (ДО и РОВД) при­
нято называть емкостью вдоха (Еад).
Представленные уровни деления объема газа,
содержащегося в легких, определяют не только
статические легочные объемы, но и соотноше­
ние величины транс пульмонального и транс­
бронхиального давления и создаваемой им объ­
емной скорости газотока в воздухопроводя ­
щей системе. Эти соотношения нелинейны, и
эта нелинейность прогрессивно увеличивается
при возрастании воздушного потока. При фор­
сированном полном вдохе из положения мак­
симального выдоха транспульмональное дав­
ление плавно увеличивается и достигает мак­
симума на высоте вдоха. Поток воздуха, не­
смотря на продолжающееся увеличение уси­
лия после выдоха 50 % ЖЕЛ, прогрессивно
снижается, достигая нуля на высоте давления.
При форсированном выдохе максимальный
поток достигается при уровне 70—80 % ЖЕЛ
на фоне прогрессирующего прироста давле­
ния. После достижения этого предела поток
уменьшается и падает до нуля гораздо резче,
чем при вдохе. Уменьшение потока газа при
одновременном нарастании давления указывает
на увеличение сопротивления газотоку. В ре­
зультате величина транспульмонального дав­
ления во время выдоха относительно больше,
чем во время вдоха. Уменьшение объемной
скорости газотока во время форсированного
выдоха, несмотря на увеличение транспульмо­
нального давления, свидетельствует об изме­
нении механических свойств легких на выдохе.
На высоте форсированного вдоха в связи
с падением внутриплеврального давления раз­
вивается градиент давления по направлению
от рта к респиронам. Поскольку наибольшее
отрицательное давление создается в респира­
торной зоне легкого, то в воздухоносной зоне
трансбронхиальное давление будет тем выше,
чем больше калибр бронха, в результате чего
и происходит расширение воздухопроводя­
щих путей, наиболее выраженное в их прокси­
мальном отделе. Во время форсированного
выдоха внутриплевральное давление становит­
ся положительным, а давление в респиратор­
ной зоне наибольшим. По ходу воздухоносной
зоны легких трансбронхиальное давление сни­
жается до атмосферного в ротовой полости.
Следовательно, на протяжении дыхательных
путей должна быть точка, в которой транспуль­
мональное давление равно нулю; она называет­
ся точкой равных давлений. Эта точка делит
дыхательные пути на два сегмента: в перифе­
рическом сегменте трансбронхиальное давле­
ние положительное, в центральном — отрица­
тельное. В бронхах, расположенных нейтраль­
нее точки равного давления, создаются усло­
вия для спадения бронхов, приводящие к фи­
зиологическому экспираторному стенозу. Сте­
пень такого бронхостеноза будет зависеть от
эластических свойств бронхиальной стенки
и соотношения статического и динамического
давлений в потоке, сумма которых является
постоянной величиной. Поэтому снижение
линейной скорости газотока приводит к увели­
чению статического давления потока, поддер­
живающего стенку бронха.
В процессе форсированного выдоха точка
равного давления смещается от трахеи к дис­
тальным, периферическим отделам воздухо­
проводящих путей. Так, после выдоха, равного
50 % ЖЕЛ, точка равного давления распола­
гается сразу за долевыми бронхами, после
выдоха 75 % ЖЕЛ она располагается в брон­
хах с сечением менее 3 мм, которые легко спа­
даются на фоне отрицательного давления. Та­
ковы соотношения, лежащие в основе экспира­
торного закрытия дыхательных путей. Любая
легочная и внелегочная патология, ведущая к
потере эластичности дыхательных путей и уско­
рению газотока на выдохе, неизбежно усили­
вает экспираторное закрытие [Щелкунов В. С.
и др., 1980]. Существенную роль в возникнове­
нии его на операционном столе играет режим
ИВЛ, характеризующийся укорочением выдоха
или созданием активного выдоха. Экспиратор­
ное закрытие дыхательных путей считается
одним из ведущих механизмов в возникнове­
нии послеоперационной гипоксемии, резистент­
ной к ингаляциям Ог, что требует специальных
методов лечения.
62
Работа дыхания. Для понимания достаточ­
ности газообменной функции легких важно
определение трех сторон работы дыхания: об­
щей механической работы, выполняемой по
ходу одного дыхательного акта или в единицу
времени, отношения между общим количест­
вом работы и той ее частью, которая затрачи­
вается на вентиляцию воздухоносных про­
странств и потребление кислорода дыхатель­
ными мышцами.
Величина работы дыхания характеризует об­
щее усилие дыхательной мускулатуры и зависит
от МОД.
Работа дыхания может быть разделена на
ряд компонентов соответственно характеру
сопротивления: рестриктивный, обструктивный
и инерционный. На преодоление эластического
' сопротивления в норме приходится 2/з, а не­
эластического— */з всей работы дыхания.
В случае ожирения, большой массы грудной
клетки и живота существенное значение начи­
нает играть инерционный компонент. Многооб­
разные механизмы регуляции дыхания обес­
печивают оптимальный дыхательный объем и
частоту дыхания при наименьшем расходе
энергии на вентиляцию. Расстройства регуляции
дыхания могут привести к нарушению этого
соответствия даже при нормальном состоянии
собственно аппарата дыхания. Когда податли­
вость легких уменьшается (при фиброзе, за­
стойных явлениях), дыхание становится частым
и поверхностным, так как при произвольном
углублении вдоха будет резко возрастать рабо­
та по преодолению эластического сопротивле­
ния. При возрастании неэластического сопро­
тивления в случаях диффузной обструкции
бронхиального дерева дыхание становится мед­
ленным и глубоким, так как учащение дыха­
ния приведет к резкому возрастанию затрат
энергии на преодоление неэластического сопро­
тивления току воздуха.
Соотношение МОД и той его части, которая
используется в газообмене (так называемой
альвеолярной вентиляции), позволяет опреде­
лить полезную работу дыхания, которая будет
меняться в зависимости от кислородного за­
проса организма. По мере увеличения венти­
ляции работа дыхания возрастает в логариф­
мической зависимости. Предельное значение
общей работы дыхания у здоровых при мак­
симальном МОД равно 51,6+18 кгм у мужчин
и 33,2+13 кгм у женщин [Кадиев Н. Н., Куз­
нецова В. К., 1976]. Предельные значения рабо­
ты дыхания у больных с легочной патологией
значительно снижены. Работа в 8—12 кгм мо­
жет оказаться непосильной для пациентов с
обструктивными нарушениями в силу значи­
тельного снижения предела увеличения венти­
ляции.
У здоровых людей эффективный предел уве­
личения вентиляции не превышает 60—70 %
максимально возможной вентиляции легких.
Дальнейший прирост вентиляции не обеспечи­
вает дополнительного поступления кислорода
в ткани вследствие того, что весь дополнитель­
но поступивший кислород потребляется самими
дыхательными мышцами, что, таким образом,
лимитирует выполнение физических нагрузок.
О потреблении кислорода дыхательными мыш­
цами судят по величине так называемой «кис­
лородной цены дыхания», которая определя­
ется по количеству кислорода, потребляемого
дыхательными мышцами при вентиляции 1 л
воздуха.
Следует отметить, что при спокойном дыха­
нии дыхательные мышцы здоровых людей ис­
пользуют лишь 5 % потребляемого организ­
мом Ог и только при значительной гипервен­
тиляции (более 50 л/мин) потребление кисло­
рода дыхательными мышцами возрастает до
20 %.
Обтурационные нарушения вентиляции,
ригидность грудной клетки и легких, ограниче­
ние подвижности диафрагмы при различных
заболеваниях и повреждениях аппарата дыха­
ния приводят к значительному увеличению
кислородной цены дыхания: уже при сравни­
тельно невысокой гипервентиляции
(15—
20 л/мин) потребление кислорода дыхатель­
ными мышцами в этих условиях составляет
25—40 %
кислородного дебита организма
[Levilhson Н., Cherniak R., 1968]. Высокая кис­
лородная цена дыхания может стать крайне
опасной для больного после резекции легкого
или при уменьшении диффузионной возмож­
ности его в связи с послеоперационными ос­
ложнениями.
ФИЗИОЛОГИЯ РЕСПИРАТОРНОЙ
ЗОНЫ ЛЕГКИХ
При дыхании вдыхаемый воздух увлажня­
ется и согревается в верхних дыхательных
путях, носовых ходах, трахее и крупных брон­
хах и по воздухопроводящей системе, емко­
стью 150—180 мл, поступает в респираторную
зону, емкость которой в норме составляет около
1300 мл. Специальные исследования показа­
ли [Weibel J., 1970], что скорость газового по­
тока резко падает при переходе из дыхатель­
ных путей, содержащих хрящи, в пути мембра­
нозного строения, составляя в них 0,1—0,01 ско­
рости потока в трахее. По ходу воздухоносных
путей возникает послойная неравномерность
состава газовой среды, концентрация основных
компонентов в которой меняется от уровня вды­
хаемого воздуха до уровня, находящегося в аль­
веолах.
63
Четкой границы между воздухопроводящей
зоной, где нет контакта между воздухом и ле­
гочными капиллярами, и респираторной зоной
нет. Скорее можно выделить переходную, или
транзиторную, зону, где наряду с проведением
воздуха происходит и газообмен в малочислен­
ных (не более 2 % от общего числа) альвео­
лах, расположенных на поверхности бронхиол.
Объем воздуха, содержащийся в транзиторной
зоне, составляет около 200 мл. Эта зона не­
постоянна по объему и положению, ибо смеща­
ется по бронхиальному дереву в зависимости
от режима дыхания и в первую очередь от ско­
рости вдоха.
В связи с небольшим диаметром респиронов
(0,45 мм на вдохе и 0,35 мм на выдохе) газы
быстро диффундируют между дыхательной
бронхиолой и диффузионной мембраной. Коэф­
фициент диффузии газов очень высок: кисло­
род диффундирует в газовую среду в 300 тыс.
раз быстрее, чем в воду, а углекислый газ —
соответственно в 13 тыс. раз. Поэтому газы с
одинаковой скоростью диффундируют через
слой воздуха в 0,45 мм (450 мкм) при разнице
парциальных давлений в 1 мм рт. ст. и через
альвеолярно-капиллярную мембрану в 2 мкм
при градиенте давлений в 60 мм рт. ст. для
кислорода и 6 мм рт. ст. для углекислого газа.
Неподвижность газа над диффузионной мемб­
раной предохраняет нежнейшие структуры лег­
ких от термического повреждения и сохраняет
жизнь человеку в экстремальных условиях. При
этом имеет значение не только респираторная
зона с ее неподвижной газовой средой, но и так
называемое «мертвое» пространство, в котором
происходят согревание, очищение и увлажне­
ние вдыхаемого воздуха.
До последнего времени величина «мертвого»
пространства учитывалась для оценки эффек­
тивности обновления газа в респираторной зо­
не, исходя из знания величины ДО. Однако
оказалось, что некоторое количество воздуха
поступает в респироны и в тех случаях, когда
до гораздо меньше объема анатомического
«мертвого пространства» (150 мл). Дело в том,
что вдыхаемый газ движется по воздухонос­
ным путям не прямоугольным, а коническим
фронтом. Переходная зона в таких случаях
смещается к трахее. Кроме того, процесс под­
держания постоянства состава газа над диффу­
зионной мембраной определяется не только
общим объемом вентиляции, но и равномерно­
стью распределения газа в легких.
Даже в здоровом организме различное уча­
стие верхних и нижних долей в вентиляции,
разное положение тела, неодинаковая податли­
вость долей и т. п. способствуют неравномер­
ному распределению вдыхаемого газа. При раз­
личных поражениях бронхиального дерева и
64
респираторной зоны вдыхаемый газ распреде­
ляется еще более неравномерно.
Наряду с неравномерностью распределения
газотока необходимо учитывать и неравномер­
ность распределения крови по другую сторону
от диффузионной мембраны, в капиллярах
легкого. Доказано, что даже при спокойном
дыхании кровоток в легких неравномерен:
хорошо известны периодические «спонтанные»
колебания открытых капилляров в одном и том
же отделе легких, большая скорость крово­
тока в периферических отделах легких по срав­
нению с центральными, возрастание ее в нап­
равлении от верхних отделов к нижним. При
глубоком дыхании разница в кровоснабжении
различных отделов легких уменьшается.
В «идеальных» условиях суммарное отноше­
ние вентиляции к кровотоку равно 0,8, так что
в респираторной зоне легких в минуту обнов­
ляется в среднем 4 л воздуха и 5 л крови. По­
этому создание адекватного вентиляционно­
перфузионного отношения, которое быстро
меняется в физиологических условиях и легко
выходит за оптимальные пределы при патоло­
гических состояниях, является основным усло­
вием оптимальности легочного газообмена.
К настоящему времени накоплено много
данных о наличии координации между венти­
ляцией и кровотоком на уровне респирона.
Основное значение в этой регуляции придается
зависимости тонуса легочных артериол от со­
става газовой среды над диффузионной мембра­
ной в каждом отдельном респироне, в частно­
сти от парциального давления кислорода
[Савицкий Н. Н., Трегубов А. А., 1940; Fichman J., 1961; Staub P„ 1963]. Влияние повышен­
ного содержания углекислого газа на тонус
и кровоток в легочных сосудах выражено менее
четко. Определенное значение имеет изменение
тонуса мускулатуры дыхательных бронхиол,
меняющих не только «вход» в респирон и диф­
фузию газа к дыхательной мембране, но и дав­
ление в респироне, что оказывает влияние на
кровоток. Существует еще один местный меха­
низм регуляции отношения вентиляции к кро­
вотоку, в роли которого выступают поверхност­
но-активные вещества. Поскольку в состоянии
покоя в газообмене участвуют не все респи­
роны, то в «закрытых» респиронах идет нако­
пление этих веществ, тогда как в активно функ­
ционирующих респиронах их запасы истоща­
ются. Это приводит к выключению «дышащих»
респиронов и включению «недышаших», но
имеющих сохраненный, хотя и редуцированный,
кровоток.
По этим причинам количественные измене­
ния минутного объема дыхания (МОД) мало­
информативны для диагностики дыхательных
нарушений у больного заболеваниями легких.
В патологических условиях регионарные
изменения отношения вентиляции к кровотоку
могут создать две крайние ситуации, при кото­
рых нарушается оксигенация крови в легких.
Первая напоминает вентиляцию «мертвого про­
странства» и приводит к увеличению отношения
выше 0,8. При такой ситуации уменьшено число
функционирующих капилляров или имеется
гипервентиляция одного из отделов легких с
нормальным кровотоком. Насыщение крови
кислородом происходит на фоне уменьшенного
эффективного объема вентиляции, при котором
значительная часть газа не достигает диффу­
зионной мембраны, а напряжение кислорода в
газовой среде респиронов постепенно снижается.
Второе крайнее состояние связано с появле­
нием значительного количества нсвентилируе­
мых респиронов и подобно шунтированию кро­
ви: отношение вентиляции к кровотоку ниже
0,8. В невентилируемых респиронах кровь окси­
генируется незначительно, сохраняет свойства
венозной и смешивается на пути оттока с пол­
ностью оксигенированной из хорошо вентили­
руемых респиронов. Если число последних доста­
точно, то задержки углекислого газа нет. Воз­
можна и истинная примесь венозной крови.
Ингаляция кислорода ликвидирует шунтопо­
добный эффект неравномерности обновления
газа над диффузионной мембраной.
Диффузия газов. Освещение процессов га­
зообмена будет неполным, если не учитывать
особенности диффузии кислорода и углекисло­
го газа через дыхательную мембрану. Аэрогематический барьер, через который диффун­
дируют эти газы в легких, имеет толщину около
2 мкм и включает в себя альвеолярный эпите­
лий, межтканевую жидкость, эпителий капил­
ляров, плазму крови, стенку и внутриклеточную
жидкость эритроцита. В функциональном отно­
шении этот барьер не является инертным водно­
тканевым слоем, а представляет собой активно
функционирующую преграду с неравновесной
структурой. Скорость прохождения газов через
нее зависит не только от градиента парциальных
давлений, определяющего диффузию газов, но и
от направления диффузии. Углекислый газ бы­
стрее выделяется из крови, чем проникает
в нее, хотя скорость диффузии для углекислого
газа в кровь примерно в 20 раз выше, чем для
кислорода. Наоборот, растворимость кислорода
в липидах поверхностно-активных веществ вы­
ше, чем в других органических веществах и
растворах [Березовский В. А., Горчаков В. Ю.,
1982]. В модельных экспериментах пленка сур­
фактанта проявляла отчетливую способность
ускорять перенос кислорода из газовой среды,
что позволяет рассматривать сурфктантную си­
стему как конденсатор кислорода, облегчающий
его транспорт через аэрогематический барьер.
5 Зак. 0517
Это особенно важно, так как время пребывания
крови в легочном капилляре всего вдвое больше
времени, достаточного для установления равно­
весия между напряжением кислорода в газовой
среде респиронов и в легочной капиллярной
крови.
Другая особенность обмена кислорода в лег­
ких состоит в том, что процесс его переноса через
аэрогематический барьер считается завершен­
ным лишь после того, как молекулы кислорода
вступят в химическую связь с гемоглобином,
причем на этапе этой реакции имеется допол­
нительное сопротивление транспорту кислоро­
да в связи с положением кривой диссоциации
оксигемоглобина, которое определяется рядом
факторов, как неспецифических (концентра­
цией Н и К', напряжением углекислого газа,
температурой тела), так и специфических для
эритроцитов (концентрацией гемоглобина, ор­
ганических фосфатов, глютатиона). Это допол­
нительное сопротивление может иногда вдвое
замедлить поступление кислорода в кровь при
отсутствии существенных изменений условий
транспорта углекислого газа.
Поэтому, говоря о нарушениях диффузии в
легких, имеют в виду в основном нарушение
диффузии кислорода. Кривая диссоциации свя­
занного углекислого газа крутая во всех уров­
нях. Уравновешивание напряжения углекисло­
го газа в респироне и в легочных капиллярах
происходит за 0,072 с, в то время как эритро­
цит находится в капилляре 0,1—0,3 с. Поэтому
значительное нарушение диффузии углегислого газа должно сочетаться с таким нарушением
обмена кислорода, при котором жизнь невоз­
можна.
Следует различать диффузионную способ­
ность легких и нарушения диффузии, ведущие
к расстройству легочного газообмена. Умень­
шение размеров диффузионной мембраны в
силу повреждения респиронов при острых и хро­
нических воспалительных процессах в легких,
выключении части капиллярного русла, удале­
нии значительной части функционирующей диф­
фузионной мембраны при резекции легких мало
сказывается на процессах оксигенации крови и
элиминации углекислого газа вне связи с на­
рушениями вентиляционно-перфузионного соот­
ношения.
Простейший тест на существование диффу­
зионных нарушений — наличие гипоксемии безгиперкапнии и увеличение гипоксемии при про­
извольной гипервентиляции [Зильбер А. П.,
1977].
Снижение Ро в артериях большого круга кро­
вообращения может быть результатом одного
или нескольких изменений функционирования
респираторной зоны. Среди них можно выделить
следующие ситуации:
65
1) гиповентиляция всех или большинства
респиронов, тотальное нарушение обновления
газовой среды респираторной зоны (в этом слу­
чае гипоксемии способствуют задержка угле­
кислого газа, гиперкапния);
2) неравномерное соотношение вентиляции
и перфузии в различных отделах легких (на­
пряжение углекислого газа в артериальной
крови в таких случаях может быть пониженным,
нормальным или повышенным в зависимости
от способности организма к гипервентиляции
в ответ на гипоксемию);
3) сброс крови из малого круга в большой
вследствие шунтирования крови через внутрилегочный или внутрисердечный шунты (в этих
случаях напряжение углекислого газа нормаль­
но или снижено, так как легкие практически
здоровы, а аппарат внешнего дыхания спосо­
бен к гипервентиляции, но существенное зна­
чение приобретает состояние легочного сосу­
дистого русла).
ГАЗООБМЕН
И ЛЕГОЧНЫЙ КРОВОТОК
По сравнению с циркуляцией крови в боль­
шом круге кровообращения легочный кровоток
имеет ряд характерных особенностей. Малый
круг кровообращения относится к системе низ­
кого давления, для которой характерны низкое
сосудистое сопротивление и большая растя­
жимость сосудов. Во время систолы сердца
крупные разветвления легочной артерии вме­
щают кровь, которая во время диастолы посту­
пает в периферическое разветвление легочных
сосудов, что поддерживает равномерность кро­
вотока в легком.
Легочные артериолы имеют диаметр 60 —
80 мкм, т. е. они в 5—6 раз шире, чем в большом
круге. Вследствие этого величина сосудистого
сопротивления в легких может быть в 6—8 раз
меньше, чем сопротивление сосудов большого
круга. При этом распределение сопротивления
по ходу кровотока также различно: в боль­
шом круге кровообращения основное сопротив­
ление оказывают артериолы, в малом значи­
тельную часть (до 30 %) составляет сопротив­
ление в венозном отделе.
Объем крови в легких, составляющий в покое
примерно ‘/4 часть всей массы циркулирующей
крови, может легко изменяться без существен­
ных изменений давления в сосудах легкого. При
кровопотере кровь из легких быстро мобили­
зуется в большой круг. Наоборот, при быстром
вливании растворов значительная ее часть не­
медленно оказывается в сосудах легких. Все
сосудосужающие факторы, повышающие со­
противление кровотоку в большом круге (кате­
холамины, боль, гиперкапния, гипоксемия и
др.), увеличивают легочный объем крови на 40—
50 %.
Растяжимость легочных сосудов обеспечи­
вает постоянство давления в капиллярах, не­
смотря на значительные колебания МОК. Хотя
давление в артериях малого круга в 6—7 раз
ниже, чем в соответствующих отделах боль­
шого круга кровообращения, увеличение МОК
в 2—3 раза не повышает давление в легочной
артерии. Некоторое повышение наблюдали
только при увеличении кровотока через легкие
в 5—6 раз [Reemstma А., 1961].
Наличие артериовенозных анастомозов диа­
метром до 400 мкм при усиленном кровенапол­
нении малого круга обеспечивает ток крови в
обход респиронов в легочные вены, предотвра­
щая перегрузку правого сердца при нарушениях
кровообращения в легких. При этом возникает
различной степении гипоксемия, зависящая
от объема шунтируемой крови.
Тонус легочных сосудов и кровоток через
малый круг регулируется нервными и гумораль­
ными механизмами в зависимости от имп^льсации с рецепторов легочных сосудов, измене­
ния сердечной деятельности, тонуса сосудов
большого круга кровообращения. Именно с этих
позиций следует оценивать многие стороны кли­
нических проявлений таких патологических
состояний, как отек легких или тромбоэмболия
легочной артерии. Решающую роль в процессе
циркуляции играет трансмуральное давление,
т. е. разность между давлением крови и давле­
нием, прилагаемым к сосуду снаружи. Для вен
и артерий легкого трансмуральное давление
представляет градиент между давлением в этих
сосудах и внутриплевральным давлением, для
легочных капилляров — между капиллярным
и внутрилегочным, альвеолярным давлением.
Так как и альвеолярное, и внутриплевральное
давление изменяются в течение дыхательного
цикла, то даже их небольшие изменения могут
оказывать существенное влияние на трансму­
ральное давление, а следовательно, просвет и
сопротивление в зоне микрососудов.
Не вдаваясь в подробности обширной обла­
сти физиологии легочного кровотока при из­
менении функционирования сердца, следует
подчеркнуть, что для кровообращения и, преж­
де всего, кровообращения в малом круге боль­
шое значение имеют механизмы и процессы,
обеспечивающие легочный газообмен.
Легочные капилляры занимают более 80—
85 % диффузионной мембраны и находятся в
тесном контакте с газовой средой респиронов.
Капиллярная сеть обеспечивает воздухоносные
пространства двух соседних альвеол одного и
того же или разных респиронов. Если в других
паренхиматозных органах стромой является
опорная соединительная ткань, то в легких она
66
находится практически вне респираторной зоны,
в области расположения более крупных сосу­
дов и бронхов. Роль опорной ткани в основном
выполняет воздух, содержащийся в респиронах. Интерстициальному (тканевому) давле­
нию в других органах, которое противостоит
транссудации и отеку, в легких соответствует
альвеолярное давление. Роль этого давления
проявляется и в определенных структурных
особенностях более крупных разветвлений ле­
гочного сосудистого русла.
Легочные артериолы относительно бедны
мышечными элементами, тогда как дыхательные
бронхиолы, играющие роль регуляторов воздухонаполненности респиронов, снабжены
мышцами, многочисленными нервными элемен­
тами. Под влиянием нервных и гуморальных
стимулов сократительные структуры бронхиол
могут действовать как сфинктер.
В мышцах и других внутренних органах эрит­
роциты большой силой гидростатического дав­
ления проталкиваются через узкие капилляры
диаметром 5—6 мкм, т. е. меньше диаметра
эритроцита. В капиллярах легких гидростати­
ческое давление низкое, но ток крови возмо­
жен, потому что их просвет больше диаметра
эритроцита (20—25 мкм). Однако этот просвет
решающим образом зависит от давления газа
в респироне. При сужении бронхиолы и выклю­
чении респирона из вентиляции он спадается,
капилляры суживаются, и циркуляция в значи­
тельной части капиллярного ложа прекращается
в связи с возрастанием сопротивления в этой
сосудистой зоне. При увеличении вентиляции и
раскрытии большей части респиронов капилля­
ры открываются, диффузионная поверхность
увеличивается. В силу большого резерва функ­
ционирующих капилляров ни острое увеличе­
ние кровотока через малый круг, ни трансфу­
зионная эмболия микросгустками при быстром
массивном переливании консервированной
крови, ни уменьшение кровеносного русла даже
наполовину (при пульмонэктомии) не вызы­
вают сколько-нибудь длительного и значитель­
ного повышения давления в легочной артерии.
Вентиляция оказывает влияние и на такие фак­
торы, обеспеч"вающие кровоток через легкие,
как сила сокращения правого желудочка, гра­
диент давления между легочными артериями и
венами, вазомоторный тонус. Количество кро­
ви, выбрасываемое правым желудочком, будет
колебаться в зависимости от фаз дыхательного
цикла. Ритмический характер колебаний дав­
ления в легком облегчает приток крови в ка­
пилляры во время обычного вдоха и опорожне­
ние во время выдоха. При чрезмерно глубоком
вдохе влияние отрицательного внутрилегочного
давления сказывается на сосудах большого и
среднего калибра. Капилляры сжимаются вслед­
5*
ствие растяжения межальвеолярных перегоро­
док, сопротивление кровотоку в малом круге
частично перемещается в зону капилляров.
Во время вдоха ударный объем правого же­
лудочка возрастает (на 15—40 %). Одновре­
менно снижаются ударный объем левого желу­
дочка сердца (на 10—15 %) и пульсовое давле­
ние в аорте. Это зависит от увеличения притока
крови к сердцу с возрастанием диастолического
наполнения правого предсердия и с растяжением
легочных вен, стенка которых связана с парен­
химой легкого. Значительное увеличение емко­
сти этих вен уменьшает приток крови к левому
предсердию, а следовательно, и ударный объем
левого сердца. Чем больше размахи транспуль­
монального давления, отражающие изменения
механических свойств легких, тем более выра­
жены колебания ударного объема сердца. Вы­
сокая корреляция показателей механики дыха­
ния и колебаний ударного объема крови на про­
тяжении дыхательного цикла позволяет вос­
пользоваться индексом дыхательных измене­
ний ударного объема как одним из критериев
оценки состояния механики дыхания [Страш­
нов В. И. и др., ] 980; Тищенко М. И. и др., 1982].
Если в этой части функциональных связей
легочного газообмена и кровообращения основ­
ное значение имеет пассивное изменение при­
тока крови к сердцу, просвета легочных капил­
ляров и вен, то существует и вторая, более ак­
тивная сторона взаимодействия дыхания и пер­
фузии легких, а именно: влияние на кровооб­
ращение состава газовой среды респираторной
зоны в целом и отдельных респиронов в част­
ности. Компенсаторное перераспределение кро­
ви из плохо вентилируемых отделов в хорошо
вентилируемые, где сопротивление току мень­
ше, может осуществляться и через вегетатив­
ную нервную систему, по типу аксон-рефлекса
или под влиянием гуморальных воздействий,
как следствие анаэробной инверсии обменных
процессов в легочной ткани, приводящих к мест­
ному образованию сосудосуживающего фактора.
Более сложные рефлекторные воздействия на
вазомоторный тонус и перераспределение крови
в легких включаются в регуляцию перераспре­
деления кровотока лишь при крайних отклоне­
ниях нормального функционирования дыха­
тельной системы или при патологических со­
стояниях.
Обычно низкий уровень кровяного давления
в сосудах малого круга кровообращения приво­
дит к выраженным влияниям на распределение
кровотока в легких гравитационных факторов.
Легко выделяются три зоны [Зильбер А. П.,
1971]. При вертикальном положении испытуе­
мого среднее легочное артериальное давление
на уровне сердца составит около 25—20 мм
рт. ст. В артериальных сосудах верхних отделов
67
легких оно снижено на величину гидростати­
ческого столба крови и приближается к нулю.
Внутриальвеолярное давление в верхушках лег­
ких в этих условиях больше артериального и
венозного, в результате чего капилляры при
спокойном дыхании спадаются и кровоток прак­
тически прекращается. В отделах легких, рас­
положенных ниже уровня сердца, происходят
противоположные явления: внутрисосудистое,
а значит и трансмуральное давление повышено,
просвет сосудов расширен, кровоток усилен.
Если испытуемого положить на спину или на
бок, то гравитационные изменения равномер­
ности кровообращения в легком будут также
прослеживаться: в вышележащем легком кро­
воток падает, в то время как в нижележащем —
возрастает.
При хирургическом лечении больных, когда
премедикация и анестезия нарушает ауторе­
гуляцию сосудистого тонуса, ИВЛ и операци­
онный пневмоторакс сообщают распределению
легочного кровотока большую неравномер­
ность. Создаются все условия для существенного
нарушения вентиляционно-перфузионных
отношений, что требует обязательного обога­
щения вдыхаемого газа кислородом для устра­
нения возможной гипоксемии. В нормальных
условиях существует тонкое и быстрое регули­
рование соответствия между распределением
вдыхаемого воздуха и циркулирующей крови
в легких, что обеспечивает эффективность окси­
генации крови. Это привело к предположению
о существовании специальных механизмов,
обеспечивающих соответствие локального кро­
вотока и вентиляции отделов легких (рефлекс
Эйлера — Лилиестранда). Основное значение в
этой регуляции имеет высокая чувствительность
тонуса легочных сосудов к изменению состава
газовой среды респиронов.
Существующее в нормальных условиях тон­
кое соответствие между распределением газа
и крови в респиронах обеспечивает почти нор­
мальное насыщение гемоглобина кислородом
при значительном снижении МОД и минималь­
ном МОК. Сужение артериол в ответ на паде­
ние Ро. в респиронах представляет до некото­
рой степени биологически полезную реакцию,
устраняющую несоответствие между вентиля­
цией и кровотоком. В таких условиях давление
в легочной артерии меняется в зависимости от
состава газовой среды респираторной зоны
[Nahas G., 1956]. Однако полезность этой реак­
ции относительна, так как снижение Ро, во мно­
гих респиронах обусловливает спазм артериол
с развитием гипертензии в малом круге. При
этом определенную роль могут играть не только
артериолы, но и посткапиллярные отделы легоч­
ного сосудистого русла и легочные вены [Gor­
don N., Katz S., 1962].
На определенном этапе дыхательных рас­
стройств эта реакция становится независимой.
При полном прекращении дыхательных дви­
жений сохраняются и кровоток через легочные
сосуды, и поглощение кислорода, но не выво­
дится углекислый газ, что послужило физиоло­
гическим обоснованием так называемого диф­
фузионного дыхания. Другим доказательством
независимости легочного кровотока от венти­
ляции является развитие первичной легочной
гипертензии с затруднением кровотока через
респираторную зону без изменения функции
внешнего дыхания.
Необходимо подчеркнуть, что второстепенным
в развитии легочной гипертензии является уве­
личение МОК в ответ на значительное и дли­
тельное падение насыщения гемоглобина в ар­
териальной крови до 80—85 %. Прямое дей­
ствие гиперкапнии, как было сказано выше,
играет незначительную роль в реакциях сосу­
дов малого круга. Наоборот, увеличение со­
держания углекислого газа в крови, раздражая
рецепторы аортальной и синокаротидной зон,
может привести к рефлекторному расширению
легочных сосудов.
Уменьшение объема функционирующего со­
судистого русла при обструктивной эмфиземе,
обострение хронического воспалительного про­
цесса в легких, нарушение отношения вентиля­
ции к кровотоку с развитием артериальной ги­
поксемии могут привести у таких больных к раз­
витию гипертензионного криза в малом круге
при повреждении легкого. Особенно опасно
вмешательство на легких у больных, уже имею­
щих отчетливую легочную гипертензию.
Имеется еще одна особенность кровотока в
легких. Дело в том, что активная реакция легоч­
ной паренхимы бодее основная, чем реакция
притекающей к легким крови. Градиент кон­
центрации [-Р в крови и тканях в случаях аци­
доза в системной артериальной крови снижа­
ется во всех органах и тканях, но повышается
в легких (при поступлении кислой венозной
крови): изменение просвета органных сосудов
на фоне ацидоза будет иметь различную биохи­
мическую основу. Расширение легочных сосу­
дов при нарушении процессов окисления и на­
коплении недоокисленных продуктов облегчает
оксигенацию крови и кислородное обеспече­
ние организма.
Этот ионный механизм дает возможность
по-новому интерпретировать некоторые защит­
но-приспособительные механизмы, связанные
с особенностями коллатерального кровотока
в легких. Кроме анастомозов, обеспечивающих
связь между сосудами малого и большого кругов
(сброс «справа налево»), на уровне респиро­
нов в легких имеются также бронхолегочные
анастомозы: бронхиальная артериола — легоч­
68
ная артериола — капилляр — венула — ле­
гочная вена. Основной особенностью этих ана­
стомозов является то, что они представляют
единственное место, где кровь из большого
круга кровообращения непосредственно пере­
ходит в малый. В этих коммуникациях всегда
одно направление тока крови, несмотря на
любые колебания давления в малом круге. Повидимому, стенки бронхолегочного анастомоза
играют роль химически регулируемых клапа­
нов, пропуская менее кислую кровь из большого
круга и не пропуская в последний более кислую
легочно-капиллярную кровь.
При тяжелой физической нагрузке или гипок­
сии, вызванной недостатком кислорода во вды­
хаемом воздухе, открывается путь для посту­
пления крови из большого круга непосредствен­
но в расширенные сосуды респираторной зоны,
что обеспечивает дополнительную экспозицию
недостаточно оксигенированной крови и более
полную (исходя из возможностей легкого) ее
оксигенацию [Парин В. В., 1946].
зависимость между активностью эфферентной
импульсации с механорецепторов и воздухонаполненностью легких [Жданов В. А., 1976].
Второй контур регулирования дыхания — хеморецепторный. Его отличительная черта — на­
личие датчиков, способных информировать
дыхательный центр о конечном физиологически
активном результате легочного газообмена —
о газовом составе внутренней среды организма.
Выделяют периферические (артериальные) и
центральные (медуллярные) хеморецепторы.
Артериальные хеморецепторы (гломус дуги
аорты и каротидные гломусы) служат аварий­
ным механизмом стимуляции дыхания при сни­
жении напряжения кислорода, росте напряже­
ния углекислого газа и концентрации ионов
водорода в артериальной крови. Медуллярные
хеморецепторы воспринимают изменения кон­
центрации ионов Н и Рсо спинномозговой и
внеклеточной жидкости мозга. Интеграция
центральных и периферических стимулов осу­
ществляется структурами моста головного
мозга, причем предпочтение отдается медул­
лярным
хемочувствительным
структурам
[Loescheke F., 1974]. Хеморецепторный кон­
тур работает по принципу обратной связи:
отклонение регулирующих параметров воздей­
ствует так или иначе на дыхательный центр,
а изменения дыхания приводят к уменьшению
возникших отклонений.
В системе регуляции дыхания реализован и
еще один принцип регулирования — по возму­
щению [Шик Л. Л., 1970]. Он заключается в
том, что изменения вентиляции могут происхо­
дить еще до отклонения в газовом составе крови.
Данные, полученные в ходе физических нагру­
зок, позволяют утверждать, что изменение
активности внешнего дыхания до начала мы­
шечной деятельности предупреждает предстоя­
щие изменения легочного газообмена. Управле­
ние внешним дыханием по принципу возму­
щения осуществляется с помощью более цент­
ральных (в том числе и корковых) механизмов
и может совершенствоваться путем тренировок.
С этих позиций понятно значение методически
правильно построенной дыхательной гимнасти­
ки во время предоперационной подготовки и
в послеоперационном периоде, когда особое
значение имеют оптимальный ритм и глубина
дыхания при минимальных энерготратах.
Полагают, что, кроме указанных, существует
и другой аспект построения регуляции дыхания.
В его основе лежит принцип оптимальности
функционирования при минимизации работы.
Регуляция направлена на выбор оптимальной
частоты и глубины дыхания и осуществляется
поисковым способом. Параметры последующе­
го дыхательного цикла программируются по ре­
зультатам предыдущего. При этом дыхательный
РЕГУЛЯЦИЯ ЛЕГОЧНОГО ГАЗООБМЕНА
И ДЫХАТЕЛЬНАЯ НЕДОСТАТОЧНОСТЬ
Физиологические и анатомические изыска­
ния позволили выдвинуть предположение, что
управление внешним дыханием осуществляет
центральный аппарат регуляции, обозначаемый
термином «дыхательный центр». Основное про­
явление активности дыхательного центра —
ритмогенез, формирование длительности и ча­
стоты фаз вдоха и выдоха, что определяет в
итоге МОД, который соответствует интенсив­
ности метаболизма в широком диапазоне из­
менений жизнедеятельности. Дыхательный
ритм формируется в результате взаимодейстия
между функционально различными группами
дыхательных нейронов.
Структурно-функциональная схема регуля­
ции дыхания содержит два основных контура
регулирования: механорецепторный и хеморецепторный. Оба контура, кроме центрального
регулятора, имеют единый эффекторный выход.
Эфферентная импульсация из дыхательного
центра продолговатого мозга поступает к мо­
тонейронам спинного мозга, а затем по диафраг­
мальным и межреберным нервам передается
к дыхательным мышцам, вызывая их сокраще­
ние. Степень растяжения легких и сокращения
дыхательных мышц контролируется механо­
рецепторами. Импульсы с этих рецепторов по­
ступают по межреберным нервам, восходящим
путям спинного мозга и по блуждающим нервам,
достигают дыхательного центра, замыкают
контур механорецепторного регулирования.
Этот контур работает по принципу управления
по отклонению. Установлена прямая линейная
69
центр контролирует эффект по механо- или
хеморецепторным данным и возвращает всю
систему в исходное состояние за минимальное
время и при затрате минимума энергии [Di­
euse L. et al., 1976]. Этот подход нуждается
в дальнейшем экспериментальном обосновании.
Рефлекторные влияния с висцеральной плев­
ры и рецепторов воздухоносных путей, баро- и
хеморецепторов крупных сосудов, проприорецепторов скелетных мышц способствуют быст­
рой перестройке работы аппарата дыхания, на­
ступающей раньше, чем изменится состав газо­
вой среды респиронов (например, при стенози­
ровании воздухоносных путей) или изменится
состав крови в связи с поступлением кислых
продуктов из областей нарушенного обмена.
С проблемой регуляции внешнего дыхания
тесно связано клиническое понятие дыхатель­
ной недостаточности. Поскольку основной эф­
фект внешнего дыхания и газообменной функ­
ции легких — артериализация венозной крови
и удаление избытка углекислого газа — конт­
ролируется аппаратом регуляции, то реализа­
ция физиологического результата легочного
газообмена будет зависеть от деятельности
самого аппарата, возможностей внешнего дыха­
ния и структурно-функционального состояния
респираторной зоны легкого. Это, наряду с ха­
рактером и продолжительностью патологиче­
ского процесса в легких, выраженностью пато­
логических последствий анестезии и операции,
определяет пределы компенсации нарушения
внешнего дыхания. Исходя из этих положений
под дыхательной недостаточностью понимают
«...состояние организма, при котором не обеспе­
чивается поддержание нормального газового
состава артериальной крови либо последнее
достигается ненормальной работой аппарата
внешнего дыхания, приводящей к снижению
функциональных возможностей организма».
Это определение дано 15-м Всесоюзным съез­
дом терапевтов. Многие трудности интерпре­
тации накопленных в последующем данных и
разногласия в определении этого понятия обус­
ловлены прежде всего тем, что при оценке
нарушений дыхания опираются на выявление
различного конечного физиологического ре­
зультата, постоянство которого поддерживает­
ся дыханием: газовым составом артериальной
крови, величиной реального транспорта кисло­
рода, эффективностью тканевого обмена. Одна­
ко, опираясь только на исследование резуль­
тата без изучения механизмов компенсации
нарушения, которые снижают функциональные
возможности организма, невозможно устано­
вить опасность нарушения для данного кон­
кретного больного. Это утверждение особенно
верно в случаях острого развития дыхательной
недостаточности, которая в таких обстоятель­
ствах сводится к нарушению легочного газо­
обмена.
Острота возникновения дыхательных рас­
стройств и их природа определяют необходи­
мость выбора и интенсивности лечебных меро­
приятий. В некоторых случаях молниеносное
(минуты) прогрессирование острой дыхательной
недостаточности ставит под угрозу жизнь боль­
ного и вынуждает проводить реанимационные
мероприятия с дополнением их специальными
пособиями по восстановлению эффективного
легочного газообмена. Нередко дыхательная
недостаточность протекает остро (часы) и приз­
наки ее прогрессирования заставляют наращи­
вать объем лечебных мероприятий. Чаще она
протекает подостро (дни) с постепенным регрес­
сом нарушений легочного газообмена, особенно
при профилактическом лечении. Реже дыха­
тельная недостаточность носит приступообраз ­
ный характер (при бронхиальной астме, повтор­
ных тромбоэмболиях) или возникает на фоне
хронического легочного заболевания с нестой­
кой компенсацией дыхательных расстройств.
Точная диагностика вида острой дыхательной
недостаточности проходит три этапа: опреде­
ление глубины нарушений легочного газообмена,
выявление основного функционального рас­
стройства, определяющего развитие дыхатель­
ной недостаточности, полная патофизиологи­
ческая характеристика этого состояния. В боль­
шинстве случаев дыхательной недостаточности
первостепенное значение имеет исследование
РСОг и Ро. артериальной крови. По этим данным
можно установить характер нарушения легоч­
ного газообмена (вентиляционное или парен­
химатозное) и его глубину [Шанин Ю. Н.,
Костюченко А. Л., 1982]. Быстродействующие
газоанализаторы
(масс-спектрографы,
хро­
матографы, капнографы) выдыхаемого воз­
духа, пневмотахографы и малоинерционные
спирографы на следующем этапе функцио­
нальной диагностики позволяют определить ряд
непосредственных и произвольных критериев,
уточняющих особенности дыхательных рас­
стройств. Эффективность и напряжение вен­
тиляции определяют по величинам дыхатель­
ного объема, форсированного выдоха, мощно­
сти выдоха, коэффициенту использования кис­
лорода, а также электрической активности ды­
хательных мышц и коэффициенту дыхатель­
ных изменений ударного объема при исследо­
вании центральной гемодинамики с помощью
интегральной реографии тела. Последователь­
ное определение Рао, при дыхании воздухом,
затем Ра0, и Расо при дыхании 100 % кисло­
родом в течение 20 мин позволяет определить
альвеолярно-артериальное различие для РОг,
которое возрастает при увеличении «истинного»
шунтирования крови в легких.
70
Турбулентность, возникающая при прохожде­
нии воздушного потока через дыхательные пути,
способствует удалению значительного количе­
ства механических частиц диаметром более
2—3 мкм. В результате инерционного столкно­
вения они быстро укрупняются и оседают на
поверхности слизистой оболочки бронхов. Ана­
томическая особенность бифуркационно-труб­
чатой архитектоники бронхиального дерева
способствует такой аэродинамической фильт­
рации. Попутно в крупных бронхах из вдыхае­
мого воздуха адсорбируются и раздражающие
газы (аммиак, двуокись серы, хлор). Все это
защищает диффузионную мембрану от боль­
шинства крупных частиц, взвешенных в воздухе.
Аэродинамичесая фильтрация может быть из­
менена рядом факторов окружающей среды.
Увлажнение вдыхаемого воздуха усиливает
гигроскопичность частиц с отложением их в
более верхних отделах бронхиального дерева.
Большинство более мелких частичек и часть
крупных эвакуируются мукоцилиарным покры­
тием бронхов и кашлевым механизмом. Эти
два механизма защиты взаимосвязаны.
Мукоцилиарный эскалатор — важнейший
защитный фактор легких. Плотно прилегая
друг к другу, реснитчатые эпителиальные клет­
ки выстилают внутреннюю поверхность возду­
хопроводящей зоны от трахеи до терминаль­
ных бронхиол. В месте перехода терминальных
бронхиол в дыхательные реснитчатый эпите­
лий резко обрывается и переходит в однослой­
ный плоский. Эти особенности определяют и
различия очищения воздухопроводящей и рес­
пираторной зон. В тех случаях, когда частицы
оседают на слизистой оболочке, покрытой рес­
нитчатым эпителием, они переносятся к трахее
течением слизи вдоль дыхательных путей за
счет волнообразного мерцания ресничек: биение
каждой реснички сочетается с последователь­
ным сокращением другой.
Деятельность ресничек осуществляется цик­
лически: их активные движения чередуются
с паузами в соотношении 1:4. Количество сли­
зи, ее вязкость, другие физические свойства,
определяющие способность к ретракции комка
слизи, имеют значение для систематического
ритмичного мерцания. Оно направлено в одну
сторону: от респираторной зоны до межчерпа­
ловидного пространства гортани, где слизь вы­
кашливается или заглатывается. Примерно
90 % осевших на бронхиальной слизи частиц
эвакуируется (при нормальном состоянии му­
коцилиарного эскалатора) в первый час после
оседания [Nagaishi С., 1976], что обеспечива­
ется большой скоростью движения слизи: 0,5—
1 мм/мин в бронхиолах и 15—20 мм/мин в тра­
хее. При этом слизь может транспортировать
частицы массой до 10—12 мг.
Такое сочетание клинического обследования
больного и углубленного функционального ис­
следования не всегда возможно даже в условиях
специализированных пульмонологических ста­
ционаров. Более доступен ограниченный объем
исследований, например анализ артериальной
крови, результаты которого не следует абсо­
лютизировать. Так, один и тот же уровень ар­
териальной гипоксемии (при паренхиматоз­
ных нарушениях) может неодинаково перено­
ситься различными больными и обусловливать
необходимость различных по интенсивности
лечебных мероприятий. При остром развитии
артериальной гиперкапнии в 60 мм рт. ст. вопрос
о необходимости немедленного перевода боль­
ного на ИВЛ не вызывает сомнений, а при хрони­
ческой легочной недостаточности с таким уров­
нем РаСОг больные живут долго, во всяком слу­
чае, до следующего обострения. Поэтому наря­
ду с определением степени нарушения легоч­
ного газообмена, которое соответствует обыч­
ному понятию дыхательной недостаточности,
следует использовать понятие «несостоятель­
ность дыхания».
Несостоятельность дыхания — это клиниче­
ская характеристика патологических явлений,
при которых физиологические механизмы до­
стижения конечного результата функции дыха­
ния (обеспечение тканевого обмена Qz) при дан­
ном уровне нарушений легочного газообмена
стали несостоятельными и прогрессируют в на­
правлении глубоких расстройств жизненно
важных функций (кровообращения, нервной
деятельности) с опасностью развития терми­
нального состояния. Темп развития этих явле­
ний и возможности восстановления физиоло­
гических механизмов достижения конечного
результата дыхания определяют прогноз лече­
ния данного больного.
Для понимания расстройств газообменной
функции легких необходимо иметь представ­
ление не только об участии в ее осуществлении
аппарата внешнего дыхания и аппарата регу­
ляции дыхания, но и о состоянии защитных
факторов легких.
ЗАЩИТНЫЕ ФАКТОРЫ ЛЕГКИХ
Различают неспецифические и специфиче­
ские (иммунные) защитные механизмы. К пер­
вым относят аэродинамическую фильтрацию,
кашель, движение слизи по воздухоносным
путям за счет физических законов или благо­
даря активности мерцательного реснитчатого
или цилиарного эпителия, растворение, деток­
сикацию и склеивание ингалированных частиц
постоянными фагоцитами и легочными альвео­
лярными макрофагами [Трещинский А. И., Троцевич В. А., 1979].
71
цией в первые часы после повреждения. А на
репарацию его требуется более 3 сут. Это дока­
зывает необходимость самого дифференциро­
ванного подхода в показаниях к эндобронхиаль­
ным манипуляциям («слепой» назотрахеальной
аспирации, промыванию бронхов, чрескожной
катетеризации трахеи, бронхоскопии и др.),
которые еще недавно широко пропагандирова­
лись для борьбы с гиперсекрецией и задержкой
мокроты. Большим вниманием должны пользо­
ваться методы, повышающие эффективность
естественных механизмов очищения бронхи­
ального дерева.
При уменьшении эффективности мукоцилиар­
ного эскалатора кашель становится основным
механизмом эвакуации бронхиального секре­
та. С физиологической точки зрения, кашель —
мощный рефлекторный выдох через частично
суженную голосовую щель. Он вызывается раз­
дражением окончаний блуждающего нерва в
крупных и средних бронхах скопившейся сли­
зью, патологическим материалом и ингалиро­
ванными частицами. Чем ближе к респираторной
зоне легкого, тем менее выражена чувствитель­
ность к раздражению. Кашель также может
быть произвольным или вызываться раздраже­
нием слизистой оболочки глотки, пищевода,
плевры, выстилки наружного слухового прохода.
Надавливание на передний край трапециевид­
ной мышцы, надбровье или введение пальца
за грудину (прием Cullen) также вызывают
кашель.
В силу наличия коллатеральной вентиляции
и действия поверхностно-активных веществ
при глубоком вдохе в первую фазу кашлевого
акта объем газа в респиронах возрастает даже
при обтурации бронхиол. Последующее воздей­
ствие спадающейся грудной клетки и быстрый
подъем диафрагмы настолько увеличивают дав­
ление в респиронах, что пробки из бронхиол
выдавливаются в воздухоносные пути большего
калибра, откуда они удаляются при последую­
щих кашлевых толчках. Возможность смеще­
ния пробок лежит в основе эффектов перкус­
сионного или вибрационного массажа, широко
применяемого в практике интенсивной тепапии
для предупреждения и лечения микроателектазирования [Шанин Ю. Н. и др.„ 1978; Голо­
горский В. А. и др., 1981].
Для выполнения совершенного кашля боль­
ной должен иметь возможность значительно
повышать объем легких, плотно закрывать голо­
совую щель и иметь достаточно мощные в функ­
циональном отношении мышцы выдоха при фик­
сированном каркасе грудной клетки. Поэтому
у больных с диффузным фиброзом легких или
ограничением вдоха другого генеза, с парали­
чом голосовых связок, при повреждении диа­
фрагмального нерва или костного остова груд­
Реснички не могут сокращаться без покры­
вающей их слизи. В то же время показано, что
мукоцилиарная активность зависит от ритмич­
ного перистальтического сокращения бронхов,
связанного с дыханием. Именно деятельность
цилиарного эпителия и одновременной пери­
стальтики бронхов образует защитный меха­
низм, который носит название мукоцилиарного
«эскалатора».
По современным представлениям, слизистый
компонент мукоцилиарного эскалатора пред­
ставляется не в виде непрерывного «слизистого
одеяла», а распределен дискретно в форме
микрочастиц, состоящих из двух слоев — внут­
реннего серозного, жидкого — золя и внешнего
(по отношению к стенке бронха), густого —
геля. Толщина золя может варьировать от мономолекулярного до такого, в который погру­
жена вся ресничка. Частицы геля транспорти­
руются на уровне кончиков ресничек.
Продуцентами слизи служат секреторный
эпителий слизистых и серозных желез крупных
бронхов и бокаловидные клетки — мелких. В со­
став слизи, кроме того, входит сурфактант, по­
ступающий из респираторной зоны, составные
части плазмы (альбумин, фибриноген) и секре­
тируемые местно белки: иммуноглобулины,
протеазы, а также муцин, который представлен
гликопротеидами с низким содержанием белка,
значительным количеством сиаловой кислоты,
и нуклеиновые кислоты, в частности ДНК. Вве­
дение атропина и дыхание сухими газовыми
смесями в течение длительного времени при­
водят к высушиванию слизистой оболочки даже
при отсутствии системной дегидратации и угне­
тают мукоцилиарную активность (Burton J.,
1962; Annis Р. et al., 1976). Высыхание слизи
ведет к разрушению эскалатора, а его «облом­
ки» (корки высохшей слизи) обтурируют дыха­
тельные пути.
Мукоцилиарный эскалатор значительно по­
вреждается при курении: табачный дым не толь­
ко парализует деятельность ресничек на не­
сколько часов после каждой выкуренной папи­
росы, но и нарушает архитектонику эпителиаль­
ной выстилки бронхов. Метаплазия цилиарного
эпителия в плоский под влиянием хроническо­
го курения заметно и на долгий срок нарушает
мукоцилиарную активность после полного пре­
кращения курения.
Незначительное механическое воздействие
(например, проведение по слизистой оболочке
хлопковой нитью) влечет за собой потерю рес­
ничек; действие эскалатора в этом месте пре­
рывается. Более значительное повреждение
(простое введение аспирационного катетера) со­
провождается отторжением всей толщи цилиар­
ного эпителия, нарушением архитектоники
всего многорядного слоя, обширной десквама-
72
ной клетки, с дряблой или поврежденной перед­
ней стенкой живота, некупированным болевым
синдромом эффективность кашлевого акта зна­
чительно снижена и нередко полностью отсут­
ствует. Принуждение таких больных к кашлю
или использование рефлекторных способов его
стимуляции совершенно бесполезны.
Механизмы очищения респираторной зоны
существенно отличаются от характерных для
воздухопроводящей зоны. Очищение легочных
структур, расположенных дистальнее терми­
нальных бронхиол, занимает от нескольких дней
до нескольких лет. Выделяют следующие воз­
можности очищения респираторной зоны.
Нерастворимые частицы могут выноситься
током альвеолярной жидкости из просвета респиронов к мерцательному эпителию терминаль­
ных бронхиол с дальнейшим транспортом на
мукоцилиарном эскалаторе. Они могут погло­
щаться в просвете респиронов альвеолярными
макрофагами, которые затем мигрируют через
интерстиций в специализированные лимфоэпи­
телиальные структуры, расположенные на уров­
не терминальных бронхиол на поверхности
мукоцилиарного эскалатора. В противополож­
ность этому хорошо растворимые вещества про­
никают в кровеносные сосуды; при этом кисло­
ты нейтрализуются в связи с основной реакцией
легочной паренхимы [Murrow Р., 1971]. Еще
один путь — адсорбция в интерстиций и пере­
нос к конечным лимфатическим сосудам, в по­
следующем — к прикорневым и паратрахеальным лимфатическим узлам. Некоторые из час­
тиц перемещаются по току интерстициальной
жидкости к плевре и задерживаются на долгий
срок в субплевральной периваскулярной и ин­
терстициальной ткани воздухопроводной зоны,
создавая особые формы легочной патологии
(гемосидероз, антракоз, асбестоз и т. д.). Нако­
нец, некоторые из частиц могут располагаться
внутри альвеолоцитов.
Этим не исчерпываются неспецифические
защитные факторы легких. Так, бронхиальная
слизь имеет защитное значение не только как
необходимое условие действия мукоцилиарного
эскалатора, но и в силу своей антибактериаль ­
ной и противовирусной активности. В значи­
тельной степени эта функция слизи определя­
ется компонентами ферментной защиты, к кото­
рым относят лизоцим, лактоферрин, интерфе­
рон, пирогены, неспецифические ингибиторы
протеиназ и др. Эти факторы секретируются
клетками слизистой оболочки бронхов, макро­
фагами, нейтрофилами и лимфоцитами.
Наличие воспалительного вала (шов бронха,
пролежень выстилки трахеи или бронха на ме­
сте стояния интубационной трубки) не только
прерывает движение слизи, но и создает усло­
вия для размножения в ней микроорганизмов.
73
Вместе с экссудатом, разрушенными клеточ­
ными элементами и активными полинуклеарами слизь приобретает новое качественное состоя­
ние — она становится мокротой. Значение
микробного компонента в такой трансформа­
ции существенно, и чаще всего оно определя­
ется дефицитом иммунных факторов защиты
легких.
К общим иммунным факторам защиты лег­
ких относят естественные антитела и компле­
мент, обычно содержащиеся в бронхиальной
слизи. Основная их роль — контроль за микро­
флорой дыхательных путей, ограничение ее
размножения и рассеивания из верхних в ниж­
ние отделы воздухопроводящей зоны. В норме
непатогенные микроорганизмы
(коменсалы,
сапрофиты) легко фагоцитируются и разруша­
ются макрофагами именно благодаря действию
естественных антител. Они же осуществляют
защиту от патогенных микроорганизмов путем
их прямого лизиса при участии системы компле­
мента. Антимикробное действие этих факторов:
фагоцитоз альвеолярных макрофагов и нейтро­
филов слизистой оболочки воздухоносных пу­
тей, наличие в слизи естественных антимикроб­
ных субстанций (лизоцим, лактоферрин и др.) —
усиливается наличием специфических иммунных
факторов защиты легких.
Местные иммунные механизмы легких и дыха­
тельных путей играют важную роль в защитном
ответе на антигенную информацию. С другой
стороны, повышенная местная чувствительность
к антигенам, поступающим с ингалированным
воздухом или по кровотоку, может привести
к патологическим процессам, нарушающим
функцию легочного газообмена (аллергиче­
ский альвеолит, бронхиальная астма и другие
формы бронхоспастического синдрома) [Кома­
ров Ф. И. и др., 1979]. Макрофаги принимают
участие лишь в подготовке антигенов к превра­
щению их в иммуногенную форму. Наиболее
существенна роль лимфоидной ткани, которая
размещена вдоль всей воздухопроводящей зо­
ны — от носоглотки до дыхательных брон­
хиол.
Местные иммунные ответы в легких отлича­
ются от системных, что определяется действием
как гуморальных, так и клеточных факторов.
Местный гуморальный иммунитет рассматри­
вают как доминирующий защитный механизм
против дыхательной пиогенной инфекции, в
то время как клеточный имеет большое зна­
чение в реакции организма против внутрилегочных (бактериальных и вирусных) возбудителей.
Полагают, что причиной нарушения специ­
фических защитных механизмов легких чаще
являются вторичные, т. е. приобретенные, имму­
нодефициты. К числу возможных этиологиче­
ских факторов приобретенной иммунной недо­
статочности относят хронические лимфопро­
лиферативные заболевания, злокачественные
опухоли, белковую недостаточность, лучевое
поражение, влияние некоторых лекарственных
препаратов.
В реакциях клеточного иммунитета в легких
имеют значение не только подвижные клетки.
Исследования J. Laweryns, J. Baert (1977) пока­
зали существенную роль фиксированных кле­
ток и эндотелия конечных лимфатических со­
судов. Именно клетки лимфатических сосудов,
а не эндотелий кровеносных капилляров, обла­
дают высокой эндоцитотической активностью,
включая абсорбцию, аккумуляцию и перевари­
вание абсорбированного материала, что считает­
ся их важным функциональным отличием. Это
позволило сравнивать эндотелиальные лимфа­
тические клетки легких с купферовскими клет­
ками печени и считать, что они относятся к РЭС
или к так называемой мононуклеарной фагоци­
тарной системе.
Специфические факторы защиты снижаются
(несмотря на свою многогранность) под дей­
ствием многих экзогенных и эндогенных фак­
торов — алкоголизма, кортикоидной терапии,
высокой концентрации кислорода, уремии, аци­
доза. Такие факторы, как стресс, падение пери­
ферического кровотока в легких при шоке, при­
менение вазопрессоров, общая анестезия, лекар­
ственная терапия, могут изменять и извращать
иммунные реакции у оперированных больных.
НЕГАЗООБМЕННЫЕ ФУНКЦИИ ЛЕГКИХ
ТЕПЛООБРАЗУЮЩАЯ
И ТЕПЛОРЕГУЛИРУЮЩАЯ
ФУНКЦИЯ ЛЕГКИХ
Теплопродукция в целостном организме свя­
зана с определенными биохимическими превра­
щениями энергетического материала в процес­
сах, сопряженных с дыханием. В обычных усло­
виях химическая теплопродукция зависит от
сокращения произвольных и непроизвольных
мышц (терморегуляционный тонус мышц, хо­
лодовая дрожь) и от так называемого несокра­
тительного термогенеза [Иванов К. П., 1965].
Считается, что для оптимальной теплопродук­
ции необходимо достаточное обеспечение кисло­
родом и энергетическими субстратами мышц.
Тем не менее свойство поддерживать постоян­
ство температуры внутренней среды у человека
сохраняется и при значительных нарушениях
этого обеспечения (при гипоксии, голодании).
Долгое время легкое и воздухоносные пути
рассматривали только как орган терморегуля­
ции, при котором отдача тепла происходит за
счет испарения с огромной поверхности раз­
дела с воздушной средой. Сейчас доказано, что
74
Рис. 40. Терморадиационный эффект легких при травмати­
ческом шоке.
К — контроль; Шв — у пострадавших с шоком, но выживших;
ШуМ — у пострадавших с шоком, но умерших. 1 — выделяемое
тепло, кал/мин; 2 — средняя температура выдыхаемого воздуха,
°C.
в отличие от других органов, теплопродукция
которых зависит от окисления углеводов и ами­
нокислот, легкие являются органом химической
теплопродукции, сопровождающей обменные
процессы в этом органе. Имея низкий основной
обмен, легкие могут повышать его в 8—9 раз
при развитии гипоксических состояний, задер­
живая и расщепляя жиры и окисляя НЭЖК.
Именно этой особенностью функционирова­
ния легких объясняется «гипоксический пара­
докс»— явление неизменного или повышенного
потребления организмом Ог в условиях гипоксии.
Участию легких в тепловыделении отводится
более скромная роль: на это приходится всего
15 % тепла, теряемого организмом. Однако
тепловой поток из легких концентрируется в
узком коридоре, образуемом дыхательными
путями. Это позволяет регистрировать его и
использовать с диагностической целью при кри­
тических состояниях. Ю. Н. Цыбин, В. Н. Лап­
шин (1982) показали возможность использо­
вания теплорадиационной возможности легких
для оценки тяжести травматического шока
и степени повреждения респираторной зоны
(рис. 40). Изменение функционирующей диф­
фузионной поверхности в связи с прямым по­
вреждением легких мало отразится на темпера­
туре крови в легочной артерии, но в силу изме­
нения теплообразующей функции легких суще­
ственно повлияет на количество выделяемого
при дыхании тепла, среднюю температуру выды­
хаемых газов. Также возрастает разница между
средней и максимальной температурой в газо­
вом потоке, поступающем из легких при вы­
дохе (рис. 41).
Рис. 41. Терморадиационный эффект легких у пострадав­
ших со скелетной травмой (СТ) и изолированной травмой
грудной клетки, осложненной шоком (ТТ).
Обозначения те же, что на рис. 40.
Из вышеизложенного вытекает ряд практи­
ческих выводов для ведения послеоперационно­
го периода после травм легкого и вмешательств
на легких. Больной с тяжелой гипоксией в ост­
ром периоде должен часто получать горячие
ингаляции или находиться в теплой влажной
атмосфере, чтобы уменьшить теплоотдачу с по­
верхности дыхательных путей. Перегрузки ра­
циона жиром или вливание жировых эмульсий
следует применять осторожно, чтобы не усили­
вать «гипоксический парадокс» и не повышать
кислородное голодание других тканей. Наоборот,
после купирования острой гипоксии необходи­
мы свежий воздух и увеличение жирового ком­
понента диеты.
ВОДНО-СОЛЕВОЙ ОБМЕН
И ЛЕГКИЕ
В обычных условиях путем перспирации теря­
ется 0,5—0,75 л воды за сутки. Пропотевая из
сосудов малого круга в респираторную зону и
из большого — в воздухопроводящую зону, это
количество жидкости удаляется из организма
в процессе вентиляции. Гипервентиляция, дыха­
ние ртом или через трахеостому могут увеличить
это количество жидкости в 5—6 раз.
Водно-солевой обмен в самих легких опре­
деляется движением жидкости через альвеоляр­
но-капиллярную мембрану и зависит как от осо­
бенностей тканевого дыхания в этом органе,
так и от состава циркулирующей жидкости. Он
определяется также особенностями паракапиллярной циркуляции в зоне легочных капилля­
ров. Установлено, что все биохимические систе­
мы, регулирующие это перемещение, метаболи­
чески зависимы и поэтому в ряде случаев из­
менение обмена воды в легочной перенхиме
может стать причиной отека легких, и, наоборот,
отек легких, нарушая продукцию поверхностно­
активных веществ, расстраивая тканевой обмен,
вторично углубляет задержку воды в легочной
паренхиме.
При нормальном состоянии легких вода, по­
павшая в респираторную зону, быстро, в тече­
ние минут, может всасываться в кровоток, чему
способствует различие между онкотическим
(25—30 мм рт. ст.) и гидростатическим (8—
10 мм рт. ст.) давлениями крови в легочных
капиллярах. Эта способность поглощать воду
исключает необходимость традиционных прие­
мов удаления воды из легких при утоплении и
является обоснованием введения медикамен­
тов в легкие при недоступности вен. Через лег­
кие можно вводить атропин, адреналин, инсу­
лин, лазикс и другие водорастворимые пре­
параты с помощью ингаляции мелкодисперсно­
го аэрозоля, несколько хуже — вливая раствор
в интубационную трубку или путем прокола
трахеи, что следует использовать и при прове­
дении реанимации [Цыбуляк Г. Н., 1979].
Легкие оказывают влияние на осмолярность
внутренней среды организма в связи со значи­
тельной осмоэкскрецией: в течение суток через
легкие удаляется 15—30 осмомолей углекислого
газа по сравнению с 0,5—1 осмомолем всех
солей, удаляемых почками. Не меньшее влияние
оказывают легкие на кислотно-основное состоя­
ние [Шанин Ю. Н., Костюченко А. Л., 1969],
с которым теснейшим образом связан транспорт
углекислого газа в организме.
Среди трех механизмов, стойко удерживаю­
щих активную реакцию крови на постоянном
уровне,— буферной емкости крови, экскретор­
ной функции почек и вентиляции легких,— по­
следний является наиболее мощным. Возмож­
но, и эта сторона деятельности организма спо­
собствует внутриорганной нормализации вод­
ного баланса.
В связи с легочным кровотоком и общим ба­
лансом воды и электролитов в организме в лег­
ких постоянно образуется так называемая внесосудистая вода, состоящая из межклеточной
жидкости и жидкостного слоя, выстилающего
альвеолы. Ее количество составляет не менее
60 % от массы легких [Зильбер А. П., 1977].
Как только изменяется легочный кровоток, из­
меняется и объем внесосудистой воды в легких.
Так, при постгеморрагической гипотензии, со­
провождающейся повышением легочно-сосуди­
стого сопротивления, этот показатель возраста­
ет до 88 % от массы органа, хотя общее коли­
чество воды в организме практически не изме­
няется.
75
Для нормализации содержания внесосудистой
жидкости определенное значение имеет лимфа­
тический дренаж легких, который в значитель­
ной степени регулирует объем межклеточной
жидкости, белковый и электролитный обмен в
этом органе.
В физиологических условиях фильтрация,
абсорбция и лимфатический дренаж уравно­
вешены, поддерживая достаточно стабильный
объем интерстициальной и внутриальвеолярной
жидкости. Нарушения этого равновесия при
трансфузионной микроэмболии приводят к за­
держке жидкости, ухудшая механические свой­
ства легкого, нарушая условия газообмена
и кислородного транспорта [Лыткин М. И.
и др., 1980].
пидным комплексом, способствующим превра­
щению протромбина в тромбин. Некоторые
авторы даже связывают большую частоту тром­
боэмболических осложнений при раке легких
именно с повышенной продукцией поражен­
ными легкими этого вещества. Легкие продуци­
руют и другие кофакторы свертывания (антигемофильный глобулин А, фактор VI).
В то же время этот орган богат и факторами
антисвертывающей системы, прежде всего гепа­
рином, который продуцируется тучноклеточ­
ным аппаратом респиронов. Гипоксия, ацидоз,
воспаление приводят к недостаточности про­
дукции эндогенного гепарина, усиливают гипер­
коагуляцию, адгезию и агрегацию форменных
элементов в зоне легочной микроциркуляции.
Отсюда понятна целесообразность применения
заместительной терапии экзогенным гепарином
при длительно не разрешающихся пневмониях,
прогрессирующем уплотнении легкого при шоке
и т. д.
В легких содержатся в большом количестве
и активаторы, превращающие тканевой и кро­
вяной плазминоген в плазмин. Тем самым лег­
кие и приобретают свойство воздействовать на
задержанные в них тромбы. Одновременно этот
механизм поддерживает фибринолитическую
активность всей циркулирующей крови: в кри­
тических ситуациях, протекающих с гипоксией,
на фоне несовершенного обезболивания [Пле­
шаков В. Т„ 1964; Соловьев Г. М. и др., 1970,
и др.] развивается фибринолизный криз. Нару­
шения внутрилегочных механизмов регуляции
свертывающей системы крови играют важную
роль в развитии тромбоэмболии и тромбоза вет­
вей легочной артерии, жировой эмболии лег­
ких, синдрома дыхательных расстройств при
травматическом или септическом шоке.
ФИЛЬТРАЦИОННАЯ
ФУНКЦИЯ ЛЕГКИХ
Легкие являются мощным фильтром, очи­
щающим смешанную венозную кровь от кон­
гломератов клеток, свертков фибрина, капель
жира, пузырьков воздуха и других эндогенных
и экзогенных субстратов. Расположение легких
между правой и левой половинами сердца и
прохождение через легкие практически всей
массы циркулирующей крови обеспечивают
очистку крови от механических примесей, пре­
дупреждая эмболизацию ими сосудов большого
круга.
Легочная сосудистая сеть стабилизирует уро­
вень лейкоцитов и тромбоцитов в крови, легко
иммобилизуя аллогенные кровяные клетки. От­
сюда сомнения относительно ценности приме­
нения лейкотромбовзвеси, приготовленной из
донорской крови.
Этот фильтр задерживает даже бактерии, раз­
мер которых отчетливо меньше сечения легоч­
ного капилляра. Такое свойство легочных капил­
ляров объясняется их способностью изменять
диаметр и форму сечения, возможностью уве­
личивать адгезивность эндотелиальной стенки,
наличием особых «шпор» в области бифурка­
ции микрососудов, позволяющих отклонять ток
крови и закрывать их просвет [Поликар А.,
Гали П., 1972].
Но легкие — не просто фильтр механической
очистки: задержанные органические субстан­
ции подвергаются в легких перевариванию.
ЛЕГКИЕ И БИОЛОГИЧЕСКИ
АКТИВНЫЕ ВЕЩЕСТВА
Пропуская через себя всю циркулирующую
кровь, легкие служат местом приложения дей­
ствия биологически активных веществ и участ­
вуют в их метаболизме [Cillis С., 1973]. Как
и в отношении регуляции свертывающей систе­
мы, легкие играют роль функционального фильт­
ра, регулируя содержание в крови гистамина,
серотонина, катехоламинов, кининов и проста­
гландинов. Многие стороны этого явления до
конца не раскрыты, но значение такой регуля­
ции для функционирования легких и всего орга­
низма несомненно.
Так, легкие синтезируют гистамин из гисти­
дина [Гончарова В. А., Сыромятникова Н. В.,
1978], но инактивируют лишь небольшое коли­
чество этого амина, поступившего с венозной
кровью. Не вызывает сомнения участие гиста­
РОЛЬ ЛЕГКИХ В РЕГУЛЯЦИИ
СВЕРТЫВАНИЯ И ФИБРИНОЛИЗА
КРОВИ
Легкие существенно влияют на свертывание
крови не только благодаря своему регулирующе­
му влиянию на концентрацию тромбоцитов.
Этот орган богат тромбопластином — фосфоли­
76
мина и других биологически активных полипеп­
тидов в механизмах и клинических проявлениях
отека легких, бронхиальной астмы [Зальбер А. П., 1977]. Гистамин влияет и на механику
дыхания: даже у здоровых людей он отчетливо
повышает неэластическое сопротивление лег­
ких, снижает объем форсированного выдоха
и жизненную емкость [Newhall J., Keiser S„
1973].
Легкие синтезируют и одновременно избира­
тельно извлекают из циркулирующей крови
серотонин, инактивируя, в отличие от гистамина,
95 % вещества, поступившего в малый круг кро­
вообращения. Скорость этой реакции зависит
от температуры тела, интенсивности окисли­
тельных реакций и гликолиза в легочной ткани:
инактивирование серотонина требует значитель­
ных затрат энергии [Gzuby L. er al., 1971; Stein­
berg R. et al., 1975].
Фенотиазины, опиаты, ингибиторы моноок­
сидаз и трициклические антидепрессанты тор­
мозят инактивацию серотонина, особенно на
фоне гиперкоагуляции, когда снижена концент­
рация его естественного антагониста — гепа­
рина. При тромбоэмболии происходит локаль­
ное освобождение серотонина из тромбоцитов,
особенно значительное при продолженном
тромбозе. Снижение метаболизма серотонина
в респираторной зоне на фоне ишемии ухудша­
ет течение патологического процесса вслед­
ствие усиления агрегации тромбоцитов, генера­
лизованного бронхиолоспазма, сосудистого
коллапса в большом круге кровообращения,
активной вазоконстрикции легочных артерий
и вен. Уже поэтому оправданно в таких ситуа­
циях срочное введение антагонистов серото­
нина и, прежде всего, гепарина.
Патология легких различного характера мо­
жет замедлять процессы инактивации серото­
нина и увеличивать выброс гистамина, что мо­
жет влиять на кровообращение в легком во
время операции [Гимельфарб Г. Н. и др., 1981].
Так, при хронических гнойных заболеваниях
легких (в отличие от опухолевых) отмечено
снижение инактивации серотонина. Поэтому
к концу операции у этих больных концентрация
полипептида в артериальной крови возрастает.
Обнаружена положительная корреляция между
средним давлением в легочной артерии и кон­
центрацией этого вазоактивного вещества в
крови.
Легкие могут как синтезировать катехол­
амины, так и регулировать их содержание в кро­
ви. В респираторной зоне легкого обнаружены
все основные компоненты биосинтеза этих гор­
монов и все необходимые ферменты [Гончаро­
ва В. А., Сыромятникова Н. В., 1969]. Оказа­
лось, что дофамин и адреналин свободно прохо­
дят через легочный сосудистый фильтр, а нор­
адреналин задерживается и довольно быстро
разрушается в легочной паренхиме. Легкие
извлекают за один кругооборот крови 20—25 %
норадреналина. Гипотермия, наркоз, искус­
ственное кровообращение, адреноблокаторы
снижают метаболическую активность легких
в отношении норадреналина, усиливают гипо­
ксическую легочную вазоконстрикцию. При
этом, чем глубже наркоз, тем больше норадре­
налина проходит через легкие. Системная адре­
ноблокада, как и регионарная симпатическая
блокада (перидуральная анестезия), увеличи­
вает альвеолярный шунт, снижая Рао [Соло­
вьев Г. М. и др., 1973].
Легкие играют существенную роль в обмене
кининов: они обладают высокой калликреиновой активностью и содержат в больших коли­
чествах как кининоген, так и ингибитор калликреина — трасилол, способный к образованию
и инактивации брадикинина. Выброс брадики­
нина происходит под влиянием различных пато­
логических состояний, включая отек легких,
анафилактический, геморрагический и септиче­
ский шок [Лыткин М. И. и др., 1981]. Паро­
ксизмальный выброс брадикинина наблюдается
при карциноидном синдроме, клинические про­
явления которого во многом определяются
уровнем концентрации брадикинина в крови
[Oates S. et al., 1974]. Кинины могут вызвать
выделение катехоламинов легкими, принимают
активное участие в реализации реакций, сопро­
вождающих тромбоэмболию. Они действуют
избирательно на легочный кровоток: в неболь­
шом количестве увеличивают давление в сосу­
дах (артериолах и венах) малого круга крово­
обращения, в большом — снижают его. Это
различие в действии зависит, по-видимому, от
того, что ферментная инактивация кининов
в легких определяется ангиотензин-конвертазой, которая принимает участие в образовании
другого вазоактивного полипептида — ангио­
тензина II из неактивного ангиотензина 1. Лег­
кие считаются единственным крупным орга­
ном, не инактивирующим ангиотензин II, поэто­
му загрузка ферментной системы избытком
кинина выключает синтез этого вазоактивного
вещества со снижением легочного сосудистого
давления.
В инактивации кининов, наряду с кининоинги­
бирующими ферментами, важную роль играют
поверхностно-активные вещества. Однако, если
в условиях здорового организма их количество
в гипофазе достаточно для инактивации поли­
пептидов, попавших в легкие с током крови,
то при септических процессах, когда уровень
кининов и протеолитических ферментов в веноз­
ной крови резко возрастает, сам сурфактант
начинает разрушаться, не успевая справляться
с избытком кининов [Ивашкевич Н. Г., Хим­
77
ка А. С., 1983]. Можно думать, что замедление
расправления легкого, оперированного до подав­
ления активности распространенного гнойного
процесса в нем, имеет тот же генез.
К негазообменным функциям легких следует
отнести синтез и инактивацию простагланди­
нов — жироподобных веществ, производных
пропионовой кислоты, являющихся по своей
структуре ненасыщенными жирными кисло­
тами.
Легкие играют исключительную роль в ме­
таболизме циркулирующих простагландинов.
Установлено, что до 85—90 % простагланди­
нов Е и F2onpH прохождении через малый круг
кровообращения исчезают из крови, тогда как
простагландины Ai и Аг остаются в артериаль­
ной крови в неизменной концентрации.
Существенна роль простагландинов в форми­
ровании газообменной функции легких в усло­
виях гипоксии, микроэмболии в системе легоч­
ной артерии при воспалительных процессах
в легких.
КЛИНИЧЕСКАЯ
ФИЗИОЛОГИЯ ПЛЕВРЫ
Плевре принадлежит важная роль в функцио­
нальной организации внешнего дыхания и нор­
мальном функционировании респираторной
зоны легких.
Плевре придается важное значение в осу­
ществлении всей биомеханики дыхательного
акта. Особенно четко это прослеживается при
патологических процессах, захватывающих
плевру.
Отрицательное давление, равномерно рас­
пределяющееся по всей свободной плевральной
щели во время вдоха, играет существенную роль
в присасывающем действии грудной клетки,
влияет на крово- и лимфоток в легких, так же
как и на деятельность сердечно-сосудистой
системы. Как только это давление исчезает
(например, вследствие скопления жидкости
или воздуха), нарушается не только биомеха­
ника дыхания, но и снижаются барьерные воз­
можности плевры.
Плевра обладает функцией гистогематического барьера, защищающего организм от ток­
сических веществ, образующихся при систем­
ных или местных нарушениях тканевого обме­
на. Париетальный и висцеральный листки плевры
объединены общностью барьерной функции,
которая неразрывно связана с циркуляцией
внутриплевральной жидкости. Оба плевраль­
ных листка осуществляют свою барьерную
функцию с помощью бесклеточных структур
(в том числе и эластических и коллагеновых
волокон), клеточных элементов мезотелия и
сосудистого эндотелия, а также мигрирующих
сюда (при воспалении и других патологиче­
ских состояниях) клеточных элементов, вы­
полняющих функцию защиты. К этим элемен­
там могут быть отнесены как ретикулиновые
клетки, так и образующиеся из них гистиоциты
с высокими адсорбционными фагоцитарными
и детоксикационными свойствами
[Билецкий В. К., 1966].
Хотя защитное действие фиксированных
и подвижных клеток плевры по отношению
к токсинам и микроорганизмам представляется
довольно четко, роль бесклеточного вещества
плевры также несомненна. Так, ретикулярные
волокна серозных оболочек в результате поверх­
ностного натяжения задерживают в своей мел­
коячеистой сети тканевую жидкость при ее из­
быточном образовании. Базальная мембрана
мезотелия с ее аморфным межуточным веще­
ством может выполнять роль мощного фильтра,
в котором задерживаются и накапливаются
продукты обмена. Субмезотелиальный слой
ретикулярной ткани выполняет реактивную и
защитную функции в случаях десквамации
и декомплексации мезотелия и при нарастании
воспалительного процесса на плевре. Именно
этот слой выполняет пластическую роль
в процессах, изолирующих инфекционный очаг
и ограничивающих его распространение по
плевральной щели. Соединительнотканные
структуры плевры и мезотелий играют решаю­
щую роль в защитных иммунологических реак­
циях.
При просачивании через них экссудата они
задерживают и обезвреживают токсические про­
дукты и микробы, препятствуя их поступлению
в общую циркуляцию.
Париетальная плевра в обычных условиях
представляет собой редуцированный барьер
в силу наличия в ней «люков», что облегчает
всасывание из плевральной щели. Но как толь­
ко возникает воспаление и на поверхности
плевры откладываются пласты фибрина, люки
закрываются, и барьерная функция ее возра­
стает [Теппер П. А., 1960] вследствие увеличе­
ния времени воздействия факторов обезвре­
живания инфекта и токсинов, а также умень­
шения резорбции микробов и продуктов их
жизнедеятельности. Наоборот, быстрое восста­
новление всасывательной способности парие­
тальной плевры уменьшает ее барьерные свой­
ства, что проявляется повышением температу­
ры тела и другими признаками интоксикации.
Одномоментное поступление значительного
количества бактериальных токсинов и продуктов
тканевого распада может резко усилить инток­
сикацию, вызвать различные ответные реакции
организма вплоть до развития септического
шока.
78
Барьерная функция плевры неразрывно свя­
зана с циркуляцией внутриплевральной жид­
кости.
Висцеральная плевра является продуцентом
плевральной жидкости, которая поступает не­
прерывно из зоны микрососудов. Передвиже­
ние тканевой жидкости из глубины на поверх­
ность легкого постоянно; оно регулируется ды­
хательными движениями грудной клетки и лег­
кого. При физическом напряжении и углубле­
нии дыхания количество транссудата увеличи­
вается. Одновременно возрастает и его всасы­
вание париетальной плеврой. При вдохе и рас­
тяжении грудной клетки компактно прикре­
пленные к ребрам участки плевры остаются
неизмененными, плевра межреберий, так же как
и диафрагмальная плевра, на которой имеются
«люки», широко растягивается, создавая «микровакуумы» в этих зонах. Сюда устремляются
потоки жидкости из плевральной полости,
заполняя камеры «люков». При выдохе и спаде­
нии растянутой на вдохе плевры эти камеры
сдавливаются, а скопившаяся в них жидкость
скользящим движением плевры вдавливается
в «люки». Степень присасывания и интенсив­
ность транссудации больше в более низких
отделах плевры. При наличии только микро­
скопического слоя жидкости, обеспечиваю­
щего тесный контакт париетального и висце­
рального листков плевры, последние соединя­
ются в единый функциональный комплекс —
«грудная клетка — париетальная плевра —
висцеральная плевра — легкое». Нарушение
этого функционального единства в силу усиле­
ния транссудации жидкости легкими или за­
медления ее всасывания вследствие блокады
«люков», попадания воздуха, крови, хилезной
жидкости разъединяет оба листка, изменяет
градиенты давления в полости плевры и может
способствовать избыточному накоплению жид­
кости.
Введенные в плевральную полость бактерии
в незначительной степени проникают в легоч­
ную и медиастинальную плевру, а удаляются
из плевральной щели через всасывающие «лю­
ки» реберной плевры. Закрытие «люков» фибри­
ном и размножение бактерий в полости плевры
резко усиливают пропотевание жидкости в свя­
зи с действием бактериальных токсинов на со­
стояние бесклеточного вещества обоих плев­
ральных листков и на проницаемость стенки
микрососудов. Мигрирующие в полость клетки
крови, прежде всего нейтрофилы и лимфоциты,
превращают транссудат в экссудат, причем
париетальная плевра (как и висцеральная) в силу
фиксации бактерий в «люках» и фиброэласти­
ческом слое становится источником поступле­
ния инфекта в плевральную полость, поддер­
живает воспалительный процесс. Это считается
обоснованием необходимости ранней плеврэктомии у больных с гнойным плевритом
[Горшков Ю. И. и др., 1981].
Но даже при самых глубоких расстройствах
циркуляции плевральной жидкости (при эмпие­
ме после пневмонэктомии) плевральная полость
сохраняет определенные возможности саморе­
гуляции состава этой жидкости. Попытки навя­
зать этот состав, смоделировать по своему жела­
нию после самого тщательного промывания
и заполнения искусственным коллоидным кро­
везаменителем оказались безуспешными. На
другой день после такой процедуры солевой,
белковый и углеводный и даже клеточный со­
став экссудата близко соответствовал тому,
который был установлен до промывания.
Проблема воздействия на всасывательную
способность плевры смыкается еще с одной,
важной для практики хирургии легких и плевры
функциональной особенностью этой структуры.
Это способность серозных оболочек грудной
клетки сообщать крови, излившейся в полость
плевры, сохранять жидкое состояние за счет
разрушения образующегося в процессе поступ­
ления крови фибрина. Такая особенность
серозных оболочек, по мнению некоторых хи­
рургов-пульмонологов [Вагнер Е. А., Тавровский В. М., 1977], должна быть соотнесена
прежде всего с проблемой интраоперационных
и послеоперационных внутриплевральных кро­
вотечений.
Характер изменений крови, изливающейся
в закрытую плевральную щель в связи с травмой
или операцией (после ее завершения), опреде­
ляется прежде всего интенсивностью внутри­
плеврального кровотечения. Для эффективно­
сти дефибринирования, при котором излив­
шаяся в плевру кровь становится жидкой, име­
ют значение несколько факторов: темп поступ­
ления крови, степень повреждения грудной
клетки и соответственно тканей висцеральной
и париетальной плевры в процессе выделения
легкого, глубина дыхательных движений. Не­
сомненное значение имеют и коагуляционная
активность циркулирующей крови
[Чепчерук Г. С., 1976] и тканевой тромбопластин,
поступающий из раневых полей, которые обра­
зуются при разделении плоскостных сраще­
ний либо при экстраплевральном выделении
легкого.
В таких случаях восстановление плевраль­
ной щели и удаление остатка пропотевающей
крови в процессе расправления легкого приво­
дят в плоскостному выпадению фибрина, кото­
рый не только оказывает гемостатическое дей­
ствие, покрывая тонким слоем париетальную
плевру и легкое, но и способствует адгезии,
а в последующем и сращению обоих плевраль­
ных листков с облитерацией плевральной щели.
79
Глава «.J ОБЩИЕ ПРИНЦИПЫ
ОБСЛЕДОВАНИЯ БОЛЬНЫХ
ЗАБОЛЕВАНИЯМИ
ЛЕГКИХ И ПЛЕВРЫ
Обследование больных заболеваниями легких
и плевры в хирургической клинике решает две
основные задачи: 1) диагностика основного
заболевания и оценка связанных с ним сопут­
ствующих патологических изменений; 2) выясне­
ние состояния основных систем жизнеобеспе­
чения, необходимое для оценки резервных воз­
можностей организма больного и степени его
функциональной операбельности.
ДИАГНОСТИКА
ОСНОВНОГО ЗАБОЛЕВАНИЯ
ОСНОВНЫЕ МЕТОДЫ
ДИАГНОСТИКИ ЗАБОЛЕВАНИЯ
Несмотря на то, что возможности оказания
помощи больным заболеваниями легких во мно­
гом расширились с внедрением в клиническую
практику специальных приемов, появление ко­
торых обусловлено последними достижениями
в области физики, электроники, оптики и других
областях знаний, роль и место субъективных
и объективных общеврачебных методов обсле­
дования сохранили свое значение до настоящего
времени.
Расспрос больного, изучение его жалоб, осо­
бенностей возникновения и развития заболева­
ния, сведений о перенесенных болезнях, образе
жизни и работе, вредных привычках часто
являются отправным пунктом для построения
плана дальнейшего специального, более углуб­
ленного и направленного обследования, опреде­
ления последовательности применения как про­
стых (физикальных), так и более сложных
(инструментальных) методов диагностики.
Наиболее доступные методы исследования —
осмотр, пальпация, перкуссия, аускультация —
нередко позволяют отметить совокупность приз­
наков или отдельные симптомы, с большой до­
стоверностью характеризующие развитие изме­
нений, которые в сочетании с данными анам­
неза дают возможность правильно решить
вопрос не только о диагнозе, но зачастую — и ле­
чебной тактике. Так, появление конгломератов
надключичных лимфатических узлов, развитие
на передней поверхности туловища сети расши­
ренных подкожных вен, увеличение окружно­
сти шеи, одутловатость лица, отмеченные при
осмотре и физикальном обследовании больного
заболеванием легких, могут с большой долей
вероятности свидетельствовать о распространен­
ном бластоматозном процессе с вовлечением
медиастинальных и надключичных лимфатиче­
ских коллекторов, крупных кровеносных сосудов
средостения. Полученные сведения позволяют не
делать более сложные, часто сопряженные
с определенным риском инструментальные ис­
следования.
Нарастающая одышка, расстройства сердеч­
ной деятельности, появление подкожной эмфи­
земы, развившиеся в течение короткого време­
ни вслед за болевыми ощущениями в груди,
сочетающиеся с отсутствием или резким ослаб­
лением дыхательных шумов над одним легким,
коробочный звук при перкуссии в этой области
груди дают возможность распознать спон­
танный напряженный пневмоторакс.
Среди основных специальных методов обсле­
дования больных заболеваниями легких веду­
щее место принадлежит рентгенологическому
исследованию.
Р ЕНТГЕНОЛОГИ Ч ЕСКОЕ
ИССЛЕДОВАНИЕ
Обязательным условием рентгенологического
исследования больных заболеваниями легких
следует считать рентгеноскопию. Применение
электронно-оптических преобразователей и
использование реитгенотелевидения значитель­
но уменьшили лучевую нагрузку на обследуе­
мого пациента и медицинский персонал, по срав­
нению с аппаратами обычного типа, увеличили
яркость и разрешаемость рентгеновского изо­
бражения.
Появилась возможность документировать ре­
зультаты исследования на кино- или магнит­
ной ленте.
80
Рис. 42. Электрорентгенограмма грудной клетки. Норма.
Рис. 43. Электрорентгенограмма грудной клетки. Слева
в базальных отделах — остаточная полость.
В первую очередь рентгенологическая диагно­
стика включает ориентировочный осмотр легоч­
ных полей, при этом определяются сторона и
объем поражения. Обращается внимание на
подвижность купола диафрагмы, состояние ре­
берно-диафрагмальных синусов, прозрачность
легочных полей, структурность корней легких,
размеры и конфигурацию срединной тени, фор­
мируемой органами средостения.
Последующее рентгенографическое обсле­
дование должно углублять и расширять пред­
ставления о характере изменений в легких и
грудной полости. Эти исследования проводят
в прямой (переднезадней) и боковой проекциях,
дополняя их при необходимости снимками
в косых проекциях и прицельными рентгено­
граммами. Важным достоинством рентгено­
графии являются объективность и достовер­
ность полученных результатов, возможность
сопоставления с данными ранее проведенных
рентгенографических обследований, т. е. воз­
можность динамического наблюдения. По­
следнее нередко является одним из важнейших
факторов для установления правильного диаг­
ноза.
Рентгенографическое обследование в двух
проекциях позволяет с наибольшей точностью
определить локализацию и распространенность
поражения легких, изменения в средостении,
состояние междолевых щелей. Оценка и сопо­
ставление степени прозрачности участков легко­
го в различных его отделах позволяют устано­
вить возможные отклонения от нормы.
Рентгенограммы, выполненные с прямым уве­
личением изображения, позволяют выявить мел­
кие и мельчайшие очаговые тени, что особенно
ценно при проведении дифференциального диаг­
ноза между туберкулезом легких, саркоидозом,
пневмокониозом и другими заболеваниями,
дающими исходные рентгенологические из­
менения.
Для улучшения визуализации трахеоброн­
хиального дерева и уплотненных лимфатиче­
ских узлов средостения используются так на­
зываемые переэкспонированные снимки грудной
полости. На них особенно четко определяются
элементы корня легкого на фоне как бы выве­
денного на «второй план» легочного рисунка.
В последние годы для получения первой, наи­
более общей, информации о характере рентгено­
логических изменений в легких и грудной поло­
сти (наряду с флюорографией) стала использо­
ваться электрорентгенография.
Важнейшим
достоинством метода электрорентгенографии
являются его высокая экономическая эффек­
тивность, исключение расходов на оснащение
специальных фотолабораторий и реактивов,
необходимых для рентгенографии. Процесс
электрорентгенографии не зависит от водоснаб­
жения, получение крупноформатных снимков
происходит на свету. Изображение воспроиз­
водится на селеновой пластине и затем перено­
сится на бумагу (рис. 42, 43).
Электрорентгенография имеет неоспоримые
преимущества при проведении неотложной рент­
генологической диагностики.
Томографическое (послойное) исследование
органов грудной полости дает возможность
выделить участки легкого с предполагаемыми
зонами поражения в любой заранее рассчи-
6 Зак. 0517
81
Рис. 44. Компьютерная томография органов грудной клетки.
Норма.
Рис. 45. Компьютерная томография органов грудной клетки.
Эмфизема легких.
тайной глубине. Томографическое исследование
органов грудной полости также выполняется
в прямой и боковой проекциях. Количество
томограмм, выполняемых при различных пато­
логических изменениях в органах грудной поло­
сти, зависит от поставленных задач и определя­
ется для каждого больного индивидуально. При
необходимости томограммы, сделанные в пря­
мых проекциях, могут быть дополнены томо­
граммами в косых проекциях. Оптимальными
срезами считаются срезы в промежутке от 8 до
12 см, отступя от остистых отростков позвон­
ков.
Выполнение томографического исследования
позволяет уточнить данные, полученные при
обзорной рентгенографии: определяются точ­
ная локализация и характер патологического
процесса в легком, его распространенность, отно­
шение к сосудам и бронхам легкого, плевре
и органам средостения. С помощью томогра­
фии удается оценить проходимость трахеи и
бронхов, выявить в просвете дыхательных путей
новообразования, инородное тело. Томография
служит важным вспомогательным приемом для
изучения характера изменений в лимфатических
узлах средостения, в костных образованиях,
формирующих каркас грудной полости.
Возможности рентгенологической диагно­
стики заметно расширились за счет становле­
ния и клинического использования компьютер­
ной рентгенотомографии. По сравнению с обыч­
ной рентгенографией компьютерная рентгено­
графия имеет в десятки раз большую разре­
шающую способность и позволяет различать
ткани с разностью по плотности до 0,5 %. Это
дает возможность четко определять границу
между нормальной и патологически изменен­
ной легочной тканью. На компьютерных томо­
граммах органов грудной полости удается не
только локализовать патологический очаг, но
и определить его размеры, оценить плотность
и однородность, соотношение с соседними ана­
томическими образованиями и органами [Пе­
рельман М. И. и др., 1981].
Компьютерная томография дает возмож­
ность получить наиболее полную рентгеноло­
гическую информацию об опухолях и кистах
средостения, сосудистых изменениях в легких,
аневризмах, о состоянии трахеобронхиального
дерева, характере и структуре «шаровидных
образований в легких», патологических изме­
нениях в плевре, грудной стенке, особенно при
ее злокачественных поражениях (рис. 44—46).
БРОНХОСКОПИЯ
Эндоскопическому обследованию трахеоброн­
хиального дерева в настоящее время придает­
ся очень большое значение, так как с его помо­
щью у большинства больных получают досто­
верную информацию о характере изменений в
трахеобронхиальном дереве, что особенно важ­
но в диагностике опухолевых заболеваний тра­
хеи и бронхов.
Диагностические возможности бронхоско­
пии расширялись по мере совершенствования
и создания новых моделей бронхоскопов. Брон­
хоскопы конструкции Брюнингса, Мезрина по­
степенно уступили место более удобной и безо­
пасной модели бронхоскопа системы Фриделя.
82
Рис. 46. Рак верхней доли левого легкого.
а — прямая рентгенограмма; б — боковая рентгенограмма; в —
компьютерная томограмма.
Последний обеспечивает адекватную вентиля­
цию легких во время бронхоскопии. Бронхо­
скопы этой конструкции (так называемые «ды­
хательные») до настоящего времени широко
используются в бронхологической, пульмоно­
логической и хирургической практике.
Применение оптических приставок в сочета­
нии с надежной, устойчивой вентиляцией лег­
ких, снабжение дыхательных бронхоскопов
источниками «холодного» света во многом опре­
делили широкое применение жестких моделей
бронхоскопов. Несомненным достоинством
дыхательных бронхоскопов является возмож­
ность выполнения с их помощью не только
6*
диагностических, но и некоторых лечебных
манипуляций на бронхах (удаление инородных
тел и небольших доброкачественных опухолей
при помощи набора щипцов, обработка слизи­
стой оболочки лекарственными препаратами,
в том числе лечение бронхиальных свищей).
Дыхательные бронхоскопы жесткой конструк­
ции позволяют выполнить длинной иглой пунк­
ционную трансбронхиальную биопсию бифур­
кационных и некоторых групп внутрилегочных
лимфатических узлов. В последние годы с по­
мощью дыхательных бронхоскопов выполняют
лечебные окклюзии бронхиального дерева при
гнойно-деструктивных поражениях легких,
83
пневмотораксе, а также осуществляют дрени­
рование бронхов. Есть все основания полагать,
что применение дыхательных бронхоскопов
в пульмонологической практике будет необхо­
димо на протяжении еще длительного периода
времени.
Вместе с тем диагностические возможности
жестких моделей бронхоскопов ограничива­
ются пределами главных, долевых и начальны­
ми отделами сегментарных бронхов, т. е. цент­
рально расположенными отделами дыхательных
путей. Это обусловлено жесткостью конструк­
ции и относительно крупными их размерами.
Оптические приставки позволяют только осмот­
реть начальные отделы сегментарных бронхов
и исключают возможность выполнения биоп­
сии. Кроме того, повышенная травматичность
исследования трахеобронхиального дерева
с помощью жестких моделей бронхоскопов
вынуждает прибегать при их применении к об­
щему обезболиванию.
Дальнейшее развитие возможностей брон­
хоскопической диагностики появилось в связи
с созданием и использованием волоконно-опти­
ческих эндоскопов — фибробронхоскопов.
К числу наиболее важных достоинств фибро­
бронхоскопов относятся высокая эластичность
прибора, небольшие размеры диаметра диагно­
стического тубуса (до 6 мм), надежная система
мощного потока «холодного света». Диагности­
ческий канал фибробронхоскопа и набор био­
псийных щипчиков и скарификаторов позволяют
получать материал для морфологического ис­
следования не только из отделов трахеоброн­
хиального дерева, доступных визуальному конт­
ролю, но и из более дистальных. С помощью
волоконно-оптических моделей фиброброн­
хоскопа стали возможны детальный осмотр
бронхиального дерева и получение материала
для морфологического изучения вплоть до сег­
ментарных, субсегментарных, а для отдельных
долей (нижней, средней, части сегментов верх­
них долей) — и суб-субсегментарных бронхов.
Практически важным является то положение,
что эффект оптического увеличения при осмот­
ре через фибробронхоскоп требует специаль­
ного навыка при выполнении диагностических
исследований. Достоверность визуальной диа­
гностики несколько снижается по мере продви­
жения тубуса фибробронхоскопа к зонам суб­
сегментарного деления бронхиального дерева.
Диагностическая ценность фибробронхос ко­
пии заметно повышается при дополнении ви­
зуального исследования взятием материала для
морфологического (гистологического и цито­
логического) изучения: щипцовой и скарифи­
кационной биопсией, направленной аспирацией
промывных вод из участков предполагаемого
поражения легкого.
При выполнении этих условий, как показали
исследования, проведенные в клинике госпиталь­
ной хирургии [Шариф М. С., 1980], точность
диагностики с помощью фиброгастроскопии
при раке легкого достигает 90—95 %.
Конструкция современных волоконно-опти­
ческих бронхоскопов позволяет широко прово­
дить обследование трахеобронхиального дерева
с использованием местного обезболивания. Это
во многом расширяет диапазон их применения
в поликлинической практике, в специально при­
способленных бронхологических кабинетах.
Проведению бронхологических обследований
на амбулаторном уровне способствует также
появление новых терминальных анестетиков,
обладающих широким диапазоном терапевти­
ческого действия и невысокой токсичностью
(лидокаин, тримекаин). Они пришли на смену
ранее использовавшимся для этих целей пре­
паратам типа дикаина, нередко вызывавшим
у обследуемых тяжелые общие расстройства.
Для местного обезболивания при фибробронхоскопии в амбулаторной практике применя­
ется следующая методика. За 10—15 мин до
начала обезболивания больным вводят 1 мл
2 % раствора пантопона и 1 мл 0,1 % раствора
атропина. Затем с помощью пипетки в носовые
ходы больного вводят 2,5 % раствор тримекаина по 10—12 капель с каждой стороны. Уже
спустя 2—3 мин наступает обезболивающий
эффект. В течение этого времени оценивают
состояние больного — выявляют нежелатель­
ные общие реакции как проявление индивиду­
альной непереносимости тримекаина. Опыт
госпитальной хирургической клиники в этом
направлении, превышающий более 2500 иссле­
дований, показал безопасность метода: ни в од­
ном из наблюдений не было отмечено нежела­
тельных расстройств, обусловленных примене­
нием тримекаина, потребовавших специального
лечения или прекращения процедуры.
После анестезии слизистой оболочки носо­
вых ходов с помощью трансназально введенного
резинового катетера достигают надсвязочного
пространства гортани и орошают голосовые
связки 2—3 мл раствора тримекаина. Затем
проводят катетер в трахею и с помощью шпри­
ца вводят еще 10—12 мл раствора, достигая
анестезии слизистой оболочки дыхательных
путей. Кашель, закономерно возникающий в от­
вет на проведение конца катетера в подскла­
дочное пространство, прекращается в течение
20—30 с. С потоком воздуха на вдохе раствор
тримекаина достигает уровня долевых и сегмен­
тарных бронхов. Наступающая вслед за этим
местная анестезия является вполне достаточ­
ной для проведения фиброброихоскопии. Об­
щее количество 2,5 % раствора тримекаина,
расходуемого для выполнения обезболивания,
84
Во-первых, в процессе бронхологического
обследования под наркозом, как и в условиях
местного обезболивания, должна сохраняться
полная возможность использования всех пре­
имуществ и достоинств фибробронхоскопа,
предусмотренных его конструкцией.
Во-вторых, при проведении наркоза с мио­
релаксантами искусственная вентиляция легких
должна осуществляться непрерывно, быть
эффективной и исключать возможность раз­
вития гипоксических расстройств (фибробронхоскоп в конструктивном отношении не рассчи­
тан на обеспечение вентиляции легких).
Указанным требованиям отвечает проведе­
ние искусственной вентиляции легких под нар­
козом с миорелаксантами инжекционным мето­
дом, принцип которого разработал R. Sanders
(1967).
В сравнении с другими способами искусствен­
ной вентиляции инжекционный метод имеет то
преимущество, что не требуется герметизации
системы аппарат — легкие. Напротив, свобод­
ное сообщение просвета дыхательных путей
через инжекционное устройство с атмосферой
является одним из непременных условий про­
ведения эффективной инжекционной вентиля­
ции легких в состоянии миорелаксации. Для
проведения инжекционной искусственной вен­
тиляции легких в процессе выполнения фибробронхоскопии наиболее удобно использовать
специальную приставку-инжектор к эндотрахеальной трубке, разработанную в госпитальной
хирургической клинике. Открытый доступ в
просвет дыхательных путей позволяет, не нару­
шая ритма и не снижая эффективности вен­
тиляции легких, вводить в трахеобронхиальное
дерево тубус фибробронхоскопа.
Выполнять фибробронхоскопию под нарко­
зом наиболее удобно в специально оборудован­
ном бронхологическом кабинете на бронхоско­
пическом столе конструкции Г. К. Орджоникид­
зе (1965). Канюлируя локтевую вену, вводят
0,5 мг атропина и 0,5 г глюконата кальция.
Через 3—5 мин после инсуффляции кислорода
масочным способом внутривенно медленно вво­
дят 2 % раствор тиопентал-натрия или гексенала (в среднем 0,4 г) до исчезновения рого­
вичного рефлекса. Затем внутривенно вводится
20 мг 2 % раствора диплацина и в последую­
щем — деполяризующие миорелаксанты в
дозе 0,75 мг/кг. Необходимость дополнитель­
ного введения раствора тиопентал-натрия или
гексенала и миорелаксантов диктуется длитель­
ностью исследования.
Интубацию трахеи при фибробронхоскопии
под наркозом выполняют эндотрахеальной
трубкой без надувной манжеты, чтобы исклю­
чить возможность повреждения легких кисло­
родом под давлением. К трубке присоединяют
составляет обычно 13—15 мл. Продолжитель­
ность местной анестезии при этом обеспечива­
ется в течение 15—20 мин, что вполне достаточно
для обследования трахеобронхиального дерева.
Перспективным для применения в амбулатор­
ных условиях является местное обезболива­
ние ингаляцией аэрозоля 5 % раствора тримекаина. Такое обезболивание в еще меньшей
степени причиняет неудобства больным. Ингаля­
ционную аэрозольную анестезию удобно вы­
полнять при помощи передвижного ультра­
звукового аэрозольного ингалятора, который
обеспечивает создание аэрозольного потока
раствора. После анестезии носовых ходов раст­
вор тримекаина через сменный загубник или
маску глубоко вдыхается в течение 9—10 мин
и распределяется на поверхности слизистых
оболочек трахеи и бронхов. Как правило, к мо­
менту завершения обезболивания появляются
чувство «неловкости при глотании» и своеоб­
разное ощущение «облегчения глубины вдоха».
Несмотря на достоинства фибробронхоско­
пии под местным обезболиванием, полностью
отказаться от применения наркоза при этом
исследовании не представляется возможным.
У многих больных только под наркозом, в усло­
виях полной релаксации, обеспечивается доступ­
ность визуальной диагностики изменений в тра­
хеобронхиальном дереве. К числу таких боль­
ных относятся лица с неустойчивой, эмоцио­
нально-лабильной психикой, дети, а также боль­
ные с признаками аллергизации к препаратам,
используемым для местного обезболивания.
Кроме того, бронхологическое обследование
целесообразно выполнять под наркозом в тех
случаях, когда диагностика затруднительна:
обследование продолжается длительное время
или требуется совместный осмотр и обсужде­
ние выявленных изменений несколькими спе­
циалистами. Считается оправданным выполне­
ние бронхоскопии под наркозом у медицинских
работников, особенно если имеется подозре­
ние на опухолевый процесс.
При разработке методов фибробронхоскопии под наркозом в клинике в полной мере был
обобщен и использован значительный (более
10 000 исследований) опыт проведения общего
обезболивания при обследованиях, выполнен­
ных с помощью дыхательных моделей жест­
ких бронхоскопов. Некоторые изменения в эту
методику были внесены с учетом конструктив­
ных особенностей и возможностей волоконнооптических эндоскопов, которые по замыслу их
создателей были предназначены для обследо­
вания только под местным обезболиванием.
Поэтому появилась необходимость в разра­
ботке приемов для проведения обследований
фибробронхоскопом под наркозом с учетом
следующих двух основных положений.
85
приставку-инжектор. Подавая кислород пре­
рывисто в инжекционное устройство с частотой
18—20 раз в 1 мин, осуществляют искусствен­
ную вентиляцию легких. На вдохе кислород
под давлением проходит по инжекционной си­
стеме, засасывая воздух через открытую часть
приставки (эффект Вентури), и расправляет
легкие. Когда воздушно-кислородная смесь
перестает поступать, происходит пассивный
выдох.
Через открытый конец приставки-инжектора
вводят тубус фибробронхоскопа, осуществля­
ют эндоскопическое исследование с фотографи­
рованием, биопсию, скарификацию слизистой
оболочки, аспирацию патологического содер­
жимого трахеобронхиального дерева, введение
лекарственных препаратов. При этом, не нару­
шая эффективности инжекционной искусствен­
ной вентиляции легких, имеется возможность
неоднократно вводить и извлекать фибробронхоскоп, если в этом возникает необходимость
в процессе исследования.
После завершения бронхологического обсле­
дования фибробронхоскоп извлекают, а искус­
ственную вентиляцию инжекционным способом
продолжают по вспомогательному типу — до
восстановления адекватного самостоятельного
дыхания. Показанием к экстубации, помимо
эффективного самостоятельного дыхания,
является способность больного поднимать голову
и удерживать ее в этом положении. Минимальное
время, необходимое для выполнения фибробронхоскопии под наркозом, составляет в среднем
10—15 мин. После экстубации под наблюдением
врача-анестезиолога больной самостоятельно
переходит для отдыха на кушетку, находящуюся
в эндоскопическом кабинете. Через 20—30 мин
после завершения обследования всем больным
проводят парокислородные ингаляции с лекар­
ственными травами (ромашкой, мятой, чабре­
цом, листом эвкалипта) или медикаментозными
препаратами (ароматическими маслами, анти­
биотиками, бронхорасширяющими, мокротораз­
жижающими и другими средствами). Спустя
10—15 мин после контрольной оценки состояния
больного ему разрешается покинуть бронхо­
скопический кабинет. При такой организации
выполнение фибробронхоскопии под наркозом
с миорелаксантами и инжекционной искусствен­
ной вентиляцией легких является практически
безопасным исследованием и может выполнять­
ся в амбулаторных условиях.
Распознавание изменений в трахеобронхи­
альном дереве, определение и оценка признаков
развития заболевания представляют весьма
ответственную задачу и требуют применения
специальных методических приемов. Это тем
более важно, что информация, получаемая в
процессе осмотра трахеобронхиального дерева,
во многом определяет весь ход последующего
бронхологического обследования, а иногда —
и лечебную тактику. Поэтому при осмотре
через фибробронхоскоп следует придерживаться
единой системы, предусматривающей получе­
ние наиболее полных данных о состоянии и из­
менениях в трахеобронхиальном дереве.
В обязательном порядке оценивается состоя­
ние всех доступных осмотру отделов трахеоброн­
хиального дерева. Особое внимание уделяется
области тех изменений, которые отмечены при
рентгенологическом обследовании.
После проведения тубуса фибробронхоскопа
в гортань тщательно осматривают голосовые
связки. При этом оценивают характер и сте­
пень их подвижности: ограничение подвижно­
сти (парез) голосовой складки может свиде­
тельствовать о вовлечении в патологический про­
цесс возвратной ветви блуждающего нерва.
В трахее детально осматривают ее стенки
(передняя, задняя, боковые) на всем протяже­
нии — от подскладочного пространства до
бифуркации — места ее деления на правый и
левый главные бронхи.
Информация, получаемая на этом этапе брон­
хоскопии, может быть несколько расширена за
счет приема, позволяющего оценить подвиж­
ность отдельных участков трахеи и бронхов
(стенок, гребешков). Если при проведении
исследований жесткими моделями бронхоско­
пов смещение стенок и гребешков трахеи и брон­
хов тубусом эндоскопа выполняется без особого
труда, то для эластичных эндоскопов с воло­
конной оптикой это трудновыполнимо. В кли­
нике разработан и применяется специальный
методический прием. Используются подвижная
секция и тяги фибробронхоскопа. Изменяя
положение рычага управления подвижной сек­
цией фибробронхоскопа, удается получать ин­
формацию о степени подвижности стенок тра­
хеи, бронхов, гребешков в местах их деления.
Правильная интерпретация получаемых при
этом ощущений ригидности, передаваемых
через тяги фибробронхоскопа, сложнее, чем
в жестких моделях эндоскопов, но с опытом
удается получить весьма важные сведения о
характере изменений в тканях и образованиях
вблизи бронхов, трахеи.
Завершив осмотр трахеи, переходят к изу­
чению киля ее бифуркации, начальных отделов
главных бронхов. При этом, наряду с оценкой
состояния слизистой оболочки бифуркации,
специальное внимание уделяют ее конфигура­
ции. Так, уплощение или «развертывание» киля
бифуркации трахеи, отклонение его в сторону,
ограничение или отсутствие подвижности чаще
всего свидетельствуют о значительных измене­
ниях в расположенных рядом группах лимфа­
тических узлов средостения: их увеличении,
86
формировании плотных малоподвижных кон­
гломератов. Все это позволяет судить о рас­
пространенности патологических изменений в
легких, органах средостения.
После обследования бифуркации трахеи
переходят к осмотру бронхов. Методически
правильно начать его с изучения просвета дыха­
тельных путей легкого, в котором не предпола­
гается патологических изменений. Такой под­
ход позволяет сформировать общее представ­
ление о состоянии слизистой оболочки просвета
дыхательных путей у данного конкретного боль­
ного (хронический бронхит, атрофический брон­
хит и т. п.). Тогда, зная эти «фоновые» измене­
ния, при осмотре слизистой оболочки бронхов
пораженного легкого легче обнаружить даже
небольшие изменения, вызванные заболева­
нием (признаки воспаления, перестройки рель­
ефа).
В пределах легкого осмотр главных бронхов,
отходящих от него долевых и далее — сегмен­
тарных, субсегментарных и более мелких осу­
ществляют по единой системе, с обязательной
регистрацией состояния гребешков в зонах их
деления, а также респираторных движений
бронхов, степени сократительной способности
их устьев. Осмотр бронхиального дерева в пре­
делах каждого легкого производят сверху вниз:
от верхнедолевых бронхов до бронхов базаль­
ной пирамиды.
При скоплении в просвете дыхательных путей
патологического содержимого, препятствующе­
го проведению осмотра, затрудняющего интер­
претацию полученных данных, его удаляют с
помощью электроотсоса. При необходимости
бронхиальное дерево промывают изотониче­
ским раствором натрия хлорида или раствором
антисептика (фурацилин 1:5000).
Уже на основании только осмотра при фибробронхоскопии имеется возможность получить
точное представление о характере патологиче­
ских изменений в легких более чем у 60 %
больных. Так, при опухоли в просвете бронха
определяется «плюс-ткань» в виде бугристых
грибовидных, папилломатозных, гранулематоз­
ных, полиповидных разрастаний; при наличии
инфильтратов стенки бронха видно плоское или
бугристое с гладкой или шероховатой поверх­
ностью выбухание, а также сужение просвета
бронха с какой-либо стороны или концентриче­
ского характера. Как правило, в зоне измене­
ний слизистая оболочка также изменена: рых­
лая, легко кровоточащая, лишенная респиратор­
ной подвижности. Документировать результаты
осмотра при фибробронхоскопии позволяет фо­
тографирование выявленных изменений в тра­
хеобронхиальном дереве.
Наряду с детальным осмотром и определе­
нием патологических изменений в трахеоброн­
хиальном дереве эндоскопическое обследование
больных с заболеваниями легких обеспечивает
взятие материала для морфологической вери­
фикации заболевания. У большинства больных
это позволяет успешно завершить этиологиче­
скую и топическую диагностику заболевания.
Особенно важными становятся результаты мор­
фологической диагностики при подозрении на
рак легкого. Предпринятые в начальном перио­
де обследования больного, они дают возмож­
ность в короткое время установить правильный
диагноз и определить показания к наиболее
рациональному лечению.
Большое практическое значение результатов
морфологических исследований материала,
получаемого при бронхоскопии, определило
разработку и усовершенствование специальных
приспособлений для его получения. К ним отно­
сятся наборы биопсийных щипцов, кюретки,
щеточки-скарификаторы, иглы для выполне­
ния чрезбронхиальной биопсии, всевозможные
аспираторы.
Как убеждает опыт, применение фибробронхоскопа, несмотря на достоинства прибора,
не позволяет ответить на вопрос о протяжен­
ности патологических изменений за пределами
видимых бронхов. Фактические границы их рас­
пространения, особенно при раке легкого, как
правило, бывают более значительными, чем
можно предполагать на основании данных эн­
доскопического обследования.
Это определяет необходимость дальнейшего
совершенствования способов диагностики, при­
менение различных, взаимно дополняющих
друг друга методов обследования больных.
ДИАГНОСТИЧЕСКАЯ ПУНКЦИЯ
ПЛЕВРАЛЬНОЙ ПОЛОСТИ
Пункция плевральной полости относится к
числу широко распространенных диагностиче­
ских приемов при заболеваниях легких и плев­
ры. Получаемая при этом информация нередко
позволяет судить о характере патологических
изменений и определяет последующую лечеб­
ную тактику. Кроме того, освобождение плев­
ральной полости от экссудата или воздуха чаще
всего позволяет предпринять последующее
обследование с применением более сложных
приемов и методов как за счет улучшения со­
стояния больных, так и вследствие восстанов­
ления нормальных анатомических взаимоот­
ношений органов грудной полости, расправле­
ния коллабированного или ателектазированного
легкого.
Показания к пункции определяют при выяв­
лении физикальными и рентгенологическими
методами обследования скопления жидкости
или газа в плевральной полости. В зависимости
87
от характера этих находок уточняются место
и задачи плевральной пункции.
При скоплении в плевральной полости жидко­
сти пункция выполняется в положении боль­
ного сидя с опорой-подставкой под руку со
здоровой стороны туловища. Место для пунк­
ции намечают сзади, в нижних отделах груд­
ной полости, чаще всего — по ходу седьмого
межреберья между среднеподмышечной и лопа­
точной линиями.
В намеченной для пункции точке выполняют
послойную анестезию тканей грудной стенки.
Обязательным условием плевральной пункции
является предупреждение сообщения полости
с внешней средой — в плевральную полость
не должен попасть воздух. С этой целью па­
вильоны иглы соединяют со шприцем через
специальный переходник-краник, с помощью
которого обеспечивается герметичность иглы при
отсоединении шприца.
Вид и характер жидкости в полости, ее коли­
чество уже в процессе проведения пункции не­
редко решают многие вопросы диагностики
(гной, хилезная жидкость, кровь, серозный
экссудат). Тем не менее принципиально важ­
ным является специальное изучение жидкости.
Определяются ее плотность, биохимический
и цитологический состав, характер микрофло­
ры и чувствительность ее к антибиотикам. Часть
жидкости рекомендуется оставить в пробирке
на сутки для макроскопической оценки осадка.
При наличии в плевральной полости воздуха
пункцию выполняют спереди во втором меж­
реберье по среднеключичной линии. Использо­
вание при этом пневмотораксного аппарата
позволяет не только удалить из плевральной
полости воздух и установить его количество, но
и уточнить характер сообщения плевральной
полости с воздухоносными путями. Это часто
является определяющим при решении вопросов
последующей лечебной тактики. Для этой цели
используют плевроманометрию, дающую воз­
можность на разных этапах эвакуации воздуха
определить степень и устойчивость отрицатель­
ного даыения в плевральной полости.
При скоплении в плевральной полости воз­
духа и жидкости чаще всего требуется выпол­
нение плевральных пункций из нескольких
точек. Выбор места пункции определяется об­
ластью скопления жидкости или газа, диагно­
стированных при рентгенологическом исследо­
вании. Пункцию плевральной полости рекомен­
дуется завершать контрольным рентгенологи­
ческим исследованием, которое позволяет судить
об эффективности пункции, а также может
дать дополнительную информацию о характере
изменений в легких или плевральной полости,
получение которой ранее — на фоне экссудата
или воздуха — было затруднительно.
ДОПОЛНИТЕЛЬНЫЕ МЕТОДЫ
ДИАГНОСТИКИ ЗАБОЛЕВАНИЯ
ДИАГНОСТИЧЕСКИЙ ПНЕВМОТОРАКС
Диагностический пневмоторакс применяется
для уточнения места расположения солидных
образований, изучение которых при рентгено­
графии или томографии не позволяет решить:
исходят ли они из средостения и других образо­
ваний, формирующих грудную полость, или
располагаются в легком. С помощью диагно­
стического пневмоторакса можно уточнить
наличие или отсутствие сращений в плевраль­
ной полости, степень фиксации ими легкого.
На рентгенограммах, выполненных после
наложения пневмоторакса, удается установить,
отошло ли образование вместе с легким, или
же осталось связанным с грудной стенкой,
диафрагмой, средостением.
Наиболее удобным местом для пункции плев­
ральной полости с целью наложения диагности­
ческого пневмоторакса являются второе меж­
реберье по среднеключичной линии (в положе­
нии больного сидя) или третье — пятое меж­
реберья по средней подмышечной линии (в по­
ложении больного лежа на здоровом боку).
В намеченной точке на всю глубину грудной
стенки выполняется послойная местная анесте­
зия. На то, что игла находится в плевральной
полости, указывают свободное поступление
анестезирующего раствора из шприца, само­
произвольные перемещения его поршня в ритме
дыхания больного; на подключенном пневмо­
тораксном аппарате регистрируются перепады
давления на манометре.
Убедившись в том, что игла находится в плев­
ральной полости, с помощью пневмотораксно­
го аппарата в нее дозированно вводится 750—
1000 мл воздуха или кислорода. При этом на
манометре регистрируется «положительное —
положительное» давление. Игла извлекается.
Больному придается положение, необходимое
для оттеснения легкого газом от той или иной
части стенки грудной полости. Затем выпол­
няется рентгенологическое исследование.
После завершения исследования газ из плев­
ральной полости удаляется.
ДИАГНОСТИЧЕСКИЙ
ПНЕВМОПЕРИТОНЕУМ
Показанием к введению воздуха или кисло­
рода в брюшную полость с последующим рент­
генологическим обследованием являются обра­
зования, прилежащие к нижним долям лег­
ких и куполу диафрагмы, когда не удается отве­
тить на вопрос: располагаются ли они в легком,
исходят из диафрагмы или находятся в под-
88
Рис. 47. Доброкачественная опухоль правого легкого в усло­
виях искусственного пневмоперитонеума.
а — прямая рентгенограмма; б — боковая рентгенограмма.
диафрагмальном пространстве, например в печени (рис. 47).
Методика наложения пневмоперитонеума
состоит в следующем. В положении больного
на спине в точке, располагающейся на 2—3 см
выше и левее пупка, на всю глубину брюшной
стенки выполняется послойная местная анесте­
зия. В момент прокола париетальной брюшины
появляется ощущение свободного, без сопро­
тивления вытекания обезболивающего раствора
из шприца даже при отсутствии давления на
поршень. После этого иглу присоединяют к
пневмотораксному аппарату и в брюшную по­
лость дозированно в течение 3—5 мин вводят
1000—1200 мл кислорода, воздуха или закиси
азота. Последний удобен ввиду быстрого рас­
сасывания и некоторого анальгезирующего
эффекта. Больному на 20—30 мин придается
положение на здоровом боку с несколько при­
поднятой верхней частью туловища. При этом
введенный газ перемещается под купол диа­
фрагмы, оттесняя его кверху. На рентгенограм­
мах удается четко дифференцировать нижнюю
поверхность диафрагмы. В удалении газа из
брюшной полости необходимости нет. В течение
3—8 сут воздух рассасывается самостоятельно.
Кислород и закись азота исчезают раньше,
обычно к исходу первых суток.
ДИАГНОСТИЧЕСКИЙ
ПНЕВМОМЕДИАСТИНУМ
Пневмомедиастинография применяется для
уточнения расположения образований, которые
на рентгенограммах и томограммах прилежат
к органам средостения, сливаясь с ними. Кроме
того, этот метод может быть использован для
более четкого выявления различных новообра­
зований средостения, уточнения их взаимоот­
ношения с расположенными здесь органами.
Оттесняя медиастинальную плевру со стороны
средостения, удается уточнить расположение
новообразований по отношению к легкому в слу­
чаях, когда сращения в плевральной полости
не позволяют наложить пневмоторакс.
Для наложения переднего пневмомедиастинума больного укладывают на спину с неболь­
шим валиком под лопатками и отведенной кза­
ди головой. В области яремной вырезки гру­
дины делают местную анестезию кожи и под­
89
кожной клетчатки. За грудину вводят тонкую
иглу, предпосылая раствор анестетика. Убедив­
шись, что конец иглы находится в клетчатке
средостения, а не в сосуде, к павильону ее при­
соединяют пневмотораксный аппарат и мед­
ленно, дозированно в течение 7—10 мин, вводят
500—750 мл воздуха или кислорода. Больному
придается положение на спине с приподнятым
ножным концом, а затем — на здоровом боку,
что необходимо для более направленного рас­
пределения газа в пределах клетчаточных про­
странств. После этого выполняется рентгено­
логическое обследование.
При наложении заднего пневмомедиастинума
используют пресакральный доступ, откуда газ
по клетчатке забрюшинного пространства до­
стигает задних отделов средостения.
Для этого в положении больного на животе
ниже верхушки копчика выполняют местную
послойную анестезию. Длинную тонкую иглу,
предпосылая раствор анестетика, проводят под
копчик и далее выше в направлении к передней
поверхности крестца. Убедившись в том, что
конец иглы располагается в пресакральной клет­
чатке, а не в прямой кишке, с помощью пневмо­
тораксного аппарата поэтапно вводят до 1500—
2000 мл воздуха (не кислорода!). После завер­
шения этого этапа исследования больной в тече­
ние часа находится в вертикальном или полусидячем положении. Периодически рентгено­
логическим методом уточняется перемеще­
ние газа в восходящем направлении к заднему
средостению. После достижения им клетчаточ­
ных пространств заднего средостения выполня­
ется рентгенологическое обследование.
ровые ингаляции, ингаляции с муколитиками,
ферментами, эндотрахеальные вливания, ле­
чебные бронхоскопии. Только убедившись
в полноценности и эффективности предприня­
той подготовки, приступают к исследованию.
В качестве контрастного вещества наиболее
удобной является смесь сульфата бария и по­
рошка из корня алтея. Как показали наши на­
блюдения, эта смесь не вызывает аллергических
реакций, явлений йодизма, хорошо удаляется
из просвета дыхательных путей. Перед введе­
нием смесь подогревается до 36—37 °C.
В большинстве случаев исследование прово­
дится под местным обезболиванием. Для этой
цели используют препараты дикаина, растворы
новокаина, тримекаина.
Для введения контрастной смеси применяют
стандартные управляемые катетеры Розенштрауха — Смулевича.
После анестезии верхних дыхательных путей
проводится обезболивание бронхиального дере­
ва исследуемой стороны в различных положе­
ниях больного: на спине, на животе, на боку
с опущенным головным концом. В дальнейшем,
в зависимости от поставленных задач, проводят
исследование бронхиального дерева всего лег­
кого, его доли или сегмента. Заполнение брон­
хов производится под контролем рентгенотеле­
визионного экрана. Рентгенограммы выполня­
ются в прямой, боковой и косых проекциях
в положении больного стоя или лежа на латероскопе.
После завершения исследования бронхиаль­
ное дерево с помощью электроотсоса, присо­
единяемого к введенному в просвет бронхов
катетеру, по возможности максимально осво­
бождают от контрастного вещества, промывают
теплым антисептическим раствором. В тече­
ние последующих суток больному выполняются
паровые ингаляции. На следующий день целе­
сообразна контрольная рентгеноскопия. Она
позволяет судить о полноте освобождения брон­
хиального дерева от контрастного вещества, а
также, что не менее важно, может выявить из­
менения, не обнаруженные в ходе исследова­
ния (остаточные полости, кисты, в которых за­
держивается контрастное вещество).
Бронхография легких может быть выполнена
под наркозом. Особенность ее проведения за­
ключается в том, что больной лежит на спине,
осуществляется искусственная
вентиляция
легких в условиях миорелаксации. Контрастное
вещество вводят через интубационную трубку
и в период кратковременного апноэ выполняют
рентгенограммы обоих легких в прямой и косых
проекциях (рис. 48).
Перспективным представляется применение
аэрозольных бронхографий с использованием
в качестве контрастного вещества порошка тан-
БРОНХОГРАФИЯ
На протяжении многих лет клинического ис­
пользования показания к применению бронхо­
графии при разных заболеваниях легких много­
кратно пересматривались, уточнялись. Основ­
ными показаниями к применению этого метода
в настоящее время являются: подозрение на
аномалию трахеи и бронхов, бронхоэктазии,
другие хронические нагноительные заболева­
ния легких, туберкулез, некоторые формы
пневмос клерозов.
Для успешного выполнения бронхографии
требуется специальная предварительная под­
готовка больных, особенно отделяющих значи­
тельное количество мокроты, так как в этом
случае получить хорошее заполнение бронхов
не представляется возможным.
Для освобождения трахеобронхиального
дерева от патологического содержимого при­
меняются как медикаментозные средства (от­
харкивающие, мокроторазжижающие, спазмо­
литические), так и специальные методы — па­
90
Несмотря на определенные достоинства аэро­
зольной бронхографии, она еще не получила
широкого распространения в клинической прак­
тике, что связано с отсутствием заводского про­
изводства порошковых композиций, необхо­
димых для ее проведения.
ПЛЕВРОГРАФИЯ И ФИСТУЛОГРАФИЯ
Плеврография — метод исследования, с по­
мощью которого удается выявить, точно лока­
лизовать, определить размеры и конфигурацию
остаточной плевральной полости при эмпие­
мах, ригидном легком, спонтанном пневмото­
раксе и т. п.
Фистулография выполняется для определе­
ния направления и протяженности свищевых
ходов, распознавания поддерживающих их
причин (инородное тело, остеомиелит ребра),
а также для выяснения формы и размеров оста­
точной полости при сообщении ее с просветом
бронхиального дерева.
В качестве контрастного вещества использу­
ются водорастворимые вещества — кардиотраст,
уротраст и др.
В плевральную полость контрастное веще­
ство вводят путем пункции в точке, ранее наме­
ченной по рентгенограммам или при рентгено­
скопии, а в случае плеврокожного свища —
через введенный в свищевой ход катетер или
иглу с булавовидным концом. После заполне­
ния полости наружное отверстие свища закры­
вают полоской лейкопластыря.
Рентгенографию выполняют стоя (в двух
проекциях) и лежа на латероскопе. Плевро­
графия и фистулография в настоящее время
являются наиболее распространенными из
методов, дающих возможность определить,
локализовать и оценить размеры остаточной
плевральной полости. Необходимо иметь в
виду, что размеры полостей, как правило, пре­
вышают их контрастное изображение на рент­
генограммах.
Рис. 48. Поднаркозная бронхография у ребенка. Косая
проекция. Норма.
тала. Экспериментальные работы J. Nadel и
соавт. (1968) показали, что при этом не возни­
кает каких-либо серьезных осложнений.
Тантал, покрывая слизистую оболочку трахеи
и бронхов, позволяет с большой четкостью
выявить детали ее строения — складки, желе­
зистый аппарат.
Клинические наблюдения А. А. Криштафовича и соавт. (1961), Р. М. Рабиновича (1981),
М. Zammel и соавт. (1970) убеждают в простоте
техники танталовой аэрозольной бронхографии.
Контрастное вещество в виде мелкодисперсного
порошка вводится в просвет дыхательных путей
при помощи специального устройства — рас­
пылителя. Отмечены хорошая переносимость
процедуры больными, высокая информативность
полученных результатов.
По мнению А. А. Криштафовича и соавт.
(1982), аэрозольная бронхография особенно
предпочтительна в тех случаях, когда необхо­
димо точно оценить рельеф слизистой оболоч­
ки трахеобронхиального дерева, диагностиро­
вать стенозы трахеи и крупных бронхов, осо­
бенно у больных с низкими функциональными
резервами, в том числе у лиц, перенесших опера­
ции на легких.
АНГИОПУЛЬМОНОГРАФИЯ
Ангиопульмонография — способ контраст­
ного исследования сосудов малого круга кро­
вообращения. Чаще всего показания к ангиопульмонографии определяются как дифферен­
циально-диагностические: при пороках разви­
тия легкого, нагноительных заболеваниях,
бластоматозном процессе. Она дает также воз­
можность определить функциональное состоя­
ние паренхимы легкого, оценить гемодинамику.
Различают четыре способа ангиопульмонографии: 1) общую ангиопульмонографию, вы­
полняемую путем внутривенного введения конт­
растного вещества или посредством ангиокар-
91
Рис. 49. Ангиопульмонография.
а — артериальная фаза; б — капиллярная фаза; в — венозная
фаза.
диографии из правого желудочка сердца; 2)
селективную ангиопульмонографию, выпол­
няемую из ствола или ветвей легочной артерии;
3) суперселективную ангиопульмонографию,
включающую контрастирование из долевых,
сегментарных ветвей легочной артерии; 4) ок­
клюзионную ангиопульмонографию, выполня­
емую при заклинивании субсегментарной или
лобулярной ветви легочной артерии концевой
частью сердечного катетера или при блокирова­
нии баллоном катетера магистральной ветви
легочной артерии.
Ангиопульмонография производится в рент­
генооперационных, обеспечивающих телеви­
зионный рентгенологический и физиологиче­
ский контроль, оснащенных автоматическими
инъекторами для быстрого, дистанционного и
синхронного с рентгенографией введения конт­
растного вещества (уротраст, верографин и др.)
в сосуды и сердце.
Сердечный катетер вводится в сосуды, как
правило, чрескожно-чрезбедренным способом.
При этом применяется телевизионный контроль,
92
катетер устанавливается в правом предсердии,
правом желудочке, легочной артерии.
При анализе ангиопульмонограмм обраща­
ют внимание на пофазовое продвижение кон­
трастного вещества по различным регионам
легкого: легочной артерии, капиллярного рус­
ла, венозной системы малого круга кровообра­
щения (рис. 49).
По комбинации ангиографических признаков
представляется возможным охарактеризовать
вид и распространенность патологического
процесса (при двухпроекционной сериографии — посегментарно) в легком, при этом обра­
щается внимание на наличие деформации сосу­
дов, смещение, контуры, разреженность сосу­
дистого рисунка (рарефикацию), степень раз­
вития сосудов отдельных сегментов, долей,
легкого, характер расположения камер сердца,
ротацию сердца и др.
Качественная диагностика ангиопульмоно­
грамм может быть дополнена количественной
оценкой регионарного легочного кровотока
с помощью способа, разработанного в клинике
[Лыткин М. И. и др., 1984], при котором уточ­
няется, в каких сегментах сохранено и преи­
мущественно осуществляется кровообращение
в малом круге и в каком количественном объеме.
Комплексная оценка ряда показателей (дав­
ление в правых камерах сердца и системе легоч­
ной артерии, насыщение кислородом артериаль­
ной и смешанной венозной крови, а также в
различных регионах малого круга и др.) позво­
ляет определить резервные возможности малого
круга кровообращения и рационально планиро­
вать лечение пульмонологических больных.
В сочетании с количественной оценкой регио­
нарного легочного кровотока, определение ле­
гочных объемов крови значительно расширяет
и углубляет представления о резервных воз­
можностях организма.
При селективной ангиографии бронхиальных
артерий катетер вводится в грудную аорту и да­
лее — до устья бронхиальных сосудов; введе­
ние контрастного вещества осуществляется
с помощью автоматического инъектора. Сериография, проводимая, как правило, в передне­
задней проекции, может быть дополнена рент­
генограммами в боковой или косой проекциях
в зависимости от задач исследования (рис. 50).
При анализе бронхиальных ангиограмм опре­
деляются уровень и тип анатомического ветвле­
ния сосудов, положение, форма, диаметр, харак­
тер контуров сосуда, извитость его и проходи­
мость, характер и уровень окклюзии, степень
развития коллатеральных ветвлений и их взаи­
мосвязь с легочной артерией. Учитываются
уровни анастомозирования двух систем крово­
обращения легких (субсегменты, сегменты, доли
или лобулярные ветви легочной артерии) и сте-
Рис. 50. Селективная ангиография бронхиальных артерий.
пень выраженности артериального шунтирова­
ния в легочную артерию. Изучается состояние
сосудов контрастированных сегментов легоч­
ной артерии.
Бронхиальную артериографию целесообразно
выполнять в сочетании с катетеризацией легоч­
ной артерии и изучением показателей давления,
оксиметрией в регионах выше и ниже выявляе­
мых анастомозов двух систем кровообращения
легких.
При контрастном исследовании сосудов сре­
достения можно установить признаки пораже­
ния расположенных здесь лимфатических уз­
лов при раке легкого.
Контрастное исследование сосудов средосте­
ния включает в себя флебографию и аортогра­
фию. Флебография выполняется с учетом ха­
рактера патологического процесса, выявляемого
при помощи рентгенографии, томографии, брон­
хографии. При указании на вероятное пора­
жение лимфатических узлов переднего средо­
стения выполняют верхнюю кавографию и конт­
растное исследование внутренних грудных вен,
а при подозрении на поражение лимфатических
узлов заднего средостения — азигографию.
Аортография при заболеваниях легких выпол­
няется в случаях предположения о распростране-
93
Рис. 51. Верхняя кавография. Контрастированы верхняя
полая вена, безымянная вена и правое предсердие.
Рис. 52. Флебограмма внутренних грудных вен.
нии патологического процесса на аорту или ее
ветви. Верхняя кавография наиболее часто вы­
полняется путем пункции локтевых вен или их
катетеризации. Другим вариантом верхней
кавографии является ретроградная катетериза­
ция верхней полой вены через нижнюю полую
вену и правое предсердие. При введении конт­
растного вещества регистрируется продвижение
его по венам переднего средостения, а также
сосудам малого круга (рис. 51).
Контрастное исследование внутренних груд­
ных вен выполняется введением контрастного
вещества в грудину на уровне четвертого меж­
реберья. На флебограммах внутренние грудные
вены видны в виде двух контрастируемых сосу­
дов, расположенных параллельно обеим сторо­
нам грудины (рис. 52). Признаками, указываю­
щими на наличие увеличенных лимфатических
узлов парастернальной области, считают ло­
кальные сужения просвета вен вплоть до пол­
ного блока, появление ретроградного кровотока,
коллатеральных ветвей, участков расширения
вен на ограниченном протяжении.
Контрастное исследование непарной и полу­
непарной вен — азигография — может быть
выполнено как с помощью внутрикостного введе­
ния контрастного вещества, так и посредством
прямой катетеризации устья непарной вены.
Для внутрикостного введения обычно исполь­
зуют остистый отросток одного из нижнегруд­
ных позвонков, а также задние сегменты IX
и X ребер. При этом контрастное вещество за­
полняет, кроме непарной вены, полунепарную
и вены позвоночных сплетений.
При прямой катетеризации устья непарной
вены катетер с проводником вводится в ниж­
нюю полую вену, правое предсердие, верхнюю
полую вену. Проводник удаляется. Концевая
часть катетера, имеющая двойной изгиб, в верх­
ней полой вене принимает исходно приданную
ему форму. Конец катетера устанавливают в
устье непарной вены, а затем производят ретро­
градное заполнение ее. Тугое и интенсивное
заполнение всей системы непарной и полунепар­
ной вен, а также восходящих поясничных вен
получают при введении 20—30 мл контраст­
ного вещества с объемной скоростью до 15 мл/с
(рис. 53).
Интерпретацию ангиографических призна­
ков анатомических и функциональных изме­
нений венозной системы средостения проводят
с учетом вариантов развития и индивидуаль­
94
ных особенностей строения безымянной, пле­
чеголовной, верхней полой, непарной и полуне­
парной вен. При метастазировании рака лег­
кого в средостение податливые венозные сосуды
оттесняются увеличенными лимфатическими
узлами и их конгломератами. Нарушение кро­
вотока в системе верхней полой вены приводит
к расширению сосудов непарной вены, которая
становится основным коллатеральным путем
оттока.
Наиболее характерные ангиографические
признаки, указывающие на увеличение лимфа­
тических узлов средостения, можно по данным
флебографии охарактеризовать следующим
образом: дефекты наполнения, блок сосуда,
сужение различной степени и протяженности,
изменение конфигурации сосуда, смещение и
вынужденно фиксированное его положение,
различные формы обструкции сосудов, раз­
витие коллатерального кровотока и степени его
выраженности, сопровождающееся расширением
сосудов, повышенной их извитостью.
Флебография позволяет дифференцированно
оценить органические и функциональные изме­
нения вен средостения, однако для этого необ­
ходимо отчетливо представлять физиологиче­
ские места сужений верхней полой вены (у ме­
ста впадения в правое предсердие), внутренних
грудных вен (на уровне грудино-реберного
сочленения) и др. При выявлении дефекта на­
полнения оценивается его форма (округлый
одиночный или полициклический, ровный или
изъеденный контур сосуда). Если для сдавле­
ния вены характерен ровный контур, то для
прорастания ее стенки — изъеденный, неров­
ный. Полицикличность контуров сосуда и циркулярность сужения вены указывают на рас­
пространенность процесса в средостении. Пол­
ная блокада вены выявляется в виде различных
форм ее культи: цилиндрической, конусообраз­
ной, округло-выпуклой или с округло-вогнутым
контуром. Форма культи может косвенно ука­
зывать на характер и причину окклюзии — сдав­
ление, сдавление-тромбоз или прорастание
опухолью. Если блок расположен в районе опу­
холи, то изменения сосуда наиболее вероятно
связаны с ней. Обструкция вены на значитель­
ном расстоянии от опухоли указывает на ее
тромбоз. Неровность нижнего контура левой
плечеголовной вены патогномонична для увели­
чения преаортокаротидных лимфатических
узлов и смещения кверху и кпереди дуги аорты.
Близкое положение дуги аорты к плечеголов­
ной вене создает передаточную пульсацию на
ее нижнюю стенку, что при ангиографии прояв­
ляется неровностью контура сосуда. Различным
уровням обстукции сосудов средостения соот­
ветствуют определенные варианты коллате­
рального кровообращения.
Рис. 53. Флебограмма непарной и полунепарной вен.
При аортографии удается определить отно­
шение патологического процесса в средостении
к аорте и ее магистральным ветвям. В соот­
ветствии с данными флебографии средостения
(кавографиц, азигографии и др.) это дает воз­
можность более полно оценить степень распро­
страненности процесса в лимфатических узлах
переднего и заднего средостения.
РАДИОИЗОТОПНЫЕ МЕТОДЫ
ИССЛЕДОВАНИЯ ЛЕГКИХ
Радиоизотопные методы исследования лег­
ких основаны на регистрации излучения радио­
активных изотопов, введенных в организм боль­
ного через дыхательные пути или кровеносную
систему. При проведении вентиляционной ра­
диографии легких используют радиоактивный
изотоп ксенона (133Хе). Вдыхание смеси ксе­
нона с кислородом дает возможность судить
о состоянии бронхиального дерева, оценить
участие в вентиляции различных отделов па­
ренхимы легкого. Однако применение радиоак­
тивных газов не позволяет получить картину
сосудистого русла легких.
Об интенсивности легочного кровотока, диф­
фузионной способности альвеол судят по ска­
95
нограммам, полученным при введении радио­
активных препаратов в кровеносное русло. Для
этой цели используется альбумин человеческой
сыворотки, меченный радиоактивными изото­
пами 131I, |251, 51Сг, 9(>Гс. Сразу же после внут­
ривенного введения меченый альбумин с части­
цами размерами не более 10 мкм задержива­
ется в капиллярном русле легких. у-Излучение
изотопа, которым мечен альбумин, регистри­
руется сканером. В результате исследования
получают точную информацию о характере ка­
пиллярного кровотока в различных участках
легкого.
Радиоизотопное сканирование легких позво­
ляет оценить различные нарушения кровооб­
ращения, особенно при тромбоэмболических
поражениях сосудов, при бластоматозных по­
ражениях. В этих случаях на сканограммах об­
наруживаются сужение легочных полей и разре­
жение или полное отсутствие записи в зоне
расположения опухоли, что может быть решаю­
щим для диагноза.
При тромбоэмболиях сосудов малого круга
кровообращения в остром периоде сканирова­
ние позволяет диагностировать и оценить объем
нарушения легочного кровообращения. Повтор­
ные исследования дают возможность контро­
лировать степень и характер восстановления
легочного кровообращения.
Возможности отдельных методов, использу­
емых при обследовании больных заболеваниями
легких, могут быть расширены за счет их соче­
танного использования.
Так, в клинической практике получило при­
знание сочетание эндоскопического и рентге­
нологического методов обследования. В слу­
чае необходимости направленного взятия мате­
риала для морфологического изучения из участ­
ков легкого, расположенных в дистальных от­
делах бронхиального дерева, недоступных
визуальному контролю через фибробронхоскоп,
биопсийные щипчики или щеточки-скарифика­
торы направляются к патологическому очагу
под контролем рентгеновского экрана. Подобный
прием возволяет сделать биопсию наиболее пе­
риферических отделов легкого.
Используя аналогичный прием, возможна
катетеризация субсегментарных бронхов и се­
лективная, строго направленная в отношении
измененных участков легкого бронхография.
Следует отметить, что выполнение подобных
исследований пока еще ограничивается специа­
лизированными пульмонологическими стацио­
нарами, имеющими необходимое оснащение и
подготовленный для проведения такого обсле­
дования персонал.
Для выполнения сочетанных исследований
следует также применять специальный (экра­
нированный) фибробронхоскоп.
ДИАГНОСТИЧЕСКИЕ
ОПЕРАТИВНЫЕ ВМЕШАТЕЛЬСТВА
ТРАНСТОРАКАЛЬНАЯ ИГЛОВАЯ
БИОПСИЯ ПЛЕВРЫ
Показанием к выполнению пункционной
биопсии плевры чаще всего является предполо­
жение о туберкулезном или бластоматозном
ее поражении.
В точке, намеченной по рентгенограммам
и томограммам, проводится послойное мест­
ное обезболивание грудной стенки, после чего
с помощью специально предложенной для этой
цели иглы Эбрамса [М. Abrams], имеющей на­
ружный диаметр 4 мм, вращательным движе­
нием высекается цилиндрик мягких тканей груд­
ной стенки с париетальной плеврой. Полученный
материал направляется для гистологического
изучения.
Принципиальным недостатком этого метода
является то, что выполняется он, по существу,
вслепую. Поэтому при свойственном плевраль­
ным листкам очаговом характере поражения
при определении этиологического диагноза учи­
тывать следует лишь положительный результат
исследования.
ТРАНСТОРАКАЛЬНАЯ ПУНКЦИОННАЯ
БИОПСИЯ ЛЕГКОГО
Показанием к пункционной биопсии явля­
ется формирование в периферических отделах
легкого так называемых «шаровидных образо­
ваний», морфологическая структура которых
неясна, а торакотомия сопряжена с повышен­
ным риском.
Биопсия выполняется в рентгеновском каби­
нете под контролем экрана электронно-оптиче­
ского преобразователя. Определяется кратчай­
шее расстояние от поверхности кожи до обра­
зования в легком, и в намеченной точке выпол­
няется послойная анестезия тканей грудной
стенки. Для пункции используются игла Сильвермена или различные ее модификации. В кли­
нике для этой цели применяется игла-троакар
с концом, заточенным в виде фрезы. Под конт­
ролем рентгеновского экрана игла с троакаром
вводится в образование в легком. Убедившись
в правильном расположении конца иглы, тро­
акар извлекают, а иглу медленно продвигают
вперед, вращая по часовой стрелке. Режущий
фрезевой конец высекает участок образования.
Затем с помощью шприца создается неболь­
шой вакуум, удерживающий в просвете иглы
биопсийный материал, и игла извлекается. По­
лученный материал подлежит морфологиче­
скому изучению.
Из наиболее частых осложнений транстора­
кальной биопсии легкого следует отметить:
96
пневмоторакс, небольшое кровохарканье; при
инфицированном исследуемом образовании
(формировании в нем абсцесса) возможен пере­
нос инфекции по ходу иглы с развитием флег­
моны грудной стенки. Возникновение имплан­
тационных метастазов при пункции злокаче­
ственной опухоли относится к числу очень ред­
ких осложнений.
ТОРАКОСКОПИЯ
Этот диагностический прием имеет значение
при обследовании больных туберкулезом лег­
ких, спонтанным пневмотораксом. Кроме того,
с помощью торакоскопии возможны уточнение
локализации и характера бронхоплевральных
свищей при хронической эмпиеме плевры, а так­
же осмотр париетальной и висцеральной плев­
ры при подозрении на поражение их опухолью
с направленным взятием материала для мор­
фологического изучения. Исследование выпол­
няется в перевязочной или операционной. Перед
торакоскопией на стороне поражения наклады­
вается пневмоторакс.
Больной укладывается на здоровый бок с за­
веденной за голову рукой. Наиболее удобным
местом для введения прибора является область
пересечения третьего — пятого межреберий
со средней подмышечной линией, но в зависи­
мости от целей исследования и характера рент­
генологических изменений оно может быть
соответственно изменено. При сформировавшем­
ся плеврокожном свище эндоскоп вводится в
плевральную полость по этому каналу.
Кожа после обезболивания прокалывается
остроконечным скальпелем, а через остальные
слои грудной стенки проходят в плевральную
полость с помощью троакара с мандреном из
комплекта торакоскопа. После извлечения
мандрена через троакар проводится торакоскоп.
Вращая торакоскоп вокруг оси и изменяя угол
его наклона, производят осмотр легкого, вис­
церальной и париетальной плевры. С помощью
биопсийных щипчиков направленно, под конт­
ролем зрения, берется материал для морфоло­
гического изучения.
В качестве торакоскопа может быть исполь­
зован фибробронхоскоп, небольшой наружный
диаметр которого, системы надежного и интен­
сивного освещения и управления, а также уст­
ройства для выполнения биопсии расширяют
возможности метода.
После окончания исследования эндоскоп и
троакар извлекаются, на грудную стенку на­
кладываются швы. Удаляется воздух из плев­
ральной полости. В числе возможных осложне­
ний торакоскопии иногда отмечают формирова­
ние реактивного выпота, лечение которого осу­
ществляется пункциями.
7 Зак. 0517
АБСЦЕССОСКОПИЯ
Волоконно-оптический эндоскоп может быть
использован для оценки состояния полости
абсцесса легкого, осмотра дренирующего брон­
ха, динамического контроля за процессами очи­
щения и заживления гнойной полости.
Для выполнения исследования эндоскоп в
полость абсцесса вводится через сформировав­
шийся свищевой ход или путем торакоцентеза.
Перед проведением троакара следует убе­
диться в том, что легкое в зоне расположения
абсцесса спаяно с париетальной плеврой. После
этого выполняется пункция полости абсцесса.
По ходу иглы через стенку грудной полости
проводится троакар с мандреном. После извле­
чения мандрена с помощью резинового катетера
и электроотсоса удаляется гнойное содержи­
мое, промывается полость. Через троакар прово­
дится эндоскоп. Полость осматривается, берет­
ся материал для морфологического и микроби­
ологического исследований.
БИОПСИЯ НАДКЛЮЧИЧНЫХ
ЛИМФАТИЧЕСКИХ УЗЛОВ
Показанием к выполнению этого диагности­
ческого приема чаще всего является оценка рас­
пространения опухоли легкого или других ор­
ганов грудной полости. Определенное значение
биопсия надключичных лимфатических узлов
имеет для дифференциальной диагностики с
заболеваниями, при которых имеются внешне
сходные изменения в лимфатическом аппарате
(лимфогранулематоз, туберкулез).
Для выяснения состояния нижних шейных
лимфатических узлов применяют прескаленную биопсию [Daniels А., 1949]. При этом под
местным обезболиванием или под наркозом
удаляется клетчатка с расположенными в ней
лимфатическими узлами второго клетчаточного пространства шеи. Эта анатомическая область
ограничена внутренней яремной и подключич­
ной венами у места их слияния в плечеголов­
ной венозный ствол и нижним брюшком лопа­
точно-подъязычной мышцы. Располагающиеся
здесь лимфатические узлы (нижние глубокие
яремнце) иссекаются и подвергаются гистоло­
гическому исследованию. По данным А. Н. Матыцина (1969, 1977), О. Brantigan и соавт.
(1976), метастазы опухоли легкого при этом
в увеличенных лимфатических узлах обнару­
живаются в 17—32 % наблюдений, а в неувеличенных, внешне не измененных, не опреде­
ляемых при пальпации — в 6—12 %.
Возможным вариантом морфологической
оценки состояния надключичных лимфатиче­
ских узлов является пункционная биопсия. Этот
менее травматичный прием используется глав-
97
ным образом для исследования измененных
лимфатических узлов — увеличенных, четко
пальпируемых. По мнению А. С. Павлова и
соавт. (1979), выполнение этого простого в ме­
тодическом отношении диагностического при­
ема дает возможность при цитологическом
исследовании материала обнаружить у 66,6 %
больных раком легкого метастазы опухоли.
Однако необходимо иметь в виду, что медиа­
стиноскопия не может дать полного представ­
ления о состоянии средостения на всем протя­
жении. Затруднено исследование задних его
отделов, лимфатических узлов области «аор­
тального окна»; не всегда возможно определить
отношение первичной опухоли к сосудам корня
легкого, перикарду.
МЕДИАСТИНОСКОПИЯ
ПАРАСТЕРНАЛЬНАЯ (ПЕРЕДНЯЯ)
МЕДИАСТИНОТОМИЯ
Выполнение медиастиноскопии предназна­
чено для решения вопроса о состоянии лимфати­
ческих узлов средостения (паратрахеальных,
трахеобронхиальных, претрахеальных, бифур­
кационных) путем их визуального исследо­
вания, инструментальной пальпации и взятия
пункционной или прямой биопсии. Таким обра­
зом, основной задачей медиастиноскопии явля­
ется оценка характера и степени распростра­
ненности бластоматозного процесса. Именно
с этой целью она была разработана Е. Carlens
в 1959 г.
Исследование выполняется под наркозом.
В положении больного на спине, с валиком, под­
ложенным под лопатки, и отведенной кзади
головой над яремной вырезкой грудины дела­
ется поперечный разрез кожи, рассекаются фас­
циальные образования. Тупо, с помощью пальца
и инструментов расслаивается клетчатка за гру­
диной и в переднем средостении, формируется
канал для введения эндоскопа (медиастиноскопа). Осматриваются анатомические образова­
ния переднего средостения, расположенные
здесь группы регионарных лимфатических уз­
лов. С помощью иглы, биопсийных щипчиков
или зажимов измененные или подозрительные
в отношении поражения патологическим про­
цессом ткани и лимфатические узлы берут для
морфологического изучения. Исследование за­
вершается гемостазом, наложением швов на
рану.
Медиастиноскопия может сопровождаться
рядом осложнений. По сводным данным Е. Adler
(1976), на 7000 исследований в 0,1 % возникли
тяжелые кровотечения, в 0,32 % — парез воз­
вратного нерва, в 0,04 % — повреждение пище­
вода. Имелись случаи развития медиастинита,
пневмоторакса.
По данным А. М. Авдеева (1968, 1971), ме­
диастиноскопия, предпринятая у больных раком
легкого, позволила в 18,3 % наблюдений уста­
новить метастазы в медиастинальных группах
лимфатических узлов. Выполнение медиасти­
носкопии у больных раком легкого, имевших
рентгенологические признаки метастазов в лим­
фатических узлах средостения, увеличивает
этот показатель до 32—43,4 % [Вагнер Р. И.,
Волков О. Н., 1969; Павлов А. С. и др., 1979].
Определенная неудовлетворенность возмож­
ностями и результатами исследования средосте­
ния с помощью медиастиноскопии по Е. Carlens
(1959) явилась основанием для разработки и
предложения диагностической парастернальной
(передней) медиастинотомии [Пирогов А. И.,
Чхиквадзе В. Д., 1970, 1973; Stemmer L. et al.,
1965; Fajgeli F., 1968; Overholt R. et al., 1970].
Парастернальная медиастинотомия обеспе­
чивает лучший доступ к лимфатическим узлам
средостения, дает возможность исследования
клетчаточного пространства впереди от верхней
полой вены и дуги аорты, «аортального окна»
и корня легкого, более свободного визуального
контроля, широкого пальпаторного исследова­
ния средостения и взятия для изучения не­
скольких лимфатических узлов из различных
участков регионарных коллекторов.
Исследование выполняется в операционной.
В большинстве наблюдений, когда при медиасти­
нотомии принимается решение о радикальной
операции, сразу же после ее завершения при­
ступают к торакотомии [Павлов А. И. и др.,
1979].
Под наркозом, в положении больного на спи­
не, с валиком под плечами и головой, справа
или слева от края грудины, параллельно и отсту­
пя от него кнаружи на 1 см, выполняется верти­
кальный разрез кожи между I—III ребрами.
Послойно достигают хряща II ребра, который
поднадхрящнично резецируется на протяжении
2,5—3 см. При необходимости углубленного
исследования нижнего края корня легкого и
околопищеводных групп лимфатических узлов
дополнительно резецируется также хрящ III
ребра. Выделяются и перевязываются внутрен­
ние грудные артерии и вены. Тупо отслаивается
кнаружи медиастинальная плевра. Из образо­
ванного доступа проводится обследование сре­
достения и расположенных в нем органов (верх­
няя полая вена, аорта, регионарные лимфати­
ческие узлы, элементы легкого). При необ­
ходимости клетчатка и отдельные лимфатиче­
ские узлы берутся для гистологического иссле­
дования. Исследование завершается гемоста­
зом, а при нарушении целости медиастиналь­
ной плевры и развитии пневмоторакса — дре­
98
нированием плевральной полости. После медиастинотомии проводится контрольное рентгено­
логическое исследование.
диагностическая' торакотомия
В тех случаях, когда иными методами уста­
новить точный диагноз или распространенность
патологических изменений не представляется
возможным, особенно у больных, совокупность
результатов обследования у которых не поз­
воляет исключить развитие рака легкого, оправ­
дана диагностическая торакотомия.
Во время торакотомии выполняются срочная
биопсия очага поражения, лимфатических уз­
лов или резекция измененного участка легкого
(лобэктомия, сегментэктомия, атипичная ре­
зекция) в целях морфологического изучения.
Обнаружение при этом рака легкого делает
диагноз достоверным и позволяет судить о рас­
пространенности бластоматозного поражения.
Чаще всего такое диагностическое оперативное
вмешательство сразу же переходит в лечебное.
По понятным причинам выполнение диагно­
стической торакотомии противопоказано у
больных, не подлежащих хирургическому ле­
чению вследствие тяжести общего состояния,
обусловленной основным или сопутствующими
заболеваниями. В этих случаях диагностиче­
ские трудности преодолеваются путем исполь­
зования более щадящих методов, применяемых
в процессе динамического наблюдения и симпто­
матического лечения.
ДИАГНОСТИКА ОТДАЛЕННЫХ
МЕТАСТАЗОВ РАКА ЛЕГКОГО
Метастазы рака легкого чаще всего локали­
зуются в печени, почках, надпочечниках, голов­
ном мозге, костях. Поэтому определение состоя­
ния органов брюшной полости, которые при
раке легкого стоят на втором месте после пора­
жения лимфатических коллекторов средосте­
ния, имеет важное значение.
Среди специальных методов исследования
печени, предпринимаемых для этой цели, наибо­
лее часто используются радиоизотопная гепатография и гепатосканирование. Метод позво­
ляет обнаружить в печени образования, имею­
щие поперечные размеры более 3 см [Зубов­
ский Г. А. и др., 1976]. Однако, как свидетельсгвуют данные A. De Priest и соавт. (1973),
с абсолютной точностью поражение печени
метастазами опухоли можно предсказать лишь
у 52,6 % больных с патологическими измене­
ниями в ней, выявленными при сканографии.
Для определения метастазирования опухоли
в ткань печени используются также термогра­
фия [Mansfield V. et al., 1970], ультразвуковая
эхолокация [Упырев А. 3., 1968; Lavac-Jeantet Е.
et al., 1975], ангиография [Марморштейн С. Я.,
Гелонский В. М., 1972; Viallet R. et al., 1976].
Перспективным является применение компью­
терной рентгенотомографии.
При больших изменениях в печени, выявлен­
ных с помощью неинвазивных методов иссле­
дования, для установления этиологического
диагноза выполняется пункционная биопсия.
По данным С. Conn, A. Gesner (1963), у поло­
вины обследованных больных раком легкого
подтверждается ее бластоматозное пораже­
ние.
Выявление и гистологическая верификация
метастазов опухоли в печень возможны с по­
мощью лапароскопии [Бидяк И. В., 1974; Пиро­
гов А. И. и др., 1976; Cuschieri J., 1975]. Однако
существенным недостатком лапароскопии явля­
ется недоступность для обозрения органов, рас­
положенных в забрюшинном пространстве.
Диагностическая лапаротомия при раке лег­
кого дает возможность наиболее полно оце­
нить состояние органов брюшной полости и
забрюшинного пространства. Впервые с этой
целью она была применена R. Bell и соавт. в
1963 г., а в последующем ею пользовались и дру­
гие авторы.
По мнению А. С. Павлова и соавт. (1979),
представивших анализ 148 лапароскопий и ла­
паротомий у больных раком легкого, эти иссле­
дования вносят коррективы в результаты, полу­
ченные при радиоизотопном исследовании пе­
чени, и позволяют уточнить распространенность
опухолевого процесса. Однако широкого рас­
пространения диагностическая лапаротомия
при раке легкого не получила.
В последние годы для оценки состояния над­
почечников у больных раком легкого при подо­
зрении на развитие в них метастазов опухоли
предложена прямая супрареноскопия [Матыцин А. Н., 1983].
С помощью специального прибора — супрареноскопа — удается осмотреть органы забрю­
шинного пространства — почки, надпочечники.
При необходимости визуальная диагностика
может быть расширена взятием материала для
морфологического изучения.
ОЦЕНКА ФУНКЦИОНАЛЬНОЙ
ОПЕРАБЕЛЬНОСТИ БОЛЬНЫХ
ОЦЕНКА ФУНКЦИИ
ВНЕШНЕГО ДЫХАНИЯ
Учитывая то обстоятельство, что операция
на легких и плевре усугубляет прежде всего
функциональные изменения в системе внешнего
дыхания, о состоянии последнего определен­
ную информацию представляют анамнез и дан­
ные обычного клинического обследования.
Быстрая утомляемость, одышка во время
ходьбы и при движениях, учащение дыхания
с участием вспомогательных мышц в покое,
цианоз слизистых оболочек и кожи, нарастаю­
щий во время умеренной физической нагрузки,
указывают на предельное снижение резервов
дыхания. Медленное прогрессирование дыха­
тельных расстройств может быть не замечено
пожилыми больными, так как с возрастом по­
степенно ограничивается физическая актив­
ность. Поэтому субъективное ощущение пере­
носимости нагрузок, например возникновение
одышки при ходьбе, должно быть подкреплено
объективными исследованиями.
У больных старшей возрастной группы исполь­
зуется простой тест: реакция больного на подъ­
ем по лестнице с этажа на этаж. Преодоление
двух-трех маршей лестницы в обычном темпе
(рядом с врачом) без значительного учащения
дыхания и выраженной одышки свидетельству­
ет об отсутствии существенных расстройств
дыхания. Если частота дыхания и пульса восста­
навливается через 2—3 мин после этой пробы,
то больной, как правило, переносит резекцию
одной или двух долей легкого без тяжелых
функциональных последствий.
Пробы с задержкой дыхания на вдохе (Штан­
ге) и на выдохе (Саабразе — Генча) позволяют
оценить достаточность дыхания (при задержке
более 35—40 с). В то же время уменьшение вре­
мени задержки до 10—15 с еще не дает воз­
можности сделать обоснованное заключение
о функциональной неоперабельности, так как
на результаты этих проб влияет субъективный
фактор.
Для оценки степени снижения функциональ­
ных резервов дыхания используются, величины
жизненной емкости легких (ЖЕЛ), минутного
объема дыхания (МОД), максимальной минут­
ной вентиляции (ММВ) и коэффициента ис­
пользования кислорода (КИОг). Определение
подразделений ЖЕЛ не дает каких-либо допол­
нительных критериев, хотя предельное сниже­
ние резервного объема выдоха до нуля и появ­
ление симптома «воздушной ловушки» (при
спокойном, нефорсированном выдохе после глу­
бокого вдоха) свидетельствуют о значительных
эмфизематозных изменениях легких. Счита­
ется, что уменьшение ЖЕЛ до 50 % от долж­
ной величины является предельным, при кото­
ром возможна обширная резекция легких. Опыт
клиники убеждает, что больные, которые успеш­
но переносили пневмонэктомию, нередко имели
ЖЕЛ, составлявшую 40—45 % от должной.
Определение односекундной ЖЕЛ (той части,
которая выдыхается в первую секунду) наибо­
лее ценно для определения выраженности об­
структивных процессов в конечных разветвле­
ниях бронхиального дерева. Для выяснения
степени скрытого бронхоспазма в случаях зна­
чительного снижения ЖЕЛ необходимо про­
водить пробы с бронхолитиками (новодрином,
эуспираном и др.) или fi-блокаторами (обзиданом). Заметное увеличение этого показа­
теля спирограммы на фоне действия бронхо­
литика позволяет более уверенно оценивать
функциональную обеспеченность внутригрудного вмешательства.
Для оценки обструктивных изменений внеш­
него дыхания целесообразно использовать пневмотахометрические способы с учетом субъек­
тивного фактора: снижение функциональной
жизненной емкости до 60 % и уменьшение мак­
симальной скорости выдоха ниже 3 л/с указы­
вают на значительное уменьшение вентиляцион­
ных возможностей легких. Важным показателем
является соотношение скорости выдоха и вдоха.
Г. Плаушенене (1967) установила, что величи­
на этого соотношения соответствует изменениям
остаточного объема легких: если она снижа­
ется до 0,7—0,6, то остаточный объем легких
составляет 54 % от общей емкости, т. е. уровня,
при котором удаление части функционирую­
щей легочной паренхимы или даже временное
снижение легочной функции (торакотомия)
считается, непереносимым.
Достаточно информативной является оценка
связи между производными показателями ЖЕЛ
в процентах к должной и отношения макси­
мальной скорости выдоха к абсолютной вели­
чине ЖЕЛ, что позволяет определять тип и сте­
пень нарушения внешнего дыхания (рис. 54).
Определение МОД и КИОг мало дополняет
оценку спирограммы, хотя снижение КИОг до
20—25 при увеличении МОД следует рассмат­
ривать как предельное, при котором допустимо
оперативное вмешательство на легком.
При оценке показаний к вмешательству необ­
ходимо ориентироваться не только на выра­
женность обструктивных и рестриктивных из­
менений внешнего дыхания, но и на величину
дыхательного резерва (отношения ММВ к
МОД), а также на раздельное определение функ­
ции каждого легкого в ходе общей спирографии
латеральным тестом J. Bergan (1960), а иногда
и раздельной спирографией при сомнениях
в функциональной операбельности больного
[Гаврилова Н. И., Ребане Л. Е., 1967]. Резкое
снижение общей ЖЕЛ и незначительное уча­
стие в вентиляции непораженного легкого ста­
вят под сомнение возможность проведения
не только минимального по объему радикаль­
ного вмешательства, но даже и диагностиче­
ской торакотомии.
В сомнительных случаях необходимо еще
до операции определить показания к проведе-
100
I
II
0,4
МВЛ %
III
0,6
0,B
1,0
1,2
1,4 ЖЕЛ
Рис. 54. Диаграмма для определения вида и выраженности
нарушений внешнего дыхания (по Т. И. Черницкому, 1973).
I—III — степени рестриктивных нарушений; 1—3 — степени об­
структивных нарушений.
Рис. 55. Диаграмма для определения степени вентиляцион­
ных нарушений и функциональной операбельности по ин­
дексу вентиляции.
нию профилактической ИВЛ, используя моди­
фицированную гипервентиляционную пробу
[Шанин Ю. Н., Костюченко А. Л., 1975], или
даже применить «функциональную пульмонэктомию»: бронхоспирометрию с блокадой
соответствующего бронха и ветви легочной
артерии. Временная окклюзия бронхов поро­
лоновой пломбой позволяет производить «функ­
циональную резекцию» (нижняя доля, все лег­
кое) и оценивать переносимость вмешательства
в менее острой ситуации. Аналогичные задачи
позволяет решить использование искусственного
пневмоторакса (при незапаянной плевральной
щели), наложенного за 2—3 дня до предпола­
гаемой операции,— приема, хорошо известного
и незаслуженно забытого.
Эффективность легочного газообмена по
напряжению газов артериальной крови (РаОг
и Расо.) определяется за несколько дней до
оперативного вмешательства с тем, чтобы полу­
чить исходные данные, ориентируясь на кото­
рые можно оценивать состояние легочного га­
зообмена во время вмешательства или после
него. Для этого следует учитывать возрастную
норму для Раог по специальным формулам.
Наиболее корректна формула, предлагаемая
Н. В. Путовым и В. С. Щелкуновым (1978):
РаО! (мм рт. ст) = 102,6 — 0,32Х В, где В —
возраст больного. Следует отметить, что при
отсутствии очевидной причины гипервентиля­
ции (лихорадка, интоксикация) сочетание ги­
поксемии с гипокапнией указывает на значи­
тельное напряжение дыхания, а гипоксемия
даже с умеренной гиперкапнией (50 мм рт. ст.)
свидетельствует о явной недостаточности ле­
гочного газообмена и необходимости специ­
альной подготовки и лечения в послеопераци-
ИВ — индекс вентиляции (произведение МВЛ и ЖЕЛ в % к долж­
ным величинам); ПО — полная операбельность; УО — удовлет­
ворительная операбельность; СО — сомнительная операбель­
ность; ПНО — практически неоперабельны.
онном периоде, если показания к операции на
легких абсолютные.
Наиболее трудным является определение
ближайшего прогноза, когда выявленные функ­
циональные изменения дыхания не уклады­
ваются в те величины, которые названы пре­
дельными. При использовании различных пока­
зателей: спирографии, пневмотахографии, об­
щей плетизмографии и др.— как отечествен­
ные, так и зарубежные пульмонологи считают,
что ни один из тестов в отдельности и ни одна
из их комбинаций не дают разительных пре­
имуществ перед обычными клиническими мето­
дами определения функциональной операбель­
ности.
Вариантом решения такой задачи представ­
ляется подход, предлагаемый М. Я. Авруцким
и соавт. (1978), которые на основании данных
дооперационного обследования больных в со­
поставлении с послеоперационными оценками
состояния составили нелинейные шкалы инфор­
мативных показателей. Прогноз определяется
суммированием величины баллов: 3—4 балла
указывают на благоприятное течение после­
операционного периода; 4—8 баллов — на воз­
можность осложнений средней тяжести: более
9 баллов — на реальное развитие тяжелого
состояния из-за легочных осложнений с не­
состоятельностью дыхания. Прогноз совпадал
с послеоперационной оценкой в 2/з наблюдений.
Подобный подход предложили М. Ю. Репин
и И. Я. Цукерман (1980), которые прогнози­
101
руют функциональные исходы операций на
основании графического метода оценки основ­
ных показателей спирограммы, исходя из вы­
числения индекса вентиляции (ИВ), представ­
ляющего произведение процентных значений
ЖЕЛ и ММВ, отнесенных к должным вели­
чинам (рис. 55). Выделено пять степеней вен­
тиляционных расстройств. Номограмма одно­
временно позволяет определить исходный тип
этих нарушений: часть графика внизу и справа
от центрального сектора соответствует зоне
преимущественно обструктивных нарушений,
а вверху и слева от сектора — преимуществен­
но рестриктивным расстройствам. Если при
I—II степени ИВ летальный исход наблюдали
у 8,4 % больных, то при IV—V степенях ИВ
ниже уровня границ переносимости — 2/3 боль­
ных, несмотря на все меры интенсивной тера­
пии, включая вспомогательную ИВЛ. Повыше­
ние ИВ после курса специальной предопераци­
онной подготовки свидетельствует о возмож­
ности расширения показаний к операции, так
как объем ее не играет ведущей роли как фактор
риска. Более того, наименьший риск представ­
ляют пневмонэктомии, после которых выра­
женность нарушений легочного газообмена в
послеоперационном периоде будет меньше, чем
после лобэктомии (см. гл. 2).
ФУНКЦИОНАЛЬНОЕ СОСТОЯНИЕ
КРОВООБРАЩЕНИЯ
Наряду с определением функциональной
операбельности по состоянию внешнего дыха­
ния важно также оценить компенсаторные воз­
можности системы кровообращения: сократи­
тельную способность миокарда, степень пато­
логических изменений сосудистой системы как
в целом, так и в отдельных ее бассейнах (в малом
круге, коронарное, мозговое кровообращение).
У ряда больных до операции выявляется так
называемая энергодинамическая недостаточ­
ность миокарда, которая возникает в связи с глу­
бокими нарушениями обмена в мышце сердца
под влиянием раковой или гнойной интоксика­
ции, гипопротеинемии, анемии и гипокалиемии.
Появление значительной одышки при подъеме
по лестнице у больного с отсутствием выражен­
ных расстройств вентиляции и газообмена
позволяет заподозрить именно такой вариант
недостаточности кровообращения. Более точ­
ные доказательства ее дает проба с дозирован­
ной физической нагрузкой на велоэргометре:
удлинение более чем на 9 мин времени восста­
новления исходной величины МОД, КИОг и
выделения углекислого газа. Если период вос­
становления этих показателей превышает 12 мин,
то резекция легких непереносима [Bie N. et al.,
1960].
Застойная сердечная недостаточность в анам­
незе или непосредственно в предоперационном
периоде обязывает к углубленному изучению
ее причин и выяснению возможностей ее устра­
нения.
Если наблюдавшаяся в свое время сердеч­
ная недостаточность была обусловлена гипер­
тонической болезнью или ишемической болезнью
сердца и ее удавалось устойчиво компенсиро­
вать медикаментозной терапией, то можно на­
деяться на возможность предотвращения реци­
дива сердечной недостаточности рационально
спланированным интенсивным лечением. Высо­
кая артериальная гипертензия в момент осмот­
ра не является противопоказанием к вмеша­
тельству по поводу заболевания легких и плев­
ры, так как в определении операционного риска
имеет значение не только первоначальный уро­
вень системного АД, но особенно его снижение
под влиянием терапии, включающей гипотен­
зивные средства, транквилизаторы, ограниче­
ние соли в пище, салуретики.
Если недостаточность кровообращения про­
текала прежде с декомпенсацией по типу пра­
вожелудочковой недостаточности в результате
хронического легочного заболевания, то внутригрудное вмешательство и удаление части сосу­
дистой сети малого круга еще больше нарушат
кровообращение в нем и неизбежно вызовут
рецидив недостаточности. Выраженная право­
желудочковая недостаточность является основ­
ным проявлением «хронического легочного
сердца» и давно считается противопоказанием
к резекции значительного объема легочной
паренхимы [Муравьев М. В. и др., 1961; Апсит С. О. и др., 1965]. В стадии компенсации
и субкомпенсации признаки правожелудочко ­
вой недостаточности выявляются при исследо­
вании показателей внешнего дыхания.
Более точно выраженность легочной гипертен­
зии определяют прямым исследованием давле­
ния в системе легочной артерии, к которому
следует прибегать при сниженных резервах
дыхания, электрокардиографических признаках
перегрузки правого сердца и при таком распро­
странении процесса в легком, по поводу кото­
рого необходима значительная по объему час­
тичная резекция или пневмонэктомия. W. Adams
и соавт. (1962) установили, что больные со
средним легочным артериальным давлением
выше 30 мм рт. ст. могут перенести операцию
такого объема только при полной гарантии не­
осложненного течения послеоперационного
периода. Н. В. Антелава и соавт. (1968) пришли
к выводу, что если после нагрузки среднее дав­
ление в легочной артерии поднимается выше
50 мм рт. ст., показания к распространенной
резекции следует ставить с особой осторожно­
стью. W. Hartel и соавт. (1970) установили зна­
102
чение не только подъема, но и нормализации
уровня легочного давления: замедленный воз­
врат к исходному уровню после значительного
подъема всегда указывает на необходимость
возможного сокращения объема вмешатель­
ства.
Электрокардиография дополняет данные кли­
нического обследования, позволяет уточнить
диагноз ишемической болезни сердца и наличие
склеротических изменений в миокарде. Однако
данные электрокардиографии, свидетельствую­
щие об очаговых изменениях в миокарде и пост­
инфарктных рубцах, далеко не всегда являются
основанием для отказа от обширного внутригрудного вмешательства. Они указывают на
вероятность развития выраженной циркулятор­
ной гиподинамии с угнетением сократительной
способности и нарушениями трофики миокарда,
но при соответствующей предоперационной
подготовке, анестезиологическом пособии и
послеоперационном лечении тяжесть операции
у больных с отчетливой ишемической болез­
нью существенно не отражается на ее непо­
средственном исходе [Шанин Ю. Н., Костю­
ченко А. Л., 1975; Лебедева Р. Н. и др., 1977].
Недостаточность кровообращения мозга,
перенесенные ранее инсульты значительно по­
вышают риск оперативного вмешательства
даже средней тяжести, особенно если опера­
ция проводится на стороне ранее перенесенного
пареза. Стабильность кровообращения по ходу
вмешательства, послеоперационная терапия
с достижением адекватной оксигенации, пред­
отвращением циркуляторной гиподинамии,
снижением системного АД и выраженной гипер­
коагуляции уменьшают опасность повторных
нарушений мозгового кровообращения, однако
гемипарез с нарушением функции дыхательных
мышц является противопоказанием к резекции
легких даже при относительно мало изменен­
ных показателях внешнего дыхания.
Однократное исследование минусного объема
кровообращения (МОК) методом Фика или
одним из методов разведения индикатора (кра­
ски, меченного радионуклидами альбумина или
терморазведения) мало что добавляет к оценке
гемодинамики у обследуемых больных. Тем
не менее его определение оправдано в экстрен­
ных ситуациях (травма легкого, легочное кро­
вотечение, прогрессирующая гангрена легких),
когда гемодинамика особенно неустойчива.
Интегральная реография тела по М. И. Ти­
щенко позволяет более глубоко оценить резер­
вы гемодинамики.
Кроме возможности оценить в плане пред­
операционного обследования реакцию кровооб­
ращения (УО, частота пульса, МОК) на дози­
рованную физическую нагрузку (10 раз сесть
из положения лежа в произвольном темпе),
метод позволяет выяснить состояние тонуса
сосудов большого круга кровообращения (по
коэффициенту интегральной тоничности),
определить наличие повышения резистентно­
сти сосудов малого круга и степень задержки
воды в организме, а также оценить степень
гемодинамической обеспеченности недостаточ­
ности внешнего дыхания [Колесников И. С.
и др.].
По мере нарастания нарушений внешнего
дыхания увеличивается сердечная недостаточ­
ность (за счет снижения УО). Вероятно, эти
изменения обусловлены перегрузкой правого
желудочка, так как параллельно им нарастают
качественные проявления легочной гипертен­
зии. Гипердинамический эффект расстройств
дыхания выявляется у части больных с умерен­
ными изменениями, но на фоне других факто­
ров повреждения миокарда (при гнойной инто­
ксикации, например) он уступает место сердеч­
ной недостаточности, особенно при переходе
к выраженным изменениям внешнего дыхания.
Заслуживает внимания повышение сис тем­
ного артериального тонуса, которое у больных
с длительно текущими заболеваниями легких
наступает заметно чаще, чем сердечная недо­
статочность, что подтверждает правильность
представлений о существовании «пульмоногенной» артериальной гипертензии [Мухарлямов А. М. и др., 1974]. При выраженных нару­
шениях внешнего дыхания, компенсированных
кровообращением, уровень системного объем­
ного кровотока (МОК) у больных в 1,5—1,9 раза
превышает их индивидуальные нормальные
величины.
По мере углубления дыхательных расстройств
увеличивается неравномерность значений удар­
ного объема по его изменениям внутри дыха­
тельного цикла — коэффициенту дыхательных
изменений (КДИ), отношению наибольшего
УО к наименьшему.
В оценке наблюдаемых взаимосвязей дыха­
ния и кровообращения особого внимания заслу­
живает показатель напряженности дыхания,
который представляет собой произведение ча­
стоты дыхания на коэффициент дыхательных
изменений У О. При умеренной напряженности
внешнего дыхания этот показатель более 26,5,
а в случаях выраженной напряженности он
превышает 36,5. Есть основание полагать, что
показатель напряженности дыхания косвенно
характеризует увеличение энерготрат на работу
дыхания.
На основании кросс-корреляционного ана­
лиза связанных изменений показателей внеш­
него дыхания и гемодинамики наибольший
интерес представляют взаимосвязи Ж ЕЛ и КДИ,
резерва дыхания (РД — отношения ММВ к
МОД) и коэффициента резерва гемодинамики
103
ЖЕЛ
ДЖЕЛ
1. ЖЕЛ = 240- 116 ИДИ
100 80 60 -
40 20
>
....................................... ....... I
I
I
I
I
I
I
I
I—J—I—I—I-------------
1,20 1.30 1,40 1,50 1,60 1.70 1,80 1,90 2,00 2,10
ИДИ
Рис. 56. Уравнение ,инейной регрессии, выражающее связь
ЖЕЛ — КДИ.
1 — у больных раком легкого; 2 — у больных хроническим на­
гноением легкого; 3 — у больных острыми гнойно-деструктив­
ными заболеваниями легких.
Рис. 57. Уравнение линейной регрессии, выражающее связь
резерва дыхания (РД) и коэффициента гемодинамического
резерва (КР).
1 — у больного раком легкого;" 2 — у больного хроническим на­
гноением легкого; 3 — у больного острым гнойно-деструктив­
ным заболеванием легкого.
(КР отношения МОК к должному). На основа­
нии проведенных исследований появилась воз­
можность количественно характеризовать ука­
занные взаимосвязи с помощью уравнений ли­
нейной регистрации для каждой из основных
групп заболеваний легких: рак, хронические не­
специфические заболевания и острые гнойно­
деструктивные процессы в легких [Колесни­
ков И. С. и др., 1982]. Раздельные графические
изображения корреляционных связей ЖЕЛ-КДИ
и РД-КР (рис. 56) могут быть использованы в ка­
честве номограмм для приблизительного (с уче­
том доверительного интервала) вычисления
значения одного из взаимосвязанных показа­
телей по величине другого в соответствующих
группах больных. Практический смысл урав­
нений ЖЕЛ-КДИ заключается в том, что, рас­
полагая только данными интегральной реографии, можно на основании КДИ косвенно
оценить степень снижения ЖЕЛ. Зная величину
резерва дыхания данного больного, можно
рассчитать величину гемодинамического резер­
ва (рис. 57), необходимого для компенсации
имеющейся дыхательной недостаточности.
Если фактическое значение КР конкретного
больного меньше математически ожидаемого,
то это дает возможность не только констатиро­
вать «легочное сердце», но и оценить степень
декомпенсации кровообращения.
Специальные исследования, проведенные
у различных категорий больных, показали,
что устойчивость системы кровообращения по
отношению к неблагоприятным воздействиям
анестезии и операции определяется достаточ­
ностью объема циркулирующей крови (ОЦК) и
его компонентов: плазмы (ПО) и эритроцитов
(ЭО). Значительное снижение ОЦК с уменьше­
нием ЭО и содержания плазменного белка по­
вышает чувствительность гемодинамики к раз­
личным факторам операции и послеоперацион­
ного стресса с падением сердечного выброса
и нарушением кровообращения на уровне микро­
сосудов. Более редким волемическим расстрой­
ством является гиперволемия. Превышение
величины ОЦК на 20 % и более может зависеть
от право желудочковой недостаточности и долж­
но учитываться при определении функциональ­
ной операбельности как один из признаков «ле­
гочного сердца» [Балезина 3. Н. и др., 1978].
У больных без отчетливых функциональных
нарушений кровообращения и явлений интокси­
кации отклонения ОЦК составляют примерно
10%, преимущественно за счет ЭО. Изменения
в сторону гиповолемии такой степени выражен­
ности характерны для физиологической гипо­
волемии пожилых [Haxbe J., 1969]. Однако и
более значительный дефицит ОЦК не следует
считать патологией, он не всегда является пока­
занием к немедленной трансфузионной кор­
рекции. Величина ОЦК у здоровых и малоисто­
щенных больных в пожилом возрасте при гипо­
динамии и хроническом нагноении легких в ста­
дии ремиссии может отличаться от «должной»,
так как циркуляторный гомеостаз переходит
у них на другой уровень функционирования.
Сочетание гиповолемии со значительным
дефицитом циркулирующего гемоглобина явля­
ется неблагоприятным признаком: при раке
легких это один из косвенных признаков рас­
пространенности процесса. Нарастание гипово­
лемии, несмотря на попытки уменьшить вред­
ное воздействие патологического процесса в
легком средствами общей и местной детокси­
кации, усиленным питанием, устойчивость к
трансфузионной коррекции этих расстройств,
является показанием лишь к паллиативной опе,рации или даже выполнению ее в несколько эта­
пов.
104
ВОДНО-ЭЛЕКТРОЛИТНОГО ГОМЕОСТАЗА
В случаях волемических расстройств при
заболеваниях легких обычно наблюдаются
изменения и водно-электролитного равнове­
сия, в значительной степени снижающие сокра­
тительную способность миокарда, усложняющие
коррекцию гипопротеинемии и санацию брон­
хиального дерева. Эти изменения могут стать
одной из причин нарушений легочного газообме­
на и кровообращения во время операции или
сразу после нее.
При оценке операбельности и подготовлен­
ности больного по этим критериям следует ори­
ентироваться на результаты исследования кон­
центрации основных электролитов в плазме цир­
кулирующей крови и в моче.
На фоне хирургических заболеваний легких
и плевры, особенно гнойно-деструктивных,
отмечается расширение внеклеточного жидкост­
ного пространства организма (преимуществен­
но его интерстициального сектора) со сниже­
нием концентрации натрия, несмотря на за­
держку его ионов в организме.
Регрессия воспаления под влиянием эффек­
тивного лечения сопровождается восстановле­
нием плазменной концентрации натрия. Пока­
затели концентрации других естественных осмо­
тически активных веществ (глюкозы и моче­
вины) сохраняются примерно на одном уровне
на всех этапах заболевания. Поэтому одновре­
менно с гипонатриемией отмечается и сниже­
ние осмоляльности, хотя задержка натрия в
организме отчетлива. Синдром гипоосмии, обус­
ловленной гипонатриемией в сочетании со сни­
жением экскреции натрия с мочой и одновре­
менным расширением внеклеточного простран­
ства, характерен и для ряда невоспалительных
заболеваний легких.
При этом необходимо учитывать факт, что
с возрастом постепенно ослабевают энергети­
чески зависимые процессы, поддерживающие
ионную асимметрию в организме: калий —
преимущественно в клетках, натрий — во вне­
клеточном жидкостном пространстве. Нара­
стает тенденция к перемещению калия во вне­
клеточную жидкость с потерей его ионов через
почки, а натрий поступает в клетки [Шве­
дов К. И., Крохалев А. А., 1968]. Процесс транс­
минерализации усиливается при нарушении
биоэнергетики клеток (при гипоксии, гнойной
интоксикации, лихорадке, истощении).
Клиника недостаточности вну гриклеточного
калия выявляется при крайних степенях дефи­
цита его ионов в организме (снижение калийуреза) на фоне длительного голодания и интен­
сивных потерь с мокротой и гнойным плевраль­
ным экссудатом. Электрокардиографические
снижением концентрации калия в плазме: при
умеренном дефиците ионов К наблюдают сни­
жение интервала S — Т ниже изолинии, удли­
нение Q — Т, уплощение и инверсию зубца Т.
Участие калия в тканевых энергетических и
синтетических процессах сказывается и на из­
менениях циркуляторного гомеостаза.
В. В. Мазинову (1971) удалось показать су­
ществование высокой зависимости между дефи­
цитом ОЦК и концентрацией калия в плазме
и эритроцитах при длительном течении забо­
левания легких. Значительное снижение содер­
жания калия в плазме соответствует дефициту
его ионов в организме, тогда как нормальная
или даже повышенная концентрация еще не
исключает дефицита. Исследование в таких
случаях внешнего баланса калия по калийурезу
после пероральной нагрузки 4,5—6 г калия хло­
рида (60—80 ммоль) в сочетании с определе­
нием трансмембранного потенциала эритроци­
тов по калию (отношение калия в эритроцитах
к калию в плазме) позволяет более точно выя­
вить дефицит К+. У больных с хирурги­
ческими заболеваниями легких он встречается
чаще, чем регистрируется при исследовании
ионограммы плазмы.
Иногда дефицит внутриклеточного калия
сочетается с дефицитом других внутриклеточ­
ных ионов, например магния. Диагностика
этого нарушения гомеостаза еще более трудна,
тогда как роль магния в процессах жизнедея­
тельности не уступает значению калия. При
дефиците магния в организме ухудшается син­
тез белка, нарушая восстановление белкового
равновесия, снижаются утилизация глюкозы в
мышцах и эффективность мышечного сокра­
щения, функционирования мукоцилиарного
эскалатора.
Нарушения содержания электролитов при
заболеваниях легких и плевры нередко соче­
таются с расстройствами кислотно-основного
состояния. Только в случаях острейших состо­
яний (кровотечение) или при значительных
нарушениях функции почек (амилоидоз) они
протекают по типу недыхательного ацидоза.
Более часто возникает недыхательный, мета­
болический алкалоз, что связано с нарушением
кислородного обеспечения организма.
СОСТОЯНИЕ ПИТАНИЯ
И БЕЛКОВОГО ОБМЕНА
Основным внешним проявлением белковой
недостаточности считаются анемия и гипопро­
теинемия с характерной диспротеинемией в виде
уменьшения содержания альбуминов и повыше­
ния a-фракций глобулинов, а по мере развития
заболевания — у-фракций, что особенно четко
105
выявляется в концентрационном выражении
(в г/л плазмы). При сохраненном энтеральном
поступлении белка и отсутствии значительных
внесосудистых потерь протеинов (экссудат,
мокрота) основными факторами, от которых
зависит выраженность гипоальбуминемии,
считаются тяжесть и длительность существо­
вания патологического процесса в легком, по
поводу которого выполняется операция.
В возникновении и прогрессировании белко­
вой недостаточности имеют значение повыше­
ние проницаемости капилляров, ускорение рас­
пада лабильных белков в условиях воспаления
и опухолевого роста, потери белка с экссудатом.
Одновременно снижается темп наработки аль­
бумина из-за недостаточности энтерального
поступления пищевого белка (снижение аппети­
та) и непосредственного нарушения белоксинтезирующей функции печени. Снижение кон­
центрации альбумина сопровождается повы­
шением концентрации си- и особенно И2-глобулинов и входящих в состав этих фракций гли­
копротеидов. Динамика содержания у-глобулинов (фибриногена, участвующего в процессах ге­
мостаза и репарации; пропердина и комплемен­
та, играющих важную роль в формировании не­
специфического иммунитета; специфических
иммуноглобулинов и т. д.) отражает состояние
защитной реакции организма. В силу перерас­
пределения белковых фракций величины кон­
центрации и содержания общего белка могут
оказаться нормальными, несмотря на прогрес­
сирующий деструктивный процесс в легком
[Федоров Б. П., Воль-Эпштейн Г. Л., 1976; Лесницкий Л. С., 1984].
Полное представление о степени декомпенса­
ции белкового обмена можно получить, зная
абсолютные величины содержания плазмен­
ных белков, так называемую массу циркули­
рующего белка, а также отношение концентра­
ции аг- и у-глобулинов к концентрации альбу­
мина.
Гипоальбуминемия порядка 30 г/м2 свидетель­
ствует о тяжелой белковой недостаточности,
особенно если она сочетается с признаками
энергетической несостоятельности организма
(пониженная концентрация холестерина сыво­
ротки, низкая активность сывороточной холин­
эстеразы, снижение выделения рибофлавина
с мочой и пр.). При уровне альбумина плазмы
в 20 г/м2 (норма — 50 г/м2) больные гангре­
ной легких еще переносят радикальные вме­
шательства, но погибают от многочисленных
осложнений, несмотря на заместительную тера­
пию альбумином (по 30—50 г/сут на протяже­
нии первых 3—5 дней). По величине абсолют­
ной концентрации белков плазмы можно судить
о водоудерживающей функции плазменного
белка, поскольку 1 г альбуминов удерживает
16 мл воды, air глобулинов — 7 мл [Lindenschmidt S., Cartensen О., 1966].
Использование такого подхода при оценке
состояния белкового обмена больного с заболе­
ваниями легких и плевры во многом раскры­
вает динамику волемических изменений в слу­
чаях отностельно медленного течения заболе­
вания — когда каждому уровню диспротеинемии соответствует определенное состояние
ОЦК и его компонентов. В стадии белкового
истощения и декомпенсации белкового обмена
снижаются концентрация и содержание фибри­
ногена, что может сказаться на коагуляционной
активности крови.
СИСТЕМА ГЕМОСТАЗА
И ЭНДОКРИННЫЙ ФОН
При изучении анамнеза и обследовании боль­
ного следует выяснить, нет ли признаков ге­
моррагического диатеза (частые носовые кро­
вотечения, значительные подкожные кровоиз­
лияния при легких ушибах и т. п.). Исследова­
ние коагулограммы при заболеваниях легких
и плевры считаем правилом; оно включает опре­
деление количества тромбоцитов, времени свер­
тывания крови или рекальцификации плазмы,
концентрации факторов протромбинового
комплекса и фибриногена, активности фибри­
назы (фХШ), уровня спонтанного фибрино­
лиза. При более углубленном обследовании
стандартную коагулограмму желательно до­
полнить исследованием концентрации гепарина
в крови, продуктов деградации фибрина. Сниже­
ние уровня протромбина до 60 % и ниже, низкий
уровень фибриногена (ниже 2 г/л и 3 г/м2
поверхности тела больного), активность фиб­
риназы менее 40 с говорят о том, что больной
находится в состоянии гнойного истощения
и декомпенсации, при которых опасность кро­
вотечения во время и после операции весьма
реальна. Сдвиг в сторону гиперкоагуляции,
наблюдающийся у большинства больных раком
легких и гнойно-деструктивными заболева­
ниями: высокий уровень протромбина, концент­
рация фибриногена выше 8 г/л, снижение со­
держания гепарина и предельное угнетение
фибринолиза — должен настораживать в отно­
шении тромботических осложнений, особенно
при наличии хронического тромбофлебита.
Обязательно следует оценить состояние вен
нижних конечностей, патологические измене­
ния которых (варикозная болезнь, тромбофле­
бит в анамнезе) предрасполагают к возникно­
вению тромбоэмболических осложнений. Сте­
пень тромбоопасности может быть уточнена
жгутовой пробой Б. А. Кудряшова [Дедкова Е. М., Лукомский Г. И., 1969]. Отсутствие
повышения спонтанного фибринолиза и кон­
106
центрации гепарина в крови, взятой из вены лок­
тевого сгиба после венозного застоя под жгу­
том в течение 15 мин, позволяет считать такого
больного «тромбоопасным» при прочих ослож­
няющих факторах и заставляет заранее наме­
тить план профилактики неизбежной патоло­
гической гиперкоагуляции после обширного
вмешательства на легких и плевре.
Функциональная операбельность в определен­
ной степени может определяться эндокринным
статусом больного, что требует клинической
оценки и соответствующих медикаментозных
воздействий. Тяжелый гипертиреоз с психиче­
скими и висцеральными проявлениями необ­
ходимо уменьшить до допустимых пределов
лекарственными воздействиями при плановом
вмешательстве, и необходимо быть готовым к
профилактике и лечению гипертиреоидного
криза в ходе срочного вмешательства с помощью
дроперидола, 6-блокаторов и глюкокортикои­
дов.
Среди других нарушений, сопутствующих
заболеваниям легких и плевры, следует выяв­
лять скрытую надпочечниковую недостаточность,
которая может проявиться иногда только на
фоне стресса. Обычно ей способствуют деструк­
ции в области надпочечников (туберкулез, ме­
тастаз опухоли легкого) или хроническое ле­
гочное нагноение с длительной интоксикацией.
Значительное уменьшение массы тела больного,
анорексия и мышечная слабость, быстрая
утомляемость, пигментация кожи щек, век,
тыльной поверхности пальцев, необычная для
пожилого возраста артериальная гипотензия
и тахикардия, упорные запоры позволяют за­
подозрить поражение надпочечников. Пред­
положение подтверждается низкой концентра­
цией натрия и хлора в плазме, повышением
плазменной, а иногда и эритроцитарной кон­
центрации калия, низким содержанием 17-оксикортикостероидов в крови и 17-кетостероидов в моче. Разительное уменьшение симптомов
при пробном введении гидрокортизона еще
больше подтверждает их надпочечниковую при­
роду и обязывает быть готовым к необычным
изменениям состояния больного во время вме­
шательства и в послеоперационном периоде.
Сахарный диабет изменяет течение легоч­
ного заболевания, особенно если оно осложня­
ется гнойной инфекцией. Очаг гнойной деструк­
ции в легком вызывает декомпенсацию диабета,
что неблагоприятно сказывается на обменных
процессах, замедляя репарацию и регенерацию
тканей [Генес С. Г., 1968; Соколовский В. Д.,
1968, и др.]. В условиях диабета даже ограни­
ченный гнойный процесс протекает с повыше­
нием температуры тела до 39-4-40° С, высокой
гипергликемией (12 ммоль/л), глюкозурией и
кетонурией. Порочный круг иногда становится
настолько прочным, что компенсации диабета
(а иногда и ликвидации кетоацидоза) можно
добиться только при устранении очага инфек­
ции в легком. У больного диабетом раковая
опухоль увеличивается относительно быстрее
при одновременном снижении гипергликемии
и глюкозурии, смягчении основных проявлений
эндокринопатии, но при прогрессировании рас­
стройств гомеостаза в виде выраженной гипо­
калиемии, диспротеинемии, причем степень
гипокалиемии имеет значение при решении
операбельности больных. Учитывая нарастание
частоты скрытого диабета с возрастом, исследо­
вание уровня гликемии и глюкозурии должно
быть правилом при планировании обследования
больных с хирургическими заболеваниями лег­
ких и плевры. Рак легких может вызывать и
другие эндокринопатии, которые иногда явля­
ются масками неопластического процесса, на­
пример миастеноподобный синдром или состоя­
ние, напоминающее несахарный диабет с высо­
кой полиурией и стойкой гипонатриемией.
Установлено, что, кроме типичных эндокрин­
ных заболеваний, которые нередко диагностиру­
ются у таких больных задолго до клинических
проявлений опухолевого роста, необходимо
учитывать и возможность эндокринопатий, ко­
торые связаны с самим заболеванием (чаще
всего злокачественным) и приводят к так назы­
ваемому карциноматозному гормоногенезу
[Ross J., 1980]. Гормоны, выделяемые опухо­
лями легких, бронхов и плевры, в таких случаях
не только систематически определяются в кро­
ви, но их уровень резко снижается при успешном
лечении заболевания с помощью хирургиче­
ского вмешательства, лучевой терапии или цито­
токсических препаратов. Частота эндокринопа­
тий такого типа может достигать 10 %, но кли­
нически выраженные проявления наблюдаются
значительно реже.
Гиперсекреция опухолью легких кортикотро­
пина (АКТГ) проявляется локализованными
отеками в области локтей и лодыжек, иногда—
артериальной гипертензией в связи с задерж­
кой натрия, мышечной слабостью из-за усилен­
ной экскреции калия. Избыток циркулирующе­
го кортизола приводит к гипергликемии и глю­
козурии, иногда — к изменению поведения
больного, которое может прогрессировать вплоть
до выраженного психоза. Кардинальным био­
химическим признаком «эктопического АКТГсиндрома» является гипокалиемический алка­
лоз как результат интенсивных потерь калия
с мочой и калом. Плазменная концентрация
кортизола постоянно высокая и продолжает
нарастать по мере развития опухоли легких,
достигая уровня, заведомо (в 3—4 раза) выше
той, которую наблюдают при классическом
синдроме Иценко — Кушинга (200 мкг/л). Ко­
107
лебания уровня кортизола на протяжении суток,
характерные для обычного состояния надпо­
чечников, у больных с опухолями легких отсут­
ствуют [Буравцов В. И„ 1976].
Другой тип карциноматозного гормоногенеза связан с выделением активных субстанций,
напоминающих антидиуретический гормон
(АДГ), что приводит к неспособности экскрети­
ровать воду и может привести к водному «отрав­
лению». Клиника этого синдрома состоит в про­
явлениях гипергидратации клеточного и внекле­
точного жидкостных пространств, но особенно
четко проявляется в отношении мозга: его нара­
стающий отек приводит к психическим наруше­
ниям, повышенной возбудимости, затем к ле­
таргии, а в последующем — к судорогам, мозго­
вой коме и смерти. Так как плазменный компо­
нент крови обычно увеличен, у больных не бы­
вает нарушений гемодинамики, как при натрие­
вом истощении. Наоборот, артериальное дав­
ление часто повышено. Ключом к диагнозу в
этих случаях является обнаружение гипонатри­
емии разведения, которая зависит скорее от
задержки воды, чем от потерь натрия, так харак­
терных для надпочечниковой недостаточности.
Все концентрационные константы плазмы сни­
жены: уровень натрия, хлора, мочевины, креати­
нина. Осмолярность плазмы низкая (ниже
270 мосмомоль/л), тогда как в моче этот пока­
затель значительно выше (350 мосмомоль/л).
Клубочковая фильтрация почек остается нор­
мальной или даже превышает нормальный уро­
вень. Полипептид, повышающий активность
АДГ в плазме крови и пунктатах опухоли, иден­
тичен гипоталамическому аргинин-вазопрессину. Состояние таких больных можно улучшить
или даже вернуть их к привычным бытовым
нагрузкам введением больших доз (2—10 мг
в день) ингибитора АДГ-флюрогидрокортизона, особенно при одновременном введении пре­
паратов калия.
Паратиреоидный тип карциноматозного гормоногенеза опухолью легкого имеет типичные
клинические признаки избытка этого гормона.
Гиперкальциемия, как правило (в отличие от со­
стояний, связанных с метастазами в кости),
сочетается с гипофосфатемией без повыше­
ния активности щелочной фосфатазы. Клини­
ческие проявления эндокринопатии этого типа
обычны для гиперкальциемии любого проис­
хождения, а именно: жажда, полиурия и никту­
рия в сочетании с мышечной слабостью и гипо­
тонией, миоклонус, анорексия, схваткообраз­
ные боли в животе, рвота и запоры, психиче­
ские расстройства вплоть до выраженного пси­
хоза. Гормоноподобная субстанция, которая
выделяется опухолью легких, не идентична (по
молекулярному строению) той, которая секре­
тируется паращитовидными железами. Она пред­
ставляет полипептидную цепь из 84 аминокис­
лот (паратгормон — полипептидная цепь кото­
рого состоит всего из 34 аминокислот). Следует
отметить, что гиперкальциемия может наблю­
даться ■ и при отсутствии эктопического гормоногенеза, например при избыточной секреции
простагландинов Е или витамин D-подобной
субстанции.
Более редко обнаруживаются другие эндокрйнопатии, например гипертиреоидизм с типич­
ной клиникой потери массы тела, несмотря на
повышение аппетита, непереносимостью тепла,
нервозностью и раздражительностью, жаждой,
мышечной слабостью и тахикардией, которые
корригируются ингибиторами типа мерказолила. Спонтанная гипогликемия более характерна
для опухолей, в основном мезенхимального
происхождения, включая фибросаркому, лейо­
миосаркому и другие новообразования разных
типов. Около 25 % этих опухолей локализуются
в пределах плевральной полости, но такого рода
эндокринопатия может возникнуть и при пло­
скоклеточном раке легких с ороговением. Повидимому, снижение активности диабета при
других формах рака легких связано с усиленной
продукцией опухолевой тканью инсулиноподоб­
ных субстанций. Все эти данные должны учи­
тываться при обследовании больных, и оконча­
тельное решение об операбельности может
быть принято после консультации эндокрино­
лога, знакомого с клиникой опухолевых эндокринопатий.
ЭНДОГЕННАЯ ИНТОКСИКАЦИЯ
И ФУНКЦИОНАЛЬНАЯ ОПЕРАБЕЛЬНОСТЬ
Наиболее часто значение имеет интоксикация
инфекционного происхождения (при гнойно­
деструктивных процессах в легочной паренхи­
ме или в плевре), которая обусловлена не только
недостаточной дезактивацией и накоплением
в очагах деструкции токсинов бактерий, грибов
или вирусов, но и токсическим воздействием
продуктов распада легочной ткани, изменившей­
ся регуляцией уровня биологически активных
веществ в крови (серотонина, гистамина, кини­
нов и пр.). В связи с этим проявляются сово­
купно или доминируют в отдельности три основ­
ных фактора: деструкции, резорбции и потери.
Последний фактор (потери с мокротой, гной­
ным плевральным экссудатом) приводит к тому,
что вне соответствующих терапевтических и
хирургических воздействий на очаг нагноения
синдром гнойно-резорбтивной лихорадки может
перейти в синдром гнойно-резорбтивного исто­
щения и хирургическое вмешательство в этой
фазе окажется непереносимым. Взаимодействие
перечисленных факторов характеризуется зна­
чительным возрастанием процессов катаболиз­
108
ма [Лукомский Г. И. и др., 1982]. В условиях
своевременного местного лечения и вспомога­
тельного парентерального питания наибольшее
значение в выраженности эндогенной интоксика­
ции приобретают факторы резорбции.
В клинической практике глубину интоксика­
ции определяют по психоэмоциональному ста­
тусу больного (по эйфории, возбуждению или
угнетению), по выраженности тахипноэ и та­
хикардии, особенно при субнормальной вели­
чине ОЦК и МОК, если эти проявления не обус­
ловлены значительным нарушением легочного
газообмена. Существенным критерием глубины
может быть лейкоцитарный индекс интоксика­
ции [Кальф-Калиф Я. Я., 1947; Волков В. Е„
1983].
Другим ориентиром выраженности интокси­
кации считаются признаки нарушений функций
печени по общедоступным биохимическим те­
стам — содержанию сывороточных белков и
фибриногена, активности факторов протромби­
нового комплекса, степени билирубинемии и
ее фракционному составу, по активности транс­
аминаз (с определением отношения Ас АТ/
АлАТ), альдолазы. В отличие от других кате­
горий хирургических больных активность
щелочной фосфатазы отражает преимущест­
венно степень деструктивного процесса в лег­
ком, чем поражение печени [Колесников И. С.
и др., 1983].
Наряду с нарушениями антитоксической
функции печени на течение интоксикации, осо­
бенно при прогрессирующем развитии патоло­
гического процесса в легком, существенно вли­
яют нарушения выделительной функции почек.
Гломерулонефрит и уремия в анамнезе, пиело­
нефрит, изостенурия и никтурия должны учи­
тываться при составлении плана обследования
больного. Низкая относительная плотность
мочи в сочетании с патологическими включе­
ниями в мочевом осадке (протеинурия, цилиндрурия) в предвидении тяжелого хирургического
вмешательства служат показанием для углуб­
ленного исследования функции почек (проба
Зимницкого, исследование парциальных функ­
ций почек и др.). При этом следует учитывать,
что значительные нарушения функции почек
несвойственны даже больным гангреной легких,
а изменения анализа мочи, которые выявля­
ются, неспецифичны.
Считается, что деструктивный процесс в лег­
ком создает все условия для избыточного на­
копления в организме осмотически активных
метаболитов (исходя из действия фактора ре­
зорбции), что приводит к возникновению зна­
чительных нарушений осмоляльности наряду
с существенными расстройствами водно-элек­
тролитного обмена [Шаталюк Б. П., Черно­
бровый Н. П., 1970; Путов Н. В. и др., 1977].
Рис. 58. Состояние азотовыделительно и функции почек
по клиренсу эндогенного креатинина (1) в мл/мин и по
клиренсу мочевины (2) в % к должной величине. Зависи­
мость от фазы воспалительного процесса в легких.
А — острое воспаление; Б — разрешение воспаления; В — оста­
точные явления.
Проведенные в нашей клинике исследования
[Костюченко А. Л. и др., 1983] привели к заклю­
чению, что на фоне острой фазы нагноительного процесса в легком или плевре в циркули­
рующей крови практически отсутствуют осмо­
тически активные метаболиты, хотя их наличие
можно предположить, учитывая интенсивный
процесс тканевой деструкции. При появлении
же в связи с нагноением изолированного жид­
костного пространства (плевральный экссудат)
содержание осмотически активных метаболи­
тов в экссудате возрастает в 4 раза. Наличие
их в плевральной полости и отсутствие их в
циркулирующей крови позволяют предполо­
жить, что организм больного активно освобож­
дается от этих метаболитов, используя наибо­
лее обычный путь детоксикации — через почки.
При отсутствии олигурии почки удовлетвори­
тельно справляются с ролью регулятора внут­
ренней среды, хотя содержание мочевины и
натрия в моче в острой фазе существенно ниже,
чем при разрешении нагноения, особенно в фазе
остаточных явлений. Таким показателем изме­
нения содержания осмотически активных ве­
ществ, как и для крови, считаем разницу между
рассчитанной по соответствующим формулам
и измеренной осмоляльностью мочи (рис. 58).
Косвенным подтверждением усиленной экскре­
ции продуктов тканевого распада по мере их
поступления во внутреннюю среду является
низкий клиренс осмотически свободной воды
(менее 1 мл/мин) на фоне острой фазы нагно­
ения, тогда как фильтрация и клиренс моче­
вины остаются в пределах нормальных вели­
чин (рис. 59).
109
Рис. 59. Состояние азотовыделительной функции почек
по осмотическому клиренсу (Cosm) и клиренсу осмотически
свободной воды (Сн,о) в зависимости от фазы воспалитель­
ного процесса в легких.
Обозначения те же. что и на рис. 58.
Такая интерпретация проведенных исследо­
ваний не означает, что почки не повреждаются
при сохранении эндогенной интоксикации. У не­
которых больных гангреной легких клубочко­
вая фильтрация падает до критических вели­
чин (20—25 мл/мин) при одновременном сни­
жении интенсивности реабсорбции (до 96 %).
После успешного удаленйя очага интоксика­
ции, его эффективного дренирования выдели­
тельная функция почек восстанавливается.
ФУНКЦИОНАЛЬНАЯ ОПЕРАБЕЛЬНОСТЬ
И ВОЗРАСТ
На основании статистического анализа дооперационной оценки и исходов большой группы
больных, оперированных в нашей клинике
[Буравцов В. И. и др., 1984], пришли к выводу,
что состояние легочного газообмена и крово­
обращения, а также возраст больного имеют
прогностическую значимость и должны учи­
тываться лишь при определении функциональ­
ной операбельности конкретного больного.
Однако ни один из них не может служить аб­
солютным противопоказанием к операции. В зна­
чительной части случаев больные старше 65 лет
с выраженными функциональными нарушениями
внешнего дыхания и гемодинамики опериро­
вались с благоприятным исходом. Не удалось
убедительно с помощью вычислительной тех­
ники прогнозировать и развитие смертельно
опасных осложнений на основании функцио­
нальных исследований. Лишь у больных с выра­
женными рестриктивными нарушениями (рав­
номерное снижение ЖЕЛ и ФЖЕЛ) после
операции чаще развивается пневмония, при­
водящая к летальному исходу.
Окончательное решение о функциональной
операбельности в нашей клинике принимают
хирург и анестезиолог (иногда с привлечением
клинического физиолога) при совместном об­
суждении данных проведенного обследова­
ния. Признаками иноперабельности при пульмонэктомии, следует считать:
1. Непереносимость обычной двигательной
нагрузки.
2. Предельное уменьшение резервов внешнего
дыхания: снижение ЖЕЛ до 40 % должной
величины с равномерным распределением вен­
тиляционной функции между легкими; одно­
секундная ЖЕЛ менее 1 л, составляющая 50 %
от форсированной ЖЕЛ; соотношение между
максимальной скоростью выдоха и вдоха менее
0,7, несмотря на применение бронхолитиков;
КИОг ниже 20; индекс вентиляции по Репину—
Цукерману ниже 1225, резерв дыхания (отно­
шение ММВ:МОД), равняющийся 3—4, с отри­
цательным или иногда нулевым результатом
гипервентиляционной пробы.
3. Клинически выраженная и резистентная
к терапии право желудочковая недостаточность,
подтвержденная исследованиями ЭКГ и ИРГТ,
при отчетливом повышении сопротивления
в легочных сосудах, возрастающем при на­
грузке (среднее давление в легочной артерии
выше 45 мм рт. ст.).
4. Тяжелый атеросклероз коронарных сосу­
дов с частыми приступами стенокардии покоя
с нарушениями ритма и признаками сердеч­
ной недостаточности, которая не поддается
короткому курсу терапии дигиталисом, препара­
тами калия, мочегонными.
5. Гипертоническая болезнь Пб—III стадии
с постоянно высоким уровнем АД, явлениями
сердечной недостаточности и мозговыми рас­
стройствами, которые не поддаются направлен­
ному медикаментозному лечению.
6. Тяжелая анемия (концентрация гемо­
глобина менее 90 г/л), гипопротеинемию и гипоальбуминемию (менее 20—25 г/л) на фоне
значительной потери массы тела, устойчивые
к инфузионно-трансфузионной терапии и вспо­
могательному парентеральному питанию.
7. Значительные нарушения выделительной
функции почек (азотемия, превышение изме­
ренной осмоляльности над расчетной на 25—
30 мосмомоль/л), а также глубокие расстрой­
ства внутренней среды другой природы (гипо­
калиемия, метаболический алкалоз), которые
не удается корригировать.
8. Последствия перенесенного мозгового
инсульта с выраженными паретическими изме­
нениями скелетной и дыхательной мускулатуры.
Показания к лобэктомии и экономным ре­
зекциям легких, к вмешательствам на плевре
и грудной клетке ставят более свободно.
Глава Т ПОДГОТОВКА
БОЛЬНЫХ К ОПЕРАЦИИ
В наиболее общем виде подготовка больного
к операции на легких и плевре должна опираться
на решение трех кардинальных задач: добиться
правильного отношения больного к хирургиче­
скому лечению (психологическая подготовка),
улучшить компенсаторные возможности лег­
кого как органа, наиболее повреждаемого пря­
мым воздействием операционной травмы (ор­
ганная подготовка), и повысить резистентность
основных систем жизнеобеспечения, функ­
циональное состояние которых может быть
нарушено операцией и послеоперационной
болезнью (системная подготовка).
Психологической подготовке часто не уде­
ляют достаточно внимания. А между тем от
нее зависит не только само согласие больного
на операцию, но и его доверие ко всем действиям
персонала после нее, коммуникабельность,
активное участие в лечебном процессе. Для
достижения этой цели необходимо применить
все доступные средства убеждения в необходи­
мости именно данного варианта хирургического
лечения и устранить излишние опасения боль­
ного. Больной должен получать правдивую ин­
формацию о своей болезни, предполагаемой
операции и послеоперационном состоянии от
врача — иначе его дезинформируют некомпе­
тентные лица. Индивидуальные беседы орди­
натора или начальника отделения с больным,
контакт с его родственниками и близкими, вни­
мательное отношение персонала, хороший уход,
предоперационный осмотр анестезиолога с
уточнением многих сторон подготовки больного
к предстоящей операции и в послеоперационном
периоде, обязательное использование пись­
менной инструкции «Что надо знать больно­
му»— это тот арсенал приемов, которые необ­
ходимо использовать всегда.
Неправильно скрывать от больного, что хирур­
гическое вмешательство связано с определен­
ными физическими страданиями и риском
осложнения. При современном общем уровне
информации такие попытки обречены на неуда­
чу и подрывают доверие к врачу, тем более,
что исключить контакт с больными, уже пере­
несшими такое вмешательство, при современной
организации лечения в стационарах невоз­
можно. Но, откровенно утверждая, что опера­
ция на легких небезопасна, врач должен разъ­
яснить пациенту, насколько опаснее оставлен­
ная без хирургического лечения болезнь.
При злокачественных опухолях или подозре­
нии на злокачественность поражения послед­
ним аргументом является общеизвестная не­
излечимость рака. Следует считать ошибочным
существующее мнение, что надо скрыть от боль­
ного истинный диагноз и одновременно пред­
лагать ему под другим предлогом тяжелую опе­
рацию (например, пульмонэктомию), да еще
в ближайшие дни. Такая противоречивая пози­
ция лишь порождает сомнения в компетенции
врача, независимо от его званий и служебного
положения. Если больной операбелен по функ­
циональным критериям, то и обоснованное пред­
положение, и бесспорный характер рака легких
могут быть доведены до его сведения. Тяжесть
такого сообщения уравновешивается тут же
предлагаемым выходом — операцией, а мыслям
о смертельности заболевания лечащий врач
противопоставляет тезис об излечимости сво­
евременно выявленного рака.
Необходимость считаться с психологией
иногда длительно болеющего человека уже
сама по себе обязывает возможно раньше
наметить конкретный план его обследования
и лечения. Больной должен быть с самого нача­
ла посвящен в этот план и сроки его осуществле­
ния, учитывая современный культурный уро­
вень больных, которые не приемлют врачебных
действий, если они не аргументированы. Не­
редко особенности поведения и настроения
больного должны быть учтены в первую оче­
редь и им подчинены все специфические обстоя­
тельства предоперационной подготовки. Иног­
да следует прибегать к помощи психоневро­
логов, консультация которых позволяет опре­
делить наиболее рациональный выбор психо­
миметиков.
Ставя задачу улучшить компенсаторные воз­
можности самого болеющего органа — легких,
преследуют прежде всего две цели: уменьшить
активность сопутствующего бронхита и снять
воспаление в легочной паренхиме, окружающей
очаг поражения.
111
Обычно этот компонент предоперационной
подготовки включает в себя дыхательную гим­
настику, ингаляции и интратрахеальные вли­
вания антибиотиков (соответственно спектру
микрофлоры) и антисептиков (солафур, димексид) в комбинации с бронхолитиками (эфедрин,
новодрин, алупент) и муколитиками (протеоли­
тические ферменты, ацетилцистеин). Использо­
вание ультразвуковых туманообразователей
обеспечивает поступление лекарственных ве­
ществ к самой респираторной зоне легкого и
ускоряет разрешение воспалительных изменений
[Королев Б. А., Шмерельсон М. Б., 1975].
Однако только лишь рациональное откашли­
вание в дренажном положении и вибрационный
массаж грудной клетки оказывают существен­
ное и быстрое благоприятное влияние на меха­
нику дыхания и легочный газообмен [Гологор­
ский В. А. и др., 1981].
Отсюда немаловажное значение дыхательной
гимнастики.
Дооперационная лечебная физкультура под
контролем методиста улучшает газообмен,
тренирует дыхательные мышцы. В ходе ее боль­
ные обучаются рациональному дыханию и дыха­
тельным упражнениям раннего послеоперацион­
ного периода. Обучение диафрагмальному дыха­
нию, дренажным положениям, эффективному
кашлю закрепляется упражнениями, которые
больные самостоятельно выполняют несколько
раз в день.
В отдельных случаях (при значительном
уменьшении жизненной емкости легких и ре­
зерва дыхания, высоком коэффициенте дыха­
тельных изменений УО (более 2) и одновре­
менном «гипоксическом» МОК (более 4 л/м2
в 1 мин) показано использование сеансов вспо­
могательной искусственной вентиляции легких
через загубник с помощью стандартных объем­
ных аппаратов типа РО (адаптация «повисанием на респираторе») илй аппаратов ИВ Л с
откликающимися устройствами (Бёрд Марк-8)
по 1—2 ч в сутки на протяжении 2 нед. Сеансы
вспомогательной искусственной вентиляции
повышают функциональные возможности внеш­
него дыхания у 50—60 % больных с крайне
ограниченными резервами [Юревич В. М. и др.,
1969; Репин Ю. М., Цукерман И. Я., 1981].
Механическое удаление мокроты, так называе мая санация бронхиального дерева с помощью
курса бронхоскопий с одновременной инстил­
ляцией антибактериальных препаратов и муколитиков, позволяет ускорить разрешение вос­
палительного процесса в бронхах, улучшает
эвакуацию мокроты за счет прицельной аспи­
рации ее из устья дренирующего бронха. Одно­
временный систематический осмотр слизистой
оболочки бронхиального дерева позволяет су­
дить о темпе снижения остроты бронхита, умень­
шении его макроскопических проявлений при
фибринозно-гнойном воспалении слизистой
оболочки.
В некоторых случаях стойких воспалитель­
ных изменений на периферии бронхиального
дерева показано транстрахеальное или чрес­
кожное трансторакальное введение санирую­
щего катетера в пораженные отделы легких.
Катетеризация бронхов используется для си­
стематической (на протяжении нескольких
дней) санации бронхиального дерева за счет
вливания муколитиков и стимуляции кашля.
Исследования, проведенные в клинике, показа­
ли, что в некоторых случаях хронических легоч­
ных нагноений чрескожное трансторакальное
дренирование бронха пораженной доли обес­
печивает быстрое и надежное уменьшение ост­
роты воспаления, может сократить период под­
готовки внутригрудной операции либо послу­
жить основанием для эффективного местного
лечения [Плешаков В. Т. и др., 1979; Ворон­
цов С. А., 1981 ].
Начальное системное, парентеральное приме­
нение антибиотиков широкого спектра дей­
ствия с переходом на целенаправленную анти­
бактериальную терапию после установления
чувствительности флоры из очага или смывов
бронхов не всегда оказывается эффективным.
Использование так называемых «птитиков»
(нитрофурановые препараты, малые дозы цито­
статиков) при обширном перифокальном воспа­
лении повышает эффективность антибактери­
альной терапии. Благотворно сказывается
также внутривенное вливание 1 % раствора каль­
ция хлорида по 300—400 мл (1—2 раза в день),
особенно у больных с ретростенотическим рас­
падом и выраженным хроническим бронхитом
[Дмитришен Л. Г., 1968, и др.].
Перспективным представляется метод мест­
ного антибактериального воздействия с по­
мощью внутритканевого электрофореза [Соко­
лов С. Б. и др., 1981], разработанный в Ялтин­
ском НИИ курортологии и физических мето­
дов лечения им. И. М. Сеченова.
Этот метод основан на принципе электро­
эмиссии лекарственных препаратов (антибио­
тиков) через кожу груди и благоприятном влия­
нии электрического поля на воспаленную легоч­
ную паренхиму, что ускоряет рассасывание вос­
палительной инфильтрации.
Для гальванизации используются аппарат
типа «Поток-1» (АПГ-32), свинцовые электро­
ды площадью 300 см2, фланелевые прокладки
толщиной 1 см. Электроды размещают на груд­
ной клетке в переднезаднем направлении. Плот­
ность тока на электродах — 0,05 мА/см2. Галь­
ванизацию начинают после внутривенного ка­
пельного вливания 1/з лечебной смеси, состоя­
щей из суточной дозы бактерицидного анти­
112
биотика, растворенного в 400 мл изотониче­
ского раствора электролитов. Длительность
сеанса — 30—50 мин.
Г. Г. Горовенко и соавт. (1982) реализовали
идею гальванизации воспаленной легочной
ткани при другом пути введения антибиотика:
капельно со скоростью 10 кап/мин через мик­
ротрахеостому. И этими авторами отмечена
быстрая и четкая положительная динамика кли­
нических и рентгенологических показателей,
свидетельствующая об уменьшении перифо­
кального воспаления: нормализация темпера­
туры тела, содержания лейкоцитов, лейкоци­
тарной формулы, протеинограммы.
Конкретный выбор пути введения антибиоти­
ка определяется условиями и особенностями
лечения больного.
Как только температура тела нормализова­
лась или стала субфебрильной, значительно
уменьшились изменения показателей крови
(концентрации лейкоцитов, СОЭ, лейкоцитар­
ного индекса, выраженность воспаления в брон­
хиальном дереве), количество мокроты суще­
ственно снизилось, а рентгеновские тени в лег­
ком обрели стабильность, можно считать, что
цель местной подготовки достигнута и может
быть назначено оперативное вмешательство.
Повторное исследование внешнего дыхания
или показателей интегральной реографии тела,
определяющих связь внешнего дыхания и гемо­
динамики, позволяет объективизировать функ­
циональный эффект противовоспалительной
терапии и подтвердить готовность больного
к вмешательству.
Необходимо подчеркнуть, что стихание вос­
палительного процесса в респираторной зоне
благотворно сказывается на состоянии легоч­
ной гемодинамики, уменьшает проявления
правожелудочковой недостаточности сердца.
Улучшению показателей легочной гемодина­
мики способствует и проведение лечебной физ­
культуры (особенно в кислородной маске).
Снижение перегрузки правого сердца дости­
гается внутривенным одновременным влива­
нием эуфиллина по 0,24 г 1—2 раза в день
в течение 5—7 дней.
Если воспаление не поддается консерватив­
ному лечению в течение 10—15 дней (при яв­
ных показаниях к операции), то дальнейшая
противовоспалительная терапия не оправдан­
на. Некупируемый консервативно деструктив­
ный процесс или даже его прогрессирование
заставляют использовать единственный выход —
радикальное вмешательство, когда вместе с
очагом деструкции удаляются и окружающие
воспаленные ткани, иногда противопоставляя
лобэктомии или комбинированным резекциям
пульмонэктомию. Еще более веским доводом
в пользу решения о срочной операции явля­
8 Зак. 0517
ются ухудшение состояния на фоне многоком­
понентной терапии или непереносимость ле­
карств, необходимых для консервативного ле­
чения.
Так же не может быть поводом к продлению
подготовки и острое воспаление легочной па­
ренхимы, сопровождающее рак легкого (при
параканкрозной пневмонии, ретростенотическом абсцессе). Противовоспалительное лечение
проводится в таких случаях в пределах вре­
мени, затрачиваемого на обследование и реше­
ние вопроса об операции.
Не все хирурги разделяют необходимость
использования в предоперационном периоде
антибиотиков для снятия перифокального вос­
паления, так как нередко можно добиться
уменьшения его выраженности или даже разре­
шения нагноения, используя только санацию
очага антисептиками через дренаж, введенный
в полость деструкции торакоцентезом [Лесницкий Л. С., 1970]. Более того, ряд авторов
предлагают использовать дренирование ограни­
ченных гангренозных полостей как альтерна­
тиву лобэктомии [Cameron Е., Whitton J., 1977;
Vainrub В. et al., 1978] или считают целесообраз­
ным воспользоваться практически одним дре­
нированием, чтобы подготовить больного ган­
греной легких к резекции [Вагнер Е. А. и др.,
1980].
Другие считают более важным повышение
иммунорезистентности, учитывая нередкие
иммунодефициты у больных с заболеваниями
легких. Отсюда возникает проблема стимуляции
иммунной защиты за счет увеличения содержа­
ния в крови лимфоцитов при значительных
лимфопениях (тималином или леакадином), в
том числе и активных Т-лимфоцитов. Второе
направление — применение препаратов, повы­
шающих (активно или пассивно) уровень гу­
морального иммунитета. Для этого использу­
ют анатоксин, специфический бактериофаг,
антистафилококковый глобулин или гиперим­
мунную плазму. Результаты использования
последнего подхода показали определенный
успех консервативной терапии острых легоч­
ных нагноений (чаще полное выздоровление,
реже — переход в хроническую форму), но
применение иммунных препаратов не позволило
улучшить непосредственные результаты опера­
тивного лечения [Стручков В. И. и др., 1981].
Наряду со снятием воспаления для улучше­
ния компенсаторных возможностей легких пе­
ред операцией необходимо добиться стойкого
уменьшения выраженности бронхоспастиче­
ского синдрома, особенно при сопутствующей
бронхиальной астме. Курсовое применение
интала, бриканила, сальбутамола не всегда
эффективно. Выраженные изменения тонуса
бронхиальной мускулатуры иногда заставляют
113
в качестве подготовительного мероприятия
применить гломусэктомию с синокаротидной
денервацией по Накаяма — Рудовскому [ Рудовски Е. М„ 1971; Репин Ю. М., Цукер­
ман И. Я., 1981].
Повышение состоятельности систем жиз­
необеспечения должно проводиться по разным
направлениям.
Выбор гипотензивного препарата (при ги­
пертензии) определяется видом артериальной
гипертензии: идиопатическая (гипертоническая
болезнь) или симптоматическая (почечная
гипертензия, феохромоцитома, болезнь Иценко — Кушинга), эффектом предшествующего
медикаментозного лечения. В ходе предопе­
рационной подготовки важно снизить систем­
ное артериальное давление до такой степени,
чтобы устойчиво устранить общие проявления
артериальной гипертензии.
Большие дозы изобарина, препаратов раувольфии в силу их длительного последействия
существенно влияют на выбор анестезии, а пото­
му должны применяться с осторожностью и
обязательной отменой за 2 дня до операции.
Особенно трудны для подготовки больные, у
которых артериальная гипертензия сочетается
с ишемической болезнью сердца. В этих слу­
чаях выход состоит в том, чтобы проводить
лечение, направленное на коррекцию основных
компонентов, определяющих нарушение кро­
вообращения: высокое артериальное давление и
повышение периферического сосудистого со­
противления, депрессия инотропной функции
миокарда и нарушенная трофика мышцы сердца
в связи с ишемической болезнью миокарда.
Препаратом выбора для регуляции артериальной
гипертензии может быть клофелин (гемитон,
катапресан) либо метилдофа (допегит), так
как эти препараты умеренно действуют на со­
судодвигательный центр и не истощают депо
катехоламинов в организме [Prys-Roberts N. et
al., 1971].
Одновременное использование транквилиза­
тора усиливает действие гипотензивных средств,
купируя психоэмоциональное напряжение,
оказывает непосредственное коронарорасширяющее действие [Ikram S. et al., 1973]. Опыт
клиники позволяет полностью солидаризиро­
ваться с В. А. Гологорским и соавт. (1977),
Ch. Pinaud и соавт. (1979) в том, что сердеч­
ные гликозиды следует назначать до операции
на легком не только при клинически отчетливой
сердечной недостаточности, но и при ее латент­
ных формах, которые могут быть диагностиро­
ваны с помощью интегральной реографии тела
при УИ менее 35 мл/я2.
На таком фоне данные ЭКГ, свидетельствую­
щие об очаговых изменениях в миокарде и
постинфарктных рубцах, не являются основа­
нием для отказа от радикального вмешатель­
ства, но указывают на необходимость система­
тического применения коронаролитиков (дли­
тельно действующих нитритов — сустака, нитронга, нитросорбита) и препаратов, снижаю­
щих потребление кислорода миокардом (интенсаин, рибоксин) с одновременным улучше­
нием коллатерального кровообращения — дипи­
ридамолом (персантин, курантил). В случаях
значительного нарушения трофики миокарда
(при истощении, эндогенной интоксикации) не­
обходимо включать препараты, повышающие
пластические свойства миокарда (оротат калия,
анабиотики, панангин и др.). Медикаментоз­
ная терапия небезупречных по гемодинамиче­
ским резервам больных оказывается эффек­
тивной только при ее проведении по всем трем
направлениям [Архипов И. В. и др., 1983].
В таких условиях вазоконстрикция, возни­
кающая от использования сердечных глико­
зидов, и возможность увеличения постнагрузки
на миокард [Вотчал Б. Е., Слуцкий М. Е., 1973]
нивелируются действием вазодилататоров (ме­
тилдофа, нитриты, дипиридамол), тогда как
изолированное систематическое применение
нитритов, снижая сосудистое сопротивление
и в системном кровотоке, может нарушить пер­
фузию миокарда [Чазов Е. И., Руда М. Я.,
1979]. Направленное лечение нарушений ритма
сердца на фоне такой терапии сопутствующих
заболеваний сердечно-сосудистой системы поз­
воляет больным переносить самые тяжелые
операции.
На основании исследований и клинических
наблюдений, проведенных за последние годы
в клинике госпитальной хирургии и в других
лечебных учреждениях, показано, что включение
в программу предоперационной подготовки
сеансов гипербарической оксигенации в тера­
певтической барокамере (OKA-МТ) оказывает
несомненный благоприятный функциональный
эффект. Патогенетическая обоснованность
применения гипербарической оксигенации для
профилактики инфекции и при гнойно-септи­
ческих заболеваниях базируется на устране­
нии кислородной недостаточности (чаще всего
гемодинамического типа), непосредственного
влияния на возбудителя инфекции (анаэроб­
ной флоры), восстановлении иммунного гомео­
стаза макроорганизма и возможности потен­
цирования действия медикаментозной (в том
числе и антибактериальной) терапии [Бело­
куров Ю. Н., Рыбачков В. Р., 1981; Буравцов В. И. и др., 1981]. Однако использование
гипербарической оксигенации в лечении гной­
но-деструктивных заболеваний легких и плевры
сдерживается существующими представле­
ниями о токсическом действии гипербарической
оксигенации на легочную паренхиму и возмож­
114
ности развития баротравмы легкого при декомп­
рессии.
На основании проведенных экспериментов
и клинических исследований установлено, что
декомпрессия не вызывает баротравмы лег­
кого, пораженного острой пневмонией. Наличие
абсцесса в легком или пневмоторакса не явля­
ется противопоказанием к проведению этого
метода. В том случае, если в полости абсцесса
или плевры находился дренаж, больного поме­
щали в камеру с водозапорным клапаном; в
последующих сеансах дренажную трубку про­
сто герметично закрывали. В барокамере боль­
ной обязательно должен иметь возможность
собрать мокроту, поскольку во время сеанса
у большинства больных отмечается увеличе­
ние ее отхождения.
В парных исследованиях до и после одного
сеанса гипербарической оксигенации
(при
давлении кислорода 1,8 ата и экспозиции 45 мин)
с помощью известных методик [Винницкая Р. С.
и др., 1976; Редхамер Р„ 1976] не установлено
статистически значимых отличий в диффузи­
онной способности легких и не обнаружено
ухудшения вентиляционно-перфузионных со­
отношений в легочной паренхиме, что подтвер­
ждает отсутствие токсического действия кисло­
рода при такой экспозиции.
У большинства больных (у 84 %) обнаружены
отчетливые признаки клинического улучшения
общего состояния, которого не удавалось до­
биться до того многокомпонентным лечением
в пульмонологическом отделении. Они проявля­
лись в улучшении общего состояния, нормали­
зации нарушенного сна и аппетита, исчезнове­
нии раздражительности, уменьшении или исчез­
новении одышки в покое, в позитивном отно­
шении больного к данному методу лечения и
уверенности в благоприятном исходе необходи­
мой операции, нормализации температуры
тела, улучшении физикальных данных, харак­
теризующих основное состояние патологии
легких. Одновременно улучшается механика
дыхания, возрастают ЖЕЛ и КИОг, снижается
работа дыхания, что было подтверждено поло­
жительной динамикой показателя напряжен­
ности дыхания по данным интегральной реографии: даже после одного сеанса гипербари­
ческой оксигенации он снижается до пределов
нормальных величин. Анализ полученных в
динамике данных интегральной реографии по­
казал, что при исходном высоком уровне МОК
его снижение до должных величин для условий
физиологического покоя является правилом.
Уже в ходе одного сеанса удавалось устранить
гемодинамические проявления недостаточно­
сти легочного газообмена, если считать, что
прямым путем компенсации гипоксемии, воз­
никающей при нарушениях внешнего дыхания,
8*
является повышение объемной скорости кро­
вотока. После гипербарической оксигенации
восстанавливается трофика миокарда. Показа­
телем нормализации метаболизма миокарда
служит исчезновение сердечных аритмий, а
снижение повышенного МОК происходит за
счет достоверного снижения частоты сердеч­
ных сокращений. При наличии сердечной недо­
статочности гипербарическая оксигенация,
наоборот, способствует достоверному повы­
шению У О. Необходимо отметить и благоприят­
ный эффект повышения толерантности глико­
зидной терапии сердечной недостаточности,
в том числе и в тех случаях, когда воспалитель­
ный или опухолевый процесс в легких сочета­
ется с приобретенным пороком сердца.
После 5—7 сеансов гипербарической окси­
генации уменьшается характерное для легоч­
ных воспалительных процессов извращение
белкового обмена, деятельности окислительных
ферментных систем
(лактатдегидрогеназа),
процессов метаболизма аминокислот, полностью
исчезают нарушения кислотно-основного со­
стояния [Булынин В. И. и др., 1982]. По-види­
мому, улучшение тканевого кислородного обес­
печения приводит к преодолению прежде всего
истощения биоэнергетики, что проявляется
ликвидацией гипохолестеринемии, переходом
катаболизма в анаболизм и значительным умень­
шением деструкции легочной ткани. Улучше­
ние пластических процессов в организме при­
водит к нормализации синтеза гемоглобина.
Достоверное, хотя и умеренное, повышение
концентрации гемоглобина в цельной крови,
при неизменности его концентрации в одном
эритроците, одновременно служит доказатель­
ством отсутствия ингибирующего действия
высокого напряжения кислорода во вдыхаемом
воздухе на эритропоэтическую функцию кост­
ного мозга. Отсутствует и воздействие кисло­
рода на интимные механизмы кислородтранспортной функции крови, что подтверждается
сохранением положения кривой диссоциации
оксигемоглобина.
Обеспечивая восстановление, пусть времен­
ное, кислородного режима организма, гиперба­
рическая оксигенация изменяет метаболиче­
ский фон, на котором развивается заболевание
легких, стабилизирует жизненно важные функ­
ции, повышает возможность механизмов есте­
ственной детоксикации. Под действием корот­
кого курса происходит не только снижение лей­
коцитарной реакции на воспалительный про­
цесс, но и изменяется лейкоцитарная формула,
что приводит к снижению высокого лейкоцитар­
ного индекса интоксикации по Кальф-Калифу.
Одновременно отмечено относительное повы­
шение содержания лимфоцитов в тех случаях,
когда с уверенностью можно думать об имму-
115
нодепрессии. Средняя концентрация лимфо­
цитов у таких больных повышалась от 0,34±
±0,09 • 109/л до 1,66±0,26 • 109/л. Одновре­
менно уменьшились явления дизрегуляции гу­
морального иммунитета, которые характеризо­
вались повышением уровня IgA при уменьшен­
ном содержании IgM на фоне нормального или
повышенного уровня IgG, снижением микробной
обсемененности кожи по Н. Н. Клемпарской.
Все эти функциональные сдвиги не только спо­
собствуют эффективности комплексного лече­
ния больных с гнойно-деструктивными пора­
жениями легочной паренхимы, но могут стать
решающим звеном такой терапии.
Естественно, что эффективность такого лече­
ния и переносимость последующей операции во
многом определяются выраженностью волеми­
ческих расстройств, состояния кислородной
емкости крови. Для плановых больных с забо­
леваниями легких характерно отсутствие су­
щественных различий основных показателей
циркулирующего эритрона, как концентраци­
онных, так и объемных. Умеренное снижение
этих показателей связано лишь с возрастом,
некоторой гиподинамией таких больных: цир­
куляторный гомеостаз, как указывалось выше,
у таких больных переходит на другой уровень
функционирования. Попытки корригировать так
называемую «гиповолемию» и несколько сни­
женный ЭО трансфузиями крови, как правило,
оказывались безуспешными. Умеренный дефи­
цит ОЦК сохраняется, а навязанный объем
крови быстро снижается до исходного уровня
при поступлении в стационар. Иногда состояние
таких больных после переливания крови даже
ухудшается.
Лишь при острых заболеваниях (при гангре­
не легких, тотальном пиопневмотораксе), не
говоря о легочных и внутриплевральных кро­
вотечениях, снижение кислородной емкости
может стать критическим и потребовать пере­
ливаний свежей крови, учитывая неблагоприят­
ные влияния инфекции, особенно грамотрицательной, на восстановление сродства гемо­
глобина к Ог. С неменьшим успехом может
использоваться в таких случаях и компонент­
ная трансфузия: размороженные эритроциты
и альбумин. Но и при этих обстоятельствах нет
необходимости стремиться к «полному» вос­
становлению нормальной концентрации гемо­
глобина. Достаточно добиться тенденции к воз­
растанию этого показателя (на фоне действия
и других компонентов предоперационной под­
готовки) с относительной стабилизацией со­
держания гемоглобина на уровне 120 г/л и 320—
360 г/м2.
Данные длительного использования в кли­
нике рутинного контроля волемии на различ­
ных этапах хирургического лечения больных с
заболеваниями легких [Мороз В. В., 1969;
Малахов С. Ф., 1972; Брюсов П. Г., 1971] по­
зволили начать с 1972 г. исследования по изуче­
нию возможностей предоперационного забора
крови или плазмы (при условии проведения
плазмафереза) у больных для последующего
возмещения этими средами операционной кро­
вопотери [Колесников И. С. и др., 1979|.
Клинические наблюдения и исследование
реакции гемодинамики показали, что при отда­
ленном резервировании аутокрови наиболее
целесообразным следует считать забор 400—
600 мл крови за 5—6 дней до вмешательства,
причем, по данным О. И. Жукова и соавт. (1980),
гемодинамическая реакция на такую заготовку
аутокрови даже у больных переходного и по­
жилого возраста со скомпрометированной сер­
дечной деятельностью минимальна, что позво­
ляет использовать заготовку аутокрови в ле­
гочной хирургии довольно широко.
Отсутствие гипопротеинемии у большинства
больных раком легких позволяет, как оказалось,
использовать предоперационный период у них
и для заготовки аутоплазмы
(до 800—
1000 мл/нед). Аутоплазма может быть приме­
нена как компонент инфузионно-трансфузион­
ной терапии во время внутригрудного вмеша­
тельства и в ближайшем послеоперационном
периоде. Двойной плазмаферез у больных ра­
ком легких не вызывает нарушений гемодина­
мики. Наблюдаемые функциональные сдвиги
не носят патологического характера, хотя и
выражаются в менее выраженной реакции на
нагрузку. С учетом нарушений системного ар­
териального тонуса сроком планового оператив­
ного вмешательства или повторного плазмафе­
реза следует считать 4—5-й день. Операцию на
легких или повторный плазмаферез у таких
больных можно проводить на 3—4-й день после
последнего забора.
Одним из существенных подготовительных
мероприятий к оперативному лечению заболе­
ваний легких и плевры может явиться заготовка
аутологичной костномозговой взвеси. В тече­
ние последнего десятилетия в клинике накоплен
определенный опыт трансфузий аутологичного
костного мозга для стимуляции регенерации
эритроцитов в послеоперационном периоде,
учитывая возможность развития длительной
анемии гипорегенераторного характера, плохо
поддающейся после ее возникновения обыч­
ной инфузионно-трансфузионной и медикамен­
тозной терапии [Малахов С. Ф. и др., 1982].
Более совершенной со всех точек зрения яв­
ляется методика миелоцитафереза с криокон­
сервацией костномозговых клеток в жидком
азоте при —196 °C. Криоконсервация дает
возможность производить заготовку кост­
ного мозга задолго до оперативного вмешатель­
116
ства, вскоре после поступления больного в ста­
ционар.
Кроме коррекции волемических расстройств,
необходимо обратить внимание и на выражен­
ность нарушений водно-электролитного равно­
весия, которые в значительной степени могут
снижать эффективность предоперационной под­
готовки, нарушая сократительную способность
миокарда, санацию трахеобронхиального де­
рева, пассаж пищи. При неглубоких нарушениях,
умеренном дефиците калия обычно использо­
вали энтеральный путь насыщения этим элек­
тролитом, вводя в рацион богатые калием про­
дукты (творог, сухофрукты, фруктовые соки)
и подкрепляя их введением оротата калия и
панангина. Безусловно, действие последнего
выходит за пределы простой коррекции гипо­
калиемии, так как, уменьшая поляризацию мем­
бран миоцитов и активируя клеточное фосфо­
рилирование, панангин (аспаркам, инцолен)
считается одновременно средством профилак­
тики отрицательных эффектов сердечных гли­
козидов.
При выраженной гипокалиемии и гнойной
интоксикации, активном дренировании гнойного
экссудата из плевральной полости прибегали
к парентеральному введению 3—6 г калия хло­
рида в составе полиионных глюкозированных
растворов с инсулином. Длительность терапии
определялась динамикой концентрационных
и ЭКГ-показателей калиевого обмена и контро­
лировалась исследованием калийуреза. Наличие
магния в оптимальных соотношениях с кальцием
в составе разработанных в клинике полиионных
растворов [Шанин Ю. Н. и др., 1978] обеспечи­
вало более полную коррекцию нарушений внут­
ренней среды, учитывая, кроме того, и влияние
на биоэнергетику организма больного вводимой
глюкозы с инсулином, стимуляцию анаболиче­
ских и пластических процессов.
Чаще всего в дооперационном периоде избе­
гают непосредственной коррекции белкового
состава плазмы за счет переливаний альбумина,
протеина или донорской плазмы (нативной,
лиофилизированной). Лишь на фоне белковой
недостаточности у истощенных пациентов ис­
пользуется инфузионная терапия с включе­
нием аминокислотных препаратов при соответ­
ствующем соотношении пластических и энер­
гетических компонентов парентерального
питания: 1 г аминоазота или 6,25 г аминокислот
на 150—200 ккал, поступающих с энергетиче­
скими компонентами (глюкоза, сорбит , жировые
эмульсии). Эффект такого лечения дополняется
другими компонентами терапии, позволяющими
подавить как причину гнойной интоксикации
(антибиотики, иммунотерапия), так и воздей­
ствие интоксикации на энергетический обмен
и катаболизм (анаболиты). При высокой лихо­
радке нужно добиваться ее снижения вплоть
до применения наружного охлаждения на
фоне адреноблокады, поскольку действие бак­
териальных токсинов на фоне гиперпирексии
возрастает в несколько десятков раз по отно­
шению к нормальному уровню температуры тела
[Atwood F„ Kass R., 1964]. Одновременно на
фоне лихорадки усиливается распад эритро­
цитов [Harms А., 1966]. Если этими мерами
удается преодолеть катаболизм или хотя бы
свести обмен к уровню анаболизма, то динамика
фаз белково-волемического состояния организ­
ма определяет более благоприятный прогноз
такого заболевания и вмешательства.
На фоне такой «энергетической» парентераль­
ной терапии уменьшается и выраженность сер­
дечной недостаточности, разрешаются явления
метаболического ацидоза или алкалоза, сни­
жается эндогенная интоксикация. Основную
роль в уменьшении проявлений фактора резорб­
ции должны играть различные приемы актив­
ного дренирования очага интоксикации (поло­
сти абсцесса, плевральной гнойной полости),
которые позволяют в значительной степени
«выбросить» токсические продукты наружу, не
допуская их поступления во внутреннюю среду
больного.
Сохранность функции почек по выведению
продуктов тканевого распада и бактериальных
токсинов редко заставляет применять специаль­
ные методы активной детоксикации у таких
больных (форсированный диурез, гемодиализ)
даже при гнойных процессах в легких. В слу­
чаях тяжелых деструктивных процессов и при
септическом состоянии легочного происхожде­
ния достаточным оказывается инфузия деток­
сикационных кровезаменителей — гемодеза,
полидеза. Особенно эффективны полифункциональные растворы (полидез-глутамат, поливисолин), которые не только образуют комплек­
соны с эндотоксинами и продуктами тканевого
распада, но и оказывают нормализующее влия­
ние на биоэнергетику за счет естественных ком­
понентов, содержащихся в таких растворах
(глюкоза, глутамат).
В случаях наиболее выраженной эндоген­
ной интоксикации, обусловленной прежде всего
фактором резорбции во внутреннюю среду ор­
ганизма, рекомендуют применить гемосорбцию
на активированном угле, что позволяет элими­
нировать среднемолекулярные тканевые и
микробные гидрофобные токсины или даже
микробные тела, если они интенсивно поступают
в кровоток. Показано, что наряду с субъектив­
ным улучшением состояния в ближайшие дни
после одного-двух сеансов гемосорбции боль­
ные становились более активными, у них улуч­
шался аппетит, значительно уменьшалось коли­
чество гнойной мокроты и плеврального отде­
117
ляемого, исчезал зловонный запах [Лукомский Г. И. и др., 1982]. Одновременно снижа­
лась температура тела, иногда до нормального
уровня, нормализовалась величина лейкоцитар­
ного индекса интоксицации. В то же время уро­
вень гемоглобина в крови сохранялся, суще­
ственно не менялись электролитный состав
крови и другие константы гомеостаза. Рентгено­
логически не только уменьшалась инфильтра­
ция легочной ткани вокруг очагов деструкции,
но и происходило существенное уменьшение
размеров полостей.
Среди эндокринопатий, сопутствующих за­
болеваниям легких, наибольшую трудность
в подготовке к операции представляет сахарный
диабет. Это большая проблема как в тех слу­
чаях, когда он выявляется в процессе обсле­
дования, так и у тех больных, у которых диабет
диагностирован давно и откорригирован за
счет диетического питания и регулярного при­
ема антидиабетических сульфаниламидов.
Особую «диабетическую» настороженность
следует проявлять у больных старше 50 лет
с гнойно-деструктивными процессами в легких.
Не лечившиеся больные или пациенты с не­
достаточно компенсированным диабетом не
должны подвергаться риску плановой опера­
ции без предварительного лечения, определяе­
мого с участием эндокринолога. Ацетонурия
не считается абсолютным противопоказанием
даже к срочному вмешательству, так как не­
редко удаление патологического очага облегчает
нормализацию углеводного обмена. Наблюде­
ния многих эндокринологов показывают, что
чем стабильнее и ниже гликемические показа­
тели перед вмешательством на легком, тем
легче регулировать уровень сахара на операции
и после нее [Плотников М. Н и др. 1978|.
Допускается сохранение уровня гликемии не
выше 10—11 ммоль/л (180—200 мг %), а глю­
козурии — 5 % от углеводной ценности суточ­
ного рациона при отсутствии ацетона в моче
и диабетических жалоб.
Использование преимущественно белковой
диеты наиболее выгодно только у тучных
больных, так как белки способствуют повыше­
нию основного обмена и снижению массы тела.
У истощенных пациентов приходится исполь­
зовать в питании и жиры, и углеводы. При сахар­
ном диабете тяжелой степени ежесуточно
необходимо три инъекции простого инсулина
или две инъекции простого и одна — суспензии
инсулина (в случаях повышения уровня сахара
к утру и появления диабетических жалоб).
Суточная доза инсулина должна быть адекват­
ной количеству принимаемых углеводов с уче­
том двигательной активности больного.
У некоторых пациентов с тяжелой степенью
диабета иногда наблюдаются явления недыха­
тельного ацидоза с ацетонуриеи и соответ­
ствующими клиническими проявлениями, не­
смотря на использование значительных доз
инсулина. Ацидоз затрудняет подбор дозы инсу­
лина от суток к суткам, так как на фоне аци­
доза эффективность действия гормона падает.
В таких случаях показано вливание 100—150 мл
5 % раствора гидрокарбоната натрия, 400 мл
гемодеза и 500 мл 10 % раствора глюкозы с
20 ME инсулина, лучше в виде раствора Лабори.
Из диеты временно исключаются жиры и на­
значаются липотропные продукты (овсянка,
творог), витамины комплекса В. При компен­
сированном (с помощью сульфаниламидов
или суспензии инсулина) диабете необходимо
незадолго до операции «перевести» больного
на простой инсулин, распределив его дозу на
протяжении суток таким образом, чтобы при
диетическом питании гликемия оставалась на
таком же уровне, как при обычном состоянии
больного. Следовой эффект антидиабетических
сульфаниламидов, занижая вначале истинную
потребность в инсулине, может дезориентиро­
вать врача, поэтому перевод на введение инсу­
лина желателен за несколько дней до операции.
В таком варианте можно считать предопераци­
онную подготовку законченной, что должно быть
отмечено в предоперационном осмотре анесте­
зиолога.
Во время предоперационного осмотра, кото­
рый проводится незадолго до операции, сле­
дует уточнить такое важное для послеопера­
ционного лечения обстоятельство, как непере­
носимость или повышенная чувствительность
к медикаментам (прежде всего к антибиоти­
кам). Исходя из плана предстоящей операции,
опроса больного и результатов определения пе­
реносимости именно анестезиологу необходимо
выбрать антибактериальные препараты, которые
будут использоваться во время вмешательства.
Совершенно необходимо непосредственно
перед операцией еще раз разъяснить больно­
му значение глубокого дыхания, эффективности
кашля, ранней двигательной активности для
профилактики осложнений и быстрейшего вы­
здоровления, проверить знания приемов смены
положения в постели, элементов дыхательной
гимнастики. Больным еще раз следует объяс­
нить, что подвижность зоны вмешательства,
несмотря на начальную боль, уменьшает дис­
комфорт, связанный с повреждением грудной
клетки, безопасна для заживления операцион­
ной раны и обеспечивает раннее вставание. При
предельном снижении вентиляционных пока­
зателей пациента предупреждают о возмож­
ности профилактической искусственной венти­
ляции легких. В процессе окончательного
осмотра определяются характер и состав не­
посредственной премедикации к анестезии.
Глава kJ АНОМАЛИИ
РАЗВИТИЯ ЛЕГКИХ
К аномалиям развития легких в настоящее
время относят более 50 различных пороков.
Для удобства рассмотрения можно классифици­
ровать их следующим образом.
Классификация аномалий развития легких
Пороки легких, связанные с их недоразвитием: пороки
отсутствия (апневмия, агенезия или аплазия легких, аге­
незия или аплазия трахеи и бронхов, агенезия или аплазия
сосудов малого круга кровообращения); стенозы легочной
артерии; стенозы трахеи и бронхов; аневризмы легочной
артерии; варикозное расширение вен малого круга крово­
обращения; артериовенозные аневризмы легких; аневриз­
мы бронхиальных артерий; варикозное расширение брон­
хиальных вен; расширения трахеи, бронхов, бронхиол:
лобарная эмфизема («исчезающее легкое»).
Пороки легких, обусловленные избыточным развитием
тканей или элементов легких: добавочное легкое (интраабдоминальное, интраторакальное, трахеальное).
Пороки развития легких, обусловленные внутрилегочным аномальным делением и перемещением элементов
легкого; сепарация и транспозиция бронхов; добавочные
бронхи; аномалии отхождения сегментарных и субсег­
ментарных ветвей легочной артерии; аномалии развития
междолевых щелей легких; добавочная доля легкого.
Сочетанные пороки развития легких: гипоплазия легких
(«простая» или «кистозная»); поликистоз легких; секвестра­
ция легких; синдром Зиверта—Картагенера.
Зеркальное легкое.
Патологические сообщения элементов легких с другими
органами: пищеводно-трахеальный, пищеводно-бронхиаль­
ный, аортолегочный свищи, открытый артериальный проток,
коммуникация легочной артерии с предсердием, анома­
лии впадения легочных вен.
Внутрилегочное изолированное аномальное развитие
тканей легкого и других органов: тератомы, гамартохондромы, дермоидные кисты легких.
Пороки развития лимфатической системы легких: лимфангиоэктазии легких; недостаточность клапанов лимфати­
ческих сосудов легких.
Врожденные дефекты иммунологической системы лег­
ких: муковисцидоз легких (альвеолярный протеиноз); бо­
лезни гиалиновых мембран (врожденные дефекты сурфак­
тантной системы легких); врожденная эмфизема легких,
обусловленная наследственным дефицитом а, -антитрип­
сина; аномалии развития местного иммунитета легких.
Агенезия или аплазия легкого. Двусторон­
няя апневмия, агенезия и аплазия легких не­
совместимы с внеутробной жизнью.
Агенезия и аплазия легкого с одной стороны
встречаются у одного из 15 тысяч новорожден­
ных. В мировой литературе описано около 230
таких случаев [Стручков В. И. и др., 1969; Пипия В. И. и др., 1971; Daurnovo Р., 1976; Наsche Е., 1978, и др.].
Подавляющее большинство наблюдений от­
носится к детям и подросткам, причем в 50—
60 % случаев аплазия и агенезия легкого соче­
тались с аномалиями других органов и сердеч­
но-сосудистой системы [Долецкий С. Я., 1963;
Сазонов А. М. и др., 1981]. У девочек агенезия
и аплазия отмечаются чаще, чем у мальчиков,
преобладает левосторонняя локализация. Ле­
тальность при агенезии и аплазии легких высо­
кая: к пятилетнему возрасту погибает 50 %
детей.
Клиническая картина зависит от степени
выраженности легочной и сердечно-сосудистой
недостаточности. Состояние больных может
быть удовлетворительным, но чаще имеются
признаки декомпенсации в виде выраженной
одышки в покое, затруднения дыхания и циа­
ноза губ.
Нередко уже в первые дни и месяцы жизни
ребенка отмечается одышка, может присоеди­
ниться инфекция дыхательных путей. Если
в этот период времени проводится рентгеноло­
гическое исследование, то выявляется тоталь­
ное затенение на стороне поражения.
Обзорная и полипозиционная рентгеногра­
фия и томография позволяют выявить или за­
подозрить отсутствие легкого. На обзорных
рентгенограммах обнаруживается смещение
сердца в одну из плевральных полостей, а при
полипозиционном исследовании — легочная
грыжа в переднем средостении, переходящая
нередко на сторону отсутствующего легкого
(рис. 60).
Для окончательного диагноза требуются
бронхоскопия с бронхографией, а также кате­
теризация сердца с контрастным исследова­
нием малого круга или ангиокардиографией из
правого желудочка сердца. Следует подчеркнуть,
что применение инструментальных методов
исследования у больных с агенезией и аплазией
легкого, находящихся в стадии декомпенсации,
представляет подчас большой риск.
При бронхоскопии в случаях агенезии обна­
руживается отсутствие бифуркации трахеи
119
Рис. 60. Агенезия нижнедолевого бронха левого легкого,
а — обзорная рентгенограмма: б — бронхограмма. Видно отсут­
ствие нижней доли легкого.
Рис. 61. Ангиопульмонография при агенезии левого легкого.
Контрастирована широкая правая ветвь легочной артерии. Левая
ветвь отсутствует.
и нет второго главного бронха, а при аплазии —
бифуркация трахеи едва намечаема; имеется
небольшой рудиментарный бронх в виде ме­
шочкообразного, слепо заканчивающегося
выпячивания. Главный бронх контралатераль­
ного легкого является непосредственным про­
должением трахеи.
Катетеризация сердца позволяет выявить
состояние нижней полой вены, положение серд­
ца, его поворот в сторону отсутствующего лег­
кого. Анализ газов крови исключает пороки раз­
вития сердца (дефект междпресердной и меж­
желудочковой перегородок). Ангиопульмоно­
графия (рис. 61) выявляет широкий развернутый
ствол легочной артерии контралатерального лег­
кого и округлой формы мешочкообразную «куль­
тю» с ровными контурами, указывающую на от­
сутствие легкого.
Агенезия и аплазия легкого не подлежат опе­
ративному лечению, если эти пороки развития
не сочетаются с другой патологией, например
диафрагмальной грыжей, пороком сердца. Боль­
ные агенезией и аплазией легких даже в состоя­
нии компенсации являются ограниченно тру­
доспособными (инвалидами III—II групп).
Агенезия и аплазия трахеи и бронхов отно­
сятся к порокам развития бронхиального дерева.
Изолированное отсутствие бронхов может быть
диагностировано с помощью бронхологических
методов, включая бронхографию.
120
Остановка развития трахеи наблюдается у
эмбриона в возрасте 28—32 дней, когда прекра­
щается дальнейшее развитие бронхопульмо­
нальной почки [Streeter G., 1951]. У эмбриона
32—34 дней изолированная остановка развития
бронхопульмональной почки ведет к образова­
нию агенезии долевого бронха и доли легкого.
Изолированная остановка развития бронхиаль­
ного дерева на 10--14-й неделе может привести
к агенезии сегментарных и субсегментарных
бронхов, так как в этот период происходит наи­
более активное развитие бронхиального де­
рева внутри сегментов [Путов Н. В. и др., 1982].
Агенезия или аплазия сосудов малого круга
кровообращения сопутствуют этому пороку
развития бронхиального дерева, но могут быть
и самостоятельным пороком. Прижизненное
распознавание изолированной агенезии сосудов
малого круга возможно с помощью селектив­
ной ангиографии. Отсутствие правой или левой
ветви легочной артерии сопровождается рас­
ширением легочной артерии и ее ветвей в конт­
ралатеральном легком, которые представляют
собой все артериальное русло малого круга.
Обычно степень развития сосудов малого
круга, в частности легочной артерии, соответ­
ствует степени развития бронхиального дерева
соответствующего легкого, так как эмбриоло­
гически развитие сосудов малого круга следует
за развитием бронхиального дерева. Однако при
гипоплазии легкого недоразвитие бронхиаль­
ного дерева и сосудов малого круга не всегда
совпадает; как правило, отмечается более выра­
женное недоразвитие легочной артерии и со­
судов малого круга.
Изолированная агенезия долевых, сегментар­
ных сосудов может быть выявлена только при
серийной двухпроекционной ангиопульмонографии. Эта аномалия характеризуется дис­
плазией прилежащих долевых и сегментарных
сосудов, расширением их просвета и увеличен­
ной васкуляризацией периферических отделов
этих сегментов. В зоне аплазии легочной арте­
рии выявляется культя сосуда с ровными кон­
турами (рис. 62).
Изолированная агенезия долевой или сегмен­
тарной артерии может сочетаться с гипопла­
зией прилежащих ветвей легочной артерии.
Поэтому при полипозиционном исследовании
сосудистого рисунка легкого и на обзорных рент­
генограммах можно по изолированной зоне
васкуляризации только предположить этот
порок развития малого круга, так как его кли­
нико-рентгенологические признаки весьма схо­
жи с признаками изолированной гипоплазии,
бронхоэктазий, воздушной кистой легкого
и дифференциальная диагностика невозможна
без обследования, включающего бронхогра­
фию и контрастное исследование сосудов легких.
Рис. 62. Ангиопульмонография при гиноп.ы ши артерий
нижней доли правого легкого.
Широкие сегментарные ветви артерий верхней доли, суженные
ветви артерий нижней доли; артерии средней доли отсутствуют.
Клинически изолированные формы агенезии
долевых и сегментарных ветвей легочной арте­
рии, как правило, ничем себя не проявляют.
Общее состояние больных удовлетворитель­
ное, нет признаков дыхательной и сердечной
недостаточности, а сопутствующая патология
бронхов в виде бронхоэктазий и кистозных
изменений иногда выступает на первый план,
являясь основанием для углубленного обсле­
дования, при котором выявление агенезии до­
левых и сегментарных ветвей легочной арте­
рии обнаруживается случайно. В литературе
этот порок развития малого круга рассматрива­
ется как редчайшая казуистика.
Изолированная агенезия легочной артерии
всего легкого в клинике наблюдалась у одной
больной (рис. 63), у которой она сочеталась
с гипоплазией бронхиального дерева правого
легкого. На бронхограммах у этих больных
выявлялось сформированное бронхиальное
дерево с признаками гипоплазии сегментарных
и субсегментарных бронхов, которые местами
имели булавовидные расширения. Во время опе­
рации агенезия легочной артерии правого лег­
кого была подтверждена, кровоснабжение лег­
кого осуществлялось из сосудов бронхиальной
системы. Венозный отток происходил в левое
предсердие через не измененные вены.
121
Рис. 63. Агенезия легочной артерии правого легкого, соче­
тающаяся с гипоплазией бронхиального дерева.
а — прямая ангиопульмонограмма, артериальная фаза; б —
прямая ангиопульмонограмма, венозная фаза; в — бронхограм­
ма.
Стенозы легочной артерии. Под стенозами
легочной артерии понимают локальные одиноч­
ные или множественные сужения просвета со­
суда, расположенные как проксимальнее, так
и дистальнее клапана легочной артерии.
Нарушение эмбриологического развития
перегородки артериального ствола, обусловлен­
ное отклонением его в сторону формирующего ­
ся ствола легочной артерии, ведет к образова­
нию сужения легочной артерии. Подклапанный
стеноз образуется вследствие усиленного раз­
растания мышечных волокон в области конуса
легочной артерии, а усиленное развитие за­
кладок клапанного аппарата формирует ее кла­
панный стеноз. Множественные периферические
стенозы легочной артерии формируются к концу
6-й недели развития эмбриона вследствие нару­
шения закладки и развития ветвей этого сосуда
в период появления бронхолегочных сегментов
[Малишевская В. А., 1967].
122
Стенозы легочной артерии могут быть само­
стоятельной патологией или сочетаться с раз­
личными пороками сердца. По данным Н. Rink
(1970), эта патология легких наблюдается не­
редко, составляя 0,5 % среди различных поро­
ков сердечно-сосудистой системы.
Особенностью кровообращения малого круга
больных со стенозами легочной артерии явля­
ется затрудненный приток крови к альвеолам,
обусловленный сужениями магистральных вет­
вей легочной артерии на различных уровнях.
При множественных периферических стенозах
возникает гемодинамическая ситуация много­
ступенчатого блока, приводящая к значитель­
ному снижению не только пульсового, но и сред­
него давления. Возникающее дополнительное
сопротивление в системе легочной артерии при­
водит к гипертрофии правого желудочка серд­
ца, увеличению его полости и к гипертрофии
папиллярных мышц, что обнаруживается при
ангиокардиографии. В зависимости от уровня
расположения стеноза при контрастном иссле­
довании выявляются сегментарно суженные
участки легочной артерии, сочетающиеся с
прилежащими сегментами расширения легоч­
ной артерии. Такая картина обусловлена эффек­
том гидродинамического действия протекаю­
щей крови. В суженной части артерии линей­
ная скорость кровотока значительно выше,
чем в расширенной. При значительном суже­
нии сосуда поток крови осуществляется через
суженный сегмент в виде тонкой струи, которая
при изгибе сосуда ударяется в одну из его сте­
нок, вызывая ее дилатацию. Применение двой­
ного контрастного исследования (углекислый
газ и жидкое контрастное вещество типа уро­
графина) позволяет выявить этот эффект, со­
провождающийся турбуленцией в зонах рас­
ширения сосудов (рис. 64).
Больные нередко поступают в клинику для
обследования по поводу порока сердца, кото­
рый при катетеризации и ангиокардиографии
отвергается. На ЭКГ у больных со стенозом
легочной артерии выявляется гипертрофия
правого желудочка с неполной блокадой правой
ножки пучка Гиса. Эти изменения обусловлены
систолической перегрузкой правого желудочка.
В зависимости от степени выраженности
стенозирования у больных может быть цианоз
в состоянии покоя или только при физической
нагрузке.
Единичные стенозы подлежат хирургической
коррекции, больные с множественными суже­
ниями, распространяющимися на долевые и
сегментарные ветви, обычно пользуются лишь
симптоматическим лечением.
Аневризма легочной артерии. Врожденные
аневризмы легочной артерии являются чрез­
вычайно большой редкостью, и причины их воз-
Рис. 64. Ангиопульмонограмма при стенозах легочной арте­
рии.
никновения неясны, но наиболее вероятной
предполагается неполноценность стенки легоч­
ной артерии врожденного генеза. Обычно анев­
ризма захватывает ствол легочной артерии и
главные ветви, реже — долевые и сегментарные.
Патофизиологические изменения при этом
пороке связаны с образованием зоны второго
течения (вихревых потоков), поддерживаемых
энергией транзитной струи крови. Возникаю­
щая турбулентность кровотока в зоне аневриз­
мы и на некотором расстоянии дистальнее ее
ведет к значительным изменениям гемодина­
мики легочных сегментов. Механическое воз­
действие турбулентных потоков создает повы­
шенное боковое давление на ее стенки, которое
значительно превышает боковое давление не­
расширенных ветвей сосуда. Высокое давле­
ние и турбулентные потоки крови в аневризма­
тическом мешке ведут к прогрессированию
дистрофических изменений в аневризматиче­
ской стенке, угрозе расслаивания и разрыва
ее.
Состояние больных аневризмой легочной
артерии зависит от ее локализации, степени
выраженности, особенностей регионарного
кровообращения в малом круге. При аневризме
ствола легочной артерии у больных развива-
123
1
Рис. 65. Аневризма артерии переднего сегмента верхней доли
правого легкого.
а — прямая ангиопульмонограмма; б — боковая ангиолулъмонограмма.
ется недостаточность ее клапанов. Наблюда­
ется появление диастолического шума в чет­
вертом — пятом межреберье слева от грудины.
Шум низкочастотный, дующего характера.
При селективной ангиопульмонографии конт­
растируется резко расширенный ствол легоч­
ной артерии, и контрастное вещество через не­
достаточные пульмональные клапаны поступает
в период диастолы в полость правого желудочка
сердца.
На обзорных рентгенограммах выявляется
резко расширенная вторая дуга левого контура
тени органов средостения. В боковой проекции
определяется высокая вторая дуга и сужено
ретростернальное пространство за счет высту­
пающего вперед легочного конуса.
При локализации аневризмы легочной арте­
рии в правой или левой ветви рентгенологиче­
ская диагностика затруднена и окончательный
диагноз устанавливается с помощью селектив­
ной ангиопульмонографии, если имеет место
резкое, превышающее двукратное сечение со­
суда, расширение просвета его.
Распознавание аневризмы легочной артерии,
исходящей из долевых или сегментарных сосу­
дов, на первых этапах диагностики проводится
с помощью полипозиционной рентгенографии
и селективной ангиографии сосудов малого
круга, позволяющих выявить булавовидное рас­
ширение легочной артерии (рис. 65).
Аневризмы легочной артерии являются пока­
занием к оперативному лечению, так как они
могут прогрессировать и сопровождаться вне­
запным кровотечением. При аневризмах ствола
легочной артерии проводят коррекцию ствола
и клапана. При периферической локализации
аневризмы применяют сегментарные резекции
или реконструкцию сосуда — резекцию его
сегмента.
Варикозное расширение вен малого круга
кровообращения. Изолированное варикозное
расширение вен малого круга кровообраще­
124
ния — чрезвычайно редкий вид сосудистой пато­
логии легких.
Варикозное расширение вен малого круга
кровообращения протекает бессимптомно; боль­
ные, как правило, жалоб не предъявляют, и
заболевание обнаруживается «случайно», при
рентгенологическом исследовании. Однако
рентгенологическое исследование позволяет
лишь заподозрить данную патологию, так как
рентгенологически выявляемая тень в легком
по своей гомогенности, четкости контура и ло­
кализации схожа с туберкулемой, раком лег­
кого, артериовенозной фистулой и другими
периферическими округлыми образованиями
легких. Только селективное контрастное иссле­
дование сосудов позволяет установить истин­
ную природу заболевания. В наблюдении кли­
ники у одной больной было варикозное расши­
рение вен III сегмента правого легкого, диагно­
стированное с помощью селективной ангиопульмонографии с применением сериографии и
киноангиографии [Попов Ю. А., Ловягин Е. В.,
19701 (рис. 66).
Патогенез заболевания неясен. Можно только
предположить, что в отдельных сосудах ацинар­
ной зоны легкого образуются патологические
сообщения бронхиальных артерий с легочной
веной. Возникающее при этом повышенное
давление крови из системы бронхиальных со­
судов приводит к локальным изменениям, рас­
ширениям венозных стволиков на уровне лобу­
лярной легочной вены. Образовавшаяся брон­
хиально-венозная коммуникация представляет
лево-левый шунт, который, вероятно, существен­
ного влияния на общую гемодинамику не оказы­
вает.
Прогрессирование заболевания, сопровож­
дающееся увеличением размеров варикса, яв­
ляется показанием к хирургическому лечению.
Хирургическое вмешательство может быть
ограничено иссечением варикса, сочетающе­
гося с регионарной перевязкой бронхиальных
артерий, или производится сегментарная резек­
ция легкого.
Артериовенозные аневризмы легких. Арте­
риовенозные свищи легких — порок развития
сосудов, вследствие которого возникает патоло­
гическое сообщение между артериями и венами
легкого. В результате появляется сброс веноз­
ной крови в артериальное русло, приводящий
к той или иной степени гипоксии. По данным
литературы, величина артериовенозного шунта
может быть весьма значительной и достигать
85 % от минутного объема малого круга.
В мировой литературе имеются сообщения
почти о 400 наблюдениях прижизненной диа­
гностики артериовенозной аневризмы легкого;
в отечественной литературе описано около 50
наблюдений.
Рис. 66. Варикозное расширение вен III сегмента правого
легкого. Ангиопульмонограмма, венозная фаза кровотока.
М. И. Перельман и соавт. (1965) в зависимо­
сти от морфологических особенностей разли­
чают три типа артериовенозных сообщений в
легких: 1) единичные соустья, располагающие­
ся между ветвями сосудов легкого крупного
колибра, по типу артериовенозных свищей;
2) множественные мелкие соустья, непосред­
ственно связывающие артерии и вены среднего
калибра; 3) обширная ангиоматозная сеть или
целый конгломерат сосудов, иногда мешковидно
расширенных по типу аневризм, которые как бы
вставлены между мелкими артериями и венами.
У большинства больных первые признаки
заболевания появляются в период полового
созревания, и полная клиническая симптома­
тика формируется обычно в возрасте 20—30 лет,
а иногда и позднее.
Через патологический шунт часть крови из
легочной артерии, минуя легочные капилляры,
поступает непосредственно в легочные вены.
Если величина артериовенозного сброса пре­
вышает ’/з всей массы крови, то развиваются
выраженные симптомы кислородного голода­
ния. Содержание кислорода в периферической
артериальной крови у таких больных, особенно
при физической нагрузке, снижается иногда
до очень низких цифр. С течением времени раз­
вивается компенсаторная эритроцитемия.
Патологический шунт в малом круге крово­
обращения приводит к увеличению минутного
объема кровообращения, к различной степени
выраженности артериальной гипоксемии.
125
Рис. 67. Систоло-диастолический шум при артериовенозной
аневризме нижней доли правого легкого. Фонограмма в
четвертом межреберье^ справа по среднеключичной линии.
Страдающие артериовенозной аневризмой
жалуются на слабость, быструю утомляемость,
одышку, усиливающуюся при физической на­
грузке. Не исключено, что некоторые неврологи­
ческие нарушения обусловлены воздушной
эмболией сосудов головного мозга [Craford С.,
1950], но большинство авторов считают, что в
основе их лежат гипоксия и полицитемия. Не­
редким симптомом артериовенозной аневриз­
мы является кровохарканье, наступающее при
разрыве телеангиэктазий слизистой оболочки
трахеобронхиального дерева или разрывах
расширенных и дегенеративно измененных
легочных сосудов.
Важно подчеркнуть, что цианоз кожи и сли­
зистых оболочек у больных усиливается при
физической нагрузке. Почти у половины боль­
ных на коже и слизистых оболочках отмеча­
ются множественные телеангиэктазии. У боль­
шинства наблюдается деформация ногтевых
фаланг по типу «барабанных палочек», реже
выявляется генерализованная форма остеоарт­
ропатии.
Патогномоничным симптомом артериове­
нозной легочной аневризмы является экстракардиальный систоло-диастолический
шум,
выслушиваемый над теми отделами легкого,
где локализуется поражение (рис. 67).
Имеется несомненная патогенетическая связь
артериовенозных легочных аневризм с врожден­
ными геморрагическими телеангиэктазиями
(болезнь Рендю — Ослера — Вебера). Сочета­
ние этих заболеваний наблюдается приблизи­
тельно у половины больных, поэтому некото­
рые авторы считают артериолегочную аневриз­
му частной формой болезни Рендю — Ослера—
Вебера.
Рентгеноскопия и рентгенография грудной
клетки выявляют различной формы и размера
достаточно четко контурированную гомоген­
ную, иногда пульсирующую тень аневризмы
в легком. Порой отмечается уменьшение тени
во время форсированного выдоха при закры­
той голосовой щели (феномен Вальсальвы).
Абсолютно доказательным методом рентгено­
логической диагностики артериовенозных анев­
ризм легких, особенно при множественных
поражениях, является ангиопульмонография.
При дифференциальной диагностике нужно
иметь в виду первичную полицитемию или
эритремию (болезнь Вакеза). Иногда ошибоч­
но диагностируется врожденный порок сердца.
Необходимо помнить о возможности сочета­
ния этих заболеваний.
Наиболее опасным осложнением артериове­
нозной аневризмы является массивное легоч­
ное кровотечение, которое возникает внезапно
вследствие разрыва бронхиальных сосудистых
сплетений, непосредственно связанных с анев­
ризмой.
В клинике наблюдался больной, у которого артериовеноз­
ная аневризма нижней доли правого легкого (рис. 68)
вызывала дважды обильное легочное кровотечение, сопро­
вождавшееся коллапсом с потерей сознания. После прове­
денных реанимационных мероприятий и последующего
комплексного обследования больному успешно выполнена
пульмонэктомия.
Лечение больных артериовенозными аневриз­
мами хирургическое.
При локализованных одиночных артерио­
венозных аневризмах проводится частичная
резекция легкого, при обширных аневризмах —
пульмонэктомия.
В случаях распространенных и локализован­
ных в обоих легких артериовенозных аневризм
показана эндоваскулярная окклюзия с помо­
щью катетеризационных методов. Это лечение
может быть выполнено сразу после проведения
диагностической ангиографии с использованием
катетера, подведенного к аневризме. Эмболизирующий материал (спирали типа Гиантурко,
спангостан) вводится через катетер в зону анев­
ризмы. Добиваются ее окклюзии (тромбоза).
Консервативное лечение больных с артерио­
венозными аневризмами бесперспективно.
Аневризмы бронхиальных артерий. Аневриз­
матическое расширение бронхиальных артерий
как порок развития в мировой литературе опи­
сывается как казуистика. Так, А. А. Вишнев­
ский, Н. К. Галанкин (1962) лишь у 1 на 1000
больных с врожденными пороками сердечно-
126
Рис. 68. Артериовенозная аневризма нижней доли правого
легкого. Ангиопульмонограмма. Артериальная фаза.
сосудистой системы встретили эту патологию.
В клинике наблюдалась одна больная с такой
патологией.
Аневризматическое расширение бронхиаль­
ных сосудов чаще наблюдается при сочетан­
ных пороках развития легкого, таких как гипо­
плазия легкого, поликистоз и секвестрация.
В этих случаях расширенные бронхиальные
артерии, как правило, локализуются в правом
легком и выполняют функцию транзита крови
в систему периферических ветвей легочной
артерии, обеспечивая кровообращение в па­
ренхиме отдельных зон гипоплазированного
или поликистозно измененного легкого (рис. 69).
Клинические проявления порока развития
бронхиальных сосудов во многом определяются
величиной сброса артериальной крови в малый
круг кровообращения. Значительный сброс кро­
ви может вести к развитию легочной гипер­
тензии не только регионарного характера,
но также общего, вызывая перегрузку правого
и левого желудочков сердца, которая выявля­
ется в виде их гипертрофии и изменений мио­
карда дистрофического характера. Прогрес­
сирующее расширение бронхиальных артерий
приводит к образованию новых коммуника­
ций в бронхиально-пульмональной системе,
нередко сопровождающемуся их разрывами,
кровохарканьем и легочными кровоточениями.
При бронхиальной ангиографии выявляется
расширенная и извитая бронхиальная артерия
с несколькими бронхиально-легочными ком­
муникациями и перетоком контрастного веще­
ства в систему легочной артерии и легочной
вены. При изучении бронхиальных сосудов
с помощью селективной ангиографии у больных
с заболеваниями легких можно выделить два
различных вида аневризматического расшире­
ния сосудов. В первой группе — это аневризма,
локализованная у места отхождения бронхи­
альной артерии от аорты, а во второй группе—
в периферических отделах и центральном сег­
менте. Могут наблюдаться при этом участки
с нормальным диаметром бронхиальных сосудов
в зоне магистральной бронхиальной артерии,
и тогда они представляются на ангиограммах
в виде сегментарных стенозов сосуда (рис. 70).
Лечение аневризматического расширения
бронхиальных артерий хирургическое. Диаг­
ностическая катетеризация бронхиальных
артерий (после установления, диагноза) может
быть использована для лечебной цели — ее
окклюзия с помощью спиралей типа Гиантурко
в сочетании с введением фрагментов спангогеля или спангостана. Адекватность окклю­
зии аневризматически расширенной бронхи­
альной артерии контролируется в момент эм­
болизации фракционным введением контраст­
ного вещества (урографин, уротраст). В случае
невозможности эмболизирующей окклюзии при­
бегают к торакотомии и открытой перевязке
измененных бронхиальных артерий.
Консервативное лечение аневризмы брон­
хиальных артерий бесперспективно.
Варикозное расширение бронхиальных вен
чаще наблюдается у больных с сочетанными
пороками развития легких. Ангиографически
эта разновидность патологии встречается в виде
гроздевидного ячеистого характера скопления
контрастного вещества в стенке бронха. Ва­
рикозное расширение бронхиальных вен может
рассматриваться как один из видов порока раз­
вития сосудистой системы легких. Эта патоло­
гия чаще всего сопутствует таким порокам
развития легких, как гипоплазия и поликистоз
(рис. 71).
Трахеобронхомегалия
(синдром Мунье —
Куна, трахеобронхоэктазии)
представляет
собой порок развития, характеризующийся
значительным расширением трахеи и крупных
бронхов, сопровождающийся инфекцией дыха­
тельных путей. Порок довольно редкий: в ми­
ровой литературе описано около 80 наблюде­
ний этой аномалии [Долецкий С. Я., Климкович И. Г., 1966; Эпштейн Г. Л., 1967].
Трахеобронхомегалия рассматривается боль­
шинством авторов как результат врожденного
127
Рис. 69. Аневризматическое расширение бронхиальных
артерий нижней доли правого легкого. Селективная ангио­
грамма бронхиальной артерии. Шунтирование контрастного
вещества в легочную артерию.
Рис. 70. Аневризматическое расширение бронхиальных
артерий верхней доли левого легкого. Селективная ангио­
грамма бронхиальной артерии.
недоразвития эластических и мышечных волокон трахеи и бронхов. Сопутствующий воспа­
лительный процесс накладывает свой морфоло­
гический отпечаток. Трахеобронхомегалия
часто сопровождается бронхоэктазиями, хро­
нической пневмонией, бронхитом, пневмо­
склерозом.
Как правило, все больные имеют длительный
«легочный анамнез». Клиническими симпто­
мами заболевания являются кашель с гнойной
мокротой, кровохарканье, одышка, частые
повышения температуры тела.
Расширение главных бронхов плохо заметно
на обычных рентгенограммах. Томография
дает возможность получить более отчетливое
представление о размерах трахеи и бронхов.
При бронхоскопии определяются необычно
большие размеры трахеи и крупных бронхов,
что порой затрудняет ориентировку. В ре­
зультате пролабирования задней стенки тра­
хеи и большого диаметра ее бронхов возникает
недостаточная освещенность при исследова­
нии. У некоторых больных в мембранозной
части трахеи обнаруживаются мешковидные
впячивания, но нередко эти изменения при
эндоскопии ускользают от внимания исследо­
вателя.
Основным методом диагностики является
бронхография. Расширенные трахея и бронхи
медленно заполняются контрастным веществом.
Дыхательные движения трахеобронхиального
дерева отсутствуют или мало заметны. При
этом хорошо видны очертания трахеи и брон­
хов, а также мешковидных выпячиваний в их
мембранозной части, содержащих «лужицы»
контрастного вещества.
В редких случаях трахея бывает обычных
размеров, а расширены только главные бронхи.
Возможна и обратная картина.
Хирургическое лечение трахеобронхомегалии, как правило, не показано из-за распростра­
ненности процесса.
Дивертикулы трахеи и бронхов. Когда недо­
развитие эластических и мышечных волокон
носит локальный, а не диффузный характер,
образуется не трахеобронхомегалия, а дивер-
Видны сегментарные стенозы сосуда.
128
Рис. 71. Варикозное расширение бронхиальных вен. Селек­
тивная ангиограмма бронхиальных сосудов.
тикулы трахеи или бронхов, которые описаны
как трахеоцеле, воздушный зоб, трахеальная
грыжа [Феофилов Л. Т., 1964; Addington Е.,
1944; Andersen Н., 1953]. При дивертикуле брон­
ха, так же как и трахеи, иногда отмечаются
кашель, кровохарканье и легочные кровотече­
ния, Заболевание необходимо дифференциро­
вать от бронхонодулярного и бронхопищевод­
ного свища.
В случаях осложнений при дивертикуле брон­
ха показана циркулярная или клиновидная его
резекция.
Врожденная лобарная эмфизема легких
описана в литературе под различными назва­
ниями: обструктивная эмфизема, гигантская
эмфизема, гипертрофическая эмфизема.
Большинство авторов врожденную эмфизему
связывают с нарушением проходимости брон­
хов вследствие дефектов развития их хрящей
[Степанов Э. А., 1963]. Указывается на значе­
ние механизма, аналогичного клапану, возни­
кающего при гиперплазии слизистой оболочки
бронха, сдавлении бронха извне артериальным
9 Зак. 0517
протоком или расширенной веной [Fischer Н.
et al., 1952]. Предполагается также наличие
врожденного дефекта сурфактанта, при котором
легкое не спадается на выдохе.
В результате увеличения эмфизематозной
доли остальные отделы легкого сдавливаются
и выключаются из дыхания. Органы средосте­
ния смещаются в противоположную сторону.
В ряде случаев раздутая доля пролабирует в
другую половину грудной клетки через перед­
нее средостение, сдавливая противоположное
легкое.
Диагностика трудностей не представляет.
Дифференцировать врожденную эмфизему сле­
дует от обтурационной эмфиземы, возникшей
при аспирации инородного тела, напряженной
кисты легкого, спонтанного пневмоторакса,
диафрагмальной грыжи. Лечение заключается
в удалении измененной доли легкого.
Трахеальный бронх. Трахеальный бронх воз­
никает из боковых выростов трахеи, которые
в онтогенезе обычно подвергаются обратному
развитию. Как правило, такой бронх отходит
от правой стенки трахеи и устье его распола­
гается в 5—6 см над бифуркацией. Частота
этой аномалии составляет 0,5—2 % среди про­
чих аномалий.
Трахеальный бронх может заканчиваться
слепо, образуя дивертикул на правой стенке
трахеи, но чаще он вентилирует участок верхней
доли или добавочную трахеальную дольку.
Клинических проявлений обычно не наблюдает­
ся. Практическое значение трахеального брон­
ха состоит в том, что в добавочной трахеаль­
ной дольке часто возникают туберкулез или
бронхоэктазии.
Знание этой аномалии позволяет избежать
во время операции случаев повреждения главного
бронха и сосудов.
Нарушение структуры легочных борозд встре­
чается часто и не является аномалией в полном
смысле. Добавочные щели и борозды не имеют
существенного практического значения, в то
время как слияние отдельных долей затруд­
няет выполнение лобэктомии.
Практическое значение имеет так называе­
мая доля непарной вены (lobus venae azygos).
Она образуется вследствие смещения дуги не­
парной вены в легочную паренхиму и снабжа­
ется бронхами и сосудами переднего или вер­
хушечного сегмента [Гаджиев С. А., 1953;
Богач Г. Ф., 1959]. Непарная вена покрыта
складкой плевры в виде брыжейки, образуя
плевральный мешок, в котором находится уча­
сток легочной ткани верхней доли.
Рентгенологически эта аномалия развития
выявляется в виде затенения, располагающе­
гося в верхнемедиальной части правого лег­
кого над его корнем.
129
Рис. 72. Трахеобронхомегалия.
а — прямая бронхограмма; б — боковая бронхограмма.
При подозрении на долю непарной вены во
время операции следует осторожно выделять
из сращений верхнюю долю, чтобы не повре­
дить непарную вену.
Гипоплазия легких. Гипоплазия легкого —
порок развития, связанный с нарушением фор­
мирования всех элементов его, недоразвитием
бронхов и паренхимы, сосудов малого круга
в сочетании с гипертрофией системного крово­
обращения.
Гипоплазия легкого может быть в форме
«кистозной» или «простой» (без наличия кист
легкого). Нарушения развития малого круга
кровообращения в гипоплазированном легком
наблюдаются в виде гипоплазии кровеносных
сосудов (изолированной или всего легкого),
а также их аплазии. Гипоплазия бронхов мо­
жет сочетаться с кистозными их изменениями,
причем локализация этих изменений довольно
мозаична и может охватывать долевые, сег­
ментарные и субсегментарные бронхи на раз­
личных уровнях.
Гипоплазия легкого сопровождается рядом
функциональных расстройств в системе дыха­
ния и кровообращения, обусловленных не­
полноценной вентиляционной способностью
сегментов легкого. При этом большое значение
имеют объем и степень недоразвития брон­
хиального дерева и паренхимы гипоплазированных участков легких, адекватность крово­
тока в них и степень редукции малого круга
кровообращения (рис. 72).
Течение заболевания обычно доброкачествен­
ное, однако в случае присоединения инфекции
в гипоплазированном легком развивается стой­
кий, трудно поддающийся консервативному
лечению гнойный очаг. Течение инфекционно­
го процесса, как правило, хроническое, и боль­
ные обращаются к врачу с жалобами на суб­
фебрильную температуру тела, кашель с мок­
ротой, недомогание. В анамнезе обычно выявля­
ются частые простудные заболевания.
Аускультативно над легкими могут опреде­
ляться рассеянные или локализованные влаж­
ные хрипы. Других патологических изменений
при локальной или изолированной гипоплазии
легкого может не наблюдаться. У больных с
распространенной формой гипоплазии выяв­
130
ляется своеобразная клиническая симптома­
тика в виде смещения границ в сторону недо­
развитого легкого. Над грудиной можно опре­
делить тимпанит, а при аускультации тоны
сердца выслушиваются лучше со стороны спины
и в подлопаточной области (на стороне гипо­
плазии). Над легкими определяется ослаблен­
ное везикулярное дыхание, причем на стороне
поражения оно ослаблено и жесткое. Как пра­
вило, над гипоплазированным легким при
простой форме гипоплазии дыхание не опреде­
ляется. При кистозной гипоплазии над легким
определяются значительно ослабленное ды­
хание и множественные влажные разнокали­
берные хрипы при кашле; при перемене поло­
жения больного изменяются тембр и коли­
чество хрипов.
На обзорных рентгенограммах при изоли­
рованной гипоплазии находят мало выражен­
ную деформацию сосудистого рисунка легких
и может наблюдаться небольшое усиление ри­
сунка корня легкого. При кистозной гипопла­
зии выявляется затенение одной стороны, обус­
ловленное смещением сердца. Позвоночник,
как правило, оказывается на стороне здорового
легкого оголенным. В верхних отделах легоч­
ного поля можно отметить небольшие просвет­
ления.
Диагноз гипоплазии уточняется при бронхо­
графии. При кистозной гипоплазии бронхо­
графическая картина характеризуется нали­
чием развитого бронхиального дерева, в кото­
ром бронхи кистозно изменены на различных
уровнях и в различных сегментах (поликис­
тозное легкое). Для уточнения диагноза забо­
левания и дифференциальной диагностики
кистозной гипоплазии легкого от приобретен­
ных бронхоэктазий необходимо более глубокое
обследование, включающее селективную ангио­
графию легких.
При катетеризации сердца у больных простой
гипоплазией проведение катетера в правое пред­
сердие и правый желудочек выявляет необыч­
ность его положения. При гипоплазии правого
легкого катетер оказывается смещенным резко
вправо, в зону пораженного легкого. Для про­
ведения его в легочную артерию необходимо
концевой отдел катетера переместить враща­
тельным движением по часовой стрелке влево.
При гипоплазии левого легкого наблюдается
картина смещения сердца влево; при этом ствол
легочной артерии резко расширен и непосред­
ственное продолжение его представляет широ­
кая ветвь легочной артерии здорового легкого.
Легочная артерия располагается за тенью серд­
ца. Она узкая, с малым числом ветвлений, конт­
растируется не интенсивно (рис. 73). Обуслов­
лено это тем, что в гипоплазированном легком
происходит замещение кровотока недоразви9’
Рис. 73. Гипоплазия правого легкого. Ангиопульмонограмма.
Видно резкое сужение правой ветви легочной артерии.
того малого круга посредством системного кровообращения из бронхиальных сосудов. Воз­
никающий ретроградный ток крови блокирует
кровоток в малом круге.
В клинической картине гипоплазии легкого
особенности взаимоотношений двух систем его
кровообращения имеют существенное значе­
ние. Возникновение легочных кровохарканий
и кровотечений на фоне хронического воспа­
лительного процесса — явление не редкое и
наблюдается примерно у каждого пятого боль­
ного. Источником таких кровотечений являют­
ся зоны артериовенозных и артериоартериальных коммуникаций двух систем кровообращения
в легких, располагающихся в подслизистом
слое бронхиальной стенки (рис. 74).
Возникающие
расширения бронхиальных
сосудов, высокое давление в аорте обусловли­
вают значительный по объему сброс артериаль­
ной крови в малый круг. Такая компенсация
кровообращения имеет свои пределы, за кото­
рыми происходит декомпенсация.
При кистозной форме гипоплазии сосуды
малого круга в периферических отделах легких
представляются редуцированными, а лобуляр­
ные, прелобулярные и терминальные артерии
охватывают кистозные образования в легком.
Поэтому на ангиограммах становятся более
видными рельеф и контуры множественных
131
Рис. 74. Гипоплазия правого легкого. Селективная ангио­
грамма бронхиальных артерий.
Рис. 75. Кистозная гипоплазия левого легкого. Ангиопульмонограмма. Периферические ветви легочной артерии рас­
полагаются по контурам кист.
мозаично расположенных кист (рис. 75). При
наличии эмфизематозных изменений в паренхи­
ме легкого может наблюдаться увеличение углов
ветвления сосудов до 90—120°. Паренхиматоз­
ная форма кровотока в пораженных отделах
легкого резко ослаблена, а капиллярная фаза,
как правило, не прослеживается. При бронхи­
альной ангиографии наблюдается переток конт­
растного вещества в систему малого круга на
различных уровнях с образованием зон регио­
нарной легочной гипертензии, устанавливае­
мой оксиметрией и барометрией [Попов Ю. А„
1973]. Особенности гемодинамики малого кру­
га кровообращения с образованием шунта кро­
ви слева — направо на уровне малого круга
приводят к развитию легочной гипертензии и
гипертрофии обоих желудочков сердца. Дли­
тельное существование такого шунта ведет
к полному блоку малого круга гипоплазированного легкого.
У больных не отмечается цианоза даже при
поражении всего легкого, в отличие от боль­
ных с аналогичной посегментарной распрост­
раненностью патологического процесса при
приобретенных бронхоэктазиях. Длительное
существование значительного артериального
сброса крови в малый круг кровообращения
приводит первоначально к регионарной, а за­
тем общей гипертензии в малом круге крово­
обращения, гипертрофии правого желудочка
сердца и развитию легочно-сердечной недо­
статочности.
Лечение больных, как правило, оперативное,
заключающееся в удалении гипоплазированных сегментов, доли (при изолированной фор­
ме) или всего легкого (при распространенной
форме простой и кистозной гипоплазии).
Секвестрация легкого. Секвестрация легко­
го — это врожденный порок развития, обуслов­
ленный аномальным развитием части парен­
химы легкого, васкуляризация которой осуще­
ствляется посредством артерии, отходящей от
аорты. При этом отсутствует и функциональ­
ный кровоток в секвестрированном легком.
Существует множество синонимов этого за­
болевания: бронхиопульмональная диссоциа­
132
ция, бронхиопульмональная секвестрация,
врожденная бронхопульмональная киста, внутридолевая секвестрация с аномальным легоч­
ным сосудом, внутридолевая секвестрация лег­
кого, кистозное заболевание легкого с крово­
снабжением артериальной системой, бронхоле­
гочная секвестрация и др.
Современное представление о характере
порока легкого, обусловленного его секвестра­
цией, нашло отражение в классификации М. Мегlier и соавт. (1970). Авторы выделяют типич­
ные внутридолевые и внедолевые формы сек­
вестрации легкого, а также атипичные формы;
последние могут быть неполными — в виде
чистой артериальной или чистой бронхопарен­
химатозной. Кроме неполной формы, выде­
ляют комплексную и неклассическую атипич­
ные секвестрации легких.
Внутридолевая секвестрация легкого локали­
зуется в его паренхиме, а внедолевая — рас­
полагается внелегочно, представляя собой
аберрантное легкое.
Частота секвестрации легкого среди врож­
денной патологии составляет 6,4 %, а среди
больных с неспецифическими заболеваниями
легких — 0,04 % [Coman С. et al., 1973].
Существует несколько теорий формирования
этого порока развития легкого. Причиной сек­
вестрации легочной ткани одни авторы счи­
тают частичную или полную агенезию сегмен­
тарной ветви легочной артерии. Вследствие
этого происходит формирование кровоснаб­
жения этого участка легкого за счет плодных
бронхиальных артерий, отходящих от первич­
ной дорсальной аорты. Один из добавочных
сосудов в последующем развитии плода гипер­
трофируется благодаря повышенному давлению
в аорте, а соответствующий участок легочной
ткани претерпевает фиброзную трансформацию
с образованием в нем кист.
Другая распространенная теория [Pryce D.,
1946] объясняет отделение бронхолегочной
ткани при секвестрации аномалийной артерии,
идущей от аорты. Первичным в развитии пато­
логии считается артериальный компонент сек­
вестрации (добавочная артерия), а отделение
паренхимы — вторичным явлением.
Нарушение кровообращения в секвестриро­
ванном легком связано с тем, что васкуляри­
зация его осуществляется артериальным сосу­
дом.
При этом венозный отток происходит двумя
путями: либо в легочную вену, либо в систему
полунепарной или непарной вены. При веноз­
ном оттоке в легочную вену венозная кровь из
секвестрированной зоны легкого смешивается
с артериальной кровью в легочных венах, и эта
венозная примесь поступает в девые камеры
сердца. Если такой сброс значителен, то в кли­
нической картине будут признаки хронической
артериальной гипоксемии, а также признаки
перегрузки левого желудочка сердца.
В случаях венозного оттока из секвестриро­
ванной зоны в систему непарной и полунепар­
ной вен признаков артериальной гипоксемии
не будет, так как сброс венозной крови из легко­
го происходит в правые камеры сердца. У боль­
ных могут наблюдаться признаки гипертрофии
правого желудочка.
В патогенезе секвестрации легкого вентиля­
ционных нарушений не наблюдается. В слу­
чае присоединения инфекции в зоне секвестра­
ции развивается нагноительный процесс. Воз­
можен прорыв гнойного содержимого в бронх
с отхождением через трахеобронхиальное де­
рево.
Больные с секвестрацией легкого, как правило,
жалоб це предъявляют до тех пор, пока не раз­
вивается воспаление. Признаки заболевания
обычно впервые появляются в юношеском или
зрелом возрасте. Различают три этапа развития
патологического процесса: 1) до прорыва кисты
в бронх и развития нагноения; 2) после разви­
тия нагноения и образования сообщения с брон­
хиальным деревом; 3) после перехода воспа­
лительного процесса на окружающую легочную
паренхиму с развитием пневмосклеротических
изменений и бронхоэктазий.
До прорыва кисты в бронх и развития нагное­
ния в ней больные обычно предъявляют жалобы
на кашель, как правило, сухой, реже со скудным
отделением слизистой мокроты, слабость, одыш­
ку, потливость. Иногда наступают нерезко вы­
раженные обострения с подъемами температу­
ры тела, расценивающиеся как пневмония. Фи­
зикальные данные скудные. Нередко отмечаются
лишь укорочение перкуторного звука под углом
лопатки на стороне пораженного легкого и
ослабление дыхания на этом участке.
После прорыва одной из кист в бронхиальное
дерево и развития нагноения в ней классиче­
ские проявления заболевания характеризуются
в различной мере выраженными признаками
хронического нагноительного процесса. Такие
больные предъявляют жалобы на кашель с
отделением гнойной, иногда зловонной мокро­
ты, боли в груди, слабость, одышку. Периоди­
чески наступают обострения процесса, сопро­
вождающиеся длительной лихорадкой и увели­
чением количества мокроты.
В типичных случаях на рентгенограммах
выявляются затенение ячеистого характера или
воздушные кисты, локализующиеся, как пра­
вило, в заднебазальных отделах легкого. На
томограммах наблюдается связь указанного
затенения с аортой в виде дорожки. При брон­
хографии сегментарные бронхи могут огибать
кистозные образования; при этом зона секвест-
133
Рис. 76. Секвестрация правого легкого.
а — прямая рентгенограмма; б — боковая томограмма: в — брон­
хограмма. На томограмме виден сосуд, отходящий от аорты; на
бронхограмме зона секвестрации не контрастируется.
рации не контрастируется или выявляется
культя бронха, идущего в зоне «секвестра»
(рис. 76). В случаях нагноения и прорыва со­
держимого в трахеобронхиальное дерево при
бронхографии можно получить заполнение
некоторых кистозных образований.
При селективной ангиографии малого круга
в одних случаях в зоне секвестрации выявля­
ется гипоплазия сосудов с равномерным суже­
нием сегментарных артерий, в других — недо­
развитие сосудов.
Прямым доказательством секвестрации лег­
кого является контрастное исследование доба­
вочного сосуда, отходящего от аорты. Для этого
применяют аортографию в грудном ее отделе
или селективное контрастирование добавоч­
ного сосуда, васкуляризирующего зону секве­
страции легкого (рис. 77). Анатомическое поло­
жение этого сосуда вариабельно: он может от­
ходить как от грудной, так и от брюшной аор­
ты, но во всех случаях проходит в легочной
связке.
Дооперационная диагностика внутридолевой
секвестрации особенно важна, так как при вы­
полнении хирургического вмешательства по­
вреждение аберрантного сосуда приводит к вне­
запному профузному кровотечению во время
операции. Поврежденный сосуд сокращается
и уходит в средостение к аорте. Если сечение
сосуда значительное, то кровотечение бывает
смертельным.
Лечение больных с внутридолевой секве­
страцией легкого оперативное. Оно является
радикальным методом, позволяющим добиться
стойкого выздоровления. Типичной операцией
134
Рис. 77. Секвестрация правого легкого. Селективная ангио­
грамма аберрантного сосуда, отходящего от аорты.
а — прямая рентгенограмма; б — боковая ангиограмма.
у таких больных является лобэктомия. При вы­
полнении резекции легкого разделяют сраще­
ния в легочной связке и перевязывают ано­
мальный сосуд.
Внедолевая секвестрация легкого представ­
ляет собой полную эктопию или экстрадолевое
над- или поддиафрагмальное положение фраг­
мента легочной паренхимы, связанного с аор­
той посредством артериальных сосудов. Парен­
хима секвестра может быть кистозно изме­
нена.
Внедолевая секвестрация легкого имеет сино­
нимы: медиастинальное легкое, добавочное
легкое, абдоминальное легкое. Вместе с тем
добавочным легким следует называть аберрант­
ную легочную ткань, которая сообщается с тра­
хеей или главным бронхом, имеет легочное кро­
воснабжение и отдельную плевральную полость.
Findlay, Mair (1951) сообщили о 19 больных,
у которых аберрантная легочная ткань распо­
лагалась около диафрагмы. В 17 наблюдениях
она находилась между нижней долей левого
легкого и диафрагмой; во всех случаях она была
полностью покрыта плеврой, которая не имела
сращений. Артериальное кровоснабжение осу­
ществлялось в 14 наблюдениях от нисходящей
части грудной аорты, в 2 — от брюшной аорты
и по одному наблюдению — отхождение питаю­
щего сосуда от межреберной артерии, диафраг­
мальной артерии и артерии, идущей от надпо­
чечника.
Кисты при внедолевой секвестрации могут
быть как единичными, так и множественными.
Изнутри они выстланы кубическим или цилинд­
рическим эпителием. Стенки их содержат
элементы бронхов и фиброзную ткань. Полость
кисты может быть заполнена шоколадного цвета
жидкостью или гноем, но иногда содержит толь­
ко воздух. Окружающая легочная паренхима
может быть неизмененной, но в тех случаях, ког­
да в кисте развивался нагноительный процесс,
в легочной ткани возникают в различной мере
выраженные инфильтративные и склеротиче­
ские изменения.
Кистозно-измененные участки легкого снаб­
жаются кровью по одной или нескольким ано­
мальным артериям. Венозный отток происходит
либо в нижнюю легочную вену, либо в непарную
вену. Возможен и смешанный тип венозного
оттока.
При внедолевой секвестрации в случае разви­
тия нагноительного процесса показано хирур­
135
гическое лечение — удаление внедолевого сек­
вестра.
Трахео- и бронхопищеводные свищи пред­
ставляют собой один их тяжких пороков раз­
вития. По данным литературы, они встречаются
у одного из 2500 новорожденных [Баиров Г. А.,
1963].
Наличие врожденного соустья между пище­
водом и трахеей без других аномалий этих
органов бывает очень редко. Различают разные
варианты таких свищей. Среди них чаще встре­
чается короткий и широкий свищевой ход.
Свищи, как правило, локализуются высоко, на
уровне VII шейного или I грудного позвонка.
Наличие свищевого хода между пищеводом и
трахеей неминуемо ведет к аспирации жидко­
сти и развитию ателектаза и пневмоний. Своев­
ременно не распознанный и не леченный свищ
обычно является причиной гибели ребенка в
первые дни после рождения. Только очень уз­
кое соустье иногда протекает бессимптомно.
В таких случаях дети могут жить длительное
время.
Чаще приходится иметь дело с сочетанием
трахеопищеводного свища с врожденной не­
проходимостью (атрезией) пищевода. Обычно
наблюдается атрезия пищевода со слепым верх­
ним сегментом и сообщающимся с дыхательны­
ми путями нижним (95 %). Расположение сви­
ща непостоянно, но чаще он бывает на 1 —1,5 см
выше бифуркации трахеи. Иногда нижний отре­
зок пищевода сообщается с бифуркацией тра­
хеи, и очень редко с трахеей сообщается только
верхний сегмент, а нижний заканчивается слепо.
Первым признаком атрезии пищевода, соче­
тающейся со свищом трахеи, является выделе­
ние из носа и рта большого количества пенистой
слизи. Слизь временами имеет желтушную ок­
раску, что зависит от забрасывания желчи
в трахею через свищ дистального сегмента пище­
вода. В этих случаях сразу же выявляются
и признаки нарушения дыхания (цианоз, обиль­
ные хрипы в легких) и аритмия. Развивается
пневмония.
При подозрении на атрезию пищевода и тра­
хеопищеводный свищ диагностика осуществля­
ется с помощью зондирования пищевода. Про­
движение при этом резинового катетера по пи­
щеводу встречает сопротивление, а при введе­
нии воздуха через катетер он выходит с шумом
через нос или через рот. Диагноз подтвержда­
ется контрастным исследованием пищевода.
Лечение этой аномалии оперативное. Успех
вмешательства во многом зависит от состояния
новорожденного и подготовки к операции.
Операция состоит в ликвидации бронхопище­
водного свища и наложении прямого анасто­
моза концов пищевода. При бронхиальном диа­
стазе между верхним и нижним сегментами
пищевода на первом этапе разъединяют тра­
хеопищеводный свищ и верхний сегмент пище­
вода, который выводят на шею. Одновременно
проводят гастростомию для питания ребенка.
На втором этапе выполняют пластику пищевода
тонкой кишкой.
У взрослых бронхопищеводные свищи встре­
чаются редко. Больные предъявляют жалобы
на кашель, возникающий преимущественно
после приема жидкой пищи. Редко они откаш­
ливают твердую пищу. В анамнезе обычно от­
мечается рецидивирующая пневмония. Диагноз
подтверждается эзофагоскопией. При брон­
хографии свищ не всегда заполняется контраст­
ным веществом. Нередко выявляются вторичные
бронхоэктазии в нижней доле. Лечение опера­
тивное, состоит в разъединении свища, а при
необходимости — и резекции доли легкого.
Аномальное впадение легочных вен. Впаде­
ние легочных вен в общую венозную систему
представляет сравнительно редкую аномалию,
которая встречается примерно у 1 % больных
с пороками развития легких.
Различают полный и частичный аномальный
дренаж легочных вен. В свою очередь, каждая
из этих групп подразделяется на следующие
подгруппы: 1) аномальное впадение легочных
вен в левую безымянную или верхнюю полую
вену, а также в одну из ветвей последней; 2)
впадение легочных вен в правое предсердие или
коронарный синус; 3) соединение легочных вен
с системой воротной вены или непосредственно
с нижней полой веной; 4) комбинированное
впадение легочных вен на двух или трех уров­
нях (рис. 78).
Аномальное впадение нескольких легочных
вен в правое предсердие, как правило, сочета­
ется с дефектом межпредсердной перегород­
ки, но может быть и в изолированном виде.
Наиболее часто встречается аномальное впа­
дение одной или двух правых легочных вен
в правое предсердие или в верхнюю полую
вену, реже — в нижнюю полую вену, персисти­
рующую левую безымянную вену, коронарный
синус. Аномальное впадение левых легочных
вен наблюдается редко.
При аномальном дренировании крови из ле­
гочных вен гемодинамика во многом сходна с
таковой при нарушениях кровообращения,
которые наблюдаются у больных с изолирован­
ными дефектами межпредсердной перегород­
ки. Однако величина сброса крови слева на­
право у этих больных обычно значительнее,
чем у больных с изолированным дефектом меж­
предсердной перегородки.
Заболевание обнаруживается в раннем дет­
ском возрасте. Выявлению порока нередко спо­
собствует воспаление легкого, имеющего нор­
мальное дренирование вен. У таких больных
136
Рис. 78. Схематическое изображение вариантов аномаль­
ного впадения легочных вен.
I — верхняя легочная вена впадает в верхнюю полую вену; II —
верхняя легочная вена впадает в правое предсердие; III — ниж­
няя легочная вена впадает в нижнюю полую вену; IV — легоч­
ная вена впадает в коронарный синус; V — легочная вена впа­
дает в безымянную вену; VI — легочная вена впадает в правое
предсердие, имеющее дефект межпредсердной перегородки; VII —
легочная вена впадает в печеночную вену.
нарушение процессов оксигенации крови в по­
раженном легком сопровождается более тяже­
лыми расстройствами дыхания и кровообра­
щения, что нередко приводит к летальному
исходу.
Рентгенологическое исследование позволяет
выявить ряд симптомов, патогномоничных для
аномального впадения легочных вен. При рент­
геноскопии таких больных видно, что корни
легких, легочный ствол и правый желудочек
усиленно пульсируют. Легочный рисунок за
счет переполнения артериального русла зна­
чительно усилен. На обзорных рентгенограм­
мах в корне правого легкого определяются
гомогенные тени, которые переходят непосред­
ственно в тень правого предсердия. Часто уда­
ется обнаружить расширенные легочные вены,
слившиеся в ствол, который впадает в нижнюю
полую вену; легочный венозный ствол распола­
гается параллельно правому нижнему контуру
сердца. Корень правого легкого более расширен
по сравнению с левым. Часто выявляются до­
полнительные сосудистые тени в корне и парен­
химе легкого, которые сливаются с тенью пра­
вого предсердия. Предсердие увеличено, верх­
няя полая вена и аномально дренирующиеся
легочные вены расширены. Сердце расширено
в обе стороны. Легочная артерия значительно
расширена и выбухает по левому контуру сердца.
Данные зондирования сердца представля­
ются наиболее ценными для диагностики этого
порока. Особую достоверность диагноза пред­
ставляет факт проведения зонда из полых вен
в одну из легочных вен; при этом конец зонда
137
появляется вне сердечно-сосудистой тени. Ана­
лиз крови, взятой в этой позиции зонда, убе­
дительно показывает, что его конец находится
в аномально впадающей легочной вене. При
ангиокардиографии из легочной артерии или
правого желудочка происходит одновременное
контрастирование обоих предсердий. Заполне­
ние легочных вен контрастным веществом поз­
воляет проследить с большей точностью их
топографию и определить уровень их дрениро­
вания. Косвенным признаком этого порока явля­
ется длительная циркуляция контрастного ве­
щества в малом круге кровообращения.
Хирургическая коррекция этого порока воз­
можна лишь в условиях искусственного кро­
вообращения и заключается в пластическом
переводе венозного коллектора из правого пред­
сердия в левое. Однако в ряде случаев аномаль­
ное впадение легочных вен может быть ликви­
дировано прямой пересадкой их устьев в левое
предсердие. В редких случаях, при высоком впа­
дении правой верхнедолевой легочной вены
в верхнюю полую вену, когда исключается тех­
ническая возможность восстановления пра­
вильного оттока венозной крови, может быть
выполнена верхняя лобэктомия. Правосторон­
няя нижняя лобэктомия может быть предпри­
нята в ситуации сложного низкого впадения
нижнедолевой легочной вены в нижнюю полую.
Поскольку аномальное впадение легочных
вен часто сочетается в различными видами де­
фектов межпредсердной перегородки, коррек­
ция порока требует одновременного устране­
ния межпредсердного соустья.
Лимфангиэктазии. Этиология заболевания
неясна. Оно наблюдается чаще у новорожден­
ных. Существуют несколько терминов для обоз­
начения этой болезни (диффузный ангиоматоз
легких, врожденная дилатация лимфатической
системы легких и др.).
Как показывает анализ литературных дан­
ных, дети с врожденной дилатацией лимфати­
ческой системы легких рождаются в тяжелом
состоянии одышки и цианоза, которые прогрес­
сируют; острая дыхательная недостаточность
приводит к гибели детей, как правило, в бли­
жайшие сутки после рождения (63 %). На про­
тяжении 2 мес погибает 88 % новорожден­
ных, лишь единицы доживают до 5-летнего воз­
раста.
В основном этот порок обнаруживается
у недоношенных детей. Роль наследственных
факторов не установлена.
Высказывается гипотеза о том, что лимфати­
ческие эктазии легких образуются, так же как
и кисты бронхиального дерева, вследствие ин­
волюции висцеральной плевры.
Лимфатическая система легких в норме за­
нимает положение субплевральной ткани и
междольковой субстанции. Предполагается
поэтому, что лимфатическая система легких
играет определенную роль в формировании
долей легких и нарушение развития ее влечет
за собой образование лимфатических кист,
интимно связанных с сосудами и бронхами
[Fronstin М. et al„ 1967]. Можно предполо­
жить, что в патогенетической цепи развиваю­
щейся катастрофы у новорожденных с дилата­
цией их лимфатической системы имеют значе­
ние особенности перфузионных соотношений
легких на уровне его микроциркуляционного
звена, при котором высокий приток и обра­
зование лимфы сочетаются с неадекватным ее
оттоком. Это способствует дилатации лимфа­
тических сосудов и развитию перемещения
жидкостных сред из лимфатических щелей
в альвеолы.
Заболевание протекает остро, сопровожда­
ется тяжелой одышкой и цианозом с момента
рождения ребенка. Симптомы острого респира­
торного заболевания прогрессируют, и, несмот­
ря на проводимую интенсивную терапию, боль­
ные погибают.
Прогноз заболевания неблагоприятный.
Лечение — симптоматическое.
Недостаточность клапанов лимфатических
сосудов легких. Заболевание по механизму раз­
вития в известной степени может быть сравне­
но с патологией, обусловленной недостаточно­
стью клапанов вен конечностей. Теоретическое
рассмотрение вопроса указывает, что в про­
цессе акта дыхания не происходит адекватного
перемещения лимфы от альвеолярной зоны
к сосудам области средостения и в их лимфа­
тические узлы. Возникновение обратного тока
лимфы, лимфостаза в зоне недостаточности
клапанов лимфатических сосудов может сопро­
вождаться развитием локальной гипертензии
лимфатической системы легких.
Клинические проявления заболевания сход­
ны с врожденной дилатацией лимфатической
системы легких, однако они менее выражены,
так как процесс лимфостаза легких носит, как
правило, локализованный характер. Степень вы­
раженности одышки и цианоза зависит от рас­
пространенности патологических изменений.
При рентгенологическом исследовании груд­
ной клетки выявляются локальные зоны пони­
жения прозрачности легочной ткани. В случае
развития пневмонии выявляются очаги ин­
фильтрации, соответствующие фокусам воспа­
ления.
Лечение до настоящего времени остается
преимущественно консервативным, направлен­
ным на борьбу с гипоксией, на нормализацию
КОС, pH крови, ликвидацию дыхательной не­
достаточности, профилактику бактериальной
пневмонии.
138
Первичный иммунодефицит
легких может
проявляться в виде гуморальной, клеточной и
комбинированной форм.
Гуморальные формы иммунодефицита харак­
теризуются тем, что в организме больных не
происходит адекватного ответа на инфекци­
онное начало вследствие того, что нет выработ­
ки антител ко многим видам бактерий. Поэтому
у новорожденных со 2—3-го месяцев жизни
развивается клиническая картина хрониче­
ского септического процесса с локализацией
первичного очага, как правило, в легких.
Клинические проявления сопровождаются
лейкоцитозом, снижением или полным отсут­
ствием у-глобулиновой фракции белков. Воспа­
лительные процессы в легких могут сочетаться
с бронхиальной астмой; развиваются гнойные
очаги в костях, суставах, отит, менингит.
Для дисгаммаглобулинемии характерно раз­
витие рецидивирующих бронхолегочных забо­
леваний воспалительной природы, а также ки­
шечные инфекции, которые по клиническим
признакам селективного дефицита иммуногло­
булинов разделяют на три типа: дефицит IgG
и IgA с повышением IgM (первый тип), сниже­
ние IgM и IgA (второй тип) или изолирован­
ный дефицит IgA (третий тип). У больных
развивается предрасположенность к аутоим­
мунным процессам, нередко сопровождающая­
ся поражением почек, апластической или гемо­
литической анемией, тромбоцитопенией.
При развитии аплазии вилочковой железы,
полной клеточной иммунологической недоста­
точности, часто сочетающейся с врожденными
пороками сердца (синдром Di George), дети
погибают в первые два года жизни от инфек­
ции.
Наследственный алимфоцитоз обусловлен
нарушением процессов созревания лимфоци­
тов. В результате у детей в раннем возрасте
развивается септикопиемия с проявлением
гнойных очагов в легких и других внутренних
органах, а также на коже. Нередко у таких
больных присоединяется кандидоз различных
органов.
Лимфопеническая агаммаглобулинемия мо­
жет протекать с полным или частичным пора­
жением клеточных и гуморальных факторов
иммунитета. Диагноз заболевания устанавли­
вается при полном иммунологическом обсле­
довании. Заболевание проявляется в первые
месяцы жизни ребенка, сопровождается диа­
реей, пневмониями и другими инфекционными
проявлениями. Прогноз заболевания неблаго­
приятный, лечение симптоматическое.
Муковисцидоз (альвеолярный протеиноз
легких) — наследственное заболевание, вы­
званное нарушением функции эндокринных
желез и сопровождающееся образованием сли-
зи повышенной вязкости, сочетающееся с из­
менениями ее электролитного состава.
Этиология заболевания неясна. Затруднение
элиминации патологически измененной слизи
сопровождается закупоркойI выводных про­
токов железистого органа, в частности желудочно-кишечного тракта и (или) бронхиаль­
ного дерева. В результате нарушения выведения секрета в пораженном органе развивается
вторичное воспаление, Значительные изменения при этом претерпевают бронхиальное
дерево и легкие в целом, так как застой секре­
та бронхиального дерева приводит к возникно­
вению тяжелого воспалительного процесса в
слизистой оболочке бронхов, что в большей
степени ухудшает дренажную функцию брон­
хов. В повышении вязкости мокроты и брон­
хиального секрета известную роль играют сни­
жение в них концентрации натрия и калия и
повышение фосфора.
Различают четыре разновидности клиниче­
ского течения муковисцидоза: мекониальный
илеус, кишечную форму, легочно-кишечную
форму и бронхолегочную форму.
Легочно-кишечная форма характеризуется
сочетанием поражения желудочно-кишечно­
го тракта и бронхолегочной системы. У детей
развиваются гепатолиенальный синдром, одыш­
ка, общее отставание в развитии.
Бронхолегочная форма характеризуется
признаками поражения органов дыхания, воз­
никающими с первых лет жизни ребенка. Дли­
тельно текущие повторные, плохо поддающиеся
лечению пневмонии и бронхиты выступают на
передний план в клинической картине заболе­
вания. При этом кашель носит навязчивый ха­
рактер с приступами. Мокрота может быть
слизисто-гнойной или гнойной, что зависит от
степени выраженности воспалительного про­
цесса. При бронхоскопии выявляется эндоброн­
хит, причем считается характерным наличие
гнойных пробок в устьях расширенных брон­
хиальных желез.
Лечение муковисцидоза симптоматическое.
Применяется лаваж бронхов с муколитиками.
У больных с локализованной формой заболева­
ния, развитием бронхоэктазий показано опера­
тивное лечение.
Нарушение сурфактантной системы легких
(болезнь гиалиновых мембран). Этиология
заболевания неясна. Патогенез его связан с им­
мунологическим дефектом развития альвеоляр­
ных клеток II типа, которые вырабатывают сур­
фактант. До 36 нед беременности продукция
его низкая, а активный синтез осуществляется
только в поздние сроки — с 36-й недели. По
этой причине у новорожденных (как правило,
рожденных преждевременно) часто развивает­
ся недостаточность сурфактантной системы
139
легких, сопровождающаяся респираторным
дистресс-синдромом.
В нарушении продукции и обмена веществ
в легких большое значение имеет изменение
кровообращения в системе легочной артерии.
Различного рода нарушения притока крови из
системы легочной артерии к альвеолярной тка­
ни оказывают влияние на тканевой обмен и
функцию альвеолярных клеток типа И, ответ­
ственных за продукцию сурфактанта легких.
Гипоксия альвеол приводит к нарушению про­
дукции сурфактанта. Гипоксия может зави­
сеть и от многих других факторов (особенно­
стей течения поздних сроков беременности,
особенностей родов).
После рождения у ребенка с низким уровнем
сурфактанта легких не происходит адекватного
расправления легкого при первом крике, как
это наблюдается в норме, и развиваются явле­
ния респираторного дистресс-синдрома, харак­
теризующиеся прогрессирующей дыхательной
недостаточностью, гипоксией, метаболическим
и респираторным ацидозом. У новорожденного
наблюдается короткий вдох, хотя дыхательные
мышцы развивают большое усилие. Высокое
сопротивление для растяжения легких (из-за
низкого уровня сурфактанта) ведет к разви­
тию ателектазов, образованию в альвеолярных
ходах и респираторных альвеолах пленок, кото­
рые препятствуют нормальному газообмену.
Эти пленки и называют гиалиновыми мембра­
нами.
Заболевание носит прогрессирующий харак­
тер, и большинство новорожденных, несмотря
на проводимую интенсивную терапию, погиба­
ют в первые 2—5 сут.
Интенсивная терапия направлена на поддер­
жание вентиляции легких, коррекцию метабо­
лизма, кровообращения и, в частности, легоч­
ного кровотока. Кроме медикаментозных
средств, направленных на нормализацию легоч­
ного кровотока, у новорожденных с открытым
артериальным протоком проводят по срочным
показаниям оперативное его закрытие.
Профилактические меры по предупрежде­
нию развития недостаточности сурфактант­
ной системы должны проводиться на всех эта­
пах родовспоможения.
Глава kz
ОСТРЫЕ АБСЦЕССЫ
И ГАНГРЕНА ЛЕГКИХ
До настоящего времени отсутствуют обще­
принятые критерии, по которым острые деструк­
тивные процессы в легких можно было бы отне­
сти к той или иной классификационной кате­
гории (гангрена, гангренозный абсцесс, абсцесс).
Анализ материала клиники госпитальной
хирургии, охватывающего наблюдения за 509
больными с острыми гнойными абсцессами и
170 больными гангреной легких, позволяет вы­
сказать собственную точку зрения на существо
патологического процесса при гангрене и абс­
цессе.
Г ангрена легкого — это гнойно-гнилостный
некроз значительного участка легочной ткани,
чаще доли, 2 долей или всего легкого, без чет­
ких признаков демаркации, имеющий тенден­
цию к дальнейшему распространению и прояв­
ляющийся крайне тяжелым общим состоянием
больного.
Гангренозный абсцесс — гнойно-гнилостный
некроз участка легочной ткани, но имеющий
тенденцию к секвестрации и отграничению от
непораженных участков легочной ткани, что
является свидетельством более благоприятного,
чем гангрена, течения заболевания и позволяет
определить его как ограниченную гангрену.
Когда говорят об абсцессе легких, имеют
в виду гнойный или гнилостный распад некроти­
ческих участков легочной ткани, чаще в преде­
лах сегмента с наличием одной или нескольких
полостей деструкции, заполненных густым или
жидким гноем и окруженных перифокальной
воспалительной инфильтрацией легочной ткани.
Эта гнойная полость, как правило, отграничена
от непораженных участков легкого пиогенной
капсулой и в отличие от гангренозного абсцесса
не содержит секвестра.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Причины, способствующие возникновению
острых нагноений легких. Анализ обширной
литературы и наблюдений клиники с очевидно­
стью показывает, что причины и пути развития
легочных нагноений многообразны. Однако,
рассматривая механизм развития различных
по патогенезу видов легочных нагноений, нель­
зя не обратить внимания на обязательное при­
сутствие трех основных факторов, участвующих
в развитии легочных нагноений: 1) нарушения
бронхиальной проходимости; 2) острого ин­
фекционного воспалительного процесса в
легочной паренхиме и 3) нарушения крово­
снабжения, обусловливающего некроз легоч­
ной ткани.
На состоявшемся в 1976 г. в Сан-Франциско
симпозиуме, посвященном проблемам лечения
легочных нагноений, были выделены следующие
основные состояния организма, способствую­
щие возникновению аспирационных пораже­
ний: алкоголизм, наркомания, эпилепсия, трав­
мы головы, сопровождающиеся длительным
бессознательным состоянием, краниоваскулярные расстройства, общая анестезия, т. е. состоя­
ния, сопровождающиеся более или менее выра­
женным нарушением сознания, а также забо­
левания пищевода.
Значительно более частое возникновение
абсцессов и гангрены у алкоголиков и лиц, зло­
употребляющих алкоголем, отмечено многими
авторами [Даниленко М. В. и др., 1974; Митюк И. И., 1974; Углов Ф. Г., 1975; Федо­
ров Б. П., Сахаров В. А., 1977; Васюков В. Я.,
1980]. Характерной особенностью гнойных
осложнений крупозной пневмонии у алкоголи­
ков является быстрое, в течение первых дней,
расплавление легочной ткани с образованием
больших абсцессов.
Хроническая алкогольная интоксикация не
только способствует возникновению аспира­
ционных легочных нагноений из-за подавления
кашлевого рефлекса и снижения уровня созна­
ния, но и пагубно влияет на течение уже раз­
вившегося гнойного процесса в легких. Иссле­
дованиями W. MacFerland, Е. Libre (1963) до­
казано, что у алкоголиков, страдающих инфек­
ционными процессами, значительно снижен
гранулоцитарный резерв костного мозга, подав­
лены механизмы фагоцитоза и других защит­
ных реакций организма. У лиц, страдающих
хроническим алкоголизмом, острые легочные
нагноения, как правило, характеризуются мас­
сивностью поражения легочной ткани, чаще
возникающими пиопневмотораксом и эмпие­
141
мой, а также интоксикационными психозами
[Барков В. А. и др., 1982].
Наши наблюдения подтверждают положе­
ние о том, что острая алкогольная интоксика­
ция является одной из главных причин разви­
тия аспирационных пневмоний, переходящих
в абсцесс или гангрену. Так, 50,3 % из наблю­
давшихся нами больных с острыми абсцессами
легких (509 человек) злоупотребляли алкого­
лем, а 11,7% — страдали хроническим алкого­
лизмом. Среди 170 больных гангреной злоупот­
ребляли алкоголем 55,4 %, страдали хрониче­
ским алкоголизмом — 12,5 %. У 23,2 % боль­
ных гангрена легких диагностирована после
перенесенного алкогольного делирия.
Существует прямая зависимость между ча­
стотой возникновения аспирационных легоч­
ных нагноений и наличием инфекционных оча­
гов в полости рта — кариозные зубы, паро­
донтоз, хронический тонзиллит, синуситы
[Bartlett J. et al., 1975]. Гангренозные процессы
в зубах резко меняют соотношение между ана­
эробной и аэробной флорой полости рта в сто­
рону значительного преобладания анаэробов и,
следовательно, увеличивают возможность аспи­
рации анаэробной микрофлоры.
Как видно из вышеизложенного, пусковым
механизмом в патогенезе острых легочных
нагноений чаще всего являются нарушения
бронхиальной проходимости. Только в усло­
виях безвоздушной легочной ткани, т. е. ате­
лектаза, деятельность микробной флоры может
привести к расстройству кровообращения, не­
крозу и легочному нагноению. Не случайно
подавляющее большинство абсцессов и гангрен
являются аспирационными или постпневмони­
ческими, а при этих типах легочных нагноений
заболевание начинается с нарушений бронхиаль­
ной проходимости и ателектаза.
С целью изучения состояния бронхиальной
проходимости и ее влияния на течение гнойного
процесса в легких контрастированием деструк­
тивной полости через дренажную трубку была
в динамике изучена проходимость дренирую­
щих бронхов у 55 больных острыми абсцессами
и гангреной легких [Лесницкий Л. С., 1970].
Из них у 44 больных сразу же после дрениро­
вания торакоцентезом с помощью кардиотра­
ста, введенного в полость через дренаж, обна­
ружить проходимость дренирующих бронхов
не удалось. Эти данные подтверждают поло­
жение о том, что в начальный период абсцесса
и гангрены легких тяжесть состояния больных
определяется главным образом гнойной инток­
сикацией из-за невозможности эвакуации гноя
и некротических масс из полостей деструкции
естественным путем через дренирующие брон­
хи, проходимость которых нарушена вследствие
воспалительного отека слизистой, обтурации
густым гноем, детритом и мелкими секвестра­
ми легочной ткани. Если иметь в виду, что ни
у одного из больных этой группы антибиотики
не применялись ни местно в полость абсцесса
через дренаж, ни парентерально, то станет оче­
видным, что острый гнойный процесс в легочной
ткани можно ликвидировать главным образом
методами, максимально способствующими по­
стоянной эвакуации гноя и некротических тка­
ней и обеспечивающими хорошее сообщение
полостей деструкции с внешней средой через
дренирующие бронхи.
Нарушения бронхиальной проходимости у
совершенно здоровых людей встречаются, повидимому, очень редко, и аспирация инфициро­
ванного материала в трахеобронхиальное дере­
во не представляет опасности благодаря нор­
мально функционирующим механизмам само­
очищения. Иные условия создаются при хро­
нических заболеваниях органов дыхания —
бронхите, эмфиземе, пневмосклерозе, брон­
хиальной астме, хронической пневмонии.
Из хронических заболеваний легких чаще
всего острым нагноениям легких сопутствует
хроническая пневмония. По данным В. Д. Вы­
шегородцевой (1942), 25 % больных гангре­
ной легких страдали хронической пневмонией.
М. Д. Тушинский (1960) отметил различные
хронические легочные заболевания у половины
из 101 больного гангреной. Все эти больные
наблюдались автором в период, когда не приме­
нялись антибиотики и сульфаниламидные пре­
параты. Среди наблюдавшихся нами больных
острыми абсцессами и гангреной хроническая
пневмония отмечена соответственно у 39 % и
22,9 %.
На связь острых нагноений легких с тяже­
лыми хроническими системными заболеваниями
указывали С. Попкиров (1974), Ф. Г. Углов,
В. Ф. Егиазарян (1976), W. Vainrub и соавт.
(1978). Длительное течение этих заболеваний
приводит к значительному угнетению защитных
сил организма и неблагоприятному течению
возникшего гнойно-деструктивного процесса
в легких. Нередко такие условия создаются
при лечении других заболеваний стероидными
гормонами. Гормональная терапия повышает
чувствительность организма к инфекции, спо­
собствует возрастанию устойчивости микробной
флоры к антибиотикам, снижает уровень вос­
палительных реакций, клеточного и гумораль­
ного иммунитета, обусловливает замедленное
заживление ран вследствие уменьшения про­
лиферации капилляров, образования фибро­
бластов и отложения коллагена [Fishman N.
et al., 1977]. Ф. Г. Углов (1975) наблюдал 10
больных бронхиальной астмой, у которых гор­
мональная терапия осложнилась тяжелыми
поражениями легких с большими участками
142
деструкции легочной ткани. Мы наблюдали 10
случаев гангрены легких у больных бронхиаль­
ной астмой и заболеваниями крови, леченных
кортикостероидными гормонами. Шестеро
из этих больных погибли.
Таким образом, легочные нагноения, а осо­
бенно наиболее тяжелая форма их — гангрена—
развиваются чаще всего на фоне ослабленного
общего состояния организма, вызванного алко­
гольной интоксикацией хроническими воспали­
тельными заболеваниями органов дыхания,
тяжелыми системными заболеваниями, а также
преклонным возрастом. В этих условиях и реа­
лизуется деятельность патогенной микробной
флоры, которая во взаимодействии с наруше­
ниями бронхиальной проходимости и местного
кровообращения являются одной из главных
причин возникновения легочных нагноений.
Микробная флора. Данные литературы по­
следних лет свидетельствуют о существенном
изменении видового состава микробной фло­
ры, определяемой в качестве возбудителя ост­
рых гнойно-деструктивных поражений легких
и плевры. «Повинны» в этом прежде всего анти­
биотики, широкое использование которых при­
вело к значительному уменьшению менее пато­
генных микроорганизмов (пневмококк, в мень­
шей степени стрептококк), к увеличению антибиотикоустойчивости патогенной микрофлоры,
вначале стафилококка, а затем после широкого
внедрения в практику антистафилококковых
антибиотиков, грамотрицательной и анаэроб­
ной флоры [Федоров Б. П., Воль-Эпштейн Г. Л.,
1976; Стручков В. И. и др., 1978; Sherman М.
et al., 1977, и др.]. За период с середины 30-х
до начала 70-х годов частота выделения из
мокроты и гноя пневмококков уменьшилась
с 50 до 12 %, в то время как частота обнару­
жения стафилококков в этих случаях увели­
чилась с 22 до 35 %, а грамотрицательной мик­
рофлоры — с 10 до 56 %.
За период, наступивший после внедрения
антибиотиков в широкую клиническую практи­
ку, изменились не только соотношения частоты
обнаружения различных видов патогенных
микробов при гнойно-деструктивных пораже­
ниях легких. Появились и имеют тенденцию
к увеличению качественно другие виды пато­
генной микробной флоры. Данные литературы
свидетельствуют о том, что острые абсцессы
и гангрена вызываются чаще всего стафилокок­
ком, грамотрицательной флорой и анаэробами.
Ведущее место среди возбудителей острых
гнойно-деструктивных поражений легких за­
нимает гемолитический стафилококк [Сазо­
нов А. М. и др., 1972; Силинын И. А. и др., 1975].
В течение последних 40 лет накопилось до­
статочно доказательств, чтобы считать анаэроб­
ную инфекцию одной из основных причин в
этиологии абсцессов и гангрены легких [Ку­
зин М. И. и др., 1983]. Л. Г. Кузьмина и В. Ф. Егиазарян (1972) при микробиологическом обсле­
довании 200 больных острыми и хроническими
неспецифическими заболеваниями легких в
32 % обнаружили различную анаэробную фло­
ру, но об особенностях клинического течения
заболевания не упоминают. Представители
патогенных видов Clostridia найдены в 5 % слу­
чаев. Стафилококки у этой группы больных
высевались как в аэробных, так и в анаэроб­
ных условиях. Интересно, что в 23 % наблю­
дений первичный рост стафилококков отмечен
лишь в анаэробных условиях.
Доминирующим микроорганизмом, встре­
чающимся у больных острыми абсцессами и
гангреной легких, является, по нашим данным,
стафилококк. В случаях ассоциации микро­
организмов чаще всего встречается сочетание
кокковой флоры и дрожжевых грибов опять
же со стафилококком. Среди наблюдавшихся
нами больных гангреной легких грамотрицательная микробная флора встретилась в 40,4 %
случаев. Микробная флора оказалась нечувст­
вительной ко всем из применявшихся антибио­
тиков у 57,1 % больных. Чаще всего нечувстви­
тельными были кишечная и синегнойная па­
лочки.
По данным многих авторов, абсцессы легких
часто развиваются как осложнение гриппозных
пневмоний. Было замечено, что вирус гриппа не
только поражает эпителий бронхов, но и нару­
шает их дренирующую способность [Пигалевский Б. Е., 1959]. Вызванный вирусом язвен­
ный бронхиолит и массивный легочный отек
с кровоизлияниями облегчают проникновение
патогенной бактериальной флоры. Развитию
некробиотических и некротических изменений
в легочной паренхиме способствует и тромбоз
легочных сосудов, часто возникающий при грип­
позных пневмониях [Давыдовский И. В., 1939;
Бекерман Л. С., 1946]. Анализируя 32 случая
острых абсцессов легких, развившихся после
гриппозных пневмоний, Б. П. Федоров,
Г. Л. Воль-Эпштейн (1976) высказывают пред­
положение о прямом участии гриппозного
вируса в процессе абсцедирования.
К небактериальным инфекционным агентам,
вызывающим пневмонию, относится и мико­
плазма [Levis J., Sheptin С., 1972; Siegler D.,
1973; De Vos M., 1976]. Так же как и вирус грип­
па, микоплазма, вероятнее всего, играет «подго­
товительную» роль — облегчает бактериаль­
ную инвазию благодаря поражению эпителия
верхних дыхательных путей и уменьшению ре­
зистентности организма [Злыдников Д. Н. и
ДР-, 1971].
Пути возникновения абсцессов и гангрены
легких. Абсцессы и гангрена, развивающиеся
143
как осложнение пневмонии, встре­
чаются чаще всего — от 63 до 95 % [Спасо­
кукоцкий С. И., 1938; Андрианов Ю. А. и др.,
1980; Стручков В. И., 1981, и др.]. Гнойными
процессами могут осложняться как бактериаль­
ные (крупозная, очаговая), так и небактериаль­
ные (гриппозная, микоплазмоидная) пневмонии,
протекающие по очаговому или интерстициаль­
ному типам, а также смешанные пневмонии
(вирусно-бактериальные).
Исход в нагноение при крупозной пневмонии
связывается с гиперергическим характером
воспаления и резким нарушением местного
кровообращения. А. И. Абрикосов (1947),
A. И. Струков (1961) полагали, что сам пнев­
мококк может вызвать образование абсцессов,
а И. В. Давыдовский и др. (1956) связывали
абсцедирование при крупозной пневмонии с
вторичным инфицированием патогенной фло­
рой — стафилококками, стрептококками. След­
ствием вторичной инфекции, по мнению этих
авторов, является также и гангрена легких,
которая развивается в результате активного
внедрения в ткани анаэробных возбудителей,
вызывающих некроз.
Осложнения абсцессом и гангреной очаго­
вых пневмоний в прошлом наблюдались даже
чаще, чем крупозных [Этингер Н. Г., 1939].
B. Д. Вышегородцева (1942) отметила, что
у 11 % из 1092 больных очаговой пневмонией
наблюдались абсцессы и гангрена легких. По
данным Н. С. Молчанова, В. В. Ставской (1971),
гнойные осложнения очаговых пневмоний встре­
чались редко. Резкое снижение частоты гной­
ных осложнений при очаговых пневмониях в
настоящее время связано, вероятнее всего,
с использованием антибактериальных препа­
ратов [Kuhn Н. et aL, 1971].
Среди различных видов бактериальных пнев­
моний особенно часто осложняются гнойно­
деструктивными процессами стафилококко­
вые и фридлендеровские пневмонии.
Стафилококковая пневмония может возник­
нуть в любом возрасте, однако наиболее тяже­
лое, нередко молниеносное течение чаще на­
блюдается у детей, пожилых и больных, стра­
дающих хроническими заболеваниями. По дан­
ным С. Л. Либова, К. Ф. Ширяевой (1973)
среди больных стафилококковой пневмонией
взрослые составляли всего 2 %. В последние
годы участились случаи таких пневмоний у
взрослых [Кахидзе С. Я. и др., 1980; Рат­
нер Г. Л. и др., 1980].
Главной особенностью стафилококковых
пневмоний считается их склонность к раннему
образованию кортикальных гнойно-некроти­
ческих очагов в легких, часто прогрессирующих
и приводящих к перфорации участков нагное­
ния в плевральную полость.
Частота фридлендеровских пневмоний в на­
стоящее время колеблется в пределах 0,5—4 %
в структуре причин воспалений легких [Мерзля­
кова М. Т„ 1972].
Заболевание чаще всего возникает у мужчин
в возрасте старше 40 лет, случаи заболевания
у детей очень редки. Характерной особенностью
фридлендеровских пневмоний является очень
частое их осложнение распространенным не­
крозом легочной ткани [Цинзерлинг В. Д., Цинзерлинг А. В., 1963; Sharma G., Chandhry В.,
1967]. Заболевание часто протекает с массивной
секвестрацией омертвевших участков легкого
[Cameron Е., Whitton J., 1977]. Известны случаи,
когда секвестрировались и отделялись с гноем
или во время операции целые доли легкого и даже
все легкое.
Выяснение причин осложненных пневмоний
и тенденции к затяжному их течению является
центральным вопросом в пульмонологии, так
как обусловливает основные тактические прин­
ципы лечения и профилактики заболевания.
Еще М. П. Кончаловский (1937), С. И. Спасоку­
коцкий (1938), И. В. Давыдовский (1939) счи­
тали, что нагноительный процесс в легком чаще
всего развивается при неразрешившейся затяж­
ной пневмонии. Затяжными считаются островозникшие пневмонии, которые не удалось из­
лечить в течение 3 нед с момента возникнове­
ния заболевания [Сильвестров В. П., 1982].
Б. С. Брусиловский, Л. Ф. Курная (1975), ана­
лизируя причины затяжного течения пневмо­
нии у 200 больных, выделили следующие на­
иболее вероятные факторы, способствующие
такому течению: несвоевременно начатое или
неправильно проводимое лечение, наличие сопут­
ствующих внелегочных заболеваний и перене­
сенных в прошлом заболеваний легких, угне­
тение иммунобиологической активности орга­
низма. На затяжное течение острых пневмоний
влияют также профессиональные вредности
(пыль, загазованность, переохлаждение) и,
в меньшей степени, локализация воспаления
в легком.
Исходя из ведущей роли нарушений брон­
хиальной проходимости в возникновении и тече­
нии острых и затяжных пневмоний, лечение их
может считаться современным, если в перечень
обязательных лечебных мероприятий вклю­
чаются методы, направленные на восстанов­
ление и улучшение дренажной функции брон­
хов: лечебные бронхоскопии, ингаляции лекар­
ственных препаратов, промывания трахеоброн­
хиального дерева, бронхоспазмолитики, с по­
мощью которых нередко удается предотвра­
тить развитие абсцесса или гангрены легких
и купировать процесс на стадии абсцедирую­
щей пневмонии [Данович Б. 3., 1971; Коко­
сов А. Н. и др., 1972; Лохвицкий С. В., Ильи­
144
на Л. Б., 1975]. Под абсцедирующей пневмонией
следует понимать отдельную между пневмонией
и абсцессом форму нагноения в легочной тка­
ни, клинически характеризующуюся призна­
ками осложненной пневмонии, а морфологи­
чески — представляющую собой мелкие, до
0,3—0,5 см в диаметре, множественные очаги
гнойно-некротической деструкции, которые
или могут полностью разрешиться (опорожнив­
шись при благоприятных условиях через брон­
хи), или привести к формированию более круп­
ных очагов некроза и деструкции путем слия­
ния мелких, т. е. к образованию абсцесса (ган­
грены).
Если взять пневмонии в целом, не разделяя
их по этиологическому и клинико-морфоло­
гическому признакам, то, по данным различных
авторов, абсцедирование наблюдается в 1,2—
4,3 % случаев [Гукасян А. Г., 1964; Каменьщик Ю. М., Кананина Л. В., 1972; Сороки­
на Г. А., 1975]. По данным Б. П. Федорова,
Г. Воль-Эпштейна (1976), у 37,4 % больных
абсцедирование возникло в период амбулатор­
ного лечения, которое чаще всего ошибочно
проводилось по поводу гриппа или катара дыха­
тельных путей, а пневмония не была диагно­
стирована.
Патогенез постпневмонических абсцессов
и гангрены можно представить следующим
образом. Бронхогенное (чаще всего), гематоген­
ное или лимфогенное инфицирование легоч­
ной ткани вызывает воспаление паренхимы
и мелких бронхов. Нарушение проходимости
мелких бронхов из-за спазма, отека или обту­
рации секретом имеет следствием ателектаз
участков легкого. Инфильтрация и прогресси­
рующий отек тканей вследствие воспаления
приводят к прямому сдавлению воспалитель­
ным инфильтратом мелких кровеносных сосудов
и капилляров, что сопровождается расстрой­
ством кровообращения в воспаленном и безвоз­
душном участке легкого. Нарушения крово­
обращения зависят также и от токсического
воздействия продуктов жизнедеятельности
микробов и воспаления на стенки капилляров
с поражением их структур, от изменения нерв­
ной регуляции кровообращения и трофики ле­
гочной ткани. При дальнейшем прогрессирова­
нии воспаления в легком и сдавлении мелких
сосудов и капилляров нас тупает резкое замед­
ление циркуляции крови, доходящее до стаза
и тромбоза кровеносных сосудов с возникно­
вением некроза участков легочной паренхимы.
Вероятнее всего, эти морфологические изме­
нения в легком имеют своим клиническим экви­
валентом стадию затяжной, осложненной пнев­
монии. Инвазия в омертвевшие участки легко­
го патогенной микрофлоры непосредственно
из обтурированного бронха, из верхних дыха­
10 Зак. 0517
тельных путей и полости рта, лимфогенно или
гематогенно приводит к начинающемуся гной­
ному или гнилостному распаду участков омерт­
вевшего легкого (стадия абсцедирующей пнев­
монии). Преобладание в патокинезе процесса
элементов некроза или гнойного расплавления
предопределяет развитие заболевания по типу
абсцесса или гангрены легкого, что во многом
зависит от состояния реактивности организма
больного.
Аспирационный механизм раз­
вития патологического процесса является од­
ним из ведущих в патогенезе острых нагное­
ний легких. Так же как и при постпневмониче­
ских поражениях, аспирационные легочные
нагноения развиваются вследствие бронхоген­
ного попадания инфекционного начала в лег­
кое. Но если при постпневмонических нагное­
ниях патологический процесс обычно начина­
ется с воспаления в паренхиме и бронхах,
ведущего к нарушению бронхиальной прохо­
димости, ателектазу, расстройству кровооб­
ращения, некрозу и гнойному расплавлению, то
в случаях аспирационных легочных нагноений
патологический процесс начинается с аспира­
ции инфицированного материала, фиксации его
в мелких бронхах или бронхиолах и ателекта­
за. Воспалительный процесс и все последую­
щие стадии его течения вплоть до нагноения
развиваются вторично. В клинической практике
нередко очень трудно отличить постпневмони­
ческие нагноения от аспирационных. Исключе­
ние составляют лишь случаи заболевания, где
факт аспирации точно известен в анамнезе.
Поскольку в патогенезе и течении нагноительных процессов легких ведущая роль при­
надлежит нарушению проходимости бронхов,
аспирационные абсцессы и гангрена легких
развиваются значительно быстрее, чем постпнев­
монические, формирующиеся в течение 3—
4 нед от начала заболевания. Многочисленны­
ми экспериментальными данными доказано,
что аспирационный гнойник в легком форми­
руется через 8—14 дней после аспирации.
Частота аспирационных абсцессов и гангрен
легких, по данным различных авторов, колеб­
лется от 20 до 75 % в структуре вероятных
механизмов их развития. Поскольку факт
аспирации удается установить далеко не всегда,
можно предположить, что аспирационные ле­
гочные нагноения встречаются еще чаще.
В пользу преобладания аспирационного
механизма развития острых нагноений легких
свидетельствуют и данные, полученные при изу­
чении частоты поражения правого и левого
легкого, а также их сегментов. Абсцессы и
гангрена значительно чаще развиваются в пра­
вом легком, короткий и широкий главный бронх
которого, являясь как бы продолжением трахеи,
145
увеличивает вероятность попадания аспириро­
ванного материала именно в правое легкое.
Среди более 1100 больных, наблюдавшихся
в госпитальной хирургической клинике, пора­
жение правого легкого отмечено у 66,2 % боль­
ных. Многочисленными исследованиями, осно­
ванными на большом количестве личных на­
блюдений, было подтверждено более частое
поражение задних сегментов верхних долей
и верхушечных сегментов нижних, бронхи кото­
рых, отходя кзади и кнаружи, являются наибо­
лее доступными для попадания и фиксации в
них аспирированного материала, если человек
лежит на спине или на боку.
Механизм развития аспирационных абсцес­
сов и гангрены легких представляется следую­
щим образом: аспирация в трахеобронхиаль­
ное дерево инородного материала (слизь или
слюна из носоглотки, рвотные массы, желудоч­
ное содержимое и др.) при условии снижения
уровня сознания приводит к фиксации их в мел­
ких бронхах и развитию ателектаза. Кроме
наличия инфицированного материала (чаще
всего анаэробной инфекции из полости рта)
и перечисленных выше состояний организма,
снижающих уровень сознания, большое зна­
чение также имеют сопутствующие хрониче­
ские заболевания легких, изменяющие их нор­
мальную функцию и способствующие развитию
нарушений дренажной функции бронхов и кро­
вообращения. Начинающийся в бронхах воспа­
лительный процесс еще больше нарушает брон­
хиальную проходимость и приводит к развитию
ателектаз-пневмонии. Некоторые авторы эту
стадию заболевания называют пневмонитом
[Smith L., 1976], которая часто просматрива­
ется, так как не имеет четких клинических
признаков. Лишь указания в анамнезе на воз­
можность аспирации могут помочь заподоз­
рить эту стадию заболевания.
Если в стадии ателектаз-пневмонии патоге­
нетическая терапия отсутствует или начата
с опозданием, патологический процесс в ателектазированном участке легкого прогресси­
рует. Возникает некроз безвоздушной легочной
ткани из-за нарушения кровообращения вслед­
ствие тромбоза и сдавления мелких сосудов
воспалительным инфильтратом. Под воздей­
ствием микробов и продуктов их жизнедеятель­
ности начинается гнойный или гнилостный
(в зависимости от резистентности организма
и вида микробной флоры) распад мертвых
тканей с образованием множественных мелких
очагов деструкции.
Среди наблюдавшихся в госпитальной хирур­
гической клинике 509 больных острыми абсцес­
сами и 170 больных гангреной легких аспира­
ционная природа заболевания установлена
соответственно в 65 и 32,9 %.
Частота
гематогенн о-э м б о л и ч ес к и х легочных нагноений относительно не­
велика и, по клиническим данным различных
авторов, колеблется от 0,8 до 9 % [Спасоку­
коцкий С. И., 1938; Васютков В. Я и др., 1980;
Григорян А. В. и др., 1980]. По секционным
данным, частота абсцессов после инфарктов
легких составляет 0,6—4,9 % [Davison А.,
1958]. Среди больных, лечившихся в нашей
клинике, лишь у 0,9 % оказалось возможным
предположить гематогенно-эмболическую при­
роду абсцессов и гангрены легких.
Легочные нагноения развиваются значитель­
но чаще, если инфаркт легочной ткани вызы­
вается септическим эмболом, так как при этом
вследствие нарушения кровообращения и бак­
териального обсеменения тканей происходит
быстрая дезинтеграция инфицированного участ­
ка легкого. J. Macmillan и соавт. (1978), ана­
лизируя результаты обследования 60 больных
с абсцессами легких, развившихся вследствие
септического легочного эмболизма, указал на
следующие наиболее частые источники эмбо­
лов: септический эндокардит, гнойные тромбо­
флебиты вен конечностей и таза, флебиты после
длительной катетеризации периферических
вен, абсцессы различной локализации. Отрыву
инфицированных эмболов и заносу их в легкие
могут способствовать оперативные вмешатель­
ства на инфицированных тканях.
Считается, что развитие гнойных метастазов
в легких и плевре у больных сепсисом наблю­
дается сравнительно редко. Описаны метаста­
тические гнойные поражения легких у больных
с гинекологическим сепсисом [Мельник А. И.,
1971; Полякова Л. М., 1972]. Нами наблюдались
11 больных с острыми гнойно-деструктивными
поражениями легких и плевры, развившимися
как осложнение сепсиса [Лесницкий Л. С.,
1979].
Литературные данные последних лет свиде­
тельствуют о все возрастающем числе гематогенно-эмболических нагноений легких, что
связано, вероятно, с общим ростом заболевае­
мости сепсисом вообще. За период с 1975 по
1980 г. в отечественной литературе опубликова­
ны сведения о 548 случаях метастатических
гнойных поражений легких при сепсисе с ле­
тальностью 36 % [Мустафин Д. Г., 1980].
Асептические инфаркты значительно реже
осложняются нагноением. Более того, асепти­
ческая эмболия не всегда приводит к развитию
самого инфаркта из-за обилия коллатераль­
ного кровообращения. Если инфаркт участка
легочной паренхимы и наступает, то развитие
нагноения происходит вследствие вторичного
бронхогенного инфицирования.
Механизм развития гематогенно-эмболиче­
ских легочных нагноений можно представить
146
следующим образом: закупорка тромбом и ляризацией пораженных участков легкого. Ана­
тромбоз мелких ветвей легочной артерии при­ логичные данные получены Е. В. Ловягиным
(1973), И. Гулачи (1981). На основании полу­
водят к клиновидному геморрагическому ин­
фаркту участка легочной паренхимы с после­ ченных данных судить о причине непроходи­
дующим ее некрозом. Зона некроза подверга­ мости артериальных сосудов пораженной
ется гнойному или гнилостному распаду вслед­ доли при остром абсцессе и гангрене не пред­
ствие обсеменения ее флорой, попавшей в об­ ставляется возможным; вероятнее всего, она
обусловлена тромбозом, а не нарушением струк­
ласть некротических тканей или вместе с септи­
турной целостности артерий. Тромбоз сосудов
ческим эмболом, или вторично, бронхогенно,
легкого, пораженного деструктивным процес­
причем в этом случае нагноительный процесс
сом, ведет к редукции малого круга кровообра­
может развиться и в зоне асептического инфарк­
щения, увеличению общего и легочно-сосудисто­
та. Нарушения кровообращения, способству­
го сопротивления, повышению давления в ле­
ющие некрозу легочной паренхимы, являются
гочной артерии и нагрузки на правый желудо­
одним из центральных звеньев патогенеза
чек сердца, что подтверждается проведенными
острых легочных нагноений. Однако до настоя­
в клинике исследованиями центральной гемоди­
щего времени не выяснены механизмы возник­
намики.
новения некроза.
Доказано в эксперименте и подтверждено
Под обтурационным нагноени­
ем легких принято понимать гнойно-дест­
в клинике [Углов Ф. Г., 1948; MacMilian J. et
руктивный процесс, обусловленный закупоркой
al., 1978], что перевязка ветвей легочной арте­
бронха каким-либо случайно попавшим в него
рии или всего ее ствола не вызывает инфаркт
инородным телом, доброкачественной или зло­
легкого вследствие функционирования прека­
качественной опухолью, развивающейся из
пиллярных анастомозов между легочной и брон­
стенки бронха, или опухолью, сдавливающей
хиальной артериями. В то же время изолиро­
бронх извне, а также стенозом бронха вслед­
ванная перевязка легочных вен ведет к более
ствие различных воспалительных процессов
выраженным изменениям: чаще всего к гемор­
в его стенке.
рагическому инфаркту легких, кровоизлияниям
Частота легочных нагноений вследствие
в паренхиму, но тоже не всегда к некрозу, хотя
обтурации бронха инородным телом колеблется
случаи омертвения легкого вследствие тром­
от 1,5 до 23 % от общего количества наблю­
боза вен известны в клинической практике.
давшихся больных [Бакулев А. Н., Колесни­
Некроз и влажная гангрена легкого значитель­
ков Р. С., 1955; Shinoi К., 1960; Bernard W. et
но чаще возникают при одновременной пере­
al., 1962]. Сообщения последних лет, вышед­
вязке вены и артерии.
шие из специализированных клиник, где более
Трудно определенно судить о том, наруше­
широко применялся бронхоскопический конт­
ния в какой системе легочного кровотока —
роль, свидетельствуют о малой частоте обтура­
артериальной (включая бронхиальную) или ве­
ционных абсцессов и гангрен после аспирации
нозной — играют ведущую роль в возникнове­
инородных тел. Так, среди наблюдавшихся
нии некроза легочной ткани. Предположитель­
в нашей клинике больных с абсцессами легких
но можно считать, что потенциально более опас­
аспирация инородных тел как причина заболе­
ными для развития некроза легочной ткани
вания отмечена лишь у 0,3 %.
являются нарушения венозного оттока. Тромбоз
Значительно чаще легочные нагноения раз­
легочных вен чаще имеет патологические по­
виваются вследствие опухолевой обтурации
следствия еще и потому, что ведет к расстрой­
бронхов и ателектаза. Так, среди 477 больных,
ству бронхиального кровотока, поскольку отток
наблюдавшихся R. Brock (1952), рак бронха
крови из бронхиальных сосудов осуществля­
был причиной абсцессов у 83 (17,5 %) пациен­
ется, как правило, в легочные вены [Плеша­
тов. По наблюдениям D. Waterman и соавт.
ков В. Т., 1949].
(1967), из 464 больных с абсцессами легких
Все это с очевидностью определяет необхо­
у 187 (40,5 %) были «раковые» абсцессы. В на­
димость более глубоких специальных исследо­
стоящее время, когда диагностика рака легкого
ваний кровотока в сосудах легких при воспа­
лении, некрозе и нагноении. Селективная ангио­ стала более совершенной и, следовательно,
более ранней, число таких абсцессов сокра­
графия с целью изучения кровотока в пора­
тилось. По материалам нашей клиники, такие
женном легком нами была выполнена у 57 боль­
обтурационные легочные нагноения отмечены
ных (из них у 13 была распространенная ган­
лишь у 0,4 % больных.
грена). Легочная артерия пораженного легкого
Гораздо реже встречаются и поэтому труд­
катетеризировалась через бедренную вену.
нее диагностируются обтурации бронха добро­
Во всех случаях были обнаружены признаки
качественными опухолями, а также стенозы
резкого нарушения кровообращения: обрыв
бронха, вызванные различными воспалительартерии, питающей пораженную долю, с аваску10 *
147
ними процессами. Рубцовый стеноз бронха
часто возникает на почве туберкулезного брон­
хоаденита. Наиболее уязвимым для сдавления
лимфатическими узлами является бронх сред­
ней доли. Вследствие стеноза среднедолевого
бронха в средней доле может возникнуть ате­
лектаз с последующим развитием в ней нагное­
ния. Аналогичный механизм возникновения
обтурационного абсцесса и при окклюзии дру­
гих участков бронхиального дерева.
Посттравматические абсцессы и
гангрену легких можно разделить на две группы:
после повреждений непроникающих (ушибы,
сотрясения и сдавления) и после проникающих
ранений (пулевые, осколочные, ранения холод­
ным оружием). По данным Е. А. Вагнера и соавт.
(1981), посттравматические легочно-плевраль ­
ные нагноения составляют 10 % от гнойных
заболеваний легких и плевры.
Закрытая травма грудной клетки очень редко
сопровождается развитием нагноения в легоч­
ной паренхиме. Даже при множественных пе­
реломах ребер с повреждением легкого гемото­
ракс чаще всего стерилен. Нагноение может
возникнуть, если будут повреждены крупные
бронхи, в которых, как правило, имеется микро­
флора. Анализируя материал периода Великой
Отечественной войны, А. О. Берзин (1950)
ни разу не отметил возникновение острых гной­
ников легкого после закрытой травмы груд­
ной клетки. Среди больных, наблюдавшихся
в клинике, развитие абсцессов было связано
с закрытой травмой груди лишь у 5 (0,5 %)
больных.
Абсцессы и гангрена легких, развивающиеся
на почве огнестрельных ранений, также встре­
чаются редко. По данным, опубликованным
в «Опыте советской медицины в Великой Оте­
чественной войне 1941 —1945 гг.», они соста­
вили 0,47 % от всех ранений в грудь и 1,1 %
по отношению к проникающим ранениям в
грудь. Среди раненых с открытым пневмоторак­
сом абсцессы и гангрена отмечены в 1,9 % слу­
чаев [Колесников И. С., 1950].
Сроки возникновения легочных нагноений
после огнестрельных ранений различны. Ча­
стота ранних абсцессов легких за период второй
мировой войны составила 0,24—2 % от всех
ранений в грудную клетку [Тальман И. М.,
1946; Jakobs S., Barke L„ 1946]. Ранние легоч­
ные нагноения часто остаются нераспознан­
ными, так как имеются условия для спонтан­
ного опорожнения сформировавшегося гной­
ника в плевральную полость с образованием
эмпиемы плевры или бронхиального свища.
Абсцессы после огнестрельных ранений могут
возникнуть через несколько месяцев и даже
лет после травмы. Одним из наиболее частых
источников инфекции, ведущих к образованию
поздних абсцессов, являются инородные тела,
застрявшие по ходу раневого канала (ранящий
снаряд, костные осколки, обрывки одежды),
содержащие в 60—80 % случаев самую раз­
нообразную патогенную аэробную и анаэроб­
ную микрофлору.
Мелкие инородные тела нередко «вживают»
и долго ничем не проявляют себя клинически.
Вокруг крупных инородных тел (чаще всего
осколков), как правило, постоянно поддержи­
вается воспалительный процесс, который может
закончиться нагноением и формированием
хронического абсцесса с полостью, на дне или
в стенке которой находится инородное тело.
Частота таких абсцессов колеблется от 4,8 до
17 % [Колесов А. П., Толузаков В. Л., 1966,
и др.]. Среди наблюдавшихся в клинике боль­
ных они составили 4,2 %.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
И ДИАГНОСТИКА
Клиническая симптоматика острых абсцессов
и гангрены легких разнообразна и зависит от
индивидуальных особенностей организма,
объема некротизированной легочной ткани,
характера и интенсивности его распада, стадии
заболевания, возникающих осложнений, нали­
чия или отсутствия сопутствующих заболеваний.
Вначале заболевание чаще всего расценива­
ется как грипп или респираторное заболева­
ние, а у больных хронической пневмонией — как
очередное ее обострение. Неэффективность
амбулаторного лечения в течение нескольких
дней, продолжающаяся высокая температура,
усиление болевых ощущений в грудной клетке,
а иногда и отхождение гнойной мокроты в такие
ранние сроки вынуждают госпитализировать
больных в терапевтические стационары. Отме­
чаются высокая температура, слабость, боли
в грудной клетке, укорочение перкуторного звука
над зоной поражения, ослабление дыхатель­
ных шумов — признаки, которые всегда долж­
ны настроить врача в отношении возможности
дальнейшего прогрессирования патологического
процесса, трактуемого в этот период чаще всего
как сливная пневмония, и перехода ее в нагно­
ение.
Первый тип абсцедирования характеризует­
ся поначалу благоприятной динамикой пнев­
монического процесса, наступлением кризиса,
после чего вновь возникают ухудшение состоя­
ния, повышение температуры, усиление болей
в грудной клетке с последующим выделением
гнойной мокроты. Абсцесс при этом формиру­
ется через 12—20 дней после начала пневмо­
нии. Второй тип клинического течения при абсце­
дировании характеризуется симптомами затя­
нувшейся пневмонии и безуспешностью про­
148
водимого лечения: температура тела в тече­
ние длительного времени держится на высоких
цифрах, постепенно появляется и увеличива­
ется количество гнойной мокроты. Формирова­
ние легочного гнойника происходит в течение
20—30 дней от начала пневмонии. Третий тип
абсцедирования характеризуется быстротой
развития гнойно-деструктивного процесса в
легком, когда у больных уже с первых дней
заболевания отмечается выделение гнойной,
нередко зловонной мокроты, не характерной
для типичной пневмонии. В связи с этим вы­
сказывались предположения, что такие гной­
ники являются самостоятельным заболеванием,
с самого начала развивающимся как острое на­
гноение в паренхиме легкого. Анализ наших
наблюдений свидетельствует, что первый и вто­
рой типы абсцедирования свойственны постпнев­
моническим абсцессам, третий — аспирацион­
ным.
Аспирационный механизм является, по-видимому, преобладающим в патогенезе гангре­
ны легких. По наблюдениям госпитальной хи­
рургической клиники, некроз и гнойно-гнилост­
ный распад участков легкого наступают обычно
через 5—10 сут.
Позднее, на 3—4-й неделе заболевания, на­
ступление некроза и распада легкого отмечено
лишь у 6 из 170 наблюдавшихся нами больных
гангреной легких.
Состояние больных в стадии некроза и рас­
пада тяжелое. Оно определяется выраженной
интоксикацией вследствие резорбции продук­
тов распадающейся мертвой ткани, жизнедея­
тельности микробных клеток и их токсинов.
Клиническими признаками, свидетельствую­
щими о наступлении этой стадии нагноения,
являются высокая с гектическими размахами
температура и появление гнилостного запаха
изо рта при дыхании. Реже, особенно у боль­
ных с абсцессами легких, неприятный запах
изо рта может вообще отсутствовать.
Спустя несколько дней после появления за­
паха начинается выделение гнойной или гной­
но-гнилостной мокроты, что свидетельствует
о возникновении сообщения очагов распадаю­
щихся некротических тканей с бронхами и на­
чавшемся их опорожнении. Количество мокро­
ты может достигать более 500 мл в сутки.
В мокроте часто .определяется примесь крови.
Запах мокроты может быть очень неприятным,
напоминающим запах от кариозного зуба. Иног­
да, особенно при гангрене, запах бывает на­
столько резким, что пребывание окружающих
в одном помещении становится невозможным.
Мокрота у больных гангреной чаще имеет гряз­
но-серый, иногда (от примеси крови) шоко­
ладный цвет. Она — жидкой водянистой кон­
систенции, пенистая. При отстаивании делится
на три слоя: нижнии состоит из крошковатого
осадка, представляющего обрывки легочной
ткани и пробок Дитриха, средний слой, наибо­
лее выраженный,— мутный, жидкий, верх­
ний слой — слизисто-гнойный, пенистый. Обна­
руженные при микроскопическом исследовании
мокроты эластические волокна, жировые капли,
клеточные элементы и бактерии подтверждают
продолжающийся распад легочной ткани. Эла­
стические волокна обнаруживаются не всегда
из-за ферментативного их расплавления в про­
цессе жизнедеятельности бактерий. У больных
с абсцессами легких запах мокроты может от­
сутствовать; нередко она бывает более густой,
чем при гангрене, консистенции, белого или
серовато-белого цвета.
Количество мокроты зависит не только от
объема поражения легочной ткани, но и от со­
путствующего бронхита. Выделение мокроты
чаще наблюдается в утренние часы, после ее
накопления в легких в более спокойное ночное
время, сопровождается приступами мучитель­
ного и болезненного кашля, изнуряющего боль­
ного.
Повышение температуры тела считается од­
ним из характерных симптомов острых нагное­
ний легких, но выраженность температурной
реакции может быть различной. Высокая тем­
пература с гектическими размахами всегда на­
блюдается в стадии некроза и распада легочной
ткани. Когда очаги деструкции начинают дре­
нироваться через бронхи, температура обычно
снижается и в дальнейшем определяется усло­
виями дренирования. Быстрая секвестрация
некротических участков, их гнойно-гнилостный
распад и эвакуация кашлем приводят к стойкому
снижению и нормализации температуры. Про­
должающийся некроз легочной ткани, формиро­
вание множественных или одиночных крупных,
а также краевых секвестров, подвергающихся
дезинтеграции в условиях микробного обсеме­
нения, обычно сопровождаются выраженной
температурной реакцией. Нередко период сни­
жения температуры сменяется резким и стой­
ким ее повышением, что чаще всего связано
с появлением новых участков некроза или недо­
статочной эвакуацией гноя через дренирующие
бронхи. При благоприятном течении заболева­
ния и отграничении гнойно-деструктивного
процесса улучшение общего состояния, сни­
жение температуры и уменьшение количества
мокроты идут параллельно. При прогрессирова­
нии патологических изменений в легких, осо­
бенно при возникновении новых очагов некроза,
уменьшение количества мокроты может сопро­
вождаться повышением температуры тела и
ухудшением общего состояния.
После наступления гнойно-гнилостного рас­
пада изменяются физикальные признаки. При
149
формировании участков деструкции перкуссией
можно определить наличие полости в легочной
ткани. Аускультация при начинающемся рас­
паде дает больше информации: стойкие, лока­
лизованные в определенных участках влажные
хрипы подтверждают распад некротизирован­
ных тканей и указывают на расположение очага
некроза. Над зоной, соответствующей деструк­
тивному участку, дыхание делается ослаблен­
ным, реже — с бронхиальным оттенком. При
формировании больших полостей деструкции
может прослушиваться дыхание с амфориче­
ским оттенком. При тотальном поражении лег­
кого чаще прослушивается ослабленное брон­
хиальное или жесткое дыхание. Крупнопузыр­
чатые хрипы выслушиваются при абсцессах
легких; при гангрене они не звучны и чаще
очень скудны. Отсутствие при аускультации
признаков амфорического дыхания объясняется
тем, что полости заполнены гнойным содер­
жимым, некротическими тканями, а в окруж­
ности их имеются размягченные участки лег­
кого, пропитанные гноем.
Если гной, образовавшийся вследствие лизиса
омертвевших и секвестрировавшихся участков
легочной ткани, полностью эвакуируется через
дренирующие бронхи, остается сухая остаточ­
ная полость, по размерам соответствующая
омертвевшей части легкого. Это конечная ста­
дия благоприятно протекающего нагноения
легких. Сроки образования сухой остаточной
полости зависят от влияния многих факторов:
состояния больного, проводимого лечения,
локализации нагноения и размеров секвестри­
рованных участков легочной ткани. Мелкие
секвестры расплавляются быстрее. Гной, скап­
ливающийся в верхних отделах, эвакуируется
легче, поэтому сухие остаточные полости как
конечные стадии нагноения чаще всего фор­
мируются в верхних долях легких, особенно
справа.
Когда секвестрируются крупные участки
легочной ткани, особенно при нижнедолевой
локализации нагноения, процесс нередко прини­
мает затяжное течение с периодическими обо­
стрениями и ремиссиями. Крупные секвестры
фрагментируются, образуют густой гной и дет­
рит, эвакуация которых через дренирующие
бронхи затруднена. В таких случаях некроти­
зированная легочная ткань может в течение
многих месяцев выполнять сформировавшуюся
полость, не подвергаясь расплавлению.
Легочные секвестры периодически закрывают
дренирующие бронхи, вызывая резкое повыше­
ние температуры, ознобы, признаки общей инто­
ксикации организма. Такую стадию нагноения
можно назвать хронической ограниченной ган­
греной или хроническим гангренозным абсцес­
сом.
Наиболее характерным клиническим приз­
наком у больных с абсцессом и гангреной легких
является интоксикация вследствие резорбции
продуктов гнойно-гнилостного распада некро­
тических тканей. Степень интоксикации бывает
различной: от незначительно выраженной при
хорошо дренируемом абсцессе до тяжелейшей
при прогрессирующем течении распростра­
ненной гангрены легких. Интоксикация про­
является слабостью и адинамией, анемией и
снижением массы тела. Проведенными иссле­
дованиями |Лукомский Г. И., 1981] установлено,
что при острых абсцессах и гангрене легких
вследствие усиленного катаболизма наблю­
даются массивные белковые потери, достигаю­
щие 11 г азота в сутки, что адекватно распаду
275 г мышечной массы. По мнению J. Bartlett,
S. Finegold (1974), выраженная анемия и быст­
рая потеря массы тела являются наиболее
характерными признаками распространенной
гангрены легких. Наблюдения, проведенные в
клинике, в значительной мере подтверждают
это положение. Исследование функциональ­
ного состояния эритрона у больных гангреной
легких обнаружило значительное снижение
пролиферативной активности эритроидных
клеток костного мозга и отчетливое усиление
костномозговой деструкции клеток.
Изменения крови у больных нагноениями
легких характеризуются также нейтрофильным
лейкоцитозом со сдвигом лейкоцитарной фор­
мулы влево, токсической зернистостью нейтро­
филов. При прогрессирующем течении деструк­
тивного процесса в легочной ткани нередко
обнаруживается лимфопения.
Постоянно наблюдаются изменения белко­
вого спектра крови, выражающиеся в гипопро­
теинемии и, особенно, диспротеинемии со сни­
жением альбуминовых фракций белка, нередко
доходящих до критических уровней (менее
35 г/м2).
В тесной связи с нарушениями белкового
обмена находятся изменения объема цирку­
лирующей крови и ее компонентов. У большин­
ства больных при показателях объема крови,
близких к нормальным,’ выявляется отчетливая
тенденция в гиперплазмии как защитной и ком­
пенсаторной реакции организма на анемию
и интоксикацию. Глобулярный объем в преде­
лах нормальных величин встречается лишь
в отдельных случаях. У подавляющего боль­
шинства наблюдавшихся больных с абсцессами
и гангреной легких отмечается значительное
снижение этого показателя, подтверждающее
тяжелую анемию, выраженную общую и мест­
ную тканевую гипоксию. Прогрессирование
деструктивного процесса в легочной ткани, раз­
витие гнойных осложнений в плевральной поло­
сти приводят к истощению компенсаторных
150
механизмов и развитию токсико-резорбтивного
истощения, для которого характерным является
дефицит всех компонентов объема крови.
Нагноительный процесс в легких при острых
абсцессах и, особенно, гангрене легких приво­
дит к выраженным функциональным наруше­
ниям систем дыхания и кровообращения. По
данным спирографии, как правило, наблюда­
ются тахипноэ, значительное снижение жизнен­
ной емкости легких, снижение максимальной
вентиляции легких, резкое (особенно в слу­
чаях распространенной гангрены) снижение
жизненного показателя. Для большинства
больных острыми нагноениями легких весьма
характерными являются значительные гемо­
динамические расстройства. Информативным
методом для их выявления является интеграль­
ная реография тела по М. И. Тищенко (1973).
Особенно резко выражены расстройства гемо­
динамики у больных гангреной легких, что под­
тверждается значительно повышенными пока­
зателями коэффициента резерва, представляю­
щего отношение фактического минутного объе­
ма кровообращения к индивидуальной должной
величине в условиях покоя. Значительную на­
пряженность функционирования миокарда при
абсцессах и гангрене легких подтверждают
постоянно наблюдающаяся тахикардия и по­
вышение коэффициента дыхательных измене­
ний ударного объема, являющегося отноше­
нием максимального значения ударного объема
крови к минимальному за дыхательный цикл.
Проведенный анализ изменений внешнего
дыхания и центральной гемодинамики у боль­
ных острыми абсцессами и гангреной легких
позволяет высказать предположение, что ве­
дущую роль в патогенезе легочно-сердечной
недостаточности играют расстройства в си­
стеме внешнего дыхания и легочного газооб­
мена.
Большое значение в последнее время при­
дается изучению активности воспалительного
процесса и реактивности организма при острых
абсцессах и гангрене легких. М. И. Лыткин
исоавт. (1983) обнаружили резкое (в 8—10 раз)
повышение активности кислой и щелочной фос­
фатаз лизосом лейкоцитов крови, достоверно
более выраженное у больных гангреной лег­
ких, а также значительное снижение у боль­
шинства (65 %) из них титров естественных
антител сыворотки крови а- и 6-гемагглю­
тининов), что, вероятно, является одной из при­
чин, способствующих возникновению, развитию
и распространению острого гнойно-деструк­
тивного процесса в легком.
О большом напряжении механизмов защиты
у больных с острыми абсцессами и гангреной
легких свидетельствует также значительное
возрастание агрегационных свойств крови, воз­
можно, из-за ее перегрузки иммунными комп­
лексами, которые можно определить с помощью
реакции везикулообразования (РВО), моди­
фицированной в нашей клинике В. И. Печер­
ским. Число всех везикулоподобных элемен­
тов у больных с наиболее тяжелой формой
острых нагноений легких — гангреной — было
увеличено почти в 2 раза; число лейкоцитов,
участвующих в РВО, больше, чем у здоровых
людей, в 2,8—3,4 раза, а сливных элемен­
тов — в 4—5 раз. Одновременно с этим у боль­
ных острыми нагноениями легких значительно
повышаются агрегационные свойства эритроци­
тов и тромбоцитов, определяемые микроскопией
суспензии эритроцитов в собственной плазме
и фотоэлектрометрией [Тулупов А. Н., 1983].
Полученные данные подтверждают необходи­
мость проведения у больных с острыми абсцес­
сами и гангреной легких дезагрегационной
и противосвертывающей терапии.
С целью выяснения роли состояния организ­
ма в развитии острых нагноений легких в по­
следние годы стали проводиться исследования
различных факторов иммунитета больных.
Так, исследованиями иммунологической реак­
тивности у больных с острыми абсцессами,
осложненными эмпиемой, Б. А. Королев и соавт.
(1980) выявили резкое угнетение Т-системы
иммунитета, нарушение регуляции В-системы,
отсутствие адекватной реакции на циркуляцию
стафилококкового антигена, выраженную мик­
робную сенсибилизацию, дисфункцию фагоци­
тарной системы. С. Н. Захаровым и соавт. (1980)
у 52 больных острыми абсцессами и гангреной
легких изучена патогенетическая роль ауто­
агрессии. Авторы нашли, что при этих заболе­
ваниях наблюдается дисбаланс между общими
и местными проявлениями иммунитета. Он мо­
жет проявиться в виде снижения неспецифи­
ческих иммунных сил организма при высоком
напряжении местного иммунитета с преобла­
данием явлений аутоагрессии с участием противолегочных аутоантител, что сопровождается
прогрессированием деструкции легочной ткани.
Л. М. Недвецкой (1970), а также Б. П. Федо­
ровым, Г. Л. Воль-Эпштейном (1976) отмечено
значительное повышение титра противолегочных антител в сыворотке крови у больных с рас­
пространенными деструктивными процессами
в легких, что свидетельствует об агрессивности
аутоантител и вносит новые элементы в объяс­
нение патогенеза острых легочных нагноений.
Клинико-иммунологические исследования
Я. Э. Ламм и соавт. (1983), проведенные у 147
больных с острыми абсцессами легких, обнару­
жили выраженные изменения иммунологиче­
ских реакций, проявляющиеся в значительном
напряжении гуморального иммунитета (повы­
шение титров основных классов иммуноглобу­
151
линов—А, М, G), свидетельствующем о спо­
собности организма к иммунокомпетентному
ответу. Обнаружено, что высокие титры IgG
сохранялись при переходе процесса в хрони­
ческий. В зависимости от состояния гумораль­
ного звена иммунитета С. Н. Захаров и соавт.
(1982) выделяют три типа течения острых абсцесов и гангрены легких: гипоергический, нормоергический и гиперергический, встречающий­
ся чаще всего.
Исследования гуморального иммунитета
у наблюдавшихся в нашей клинике больных
с острыми абсцессами и гангреной легких по
определению титров иммуноглобулинов А, М, G
подтвердили литературные данные о наиболее
часто встречающемся гиперергическом типе
течения заболевания. Это определяет необхо­
димость в назначении таким больным препара­
тов типа азатиоприна, подавляющих аутоагрес­
сию. Относительная лимфопения, а у больных
прогрессирующей гангреной легких — резкая
абсолютная лимфопения, требует коррекции
назначением стимуляторов лимфопоэза (леакадин, левамизол и др.).
Специфических нарушений функции почек
у больных острыми нагноениями легких нет
[Колесников И. С. и др., 1983]. Примерно в 50 %
наблюдений может быть отмечена протеинурия,
встречающаяся и при других видах гнойной
инфекции. Почечная недостаточность чаще
развивается при переходе процесса в хрониче­
скую фазу или длительном осложненном (эм­
пиемой, сепсисом) течении острого нагноения.
Определение основных тенденций в течении
гнойно-деструктивного процесса (прогресси­
рование, регрессия или стабилизация) имеет
большое практическое значение, так как явля­
ется определяющим при выборе метода лече­
ния, но практическое решение этой задачи весь­
ма затруднительно, так как нередко намечаю­
щаяся было положительная динамика клини­
ческих и рентгенологических симптомов сме­
няется ухудшением состояния больного.
Анализ клинико-рентгенологических иссле­
дований у 509 больных с острыми абсцессами
легких позволил выявить следующие варианты
клинического течения: 1. Регрессирующее тече­
ние, характеризующееся удовлетворительным
общим состоянием, отсутствием или незначи­
тельной выраженностью гнойной интоксика­
ции, нормальной или субфебрильной темпера­
турой, наличием полости деструкции в легком
с небольшим количеством жидкости и незначи­
тельной зоной перифокальной инфильтрации
окружающей легочной ткани, что свидетель­
ствовало о хорошей проходимости дренирую­
щих бронхов,— у 27,5 % больных. 2. Непро­
грессирующее течение, которому были свой­
ственны отчетливые признаки гнойной интокси­
кации, постоянная лихорадка и изменения в
крови, а рентгенологически — признаки полости
с широким горизонтальным уровнем жидкости
и выраженными перифокальными воспалитель­
ными изменениями, свидетельствующими о
недостаточной проходимости дренирующих
бронхов,— у 51,1 % больных. 3. Прогрессирую­
щее течение, характеризовавшееся резкими
признаками гнойной интоксикации, дыхатель­
ной недостаточности, высокой лихорадкой,
выраженными изменениями крови воспалитель­
ного характера, а рентгенологически — массив­
ной инфильтрацией легочной ткани с множе­
ственными полостями деструкции или без ви­
димой деструкции (так называемые блокиро­
ванные абсцессы),— у 9,9 % больных. Это —
группа больных с нарушенной проходимостью
дренирующих бронхов. 4. Группа больных, у
которых острый абсцесс легких осложнился
пиопневмотораксом,— 11,1 %. Множественные
абсцессы были у 14,9 % больных, двусторон­
ние — у 8 %.
Течение гангрены легких отличается боль­
шим разнообразием. Предоставленное есте­
ственному течению заболевание быстро про­
грессирует, развиваются необратимые изме­
нения и истощение защитных сил, вследствие
чего летальный исход становится неизбежным
вне зависимости от способов лечения.
Из 170 больных гангреной, переведенных в
клинику из терапевтических отделений боль­
ниц, лишь у 32 (18,8 %) после проведенного
там лечения отмечено улучшение общего со­
стояния, но при отсутствии положительной
рентгенологической динамики деструктивного
процесса. У остальных терапевтическое лече­
ние оказалось неэффективным. Эти данные
убедительно показывают необходимость сроч­
ного перевода больных в специализированные
хирургические стационары, как только диагноз
гангрены легких становится очевидным. Все
же 24 (16,6 %) больных в силу разных причин
переведены в клинику с запущенной гангреной
легких. Продолжительность заболевания их
до перевода была от 4 до 8 нед. Все эти больные
были крайне истощены, и 79 % из них умерли.
Гангрена легких чаще всего (58,6 %) харак­
теризовалась неблагоприятным течением забо­
левания, нарастанием клинической и рентге­
нологической симптоматики и развитием ос­
ложнений, несмотря на проводимую интенсив­
ную терапию. Стабилизация клинического тече­
ния гангрены легких отмечена у 32,5 % боль­
ных. Течение заболевания в этих случаях отли­
чалось монотонностью, отсутствием прогрес­
сирующей интоксикации. У этих больных не­
редко было несоответствие между умеренно
выраженной
клинической симптоматикой
и распространенностью деструктивных изме­
152
нении в легких, определяемых на рентгенограм­
мах и томограммах.
Регрессирующее течение гангрены легких
отмечено всего лишь у 8,9 % больных. Харак­
терным в клинической картине заболевания
у них было не только улучшение клинической
симптоматики (снижение температуры, появ­
ление аппетита, уменьшение или исчезновение
гнойной мокроты, нормализация клинических
и биохимических показателей крови), но и поло­
жительные рентгенологические изменения,
подтверждающие уменьшение и отграничение
деструктивных изменений в легких.
Вместе с увеличением общей заболеваемости
гангреной легких в последние годы возросло
и количество бурно протекающих, молниенос­
ных форм этого заболевания, когда гнойно­
деструктивный процесс неуклонно прогрессирует
и приводит больных к гибели в первые недели
заболевания. Ю. И. Горшков (1976), анализи­
руя течение гангрены легких у 55 больных,
отметил следующие характерные особенности:
довольно высокий процент «молниеносных»
форм (9 %), частые двусторонние поражения
(у 12,7 %), большая частота осложнений эмпие­
мой (53 %) и кровотечением (14,6 %).
Среди наблюдавшихся в клинике больных
бурно прогрессирующая форма гангрены легких
наблюдалась у 12,7 % больных; 65 % из них
умерли.
Осложнения острых легочных нагноений.
Наиболее частыми осложнениями легочных
нагноений являются пиопневмоторакс, пора­
жения противоположного легкого и легоч­
ные кровотечения. Другие осложнения (сепсис,
пневмоперикардит, острая почечная недоста­
точность) встречаются реже.
Частота пиопневмоторакса после острых
абсцессов легких составляет, по литератур­
ным данным, от 10,6 до 38,5 % [Булынин В. И.
и др., 1980; Толузаков В. Л„ Егиазарян В. Ф.,
1984, и др.]. Гангрена легких осложняется пиопневмотораксом значительно чаще — в 18,7—
89 % [Лукомский Г. И., 1975; Горшков Ю. И.,
1975; Вагнер Е. А. и др., 1982, и др.|. Такие
различия в частоте пиопневмоторакса объясня­
ются различной продолжительностью заболе­
вания, а также элементами субъективизма в
трактовке существа нагноительного процесса
в легких при определении его как абсцесс или
гангрена.
В госпитальной хирургической клинике за
последние 12 лет лечились 128 больных с пиопневмотораксом. В большинстве наблюдений
абсцессы и гангрены, осложнившиеся пиопневмотораксом, имели аспирационный и постпнев
монический генез, о чем косвенно свидетель­
ствует более частая локализация легочных дест­
руктивных очагов в правом легком (58,6 %).
Чаще всего перфорировали в плевральную
полость и вызывали пиопневмоторакс гной­
но-некротические процессы в нижних долях
легких (61,7 %). Причина этого, вероятнее
всего, заключается в большей подвижности
нижних долей легких при дыхательных экскур­
сиях, препятствующих образованию спаек и
облитерации плевральной полости в базальных
отделах, а также в затрудненных условиях
опорожнения гнойников нижних долей есте­
ственным путем.
Симптомы перфорации гнойников легкого
в плевральную полость могут быть различ­
ными: от ярко выраженных, указывающих с
несомненностью на наличие перфорации, до
стертых и совсем незаметных, выявляемых не­
редко лишь рентгенологически. Острая форма
пиопневмоторакса отмечена лишь у 6,5 % на­
блюдавшихся больных. Анализ анамнестиче­
ских данных и сопоставление длительности
заболевания с рентгенологическими измене­
ниями позволили прийти к заключению, что
это осложнение чаще всего развивается на 3-й
неделе заболевания (у 76,6 % больных).
Эмпиема плевры при острых абсцессах и
гангрене легких, развивающаяся per continuitatem, встречается значительно реже. Среди 170
больных гангреной легких, наблюдавшихся
в нашей клинике, эмпиема плевры была отме­
чена всего у 3 больных.
Поражение противоположного легкого при
острых нагноительных заболеваниях легких
возникает довольно часто, но патологический
процесс в «здоровом» легком обычно развива­
ется у длительно болеющих, лежачих и ослаб­
ленных пациентов. Возникновение в таких слу­
чаях контралатеральных пневмоний или абсцес­
сов чаще всего связано с аспирацией гнойной
мокроты из пораженного деструктивным процесом легкого.
По нашим данным, двусторонние поражения
легких при острых абсцессах отмечены у 8 %
больных, а при гангрене легких — в 12,2 %
случаев. Частота легочных кровотечений у боль­
ных с острыми абсцессами составляет 6—12 %.
Среди 688 больных с острыми абсцессами, на­
блюдавшихся Ю. М. Лубенским и соавт. (1980),
легочные кровотечения были у 11,3 %. По дан­
ным В. И. Астафьева (1980), из 132 больных
с осложненным течением острого абсцесса
у 39 диагностировано легочное кровотечение
(29,6 %).
У больных гангреной легких кровотечение,
по данным литературы, встречается чаще, чем
при абсцессах легких,— в 10,7—53, 1 % [Уг­
лов Ф. Г., 1971; Митюк И. И., 1974; Горш­
ков Ю. И., 1975, и др.]. Еще чаще встречается
кровохарканье. В. Ф. Егиазарян (1975) на­
блюдал кровохарканье более чем у половины
153
больных гангреной легких. При кровохарканье
основным субстратом, выделяющимся из лег­
кого, является мокрота с примесью того или
иного количества крови. Выделение с мокротой
крови в количестве более 50 мл можно считать
кровотечением, которое бывает малым (до
100 мл), средним (до 500 мл) и обильным (бо­
лее 500 мл). Массивное легочное кровотечение
приводит к острой сосудистой недостаточности,
анемии и асфиксии, чаще всего являющейся
причиной смерти. Аспирация небольших коли­
честв крови вызывает обтурационные ателек­
тазы и аспирационные пневмонии. Среди на­
блюдавшихся в госпитальной хирургической
клинике больных с острыми абсцессами и ган­
греной легких легочные кровотечения отмече­
ны соответственно у 7,6 и 4,9 % пациентов.
Симптомы начального сепсиса — «пресеп­
сиса» (высокая с гектическими размахами лихо­
радка, ознобы и т. п.) часто наблюдаются при
острых абсцессах и гангрене легких, но сепсис
в виде септицемии или септикопиемии редко
выявляется при жизни больных, страдающих
этими заболеваниями. На первом месте по ча­
стоте стоит поражение головного мозга. Так,
по сводным данным И. Е. Мацуева (1952),
метастатические абсцессы мозга при сепсисе
пневмогенного происхождения наблюдались
в 83%, а из других органов — лишь в 17%
случаев. Из наблюдавшихся в нашей клинике
больных с абсцессами легких поражение голов­
ного мозга было лишь у 0,7 % , а осложнение
гангрены легких сепсисом возникло всего у
2 больных. Основной причиной относительно
редкого возникновения сепсиса при острых
гнойно-деструктивных поражениях легких яв­
ляются, по-видимому, относительно более вы­
сокий уровень местного тканевого антиинфекционного иммунитета при отграниченных про­
цессах и быстрая гибель (до развития сепсиса)
при распространенных формах поражений.
Редким, но очень опасным осложнением,
которое мы наблюдали всего у 2 больных ган­
греной легких, является прорыв гнойно-деструк­
тивных очагов легкого в полость перикарда —
пневмоперикардит. Клиническая картина пнев­
моперикардита характеризуется внезапным
резким ухудшением состояния, появлением
нарастающей подкожной эмфиземы верхней
половины туловища, шеи, головы, коллапсом.
По характеру морфологических изменений и
возникающим гемодинамическим расстрой­
ствам это осложнение является, по существу,
смертельным. Оба наблюдавшиеся нами боль­
ные погибли.
Диагностика и дифференциальная диагности­
ка. Диагноз острого абсцесса или гангрены лег­
ких ставят по данным анамнеза, оценки обще­
го состояния организма больного, клинических,
лабораторных, функциональных, иммунологи­
ческих и рентгенологических методов обследо­
вания. В целом ряде случаев по клиническим
и рентгенологическим признакам очень трудно
отдифференцировать острый абсцесс от гангре­
ны легких. Сопоставления клинического тече­
ния заболевания у больных с острыми абсцес­
сами и гангреной легких, проведенные в клини­
ке, показали, что при гангрене легких оно более
часто характеризуется прогрессированием и
возникновением осложнений, быстрее приводит
к выраженному истощению, анемии, значи­
тельной легочно-сердечной недостаточности.
Однако ни один из перечисленных показателей
клинической картины заболевания не может
служить тем надежным критерием, с помощью
которого можно было бы легко отличить абсцесс
от гангрены. Больше данных в этом отношении
дают рентгенологические методы исследова­
ний, особенно в динамике и сопоставлении с
клиническими проявлениями. В том и другом
случаях начальным рентгенологическим про­
явлением заболевания является пневмониче­
ский фокус, изначально захватывающий уча­
сток легочной ткани в пределах анатомически
обособленной части легкого. При остром абс­
цессе легкого такой частью обычно является
сегмент или два сегмента, реже — доля и совсем
редко — все легкое, т. е. для острого абсцесса
характерно изначальное сегментарное распро­
странение воспаления и последующего некроза.
Гангрена легкого как правило, развивается после
воспаления, распространяющегося на целую
долю, реже — на две доли, и еще реже — на
все легкое, т. е. для гангрены легкого характерно
изначальное долевое распространение воспале­
ния и последующего некроза.
Типичным рентгенологическим симптомом
этой начальной стадии заболевания является
гомогенное, по плотности напоминающее жид­
кость, затенение (рис. 79). В литературе эта ста­
дия заболевания вне зависимости от распрост­
раненности поражения называется лобитом,
пневмонитом [Bartlett J., Fingold S., 1974],
«плотной консолидацией с увеличением доли»
[Danner Р., 1974; O’Reilli G., 1978]. Все эти тер­
мины не лишены условности. Поскольку пато­
логический процесс в пораженном участке лег­
кого на этой стадии определяется нарушениями
бронхиальной проходимости и воспалением,
правильнее, как нам кажется, называть эту на­
чальную стадию острого легочного нагноения
ателектаз-пневмонией. В случаях ателектазпневмонии доли легкого последняя обычно уве­
личена в объеме, границы ее четко видны. Не­
редко можно наблюдать провисание главной
и поперечной междолевых щелей. На томограм­
мах в этой стадии видна плотная консолидация
легочной ткани и отсутствие деструкции.
154
Рис. 79. Ателектаз-пневмония верхней доли левого легко­
го — начальная стадия гангрены.
а — прямая рентгенограмма; б — боковая рентгенограмма. Плот­
ное гомогенное затенение верхней доли легкого.
С возникновением некроза и распада легочной
ткани на рентгенограмме легких появляются
мелкие, величиной от 0,2 до 2—3 см в диаметре,
участки просветления на фоне гомогенного зате­
нения. Эти участки местами разобщены инфиль­
трированной легочной тканью, местами слива­
ются между собой (рис. 80). При прогрессиро­
вании распада мелкие полости сливаются между
собой, образуя более крупные, с уровнями жид­
кости или без них (рис. 81). В этой стадии
заболевания процессы продолжающегося
некроза и распада идут одновременно. Коли­
чественное их соотношение зависит от резистент­
ности организма, вирулентности микробной
флоры и проводимой терапии.
Бурное прогрессирование некроза может
быстро привести к гибели больного. При более
благоприятном течении процесс в легком начи­
нает отграничиваться, окончательно локали­
зуясь в пределах пораженной доли или сегмен­
тов. Мелкие некротические участки легкого
лизируются и откашливаются в виде гнойно­
гнилостной мокроты. Крупные секвестры, для
расплавления которых необходимо больше вре­
мени, остаются в полости. Они могут быть при­
стеночными, фиксированными к одной из стенок
полости, или свободно перемещающимися в
полости распада. Секвестры легочной ткани
хорошо видны на рентгенограммах и, особенно,
на томограммах. Секвестрация некротических
участков легкого и образование демаркации —
следующая стадия благоприятно протекающего
острого легочного нагноения (рис. 82). В этот
период заболевание чаще всего определяется
как гангренозный абсцесс или ограниченная
гангрена, имея в виду, что в начале заболевания
процесс был распространенным, начавшимся
с долевой ателектаз-пневмонии. Распростра­
ненная гангрена после сегментарных ателектазпневмоний, как правило, не встречается. Если
после такой ателектаз-пневмонии некроз и раз­
вивается, то, будучи небольшими по объему,
некротические участки быстро лизируются,
и формируется типичный острый абсцесс лег­
кого (рис. 83). В случаях, когда процессы сек­
вестрации и дезинтеграции омертвевших участ­
ков протекают медленно, формируется гангре­
нозный абсцесс
(ограниченная гангрена)
(рис. 84, 85). Ограниченная гангрена, таким
образом, может возникать после воспаления,
локализующегося также в пределах анатомиче­
ски обособленной, но меньшей, чем при рас­
пространенной гангрене, части легкого — сег­
менте, двух сегментах. Гангрена поэтому может
быть ограниченной с самого начала, а может
быть стадией благоприятно протекающей рас­
пространенной гангрены.
Важное место среди рентгенологических
методов диагностики острых абсцессов и ган­
грены легких принадлежит томографии, позво-
155
80
81
Рис. 80. Прямая рентгенограмма легких того же больного,
что на рис. 79.
На фоне инфильтрации видны множественные участки просветле­
ния — некроз и распад легочной ткани.
Рис. 81. Прямая рентгенограмма легких того же больного,
что на рис. 79.
Прогрессирование процесса. Слияние мелких полостей и обра­
зование более крупных участков деструкции.
Рис. 82. Прямая томограмма того же больного, что на
рис. 79. Стадия секвестрации омертвевших участков легкого.
Рис. 83. Острый абсцесс нижней доли левого легкого.
а — прямая рентгенограмма; б — боковая рентгенограмма. Видна
полость деструкции с горизонтальным уровнем, окруженная пе­
рифокальной инфильтрацией.
82
83
156
Рис. 84. Ограниченная гангрена
правого легкого.
(гангренозный абсцесс)
а — прямая томограмма; б — боковая томограмма.
Рис. 85. Ограниченная гангрена верхней доли правого легкого
(препарат).
ляющей определить структуру пораженного
участка легкого на различной глубине, проходи­
мость дренирующих бронхов, выявить секвестры.
Легочные секвестры не только способствуют
переходу процесса в хроническую форму, но
аспирация их в более мелкие бронхи здоровых
отделов легкого может вызвать нагноение или
способствовать возникновению аспирационных
гнойников в ранее непораженных участках ле­
гочной ткани. Секвестры выявляются на томо­
граммах в 3,5 раза чаще, чем при рентгеноско­
пии, рентгенографии и на суперэкспонированных
снимках, если их величина не менее 0,8 см
в диаметре. Секвестры могут быть одиночными
и множественными, различной формы и вели­
чины: от мелких обрывков легочной ткани до
громадных массивов, соответствующих целой
секвестрированной доле (рис. 86). Такие круп­
ные секвестры, заполняя полость деструкции,
придают ей на томограмме характерный вид:
на фоне округлого затенения у одного из полю­
сов или на отдельных участках определяются
зоны просветления в виде «полумесяца», «серпа»
или прерывистого щелевидного сферического
ободка. Пристеночные секвестры, а также неотторгнувшиеся некротические массы рентгено­
логически проявляются неровностью и бахром­
чатым выбуханием внутренних контуров поло­
сти. Отделившиеся крупные секвестры могут
свободно перемещаться в полости деструкции.
157
Рис. 86. Гангрена верхней доли правого легкого. Прямая
томограмма.
Рис. 87. Гангрена правого легкого. Прямая томограмма.
Видны множественные секвестры легочной ткани.
Видна секвестрация огромного участка легочной ткани.
Мелкие секвестры, представляющие собой крош­
ковидный детрит, определяются по бесформен­
ным просветлениям, образующимся из за скоп­
ления воздуха вокруг крошек детрита (рис. 87).
Если омертвевшие участки легкого быстро
лизируются, то формируется большая полость,
содержащая жидкий гной с горизонтальным
уровнем. В этих случаях по рентгенологической
картине обычно диагностируется абсцесс лег­
кого, а затем, после его опорожнения через
бронхи — большая сухая остаточная полость
(рис. 88, 89).
В случаях осложнения острым абсцессом
или (реже) гангреной очаговых пневмоний
последние начинаются в виде небольших очагов,
чаще множественных, реже — одиночных.
Иногда воспалительный процесс начинается
в бронхе в виде бронхита, а затем переходит
на альвеолярную ткань. В других случаях на­
блюдается бронхогенная инфекция легочной
ткани без предшествующего бронхита. Поэтому
для острого нагноения, развивающегося на
фоне очаговой пневмонии, характерно отсут­
ствие массивного поражения легочной ткани.
Множественные очаги некроза могут локали­
зоваться или в пределах одной доли, но они
разделены непораженной легочной тканью, или
в различных долях легкого.
Важную характеристику функционального
состояния пораженного абсцессом или гангре­
ной легкого можно получить с помощью метода
сканирования (рис. 90, 91). Анализ получен­
ных в клинике результатов позволил заключить,
что в целом имеется соответствие объема пора­
жения легочной ткани, определяемого клиноко­
рентгенологически, зонам пониженного на­
копления радиоактивного препарата на скано­
граммах. Отсутствие накопления альбумина
131i в пораженных участках легочной ткани,
обнаруженное у всех обследованных больных,
подтверждает данные ангиографии о регионар­
ной блокаде легочного кровотока в зоне дест­
руктивных изменений. Отсутствие накопления
ингалированного 133Хе в зонах деструкции сви­
детельствует о тяжелых анатомических повреж­
дениях легочных структур (бронхиолы, альвео­
лы) , обеспечивающих вентиляцию легких. Сопо­
ставление рентгенологических и сканографи­
ческих данных показало, что зоны, где не накап­
ливается радиоактивное вещество, несколько
больше по объему, чем рентгенологически опре­
деляемые области поражения. По-видимому,
в участках легочной ткани, непосредственно
не пораженных деструктивным процессом, но
примыкающих близко к очагам деструкции,
имеются выраженные функциональные изме-
158
Рис. 88. Гангрена верхней доли правого легкого в стадии
гигантского абсцесса.
а — прямая рентгенограмма; б — боковая рентгенограмма.
Рис. 90. Гангрена правого легкого. Перфузионная скано­
грамма.
Почти полное отсутствие кровотока в пораженном легком.
Рис. 89. Гангрена верхней доли правого левого легкого в ста­
дии гигантского опорожнившегося абсцесса.
Рис. 91. Гангрена правого легкого. Вентиляционная скано­
грамма того же больного, что на рис. 90.
Отсутствие вентиляции легкого.
159
нения, заключающиеся в нарушении кровооб­
ращения и вентиляции. Это предположение
косвенно подтверждается результатами элек­
тронно-микроскопического исследования здо­
ровых участков легкого у больных острыми ле­
гочными нагноениями. Изучение ультраструк­
туры и микроциркуляции легкого показало,
что нагноительный процесс сопровождается из­
менениями в отдаленных от деструктивных
очагов участках легочной ткани, характеризую­
щимися нарушением альвеолярной и хромосом­
ной структуры, что способствует снижению
интенсивности газообмена вследствие замед­
ления микроциркуляции, несмотря на сохра­
ненную вентиляцию легких |Митюк И. И., 1974].
Таким образом, диагностика острого легоч­
ного нагноения как такового не сложна. Труд­
нее разграничить отдельные его формы —
гангрену, гангренозный абсцесс, гнойный абс­
цесс, а также своевременно распознать начинаю­
щееся нагноение. В этом отношении весьма ин­
формативным может быть метод цветной термо­
графии [Иванов Р. В. и др., 1980], основанный
на регистрации распространяющихся из очагов
гипертермии тепловых потоков. С помощью
холестерических термои иди каторов, нанесен­
ных на грудную клетку, выявляется тепловая
топография кожного покрова. Участки гипер­
термии соответствуют воспалению (пневмония,
абсцедирование), «холодные» зоны — уже
сформировавшимся полостям деструкции. Метод
цветной термографии прост, безвреден, бес­
кровен и не требует применения контрастных
веществ.
Многообразие клинической и рентгенологиче­
ской симптоматики острых абсцессов и гангре­
ны легких нередко делает дифференциальную
диагностику этих и некоторых других легочных
заболеваний весьма трудной. Многочисленные
данные литературы свидетельствуют о наиболее
частых трудностях дифференциальной диагно­
стики острых нагноений и рака легкого. Среди
больных, находившихся на лечении в госпиталь­
ной хирургической клинике по поводу абсцессов
и гангрены легких, у 12.1 % до поступления
в клинику диагностировался рак легкого. В то
же время у 3,5 % больных раком легкого забо­
левание протекало с клинической и рентгеноло­
гической симптоматикой острого легочного
нагноения.
Решающее значение в дифференциальной
диагностике опухолевых и нагноительных забо­
леваний легких принадлежит эндоскопическим
и рентгенологическим методам исследований.
При центрально расположенных раках, про­
текающих с клинической симптоматикой абсцес­
са или гангрены, сомнения разрешает диагности­
ческая бронхоскопия с последующим гистоло­
гическим изучением биоптата. В случаях пери­
ферических «полостных» форм рака всегда
необходимой оказывается пункционная биопсия
с последующей гистологической верификацией
диагноза.
В диагностически неясных случаях обсерва­
ционная тактика нецелесообразна. У таких
больных показана диагностическая торакото­
мия, после которой для уточнения диагноза
и определения в связи с этим объема оператив­
ного вмешательства всегда необходимо вначале
удалить и подвергнуть срочному гистологиче­
скому исследованию один или несколько подо­
зрительных лимфатических узлов корня легкого.
Большие трудности может представлять диф­
ференциальная диагностика острых абсцессов
и гангрены легких с кавернозной и некоторыми
другими формами туберкулеза легких. Среди
.больных с острыми абсцессами, наблюдавших­
ся в госпитальной хирургической клинике, 10,7%
первоначально госпитализировались во фтизиа­
трические стационары. Из 170 больных, по­
ступивших в клинику с гангреной легких, фиб­
розно-кавернозная форма туберкулеза выяв­
лена у 3,4 %.
Клинические проявления неспецифических
острых легочных нагноений и специфических
туберкулезных поражений во многом очень схо­
жи. Дифференциальная диагностика в таких
случаях основывается главным образом на дан­
ных динамики патологического процесса в ле­
гочной ткани и обнаружении в мокроте мико­
бактерий туберкулеза. Если заболевание про­
текает с типичной клинической и рентгенологи­
ческой картиной легочного нагноения, а мно­
гократные исследования мокроты, в том числе
методом флотации, и промывных вод бронхов
микобактерий туберкулеза не выявили, от диаг­
ноза туберкулеза можно отказаться. В случаях,
когда отсутствует эффект от проводимой терапин
острого легочного нагноения, а при рентгено­
логических исследованиях в динамике выявля­
ется бронхогенная диссеминация и обнаружи­
ваются свежие туберкулезные очаги, следует
настойчиво искать бактериологические подт­
верждения специфичности процесса. Выявле­
ние микобактерий туберкулеза разрешает все
сомнения. Необходимо, однако, помнить, что
и у больных острыми легочными нагноениями
в мокроте нередко обнаруживаются трудноотлнчнмые от микобактерий кислотоупорные
палочки. В таких случаях дальнейшая лечеб­
ная тактика и организационные вопросы лече­
ния больных решаются совместно с фтизиатром.
Очень сложной в диагностическом отноше­
нии является трактовка так называемых соче­
танных поражений, при которых неспецифи­
ческий и специфический процессы существуют
одновременно. Варианты сочетанного течения
этих заболеваний могут быть различными.
160
Анализ клинического течения заболевания
у наблюдавшихся в клинике больных, у которых
абсцесс легкого сочетался с туберкулезом, пока­
зал, что чаще наблюдалось вторичное присое­
динение туберкулезного процесса к уже суще­
ствовавшему острому нагноительному. Реже
острый нагноительный процесс наслаивался на
ранее существовавший и длительно протекав­
ший без обострений специфический туберкулез­
ный.
Диагностика сочетанных поражений весьма
трудна. Определенное значение имеют анамнез
заболевания, указания на контакты в прошлом
с туберкулезными больными, ранее диагности­
рованный туберкулез легких. Микобактерии
туберкулеза в случаях сочетанных поражений
обнаружить трудно. Анаэробная микробная
флора, которой в последнее время отводится
ведущая роль в этиологии острых нагноений
легких, приводит к гибели микобактерий тубер­
кулеза.
Тяжесть клинического течения острых нагно­
ений легких, сочетающихся с туберкулезом,
плохой прогноз и трудности диагностики часто
вынуждают прибегать к резекциям легких и ги­
стологическим исследованиям препарата.
Нередко возникает необходимость диффе­
ренцировать абсцессы легких от нагноившихся
легочных кист, имеющих врожденное проис­
хождение. Из 63 больных кистами легких, на­
ходившихся в госпитальной хирургической
клинике, нагноение отмечено в 34, из них 13
пациентов поступили с диагнозом направления
«абсцесс легкого».
Инфицирование кисты чаще всего происходит
бронхогенным путем. Воспаление, развивающее­
ся в полости кисты, а при повторных обостре­
ниях — ив окружающей легочной тканн, при­
водит к бронхиальной непроходимости, за­
держке гнойного экссудата и интоксикации,
клинически и рентгенологически проявляю­
щейся симптомами, весьма типичными для ост­
рого абсцесса легкого. Реже нагноение начина­
ется незаметно, клиническая симптоматика
нарастает постепенно. Поскольку, как и при
абсцессах легких, течение заболевания при на­
гноении кисты определяется состоянием про­
ходимости дренирующих бронхов, в клиниче­
ской картине периоды обострения могут чере­
доваться с периодами ремиссии. Частота обо­
стрений, их продолжительность и клинически
выраженные признаки хронической гнойной
интоксикации свойственны неблагоприятно
текущим хроническим абсцессам легких.
В дифференциальной диагностике нагноив­
шихся кист и абсцессов легкого важное место
принадлежит рентгенологическим методам
исследования. Полость нагноившейся кисты на
рентгенограммах чаще имеет шаровидную или
II Зак. 0517
овальную форму с тонкими ровными стенками.
Окружающая кисту легочная паренхима в ран­
ние ст начала нагноения сроки не изменена.
Кисты могут быть множественными. В таких
случаях рентгенологически определяются коль­
цевидные тонкостенные полости, наслаиваю­
щиеся друг на друга и создающие картину сет­
чатого рисунка легкого. В диагностике мно­
жественных кист большое значение имеет брон­
хография.
В клинической практике часто приходится
дифференцировать острые абсцессы легких от
гнойных процессов в плевральной полости (эм­
пиема и пиопневмоторакс).
Тщательный анализ рентгенологических
данных позволяет чаще всего разграничить
пиопневмоторакс и абсцесс легкого. Очень ши­
рокий горизонтальный уровень (более 8—10 см)
в одной из проекций или в двух проекциях,
прилегающий вплотную к внутренней поверх­
ности грудной клетки, свидетельствует в пользу
пиопневмоторакса. В отличие от абсцесса лег­
кого, стенки деструктивной полости которого
и перифокальную воспалительную инфильтра­
цию можно очертить со всех сторон, в том
числе и снизу, при пиопневмотораксе ниже гори­
зонтального уровня обычно определяется зона
гомогенного затенения, простирающаяся вниз
до диафрагмы, обусловленная скоплением жид­
кости в плевральной полости. Купол диафрагмы
при этом чаще всего не дифференцируется.
Иногда отличить внутрилегочную полость от
плевральной при пиопневмотораксе можно по
форме (при пиопневмотораксе вытянутая в
краниокаудальном направлении, а не шаровид­
ная или овальная, как при абсцессе), по тол­
щине стенок полости (более толстая медиаль­
ная при пиопневмотораксе, образованная коллабированным легким, и одинаковые по толщине
при абсцессе).
В случаях, когда легочный гнойник, перфори­
ровавший в плевральную полость, опорож­
нился не полностью, на рентгенограммах мож­
но заметить два (а иногда и больше) уровня
жидкости, находящейся на разной высоте: один,
располагающийся в полости абсцесса, и другой,
пристеночный, находящийся в плевральной
полости.
Особенно трудна, а иногда и вообще невоз­
можна дифференциальная диагностика абсцесса
легкого и прорвавшейся в бронхи междолевой
эмпиемы плевры. Рентгенологическое исследо­
вание, выявляющее расположенный в меж­
долевой щели гнойник, и диагностическая пунк­
ция с введением а полость рентгеноконтраст­
ных растворов помогают распознать такую раз­
новидность ограниченной эмпиемы плевры, но
не всегда позволяют выявить абсцесс легкого,
явившийся ее причиной.
161
В клинической практике приходится диффе­
ренцировать абсцессы легких от нагноившегося
эхинококка этого органа. Нагноение при эхино­
кокке легкого может развиваться вокруг эхино­
кокковой кисты, в самой кисте до прорыва ее
в бронх и в полости, остающейся в легком после
прорыва эхинококковой кисты. Клиническая
картина нагноившегося эхинококка легкого
(повышение температуры тела, боли в грудной
клетке, выделение гнойной мокроты) очень
напоминает абсцесс легкого. Обнаружение
в мокроте обрывков хитиновой оболочки пара­
зита, наличие эхинококкоза в анамнезе, а также
постановка специфических серологических
реакций (реакция латекс-агглютинации, реак­
ция непрямой гемагглютинации и аллергиче­
ской пробы Кацони) помогают установить пра­
вильный диагноз. Тень хитиновой оболочки
бывает отчетливо видна на рентгенограмме.
С острым абсцедированием может протекать
и актиномикоз легких. Описаны истинные акти­
номикотические абсцессы легких |Осповат В. Л.,
1963]. Актиномикоз может присоединиться
и к вульгарному нагноительному процессу. Рас­
познавание актиномикоза в таких случаях явля­
ется трудным. Окончательный диагноз актино­
микоза основывается только на данных лабо­
раторных исследований, когда в мокроте обнару­
живают Друзы и мицелии гриба. Необходимо
иметь в виду, что в мокроте могут обнаружи­
ваться сапрофитные формы актиномицета, в то
время как при типичном актиномикозе друзы
и мицелии могут отсутствовать вследствие деге­
неративных изменений и спонтанного лизиса.
Для исключения диагностических ошибок по­
добные исследования должны выполняться
в специализированных микологических лабо­
раториях.
ЛЕЧЕНИЕ
Исходя из главного принципа лечения любого
больного — патогенетичности, терапия острых
нагноений легких должна строиться по следую­
щим основным направлениям:
1. Максимально полное и по возможности
постоянное дренирование гнойных очагов лег­
кого.
2. Лечебное воздействие на микробную флору
очагов нагноений.
3. Стимуляция защитных реакций организма.
Предложено много методов, обеспечивающих
естественное (через бронхи) или искусственное
(наружное с помощью оперативных вмеша­
тельств) отведение гноя из очагов деструк­
ции. Успех или неудача любого такого вида
лечения зависит в конечном счете от того, на­
сколько быстро и полноценно восстановится
естественный дренаж гнойной полости. В слу­
чаях острых абсцессов легких, содержащих
жидкий гной и мелкие секвестры, этого до­
биться легче. При гангренозных процессах в ле­
гочной ткани, где основным морфологическим
субстратом являются крупные омертвевшие
участки легкого, консервативных методов ле­
чения, как правило, оказывается недостаточно,
и в таких случаях приходится прибегать к опе­
ративным методам лечения. Следовательно,
при выборе метода лечения нужно ориентиро­
ваться на особенности патологического про­
цесса, определяющие исход заболевания. Та­
кими особенностями, влияющими на течение
заболевания, а поэтому и на выбор метода лече­
ния, являются состояние проходимости дре­
нирующих полость гнойника бронхов и наличие
в ней некротических секвестров легочной ткани.
Определяя лечебную тактику при остром
абсцессе легкого, целесообразно, исходя из
вышеизложенного, выделять следующие группы
острых абсцессов легких:
1) с хорошим бронхиальным дренажем;
2) с недостаточным бронхиальным дренажем;
3) с полностью нарушенным бронхиальным
дренажем.
Лечение больных, полость абсцесса у которых
самостоятельно хорошо дренируется, не состав­
ляет трудной задачи. С помощью методов сана­
ции трахеобронхиального дерева можно устой­
чиво поддерживать хорошую проходимость
дренирующих бронхов. Консервативное лече­
ние больных с недостаточным бронхиальным
дренажем, о чем свидетельствуют сохраняю­
щийся уровень жидкости в полости абсцесса
и признаки интоксикации, должно преследовать
цели восстановления полноценного бронхи­
ального дренажа. В этих случаях необходимо
начинать лечение с методов санации и стре­
миться к тому, чтобы легочный гнойник опорож­
нился естественным путем через бронхи. При
отсутствии эффекта от такого лечения часто
бывает необходимо прибегнуть к одному из спо­
собов искусственного наружного дренирования
(пункция легочного гнойника, дренирование его
с помощью торакоцентеза или пневмотомии).
Лечебная тактика по отношению к больным с
острыми абсцессами легких, бронхиальный
дренаж которых полностью нарушен (блоки­
рованные абсцессы), такая же.
Среди предложенных методов консерватив­
ного лечения, способствующих оттоку гнойного
содержимого из гнойных полостей легкого,
постуральный дренаж или дренаж положением
является простейшим и наименее обремени­
тельным для больного. Выбрать постуральное
положение для больного с одиночным абсцес­
сом легкого нетрудно — стандартные положе­
ния для постурального дренажа детально раз­
работаны. При гангрене легких поражение чаще
162
иосит долевой характер. Нередко имеется пора­
жение двух долей» всего легкого, а также дву­
сторонние поражения. Поэтому «дренажное»
положение в этих случаях должен найти сам
больной, которому в доступной форме следует
объяснить смысл этой процедуры. Целесооб­
разно принимать дренажное положение как
можно чаще и по возможности более продол­
жительное время, но так, чтобы не вызвать чрез­
мерного утомления больных мучительным каш­
лем. Если это возможно, то крайне желательно
сохранять дренажное положение и во время сна,
для чего приподнимается головной или нож­
ной конец кровати. Постуральный дренаж целе­
сообразно сочетать с дыхательными упражне­
ниями, а также массажем и поколачиванием
грудной клетки. Следует особенно настаивать,
чтобы постуральный дренаж проводился утром,
сразу же после пробуждения, чтобы очистить
бронхи от скопившейся за ночь мокроты, и ве­
чером перед сном.
Для улучшения проходимости дренирующих
бронхов уже давно применялись ингаляции,
интратрахеальные вливания различных лекар­
ственных веществ, а также отхаркивающие
средства. Чаще используются распространен­
ные антисептические растворы (фурацилин,
солафур и 3 % раствор соды).
Эффективность санации трахеобронхиаль­
ного дерева у больных легочными нагноениями
значительно увеличилась после внедрения в
клиническую практику протеолитических фер­
ментов: трипсина, химопсина, эластазы, гиалу­
ронидазы, рибонуклеазы [Злыдников Д. М.,
1961; Веремеенко К. Н., 1967; Стручков В. И.,
Лохвицкий С. В., 1972]. Ферменты при любом
способе их введения в трахею и бронхи раство­
ряют мелкие секвестры, гнойные пробки, раз­
жижают мокроту, способствуя более полному
механическому удалению гнойного содержи­
мого. Обладая противовоспалительным действи­
ем, ферменты приводят к уменьшению воспа­
ления и отека дренирующих бронхов. Наиболее
часто применяют трипсин (20—40 мг), химопсин (30—40 мг) и дезоксирибонуклеазу
(2500—5000 ЕД). В указанных количествах
ферменты растворяют в 30—40 мл солафура
или другого антисептика, после чего они инга­
лируются или вводятся в трахею с помощью
катетера, проведенного через нижний носовой
ход.
Последний способ является одним из наибо­
лее эффективных- Интратрахеальная санация
может выполняться как врачом, так и специаль­
но обученной сестрой.
Если санация трахео-бронхиального дерева
с помощью постурального дренажа, ингаляций
и интратрахеальных вливаний в течение 3—5
дней оказывается неэффективной и в полости
11
деструкции сохраняется уровень жидкости,
необходимо прибегнуть к более активным ин­
струментальным методам дренирования и сана­
ции бронхов и трахеи.
Весьма эффективным является метод сегмен­
тарной катетеризации бронхов. Формоустой­
чивый рентгеноконтрастный управляемый ка­
тетер вводится в дренирующий абсцесс сег­
ментарный бронх или непосредственно в по­
лость абсцесса во время поднаркозной бронхо­
скопии или под местной анестезией трансна­
зально под контролем рентгенотелевидения.
Затем производятся отсасывание гнойного со­
держимого, промывание полости гнойника,
заканчивающиеся введением в нее протеолити­
ческих ферментов и антибиотиков, после чего
катетер удаляется [Углов Ф. Г., Егиазарян В. Ф„
1976; Перельман М. И. и др., 19801.
Осуществлять сегментарную катетеризацию
дренирующих абсцесс бронхов можно исполь­
зуя методику чрескожной катетеризации тра­
хеи. Последнюю можно пунктировать над ярем­
ной вырезкой толстой иглой типично по Сельдингеру. Через иглу в просвет трахеи, а за­
тем сегментарный бронх проводится рентге­
ноконтрастный катетер, который фиксируется
к коже. Катетер может оставаться на месте
в течение нескольких суток для многократной
санации.
У больных, выделяющих большие количества
мокроты, а также при множественных абсцессах
и гангрене легких широко используется брон­
хоскопическая санация, во время которой под
визуальным контролем удается максимально
аспирировать гнойную мокроту, промыть трахею
и бронхи антисептическими растворами. Брон­
хоскопическая санация является сейчас обя­
зательным элементом комплексного лечения
больных абсцессами и гангреной легких.
Если мокроты много, лечебные бронхоско­
пии целесообразно проводить жестким брон­
хоскопом, под наркозом, поскольку местной
анестезией у таких больных обычно не удается
достичь хорошего обезболивания. Весьма удоб­
ной является разработанная в нашей клинике
методика санационной бронхоскопии под нар­
козом с искусственной вентиляцией легких ин­
жекционным способом [Костин Э. Д. и др.,
1979]. Важно осуществлять аспирацию из тра­
хеобронхиального дерева при пробуждении
больного от наркоза и появлении кашля, когда
в просвет долевых бронхов и трахеи выделя­
ется гнойный экссудат из сегментарных и суб­
сегментарных бронхов.
Бронхоскопический метод лечения позволяет
не только санировать пораженное легкое, но и
контролировать эффективность проводимой
терапии по визуально определяемой степени
интенсивности воспалительных изменений брон­
163
хов. Опыт, накопленный госпитальной хирур­
гической клиникой, свидетельствует, что часто­
ту и количество производимых лечебных брон­
хоскопий необходимо индивидуализировать в
зависимости от состояния больного и динамики
клинического течения нагноительного процесса
в легком. Обычно число лечебных бронхоскопий
не превышает 2 процедур в неделю и 3—5 — за
курс лечения.
Лечебное воздействие на микробную флору
очагов нагноения в легких осуществляется ан­
тибактериальной терапией, эффект которой зна­
чительно усиливается, если одновременно ис­
пользуются методы, обеспечивающие адекват­
ное дренирование гнойных полостей. Эффектив­
ность антибактериальной терапии значительно
возрастает, если удается создать высокую кон­
центрацию лекарственных препаратов непосред­
ственно в очаге нагноения и окружающей легоч­
ной ткани. По этой причине практически не
назначаются антибиотики внутрь и внутримы­
шечно. Высокую концентрацию антибиотиков
в крови можно создать лишь их введением в
сосудистое русло.
Внутривенное круглосуточное введение боль­
ших доз антибиотиков (пенициллин — до
80 млн. ЕД в сутки, морфоциклин — 1 млн ЕД,
олеморфоциклин — 1000 мг, сигмамицин —
1500 мг. метициллин — 10 г, гентамицин —
180 мг, цепорин — 8—10 г и др.) может обес­
печить клинический эффект.
Одним из методов, позволяющих длительно
поддерживать высокие концентрации лекар­
ственных препаратов в патологически изменен­
ных тканях легкого, является регионарная ин­
фузия антибиотиков в легочную артерию. Этот
метод для лечения абсцессов легких начал широ­
ко применяться во ВНИИ пульмонологии
М3 СССР с 1967 г. [Углов Ф. Г. и др., 1968].
Широкому внедрению этого метода, как н род­
ственного ему способа введения антибиотиков
в бронхиальные артерии [Озолс А. Я., Михель­
сон М. О., 1972; Астафьев В. И. и др., 1980J,
препятствуют технические сложности практи­
ческого использования, а также недостаточ­
ность их теоретических обоснований. Прове­
денными в Московском институте антибиотиков
исследованиями М. И. Перельмана (1970) уста­
новлено, что концентрация антибиотиков в ле­
гочной ткани бывает одинаковой как при внут­
ривенном их введении, так и введении в легоч­
ную артерию.
Продолжаются поиски оптимальных путей
подведения антибиотиков к очагам нагноения
и деструкции в легких с целью создания там их
максимальной концентрации. Предлагаемый
А. В. Алексеенко и соавт. (1980), С. Б. Соколо­
вым и соавт. (1982) для лечения острых абсцес­
сов и абсцедирующих пневмоний метод внутри­
тканевого электрофереза основан на принципе
электроэлиминации — перемещении в ткань
легкого лекарственных препаратов (антибио­
тиков), циркулирующих в сосудистом русле,
воздействием на грудную клетку больного поля
постоянного электрического тока.
В последние годы широкое распространение
в лечении острых нагноений легких получила
антибактериальная терапия в сочетании с димексидом. Установлено [Брусиловский Б. М. н др.,
1983], что, связываясь с демиксидом несколь­
кими функциональными группами, пенициллин
и другие антибиотики удерживаются в очаге
поражения более длительно и в более высокой,
троекратной концентрации.
Подводя итог изложению вопросов антибак­
териальной терапии абсцессов и гангрены лег­
ких, можно считать, что отказываться от нее,
особенно в остром периоде заболевания, нет
основания. Однако не следует переоценивать
ее возможности. У подавляющего большинства
больных с острыми абсцессами и гангреной лег­
ких, лечившихся в госпитальной хирургической
клинике, антибиотики не применялись. В тех
случаях, где лечение антибиотиками было про­
ведено, каких-либо преимуществ такой терапии
мы отметить не смогли. К таким же выводам
пришли и другие. Так, В. И. Стручков и соавт.
(1978) с 1968 г. полностью исключили анти­
биотики из арсенала лечебных средств у больных
с острыми абсцессами и гангреной легких.
Консервативным лечением удается добиться
полного или клинического выздоровления прак­
тически у всех больных с острыми абсцессами
легких с хорошим бронхиальным дренажем в
течение 1—2 нед. У больных с острыми абсцес­
сами с недостаточным бронхиальным дренажем
такая терапия, как показали наши наблюдения,
оказалась эффективной в 81,2 % случаев. Одна­
ко ликвидация клинических признаков легоч­
ного нагноения наступала даже у излеченных
больных медленнее, чем в предыдущей группе,
обычно в период 3—4-й недели от начала лече­
ния. Кроме того, у 18,8 % больных различными
способами санации добиться выздоровления
не удалось, что вынудило прибегнуть к спосо­
бам наружного искусственного отведения гноя:
пункции легочных гиойииков, дренированию
с помощью торакоцентеза илн пневмотомии.
С этих же методов необходимо начинать лече­
ние больных с острыми блокированными абс­
цессами.
Пункционный метод лечения острых абс­
цессов легких является пограничным между
терапевтическим и хирургическим. Важное пре­
имущество его заключается в возможности
быстрой одномоментной эвакуации жидкого
гноя из полости деструкции, промывания ее и
введения непосредственно в очаг нагноения
164
лекарственных препаратов. Основным факто­
ром, определяющим лечебный эффект такой
процедуры, является уменьшение воспаления
в окружающей легочной ткани н дренирующих
бронхах, наступающее после аспирации гноя и
способствующее восстановлению их проходи­
мости. К недостаткам метода следует отнести
невозможность эвакуации густого гноя, детрита
и секвестров, необходимость в повторных пунк­
циях, опасность развития осложнений (флег­
мона мягких тканей грудной стенки, травмати­
ческий пневмоторакс, воздушная эмболия).
Более чем на 1500 пункций, произведенных
нами у 213 больных, пневмоторакс наблюдался
у 6 больных, флегмона грудной стенки — у 3,
воздушная эмболия — у 1 пациента, который
умер. По данным Ф. Г. Углова, В. Ф. Егиазаряна (1976), при проведении 908 пункций ослож­
нения имелись в 0,8 % случаев.
Техника пункции легочного гнойника не­
сложна. Прежде всего необходимо точно локали­
зовать место скопления гноя в легком и обозна­
чить на коже место наиболее близкого приле­
гания абсцесса к грудной стенке. Это делается
при многоосевом рентгеновском просвечива­
нии грудной клетки с врачом, производящим
пункцию. При этом ориентируются на уровень
жидкости в полости абсцесса, а при его отсут­
ствии — на центр воспалительного инфильтрата.
Свидетельством правильности положения
пункционной иглы является получение гноя,
который максимально аспирируется, после чего
полость обильно промывается каким-либо ан­
тисептическим раствором. Процедуру можно
завершить введением в полость абсцесса анти­
биотиков. Для профилактики флегмоны груд­
ной стенки при извлечении иглы целесообразно
надеть на нее чистый шприц с заранее заготов­
ленным раствором антибиотиков и инфильтри­
ровать им мягкие ткани по ходу извлечения
иглы.
Иногда в процессе пункции и в течение неко­
торого времени после нее наблюдается умерен­
ное кровохарканье, обычно прекращающееся
самостоятельно. Пункции производят ежеднев­
но или через день до восстановления проходи­
мости дренирующих бронхов и исчезновения
горизонтального уровня жидкости в полости
абсцесса. После этого целесообразно перейти
к лечению одним из методов санации брон­
хиального дерева. При лечении пункциями выздо­
ровели 88,2 % больных из наблюдавшихся
в клинике, у которых этот метод был применен.
У больных гангреной легких из-за распростра­
ненности и множественности деструкции, на­
личия некротических участков легочной ткани
добиться выздоровления методами санации
бронхиального дерева или пункциями, как
правило, не удается. Однако, как показал опыт
нашей клиники, лечение большинства больных
гангреной легких необходимо начинать с кон­
сервативного, в основу которого должны быть
положены принципы интенсивной терапии.
Объем и продолжительность консервативного
лечения у больных гангреной зависят от тяже­
сти состояния больного и динамики патологи­
ческого процесса. Показания к консервативному
лечению как основному и часто единственному
виду терапии:
— запущенные формы гангрены легких с
выраженной легочно-сердечной недостаточно­
стью и двусторонним поражением, когда резек­
ция легких противопоказана;
— трансформация гангренозного абсцесса
в обычный адекватно дренируемый острый абс­
цесс;
— неосложненная гангрена легких с отчет­
ливой благоприятной клинико-рентгенологи­
ческой динамикой заболевания на фоне прово­
димого лечения.
В остальных случаях гангрены легкого интен­
сивная терапия должна рассматриваться как
составная часть предоперационной подготовки
больного к хирургическому лечению, наиболее
эффективным видом которого является резекция
легких.
Гангрена легких, осложненная кровотече­
нием или повторяющимся кровохарканьем,
является показанием к срочному оперативному
вмешательству (резекции легкого). Во всех
остальных случаях резекции должны выполнять­
ся после консервативного лечения и интенсив­
ной терапии на протяжении не менее 7—10 сут.
Этот срок может быть сокращен у больных
бурно прогрессирующей гангреной легких.
Существенной частью интенсивной терапии
больных гангреной легких является инфузион­
ная терапия с целью парентерального питания,
коррекции волемических нарушений, улучше­
ния реологических свойств крови, поддержания
энергетического баланса и дезинтоксикации.
Необходимое для введения количество энерге­
тических и питательных растворов определя­
ется индивидуально для каждого больного в за­
висимости от массы тела, величины потерь белка,
воды и электролитов, динамики патологиче­
ского процесса в легких. Парентеральное пита­
ние у больных гангреной и осложненными абс­
цессами легких проводили по программе, раз­
работанной в клинике для оперированных по
поводу рака и хронических нагноительных забо­
леваний легких [Шанин Ю. Н., Костючен­
ко А. Л., 1975] - Поддержание энергетического
баланса при этом обеспечивается введением
концентрированных (25—40 %) растворов глю­
козы в дозе от 1 до 2 л/сут, а также чистого
96 % этилового спирта в дозе до 100 мл/сут
в виде слабых растворов.
165
Восполнение белковых потерь чаще всего
осуществляется с помощью белкового гидроли­
зата аминопептнда, который вводится в смеси
с концентрированной глюкозой. Доза амино­
пептида подбирается с таким расчетом, чтобы
обеспечить не менее 40—50 % потребности
в белках (аминокислотах), т. е. 0,9—1,2 л/сут.
Вспомогательное парентеральное питание долж­
но обеспечить поступление в организм больного
не менее 7—10 г азота и 1500—2000 ккал/сут.
Усвоение вводимого азота повышается при
одновременном введении анаболических гормо­
нов (неробол, ретаболил) и витаминов, особенно
группы В и С.
При гангренах и неблагоприятно протекаю­
щих абсцессах легких высокая протеолитиче­
ская активность сыворотки крови, обычно соче­
тающаяся с общей гиперферментемией, усугуб­
ляет воздействие интоксикации и определяет
необходимость применения ингибиторов протео­
лиза: контрикала в дозе до 80 тыс. ЕД/сут или
гордокса в дозе 200—300 тыс. ЕД/сут, кото­
рые вводятся в течение 5—7 дней.
Для дезинтоксикации и улучшения реологи­
ческих свойств крови, улучшения капиллярного
кровообращения применяют инфузии гемодеза
и реополиглюкина. Доза гемодеза — 2—5 мл/кг
массы тела 2 раза в неделю. Оправдано приме­
нение больным с абсцессами и гангреной лег­
ких внутривенных вливаний 1 % раствора хло­
ристого кальция по 300—400 мл 2 раза в неделю.
Этот препарат обладает противовоспалитель­
ным действием, понижает всасывающую спо­
собность капилляров, способствует нормализа­
ции функции почек.
В коррекции гипопротеинемии и анемии важ­
ная роль принадлежит гемотрансфузиям, про­
изводимым 1—2 раза в неделю. Предпочтитель­
нее переливать свежецитратную кровь, которая
не только корригирует гиповолемию н гипопро­
теинемию, но и уменьшает гипоксию тканей.
Для профилактики и лечения легочно-сердеч­
ной недостаточности у больных с острыми абс­
цессами и гангреной легких обычно приме­
няются коргликон, строфантин и эуфиллин. Ис­
пользуются также кордиамин и камфорное
масло.
Развитие острого гнойно-деструктивного про­
цесса в легочной ткани на фоне сниженной реак­
тивности организма определяет необходимость
проведения у таких больных терапии, способ­
ствующей повышению специфической и неспе­
цифической иммунореактивности. Для этих
целей используют стафилококковый бактерио­
фаг (ежедневные или через день внутримышеч­
ные инъекции в возрастающей дозировке —
0,5—1 — 1,5—2 — 2,5 мл), стафилококковый
анатоксин (подкожно в возрастающей дози­
ровке 0,1—0,3—0,6—0,8—1 мл и т. д. до 2 мл
с интервалами между введениями 3 дня), антистафилококковый полиглобулин внутримышеч­
но по 9 мл в течение 3 дней, а также препараты
неспецифической иммунизации — гаммаглобулин внутримышечно из расчета 0,2 мл/кг массы
тела 1 раз в 2 нед. Для стимуляции лейкопоэза
и лейкоцитоза назначают пентоксил, лимфо­
поэза — леакадин. Н. Б. Егорова и соавт.
(1983) для лечения больных с острыми абсцес­
сами легких применили вакцину, состоящую из
антигенных комплексов клебсиеллы, протея,
кишечной палочки и стафилококка. Вакцина­
ция способствовала улучшению состояния и
сопровождалась ростом титров гемагглютининов
ко всем антигенам, входящим в комплекс. В ка­
честве эффективных иммуностимуляторов могут
быть использованы диуцифон, бактериофаги
[Ермаков Е. В. и др., 1983J. По данным В. И.
Стручкова и Л. М. Недвецкой (1983), в группе
больных, где в комплекс лечения была включена
пассивная и активная иммунизация, полное
выздоровление наступило у 32,7 %, клиниче­
ское — у 61,3 %, процесс перешел в хрониче­
скую форму — в 6 % случаев. У больных, ле­
чившихся только антибиотиками, результаты
намного хуже: 18,8 %; 43,4 %; 33,7 % соответ­
ственно.
Больным с абсцессами и гангреной легких
показана симптоматическая терапия. Приме­
нение наркотических анальгетиков (пантопон,
морфин) с целью снятия болевых ощущений
нецелесообразно из-за резкого угнетения ими
дыхательного центра и кашлевого рефлекса.
Для этого чаще используют ненаркотические
анальгетики (50 % раствор анальгина внутримы­
шечно). Применяют также жаропонижающие
средства, препараты, нормализующие сон,
повышающие аппетит, снимающие раздражи­
тельность.
Выраженная гипоксия паренхиматозного
и циркуляторного происхождения является
одной из главных причин тяжелого состоя­
ния больных с абсцессами и. особенно, гангре­
ной легких, а также одним из основных про­
тивопоказаний к оперативному лечению гангре­
ны легких. Она занимает ведущее место в струк­
туре причин летальных исходов после резек­
ций. В госпитальной хирургической клинике,
в течение многих лет занимающейся разработ­
кой проблемы лечения нагноительных заболе­
ваний легких, это обстоятельство определило
необходимость поиска более эффективных,
чем обычная оксигенотерапия, методов борьбы
с гипоксией. Данные, полученные в эксперимен­
те и в клинической практике, показали [Лыт­
кин М. И. и др., 19821, что гипербарическая
оксигенация в определенных режимах безопас­
на у больных с острыми абсцессами и гангре­
ной легких в отношении развития баротравмы
166
легких (даже при отсутствии наружного дрени­
рования полости) и не нарушает механизмов,
обеспечивающих газообмен в функционирую­
щей зоне легочной паренхимы. Обеспечивая
восстановление кислородного режима организма
во время сеанса, она изменяет метаболический
фон, на котором развивается острый нагноительный процесс, стабилизирует жизненно важные
функции, повышает возможности механизмов
естественной детоксикации и переводит орга­
низм на наиболее экономичный режим исполь­
зования энергетических ресурсов. Клинический
эффект был достигнут у 72 % больных с остры­
ми абсцессами и гангреной легких, у которых
она применялась.
Вопрос о выборе хирургического метода ле­
чения острых нагноений легких встает всякий
раз, когда консервативная терапия, с которой
всегда начинается лечение, оказывается неэф­
фективной. Нередко этот вопрос возникает зна­
чительно раньше, сразу же после поступления
больного в хирургический стационар, особенно
в случаях бурно прогрессирующего и ослож­
ненного течения заболевания.
Применяющиеся методы хирургического
лечения острых абсцессов и гангрены легких
делятся на две группы: дренирование и резек­
ции. Дренировать гнойно-деструктивные поло­
сти в легких можно или менее травматичным
и щадящим способом — с помощью торакоцентеза и дренажной трубки, или более травма­
тичным — торакотомией и пневмотомией. Каж­
дый из способов оперативного дренирования
имеет свои преимущества и недостатки. Опера­
ции как дренирования, так и резекции предпри­
нимаются с одной целью — обеспечить быстрое
и по возможности максимально полное освобож­
дение больного от гноя и омертвевших участ­
ков легочной ткани. Если последние преоблада­
ют, задача полнее решается резекцией поражен­
ного участка легочной ткани или всего легкого.
Резекция легкого, однако, является весьма
травматичным оперативным вмешательством.
Дренирующие операции менее продолжительны
и намного менее травматичны. Они переносимы
даже тяжелобольными. Однако положитель­
ный эффект их менее выражен, особенно у боль­
ных, у которых имеются множественные поло­
сти деструкции и некротические ткани, часто
еще не отторгнувшиеся, которые вскрыть и дре­
нировать полностью обычно не удается.
Относительная простота и безопасность, но
меньшая эффективность дренирующих опера­
ций, технически большая сложность, травма­
тичность и риск, но более высокая эффектив­
ность резекций и определяют трудности, с кото­
рыми сталкивается хирург, выбирая оптималь­
ный метод хирургического лечения у каждого
конкретного больного.
Щадящую методику дренирования патоло­
гических полостей в легких путем введения
дренажа через троакар у больных с абсцессами
и гангреной легких впервые в нашей стране раз­
работал и начал использовать в госпитальной
хирургической клинике академии Л. С. Лесницкий (1968).
Показания к использованию торакоцентеза
для дренирования острых абсцессов легких
возникают у больных, у которых обычные мето­
ды санации бронхиального дерева или пункции
легочных гнойников не позволяют в течение
1—2 нед. добиться хорошего опорожнения абс­
цессов через дренирующие бронхи. Опыт кли­
ники в применении этого метода показывает,
что он может быть с успехом использован как
при множественных абсцессах в одном легком,
так и у больных с абсцессами в обоих легких.
При этом каждый гнойник дренируется отдель­
но либо одномоментно, либо с интервалом меж­
ду операциями в несколько дней.
Анализ результатов лечения гангрены легких
методом дренирования торакоцентезом пока­
зал, что в качестве самостоятельного он может
применяться лишь у больных с конечными ста­
диями гангрены, т. е. с большими деструктив­
ными полостями, содержащими жидкий гной
или мелкие секвестры. В последних случаях
целесообразно введение через дренаж фермен­
тов для ускорения лизиса омертвевших участ­
ков легочной ткани. Дренирование торакоцен­
тезом может быть использовано у тех больных
гангреной легких, у которых резекции и даже
пневмотомия представляют большой риск. Ис­
пользование дренирования торакоцентезом для
подготовки к резекции малооправданно из-за
опасности осложнений и формирования тора­
кального свища, для устранения которого необ­
ходимо дополнительное, хотя и небольшое, но
нежелательное в условиях острой гнойной ин­
фекции оперативное вмешательство.
Техника дренирования торакоцентезом
проста, но требует определенных навыков
и опыта. Вначале длинной толстой иглой произ­
водятся пункция гнойника и аспирация гноя.
Далее определяют глубину, на которую нужно
ввести троакар. Это можно сделать с помощью
второй иглы такого же размера, как и введен­
ная в полость, по разнице их длины.
Рядом с иглой производится разрез кожи
и поверхностной фасции длиной около 1,5 см,
через который по игле в межреберье и легкое
вводится троакар. Через трубку троакара в по­
лость гнойника проводится дренаж- Показа­
телем успешного дренирования служат свобод­
ный отток гноя или отхождение воздуха через
дренажную трубку. Кожная рана ушивается
швами, концы которых завязываются и фикси­
руют дренажную трубку.
167
Рис. 92. Гангрена верхней доли правого легкого в стадии
гигантского абсцесса, полость которого дренирована посред­
ством торакоцентем.
Рис. 93. Рентгенограмма того же больного, что на рис. 92.
Большая сухая остаточная полость в верхней доле правого лег­
кого. на дне которой ви 1на дренажная трубка.
После дренирования местоположение дре­
нажа контролируется рентгеноскопией. Для
оценки формы и размеров гнойника, а также
состояния проходимости дренирующих бронхов
через дренаж вводится водорастворимое конт­
растное вещество (кардиотраст, диодон) в коли­
честве 10—20 мл. Эти данные нужны для суж­
дения об особенностях патологических изме­
168
нений и их динамики при контрольных иссле­
дованиях в процессе лечения (рис. 92, 93).
Рентгеноскопия сразу после дренирования необ­
ходима и для своевременной диагностики пнев­
моторакса, являющегося наиболее частым
осложнением этого ме года дренирования.
Чтобы обеспечить постоянное отхождение
гноя через дренаж, последний можно оставлять
открытым под толстой ватно-марлевой повязкой,
впитывающей гной, или соединять с другой дре­
нажной трубкой, опущенной под воду, по Бю­
лау — Петрову. Можно использовать и вакуум­
ное дренирование с разрежением, не превышаю­
щим 20—30 см вод. ст. Более высокая степень
разрежения в деструктивной полости может
спровоцировать аррозионное кровотечение.
При промывании полости через дренаж необ­
ходимо соблюдать ряд правил: количество од­
номоментно вводимого через дренаж раствора
зависит от размеров полости, но, как правило,
при первых промываниях не должно превы­
шать К)—30 мл. Раствор следует вводить под
очень малым давлением, он должен поступать
в полость свободно. По реакции больного на
введение первой порции раствора можно судить
о степени проходимости дренирующих гной­
ник бронхов: если они проходимы, сразу же
откашливаются гнойная мокрота и вводимый
раствор. Если бронхи непроходимы, введенный
раствор вместе с гноем оттекает только через
дренаж. Промывать полость нужно до тех пор,
пока последние порции оттекающего через
дренаж раствора не станут прозрачными, не
содержащими детрита и фибринных пленок.
Если в течение 5—7 дней такой санации умень­
шается количество гнойного отделяемого по
дренажу и изменяется его характер, уменьша­
ется количество и изменяется характер мокро­
ты (нередко вначале зловонная и густая, она
постепенно становится более жидкой, слизисто­
гнойной, а затем слизистой без запаха), сни­
жается температура и улучшается общее состоя­
ние больного, то дренирование торакоцентезом можно считать эффективным. Дренаж
может быть удален, как только нормализуются
температура и картина крови, прекратится отде­
ление гнойной мокроты и гноя через дренаж,
а рентгенологическим исследованием будут
установлены исчезновение
воспалительной
инфильтрации в окружности полости, уменьше­
ние ее размеров при отсутствии в ней горизон­
тального уровня жидкости. Весьма интересным
и перспективным является метод лечения ост­
рых и гангренозных абсцессов, предложенный
М. Л. Шулутко и Г. Л. Некрич (1983), являю­
щийся усовершенствованным способом торакоцентеза и дренирования. После торакоцентеза через троакар выполняется торакоабсцессоскопия с помощью стержня-носителя с теле-
скопом и манипулятором для дробления и уда­
ления секвестров, коагуляции мелких сосудов
и обработки стенок полости. По эффективности
эта процедура близка к пневмотомии, однако
не усугубляет тяжести функциональных рас­
стройств и не сопровождается развитием бронхоплевроторакального свища.
Метод дренирования торакоцентезом был
использован нами у 80 больных с острыми абс­
цессами и 27 больных гангреной легких У 10
больных первой группы полость абсцесса зажи­
ла к моменту их выписки из клиники. 70 больных
выписались без клинических признаков легоч­
ного нагноения с сухими остаточными поло­
стями: у 29 из них полости в последующем
исчезли, у 39 они остались стойкими, но без
признаков рецидива нагноительного процесса;
2 пациента вернулись в клинику с обострением
нагноительного процесса. Результаты лечения
дренированием с помощью торакоцентеза боль­
ных гангреной легких намного хуже. Из 27 боль­
ных у 20 дальнейшее течение заболевания по­
требовало изменения лечебной тактики: 10 па­
циентам была сделана пневмотомия, у осталь­
ных 10 произведена резекция легкого. Только
у 7 больных гангреной легких в стадии гигант­
ского абсцесса дренирование торакоцентезом
было окончательным методом лечения и оказа­
лось эффективным. Причины неудач применения
этого метода при гангрене легких чаще всего
заключались в прогрессировании гангрены,
наличии множественных полостей распада и
крупных секвестров легочной ткани. Упорство­
вать в лечении больных гангреной таким дре­
нированием очень опасно, так как процесс в
легком может прогрессировать довольно быстро
и наиболее благоприятный момент для выпол­
нения резекции легкого окажется упущенным.
Остаточная полость, представляющая собой
один из вариантов эволюции острых абсцессов
легких, встречается очень часто — у 25—85 %
больных (Дубенский Ю. М. и др., 1980; Му­
стафин Д. Г., 1980]. Мнение о том, что остаточ­
ная полость ввиду потенциальной угрозы раз­
вития хронического нагноительного процесса
является показанием к радикальной операции,
не подтвердилось временем. Общепризнанной
сейчас является точка зрения, согласно которой
остаточные полости подлежат динамическому
наблюдению, а к оперативному лечению необ­
ходимо прибегать лишь в случаях обострения
нагноительного процесса или возникновения
повторяющихся кровохарканий или кровоте­
чения. Среди 374 больных, лечившихся в госпи­
тальной хирургической клинике консервативно,
68,5 % были выписаны с сухой остаточной по­
лостью, которая у большинства из них (78,8 %)
ликвидировалась после выписки в течение 2—
12 мес. Лишь у 3,4 % больных через I1/?—5 мес
после выписки наблюдался рецидив нагнонтельного процесса, и они были подвергнуты
оперативному лечению. У 17,8 % больных оста­
точные полости стали стойкими и при сроках
наблюдения от 1 года до 10 лет оставались бес­
симптомными. Скорее всего произошла эпителизация внутренней поверхности этих полостей
из устьев дренирующих бронхов, и они превра­
тились в кистоподобные образования.
К дренирующим операциям при острых на­
гноениях легких относится и пневмотомия.
В настоящее время пневмотомия является опе­
рацией выбора при гангренозных абсцессах лег­
ких с крупными секвестрами в деструктивных
полостях, а также в запущенных случаях абс­
цессов и гангрен, где консервативное лечение
бесперспективно, а резекции противопоказаны.
Клиника располагает опытом применения
пневмотомии у 42 больных с острыми абсцес­
сами и 25 пациентов — гангреной легких. Умер­
ли соответственно 6 и 28 % оперированных
больных. Выписано из клиники после пневмо­
томии 85 % больных. Казалось бы, результат
хороший. И это в действительности так, если
оценивать его с точки зрения сохраненной боль­
ному жизни. Но больной, вернувшийся к жизни,
стремится к тому, чтобы она была полноценной.
А этому мешают осложнения, с большим посто­
янством возникающие после пневмотомии н
омрачающие ее непосредственный хороший
результат. Так, лишь у 3 больных, которым были
вскрыты небольшие полости деструкции, брон­
хокожный свищ закрылся в стационаре и в даль­
нейшем обострений нагноительного процесса
не было. Все остальные выписаны со стойкими
бронхоплеврокожными свищами.
Наличие стойких торакальных свищей и необ­
ходимость в постоянном амбулаторном лече­
нии вынуждают больных, перенесших пневмо­
томию, настаивать на повторных оперативных
вмешательствах. Ликвидировать свищ, не при­
бегая при этом к резекции части легкого, в кото­
рой локализуется полость, или всего легкого,
очень трудно. Мы безуспешно пытались это
сделать у 3 больных.
Более надежным способом ликвидации свища
после пневмотомии является резекция части
легкого, несущей свищ, или всего легкого. Однако
на эту травматичную операцию и больному,
и хирургу решиться не всегда просто. В сроки
от 5 мес до l'/s лет мы выполнили 5 таких опе­
раций: две пневмонэктомии и две правосторон­
ние нижние билобэктомии, правостороннюю
верхнюю лобэктомию. Больные выздоровели.
Другим осложнением пневмотомии является
аррозивное кровотечение, наблюдавшееся нами
у 3 больных и явившееся причиной смерти у
одного из них. Двое других подверглись резек­
циям легких по этому поводу.
169
Наш опыт резекций легких у больных, кото­
рым в прошлом производилась пневмотомия,
еще невелик. Однако он показал, что в области
торакального свища всегда имеются обширные
плотные сращения, затрудняющие вскрытие
плевральной полости и выделение легкого. Вы­
деление же и обработка элементов корня лег­
кого бывают чаще всего технически даже более
простыми, чем в острой фазе абсцесса или ган­
грены легких, так как пневмотомия, обеспечи­
вая хорошее дренирование гноя, способствует
уменьшению перифокального воспаления и лим­
фаденита в корне легкого. Поэтому для закры­
тия броихокожных свищей, а также в случаях
аррозивных кровотечений следует, если позво­
ляет состояние больного, чаще прибегать к ре­
зекции легкого.
Тяжелым, но, к счастью, редким осложнением
пневмотомии у больных с абсцессами и гангре­
ной легких является флегмона грудной стенки.
В литературе имеются лишь единичные сооб­
щения об этом осложнении [Логвиненко П. И.,
1954). Мы встретились с ним у 2 больных,
которые погибли. Чтобы предупредить распро­
странение нагноения на мышцы грудной стенки,
целесообразно изолировать их, сшивая края рас­
сеченной кожи с поверхностной фасцией или
париетальной швартой.
Необходимость резекций легких у больных
гангреной не вызывает сомнений. Однако еди­
нодушия взглядов нет, когда речь заходит о
показаниях к резекциям легких у больных с
острыми абсцессами. У же говорилось о том, что
подавляющее большинство больных с острыми
абсцессами легких излечиваются консерватив­
ными методами или оперативным дренировани­
ем. Следовательно, на долю резекций легких
остается та небольшая часть больных с острыми
абсцессами легких, у которых перечисленные
методы лечения в конце концов оказались не­
эффективными.
В связи с этим встает очень важный вопрос
о критериях эффективности консервативного
лечения и сроках, в течение которых затянув­
шееся легочное нагноение может считаться
хроническим и поэтому подлежащим радикаль­
ному хирургическому лечению. Сухая остаточ­
ная полость как ближайший благоприятный
исход острых абсцессов легких большинством
хирургов не рассматривается показанием к ре­
зекции. В этом убеждает и многолетний опыт
госпитальной хирургической клиники.
При трактовке нагноительного процесса в
легких как острого или хронического нужно
ориентироваться не столько на временные сроки
существования патологического процесса в ле­
гочной ткани, сколько на клинические проявле­
ния его, общую направленность течения заболе­
вания, функциональные изменения органов
и систем. При неблагоприятном течении острого
абсцесса легкого важное значение имеет комп­
лексная оценка клинических и рентгенологиче­
ских данных. Трактовка последних должна про­
водиться строго дифференцированно и обяза­
тельно в динамике. Так, длительное существо­
вание сформировавшейся после острого абсцесса
сухой остаточной полости, даже очень большой,
но протекающей бессимптомно, допускает воз­
можность дальнейшего активного наблюдения
за больным. Невозможность купировать ост­
рый нагноительиый процесс в легком консер­
вативным лечением или оперативным дрениро­
ванием, прогрессирование заболевания по кли­
ническим и рентгенологическим данным, мно­
жественный характер поражения, повторяю­
щиеся кровохарканья или кровотечение, со­
храняющаяся вокруг полости деструкции пери­
фокальная инфильтрация или уровень жидко­
сти в полости, рецидив нагноительного процесса
в сухой остаточной полости в любые сроки опре­
деляют необходимость в оперативном лечении —
резекции легкого.
Целесообразность ранних (в сроки от 3 до
6 нед от начала заболевания) резекций легких
при острых абсцессах [Чернобровый Н. П. и др..
1970; Воронов А. А. и др., 1983] не подтвержда­
ется анализом наших наблюдений. Использо­
вание ранних резекций у больных с острыми
абсцессами легких принесет больше вреда, чем
пользы. Любые резекции, выполняемые в ост­
ром периоде заболевания, являются операция­
ми повышенного риска. Частое их применение
сопряжено с реальной опасностью роста леталь­
ности и будет дискредитировать идею радикаль­
ных вмешательств среди врачей и больных. Кро­
ме того, ориентация на ранние резекции у боль­
ных с острыми абсцессами легких препятствует
своевременному использованию оперативного
дренирования легочных гнойников, т. е. более
щадящего и безопасного метода, позволяющего
излечить большую часть больных, у которых
консервативное лечение оказалось неэффек­
тивным.
Однако наряду с этим не подлежит сомне­
нию, что полный отказ от резекций в острой
фазе был бы неправильным. Бурное прогресси­
рование заболевания или массивное легочное
кровотечение уже в ранние сроки делают оче­
видной бесперспективность самой энергичной
консервативной терапии или щадящих вмеша­
тельств. По данным П. М. Кузюковича (1978),
среди 353 больных с острыми абсцессами легких
необходимость в радикальных операциях в ост­
ром периоде заболевания возникла только у
3 % лечившихся пациентов.
Показания к ранним резекциям у таких боль­
ных расширяются при подозрении на новообра­
зование.
170
Уже первый опыт использования резекций
легких при гангрене поставил на повестку дня
несколько важных практических вопросов, а
именно: выбор оптимального срока резекции,
а также целесообразность (если да, то продол­
жительность) предоперационной подготовки.
Успешно выполненные ранние резекции, в том
числе и по поводу гангрен, осложненных кро­
вотечением, вселяли оптимизм и уверенность
в оправданности резекции в ближайшие дни
после установления диагноза гангрены легких
[Амосов Н. М., 1958; Пастухов Н. А., 1975].
Неудачи, которых не удалось избежать ни одно­
му из хирургов, оперировавших больных гангре­
ной, заставляли смотреть на резекцию легких
при гангрене как иа операцию необходимую,
но возможную лишь после стабилизации состоя­
ния больного с помощью консервативной тера­
пии [Вагнер Е. А. и др., 1971; Даниленко М. В.
и др., 1974, н др.].
Мнение о необходимости радикального хирур­
гического вмешательства при распространенной
гангрене легких становится в настоящее время
господствующим среди хирургов. Что касается
тактики при запущенных формах гангрены лег­
ких и ограниченной гангрене (гангренозном
абсцессе), то точки зрения по этому вопросу
довольно разноречивы. При ограниченных фор­
мах гангрены легких предлагаются ранние резек­
ции [Цыбырнэ К. А., 1982], дренирование торакоцентезом [Кузюкович П. М., 1978 [.
Опыт лечения гангрены легких резекциями, на­
копленный в последние годы, особого оптимизма,
однако, не вызывает. Смертность продолжает
оставаться высокой — от 27 до 70 % |Григорян
А. В. и др., 1980; Цыбырнэ К. А. и др., 1980;
Вагнер Е. А. и др., 1980, и др.|. Поэтому про­
должается поиск наименее травматичных и наи­
более надежных способов лечения. Так, А. Н. Ка­
банов и Л. А. Ситко (1980), К. Н. Сазонов и др.
(1984) предлагают придерживаться тактики ран­
них паллиативных вмешательств (пневмотомии,
торакотомии), поэтапных, после стабилизации
состояния, радикальных вмешательств, бронхо­
логических методов санации и интенсивной те­
рапии. Такая тактика лечения у 48 больных по­
зволила им снизить летальность до 23 %. У боль­
ных гангреной легких, находящихся в тяжелом
состоянии, риск резекции у которых очень велик,
предлагается трансперикардиальная окклюзия
бронха на стороне поражения и перевязка легоч­
ных очагов деструкции [Цыбырнэ К. А. и др.,
1982]. Такая операция предупреждает крово­
течение и аспирацию гноя в противоположное
легкое. В последующем, когда состояние боль­
ного стабилизируется, может быть выполнено
радикальное вмешательство. Легкое может быть
оставлено и in situ, как биологическая пломба.
Опыт клиники госпитальной хирургии, охваты­
вающий наблюдения за 170 больными гангреной
легких, 110 из которых подверглись резекциям,
позволил прийти к выводу, что лишь гангрена
легких, осложненная кровотечением или повто­
ряющимся обильным кровохарканьем, является
показанием к срочной резекции. Во всех осталь­
ных случаях резекции должны выполняться
после консервативной терапин и интенсивного
лечения на протяжении не менее 7—10 сут.
Этот срок может быть даже сокращен у больных
с бурно прогрессирующей формой заболевания.
Гангрена легких, осложненная пиопневмотораксом или эмпиемой плевры, не является про­
тивопоказанием для резекции.
Среди 144 больных гангреной легких, подверг­
шихся в госпитальной хирургической клинике
различным методам хирургического лечения,
общая летальность составила 26,3%. Леталь­
ность после резекций легких составила 27,2%,
после пневмотомии •— 26,9% и после дренирова­
ния торакоцентезом — 12,5%. Среди всех 170
больных, в том числе и лечившихся консерва­
тивно, умерли 49 (28,8%).
Глава /
ХРОНИЧЕСКИЕ
АБСЦЕССЫ ЛЕГКИХ
Острый абсцесс легкого в ряде случаев не
заканчивается выздоровлением, не наступает
своевременного адекватного его дренирования,
и течение заболевания затягивается. Некоторые
авторы выделяют в таких случаях подострые
абсцессы легких, характеризующиеся вялотеку­
щим течением, когда имеются незначительные
сдвиги к улучшению в определенные моменты
времени. Выздоровление, однако, не наступает,
и в конечном итоге болезнь принимает хрони­
ческий характер с типичными ремиссиями и
обострениями.
ПУТИ РАЗВИТИЯ
ХРОНИЧЕСКИХ АБСЦЕССОВ
ЛЕГКИХ
Трансформацию острого абсцесса в хрони­
ческий определить подчас очень трудно, а иногда
и невозможно. Существующие морфологиче­
ские критерии не могут, к сожалению, исполь­
зоваться в клинической практике. Общеприня­
тый календарный срок — 4—6 нед. (по неко­
торым данным — 3—4 нед.) часто не является
верным, так как не отражает всегда существо
морфологических изменений, большая вариа­
бельность которых определяется особенностями
клинического течения заболевания у каждого
конкретного больного.
Если при остром абсцессе легких основным
морфологическим признаком является полость
с гноем, стенки которой состоят из самой легоч­
ной ткани, то при хроническом абсцессе они
образованы соединительной тканью. По данным
И. К. Есиповой (1952), образование соедини­
тельнотканной капсулы можно отметить к исхо­
ду 6—8-й недели от начала болезни. Образо­
вавшаяся капсула утолщается за счет разрас­
тающейся соединительной ткани. Она делается
ригидной. Уплотняется также легочная ткань
вокруг полости деструкции. Продолжающийси
нагноительный процесс в полости абсцесса и
сочетанный воспалительный в окружающей
паренхиме взаимно поддерживают друг друга.
Постепенно происходит гнойная инфильтрация
окружающей хронический гнойник легочной
ткани. В окружности его могут возникать вто­
ричные гнойники, что ведет к распространению
гнойного процесса на ранее не пораженные
участки легкого. Вскрываясь в бронхиальное
дерево, множественные гнойники способствуют
генерализации процесса по бронхам. Развива­
ются диффузный бронхит, панбронхит и пери­
бронхит. Нагноительный процесс начинает рас­
пространяться и по бронхам, стенки которых
перерождаются, теряют свою эластичность.
Нарушение перистальтики бронхов, закупорка
их просвета гноем приводят к образованию оча­
говых ателектазов и вторичных бронхоэктазий.
Возникает типичный хронический нагноитель­
ный процесс в легком, основными компонента­
ми которого являются плохо дренируемый хро­
нический абсцесс, периферично расположен­
ные вторичные бронхоэктазии, а также разно­
образные изменения легочной ткани в виде
выраженного склероза, деформации бронхов,
бронхита и др. При этой форме поражения весь
деструктивный комплекс локализован участком
легочной ткани, в центре которого находится
основной очаг — первичный хронический абс­
цесс легкого.
В результате длительного течения хрониче­
ского нагноительного процесса образуется свое­
образный порочный круг, когда возможностей
для спонтанного заживления и разрешения за­
болевания практически не остается. Усиливаю­
щиеся процессы пневмосклероза ведут к нару­
шению трофнки легочной ткани, что усугубляет
течение заболевания и способствует непрекрашающемуся воспалительному процессу, кото­
рый, в свою очередь, является причиной даль­
нейшего развития и распространения деструк­
тивных изменений.
Большое практическое значение представ­
ляет изучение причин перехода острого абсцесса
в хронический, наблюдавшегося в 4,7—12,1 %
случаев [Захаров Н. А. и др., 1980; Егиазарян В. Ф., Толузаков В. Л., 1980; Мустафин Ф. Г.,
1980, и др.]. Значительно чаще — в 32,7 % —
переходят в хронические острые осложненные
абсцессы легких [Марчук И. К., 1980]. Несом­
ненно, существенную роль играет неполноцен­
ное лечение в остром периоде. У большинства
наблюдавшихся в госпитальной хирургической
172
клинике больных с хроническими абсцессами
лечение в остром периоде, проводившееся в тера­
певтических стационарах, сводилось только к
парентеральному введению антибиотиков.
Все же не подлежит сомнению, что у ряда
больных особенности острого патологического
процесса не позволяют ликвидировать его даже
при интенсивном комплексном консервативном
лечении. Причинами, способствующими пере­
ходу острого абсцесса в хронический, являются:
I) недостаточный отток гноя из полости абсцес­
са через бронхи вследствие нарушения прохо­
димости последних; 2) наличие в полости абс­
цесса секвестров, закрывающих устья дрени­
рующих бронхов и постоянно поддерживаю­
щих нагноение в самой полости и воспаление
вокруг нее; 3) повышенное давление в полости
абсцесса; 4) образование плевральных сращений
в зоне пораженных абсцессом сегментов легких,
препятствующих раннему спадению и облитера­
ции полости; 5) эпителизация полости из устьев
дренирующих бронхов.
Наибольшее значение, по-видимому, имеет
недостаточное опорожнение абсцесса от гноя,
чему способствует положение дренирующего
бронха в полости абсцесса. Считается, что по
этой причине хронические абсцессы чаще разви­
ваются в нижних долях. Среди наблюдавшихся
в клинике больных с острыми абсцессами, кото­
рые лечились консервативно, частота перехода
в хронические была одинаковой при локализа­
ции абсцессов как в верхних, так и в нижних
долях. Однако среди больных с хроническими
абсцессами все же отмечалось выраженное пре­
обладание изолированных или сочетанных пора­
жений задних сегментов (II и VI справа — у
71,5 % и VI слева — у 73,2 % больных), брон­
хи которых отходят кзадн, что создает неблаго­
приятные условия для оттока гноя при поло­
жении больного на спине. По-видимому, это
обстоятельство, учитывая редкое использова­
ние методов санации бронхиального дерева и
постурального дренажа, могло иметь опреде­
ленное значение. В то же время частота хрони­
ческих абсцессов в I и III сегментах верхней
доли правого легкого и III сегмента верхней
доли левого легкого, находящихся в наилучших
условиях естественного дренирования, была
даже большей, чем в базальных сегментах,
условия дренирования которых наименее бла­
гоприятны. Эти факты свидетельствуют о том,
что при правильном лечении отношение дрени­
рующего бронха к полости гнойника, по-види­
мому, не играет существенной роли.
Недостаточное опорожнение гноя чаще всего
зависит от нарушений проходимости дренирую­
щих бронхов в остром периоде заболевания.
Так, из 55 больных с острыми абсцессами лег­
ких, у которых методом контрастирования поло­
сти гнойника изучена проходимость дренирую­
щих бронхов, в 80 % наблюдений жидкий кар­
диотраст, введенный в полость, дренирующие
бронхи из-за их стойкой непроходимости не
заполнил. Среди наблюдавшихся больных с хро­
ническими абсцессами рентгенологическим
исследованием, включавшим бронхографию, а
также макроскопическим изучением препаратов
после резекций легких более чем у половины
были найдены нарушения проходимости дре­
нирующих бронхов. У части этих больных по­
лость абсцесса вообше ие имела сообщения
с дренирующими бронхами, т. е. была блокиро­
ванной. Среди больных с острыми абсцессами
переход их в хронические также отмечался глав­
ным образом у больных, у которых консерва­
тивным лечением не удалось восстановить на­
рушенную проходимость дренирующих бронхов.
Раннее восстановление бронхиального дренажа
всегда обеспечивало благоприятное течение
легочного гнойника при консервативном ле­
чении.
Свободные секвестры легочной ткани, пре­
пятствующие заживлению острого абсцесса
и поддерживающие хроническое нагноение,
были обнаружены у 12 из 95 больных, опери­
рованных в сроки от 2 до 6 мес от начала забо­
левания [Колесников И. С., Вихриев Б. С., 1973).
У многих больных роль секвестров играет гу­
стой замазкообразный гной. Он не может сво­
бодно оттекать через дренирующие бронхи,
закупоривает их, чем и обусловливает неблаго­
приятное течение процесса при консервативном
лечении. Среди оперированных в госпитальной
хирургической клинике больных с хроническими
абсцессами легких такого рода гнойники были
обнаружены почти у 25 % пациентов.
Причины образования такого гноя неясны.
Высказывалось предположение, что гнойное
расплавление некротизированных тканей в поло­
сти абсцесса происходит медленнее у больных,
которые лечатся антибиотиками, вследствие
угнетения жизнедеятельности микрофлоры и
снижения ее ферментативного воздействия на
омертвевшие ткани.
Клапанный механизм в устье дренирующих
бронхов, препятствующий заживлению острого
абсцесса, отмечен нами у 13 % больных с ост­
рыми абсцессами легких. Об этом свидетель­
ствовали огромные полости деструкции в нача­
ле заболевания, которые в процессе консер­
вативного лечения очень быстро уменьшались.
Повышенное давление в полости абсцесса, если
оно не является стойким, по-видимому, не явля­
ется ведущей причиной перехода острого абс­
цесса в хронический, поскольку среди больных
с острыми абсцессами, у которых клапанный
механизм в устьях дренирующих бронхов был
заподозрен, хроническое течение заболевания
173
в последующем было отмечено лишь в 2,3 %
случаев.
Эпителизация полости острого абсцесса из
устьев дренирующих бронхов, наступающая
при больших его размерах и длительном тече­
нии, способствует возникновению хронического
абсцесса потому, что образовавшаяся в резуль­
тате этого ложная киста самостоятельно никогда
не ликвидируется и постоянно таит в себе угрозу
рецидива нагноения, т, е. перехода заболевания
в хроническую форму. Развитие хронического
абсцесса на фоне сухой эпителизированной поло­
сти как исхода острого абсцесса, по данным
различных авторов, отмечается в 5—10 % на­
блюдений.
В. Ф. Егиазарян, В. Л. Толузаков (1980) об­
следовали в отдаленные сроки 111 больных с
сухими остаточными полостями: у 55 (49,5 %)
из них полости продолжали сохраняться, у 50
(45 %) — закрылись, и лишь у 6 (5,5 %) боль­
ных наступал рецидив нагноения.
Вероятность возникновения нагноения в сухой
остаточной полости увеличивается при ее боль­
ших размерах. По данным Г. Л. Некрич (1983),
при анализе отдаленных результатов у 83 боль­
ных с гигантскими абсцессами (более 6 см
в диаметре) рецидивирующее течение процес­
са отмечено у 15,7 %.
Возможность развития хронического абсцесса
возрастает также в случаях множественных
острых абсцессов, когда влияние неблагоприят­
ных факторов, способствующих переходу ост­
рого процесса в хронический, делается более
вероятным [Федоров Б. П., Воль-Эпштейн Г. Л.,
I976J. Среди больных, лечившихся в госпиталь­
ной хирургической клинике, хронические абс­
цессы были множественными намного чаще
одиночных (соответственно 47 и 16,6 %).
Таким образом, наиболее часто хронический
абсцесс легкого представляет собой вариант
исхода острого абсцесса. Этому способствуют
перечисленные выше неблагоприятные факторы,
а также дефекты проводимого консервативного
лечения. Характерным патологоанатомическим
признаком такого исхода острого абсцесса явля­
ется ограниченность поражения, чаще всего
бронхолегочным сегментом или долей. Длитель­
ное существование хронического абсцесса по­
степенно приводит к образованию пневмоскле­
роза, ателектазов и вторичных бронхоэктазий.
Хронический нагноительный процесс в легоч­
ной ткани с образованием в ней таких же морфо­
логических элементов может развиваться и по
другому, более длительному пути. Этот путь —
перенесенная в детском возрасте затянувшаяся
крупозная, гриппозная или коклюшная пневмо­
ния с последующими периодическими обостре­
ниями, диагностируемыми как бронхопневмо­
ния. С течением времени обострения наступают
все чаще, а периоды ремиссии становятся все
короче. Частые обострения приводят к склеро­
зированию легочной ткани и вовлечению в воспа­
лительный процесс всех ее элементов — аль­
веол, интерстиция, бронхов. Поражение брон­
хов на всю глубину (развитие панбронхита)
приводит к нарушению их дренажной функции,
застою воспалительного секрета. Постоянно
поддерживающийся воспалительный процесс
спососбствует лимфогенному распростране­
нию инфекции и образованию воспалительных
инфильтратов. Некротические изменения в цент­
ре их приводят к образованию множественных
гнойников.
Следовательно, чаще всего можно проследить
два пути развития хронического нагноительного
процесса в легочной ткани [Бакулев А. Н., Ко­
лесникова Р. С., 1961]. В первом случае, как это
было показано еще С. И. Спасокукоцким, оди­
ночный или множественный острый абсцесс
легкого вследствие длительного течения и воз­
никновения склероза легочной ткани переходит
в хроническое нагноение в виде одиночных или
множественных абсцессов, к которым затем,
при переходе воспаления на бронхиальное дере­
во, присоединяются бронхоэктазии. При возник­
новении хронического нагноения по второму
пути оно является результатом длительного
хронического воспаления легких с поражением
бронхиального дерева и заканчивается образо­
ванием гнойных полостей распада (абсцессов)
и бронхоэктазий.
В конечном итоге при развитии хронического
нагноения по любому пути морфологические
изменения легочиой ткани нивелируются, ста­
новится сходной и клиническая картина забо­
левания.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
И ДИАГНОСТИКА
Симптоматика и варианты клинического тече­
ния хронических абсцессов легких были под­
робно изучены в клинике | Вихриев Б. С., 1970].
Заболевание обычно протекает с чередованием
обострения и ремиссий. Наиболее постоянным
симптомом является кашель с отделением гной­
ной мокроты, количество которой может быть
различным: от незначительного до обильного,
достигающего 500—600 мл и более в сутки.
Количество мокроты увеличивается в период
обострений, в это же время она часто бывает
зловонной. Однако у 15 % больных (по мате­
риалам клиники) мокрота не отделяется совсем
или ее количество незначительно. При обиль­
ном выделении мокроты организм теряет боль­
шое количество белка и других продуктов обме­
на, что приводит к гипопротеинемии и истоще­
нию. В мокроте часто обнаруживается при­
174
месь крови (у 9 % наблюдавшихся в клинике
больных).
Больные с хроническим абсцессом жалу­
ются на слабость, плохой аппетит, бессонницу,
различной интенсивности боли в соответствую­
щей половине грудной клетки. Часто отмечают
одышку в покое, усиливающуюся при физиче­
ских нагрузках.
При осмотре нередко можно заметить блед­
ность кожных покровов, неприятный запах изо
рта при дыхании, пастозность лица. В далеко
зашедших случаях, когда развиваются пневмо­
склероз и ателектаз, отмечаются изменения
формы грудной клетки: западение ее с больной
стороны, втяжение межреберных промежутков
и некоторое сближение ребер, а также отста­
вание «больной» половины грудной клетки,
особенно хорошо заметное при сравнении под­
вижности ее со здоровой стороны.
Пальцы в виде барабанных палочек являются
одним из самых постоянных признаков хрони­
ческого гнойного процесса в легких и наблюдают­
ся в 85—95 % случаев. Следует, однако, иметь
в виду, что этот симптом встречается и при дру­
гих заболеваниях, сопровождающихся выра­
женной гипоксией тканей (митральный порок
сердца, бронхиальная астма и др.). Вместе
с утолшением ногтевых фаланг обращает на
себя внимание и деформация ногтевых пласти­
нок по типу «часовых стекол». Через 6—12 мес
после радикальных вмешательств изменения
пальцев подвергаются обратному развитию,
и нормальный их вид может свидетельствовать
о хороших отдаленных результатах резек­
ции.
Хроническая гнойная интоксикация, наблю­
дающаяся при длительно протекающих абсцес­
сах легких, нередко приводит к поражению длин­
ных трубчатых костей с развитием склероза
костной ткани и поражению суставов. Патоге­
нез этих нарушений еще неясен.
Симптоматика, выявляемая при физикаль­
ном обследовании грудной клетки, весьма раз­
нообразна, определяется локализацией пора­
жения, фазой течения заболевания, тяжестью
анатомических изменений в легочной ткани, на­
личием или отсутствием сопутствующих изме­
нений в плевральной полости. Перкуторно вы­
являются зоны укорочения, однако при глубо­
ком расположении гнойника укорочения пер­
куторного звука может не быть. Перкуторные
изменения более выражены при осложнении
нагноения в легком эмпиемой плевры. В фазе
обострения и формирования гнойника при
аускультации слышны влажные хрипы, брон­
хиальное дыхание. Сопутствующий плеврит
иногда проявляется шумом трения плевры. Пос­
ле прорыва абсцесса в бронх определяются
полостные симптомы. При поверхностном рас­
положении гнойника нередко выслушивается
амфорическое дыхание.
Хроническая гнойная интоксикация является
характерным симптомом этого заболевания и
проявляется неспецифическими, свойствен­
ными и другим нагноениям легких признаками.
Быстро изменяется морфологический состав
крови, характеризующийся высоким лейкоци­
тозом и нейтрофилезом, сдвигом лейкоцитар­
ной формулы влево, анемией. В периоды ремис­
сии эти изменения выражены неотчетливо.
При хронических абсцессах легких всегда
наблюдаются гипопротеинемия и диспротеинемия. Анализ наблюдений, проведенный в кли­
нике, позволил выявить статистически досто­
верную значимость между содержанием белков
плазмы и степенью выраженности нагноительного процесса в легочной ткани.
Исследования свертывающей и фибринолити­
ческой систем крови обнаруживают склонность
к тромбозам (Плешаков В. Т., 19641; измене­
ния электролитов крови характеризуются гипо­
калиемией (В. П. Гончаров). Клинически дефи­
цит калия проявляется слабостью, адинамией,
гипотонией, нарушениями сердечного ритма.
Дефицит натрия менее характерен для больных
с хроническими нагноениями легких и выявля­
ется лишь при тяжелых и длительно протекаю­
щих формах заболевания. Клиническая кар­
тина дефицита натрия зависит от величины и
длительности его потерь: головные боли, тахи­
кардия, гипотония.
Часто встречающиеся при хронических абс­
цессах нарушения функции почек характери­
зуются альбуминурией (у 3,1 % наблюдавших­
ся больных), а также цилиндрурией, измене­
ниями при пробе Зимницкого. Тяжелые, дли­
тельно протекающие формы хронических абс­
цессов легких, сопровождающиеся амилоидо­
зом внутренних органов, вызывают более глу­
бокие изменения функции почек, выражающие­
ся в нарушении минутного диуреза, клубоч­
ковой фильтрации и др.
Выявляемые спирографически низкие пока­
затели жизненной емкости легких, снижение
компенсаторных возможностей легких в соче­
тании с гипервентиляцией свидетельствуют
об уменьшении резервов дыхания у многих
больных с хроническими абсцессами легких
(52 %). Степень изменения показателей внеш­
него дыхания находится в прямой пропорцио­
нальной зависимости от тяжести состояния,
продолжительности заболевания и распростра­
ненности нагноительного процесса в легком.
Изменения органов кровообращения у боль­
ных с хроническими абсцессами легких явля­
ются следствием нарушений гемодинамики
малого круга кровообращения — гипертензии
в артериях пораженных отделов легкого и ле-
175
точной артерии в целом, развития коллатера­
лей между артериями большого и малого круга,
создания сосудистого шунта, обусловливаю­
щего нарушение отношения вентиляция / кро­
воток, что усугубляет дыхательную недоста­
точность и сопровождается развитием «легоч­
ного сердца». Дистрофические изменения сер­
дечной мышцы, отмеченные у 18 % больных,
являются следствием прямого токсического
действия из очагов гнойного распада в легких.
Характерной для больных с хронической гной­
ной интоксикацией является гипотония.
Проведенные в клинике наблюдения [Вихриев Б. С., 1970] позволили выделить 4 основных
типа течения хронических абсцессов легких.
Иногда (7,2 % больных) острый абсцесс лег­
кого переходит в хронический незаметно, без
отчетливого клинического улучшения состояния
больного после проводимого лечения. При этом
продолжают сохраняться высокая температура
тела и отделение гнойной мокроты. Стойко
сохраняются полость деструкции и перифокаль­
ная -воспалительная инфильтрация легочной
ткани. Причина такого течения заболевания,
как показал проведенный анализ, чаще всего
кроется в условиях затрудненного опорожне­
ния гноя ествественным путем через дренирую­
щие бронхи. Нередко причиной этому служат
мелкие секвестры. Признаки хронического
нагноительного процесса появляются у таких
больных уже в конце 2-го — начале 3-го меся­
ца. Течение заболевания при этом характеризу­
ется развитием осложнений (пиопневмоторакс
и эмпиема плевры, кровохарканье и кровоте­
чение, септические осложнения).
У большинства наблюдавшихся в клинике
больных с хроническими абсцессами (54,7 %)
развитие хронического нагноительного про­
цесса было более постепенным. Исходом ост­
рого абсцесса у этих больных было клиниче­
ское выздоровление (формирование сухой оста­
точной полости) или значительное улучшение.
Большинство больных были выписаны на ам­
булаторное лечение или в домашние условия
и считались выздоровевшими, но ретроспек­
тивный анализ клинико-рентгенологических
данных этого периода все же позволил выявить
симптомы, которым не было придано должного
внимания. К числу таких симптомов относятся
жалобы на общую слабость, иногда возникаю­
щая субфебрильная температура тела, а так­
же сохраняющаяся на рентгенограммах и, осо­
бенно, томограммах перифокальная воспали­
тельная инфильтрация легочной ткани вокруг
«сухой» полости. Достигнутая у таких больных
ремиссия оказывается непродолжительной, и
спустя 1 —3 мес наступает выраженное обостре­
ние заболевания, проявляющееся прежде всего
внезапным повышением температуры, появле­
нием неприятного запаха выдыхаемого возду­
ха и зловонной гнойной мокроты. После лече­
ния в стационаре нагноительный процесс сти­
хает, но полностью не ликвидируется. Через
несколько месяцев обострение вновь рецидиви­
рует и затем повторяется 2—4 раза в году и
даже чаще.
В случаях таких абсцессов при рентгеноло­
гическом исследовании часто определяется зона
пневмосклероза легочной ткани, на фоне кото­
рой хорошо видны одна или несколько полостей
деструкции, заполненных гноем (рис. 94, 95).
В отличие от острых абсцессов при хронических
полость деструкции часто имеет неровные внут­
ренние контуры и неправильную форму в це­
лом, что делает необходимым дифференциаль­
ный диагноз с полостными формами перифе­
рического рака легкого. Клиническая симпто­
матика заболевания у больных в этот период
определяется нарушениями бронхиальной про­
ходимости, так как заполнить полости деструк­
ции контрастным веществом во время бронхо­
графии, как правило, не удается.
В отличие от только что описанной группы
больных, течение заболевания у которых харак­
теризуется частыми обострениями нагноитель­
ного процесса, примерно у */s наблюдавшихся
в клинике больных (21,1 %) заболевание про­
текало с редкими после ликвидации острого
нагноения обострениями, частота которых не
превышала 1 —2 раз в год. Клиническая симпто­
матика заболевания в период обострения была
выражена незначительно, признаки хрониче­
ской гнойной интоксикации отсутствовали, а
если и развивались, то поздно и в более отдален­
ные сроки. Такие больные длительное время,
годами, болеки и к хирургам обычно попадают
поздно. Следует, однако, иметь в виду, что дли­
тельные «светлые» промежутки между обостре­
ниями не исключают возможность развития
тяжелых форм заболевания с глубокими изме­
нениями гомеостаза. При рентгенологическом
исследовании в этих случаях обнаруживают
полости деструкции, иногда сухие, иногда с
небольшим количеством жидкости на дне. Как
правило, определяется склероз легочной ткани,
окружающей гнойник. Вне обострения полости
могут быть выделены иногда только с помощью
томографии, суперэкспонированных снимков,
иногда при бронхографии. В отдельных слу­
чаях для более точной диагностики полезны
селективная бронхография и использование
управляемых катетеров.
Наконец, нередко (у 17 % больных) после
стихания явлений нагноения в период формиро­
вания острого абсцесса заболевание в дальней­
шем длительное время протекает спокойно,
а иногда вообще бессимптомно, и больные жа­
луются лишь на ноющие боли в грудной клетке,
176
Рис. 94. Хронический абсцесс нижней доли правого легкого,
а — прямая рентгенограмма; б — боковая рентгенограмма. Видна
полость с толстыми стенками на фоне пневмосклероза и ин­
фильтрации.
Рис. 95. Хронический абсцесс левого легкого. Прямая рент­
генограмма.
Видны множественные полости с толстыми стенками и перифо­
кальная инфильтрация.
потливость, склонность «к простудным» забо­
леваниям. Мокроты нет или ее очень немного,
слизистого или слизисто-гнойного характера.
Признаки хронической гнойной интоксикации
у этих больных или отсутствуют вовсе, или вы­
ражены очень незначительно, и нередко един­
ственным симптомом заболевания является
кровохарканье, реже — легочное кровотечение,
которые вынуждают обратиться к хирургу.
Рентгенологические проявления заболева­
ния у таких больных не типичны. Чаще всего
определяются локальный пневмосклероз и сухие
тонкостенные полости, лучше видимые на томо­
граммах. Деформация бронхов в зоне пораже­
ния и склеротические изменения легочной ткани
лучше выявляются бронхографически.
12 Зак. 0517
Осложнения хронических абсцессов чаще
наблюдаются в период обострений заболева­
ния и при длительном его течении в виде вто­
ричных бронхоэктазий, легочных кровотече­
ний, септикопиемии, амилоидоза паренхима­
тозных органов.
Вторичные бронхоэктазии встречаются, по
данным различных авторов, у 10—25 °о боль­
ных хроническими абсцессами легких. Изуче­
ние частоты возникновения вторичных брон­
хоэктазий при хронических абсцессах, прове­
денное в клинике госпитальной хирургии, под­
твердило точку зрения большинства авторов
о том, что бронхоэктазии являются наиболее
частым осложнением хронических абсцессов
легких — они были обнаружены у 8(> (31,7 °-о)
177
из 271 наблюдавшегося больного, которым были
выполнены тщательные бронхографические
исследования.
Анализ этих наблюдений показал, что частота
бронхоэктазий закономерно возрастает с уве­
личением продолжительности заболевания: при
сроках болезни до б мес они выявлены у 20,8 %,
а свыше 2 лет — у 43,9 % больных.
Вторичные бронхоэктазии чаще всего разви­
вались в базальных сегментах легких, реже —
в средней доле и язычковых сегментах левого
легкого. Часто наблюдалось сочетанное пора­
жение бронхоэктазиями IV—V и базальных
сегментов. Преимущественное поражение
бронхоэктазиями нижних отделов легких по­
зволяет предположить, что у большинства боль­
ных они возникают вследствие аспирации мок­
роты и гноя. При вторичных бронхоэктазиях
наблюдались цилиндрические бронхоэктазии.
Мешотчатые бронхоэктазии отмечены лишь у
3,3 % больных.
Кровохарканье и кровотечение в большинстве
случаев сопровождают обострения хронических
абсцессов легких и наблюдаются, как показали
оперативные вмешательства, предпринятые
по поводу легочных кровотечений, у больных
с обширными изменениями легочной ткани и
мощными плевральными сращениями [Григорь­
ев М. С., 1960]. По данным В. И. Стручкова
(1967), среди больных с хроническими нагно­
ениями легких кровохарканье и кровотечение
отмечены у 70 %, из них сильные кровотече­
ния — у 14 %. Наши наблюдения подтверждают
такую частоту этого симптома. Нельзя исклю­
чить связь между возникновением легочных
кровотечений и повышением давления в системе
легочной артерии вследствие образования кол­
латералей между большим н малым кругом кро­
вообращения, в том числе и через плевраль­
ные сращения, всегда образующиеся при дли­
тельном течении хронического нагноительного
процесса в легочной ткани.
Поставить диагноз легочного кровотечения
при хроническом абсцессе легких нетрудно.
Сложнее выявить'источник кровотечения, что
необходимо для ^определения объема резекции.
Очень трудно это сделать на фоне продолжаю­
щегося кровотечения, особенно массивного,
так как данные рентгенологического исследо­
вания при этом обычно недостаточны для топи­
ческого диагноза. Продолжающееся легочное
кровотечение опасно не только анемией, но и
аспирацией крови в легкие и асфиксией, поэтому
в таких случаях необходимы срочная бронхо­
скопия, освобождение трахеи и бронхов от
жидкой крови и сгустков с последующей вре­
менной окклюзией соответствующего бронха,
срочной резекцией пораженного участка лег­
кого.
Среди наблюдавшихся в госпитальной хирур­
гической клинике больных с хроническими абс­
цессами легких 15 пациентов были оперированы
по срочным показаниям из-за развившегося
легочного кровотечения. Все они благополучно
перенесли резекцию и выздоровели.
Хронические нагноительные процессы в лег­
ких могут стать причиной септикопиемии,
которая, по данным различных авторов, возни­
кает у 3—5 % больных и сопровождается высо­
кой летальностью. Чаще сепсис возникает в
периоды обострений, когда легочный гнойник
плохо дренируется. В таких случаях нередко
(у 1—3 % больных) появляются метастати­
ческие абсцессы в головном мозге. Среди боль­
ных, наблюдавшихся в нашей клинике, такие
абсцессы головного мозга были выявлены у
7 больных, и все они погибли. Диагностика
метастатических абсцессов головного мозга
также трудна, но это осложнение можно запо­
дозрить по появлению мучительных головных
болей на фоне ухудшающегося состояния боль­
ного и нарастания гнойной интоксикации. В бо­
лее поздние сроки появляются головокруже­
ние, рвота и спутанность сознания.
Амилоидоз, так же как и другие осложнения
хронических абсцессов, чаще возникает при
длительном течении заболевания и частых тя­
желых обострениях. Вначале возникает токси­
ческий нефрит, а затем может развиться ами­
лоидно-липоидный нефроз. Прогноз у таких
больных плохой — они погибают от почечной
недостаточности. При глубоких изменениях
в почках отмечаются увеличение печени, нару­
шение антитоксической ее функции, а также
увеличение селезенки. Появляются необрати­
мые изменения всех звеньев гомеостаза. Прог­
ноз для жизни в таких случаях становится не­
благоприятным при всех видах лечения.
Диагноз хронического абсцесса нетруден и
ставится на основании данных клинических,
лабораторных и рентгенологических исследо­
ваний, изложенных здесь и в предыдущей главе.
К дополнительным диагностическим методам,
к которым часто приходится прибегать при
подозрении на хронический абсцесс легких,
относятся бронхоскопия и бронхография. При
бронхоскопии всегда имеется возможность
визуального изучения и оценки состояния сли­
зистой оболочки трахеи и бронхов, а с помощью
направленной бронхоскопии можно детально
обследовать отдельные бронхолегочные сегмен­
ты, исключить или подтвердить наличие опухоли
легкого. Бронхоскопия у больных с хрониче­
скими абсцессами легких является и важной
лечебной процедурой, позволяющей проводить
эффективную санацию трахеобронхиального
дерева. Бронхоскопия часто проводится также
с целью последующего направленного контра­
178
стирования бронхиального дерева, а также для
аспирации контрастной массы после бронхо­
графии.
Весьма ценным диагностическим методом
у больных с хроническими нагноительными
процессами в легких является бронхография.
С помощью этого исследования определяется
топический диагноз поражения, а также состоя­
ние бронхиального дерева на больной и здо­
ровой стороне. Прежде чем произвести бронхо­
графию больным, откашливающим большое
количество мокроты, необходима настойчивая
и тщательная санация трахеи и бронхов. Иссле­
дование пораженного легкого обычно произ­
водят через 7—10 дней после исследования
противоположного легкого, оцениваемого как
здоровое. Бронхография противопоказана боль­
ным с хроническими абсцессами легких,
осложненными легочными кровотечениями,
декомпенсацией сердечной деятельности, рас­
пространенным двусторонним поражением,
острым перифокальным воспалением.
Дифференциальную диагностику хронических
абсцессов легких необходимо проводить преж­
де всего с другими хроническими нагноительны­
ми заболеваниями легких, симптоматика кото­
рых. особенно в далеко зашедших стадиях забо­
левания, весьма схожа. Большое значение здесь
имеют анамнез, жалобы, а также данные кли­
нических и рентгенологических исследований.
Особенно часто ошибки в дифференциальной
диагностике допускаются, когда речь идет о
хронических абсцессах легких и бронхоэкта­
зиях. Последние нередко развиваются вторич­
но, являясь частым осложнением длительно
и неблагоприятно текущих хронических абс­
цессов. В далеко зашедших стадиях заболева­
ния четкое разграничение хронических абсцес­
сов легких и бронхоэктазий — наиболее часто
встречающихся форм хронических нагноений
легких — подчас весьма затруднительно еще
и потому, что отсутствует единая общепризнан­
ная классификация нагноений легких.
Так, среди больных, находившихся в госпи­
тальной хирургической клинике по поводу хро­
нических абсцессов, 2,7 % поступили с диагно­
зом «бронхоэктазии». Наряду с этим 8,2 % боль­
ных бронхоэктазиями были направлены для
госпитализации с диагнозом «абсцесс легкого».
Бронхоэктазии в отличие от хронических
абсцессов чаще встречаются в молодом возрасте,
причем одинаково часто у мужчин и женщин.
Хронические абсцессы чаще поражают мужчин
зрелого возраста. Тщательно собранный анамнез
позволяет выяснить обстоятельства, характер­
ные для развития бронхоэктазий: частые воспа­
ления легких в детском возрасте и бронхит,
сохраняющийся в промежутках между обо­
стрениями. Периоды обострений у больных
12
с хроническим абсцессом редко сопровожда­
ются отхождением очень большого количества
мокроты, что весьма типично для больных брон­
хоэктазиями. при обострении которых мокрота
отходит «полным ртом», особенно по утрам после
сна. В мокроте больных бронхоэктазиями эла­
стические волокна обнаруживаются очень ред­
ко, тогда как при хронических абсцессах их
находят почти всегда. Длительность заболева­
ния у больных с хроническим абсцессом чаще
невелика, зато тяжесть состояния и интоксика­
ция в период очередного обострения выражены
намного больше. Больные бронхоэктазиями,
даже захватывающими обширные зоны лег­
кого или все легкое, нередко чувствуют себя
вполне удовлетворительно. Абсцессы легких
чаще всего локализуются в задних сегментах
верхних и нижних долей, особенно справа. Не­
редко при поражении верхней доли в воспали­
тельный процесс вовлекается соседний участок
нижней и наоборот. При бронхоэктазиях чаще
поражаются нижние доли легких, а также сред­
няя доля н язычковые сегменты. Поражение
почти всегда ограничивается анатомически
обусловленной частью легкого — сегментом,
долей и редко проникает в соседние доли лег­
кого. Разрешить сомнения помогает рентгеноло­
гическое исследование, так как даже очень дли­
тельное существование хронического абсцесса не
приводит к распространенным поражениям
бронхов и на бронхограммах определяются
большие, неправильной формы полости. При
бронхоэктазиях хорошо видны цилиндрические,
мешотчатые и смешанные расширения бронхов.
Расширенные бронхи, дающие рентгенологиче­
ски картину полостей, чаще имеют ровные кон­
туры. Очень трудно отдифференцировать хро­
нический абсцесс легкого от абсцедирую­
щих бронхоэктазий, но и в этих случаях тща­
тельно собранный анамнез, особенности тече­
ния заболевания и рентгенологические данные
помогают поставить правильный диагноз.
Другим хроническим неспецифическим за­
болеванием легких, с которым иногда необхо­
димо дифференцировать хронические абсцессы,
является хроническая неспецифическая пнев­
мония, протекающая с частыми обострениями
и абсцедированием. Здесь также важен анамнез.
При рентгенологическом исследовании обычно
отмечается сплошное затенение доли или всего
легкого с множественными мелкими полостями
деструкции.
Весьма трудной может быть дифференциаль­
ная диагностика хронических абсцессов и ту­
беркулеза легких, особенно при сочетанных
поражениях легких, неспецифических и спе­
цифических процессах. По сводным данным
В. Н. Молоткова и соавт. (1982), сочетание
туберкулеза легких с хроническими нагноитель-
179
ними заболеваниями колеблется от 4,6 до
21,9 %. Отмечается рост числа таких сочетан­
ных поражений. Если в 1965 г. они диагности­
рованы у 10,1 % больных, то в 1981 г.— у
17,6 % [Зыскин Л. Ю. и др., 1982]. Среди боль­
ных, подвергшихся в нашей клинике резекциям
легких по поводу типичных хронических абс­
цессов, у 33 % гистологическими исследования­
ми препаратов, наряду с неспецифическим про­
цессом, были выявлены изменения, характерные
для туберкулеза [Вихриев Б. С., 1970].
Все вышеизложенное определяет необходи­
мость тщательного комплексного обследова­
ния больных с хроническими абсцессами лег­
ких до операции с целью определения характе­
ра, динамики и распространенности нагноения
легких и выявления степени нарушения функ­
ций основных систем жизнеобеспечения орга­
низма.
ЛЕЧЕНИЕ
Консервативное лечение применяется в на­
стоящее время у большинства больных с хрони­
ческими абсцессами легких, однако оно рас­
сматривается как основнаи часть предопера­
ционной подготовки. Реже, в запущенных слу­
чаях заболевания, когда резекции противопо­
казаны, консервативная терапия может быть
единственно возможным методом лечения.
При наличии показаний центральным вопро­
сом хирургического лечения больных с хрони­
ческими абсцессами легких является выбор опти­
мального времени для проведения оператив­
ного вмешательства. Принимая решение под­
вергнуть больного резекции легкого, чаще всего
исходят из плохого прогноза заболевания при
других методах лечения. В связи с этим боль­
шой практический интерес представляет изуче­
ние отдаленных исходов у больных с хрониче­
скими абсцессами легких, которые по тем или
иным причинам были выписаны без операции.
Анализ таких исходов у 123 больных с хрони­
ческими абсцессами легких, проведенный Б. С.
Вихриевым, показал, что они были наиболее
неблагоприятными у больных, у которых забо­
левание протекало без выраженных ремиссий.
Плохие отдаленные результаты отмечены и у
больных, у которых заболевание протекало с
частыми тяжелыми обострениями (из 22 боль­
ных с таким течением заболевания в сроки
наблюдения до 2 лет практически здоровым
остался лишь один больной; 8 человек продол­
жали болеть, 3 — вынуждены были подверг­
нуться операциям, а 10 — погибли вследствие
прогрессирования заболевания). Лучше отда­
ленные исходы были у неоперировавшихся боль­
ных, течение заболевания у которых характе­
ризовалось редкими легкими обострениями.
Из 47 больных этой группы от прогрессирова­
ния заболевания умерли только 5, а 21 остава­
лись практически здоровыми. Большинство
больных (40 из 50), у которых заболевание
протекало без выраженных обострений, а изме­
нения в легких (сухая остаточная полость с не­
значительно выраженными явлениями пневмо­
склероза) выявлялись только при рентгеноло­
гическом исследовании, в течение длительного
времени, от 2 до 16 лет после выписки, остава­
лись в хорошем состоянии. Рецидив нагноительного процесса развился лишь у 3 больных этой
группы.
Данные литературы и опыт клиники позволя­
ют считать, что при определении показаний к
резекции легкого у больного с хроническим
абсцессом следует исходить из тяжести состоя­
ния, распространенности нагноительного про­
цесса, длительности заболевания, наличия или
отсутствия осложнений, а также динамики
течения нагноительного процесса в легочной
ткани под влиянием проводимой консерватив­
ной терапии.
Необходимость резекции не вызывает сомне­
ний при хронических одиночных и множествен­
ных абсцессах, протекающих с частыми тяже­
лыми обострениями и прогрессирующей хрони­
ческой гнойной интоксикацией, однако эти
больные нуждаются в интенсивной предопера­
ционной подготовке, с помощью которой необ­
ходимо стремиться устранить обострение на­
гноительного процесса и выполнить оператив­
ные вмешательства с минимальным риском гене­
рализации инфекции.
Тем не менее иногда, несмотря на проводимую
терапию, состояние больных не только не улуч­
шается, а, наоборот, прогрессирует. Такое те­
чение заболевания нередко бывает при ослож­
нениях хронического абсцесса вторичными
бронхоэктазиями и эмпиемой плевры. Плохой
прогноз при отказе от операции в этих случаях
очевиден, а резекция в то же время крайне
рискованна. Определить правильную лечебную
тактику в подобных ситуациях очень непросто.
Резекции легких у таких больных допустимы
только в специализированных хирургических
стационарах при условии их выполнения хирур­
гами, имеющими большой личный опыт в легоч­
ной хирургии и хорошо поставленной анесте­
зиологической и реаниматологической службе.
По данным Ю. Н. Лубенского и соавт. (1980),
из 134 больных, перенесших резекции легкого
по поводу хронического абсцесса, предопера­
ционная подготовка позволила добиться улуч­
шения состояния лишь у 63 (47 %) больных,
а у остальных 71 (53 %) она оказалась неэф­
фективной. По мнению авторов, отчетливый
благоприятный эффект давала инфузия анти­
биотиков в легочную артерию.
180
Спорным остается вопрос о тактике хирурга
при абсцессах в обоих легких. По мнению
В. И. Стручкова (1967), резекции легких при
двусторонних абсцессах противопоказаны, ког­
да с одной стороны поражено все легкое или
большая его часть, а с другой — одна доля или
более. Если поражено по одной доле с каждой
стороны — возможно поочередное их удаление.
В. И. Кукош и соавт. (1981) выполнили 35 од­
номоментных и 20 двухэтапных резекций легких
больным хроническими нагноениями легких.
После предельно допустимой резекции легоч­
ной ткаии в оставшихся долях легких проис­
ходит морфологическая перестройка. Предпо­
чтительнее, по мнению авторов, двухэтапная
резекция с оптимальным интервалом между
вмешательствами 4—7 мес. При первой опера­
ции авторы рекомендуют выполнять больший
объем резекции, что способствует более актив­
ному включению компенсаторно-приспособи­
тельных механизмов, повышающих устойчи­
вость организма к резекции второго легкого.
Установлена эффективность гипербарической
оксигенации при обширных резекциях легких.
Опыт клиники госпитальной хирургии убеж­
дает, что большинство таких больных с двусто­
ронними абсцессами часто неоперабельны.
В лучшем случае у них можно ограничиться
пневмотомией острого абсцесса, развившегося
в контралатеральном легком как осложнение
ранее существовавшего хронического. В дальней­
шем, если наступит заживление острого абс­
цесса, можно вернуться к обсуждению вопроса
о допустимости резекции по поводу хрониче­
ского абсцесса.
Резекции легких при хронических абсцессах
не показаны при неосложненном течении забо­
левания с редкими легкими обострениями, осо­
бенно если есть условия для систематического
наблюдения и оказания квалифицированного
лечения в случае необходимости. Бесперспек­
тивны резекции у больных хроническими абс­
цессами с резкими нарушениями сердечной дея­
тельности и явлениями декомпенсации, с тяже­
лым амилоидозом внутренних органов.
Осложнение хронического абсцесса легкого
кровотечением большинство хирургов считают
показанием к резекции [Колесов В. И., 1960;
Григорян А. В. и др., 1966; Кузин М. И., Волын­
ский Ю. Д., 1978; Стручков Б. И. и др., 1982,
и др.]. Продолжающееся кровотечение всегда
вынуждает к срочной резекции после диагно­
стической бронхоскопии на операционном столе
и тампонады бронха. В случаях, когда
кровотечение остановилось, решиться на резек­
цию труднее. Всегда сохраняется реальная
угроза повторного массивного кровотечения,
при котором даже срочная резекция может
оказаться запоздалой. В то же время резекция
будет более безопасной для больного, если она
будет выполнена после остановки кровотече­
ния и ликвидации его последствий. Поскольку
кровотечения обычно связаны с прогрессиро­
ванием нагноительного процесса в легких и по­
этому склонны к рецидивированию, предопе­
рационная подготовка после остановившегося
кровотечения не должна превышать 8—12 ч.
Имевшие место в анамнезе больного с хрони­
ческим абсцессом легкого легочные кровотече­
ния являются дополнительным аргументом в
пользу резекции. Целью операции является
удаление пораженных отделов легкого вместе с
источником кровотечения. В последние годы
для остановки легочных кровотечений в клини­
ческую практику внедряется метод эмболиза­
ции бронхиальных артерий [Перельман М. И.,
1977; Кузин М. И., Волынский Ю. Д., 1978].
Широкого распространения он, однако, не по­
лучил.
При абсцессах, осложненных хронической
эмпиемой плевры и бронхиальным свищом,
вопрос о необходимости резекции должен ре­
шаться в зависимости от характера поражения
легкого. При продолжающемся хроническом
нагноительном процессе в легочной ткани лю­
бые оперативные вмешательства с целью устра­
нения только плеврального очага нагноения
будут обречены на неуспех. После стабилиза­
ции состояния больного в таких случаях пока­
заны резекции пораженных отделов легкого,
несущих свищ, с одновременной плеврэктомией.
Больные с хроническими абсцессами легких,
за исключением бурно прогрессирующих форм
и осложненных кровотечением, как правило,
нуждаются в интенсивном консервативном ле­
чении, преследующем цели подготовки к ра­
дикальному оперативному вмешательству.
Основными задачами предоперационной под­
готовки больных с хроническими абсцессами
легких являются следующие.
1. Уменьшение гнойной интоксикации и лик­
видация обострения нагноительного процесса
в легких.
2. Коррекция нарушенных патологическим
процессом функций систем дыхания и крово­
обращения, ликвидация белковых, волемиче­
ских, электролитных нарушений и анемии.
3. Повышение общей иммунологической
сопротивляемости организма.
Решение первой задачи обеспечивается про­
ведением комплекса лечебных мероприятий,
воздействующих на патогенетические механиз­
мы заболевания. Имея в виду ведущую роль
в патогенезе и течении нагноительных заболе­
ваний легких нарушений бронхиальной прохо­
димости, большое внимание необходимо уде­
лить комплексной санации трахеобронхиаль­
ного дерева с целью создания условий для мак­
181
симально полного и по возможности постоян­
ного оттока гноя из полости деструкции. Спо­
собы бронхологической санации подробно из­
ложены в предыдущей главе. Следует остано­
виться лишь на некоторых особенностях сана­
ции у больных с хроническими абсцессами лег­
ких. Длительное течение нагноительного про­
цесса в легочной ткани, сопутствующий обостре­
нию нагноения разлитой трахеобронхит опре­
деляют необходимость проведения более дли­
тельных курсов санационной терапии. При хро­
нических абсцессах ле1 ких в устье бронха пора­
женного сегмента нередко развивается массив­
ный рубцовый процесс, который значительно
затрудняет эвакуацию гнойного содержимого
с помощью массивных методов санации. Поэто­
му, не отказываясь от постурального дренажа,
ингаляций и интратрахеальных вливаний лекар­
ственных препаратов, более эффективной сле­
дует считать бронхоскопическую санацию катетеризационным бронхоскопом, позволяющим
проводить зондирование гнойных полостей,
аспирацию гнойного содержимого, промыва­
ние и введение лекарственных препаратов. По
механизму своего действия они делятся на
несколько групп: механически очищающие (изо­
тонический раствор хлорида натрия, слабые
растворы новокаина), антисептические веще­
ства (фурацилин, риванол, фурагин, солафур
и др.), химиотерапевтические вещества (суль­
фаниламидные препараты и антибиотики),
вещества, уменьшающие поверхностное натя­
жение слизи (адегол, тахоликвин), противовос­
палительные вещества (протеолитические фер­
менты, антипирин). Использование веществ,
уменьшающих поверхностное натяжение слизи
(«моющих»), является, по мнению Г. И. Лукомского (1973), весьма перспективным.
Проведенными исследованиями этого автора
установлено, что в бронхах при хроническом
нагноении легких имеются оптимальные усло­
вия для действия протеолитических фермен­
тов и, в частности, химопсина. Необходимость
длительной экспозиции этою препарата (3—
4 мин) заставляет у больных, находящихся в
тяжелом состоянии, предпочесть ему ацетил­
цистеин, выраженное действие которого насту­
пает уже через 1 мин. Протеолитические фер­
менты способствуют растворению детрита, гу­
стого гноя, слизистых пробок, уменьшению
Отека слизистой оболочки бронхиального дерева,
потенцируют лечебное действие антибактери­
альных препаратов, обеспечивающих лучший
контакт с воспаленными тканями. По мнению
большинства специалистов, бронхоскопическая
санация должна заканчиваться введением анти­
биотиков. Следует иметь в виду, что многие
больные с хроническими абсцессами, как пра­
вило, получают большие дозы различных анти­
бактериальных средств на всех этапах лечения
и поэтому микробная флора подавляющего
большинства из них нечувствительна к наиболее
часто применяющимся антибиотикам. Это выну­
дило некоторых авторов (Стручков В. И. и др.,
1978] полностью исключить антибиотики из
арсенала лечебных средств больных с абсцес­
сами легких и шире использовать более актив­
ные антисептики, особенно иитрофуранового
ряда. Антибиотики, особенно широкого спектра
действия, остаются у таких больных резервными
препаратами послеоперационного периода.
По-видимому, полностью отказываться от при­
менения антибактериальных препаратов у боль­
ных с хроническими абсцессами легких не сле­
дует. Трудности идентификации изменившегося
за последние годы спектра микробной флоры
и целенаправленного подбора антибиотиков
в соответствии с данными антибиотикограммы
необходимо преодолевать совершенствованием
бактериологических методик и способов забора
материала для исследования. Оптимальным из
них является получение содержимого поражен­
ных участков легкого стерильным аспиратором
во время катетеризационной бронхоскопии.
Наиболее эффективными комбинациями анти­
бактериальных препаратов у больных с хрони­
ческими абсцессами легких являются, как пока­
зал опыт нашей клиники, сочетания аминогли­
козидов (канамицин, гентамицин) с полусинтетическими пенициллинами
(оксациллин,
метициллин, карбенициллин и др.). Эффективны
также антибиотики цефалоспориновой группы.
При тяжелой интоксикации в последние годы
в период подготовки к операции стали приме­
нять эндолимфатическое введение антибиотиков,
а также гемосорбцию | Маневич В. Л. и др..
1982], но оценить преимущества и недостатки
этих методов на основании имеющихся сообще­
ний не представляется возможным.
Для снятия гнойной интоксикации и ликви­
дации обострения у больных с хроническими
абсцессами легких могут использоваться и спо­
собы оперативного дренирования легочных гной­
ников, особенно если они одиночны и поверх­
ностно расположены. Дренирование полости
хронического абсцесса с этой целью было пред­
принято нами у 13 больных. Во всех случаях
был достигнут выраженный положительный
клинический эффект. Шести больным в после­
дующем была выполнена резекция доли, троим—
мышечная пластика полости. Четверо больных
выписаны без операции, и при сроках наблю­
дения от 1 года до 12 лет выраженных обостре­
ний заболевания у них не было. Длительность
санации полости хронического абсцесса через
дренажную трубку в среднем составила 3 нед.
Пневмотомия у больных с хроническими абс­
цессами легких не является операцией, позво­
182
ляющей добиться выздоровления. Об ослож­
нениях и недостатках этой операции подробно
говорилось выше. Однако в определенных слу­
чаях она может оказаться необходимой: при
поверхностно расположенных больших хрони­
ческих гнойниках, особенно содержащих сек­
вестры, пневмотомия может использоваться
для подготовки к резекции; у больных, резек­
ции которым из-за тяжести состояния и рас­
пространенности процесса противопоказаны,
а консервативной терапией купировать обостре­
ние нагноительного процесса не удается, эта
операция может быть паллиативной, умень­
шающей интоксикацию.
В госпитальной хирургической клинике пнев­
мотомия была использована для подготовки
к резекции у 39 больных с хроническими абс­
цессами легких. Анализ этих наблюдений пока­
зал, что добиться улучшения состояния боль­
ных, как правило, не удавалось в случаях мно­
жественных хронических абсцессов, а также
при наличии хронических гнойников, ослож­
ненных вторичными бронхоэктазиями. При
одиночных хронических абсцессах, в том числе
гангренозных и осложненных эмпиемой плев­
ры, пневмотомия способствовала быстрому
(в течение 1—2 нед.) уменьшению гнойной ин­
токсикации и создавала более благоприятные
условия для выполнения в последующем резек­
ции пораженной части легкого.
Опыт резекции легкого у 17 больных, кото­
рым в прошлом производилась пневмотомия,
показал, что в области торакального свища всег­
да формируются обширные плотные сращения,
затрудняющие вскрытие плевральной полости
и выделение легкого из сращения. Выделение
и обработка элементов корня легкого бывают
даже технически более простыми, чем у боль­
ных, оперируемых в фазе обострения заболе­
вания.
С целью предоперационной подготовки боль­
ных с хроническими абсцессами легких в комп­
лексе с методами бронхологической санации
осуществляются лечебные мероприятия для
нормализации функции сердечно-сосудистой
и дыхательной систем, коррекции волемических,
белковых, электролитных и иммунологических
нарушений. Для борьбы с гипоксией должна
широко применяться гипербарическая оксиге­
нация. С целью ликвидации анемии предпочте­
ние должно отдаваться переливанию свеже­
консервированной крови, а также прямым гемо­
трансфузиям. Содержание лечебных меро­
приятий, обеспечивающих решение постав­
ленных выше задач, подробно изложено в пре­
дыдущей главе.
Рациональным консервативным лечением
у большинства больных с хроническими абс­
цессами легких удается добиться существенного
улучшения их состояния и тем самым значи­
тельно уменьшить риск резекции. Однако иног­
да эффект подготовки бывает недостаточным
или вообще отсутствует, в связи с этим возни­
кает вопрос о допустимом сроке подготовки
к операции. Опыт клиники госпитальной хирур­
гии свидетельствует о том, что вполне доста­
точным сроком, по истечении которого можно
судить об эффективности проводимого лечения,
являются 2—3 нед. Если к окончанию этого
срока комплексная консервативная терапия
не дает существенного улучшения, продолжать
ее нецелесообразно. У таких больных для под­
готовки к резекции можно или прибегнуть к
одному из методов оперативного дренирования
хронического абсцесса, или избрать резекцию,
риск которой в этих условиях возрастает.
Ориентировочный объем резекции у больных
с хроническими абсцессами легких планируется
на основании данных рентгенографии и томо­
графии. При этом заболевании часто развивают­
ся вторичные изменения легочной ткани (броихоэктазии и пневмосклероз). Это определяет
необходимость в бронхографии.
Чаще всего поражение легочной ткани при
хроническом абсцессе ограничивается одной
долей (у 69,5 % из 498 больных, оперировав­
шихся в госпитальной хирургической клинике).
Поражение легкого с наличием множествен­
ных полостей отмечено лишь у 5,9 % больных.
В 15,2 % наблюдений хронический нагноительный процесс захватывал смежные сегменты раз­
ных долей (чаще всего II—VI сегменты правого
легкого и I—VI сегменты левого). Абсцессы,
ограниченные пределами одной доли при нали­
чии пневмосклероза и вторичных бронхоэкта­
зий в других долях, отмечены у 9,4 % больных.
Решение об окончательном объеме резекции
при хронических абсцессах легких принимается
только после выделения легкого из сращений
и его ревизии. Чаще всего прибегают к лобэкто­
мии (у 41,3 % больных, оперировавшихся в
нашей клинике). Несмотря на то, что пораже­
ние легкого при хроническом абсцессе у боль­
шинства больных ограничивается долей, к пнев­
монэктомиям приходится прибегать почти так
же часто, как и к резекциям доли (у 34,7 %
больных). Кроме случаев множественных абс­
цессов легких в разных долях, к пневмонэкто­
мии нередко вынуждают воспалительные изме­
нения в участках легкого, непосредственно не
пораженных деструктивным процессом, невоз­
можность выполнения планировавшейся доле­
вой резекции из-за выраженного спаечного про­
цесса в корне легкого и плевральной полости,
интраоперационные осложнения (кровотече­
ния, повреждения легочной паренхимы), свя­
занные с техническими трудностями, обуслов­
ленными теми же причинами.
183
При сочетанном поражении верхней доли и
верхушечного (VI) сегмента нижней доли чаще
прибегают к удалению всего легкого. Комбини­
рованная резекция пораженной доли и сегмен­
та в этих случаях технически сложнее и риско­
ваннее с точки зрения возможности развития
послеоперационных осложнений (несостоятель­
ности легочной раны, формирования остаточной
плевральной полости и эмпиемы плевры). Пнев­
монэктомию выполняют всегда при сочетанном
поражении нижних долей и II (справа) и I
(слева) сегментов верхних.
При часто встречающемся распространении
воспалительных изменений с верхней доли на
среднюю долю правого легкого избежать би­
лобэктомии можно, прибегнув к типичному уда­
лению верхней и атипичной резекции поражен­
ного участка средней доли. При хронических
абсцессах, локализующихся в верхушечном
(VI) сегменте нижней доли левого легкого, и
вторичных бронхоэктазиях в язычковых сегмен­
тах верхней доли хорошие результаты дает ком­
бинированная резекция нижней доли и язычко­
вых сегментов верхней доли. Различные вариан­
ты комбинированных резекций легких при хро­
нических абсцессах были выполнены у 7,7 %
оперировавшихся в госпитальной хирургиче­
ской клинике больных.
Билобэктомии у больных с хроническими
абсцессами легких выполняются нечасто (у
7,9 % больных). К этим операциям приходится
прибегать при невозможности разделить меж­
долевые щели, в случаях распространения вос­
палительного инфильтрата на корень легкого
или резко выраженных рубцовых изменений
в нем. Иногда к правосторонней нижней би­
лобэктомии приходится прибегать у больных
с хроническим абсцессом средней доли, когда
из-за воспалительных или рубцовых изменений
невозможно выделить артерию и бронх средней
доли, а также в случаях повреждения междоле­
вого ствола легочной артерии.
Резекции сегментов при хронических абсцес­
сах легких производить нецелесообразно, хотя
нагноительный процесс при этом нередко имеет
сегментарное распространение. Во время опера­
тивных вмешательств почти всегда обнаружи­
ваются воспалительные и рубцовые изменения
в корне легкого, исключающие возможность
сегментэктомии. Среди больных с хрониче­
скими абсцессами легких, оперировавшихся
в госпитальной хирургической клинике, сегмен­
тарные резекции были сделаны лишь 6,5 % па­
циентов. Еще реже прибегают к атипичным ре­
зекциям (у 1,9 % больных по данным клиники).
Резекции легких у больных с хроническими
абсцессами в большинстве случаев не имеют
существенной специфики, однако не лишены
некоторых своих особенностей. В техническом
отношении эти операции сложнее, чем у боль­
ных с острыми нагноениями легких, и труд­
ности определяются главным образом выра­
женными сращениями в плевральной полости
и в корне легкого. При длительном существо­
вании патологического процесса значительные
трудности может представить вскрытие плев­
ральной полости при торакотомии из-за сбли­
жения ребер и мощных шварт. Характерной
особенностью, определяющей трудности и трав­
матичность резекций у больных с хроническими
абсцессами легких, является наличие плевраль­
ных сращений, которые при длительном тече­
нии нагноительного процесса и особенно в слу­
чаях осложнения его эмпиемой бывают очень
мощными. Среди оперировавшихся в клинике
больных полная облитерация плевральной поло­
сти плотными сращениями отмечена в 38 %
случаев. Чаще всего сращения были наиболее
выражены в задних отделах плевральной поло­
сти.
Весьма перспективным может быть исполь­
зование лазерного ножа при резекциях лег­
ких по поводу их хронических нагноительных
заболеваний. Лазерный скальпель обеспечивает
бескровное и значительно более легкое разде­
ление плотных и рубцовых тканей, оказывает
бактерицидное воздействие на возбудителей
хирургической инфекции (Кабанов А. Н. и др.,
1982].
Из-за выраженных рубцовых изменений в
корне легкого и невозможности в связи с этим
типичной раздельной обработки элементов кор­
ня легкого у больных с хроническими абсцесса­
ми чаще приходится прибегать к виутриперикардиальной перевязке сосудов (у 5 % больных,
перенесших пневмонэктомию). Технические
трудности, обусловленные сращениями в корне
легкого, определяют значительную частоту по­
вреждений крупных сосудов, особенно при ча­
стичных резекциях (отрыв сегментарных арте­
рий от места их отхождения, ранение междоле­
вого ствола легочной артерии). В таких слу­
чаях для остановки кровотечения приходится
прибегать к вынужденной перевязке осиовиого
ствола легочной артерии и расширять объем
резекции до пневмонэктомии. При поврежде­
нии легочной артерии оправдано наложение
сосудистого шва. Для разделения междолевых
щелей и легочных перемычек целесообразно
чаще прибегать к аппаратному способу.
Опыт лечения больных с хроническими абсцес­
сами легких, перенесших резекции, показал, что
в послеоперационном периоде большинство из
них нуждаются в интенсивной терапии и интен­
сивном наблюдении. Основной задачей лечения
в ближайшем послеоперационном периоде
(24—48 ч) является восстановление и поддержа­
ние нарушенных болезнью и оперативным вме-
184
шателъством главных систем жизнеобеспече­
ния — дыхания и кровообращения. После ста­
билизации дыхания и гемодинамики основным
содержанием интенсивной терапии становится
профилактика инфекционных осложнений
с одновременной настойчивой поддерживающей
и корригирующей терапией. Ранний послеопера­
ционный период можно считать благополучно
завершенным, когда расправляется опериро­
ванное легкое, нормализуются показатели крови
и больной может свободно вставать и ходить.
В поздний послеоперационный период проводят
симптоматическую терапию, местное лечение и
продолжают лечение осложнений, если их не
удалось купировать ранее. В это время наступает
устойчивая стабилизация функций систем дыха­
ния и кровообращения, а также обменных про­
цессов. Более подробно содержание меропри­
ятий интенсивной терапии по профилактике и
лечению недостаточности дыхания и кровооб­
ращения, а также коррекции других систем го­
меостаза в том объеме, как это применяется в
госпитальной хирургической клинике, будут из­
ложены в соответствующем разделе настоящего
руководства.
Несмотря на успехи легочной хирургии, ле­
тальность среди больных с хроническими абс­
цессами легких после резекций остается вы­
сокой. Совершенствование техники оператив­
ных вмешательств, а также прогресс анесте­
зиологии и реаниматологии позволили снизить
летальность после резекций легких при хрони­
ческих абсцессах до 7—10 %. [Богатов А. И.,
Мустафин Д. Г., 1980; Маневич В. Л. и др.,
1982, и др.1.
Среди 498 больных с хроническими абсцес­
сами легких, подвергшихся резекциям в госпи­
тальной хирургической клинике, умерли 60
(12 %) больных. Самой высокой смертность
была после пневмонэктомий (17,9 %). После
частичных резекций летальность была вдвое
ниже (8,6 %).
Наиболее частыми причинами гибели боль­
ных были дыхательная и сердечная недостаточ­
ность (14,8 %), эмпиема плевры (11,9 %) и
кровотечения (6,5 %). Довольно высокая об­
щая летальность после резекций у больных с
хроническими абсцессами легких в госпиталь­
ной хирургической клинике — 12 % —объяс­
няется тем, что оперативные вмешательства
часто выполнялись у больных с осложненными
формами абсцессов легких, а также у пожилых
и страдавших тяжелыми сопутствующими за­
болеваниями пациентов. Многим таким больным
отказывали в операции в других стационарах.
В то же время сократилось количество больных,
оперированных по поводу легко протекавших
неосложненных абсцессов легких. У многих
больных, которым по характеру заболевания
раньше широко производились резекции, в на­
стоящее время выздоровление достигается без
операции, и длительное наблюдение за ними
свидетельствует о стабильности достигнутого
результата.
Анализ причин летальных исходов после
резекций легких у больных с хроническими
абсцессами, а также характера послеоперацион­
ных осложнений позволяет прийти к выводу
о том, что улучшить результаты лечения можно
более тщательной предоперационной подготов­
кой больных к операции, совершенствованием
техники оперативного вмешательства, своевре­
менным предупреждением и лечением разви­
вающихся послеоперационных осложнений.
8
Глава
ОСТРАЯ ЭМПИЕМА
ПЛЕВРЫ И ПИОПНЕВМОТОРАКС
Эмпиема плевры (гнойный плеврит) — это
ограниченное или диффузное воспаление вис­
церальной и париетальной плевры, протекаю­
щее с накоплением гноя в плевральной полости
и сопровождающееся признаками гнойной ин­
токсикации и нередко дыхательной недоста­
точности. В большинстве случаев эмпиема
плевры является осложнением воспалительных
и гнойнодеструктивных процессов в легких,
а также травм и оперативных вмешательств
на органах груди.
ЭТИОЛОГИЯ, ПАТОГЕНЕЗ
И ЧАСТОТА ОСТРОЙ ЭМПИЕМЫ
Острая эмпиема плевры является полиэтиологическим заболеванием. Характер течения
острого инфекционного процесса в плевре зави­
сит от вида и вирулентности возбудителя, от
аиатомо-физиологических особенностей плев­
ральных листков и органов дыхания, от состоя­
ния иммунобиологической защиты организма.
Возбудителями эмпиемы плевры могут быть
различные микроорганизмы. В зависимости
от этиологии различают специфическую, неспецифическую и смешанную эмпиемы.
Специфическая эмпиема плевры вызывается
микобактериями туберкулеза, которые прони­
кают в висцеральную или париетальную плевру
контактным, лимфогенным или гематогенным
путем из туберкулезных очагов в легких, лим­
фатических узлов, позвоночника. Иногда наблю­
дается первичный туберкулезный плеврит. Не­
которые авторы [Кузин М. И. и др., 1976] к
специфическим относят грибковые эмпиемы
(актиномикотические, кандидамикотические,
аспергиллезные). К специфическим относят
также сифилитический плеврит [Теппер П. А.,
I960), однако в настоящее время он встречается
крайне редко. Смешанной эмпиему считают
в тех случаях, когда в плевральном экссудате
находят и микобактерии туберкулеза, и какиелибо из бактерий или грибков.
Чаще наблюдается неспецифическая эмпиема
плевры, вызываемая различными гноеродными
или гнилостными микроорганизмами. До при­
менения антибиотиков в гное из плевральной
полости чаще всего находили пневмококки,
стрептококки и диплококки. За последние деся­
тилетия соотношение микробных возбудителей
гнойных процессов заметно изменилось. Чаще
других в гнойной плевральной жидкости обна­
руживаются стафилококки — до 77 % IЛуцен­
ко С. М., Тарасова Е. И., 1975]. Это объясня­
ется выраженной вирулентностью стафилококка
и устойчивостью его к большинству антибак­
териальных средств.
Очень часто, до 30—45 % случаев [Коро­
лев Б. А. и др., 1982; Kessler Б. et al., 1974],
при посевах гноя из плевральной полости полу­
чают рост грамотрицательиых микроорганиз­
мов: различные штаммы кишечной, синегной­
ной палочки, протея. Как правило, эта микро­
флора малочувствительна или устойчива к воз­
действию большинства распространенных ан­
тибактериальных средств. В некоторых слу­
чаях в плевральном гное обнаруживают не­
сколько микробов. Эмпиемы с полиморфной
микробной флорой отличаются более тяжелым
течением.
Следует отметить, что нередко гной из плев­
ральной полости оказывается «стерильным»,
несмотря на явные признаки гнойного процесса.
Отсутствие роста микробов в этих случаях объ­
ясняется проводимой до посева общей и местной
антибактериальной терапией, а также тогда,
когда не делался посев анаэробной флоры. Как
показали исследования отечественных и зару­
бежных авторов, в гное из плевральной полости
анаэробные микробы при специальном иссле­
довании можно найти в 20—76 % случаев [Ко­
четков А. В., 1983; Shermann М. et al., 19771.
Наиболее частыми возбудителями среди них
являются неклостридиальные микроорганиз­
мы — бактероиды, фузобактерии, пептококки,
пептострептококки и др.
Патогенетически различают первичную и вто­
ричную эмпиемы плевры. При первичной эмпие­
ме очаг воспаления с самого начала локализу­
ется в плевральной полости, при вторичной —
он является осложнением какого-либо другого
гнойно-воспалительного заболевания, чаще
всего легочного [Спасокукоцкий С. И., 1938].
186
Первичная эмпиема возникает на фоне не­
измененных, здоровых плевральных листков,
в результате нарушения их барьерной функции
с занесением микрофлоры. Это обычно бывает
при открытой травме груди, после операций на
легком, а также при наложении искусственного
пневмоторакса.
Развитие эмпиемы после ранений груди обус­
ловлено тяжестью и характером повреждений
органов и тканей грудной клетки, наличием ино­
родных тел и гемотораксом. По «Опыту Вели­
кой Отечественной войны 1941 —1945 гг.», ост­
рая эмпиема плевры наблюдалась у 14 % ране­
ных с огнестрельными проникающими повреж­
дениями груди (Куприянов П. А., 1946]. При
ранениях с малым гемотораксом эмпиема воз­
никала в 3 %, при среднем гемотораксе
в 21,2 %, при большом — в 34,7 % случаев
[Бочаров А. А.. 1950|. В развитии эмпиемы
большую роль играют сроки первичной хирур­
гической помощи. Так, при оказании квалифи­
цированной хирургической помощи раненым
с открытым пневмотораксом в первые 6 ч эмпи­
ема развилась у 26,4 % раненых, а после обра­
ботки. произведенной позже 48 ч,— у 41,5 %.
В мирное время имеется возможность раннего
полноценного хирургического вмешательства,
поэтому эмпиема плевры наблюдается значи­
тельно реже, чем это было во время войны:
после проникающих ранений груди — около
10—15 %, при закрытых повреждениях — не
более 5 % [Вагнер Е. А.. 19811.
В связи с развитием торакальной хирургии
и расширением показаний к оперативным вме­
шательствам на органах груди особый интерес
представляет патогенез острых послеоперацион­
ных эмпием плевры. Инфицирование плевраль­
ной полости во время оперативных вмеша­
тельств происходит в основном при вскрытии
полости абсцесса, выделении легкого из сраще­
ний, обработке культи бронха или наложении
анастомозов при операциях на пишеводе. В от­
дельных случаях причиной эмпиемы является
несостоятельность швов культи бронха, пище­
водно-желудочного анастомоза. После опера­
тивных вмешательств на органах груди без
повреждения легкого острая эмпиема плевры
наблюдается у 2—3 % больных [Аблицов Н. П.,
19761, после операций на легких — от 5 до 31 %
[Колесников И. С. и др., 1965; Boyd A., Spen­
ser F., 1972], а после операций по поводу острых
гнойно-деструктивных заболеваний легких —
до 50% [Горшков Ю. И., 1976}.
Различают также так называемые крипто­
генные первичные эмпиемы, когда источник
инфекции плевры выявить не удается [Ку­
зин М. И. и др., 1976].
По данным Г. И. Лукомского (1976), в 88 %
случаев вторичная эмпиема плевры явилась
осложнением пневмоний, острых и хронических
гнойных заболеваний легких. Пневмония может
с самого начала протекать с развитием гной­
ного плеврита (пара- или синпневмоническая
эмпиема), или же эмпиема развивается на исхо­
де пневмонии и приобретает характер самостоя­
тельного заболевания
(метапневмоническая
эмпиема). Парапневмоническая эмпиема диа­
гностируется очень редко, так как маскируется
клиникой воспаления легкого. В период до при­
менения антибиотиков и новых антибактери­
альных средств эмпиемы развивались примерно
у 6—7 % больных [Buschmann О., Hackerott Н.,
19531, а при крупозной пневмонии — у 21,8 %
[Фомина А. С., 1977}. С применением антибио­
тиков для лечения пневмонии частота гнойного
плеврита уменьшилась до 1 %, однако за послед­
ние годы вновь воспаление легких значительно
чаще осложняется эмпиемой плевры (от 2 до
5 %). При абсцессах легких эмпиема развивает­
ся у 8—11 % больных [Стручков В. И., 1967;
Колесников И. С., Вихриев Б. С., 19731, а при
гангрене легкого - у 55—90 % больных [Гор­
шков Ю. И., 1977; Колесников И. С. и др., 1983].
В единичных случаях эмпиема может развиться
как осложнение нагноившейся врожденной или
паразитарной кисты легкого, распадающегося
рака, спонтанного пневмоторакса.
Вторичная эмпиема плевры может развивать­
ся и в результате распространения воспалитель­
ного процесса на плевру из тканей грудной стен­
ки и соседних органов (при нагноении ран гру­
ди, остеомиелите ребер, позвоночника, грудины,
хондрите, лимфадените, медиастините, перикар­
дите). Источником инфицирования плевры
в редких случаях могут быть острые воспали­
тельные и гнойные заболевания органов брюш­
ной полости (поддиафрагмальцый абсцесс,
холецистит, панкреатит, перфоративная язва
желудка и др.). Проникновение микробов из
брюшной полости на плевру происходит по лим­
фатическим сосудам и через щели в диафрагме.
Возможен также гематогенный путь распростра­
нения инфекции при тромбофлебите, остеомие­
лите, аборте, послеродовом сепсисе.
Патогенез развития острого гнойного процес­
са в плевре сложен и определяется не только
и даже не столько проникновением микроор­
ганизмов в плевру, сколько образовавшимися
условиями обитания этих микробов в плевраль­
ной полости и снижением местной и общей
иммунобиологической реактивности организма.
Изменения в плевре могут нарастать остро
или постепенно с развитием фибринозного,
экссудативного или фибринозно-гнойного плев­
рита. Нарушения функции дыхания обуслов­
лены не только воспалительным или деструк­
тивным процессом в легком, но и сдавлением
легкого накапливающейся в плевральной поло­
187
сти жидкостью. При значительном количестве
жидкости происходит смещение средостения
в здоровую сторону и появляются гемодинами­
ческие расстройства.
Тяжелая гнойная интоксикация ведет к на­
рушениям функций миокарда, почек, печени,
эндокринных органов. Большое значение в раз­
витии ряда изменений имеют потери с гноем
белка и электролитов. В связи с этим падает
онкотическое давление крови и уменьшается
объем циркулирующей крови. Этому способству­
ет активация кининовой системы, наступающая
в результате действия продуктов аутолиза бак­
терий и некроза тканей. В результате гнойной
интоксикации, нарастающей гипо- и диспротеииемни понижаются активность защитных им­
мунных реакций и репаративные способности
организма.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
ПИОПНЕВМОТОРАКС А
Пиопневмоторакс — острый гнойный про­
цесс, развивающийся вследствие прорыва гной­
ника легкого в плевральную полость. Он может
возникнуть чаще всего в результате прогрес­
сирования гангрены легкого, реже — острого
абсцесса и еще реже —- при прорыве хрониче­
ского гнойника легкого в стадии обострения.
Прорыв абсцесса легкого в плевральную по­
лость сопровождается поступлением в нее гноя и
воздуха. При отсутствии сращений между парие­
тальной и висцеральной плеврой развивается то­
тальный пиопневмоторакс с тяжелой клиничес­
кой картиной за счет раздражения огромного
рецепторного поля плевры и значительной всасы­
ваемости токсинов. При наличии плевральных
спаек, что бывает чаще в верхних отделах плев­
ры, а также при хронических гнойно-деструк­
тивных процессах в легких может развиться
ограниченный пиопневмоторакс. В зависимости
от того, сохраняется ли сообщение вскры­
вшегося абсцесса с бронхом или оно прикрывает­
ся, различают пиопневмоторакс с бронхиальным
свищом или без него. Если же сообщение бронха
легкого с плевральной полостью имеет клапан­
ный механизм, то развивается клапанный пиопневмоторакс. Роль клапана могут выполнять
наружная стенка полости абсцесса, детрит,
фибрин, отечная слизистая оболочка бронха.
КЛАССИФИКАЦИЯ ЭМПИЕМ
ПЛЕВРЫ
Сознавая трудность создания полной и прак­
тически значимой классификации эмпием плев­
ры, мы обобщили и частично изменили предло­
женные ранее классификации В. М. Сергеева
(1967), М. И. Кузина и соав^. (1976), Г. И. Лукомского (1976) и В. И. Маслова (1976).
Подразделение эмпием в зависимости от их
этиологии и патогенеза представлено ниже. Из
множества факторов, положенных в основу
классификации эмпием плевры, важнее всего
выбрать те, которые определяют тактику ока­
зания помощи и выбора дальнейших диагно­
стических и лечебных мероприятий. Наиболее
существенными определяющими факторами
являются наличие или отсутствие деструкции
легкого, распространенность процесса, сооб­
щение с внешней средой и характер его, клини­
ческое течение заболевания.
Пиопневмоторакс как одна из разновидно­
стей эмпиемы с деструкцией легочной ткани
выделен нами в классификации в связи с осо­
бой тяжестью клинических проявлений и свое­
образной лечебной тактикой, особенно в началь­
ной стадии заболевания.
Различие острых и хронических эмпием
плевры на основании календарного срока забо­
левания носит противоречивый и условный ха­
рактер.
По нашему мнению, деление эмпием по ха­
рактеру течения заболевания имеет важное
практическое значение, так как острые и хро­
нические эмпиемы различаются и по клиниче­
ской картине, и по методам лечения. Основ­
ными дифференциальными критериями явля­
ются морфологические изменения плевры, осо­
бенно висцерального листка, которые опреде­
ляют возможность или невозможность расправ-
Классификация эмпием плевры
Определяющим фактор
Клиническое
течение
Острые (до 3 мес)
Хронические (свыше
3 мес)
Сообщение с внешней
средой
Деструкция
легкого
Эмпиема без деструкции лег­
кого (простая)
Эмпиема с деструкцией лег­
кого
Пиопневмоторакс
Распространен­
ность
Закрытые
Ограниченные
Открытые:
с бронхоплевральным свищом
с плеврокожным свищом
с бронхоплеврокожным свищом
с решетчатым легким
с другими полыми органами
Распространенные
188
Рис. 97. Зрелая грануляционная ткань с явлениями начи­
нающегося склероза.
Гематоксилип-эозин. Ув. 70.
Рис. 96, Грануляционная ткань с обилием капиллярных
сосудов и круглоклеточным инфильтратом.
Гематоксилип-эозип. Ув. 140.
ления легкого и ликвидации эмпиемной поло­
сти. Многочисленными клиническими наблюде­
ниями и гистологическими исследованиями
материала, полученного во время плеврэктомий, декортикаций и резекций легкого, доказано,
что на 2—3-м месяце от начала эмпиемы на
плевре, преимущественно на париетальном лист­
ке, имеются значительные фибринные напла­
стования. Воспалительная реакция плевры в
эти сроки чаще всего носит уже репаративный
характер: прорастают фибробласты, формиру­
ется грануляционная ткань. Однако последняя
еще не уплотнена, нет зрелых коллагеновых
волокон. Грануляционная ткань имеет вид тон­
кой прослойки из круглых голоядерных клеток
между сохранившимися слоями плевры и фиб­
ринозно-гнойными напластованиями (рис. 96,
97). В большинстве случаев только с 10—12-й
недели начинается интенсивное созревание
грануляционной ткани, нарастают склеротиче­
ские изменения, которые постепенно распро­
страняются с париетальной плевры на грудную
стенку, а с висцеральной — на легкое. И лишь
к концу 3-го месяца заболевания и далее фор­
мируются основные морфологические при­
знаки хронической эмпиемы плевры: ригидная
остаточная плевральная полость и плевроген­
ный склероз легкого [Policard A., Gaby Р., 1970].
Исходя из этого мы считаем оправданным
в клинической практике относить к хрониче­
ским эмпиемам те случаи, которые продолжа­
ются более 3 мес и имеют характерные клини­
ческие признаки — фазность заболевания, т. е.
периоды затихания и обострения гнойного про­
цесса. В большинстве случаев в сроки от 1 до
3 мес от начала острой эмпиемы клиническая
симптоматика обусловлена остаточными про­
явлениями гнойной интоксикации и умерен­
ными дыхательными нарушениями, но с отчет­
ливой тенденцией к улучшению. Выбор рацио­
нального плана лечения в таких случаях значи­
тельно отличается. По данным литературы и
нашим клиническим наблюдениям, в сроки до
3 мес от начала заболевания почти всегда имеет­
ся реальная возможность добиться клиниче­
ского выздоровления путем активных консерва­
тивных мероприятий. Сроки и исходы лечения
больных в этой стадии значительно улучши­
лись с внедрением в клиническую практику
современных протеолитических ферментов и
методов систематической санации плевральной
полости промываниями с активной вакуумной
аспирацией. При хронической эмпиеме плевры
эти методы позволяют заметно улучшить состоя­
ние больного, но ликвидировать остаточную
плевральную полость можно только операцией.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ ОСТРОЙ
ЭМПИЕМЫ И ПИОПНЕВМОТОРАКСА
Общие проявления в клинике различных форм
острой эмпиемы плевры начинаются прежде
всего с появления резких болей иа стороне пора-
189
же ния, с признаков гнойной интоксикации и
часто дыхательной недостаточности.
Признаки дыхательной недостаточности при
острой эмпиеме плевры обусловлены не только
накоплением жидкости в плевральной полости
и сдавлением легкого, но и гнойно-деструктив­
ным процессом легочной паренхимы, шунти­
рованием крови из коллабированных отделов
легкого, нарушением гемодинамики и бронхо­
спастическими реакциями.
У всех больных имеются боли в груди, ка­
шель, нередко с выделением значительного коли­
чества мокроты, одышка. Одышка может быть
выражена в большей или меньшей степени. Есте­
ственно, что при большом накоплении жидко­
сти в плевральной полости или пиопневмотораксе с коллапсом легкого II—III степени одыш­
ка будет значительной даже в покое. Однако
одышка может наблюдаться и при ограничен­
ной эмпиеме, особенно при базальном гнойном
плеврите, когда дыхательные движения замет­
но ограничены из-за резких болей при глубо­
ком дыхании. Чаще при острой эмпиеме боль
в груди носит постоянный ноющий характер,
усиливается при глубоком дыхании, кашле,
иногда при перемене положения тела. При во­
влечении в воспалительный процесс межребер­
ных мышц и нервов болевой синдром напоми­
нает межреберную невралгию.
Из-за болей и одышки положение больного
в постели нередко вынужденное. При ограни­
ченной эмпиеме болевой синдром менее выра­
жен и часто больные лежат на больном боку,
так как при этом дыхательные экскурсии пора­
женной половины грудной клетки ограничены.
Иногда больные предпочитают полусидячее
положение.
Кашель у больных с острой эмпиемой плевры
может быть сухим (в начальной стадии гной­
ного плеврита) или с выделением мокроты. Так
как большинство острых эмпием являются вто­
ричными, т. е. осложнениями гнойно-деструктив­
ных заболеваний легких, кашель у этих больных
сопровождается выделением значительного
количества гнойной мокроты (нередко до
500 мл/сут). При наличии бронхоплеврального
свища особенно много откашливается мокроты
в положении больного на здоровом боку.
При осмотре больного в большинстве случаев
отмечается ограничение дыхательных движе­
ний одной половины грудной клетки. При то­
тальных и распространенных острых эмпиемах
плевры нередко имеются сглаженность меж­
реберных промежутков, местный отек кожи и
подкожной клетчатки над областью скопле­
ния гноя в плевральной полости. Пальпаторно
можно определить, что на больной стороне
складка кожи несколько толще, чем на симмет­
ричных участках грудной клетки, и болезнен­
ная. В дальнейшем ткани грудной стенки в этой
зоне становятся плотными, усиливается болез­
ненность, появляется гиперемия кожи.
При перкуссии всегда над скоплением жидко­
сти в плевральной полости определяется при­
тупление, причем по распространенности уко­
роченного звука можно ориентировочно судить
о количестве экссудата в полости. При отсут­
ствии воздуха и сращений в плевральной поло­
сти верхняя граница тупости соответствует ли­
нии Эллиса — Дамуазо, а над зоной тупости
отмечается тимпанический звук из-за сдавле­
ния части легкого (признак Шкоды). При огра­
ниченной эмпиеме с небольшим скоплением
гноя в полости перкуторные данные скудны.
При аускультации отмечается ослабление
везикулярного дыхания вплоть до полного от­
сутствия его над большим количеством жид­
кости в полости. Над зоной поджатого легкого—
бронхиальное дыхание, иногда выслушивают­
ся разнокалиберные влажные хрипы, может
быть слышен шум трения плевры из-за фиб­
ринозного плеврита вокру! полости эмпиемы.
Если имеется бронхоплевральный свищ и по­
лость хорошо дренируется через бронх, то мо­
жет выслушиваться амфорическое дыхание.
Очень характерно усиление бронхофонии над
областью скопления жидкости.
Степень гнойной интоксикации может быть
различной, начиная от легкой до тяжелой и
даже септической формы. Она зависит преиму­
щественно от распространенности гнойного
процесса, вирулентности микрофлоры и инди­
видуальной реактивности больного. В большин­
стве случаев заболевание начинается с повы­
шения температуры тела, недомогания, по­
знабливания, ухудшения аппетита. Так как эм­
пиема плевры чаще всего является вторичным
заболеванием, эти признаки нередко объяс­
няют обострением воспалительного процесса
в легком, нагноением раны после ранения или
оперативного вмешательства. В течение не­
скольких дней температурная реакция как один
из важнейших признаков гнойно-резорбтив­
ного процесса становится ремиттирующей,
появляются ознобы. При гнилостной эмпиеме
лихорадка часто имеет гектический характер
с суточными колебаниями около 3 °C, сопро­
вождается резкими ознобами, потливостью,
тяжелым общим состоянием, иногда рвотой.
В связи с широким применением антибактери­
альных препаратов для лечения воспалитель­
ных заболеваний гектнческая температура в
последние годы наблюдается нечасто. У боль­
шинства больных эмпиемой плевры темпера­
тура повышается до 384-38,5 °C, причем она со­
храняется без значительных колебаний в тече­
ние нескольких суток. Нередко температурная
реакция является единственным насторажи­
190
вающим признаком, требующим проведения
повторного рентгенологического исследования
и плевральной пункции с целью обнаружения
скопления гноя.
У многих больных с острой эмпиемой плевры
гнойная интоксикация проявляется нервнопсихическими расстройствами различной сте­
пени выраженности: от головных болей, раз­
дражительности, бессонницы, быстрой утом­
ляемости до психомоторного возбуждения,
делириозного синдрома, комы.
Гнойная интоксикация приводит к дистро­
фии миокарда и энергодинамической недоста­
точности сердца (Василенко В. X., 1960]. Одно­
временно может развиться сосудистая недо­
статочность из-за нарушения функции надпо­
чечников. Сердечно-сосудистая недостаточ­
ность проявляется тахикардией, неприятными
ощущениями в области сердца, сердцебиением,
артериальной гипотензией и замедлением цир­
куляции, акроцианозом. При обследовании
определяется глухость тонов сердца, иногда
экстрасистолия, на верхушке сердца выслу­
шивается систолический шум. В последующем
при сохранении гнойной интоксикации раз­
вивается легочно-сердечная недостаточность
с нарастающей декомпенсацией кровообраще­
ния и гипертензией в малом круге, о чем сви­
детельствуют акцент II тона на легочной арте­
рии, надчревная пульсация в связи с гипертро­
фией правого желудочка, сдвиг электрической
оси сердца вправо на электрокардиограмме.
Как следствие гнойной интоксикации появ­
ляются признаки нарушений функций органов,
богатых ретикулоэндотелиальной тканью (пе­
чень, почки, селезенка, костный мозг), так как
именно они принимают основное участие в дез­
интоксикации организма. При обследовании
больных определяется увеличение печени, иног­
да небольшая иктеричность склер и кожных
покровов. Появляются признаки нарушения
белковообразующей функции печени (значитель­
ное уменьшение альбумина), уменьшается
содержание холестерина, протромбина, значи­
тельно повышается содержание трансаминаз
и фибриногена. Некоторые больные отмечают
ноющие боли в поясничной области, усиливаю­
щиеся припоколачивании в области почек. У мно­
гих больных с острой эмпиемой выявляются
признаки токсической нефропатии в виде уме­
ренной протеинурии, лейкоцитурии, микрогема­
турии и цилиндрурии, иногда отмечается гипоизостенурия. Воздействие интоксикации на рети­
кулоэндотелиальную систему костного мозга
приводит к значительному угнетению эритро­
поэза и к нарастанию анемии, несмотря на про­
водимую терапию.
Убедительными признаками гнойной интокси­
кации являются лейкоцитоз и изменение лей­
коцитарной формулы. В типичных случаях ост­
рой эмпиемы плевры наблюдаются повышение
числа лейкоцитов до (154-20) - 109/л при зна­
чительном нейтрофилезе (свыше 80 %) и повы­
шение лейкоцитарного индекса интоксикации
по Я. Я. Кальф-Калифу в среднем до 7,0+0,8
[Костюченко А. Л. и др.. 1983]. При дальней­
шем нарастании гнойно-деструктивного процес­
са в плевре абсолютное число лейкоцитов мо­
жет уменьшиться, но сохраняется нейтрофилез, развивается лимфопения, что является
неблагоприятным прогностическим признаком.
Большое значение в оценке состояния боль­
ных с острой эмпиемой имеют признаки белко­
вых, электролитных и волемических нарушений.
Неблаюприятное влияние на развитие и течение
острой эмпиемы плевры оказывают три осново­
полагающих фактора: фактор нагноения, фактор
резорбции и фактор потерь белка. Воздействие
этих факторов приводит к гипоальбуминемии
и диспротеинемии, которые являются веду­
щим компонентом в развитии волемических,
электролитных расстройств, а также иммуноло­
гических нарушений. Чем интенсивнее нагное­
ние плевры и легочной ткани, тем больше бел­
ковые потери, отчетливее диспротеинемия и
уменьшение абсолютного количества альбуми­
нов, тем быстрее развиваются расстройства
водно-электролитного обмена. В первый период
развития эмпиемы организм еще компенсирует
уменьшение количества альбумина повыше­
нием глобулинов. По мере утяжеления состоя­
ния глобулины не могут уже покрыть дефицита
альбумина. Это приводит к нарушению колло­
идно-осмотических свойств плазмы, способно­
сти ее удерживать воду. Абсолютное содержа­
ние натрия плазмы вначале несколько пони­
жено (соответствует снижению плазменного
объема), а затем повышается. Гипернатрийплазмия объясняется увеличением секреции альдо­
стерона, так как у таких больных под влиянием
длительной гипоксии развивается гиперплазия
клубочковой зоны коры надпочечников [Кли­
менко Г. А. и др., 1965]. При тяжелом течении
увеличивается калий плазмы, что объясняется
распадом тканей и гибелью клеток. Во всех
фазах имеется отчетливая гипокалийурия, обус­
ловленная потерями калия с гноем. Гипонатрийурия объясняется задержкой натрия в тканях.
Изменения водных секторов прогрессируют
по мере утяжеления процесса. Постепенно про­
исходит расширение всех водных секторов, что
проявляется вначале скрытыми отеками, а в
дальнейшем — явными.
В клинической картине некоторых форм
острой эмпиемы плевры, кроме признаков ды­
хательной недостаточности, гнойной интоксика­
ции и типичных данных физикального обсле­
дования, имеются дополнительные симптомы.
191
При ограниченной эмпиеме кли­
ника во многом определяется локализацией
скопления гноя. При этом различают верхушеч­
ное, пристеночное, наддиафрагмальное, междо­
левое и парамедиастинальное расположение
гнойника.
При верхушечной эмпнеме могут наблюдать­
ся отечность надключичной области и плеча,
плексит, иногда триада Горнера. Эти симпто­
мы развиваются в связи с вовлечением в воспа­
лительный процесс регионарных лимфатических
и венозных сосудов, а также нервных стволов.
Для пристеночных эмпием характерны бо­
лее выраженные болевые ощущения и ограни­
чение амплитуды дыхательных движений на
стороне поражения, сглаженность межребер­
ных промежутков, отечность подкожной клет­
чатки, укорочение перкуторного звука и ослаб­
ление дыхания над областью скопления гноя.
При базальной (наддиафрагмальной) эмпи­
еме боли чаще бывают в нижней части грудной
клетки и в подреберье. Они усиливаются при
глубоком вдохе, нередко иррадиируют в область
шеи н плеча. Иногда боли иррадиируют в эпи­
гастральную область и подреберье из-за раз­
дражения нижних межреберных нервов. В связи
с этим иногда бывает трудно дифференциро­
вать базальную эмпиему от поддиафрагмаль­
ного абсцесса и других хирургических заболе­
ваний органов брюшной полости.
Парамедиастинальная эмпиема может прояв­
ляться симптомами сдавления верхней полой
вены.
В дифференциальной диагностике ограни­
ченных эмпием плевры важное значение имеют
рентгенологические методы исследования и
пункции плевральной полости.
Клиническое течение посттра в м эти­
ческих острых эмпием определя­
ется прежде всего характером повреждения
грудной стенки, легкого и других внутренних
органов.
При закрытых травмах груди, ранениях без
повреждения легкого и с незначительным по­
вреждением тканей грудной стеикн эмпиема
развивается как нагноение гемоторакса. Кли­
ническая картина в таких случаях типичная,
течение относительно благоприятное.
Эмпиема плевры после ранений с повреж­
дением легкого протекает более тяжело, что
обусловлено степенью повреждения легкого,
наличием и характером бронхоплевральных
сообщений. Чаще всего гнойный процесс начи­
нается в плевральной полости как нагноение
инфицированного гемоторакса. Однако нагное­
ние может развиваться и в плевре, и в повреж­
денном легком. Клиническая картина в таких
случаях соответствует клинической картине
эмпиемы, протекающей с деструкцией легкого.
В некоторых случаях гнойный процесс начи­
нается с нагноения ушитой раны грудной стен­
ки, а в дальнейшем развивается пиопневмоторакс.
Наиболее тяжело протекают эм пнем ы после
ранений с широко открытым пневмотораксом.
Гнойный процесс в таких случаях характери­
зуется бурным клиническим течением по типу
раневого сепсиса, переходит на грудную стенку
с развитием флегмоны. Прогноз часто небла­
гоприятный.
Клиническая симптоматика послеопера­
ционных эмпием зависит ие только от
степени загрязнения плевральной полости, но
и от характера перенесенного вмешательства,
анатомических взаимоотношений органов в ито­
ге сложных торакальных операций и наличия
сообщения с легким или другими органами.
В связи с этим различают 4 группы послеопе­
рационных эмпием плевры: 1) после пневмон­
эктомии; 2) после частичной резекции легкого;
3) после операций на пищеводе; 4) после кар­
диохирургических и других операций без по­
вреждения легкого и других полых органов.
Особенности клинического течения и диагно­
стика этих форм острых эмпием плевры будут
рассмотрены дальше.
Анаэробные эмпиемы плевры от­
личаются крайне тяжелым течением. Они могут
быть молниеносными, быстропрогрессирую ­
щими и торпиднымн. Молниеносные и быстропрогрессирующие формы анаэробной эмпиемы
протекают с резчайшей интоксикацией, тахи­
кардией до 120—140 уд/мин, гектической тем­
пературой тела, психоэмоциональными рас­
стройствами вплоть до коматозного состояния.
Торпидные формы анаэробной эмпиемы тоже
отличаются тяжелой общей интоксикацией. От­
мечаются резкая бледность, желтушность склер
и кожи, нарастающая одышка. При осмотре
чаще выявляются отек подкожной клетчатки
и кожи на пораженной стороне грудной клетки,
усиление болезненности по ходу межреберий.
При газообразующих формах анаэробных воз­
будителей можно уже в ранних стадиях обна­
ружить при аускультации характерный хруст
газа в подкожной клетчатке грудной клетки.
Важную роль в диагностике анаэробной эм­
пиемы играет пункция плевральной полости,
при которой из иглы выделяется зловонный
газ. Гной обычно грязно-серого цвета, иногда
с геморрагическим оттенком, всегда с гнилост­
ным запахом. Диагноз подтверждается спе­
циальными бактериологическими исследова­
ниями.
Клиническая картина пиопневмотор а к с а определяется, прежде всего, распро­
страненностью гнойного процесса в плевраль­
ной полости, степенью деструкции легкого и
192
характером бропхоплевральных сообщений. По
тяжести клинического течения различают ост­
рую, мягкую и стертую формы пиопневмоторакса (Спасокукоцкий С. И., 19381.
Острый пиопневмоторакс наступает при про­
рыве гнойно-деструктивного очага легкого в сво­
бодную плевральную полость. Чаще всего это
встречается при острых абсцессах и гангрене
легкого, когда плевральная полость у больных
не заращена.
Перфорация абсцесса происходит нередко
во время сильного кашля и проявляется острыми
болями в груди, резчайшей одышкой, бледно­
стью кожных покровов, липким потом, циано­
зом кожи и слизистых оболочек. Артериальное
давление при этом снижается до 50—70 мм
рт. ст., пульс становится нитевидным.
Наиболее тяжело острый пиопневмоторакс
протекает при сочетании с напряженным пнев­
мотораксом. Из-за нарастающей одышки по­
ложение больного становится вынужденным —
обычно он сидит, оперевшись руками о край
кровати. Одна половина грудной клетки меньше
участвует в акте дыхания, межреберные про­
межутки расширены, голосовое дрожание
ослаблено, перкуторно определяется коробоч­
ный звук, при аускультации — бронхиальное
дыхание с амфорическим оттенком. Иногда шок
и легочно-сердечная недостаточность нарастают
так стремительно, что спасти больного может
только экстренное хирургическое вмешательство.
Если клапанного механизма нет, то состоя­
ние больного постепенно стабилизируется, ге­
модинамические нарушения и дыхательная
недостаточность несколько уменьшаются. Даль­
нейшее течение заболевания в основном зависит
от течения гнойно-деструктивного процесса
в легком. Если острый пиопневмоторакс раз­
вился на фоне гангрены легкого, то она будет
иметь тенденцию к ухудшению. Если же острый
пиопневмоторакс явился осложнением острого
абсцесса, то нередко после опорожнения гной­
ника в плевральную полость деструктивный
процесс в легком стихает, а после эвакуации
гноя из полости плевры наступает улучшение.
В дальнейшем течение эмпиемы будет зависеть
от характера сообщения плевральной полости
с бронхом, а следовательно, возможности рас­
правления легкого.
Мягкая форма пиопневмоторакса развива­
ется при перфорации в плевральную полость
небольшого периферического абсцесса легкого.
Больные отмечают усиление болей в груди,
одышки и кашля, повышение температуры тела
и другие признаки умеренной гнойной интокси­
кации. Так как сообщения с крупным бронхом
в таких случаях, как правило, нет и воздух по­
ступает в плевральную полость в небольшом
количестве, процесс локализуется в основном
13 Зак 0517
в зоне прорыва гнойника. Это ведет к ограни­
ченному пиопневмотораксу.
Стертая форма пиопневмоторакса может
быть при прорыве небольшого деструктивного
очага легкого в хорошо отграниченную спай­
ками часть плевральной полости. Чаще это встре­
чается при хронических нагноительных забо­
леваниях легких. Перфорация гнойника в по­
лость может произойти незаметно для больного.
Клиническая картина будет определяться в
основном предшествующими изменениями в
легком.
Внешний вид больного при ограниченном
пиопневмотораксе обычно не изменяется. Фи­
зикальные данные разнообразны. Голосовое
дрожание на стороне поражения ослаблено.
Как правило, определяется укорочение перку­
торного звука вплоть до абсолютной тупости
над зоной скопления экссудата. Выше зоны
укороченного перкуторного звука будет зона
тимпанита, причем взаиморасположение участ­
ков тупости и тимпанита меняется при изме­
нении положения больного. Дыхание над жид­
костью ослаблено или не прослушивается.
Нередко ограниченный пиопневмоторакс
диагностируется только при рентгенологиче­
ском обследовании, когда определяются более
или менее выраженное коллабирование лег­
кого и часто горизонтальный уровень жидко­
сти в плевральной полости. Величина и форма
эмпиемной полости зависят от наличия и харак­
тера сращений между париетальной и висце­
ральной плеврой, от количества гноя и воздуха,
поступивших в полость, а также от эластично­
сти легочной ткани. Иногда в плевральной поло­
сти сразу же образуются множественные гори­
зонтальные уровни, так как спайки удерживают
легкое от полного спадения и разграничивают
полость на несколько частично или полностью
изолированных камер (многокамерный пио­
пневмоторакс).
Дальнейшее течение заболевания при огра­
ниченном пиопневмотораксе, как и при распро­
страненном, определяется характером нагноительного процесса в легком и наличием брон­
хоплеврального сообщения. Возможны следую­
щие клинические варианты. У одних больных
нагноение легочной тканн после перфорации
прогрессирует, нарастает гнойный процесс в
плевральной полости и сохраняется бронхо­
плевральное сообщение. У других больных
абсцесс легкого частично опорожняется в плев­
ру, легкое спадается и бронхоплевральное сооб­
щение закрывается; гнойный процесс продол­
жается и в легком, и в плевральной полости,
но без сообщения между ними. У некоторых
больных абсцесс легкого опорожняется пол­
ностью и гнойный процесс в нем регрессирует;
сохраняется бронхоплевральный свищ; клини-
193
Рис. 98. Левосторонняя эмпиема плевры.
а
прямая рентгенограмма; б — боковая
рентгенограмма.
Видно скопление жидкости в заднебазальных отделах грудной
полости.
ческая картина определяется в основном эмпи­
емой плевры. Наконец, у части больных после
опорожнения абсцесса дефект на поверхности
легкого закрывается и заживает, гнойный про­
цесс регрессирует после аспирации гноя и воз­
духа из плевральной полости.
В диагностике острой эмпиемы плевры и пиопневмоторакса большое значение имеют рентге­
нологические, инструментальные, эндоскопи­
ческие и лабораторные методы исследований.
Важнейшими в исследовании больных острой
эмпиемой плевры являются рентгенологиче­
ские методы: рентгеноскопия, рентгенография,
латероскопия и латерография, плеврография,
фистулография, томография и бронхография.
Рентгеноскопия дает возможность опреде­
лить объем и локализацию жидкости в плев­
ральной полости, провести ряд функциональ­
ных тестов. Так, при ограниченных эмпиемах
определяются тени различной формы (округ­
лой, полушаровидной, треугольной) в зависи­
мости от локализации скоплений гноя и харак­
тера сращений в плевральной полости. Важно
отметить изменение контуров тени при измене­
нии положения тела, при дыхательных движе­
ниях. Многоосевое исследование позволяет
определить наиболее удачное место для пунк­
ции плевральной полости (рис. 98).
При отсутствии сращений в плевральной поло­
сти значительное количество экссудата (более
300 мл) определяется в виде характерной тре­
угольной тени с дугообразной (косой) верхней
границей в прямой проекции при вертикальном
положении больного. Интенсивность тени изме­
няется при дыхании. При большом количестве
жидкости происходит смещение средостения
в здоровую сторону, что особенно заметно при
вдохе. При затенении всей половины грудной
клетки иногда можно выявить более светлый
участок овальной формы в медиальном отделе
подключичной области, где находится поджа­
тое экссудатом легкое. Прозрачность этого
участка изменяется при глубоком дыхании боль­
ного.
Значение рентгеноскопии при обследовании
больных эмпиемой плевры особенно велико в
связи с возможностью частых повторных иссле­
дований, иногда даже два раза в день — до и
после пункции.
Рентгенография позволяет регистрировать
эти изменения. На рентгенограммах видны бо­
лее тонкие структурные изменения в плевраль­
ной полости и в легком, особенно после аспира­
ции гноя.
Исследование в вертикальном положении
позволяет определить лишь поперечные раз­
меры гнойной полости. Для оценки ее вертикаль­
ных размеров необходимо исследовать в латеропозиции (рис. 99), когда экссудат перемещается
вниз от купола диафрагмы в наружные отделы
грудной клетки и образует горизонтальный
уровень (феномен Ленка). При этом можно
обнаружить даже небольшое количество жид­
кости (100—150 мл), что очень важно для диф­
ференциальной диагностики с плевральными
спайками или облитерацией полости в зоне
реберно-диафрагмального синуса
(Фрид-
194
Рис. 99. Левосторонняя тотальная острая эмпиема,
а - прямая рентгенограмма; б боковая рентгенограмма; в
рентгенограмма в латеропозиции.
кин В. Я., 1962]. Латероскопия и особенно
латерография в положении на стороне пораже­
ния дают возможность также выявить характер
патологических изменений в нижних отделах
легкого, которые были прикрыты плевральной
жидкостью при исследовании в вертикальном
положении. Кроме того, используя методику
«перемещения газового пузыря» |Санпитер И. А.,
1976] при пиопневмотораксе или путем пунк­
ционного введения небольшого количества
воздуха в остаточную полость, рентгенограммы
в положении на боку, на спине и на животе позво­
ляют оценить все стенки полости эмпиемы.
Для уточнения размеров полости и конфи­
гурации ее стенок используется плеврорентге­
нография после введения рентгеноконтраст­
ных веществ пункционно или через дренаж.
13 *
В ряде случаев острая эмпиема протекает
по типу фибринозно-гнойного плеврита и уже
в начале заболевания определяется резкое утол­
щение стенок полости, причем утолщение парие­
тальной плевры чаще всего обусловлено фибринными напластованиями, а утолщение висце­
ральной плевры отражает суммацию тени уме­
ренных напластований фибрина и коллабированной легочной паренхимы. Конгломераты
фибрина на плевре могут быть самой различной
формы, они могут образовывать многочислен­
ные мелкие полости с уровнями экссудата
(рис. 100).
У некоторых больных стенки эмпиемной
полости остаются тонкими и ровными длитель­
ное время по типу пиогенной капсулы. Иногда
плеврорентгенография позволяет выявить нали-
195
Рис. I (JO. Правосторонняя эмпиема плевры с множествен­
ными уровнями жидкости и частичным коллапсом легкого.
Рис. 101. И. ie npoi ра м ма (фи с туло i ра м ма) п ри эм п и е ме
плевры с бронхоплеврокожным свищом после пневмонэк­
томии.
чие, локализацию и даже размеры бронхиаль­
ных свищей.
При эмпиеме с плеврокожным свищом важ­
ную информацию можно получить используя
фистулографию (рис. 101).
С целью оценки характера и распространен­
ности деструктивного процесса в легком важно
томографическое исследование. По томограм­
мам можно уточнить также характер изменений
стенок плевролегочной или плевральной поло­
сти. В ряде случаев для оценки патологических
изменений бронхиального дерева и уточнения
локализации бронхиального свища проводится
бронхография после тщательной санации брон­
хиального дерева и полости эмпиемы. Томо­
графия и бронхография позволяют решить
вопрос об объеме предстоящего оперативного
вмешательства, особенно при хронической эм­
пиеме плевры.
Пункция пзевры должна быть произведена
во всех случаях, когда при физикальном или
рентгенологическом обследовании больного
возникло подозрение на наличие гноя или эк­
ссудата в полости.
Методика проведения плевральной пункции
общеизвестна и в типичных случаях проста.
Обычно при метапневмонической эмпиеме пунк­
цию плевры производят в восьмом межреберье
по задней подмышечной линии. При атипичной
локализации гноя и ограниченной эмпиеме плев­
ры точку для пункции необходимо наметить при
тщательном физикальном обследовании и мно­
гоосевой рентгеноскопии. Плевра тьную жид­
кость максимально аспирируют, при этом опре­
деляют количество ее, цвет, запах, наличие
хлопьев. После аспирации экссудата необхо­
димо установить наличие или отсутствие ва­
куума в полости. В сомнительных случаях про­
водят манометрию плевральной полости, для
чего к пункционной игле присоединяется мано­
метр пневмотораксного аппарата. Осущест­
вляя поочередно аспирацию воздуха и мано­
метрию, можно ориентировочно судить о диа­
метре сообщения с бронхом. Аспирацию гноя
завершают обильным промыванием плевраль­
ной полости любым антисептическим раство­
ром.
Первое суждение о характере процесса в по­
лости можно сделать по виду плевральной жид­
кости. Прозрачный, слегка опалесцирующий
желтоватый экссудат будет при серозном плев
рите, геморрагический экссудат часто свидз
тельствует о карциноматозе плевры или ин
фаркт-пневмонии, мутный экссудат — об эмгзи
еме плевры. При пневмококковой эмпиеме гной
желтый, вязкий, нередко ослизненный, пр'
стрептококковой — сероватого цвета, водяш
сто-жидкий, при стафилококковой — желтьп
сливкообразный, при гнилостной — грязно
серый, с резким запахом, иногда с геморраги­
ческим оттенком, при анаэробной — зловон­
ный. Чем длительнее существует эмпиема,
тем гуще становится гной, особенно в нижних
отделах полости.
Посев экссудата обычно осуществляют на
жидкую питательную среду и ставят в термо­
стат при 37 С на сутки. Затем пересевают мате­
риал на чашки Петри с 5 °о кровяным агаром
и укладывают диски с антибиотиками. Еще через
сутки жспозиции в термостате учитывается
196
результат. Идентифицировать микрофлору мож­
но при микроскопии отдельных колоний из
чашки Петри. В хиругической практике заслу­
живает внимания метод Г. И. Богословского
(1972): пунктат засевают на чашку Петри
с 5 °0 кровяным агаром и в пробирку с сахар­
ным бульоном. Чашку и пробирку помещают
на 2—3 ч в термостат, затем тампоном или пет­
лей подсевают на чашку материал из пробирки
и сразу же размещают на агар диски с анти­
биотиками. Через 12 ч экспозиции в термостате
можно учитывать результат. Этот метод сокра­
щает срок исследования до 1 сут.
Однако бактериологические исследования
гноя нередко оказываются безрезультатными.
По данным нашей клиники, классическими мето­
дами в аэробных условиях при первом посеве
гноя из плевральной полости не получен рост
микроорганизмов у 48,3 % больных, при трех­
кратном посеве — у 37,4 °0. В таких случаях
важное значение имеет бактериоскопия мазка
из осадка экссудата при специальной окраске
его. По количеству микробов в мазке экссудата
и активности фагоцитоза можно судить о харак­
тере течения гнойного процесса, особенно при
повторных исследованиях.
Большое значение для дифференциальной
диагностики процесса по характеру экссудата
имеет цитоморфологическое исследование осад­
ка плевральной жидкости. Чаще всего в экс­
судате определяются нейтрофилы, моноциты,
лимфоциты, гистиоциты, плазматические клет­
ки, клетки мезотелия и др. При нарастающем
воспалительном процессе в плевре число лей­
коцитов экссудата увеличивается до их содер­
жания в циркулирующей крови, а при гнойном
плеврите лейкоцитоз экссудата значительно
превышает количество лейкоцитов крови. Чем
больше нейтрофилез экссудата (80 % и более
от числа всех клеток), тем более выражен вос­
палительный процесс. При нейтрофилезе свыше
90 % и значительных дегенеративных измене­
ниях клеток следует диагностировать эмпиему.
Биохимические исследования экссудата менее
информативны. Имеет значение лишь изуче­
ние содержания белков и их фракций, сахара,
электролитов, диастазы и холестерина. Однако
и эти показатели можно учитывать только при
их корреляции с данными клинического тече­
ния заболевания.
Бронхоскопия при эмпиеме является кос­
венным методом исследования. По степени
воспалительных изменений слизистой оболочки
бронхов можно судить о характере гнойно­
деструктивного процесса в легком, ориентиро­
вочно определить локализацию бронхиального
свища (по количеству гноя, аспирируемого из
доли или сегмента). Точнее можно определить
местоположение бронхиального сообщения.
если ввести в полость эмпиемы раствор мети­
ленового синего, придать больному дренажное
положение на 20—30 мин, а затем выполнить
бронхоскопию. При бронхоплевральном сообще­
нии бронхоскопия должна выполняться только
при сохраненной проходимости плеврального
дренажа.
Торакоскопия (особенно современным аппа­
ратом модели Фриделя) позволяет детально
оценить внутреннюю поверхность эмпиемной
полости, ее границы, характер плевральных на­
пластований, а также способность подлежа­
щих отделов легкого к расправлению (по под­
вижности внутренней стенки полости).
Важной задачей обследования больных эм­
пиемой плевры является установление степе­
ни функциональных нарушений дыхания и кро­
вообращения, так как это нередко имеет решаю­
щее значение в определении лечебной тактики,
особенно при выборе того или иного вида хирур­
гического вмешательства. Наиболее существен­
ными из них являются спирография, опреде­
ление газового состава крови и кислотно-основ­
ного состояния, электрокардиография и инте­
гральная реография тела по М. И. Тищенко
(1971). Уменьшение Ж ЕЛ и МВЛ при спиро­
графии более чем на 25 30 °о от дотжных
величин, снижение КИО ниже 25,0 при сни­
жении насыщения артериальной крови кислоро­
дом менее 90 % и сокращении артериовеноз­
ной разницы по кислороду требуют особого
внимания при определении показаний к слож­
ному хирургическому вмешательству.
Электрокардиография должна выполняться
у всех больных в динамике заболевания.
Интегральная реография тела позволяет
получить более информативные данные оценки
производительности сердца. В тяжелых слу­
чаях эмпиемы наблюдаются уменьшение удар­
ного объема крови, увеличение коэффициента
дыхательных изменений его [Колесников И. С.
и др., 19811.
ДИФФЕРЕНЦИАЛЬНАЯ
ДИАГНОСТИКА
ОСТРОЙ ЭМПИЕМЫ
Хотя в типичных случаях диагностика острой
эмпиемы плевры несложна, однако примерно
25—33 % больных поступают в хирургическую
клинику с ошибочным диагнозом [Струч­
ков В. И. и др., 1966; Муромский Ю. А. и др.,
1968; Лукомский Г. И., 197б|.
Трудности дифференциальной диагностики
с пневмонией обусловлены тем, что острая эм­
пиема часто является осложнением пневмонии,
протекающей с явлениями большего или мень­
шего затенения легочного поля при рентгеноло-
197
гическом исследовании. Если при этом имеется
смещение средостения в здоровую сторону,
следует думать об эмпиеме. Если же средосте­
ние не смещено (что возможно при ограничен­
ной эмпиеме), то диагностика значительно труд­
нее. При эмпиеме плевры в таких случаях чаще
можно выявить частичное выбухание и расши­
рение межреберных промежутков, локальные
боли при пальпации, ослабление голосового
дрожания, притупление легочного звука, ослаб­
ленное дыхание, усиленную бронхофонию. Иног­
да межреберные промежутки, наоборот, су­
жены и уплощены, но в отличие от ателектаза
легких средостение не смещено или слегка сме­
щено в здоровую сторону. Решающее значе­
ние в дифференциальной диагностике имеют
мног-оосевая рентгеноскопия, томография лег­
ких и пункция плевральной полости.
Трудности в дифференциальной диагностике
с ателектазом легкого возникают в связи с тем,
что и при обтурационном ателектазе бывает
выпот в плевральную полость, а компрессион­
ный ателектаз может быть следствием сдавле­
ния части легкого плевральным экссудатом.
Ведущими в диагностике являются бронхо­
скопия (при обтурационном ателектазе) и пунк­
ция плевральной полости (при компрессионном
коллапсе). В ряде случаев помогают разобрать­
ся суперэкспонированные рентгенограммы и
томограммы; при обтурационном ателектазе
периферические отделы менее интенсивно за­
тенены, чем центральные, при компрессион­
ном — интенсивность тени преобладает на пери­
ферии из-за суммации тени жидкости и слоя
поверхностного коллапса легочной паренхимы.
Иногда на суперэкспонированных рентгено­
граммах видны дополнительные линейные или
дугообразные вертикальные тени на фоне сплош­
ного затенения этой половины грудной клетки.
Наличие этого симптома дает основание исклю­
чить не только ателектаз, но и опухоли плевры.
Очень трудной является дифференциальная
диагностика ограниченной базально-пристеноч­
ной эмпиемы и ателектаза базальной пирамиды,
так как при этих состояниях нередко имеются
сходные рентгенологические признаки: затене­
ние нижних отделов грудной полости, смеще­
ние сердца в сторону поражения и подъем диа­
фрагмы. Для дифференциальной диагностики
необходимы пункция плевральной полости и
бронхоскопия.
Опухоли легких могут проявляться в виде
периферического затенения легочного поля
с переходом на грудную стенку, что может быть
поводом для ошибочного диагноза ограничен­
ной эмпиемы. При отсутствии клиники гнойного
процесса основным методом диагностики будет
трансторакальная пункционная биопсия легоч­
ной ткани.
Опухоли плевры по характеру затенения иног­
да напоминают эмпиему, особенно при большой
площади соприкосновения с грудной стенкой.
Однако при эмпиеме плевры характер тени изме­
няется при изменении положения больного.
Важное значение в дифференциальной диагно­
стике имеют анамнез и клиническая картина
заболевания: при опухоли плевры могут быть
субфебрильная температура тела и недомога­
ние, но нет выраженных признаков гнойной ин­
токсикации.
Опухоли и кисты средостения могут пред­
ставлять трудности при дифференциальной
диагностике с парамедиастинальной ограничен­
ной эмпиемой плевры. Важное место в диагно­
стике опухолей и кист средостения имеют мно­
гоосевая рентгеноскопия и томография, в неко­
торых случаях — пневмомедиастинография.
Плевральные шварты очень часто являются
поводом для предположения о наличии ограни­
ченных эмпием, особенно при сочетании с кли­
никой воспалительного процесса органов дыха­
ния. Трудно дифференцировать ограниченную
эмпиему и острый фибринозный плеврит, не­
редко развивающийся при периферических вос­
палительных очагах в легком. Диагноз уточня­
ется при пункциях плевры (нередко много­
кратных), плеврографии и бронхографии.
Абсцесс легкого, абсцедирующие пневмонии,
особенно при наличии нескольких полостей,
очень часто представляют значительные труд­
ности при дифференциальной диагностике с
острой эмпиемой плевры в связи с общностью
клинической и рентгенологической картины.
Решающее значение в дифференциальной диа­
гностике имеет бронхография: оттеснение брон­
хиальных ветвей, их деформация характерны
для эмпиемы плевры, а обрыв их у полости сви­
детельствует об абсцессе легкого.
Кисты легкого могут вызывать трудности в
дифференциальной диагностике при редко
встречающейся субплевральной локализации,
тем более, что нагноившаяся киста иногда ос­
ложняется эмпиемой плевры. В типичных слу­
чаях кисты легкого (и неспецифические, и пара­
зитарные) чаше множественные, с тонкими ров­
ными стенками, иногда с наличием обызвест­
вления.
Диафрагмальные грыжи, особенно посттрав­
матические, могут быть причиной диагностиче­
ских ошибок, так как при них в груди выявля­
ется полость или полости с уровнем жидкости,
часто пристеночно. Диагностика затруднена
именно в тех случаях, когда имеются клиниче­
ские признаки пневмонии. Однако при деталь­
ном обследовании выявляется деформация
диафрагмы, иногда дополнительные тени в груд­
ной клетке, обусловленные кишечными гаустрами, сальником. Характерно значительное из­
198
менение этих теней при исследовании на латероскопе. Основным в дифференциальной диа­
гностике является контрастное исследование
желудочно-кишечного тракта.
ЛЕЧЕНИЕ ОСТРОЙ ЭМПИЕМЫ
Лечение больных острой эмпиемой плевры
должно состоять из мероприятий местного и
общего характера.
ОБЩЕЕ ЛЕЧЕНИЕ
Дезинтоксикационная терапия в той или иной
степени показана во всех случаях, когда забо­
левание сопровождается синдромом гнойной
интоксикации. Учитывая патогенез эндогенной
интоксикации при острой эмпиеме плевры,
дезинтоксикационную терапию проводят в сле­
дующих основных направлениях.
Во-первых, она направлена на выведение из
организма токсических веществ. С этой целью
применяют обильное питье и инфузионную тера­
пию. Последняя проводится преимущественно
внутривенной инфузией изотонических раство­
ров солей, глюкозы и дезинтоксикациониых
средств (гемодеза и др.). Количество и темп
введения жидкостей устанавливают в зависи­
мости от клинического состояния больного и
волемических нарушений.
Во-вторых, она направлена на коррекцию
микроциркуляции в тканях и органах, на устра­
нение гиповолемии внутривенным введением
реологически активных низкомолекулярных
растворов типа реополиглюкина, реомакродекса и т. п. Эти препараты назначают по 500 мл
через день или ежедневно (при значительной ин­
токсикации и гиповолемии). Суточная доза их
ограничивается в связи с побочным действием.
Ускорение выведения токсических веществ
с мочой особенно эффективно достигается вве­
дением реологически активных препаратов и
форсированным диурезом. Форсированный
диурез вызывается маннитом или фуросемидом
(лазиксом). Проведение форсированного диуре­
за не всегда безопасно из-за тяжелых волеми­
ческих нарушений и возможной дезорганизации
электролитного обмена.
Следует избегать чрезмерной гиперволемии
и гипергидратации из-за опасности декомпен­
сации кровообращения с развитием отека легких,
головного мозга. Нельзя допускать также значи­
тельной гиповолемии и дегидратации с паде­
нием артериального давления в связи с опас­
ностью уменьшения диуреза вплоть до анурии,
появления флеботромбозов нз-за гемоконцент­
рации, угрожающих эмболиями сосудов малого
круга кровообращения.
За последние годы вновь больше внимания
уделяется методам внепочечного кровоочи­
щения при проведении дезинтоксикационной
терапии, в частности гемосорбции. Сорбцион­
ным методом можно удалить из крови не только
микробные токсины и микробные тела, но и
эндогенные токсины, метаболиты.
Учитывая значительные потери белков, элек­
тролитов и жидкости при тяжелых формах ост­
рой эмпиемы плевры, удовлетворительная кор­
рекция развивающихся расстройств возможна
только при использовании принципов и методов
парентерального питания. Вводятся альбумин,
протеин, плазма, свежеконсервированная кровь.
Готовые белки плазмы утилизируются организ­
мом через 16—26 дней, однако они имеют важ­
ную роль в поддержании онкотического давле­
ния в сосудистом русле и этим улучшают воз­
можности коррекции волемических расстройств.
Чаще всего используются аминокислотные
смеси (полиамин, мориамин) и белковые гидро­
лизаты (аминопептид, гидролизат казеина и др.)
из расчета 1—2 г белка на 1 кг массы тела.
Энергетические потребности обеспечиваются,
в основном, 20—40—50 % растворами глюкозы
(примерно 15—25 ккал/кг массы) в зависимо­
сти от волемических расстройств. В глюкозированные растворы обязательно добавляют
инсулин, некоторые электролиты (калнй, магний,
кальций, фосфор) и витамины для лучшего
усвоения вводимого азота и более полноценного
белкового синтеза.
Как источник энергии иногда используют
жировые эмульсии (интралипид, липофундин
и др.), этиловый спирт (1—1,5 г/кг через день
или ежедневно). Усвоение вводимого азота
повышается при использовании анаболических
гормонов (нероболил, ретаболил).
Общая антибактериальная терапия является
важным звеном комплексного лечения острой
эмпиемы плевры. Она может быть успешной
только при достаточном дренировании гнойной
полости и рациональном назначении антибак­
териальных препаратов, включая и местное, и
общее лечение, используя при этом антисеп­
тики, антибиотики и иммунные препараты.
Местное антибактериальное лечение заключа­
ется прежде всего в тщательном систематиче­
ском промывании гнойной полости антисепти­
ческими растворами с последующим внутри­
плевральным введением антибиотиков для по­
давления вегетации микроорганизмов на стенках
полости. При простой эмпиеме плевры (без
деструкции легочной тканн) этого бывает до­
статочно для достижения успеха. Однако, учи­
тывая вторичный характер подавляющего чис­
ла Эмпием плевры, в большинстве случаев
необходимо проводить и общую антибактери­
альную терапию. Большое значение имеет пра­
199
вильный подбор антибиотиков соответственно
чувствительности возбудителей гнойного про­
цесса у данного больного. Если посевы гноя
отрицательные, то оправданно назначение ан­
тибиотиков широкого спектра действия. Чаще
всего комбинируют препараты двух групп —
аминоглюкозиды (гентамицин, амикоцин, канамицин) с полусинтетическими пенициллинами
(метициллин, оксациллин, ампициллин, карбенциллин). Нередко хороший эффект можно
получить при назначении цефалоспоринов,
линкомицина.
При подозрении на анаэробную эмпиему не­
обходимо назначить антибиотики пеницилли­
нового ряда, левомицетин, линкомицин в зави­
симости от вида возбудителя. Так, пептококки,
пептострептококки, фузобактерии в большин­
стве случаев чувствительны к пенциллину, лево­
мицетину, цефалоспоринам, клиндамицину,
линкомицину, менее чувствительны к эритро­
мицину и тетрациклину, не чувствительны к
аминоглюкозидам и полипептидам (полимик­
син, колимицин). Бактероиды чувствительны к
левомицетину, линкомицину, клиндамицину,
карбенициллину и доксициклину, в меньшей сте­
пени — к тетрациклинам и цефалоспоринам,
не чувствительны к пенициллинам, аминоглю­
козидам и полипептидам (Ивченко В. Н., Мель­
ник В. М., 19831. При анаэробной эмпиеме дока­
зана необходимость назначения метронидазола,
обладающего бактерицидным действием на боль­
шинство анаэробов, за исключением коринебактерий, актиномицетов. Препарат назначают
по 500 мг 3—4 раза в день [Вишневский А. А.
и др., 1980; Сажин В. П. и др., 19811. Таким же
действием обладают тинидазол или орнидазол.
Чаще всего курс лечения избранной комбина­
цией антибиотиков продолжают 5—7 дней. При
отсутствии эффекта необходимо сменить анти­
биотики, обязательно учитывая при этом резуль­
таты повторных бактериологических исследо­
ваний.
Важное значение в общей антибактериаль­
ной терапии имеет назначение иммунных пре­
паратов. Начинают с пассивной иммунизации
введением поливалентного иммуноглобулина.
Препарат вводят внутримышечно по 3 мл через
1 —2 дня, всего 3—5 инъекций. Б. В. Петровский
и Ч. С. Гусейнов (1971) рекомендуют вводить
иммуноглобулины по 12—15 мл (0,2 мл/кг мас­
сы тела) с повторными инъекциями через 2 нед,
так как этот срок введенный у-глобулин сохра­
няется в циркулирующей крови. При значитель­
ной недостаточности антител в крови по рекомен­
дации Комитета экспертов ВОЗ (1068) у-глобулин можно вводить по 1,2—1,8 мл/кг массы
внутримышечно один раз в месяц. При под­
тверждении стафилококковой этиологии эмпие­
мы хороший эффект можно получить введением
антистафилококкового у-глобулина. При сме­
шанной инъекции его необходимо вводить со­
четанно с антибиотиками. Доказано также, что
введение у-глобулина, кроме пассивной имму­
низации, способствует стимуляции факторов
неспецифического иммунитета, в том числе
усилению фагоцитарной активности лейкоци­
тов, увеличению титра лизоцима и комплемен­
тарной активности [Земскова М. В. и др., 1969;
Голосова Т. В. и др., 1974].
Хорошими средствами пассивной иммуниза­
ции являются специфическая гипериммунная
плазма и бактериофаги. Известны антистафилококковая плазма, аитисинегнойная плазма
и плазма с повышенным содержанием антител
к протею. Антистафилококковую плазму при
острой эмпиеме переливают по 200—250 мл че­
рез 1—2 дня, .3—5 раз.
Известно, что пассивная иммунизация может
подавлять выработку собственных иммуногло­
булинов. Поэтому ее необходимо подкреплять
активной иммунизацией. Так, при стафилоккоковой эмпиеме введение стафилококкового
анатоксина способствует выработке специфи­
ческих антитоксинов (антистафилолизина,
антигиалуронидазы и др.).
Используют сокращенную схему из трех инъ­
екций анатоксина: 0,5—1 мл с интервалом 2—3
дня. По данным В. Г. Ус (1972), Л. Н. Сидареико
и соавт. (1972), титр антитоксинов повышался
в 4 раза.
Активная иммунизация аутовакциной, при­
готовленной из возбудителя, применяется реже
из-за трудности получения препарата.
При проведении иммунотерапии необходимо
учитывать состояние иммунобиологической
реактивности больного. При гиперреактивно­
сти, о чем свидетельствуют в том числе и высо­
кие титры изогемагглютининов, О-стрептолизина и иммуноглобулинов, показаны десенсиби­
лизирующая терапия, введение прогестерона.
При пониженной реактивности больного неред­
ко, наряду с проведением пассивной и активной
иммунизации, показана стимуляция Т-системы
иммунитета и неспецифических защитных сил
организма. Чаще всего это достигается вве­
дением декариса (левамизола), тимизола, леокадина.
Большое значение в коррекции иммунных
нарушений имеют переливание свежеконсер­
вированной крови или прямые гемотрансфузии,
а также нормализация белковых и волемиче­
ских расстройств.
При лечении дыхательной недостаточности
особое внимание уделяется санации бронхиаль­
ного дерева путем ингаляций, стимуляции
откашливания, промывания бронхиальных пу­
тей. Снятие болей при дыхании достигается
с помощью ненаркотических анальгетиков,
200
снятие спазма легочных артериол — введением
эуфиллина, папаверина, но-шпы и др. Для по­
вышения парциального давления кислорода во
вдыхаемом воздухе производится инсуффляция
увлажненного кислорода через носоглоточные
катетеры. За последние годы доказана высокая
эффективность гипербарической терапии, так
как при этом увеличивается количество раст­
воримого в плазме кислорода до 6 об%, что
полностью удовлетворяет все физиологические
потребности организма в кислороде даже при
значительной сопутствующей анемии.
Исследования В. И. Буравцева, проведенные
в клинике госпитальной хирургии, показали,
что оптимальным является 6—7 сеансов.
Общеукрепляющая и симптоматическая те­
рапия при острой эмпиеме плевры включает
полноценное питание, уход за больным, меро­
приятия по лечению сопутствующих заболева­
ний и предупреждению возможных осложне­
нии
МЕСТНОЕ ЛЕЧЕНИЕ
Современные способы лечения острых эмпием
плевры можно кратко представить в виде сле­
дующей схемы:
после удаления гноя полость заполняется анти­
септическим раствором, и сразу же раствор вме­
сте с остатками гнойного экссудата аспириру­
ется обратно. Количество раствора, вводимого
одномоментно в плевральную полость, зависит
от методики промывания и размеров полости,
что определяется количеством удаленного гноя.
Чаще всего вводят 20—60 мл раствора шпри­
цем, несколько меняя направление иглы, чтобы
струей раствора механически омывать доступные
стенки полости. При такой методике нередко
аспирируется не только жидкий гной, но и мно­
гочисленные хлопья фибрина и детрит, имбибированные микроорганизмами. Чередование
введения раствора в полость и аспирации его
повторяют до получения почти чистой жидко­
сти.
При больших размерах гнойной полости про­
мывание может быть эффективным, если ис­
пользовать методику санации «в две иглы»,
принцип которой предложен еще в (896 г. рус­
ским врачом С. В. Левашовым: после рентгено­
логического контроля пунктируют плевру у дна
полости и второй иглой в максимально верхнем
отделе ее. Через нижнюю иглу полость заполня­
ется антисептическим раствором до тех пор,
пока из верхней открытой иглы после выхож-
Консерватисное лечение
Систематические пленральпые пункции с аспирацией гноя,
иромыканием полости, введением фибринолитических
и антибактериальных средств
Оперативное лечение
Удаление очага инфекции и ликвидация полости:
Дренирование плевральной полости:
закрытое:
активное
пассивное
открытое:
с резекцией ребра
без резекции ребра
декортикация и цлецрэктомия
сочетание декортикации легкого с дополнительными вмешатель­
ствами
плевройневмонэктом ия
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Наиболее простым и доступным методом
санации плевральной полости при эмпиеме яв­
ляется пункция. Аспирация гноя из полости
должна быть максимально полной. При этом
важно установить наличие или отсутствие ва­
куума в плевральной полости. В сомнительных
случаях проводится манометрия с помощью
пневмотораксного аппарата. При отсутствии
легочно-плевральных сообщений пункционная
санация гнойной полости в большинстве слу­
чаев весьма эффективна, особенно при ранних
и систематических пункциях.
Предложено несколько методик санации про­
мыванием плевральной полости (при отсутствии
плевролегочного сообщения). Как правило,
дения воздуха не станет поступать промыаная
жидкость. Этим устраняется воздушная подуш­
ка и достигается контакт антисептического
раствора со всеми стенками гнойной полости.
Затем краник верхней иглы закрывают, а через
нижнюю промывную жидкость аспирируют
шприцем или электроотсосом. Такую процедуру
повторяют несколько раз, используя при этом
до 5—6 л раствора.
Для промывания полости эмпиемы применя­
ются различные антисептические растворы,
допустимо также использовать изотонический
раствор натрия хлорида. При подтверждении
этиологии эмпиемы плевральную полость луч­
ше промывать антисептиками с учетом чув­
ствительности возбудителя к ним. Чаще всего
используют фурацилин (0,02 % раствор), со-
201
лафур (0,1 %), диоксидин (1 %), хлоргексидина биглюконат (0,02 %). борную кислоту (3—
5 %), перманганат калия, йодннол, димексид,
раствор Дакена.
В конце пункции необходимо стремиться
наиболее полно аспирировать промывной раст­
вор, создать вакуум в плевральной полости с
целью максимально возможного расправления
коллабированных отделов легкого. Пункция
завершается введением в остаточную полость
антибиотиков иногда вместе с 50—70 % димексидом, который способствует проникновению их
в имбнбированные гноем фибринные напласто­
вания на стенках полости и потенцирует дей­
ствие антибактериальных средств {Данилен­
ко М. В. и др., 1977].
Для достижения успеха пункционная сана­
ция плевральной полости должна проводиться
ежедневно в первые 5—7 дней, затем через 1 —
2 дня. Последующие контрольные пункции дела­
ют в зависимости от данных клинического и
рентгенологического обследования.
Возможности пункционной санации плев­
ральной полости при острой эмпиеме значитель­
но расширились в связи с применением совре­
менных протеолитических ферментов, особенно
при гнойно-фибринозном плеврите и нагноении
свернувшегося гемоторакса. Стала возможной
так называемая биохимическая декортикация
легкого [Громова Л. С., 1959; Rross W., Gar­
binski J., 19521.
Известны многочисленные сообщения об ус­
пешном применении стрептазы, фибринолизи­
на, препаратов трипсинового ряда в санации
плевральной полости. Наши экспериментальные
и клинические исследования доказали высокую
эффективность отечественного препарата террилитина при свернувшемся гемотораксе и гной­
но-фибринозном плеврите [Чепчерук Г. С. и др.,
19811 - Препаратами выбора для местной фибри­
нолитической терапии при острой эмпиеме яв­
ляются террилитин и стрептокиназа. Эти про­
теолитические ферменты обладают значительно
большей активностью, чем фибнинолизин, трип­
син, химотрипсин и рибонуклеаза.
Ферменты вводят в полость после аспирации
гноя и промывания антисептическими раство­
рами. Дозы препарата подбираются в зависи­
мости от предполагаемого количества сгустков
в полости. Террилитин обычно вводят по 600—
1000 ПЕ, стрептазу (стрептолиазу) — по 250—
500 тыс ЕД, фибринолизин — по 20—40 тыс ЕД,
препараты трипсинового ряда — до 100—150 мг.
Фермент разводится антисептическим раство­
ром, в который добавляется суточная доза из­
бранного антибиотика.
На следующий день во время очередной пунк­
ции аспирируют образовавшуюся от лизиса
сгустков жидкость, промывают плевральную
полость и при необходимости вводят фермент
и антибактериальные препараты повторно. Чаще
всего достаточно 2—3 внутриплевральных вве­
дений протеаз.
Следует отметить, что лизис сгустков иногда
усиливает резорбцию токсических продуктов
нз плевральной полости, что сопровождается
нестойким повышением температуры тела,
ознобом. После повторного промывания гной­
ной полости эти явления проходят. Исследова­
ния, проведенные в клинике госпитальной хи­
рургии, показали, что внутриплевральное вве­
дение ферментов сопровождается повышением
протеолиза плевральной жидкости в 2—3 раза
по сравнению с циркулирующей кровью. Повы­
шения протеолитической активности крови не
наблюдается. Число лейкоцитов плеврального
экссудата после лизиса сгустков в полости резко
увеличивается, и повышается их фагоцитарная
активность. Повторные посевы плевральной
жидкости чаще всего оказываются стерильными,
однако у 10 % больных, у которых до введения
препарата посевы плеврального экссудата были
стерильны, после лизиса сгустков в аспирируе­
мой из полости жидкости находили микроор­
ганизмы, вероятно, освободившиеся из фибри­
нозно-гнойных напластований.
Результаты санации полости с использованием
протеаз при острой эмпиеме плевры тем лучше,
чем раньше начата местная фибринолитиче­
ская терапия. При нагноившемся посттравма­
тическом и послеоперационном свернувшемся
гемотораксе оптимальным сроком для приме­
нения ферментов является 4—10-й день. Введе­
ние ферментов в первые дин после операции
нежелательно из-за опасности развития повтор­
ного кровотечения в полости. В то же время в
более отдаленные сроки (через 3—4 нед) полу­
чить полный лизис сгустков трудно из-за их
уплотнения н организации. Но даже в этих слу­
чаях террилитин или препараты стрептокиназы
растворяют рыхлые гнойно-фибринозные массы
на шварте, содержащие, как правило, патогенную
микрофлору. Аспирация образующейся жидко­
сти и промывание полости антисептическими
растворами с последующим введением анти­
биотиков приводили к санации полости, а остав­
шиеся фибринозные напластования на плевре
постепенно рассасывались самостоятельно или
под воздействием физиотерапевтических про­
цедур. Нарушения внешнего дыхания у этих
больных постепенно уменьшались, показаний
к оперативному лечению, как правило, не воз­
никало.
Осложнения при плевральной пункции на­
блюдаются редко. Наиболее опасными из них
являются воздушная эмболия, повреждения
легкого, крупных сосудов, сердца, диафрагмы
и органов брюшной полости.
202
К осложнениям пункций гнойной плевраль­
ной полости следует отнести нагноение грудной
стенки, что чаще встречается при гнилостной
эмпиеме. С целью подавления развития инфек­
ции по ходу пункционного канала для анестезин
используется анестетик на антисептическом
растворе или же при извлечении иглы вводится
небольшое количество раствора антибиотиков.
Профилактической мерой является создание
отрицательного давления в плевральной полости,
так как при положительном давлении инфициро­
ванное содержимое полости может поступать
в ткани грудной стенки через поврежденную
париетальную плевру.
К ошибкам пункционной санации полости
следует отнести неоправданно длительное лече­
ние только этим методом, когда не удается рас­
править легкое, а скопление гноя в интервалах
между пункциями отягощает состояние боль­
ного, поддерживая признаки гнойной интокси­
кации, введение антибиотиков может способ­
ствовать избыточному развитию грануляций
на висцеральной плевре, которые как бы «ин­
капсулируют» коллабированное легкое. Поэто­
му при отсутствии отчетливой тенденции к рас­
правлению легкого периодическими пункциями
уже через 5—7 дней следует ставить вопрос
о показаниях к активному дренированию.
ОПЕРАТИВНОЕ ЛЕЧЕНИЕ .
Оперативные методы лечения острой эмпие­
мы плеары применяются, как правило, после
консервативного лечения пункциями. Показа­
ниями к оперативным вмешательствам, наряду
с безуспешностью применения метода пунк­
ционной санации в течение 5—7 дней, явля­
ются: 1) острая эмпиема плевры с деструкцией
легочной ткани и бронхоплевральным сообще­
нием; 2) тотальная эмпиема с резкой гнойной
интоксикацией; 3) длительное (2—3 мес) суще­
ствование острой эмпиемы с угрозой перехода
в хроническую.
Во всех случаях оперативное лечение острой
эмпиемы плевры начинается с дренирующих
вмешательств. Дренирование гнойной плевраль­
ной полости позволяет удалять гной из плевраль­
ной полости постоянно, а не периодически, как
при пункционной санации, фракпионно или
постоянно промывать антисептиками, вводить
антибиотики, создавать разрежение с помощью
вакуумных устройств.
Известны несколько методик дренирования
плевральной полости. Наиболее часто исполь­
зуется торакоцентез при помощи троакара по
Бюлау, являющийся простым и малотравматич­
ным.
При торакоцентезе и дренировании плевраль­
ной полости в избранном месте грудной стенки,
соответствующем нижнему отделу гнойной по­
лости, делается пробная пункция. В месте пунк­
ции делается небольшой разрез кожи, через
который в плевральную полость вводится троа­
кар. Прохождение инструмента в полость ощу­
щается в виде «провала», после чего стилет
троакара удаляется, а через трубку в плевраль­
ную полость вводится дренаж с 1—2 боковыми
отверстиями. Трубку троакара удаляют, при­
держивая дренаж. Положение дренажа и его
функцию контролируют пробной аспирацией
шприцем Жане и после этого фиксируют его
к коже.
Введение дренажа с помощью троакара обес­
печивает достаточно длительное сохранение
герметичности плевральной полости, так как
рана грудной стенки соответствует диаметру
трубки. При отсутствии троакара большого
диаметра (трудные условия работы врача) дре­
нажную трубку можно провести в плевральную
полость с помощью длинного изогнутого кро­
воостанавливающего зажима.
Методика с резекцией участка ребра для дре­
нирования плевральной полости применяется
крайне редко, лишь при очень узких межре­
берных промежутках. Некоторые хирурги после
резекции ребра производят малую торакото­
мию, очищают гнойную полость от сгустков кро­
ви, фибрина, секвестров, после этого полость
дренируют, а рану ушивают до дренажа. Не­
достатком этого метода является почти не­
избежное нагноение раны грудной стенки во­
круг дренажа с нарушением герметичности
плевральной полости. Иногда развивается остео­
миелит ребра, что значительно затрудняет
дальнейшее лечение. Однако одномоментная
санация гнойной полости под контролем зре­
ния весьма привлекательна.
При необходимости длительного дренирования
гнойной полости большое значение имеет ма­
териал, из которого изготовлены дренажные
трубки. Наиболее выгодны силиконовые дре­
нажи, так как они не обладают реактогенными
свойствами по отношению к тканям организма,
в связи с чем значительно реже развивается
нагноение раны грудной стенки вокруг дре­
нажной трубки. Еще выгоднее использовать
для длительного дренирования специальные
многоканальные креминйорганические медицин­
ские трубки, выпускаемые отечественной про­
мышленностью (рис. 102).
Решающее значение в эффективности лече­
ния острой эмпиемы закрытым дренированием
имеет активная аспирация с помощью различ­
ных вакуумных устройств. Чаще всего исполь­
зуются различные электроотсосы, рассчитан­
ные на длительную непрерывную работу. Наибо­
лее доступным из них является переоборудо­
ванный микровиброкомпрессор, позволяющий
203
Рис. 102. Двухпросветныс кремнийоргаиические медицин­
ские трубки с диаметром широкого просвета 6. 8 и 11 мм.
создать разрежение до 80 мм рт. ст. Очень удоб­
ным является специальный отсасыватель ОП-1
(Лавринович Л. Л., 1978] с регулируемым раз­
режением от 20 до 120 см вод. ст. и индикато­
ром, позволяющим судить о наличии или отсут­
ствии вакуума в плевральной полости. В ус­
ловиях специализированного стационара луч­
шей вакуумной установкой является центра­
лизованная система с электромотором (компрес­
соры Казанского завода медоборудования) и ин­
дивидуальными вакуумметрами у постели боль­
ного. Она обеспечивает вакуум от 15 до 800 мм
рт. ст.
Степень разрежения, необходимого при ак­
тивной аспирации для расправления легкого,
зависит от сроков заболевания, наличия и вели­
чины бронхоплевральных сообщений. При гер­
метичной плевральной полости обычно доста­
точно создать вакуум около 50 мм рт. ст. Если
коллабированные отделы легкого покрыты фибринными напластованиями, но еще сохраняют
способность к расправлению, ликвидировать
остаточную полость можно при разрежении до
150 мм рт. ст., причем требуется длительная
непрерывная аспирация экссудата, периоди­
чески разжижаемого протеолитическими фер­
ментами в антибактериальных растворах.
Для первых промываний полости, когда не­
известен возбудитель гнойного процесса, при­
меняются любые растворы, в том числе изото­
нический раствор натрия хлорида или стериль­
ная кипяченая вода. Основная задача первых
промываний состоит в удалении гноя и детри­
та. Некоторые авторы [Чистихин В. С. и др.,
1973| используют для этого до 7—9 л раствора
в сутки. В последующем при уточнении этио­
логии эмпиемы используются антисептические
растворы целенаправленно с учетом чувстви­
тельности микрофлоры. Так, при гнилостной
эмпиеме чаще применяются раствор перман­
ганата калия, раствор Дакена и другие дезодо­
ранты в сочетании с совместимыми антибио­
тиками и протеолитическими ферментами. При
обнаружении стафилококков, стрептококков,
кишечной палочки чаще используют 0,1 % раст­
вор солафура, 1 % раствор диоксидина, йодинол.
На стафилококк хорошо действует 0,25 % раст­
вор хлорфиллипта. При синегнойной эмпиеме
применяют 3—5 % раствор борной кислоты,
1 % раствор диоксидина, 0,02 % раствор хлоргексидина биглюконата. При длительном лече­
нии полезно практиковать смену антисептиков,
используемых для промывания.
Промывание гнойной полости шприцем Жане
является весьма эффективным методом ее сана­
ции, так как через дренаж удается аспирировать
не только жидкость, но и множество имбибированных гноем фибриниых хлопьев, детрит.
Однако промывание 1-—2 раза в сутки при пас­
сивном дренировании между промываниями
часто не может обеспечить расправление лег­
кого.
Более эффективными являются фракцион­
ное промывание и непрерывная аспирация через
двухпросветную дренажную трубку. Схема та­
кого промывания плевральной полости с ис­
пользованием двухпросветного дренажа и ва­
куумного устройства ОП-1 представлена на
рис. 103. Через узкий просвет двухпросветного
дренажа (1) при закрытом широком просвете
ниже переходной трубки (2) плевральная по­
лость капельно заполняется антисептическим
раствором примерно наполовину ее объема.
Во время экспозиции, которая длится 30—
60 мин (при добавлении протеаз — около 3 ч),
больной осторожно меняет положение в постели
для перемещения воздуха в полости и обеспе­
чения контакта раствора со всеми стенками
ее. После этого дренаж открывается и содер­
жимое аспирируется. Такие промывания про­
должаются многократно до получения относи­
тельно чистого раствора из полости. После та­
кого сеанса продолжается постоянная активная
аспирация.
Фракционное промывание позволяет удалить
гной, очистить и стерилизовать стенки полости,
а непрерывная активная аспирация способ­
ствует расправлению легкого и ликвидации
остаточной плевральной полости. За последние
годы благодаря разработке отечественного ко­
мандного электромеханического программного
устройства (КЭП-12-У) стали применять авто­
матическое промывание гнойных полостей через
двухпросветный дренаж до 48 раз в сутки (Каншин Н. П., 1983]. Такие промывания с помо­
щью автоматизированной системы позволяют
в короткие сроки очистить полость эмпиемы.
Критериями эффективности санации гнойной
полости при эмпиеме являются клинические
204
Рис. 103. Промывание плевральной полости через двупро­
светный дренаж с использованием вакуумного устройства
ОП-1.
данные (снижение температуры тела, умень­
шение или полное исчезновение признаков гной­
ной интоксикации), стерильность плеврального
экссудата при повторных бактериологических
исследованиях и уменьшение лейкоцитоза
экссудата. Продолжительность дренирования
зависит от эффективности такой санации у дан­
ного больного и темпа расправления легкого.
Результаты лечения можно считать хорошими,
если инфекционный процесс в плевре ликвиди­
рован или резко подавлен, а легкое распра­
вилось полностью или остается небольшая оста­
точная полость, объемом не более 20—40 мл.
Дренаж в таких условиях можно удалить с гер­
метичным ушиванием раневого канала. Дальней­
шая судьба такой остаточной полости, как пра­
вило, благоприятная с исходом в ограниченный
фиброторакс.
Промывание полости при острой эмпиеме
без бронхиального свища с последующей по­
стоянной активной аспирацией ведет к выздо­
ровлению примерно в 60—90 % случаев (Мас­
лов В. И., 1976; Уткин В. В., Башко Я. Я., 1978;
Королев Б. А. и др., 1980]. При наличии легочно­
плевральных сообщений или бронхиального
свища активное дренирование плевральной по­
лости может стать окончательным методом лече­
ния только у 20- 25 % больных (Сергеев В. М.,
1967]. В остальных случаях этим методом уда­
ется значительно быстрее подготовить больных
к более сложным вмешательствам.
Одним из методов санации плевральной поло­
сти при острой эмпиеме с пнопневмотораксом
в случаях со стойким бронхоплевральиым сооб­
щением является искусственная герметизация
бронхиального дерева [Гераськин В. А. и др„
1974; Rafinski R., 1968].
Временная окклюзия бронхов выполняется
во время бронхоскопии под наркозом. В каче­
стве пломбы для окклюзии используется поро­
лоновая губка или специальная коллагеновая
саморассасывающаяся пломба отечественного
производства. Герметизация бронхиального
дерева позволяет в ряде случаев провести эф­
фективную санацию гнойной полости методом
фракционного лаважа с непрерывной активной
аспирацией через двухпросветный дренаж. Пос­
ле 2—3-дневного интенсивного промывания
полости эмпиемы продолжается только актив­
ная аспирация с разрежением около 120—150 мм
рт. ст., иногда до 400—500 мм рт. ст.
Проведенные в нашей клинике исследования
(Гришаков С. В. и др., 1983] показали, что уже
в первые часы после временной окклюзии брон­
ха улучшается насыщение артериальной крови
кислородом, уменьшается парциальное напря­
жение СОу, уменьшается дефицит оснований.
Окклюзия пораженного бронха создает усло­
вия для закупорки периферических отделов
бронхиального дерева слизью, фибрином, а так­
же для образования сращений пораженных
отделов легкого с париетальной плеврой и лик­
видации плевральной полости.
Временную окклюзию бронха сохраняют
др 2 3 нед. Признаков обострения гнойного
процесса в плевре и легком в связи с окклю­
зией обычно не наблюдается. Нередко имеется
повышение температуры тела, что обусловлено,
вероятно, повышенной резорбцией из бронхов
герметизированной доли. Удаление пломбы
производится при бронхоскопии и обязательно
сопровождается тщательной санацией бронхи­
ального дерева. После этого температура тела
обычно нормализуется. Активную аспирацию
из плевральной полости через дренаж сохраняют
еще 2—3 дня, затем выполняют плеврографию
и, убедившись в расправлении легкого, дренаж
удаляют. Раневой канал герметизируется
одним — двумя швами.
Безуспешное лечение дренированием бывает
при значительных бронхиальных свищах, обыч­
но большого диаметра.
205
Формирование остаточной полости эмпиемы
может быть обусловлено несколькими причи­
нами. К ним относятся ошвартование коллабированных отделов легкого плотными орга­
низованными фиброзными массами, не под­
дающимися литической терапии, значительное
уплотнение и склероз легочной ткани, несоот­
ветствие объемов резецированного легкого и
плевральной полости, ателектаз части легкого
из-за обструкции бронхиального дерева сли­
зью, детритом. Когда расправить легкое из-за
этого изложенными выше методами не уда­
ется, возникает вопрос о показаниях к опера­
тивному лечению: декортикации легкого, то­
ракопластике или мышечной пластике остаточ­
ной полости. Следует отметить, что декортика­
ция не всегда возможна в связи с плотными
сращениями фиброзных напластований с вис­
церальной плеврой. Иногда и после декортика­
ции не удается расправить легкое из-за выра­
женных склеротических изменений его. Пока­
зания к торакопластике, операции травматич­
ной и резко деформирующей грудную клетку,
за последние годы значительно сужены [Земс­
ков Н. Н. и др., 1979; Слепуха М. М., Мель­
ник В. М., 1982; Чухриенко Д. П., 1982]. Мы­
шечная пластика возможна лишь при наличии
хорошо развитых мышц рядом с остаточной
полостью эмпиемы.
Более перспективным нам представляется
использование биологической пломбы, приго­
товленной из раствора фибриногена. Возмож­
ность такой пломбировки подсказана наблюде­
ниями за судьбой плевральной полости после
пневмонэктомии. Как известно, полость в таких
случаях постепенно заполняется экссудатом,
из которого выпадет фибрин на стенках поло­
сти и в виде лентовидных спаек, пересекающих
остаточную полость. Организация экссудата
с утолщением фибринных пленок и наслоений
фибрина на стенках приводит в различные сро­
ки (от 2*/г до 12 мес по данным Б. Э. Абарбанель, 1962) к формированию фибриноторакса.
В дальнейшем происходит прорастание фибро­
бластов из стенок полости и преобразование
фибрина в глыбчатый коллаген [Есипова И. К.,
Рыжков Е. В., 1957]. Эти наблюдения, а также
проведенные нами экспериментальные исследо­
вания позволили Г. С. Чепчеруку применить
фибринную пломбу для заполнения стойкой
остаточной плевральной полости у 24 больных:
7 из них перенесли эмпиему после пневмонэкто­
мии, у 5 была эмпиема после частичных резек­
ций легкого, у 2 — эмпиема после ранений гру­
ди и у 8 — постпневмоническая эмпиема плев­
ры. У всех больных после санации эмпиемы
сформировалась стойкая остаточная полость,
которая была заполнена антибактериальной
фибринной пломбой. Для предупреждения ре­
цидива эмпиемы фибриноген растворяли анти­
септическим раствором (солафур, диоксидин)
и добавляли большие дозы антибиотиков с уче­
том чувствительности высеваемых ранее у это­
го больного микроорганизмов (рационализа­
торское предложение № 4620 от 21.09.81 г.).
Методика пломбировки состоит в следующем.
1 г лиофилизированного фибриногена, выпу­
скаемого отечественной медицинской промыш­
ленностью, растворяют антисептическим раст­
вором. Пункционно через две иглы или через
дренаж и иглу (нгла в верхнем отделе полости
необходима для удаления воздуха) остаточную
полость полностью заполняют раствором фибри­
ногена, затем вводят высшие суточные дозы 2—3
антибиотиков с учетом антибиотикограммы и
после этого — тромбинкальциевую смесь 125
ЕД тромбина и 10 мл 10% раствора кальция
хлорида.
Раствор фибриногена свертывался, и в оста­
точной полости оставалась антибактериальная
фибринная пломба.
Оценка отдаленных результатов (от 3 мес до
3 лет) показала, что при применении антибак­
териальной фибринной пломбы у 19 из 24 боль­
ных удалось ликвидировать остаточную плев­
ральную полость и предупредить рецидив эм­
пиемы. У 5 больных фибринная пломба в по­
следующем нагноилась. Причиной рецидива
эмпиемы плевры у трех больных была вторич­
ная несостоятельность культи бронха, а у двух,
вероятно, недостаточная санация стенок полости
от фибринозно-гнойных напластований перед
пломбировкой. Анализ наших наблюдений поз­
воляет сделать заключение, что важнейшими
условиями успешного применения антибакте­
риальной фибринной пломбы для ликвидации
стойкой остаточной полости и предупреждения
рецидива эмпиемы плевры являются тщатель­
ная санация стенок полости и ликвидация брон­
хоплеврального свища.
Следует подчеркнуть простоту и безопасность
этого метода пломбировки стойкой остаточной
плевральной полости. Применение раствора
фибриногена с большими концентрациями ан­
тибактериальных средств позволяет заполнить
полость даже через пункционную иглу с после­
дующим свертыванием его и формированием
фибринной пломбы с депо антибиотиков. В слу­
чае рецидива эмпиемы не требуется повторного
оперативного вмешательства для удаления
пломбы, а необходимо лишь введение протео­
литических ферментов для лизиса фибрина и
санации полости с целью подготовки к повтор­
ной пломбировке или же к торакопластике.
К оперативным методам относится открытое
дренирование плевральной полости. Сущность
заключается в искусственном создании стой­
кого торакального свища с целью быстрейшей
206
очистки гнойной полости, расправления легкого
или подготовки к радикальному оперативному
вмешательству (Л. С. Лесницкий и др., 1987).
Известны различные методы открытого дре­
нирования плевральной полости. Дренирова­
ние без резекции ребра в настоящее время не
применяется из-за быстрого закрытия раневого
дефекта сближающимися ребрами.
Открытый дренаж с резекцией одного или
нескольких ребер был предложен W. Roser
(1859) и F. Konig (1864) и получил широкое
распространение. По сводным данным В. М. Сер­
геева (1967), с внедрением этого метода уда­
лось сократить летальность при острой послео­
перационной эмпиеме с 80—90 % до 15—30 %.
Однако все еще высокая летальность и большое
число (свыше 20 %) хронических эмпием с
незаживающими торакальными свищами зна­
чительно сократили показания к открытому
дренированию плевральной полости. В настоя­
щее время это вмешательство при острой эм­
пиеме производится в основном по жизненным
показаниям при распространенном нагноительном процессе в плевре и легком, когда предва­
рительными пункциями и активным закрытым
дренированием не удалось очистить полость
от гноя и уменьшить явления гнойной инток­
сикации, а радикальное вмешательство крайне
рискованно из-за тяжести состояния больного.
В связи с наличием бронхиального свища и
опасностью аспирации гноя из полости в дру­
гое легкое торакостомия нередко выполняется
в положении больного сидя под внутривенным
обезболиванием (рис. 104). Разрезом длиной
12—15 см между средней подмышечной и лопа­
точной линиями у дна гнойной полости обна­
жается и поднакостнично резецируется участок
ребра (чаще VIII или IX) длиной до 10 см.
Небольшим разрезом через ложе ребра вскры­
вают полость эмпиемы, аспирируют гной, про­
мывают полость, предохраняя от загрязнения
рану мягких тканей. После промывания поло­
сти рассекают реберное ложе н утолщенную
париетальную плевру. Стенки полости эмпиемы
вторично промывают, удаляют детрит, секвест­
ры, фибринные сгустки. Затем стенки осторож­
но выскабливают острой ложкой Фолькмана
при наличии значительных фибринозно-гной­
ных напластований. Для формирования доста­
точного торакального свища край надкостницы
ребра подшивают к фасции [Clagett J., Gera­
ci J., 19631 или к коже (Маслов В. И., 1976].
Последнее предложение выгоднее, так как поз­
воляет лучше изолировать рану мягких тка­
ней от прямого контакта с гноем. Нередко торакостома получается очень узкая, щелевидная.
Поэтому при большой гнойной полости откры­
тое дренирование будет эффективнее, если ре­
зецировать фрагменты двух, иногда трех ребер
Рис. Ю4. Положение больного на операционном столе цля
выполнения торакостомии.
Рис. 105. Сформированная торакостома у больного с эмпие­
мой и свищом культи бронха после пневмонэктомии.
(рис. 105). В таких случаях ткани межребер­
ного промежутка между резецированными реб­
рами иссекаются как при операции Коннорса
[Connors J., 1931]. Наши наблюдения показы­
вают, что оперативное закрытие широкого плев­
рокожного свища, планируемое заранее, в по­
следующем производится так же, как и после
торакостомии с резекцией одного ребра. Реко­
мендуемая Eloesser (1935), Р. Symbas и соавт.
(1971) торакостомия с подшиванием кожноподкожно-фасциального лоскута к диафрагме
и внутригрудной фасции не имеет преимущеществ. В то же время она более травматична
и ликвидировать ее технически труднее.
207
Преимуществами открытого дренирования
являются техническая простота и возможность
эффективной санации гнойной полости даже
у тяжелобольных.
Ведение больных с торакостомией может
быть разным. Чаще всего в первые дни дела­
ются ежедневные перевязки, промывания поло­
сти антисептическими растворами. Хороший
эффект дают ультразвуковая обработка с про­
теолитическими ферментами, тампоны с полиэ­
тиленгликолем. Стенки полости очищаются,
а под воздействием дыхательной гимнастики
легкое частично расправляется, остаточная по­
лость уменьшается. Через 2—3 нед больного
можно выписать иа амбулаторное лечение.
Постепенно стенки полости покрываются гра­
нуляциями.
Показания к ликвидации торакального сви­
ща обычно ставят через 1—2 мес [Подзо­
лов В. В., 1963; Clagett J., Geraci J., 1963]. Края
свища иссекают и рану грудной стенки послой­
но ушивают. Остаточную полость эмпиемы, если
нет бронхиального свища, ведут пункционно­
аспирационным способом до формирования
ограниченного фиброторакса.
Некоторые хирурги после торакотомии с ре­
зекцией ребра применяют тампонаду полости
по А. В. Вишневскому (1938): полость запол­
няют масляно-бальзамическими тампонами,
которые меняют через 2 нед. Постепенно полость
уменьшается, количество тампонов уменьша­
ют и так продолжают длительное время до вы­
полнения полости грануляциями с последую­
щим развитием фиброзной ткани.
Открытое дренирование плевральной полости
имеет ряд существенных недостатков: наличие
открытого пневмоторакса иногда ведет к уве­
личению коллапса легкого и флотированию
средостения, особенно при торакостомии в ран­
ней стадии острой эмпиемы; постепенно легкое
фиксируется швартами в спавшемся состоянии,
что ведет к плеврогенному склерозу легочной
паренхимы; операция не обеспечивает быстрого
расправления легкого, требует длительного
лечения и повторных оперативных вмешательств;
торакостомия малоэффективна при продолжаю­
щемся деструктивном процессе в легком. Имен­
но поэтому показания к открытому дрениро­
ванию гнойной плевральной полости весьма
ограниченны. Торакостомию следует рассмат­
ривать не как самостоятельный метод лечения,
а как временный и очень важный этап, спасаю­
щий жизнь больных в тех случаях, когда кон­
сервативное лечение неэффективно, а сложные
операции невозможны.
Операции на плевре и легких с целью тща­
тельной санации полости, мобилизации коллабированных отделов легкого н удаления очага
инфекции показаны в тех случаях, когда пунк­
ционной санацией или закрытым дренированием
с активной аспирацией не удалось расправить
легкое и ликвидировать эмпиему. Чаще всего
из таких операций применяется декортикация
легких. Эта операция является восстановитель­
ной, органосохраняющей, так как после мобили­
зации коллабированные отделы легкого расправ­
ляются и постепенно их функция нормализу­
ется.
Эффективность декортикации определяется
прежде всего сроком заболевания. Наиболее
успешна она в первые 3—4 нед, так как в более
поздние сроки фибринозные напластования глу­
боко прорастают в плевру и их удаление стано­
вится возможным только вместе с плеврой, т. е.
необходима плеврэктомия. Клиническими на­
блюдениями и патоморфологическими исследо­
ваниями доказано [Громова Л. С.. 1959], что
при эмпиеме плевры напластования фибрина на
висцеральной плевре меньше, чем на париеталь­
ной, их сращения с плеврой не столь глубоки,
поэтому удаление происходит только с поверх­
ностными слоями плевры. Основные слои ее
(глубокий коллагеновый и эластическая мем­
брана) остаются на легком, поверхность его
сохраняется герметичной, эластичной. Склеро­
тические изменения париетальной плевры в эти
же сроки более выраженны, сращения ее с фиб­
розными швартами плотнее, поэтому удалить
их чаще всего удается вместе с париетальной
плеврой, отделяя их от внутригрудной фасции.
Техника операции состоит в следующем. Под
эндотрахеальным наркозом осуществляется
переднебоковая, боковая или заднебоковая
торакотомия в зависимости от локализации
полости эмпиемы. При острой эмпиеме не
удается удалить весь эмпиемный мешок цели­
ком, поэтому полость обычно сразу вскрывают,
аспирируют гнойный экссудат, салфетками уда­
ляют детрит, сгустки крови, рыхлые фибриноз­
но-гнойные напластования, а стенки гнойной
полости тщательно промывают (раствором первомура с изотоническим раствором натрия хло­
рида в соотношении 1:3) или обрабатывают 5 %
спиртовым раствором йода. После этого меняют
инструменты, перчатки, отграничивающие сал­
фетки и приступают к декортикации легкого.
В ранние сроки заболевания (до 2—3 нед) фиб­
рин! ibie пленки с легкого снимаются легко, иног­
да с помощью салфетки и тупфера. Шварты
на висцеральной плевре рассекают осторож­
ными движениями скальпеля, чтобы не пов­
редить легочную ткань. Край шварты отделяют
от висцеральной плевры и отсепаровывают
в виде полос различной ширины. Отслойку
шварты производят тупфером или пальцем,
надавливая на фиброзную ткань, а не на легкое.
Важнейшее правило декортикации — это про­
никновение в слой между фиброзной швартой
208
и плеврой. Это значительно облегчается при
использовании гидравлической препаровки.
Расширяя зону декортикации, постепенно уда­
ется высвободить легкое. Однако нельзя стре­
миться выполнить декортикацию всех отделов
легкого, если имеются очень плотные сращения,
так как это. как правило, сопровождается по­
вреждением легочной паренхимы, что потре­
бует ее ушивания, герметизации и может све­
сти на нет все, достигнутое декортикацией. Плот­
ные участки сращений лучше оставлять на лег­
ком. В некоторых случаях плотные шварты на
висцеральной плевре рассекают параллельными
и перпендикулярными разрезами на расстоянии
1,5—2 см друг от друга, не повреждая легкое
[Маслов В. И., 1971]. Образующиеся участки
шварты иссекают параллельно легочной поверх­
ности, наиболее плотно фиксированные участки
шварты остаются на легком.
Декортикация будет эффективнее, и легкое
лучше расправится после операции, если раз­
делить междолевые щели и произвести моби­
лизацию всего легкого (пневмолиз). Для этого
необходимо рассечь и иссечь переходные склад­
ки эмпиемного мешка с участком париетальной
плевры, рассечь легочную связку, освободить
диафрагмальную поверхность легкого, удалить
костодиафрагмальные шварты. По мнению
В. И. Маслова (1976), декортикация должна
обязательно сочетаться с диафрагмолизом,
т. е. освобождением от шварт и мобилизацией
диафрагмы. Восстановление подвижности
диафрагмы имеет большое значение для бли­
жайших и отдаленных результатов операции.
Удаление париетальной плевры (плеврэктомия) вместе с фиброзными швартами на ней
рекомендуется не всеми хирургами. При ост­
рой эмпиеме плевры толщина фиброзных нашвартований относительно небольшая, и доста­
точно их высвободить.
Декортикация и плеврэктомия завершаются
тщательным гемостазом и восстановлением гер­
метичности легкого. Небольшие повреждения
легочной паренхимы можно герметизировать
с помощью медицинского клея МК-6 или МК-7.
Перед ушиванием торакотомной раны полость
обильно промывают антисептическим раство­
ром, нередко с использованием ультразвуко­
вой обработки стенок, устанавливают два дре­
нажа с последующей активной аспирацией и
расправлением легкого.
Декортикация легкого и плеврэктомия в чи­
стом виде могут быть выполнены очень ограни­
ченному контингенту больных при отсутствии
значительной деструкции легкого и бронхо­
плевральных свищей. Чаще всего эту операцию
необходимо сочетать с дополнительными вме­
шательствами: резекцией пораженных отделов
легкого, ушиванием небольших бронхиальных
14 Зак 0517
свищей, реампутацией культи бронха, корри­
гирующей торакопластикой и др.
Сочетание декортикации с частичной резек­
цией легкого показано при наличии деструктив­
ного процесса в нем (абсцессы, бронхоэктазии,
множественные бронхиальные свищи) или вы­
раженной карнификации доли легкого. Необхо­
димость одновременной резекции легкого пла­
нируется еще до операции на основании рент­
генографических и бронхографических иссле­
дований, а объем резекции окончательно опре­
деляется после визуального и пальпаторного
исследования легкого во время вмешательства.
Обычно в таких случаях выполняется лобэкто­
мия, реже — билобэктомия с декортикацией
оставшихся отделов легкого и частичной плеврэктомией (по показаниям). Лишь в исключи­
тельных случаях при небольшой периферической
деструкции легкого допустима атипичная клино­
видная резекция.
Небольшие бронхиальные свищи при отсут­
ствии деструкции легочной паренхимы можно
ушить атравматичными иглами вместе с сосед­
ней легочной тканью, желательно с дополни­
тельной мышечной пластикой свища и неболь­
шой остаточной полости. Реампутация культи
бронха показана при послеоперационной эмпие­
ме, если размеры культи превышают 1 см. Такое
вмешательство можно выполнить ручным спо­
собом или с помощью аппарата УК Б, обязатель­
но завершая его тщательной плевризацией куль­
ти, декортикацией остающихся отделов лег­
кого и диафрагмолизом, чтобы обеспечить быст­
рое расправление легкого.
Некоторые хирурги после сочетанной декор­
тикации с частичной резекцией легкого, особен­
но после плевробилобэктомии, выполняют кор­
ригирующую торакопластику или перемещение
купола диафрагмы во время операции [Каба­
нов А. Н. и др., 1978]. Оправдано с целью умень­
шения размеров плевральной полости выполнить
тщательную мобилизацию диафрагмы во время
операции и наложить пневмоперитонеум в бли­
жайшие 1—2 дня после вмешательства.
Плевропневмонэктомия является наиболее
тяжелым вмешательством, предпринимаемым
только при распространенном деструктивном
процессе в легком, чаще всего гангрене, ослож­
ненной пиопневмотораксом.
Иногда плевропневмонэктомия выполняется
при острой эмпиеме плевры, развившейся как
осложнение хронического гнойио-деструктивного заболевания легкого, если во время опера­
ции устанавливается, что поражены две доли
легкого. Поэтому во всех случаях оперативного
лечения, планируемого вначале как частич­
ная резекция, нужно иметь в виду возмож­
ность вынужденного расширения объема вме­
шательства вплоть до удаления всего легкого.
209
Глава 2? ХРОНИЧЕСКАЯ
ЭМПИЕМА ПЛЕВРЫ
И БРОНХИАЛЬНЫЕ СВИЩИ
ХРОНИЧЕСКАЯ ЭМПИЕМА
ПЛЕВРЫ
Хроническая эмпиема плевры — гнойно-де­
структивный процесс в остаточной плевральной
полости с грубыми и стойкими морфолошческими изменениями, характеризующийся дли­
тельным течением с периодическими обостре­
ниями.
Возникновение хронической эмпиемы отмеча­
ется у 4—20 % больных острой эмпиемой [Ко­
лесов В. И., 1955; Стручков В. И., 1967; Мас­
лов В. И., 1976J. Большие различия в частоте
хронической эмпиемы такого происхождения
обусловлены прежде всего отсутствием еди­
ного представления о критериях перехода ост­
рой формы этого заболевания в хроническую.
Гистологическими исследованиями материала,
полученного во время плеврэктомий, декортика­
ций и резекций легкого, доказано, что стойкие
и необратимые морфологические изменения
плевры и подлежащих тканей развиваются лишь
к исходу 2—3 мсс от начала заболевания. В эти
же сроки чаще появляются признаки наруше­
ния регенеративных механизмов и обострения
гнойного процесса.
Исходя из этого мы считаем наиболее оправ­
данным относить к хроническим эмпиемам те
случаи, когда эмпиема существует более 3 мес
и течение заболевания имеет характерные кли­
нические признаки — периоды затихания и
обострения гнойного процесса.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Хроническая эмпиема плевры может под­
держиваться различными микроорганизмами.
В отличие от острой эмпиемы значительно чаще
встречается смешанная флора с преобладанием
грамотрицательных бактерий (кишечной, синешойной палочек).
Основными условиями развития хронической
эмпиемы плевры являются недостаточное рас­
правление легкого с формированием стойкой
остаточной плевральной полости и поддержание
инфекции в стенках этой полости. Главными
поддерживающими факторами служат бронхи­
альные свищи, хондриты, склеротические из­
менения коллабировапных отделов легкого, а
при послеоперационных эмпиемах — несоответ­
ствие размеров оставшегося после резекции
легкого объему плевральной полости.
Бронхоплевральные свищи являются на­
иболее частой причиной развития стойкой плев­
ральной полости и хронической эмпиемы плев­
ры.
Нередко причиной хронической эмпиемы
плевры являются патологические изменения
легкого с продолжающимся в нем инфекцион­
ным процессом (бронхоэктазии, хронический
абсцесс, пневмосклероз) инородные тела в плев­
ральной полости, периферических отделах
легкого, 1 рудной стенке. Инородными телами
чаще всего являются осколки от снарядов, пули,
которые длительное время сохраняются в поло­
сти после огнестрельных ранений.
Иногда хроническая эмпиема поддержива­
ется остеомиелитом илн хондритом ребра (.чаще
после огнестрельных ранений или оперативных
вмешательств). В таких случаях формируются
небольшие пристеночные полости, в которых
имеются секвестры и костные отломки.
Инфекционный процесс в стенках полости
может длительное время сохраняться из-за не­
своевременной и плохой санации от фибриноз­
но-гнойных напластований па плевральных
листках, в которых развиваются патологиче­
ские грануляции с участками повторной де­
струкции и образованием мелких полостей.
Кроме того, такие напластования способству­
ют развитию пневмосклероза и сохранению
гнойной полости.
В основе всех этих причинных факторов,
способствующих или ведущих к развитию хро­
нической эмпиемы плевры, лежат несвоевре­
менное или недостаточное лечение острой эм­
пиемы, ошибки в лечебной тактике, тяжелые
деструктивные изменения в легком, плевре
и грудной стенке.
Известны случаи развития хронического
гнойного процесса в плевральной полости после
пневмонэктомии, несмотря на неосложненное
течение раннего послеоперационного перио-
210
да. Иногда эмпиема плевры диагностируется дят фиброзные тяжи за пределы внутригрудной
впервые через несколько лет после удаления фасции и в межреберные промежутки, вызы­
легкого. Следовательно, у таких больных оста­ вая сдавление и облитерацию кровеносных со­
точная полость после пневмонэктомии не обли­ судов, ишемию с постепенным прогрессирую­
терировалась, воспаление сохранялось, но про­ щим фиброзом внутреннего слоя мышц.
II стадия (от 5 мес до года) проявляется
текало торпидно. При понижении сопротивляе­
мости организма произошло клиническое обо­ клиническими признаками хронической инток­
стрение. Такие эмпиемы плевры следует счи­ сикации с более редким, чем в нервом периоде,
тать первично-хроническими. При диагностике обострением гнойного процесса. Патоморфо­
эмпиемы в таких случаях уже определяются логические изменения более выражены: тол­
все морфологаческие признаки хронического щина фиброзных шварт на париетальной плевре
процесса вплоть до обызвествления стенок поло­ достигает 3—4 см и более, межреберные мышцы
сморщиваются и замещаются соединительной
сти.
Возможно развитие хронической эмпиемы тканью, межреберные промежутки суживаются,
плевры как результат специфических хрониче­ диафрагма уплощается из-за массивного ошварских инфекций — туберкулеза, актиномикоза. тования ее, объем плевральной полости умень­
Она также нередко диагностируется поздно, шается. В толщине шварт волокнистая фибро­
зирующая соединительная ткань становится
уже в хронической стадии.
Патоморфологические изменения при хрони­ плотнее, кровоснабжение ее уменьшается и
ческой эмпиеме развиваются не только в по­ происходит склерозирование ее с гналинозом.
верхностных слоях плевры, как при остром про­ Воспалительный процесс распространяется на
цессе, а захватывают все слои плевры, ткани надкостницу ребер и ребра.
Висцеральная плевра также уплотняется,
легкого, грудной стенки, органов средостения,
вызывая значительные функциональные нару­ однако толщина фиброзных шварт здесь не пре­
вышает 0,5—1 см. Грануляционная ткань выра­
шения.
На основании клинико-морфологических жена слабо, на поверхности имеется гнойный
признаков различают три стадии хронической налет. Барьерная функция висцеральной плевры
эмпиемы плевры |Линберг Б. Э., 1945: Серге­ между гнойно-фибринозными наложениями и
тканью легкого нарушена: по междольковым
ев В. М., Катковский Г, Б., 1975].
I стадия, продолжительностью до 5 мес от перегородкам в легочную ткань прорастают фиб­
начала острой эмпиемы, характеризуется зати­ розные тяжи. Изменения в легком постепенно
ханием воспалительного процесса в плевре и прогрессируют, в процесс вовлекается пернбронпостепенным утолщением плевральных листков хиальная ткань, что ведет к деформации брон­
за счет развивающейся грануляционной ткани хов и нарушению их дренажной функции. Хро­
в плевре и фибринозных напластованиях. Вокруг нический воспалительный процесс в легком
остаточной полости формируются массивные нарастает, и развиваются пневмофиброз, брон­
внутриплевральные шварты, отграничивающие хоэктазии. Нередко в поверхностных слоях лег­
гнойный очаг. Форма и размеры полости эмпие­ кого образуются мелкие абсцессы. Значитель­
мы различные: чаще всего образуется присте­ ное сдавление легкого швартами и прогрессиру­
ночная или базально-пристеночная ограничен­ ющий нневмофиброз ведут к выраженным дыха­
ная эмпиема, реже — верхушечная эмпиема тельным расстройствам.
III стадия хронической эмпиемы плевры про­
плевры, еще реже — междолевая. Емкость гной­
ной полости, как правило, 100- 300 мл, и лишь текает с еще более выраженными морфологи­
в редких наблюдениях (примерное 10 % случаев ческими и клиническими проявлениями. Колот числа всех хронических эмпием) встречается лагенизация и гиалиноз плевральных шварт со­
субтотальная эмпиема. Тотальная эмпиема провождаются отложением солей кальция и
формированием костных структур («плевраль­
возникает обычно после пневмонэктомии.
В I стадии хронической эмпиемы плевральные ные кости» или «кальциевые пластинки плев­
шварты представляют собой зрелую, обильно ры»), В легочной паренхиме нарастают деге­
инфильтрированную гистиолимфоцитарными неративные изменения, на фоне которых разви­
клетками соединительную ткань. Постепенно ваются вторичные гнойные процессы по тип}
происходит дальнейшее созревание и фибрози­ бронхоэктазий. Нередко перибронхит и бронхо
рование соединительной ткани. При прогресси­ эктазии развиваются и в другом легком [Вайль
ровании гнойного процесса могут образоваться С. С., 1946].
новые наложения фибрина и формируется слой
Зона плеврогенного склероза распространя­
более молодой грануляционной соединительной ется еще глубже, в ткани грудной стенки. Руб­
ткани. Деструктивный процесс распространяется цовое перерождение мышц, почти полное сбли­
в более глубокие слои плевры, окружающие жение ребер, изменение их формы и подвиж­
ткани и органы. От париетальной плевры отхо­ ности, наряду с резким нарушением подвижно­
14
211
сти диафрагмы и значительным прогрессиро­
ванием патологических изменений в легком,
обусловливают нарастающую дыхательную не­
достаточность.
Деформация грудной клетки и уменьшение
объема плевральной полости ведут к смещению
средостения, иногда к вторичному перикардиту,
к стойкому перегибу крупных сосудов (полых
вен, легочной артерии и вен), что сопровожда­
ется гемодинамическими расстройствами.
Хроническая гнойная интоксикация приводит
к развитию амилоидоза внутренних органов.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
Клиническая картина хронической эмпиемы
определяется прежде всего величиной гнойной
полости, наличием или отсутствием бронхоплев­
рального и плеврокожного свищей, морфоло­
гическими изменениями плевры и подлежащих
тканей, т. е. стадией эмпиемы. Переход острой
эмпиемы в хроническую происходит постепенно.
Основными признаками такого перехода явля­
ются снижение температуры тела до нормаль­
ной или субфебрильной, улучшение самочувст­
вия, уменьшение гнойного отделяемого и ста­
билизация объема остаточной плевральной
полости. В I стадии хронической эмпиемы со­
стояние больного удовлетворительное, боли в
груди уменьшаются или исчезают, почти нет
признаков гнойной интоксикации и дыхатель­
ной недостаточности. Только наличие стойкой
остаточной полости с небольшим количеством
гноя или скудные гнойные выделения из плев­
рокожного свища свидетельствуют о хрониче­
ском воспалительном процессе. Лабораторные
признаки гнойного процесса также мало выра­
жены: сохраняются лишь умеренное повыше­
ние СОЭ, незначительная анемия, диспротеинемия.
Однако благополучие это кажущееся, так
как нагноительный процесс продолжается и
медленно прогрессирует, устойчивость орга­
низма к инфекции понижается, и при малей­
ших неблагоприятных обстоятельствах (ох­
лаждение, переутомление, сопутствующие за­
болевания) развивается обострение.
Во время обострения повышается температура
тела, появляются ознобы, усиливаются боли
в груди, нарастают признаки гнойной интокси­
кации (особенно при наличии большой эмпиемной полости), увеличивается количество гной­
ных выделений из плеврокожного свиша или
количество гнойной мокроты (при эмпиеме с
бронхоплевральным свищом). Нарастают ане­
мия и диспротеинемия, повышаются число лей­
коцитов в крови и нейтрофильный сдвиг влево.
В плевральной жидкости резко увеличивается
число лейкоцитов (до 15 • 10ч/л), причем ней-
трофилез экссудата достигает 95—99%; зна­
чительно увеличено количество разрушенных клеток.
II стадия хронической эмпиемы плевры ха­
рактеризуется более тяжелой клинической кар­
тиной, так как длительное течение нагноительного процесса отражается на общем состоянии
больного, усиливаются общее недомогание,
разбитость, ухудшается аппетит, нарастают
одышка и сердцебиение. При сопутствующем
процессе в легком значительно усиливается
кашель, увеличивается количество гнойной мо­
кроты. Боли в груди непостоянны, часто колю­
щего характера, возникают или усиливаются при
физической нагрузке. При переходе воспаления
на ткани грудной стенки и вовлечении в процесс
нервных стволов боли могут иррадиировать в ру­
ку, лопатку, живот.
При осмотре таких больных обращает на себя
внимание их бледность, иногда цианоз. Грудная
клетка неравномерно участвует в акте дыхания.
Пальпаторно нередко определяются отечность
и инфильтрация мягких тканей над полостью
эмпиемы, особенно при наличии плеврокожного
свища. Данные перкуссии и аускультации раз­
личные в зависимости от положения и величины
гнойной полости, количества жидкости в ней.
толщины шварт. Чаще всего определяется значи­
тельное притупление перкуторного звука в ниж­
них отделах полости, переходящее в тимпанит
над воздушной подушкой. Дыхание над проек­
цией жидкости резко ослаблено или не выслу­
шивается. Вне полости нередко выслушиваются
разнокалиберные хрипы. Тахикардия более стой­
кая, чем в I стадии, что объясняется не только
гнойной интоксикацией, но и смещением средо­
стения. Границы сердца могут быть смещены.
При электрокардиографии и интегральной реографии тела определяются гемодинамические
нарушения с признаками легочной гипертензии.
В III стадии хронической эмпиемы (с продол­
жительностью заболевания более года) отме­
чается значительная деформация грудной клет­
ки, ребра на стороне поражения малоподвиж­
ны, межреберные промежутки резко сужены,
надплечье опущено. Почти всегда имеется плев­
рокожный свищ, нередко остеомиелит ребра
или хондрит. Закрытые хронические эмпиемы
могут протекать бессимптомно из-за плотного
осумкования гноя. В таких случаях только
внимательное клиническое и рентгенологиче­
ское обследование ослабленного больного поз­
воляет заподозрить наличие гнойного очага,
а пункция остаточной плевральной полости
подтверждает наличие эмпиемы. В клинической
картине этой стадии преобладают явления дли­
тельной дыхательной недостаточности и хрони­
ческой гнойной интоксикации. При обострении
гнойного процесса и нарушении оттока из поло­
сти состояние больных значительно ухудша-
212
ется, нарастает интоксикация. Длительное тече­
ние гнойного процесса сопровождается разви­
тием истощения больного, анемией, иногда ами­
лоидным перерождением почек и других внут­
ренних органов.
ДИАГНОСТИКА
Диагностика хронической эмпиемы, как прави­
ло, несложна. Решающее значение имеют рент­
генологические методы исследования (рис.106).
Обычно исследование начинается выполнением
стандартных рентгенограмм грудной клетки
в двух проекциях, в ряде случаев необходима
латерография. Характер содержимого оста­
точной плевральной полости устанавливается
при пункции ее.
Для уточнения локализации и размеров гной­
ной полости, конфигурации ее стенок показаны
плеврография, фистулография. Большое значе­
ние для оценки состояния легкого и выбора
лечебной тактики имеют томография, бронхо­
графия и ангиопневмография. При длительном
существовании хронической эмпиемы в коллабированном легком наступают необратимые
морфологические изменения, значительно на­
рушающие функциональные возможности лег­
кого.
Бронхография дает возможность выявйть
состояние бронхиального дерева, определить
локализацию и характер бронхоплевральных
свищей, установить причину хронического тече­
ния процесса (бронхоэктазии, хронический абс­
цесс и т. п.). Бронхографическими признаками
тяжелых изменений в легких являются: 1) на­
личие «пустой зоны» из-за неконтрастируемых
бронхов в спавшихся отделах легкого; 2) сбли­
жение бронхов с уменьшением углов разветвле­
ния их; 3) различные виды деформаций, пере­
гибов бронхиального дерева, нередко с образова­
нием бронхоэктазий [Сергеев В. М., Катковский Г. Б., 1975].
Ангиопульмонография (общая или селектив­
ная) показана лишь в тех случаях, когда неин­
вазивные методы исследования не дают четкого
представления о состоянии легкого над швартой. При получении серийных ангиопневмо­
грамм всех трех фаз контрастирования сосу­
дов (артериальной, капиллярной и венозной)
надо считать, что в легком отсутствуют необ­
ратимые склеротические изменения, функция
его после декортикации и плеврэктомии может
восстановиться. Если же капиллярная фаза от­
сутствует, а ветви легочных сосудов не только
сближены, но и деформированы, сужены, при­
чем контрастное вещество задерживается в со­
судах легкого более 10 с, то это свидетельствует
о развившемся плеврогенном склерозе легкого.
В таких случаях плеврэктомия может быть
Рис. 106. Хроническая эмпиема плевры. Прямая рент|енограмма.
выполнена лишь в сочетании с частичной резек­
цией легкого.
Наиболее полное представление об измене­
ниях в легочной паренхиме дает сопоставление
данных бронхографии и ангиопневмографии.
По данным В. М. Сергеева (1967), обнаруже­
ние грубого деформирующего бронхита или
бронхоэктазий соответствует значительной
деформации сосудов легкого и отсутствию ка­
пиллярной фазы на ангиопневмографии.
Тензометрия в системе легочных артерий
и в правых полостях сердца значительно допол­
няет данные ангиопневмографии. Если давле­
ние в легочных артериях нормальное, то изме­
нения в легких еще обратимы. Легочная гипер­
тензия указывает на отсутствие резервных воз­
можностей легочных сосудов.
Электрокимография используется для изу­
чения легочного кровообращения. Этим методом
можно получить более объективную информа­
цию, чем ангиографическим исследованием
|Марморштейн С. Я., Абарбанель Е. Э., 1966].
Сканирование легких дает возможность изу­
чить легочное кровообращение (перфузионное
сканирование) и легочную вентиляцию (венти­
ляционное сканирование).
213
ЛЕЧЕНИЕ
Лечение хронической эмпиемы плевры со­
стоит из мероприятий общего характера, на­
правленных на организм больного в целом,
и мероприятий по санации и ликвидации гной­
ного очага.
При обострении гнойного процесса задачи
общего лечения те же, что и при острой эмпиеме
плевры. В стадии ремиссии, когда заболевание
проявляется в основном наличием плеврокожного свища без признаков интоксикации и вы­
раженных нарушений гомеостаза, проводится
лишь общеукрепляющее лечение и лечение
сопутствующих заболеваний, если таковые
имеются. Длительность и объем предопера­
ционной подготовки определяются индивидуаль­
но для каждого больного. При этом должны
быть использованы все средства, способствую­
щие устранению задержки гноя в полости, очи­
щению стенок эмпиемы и уменьшению размеров
остаточной плевральной полости.
При отсутствии бронхиального свища эмпиемную полость можно санировать пункциями с
максимальной аспирацией гноя и промыванием
антисептическими растворами, а также актив­
ным вакуумным дренированием полости. Мест­
ная фибринолитическая терапия внутриплев­
ральным введением протеаз с последующими
систематическими промываниями позволяет
ликвидировать рыхлые гнойно-фибринозные
напластования на стенках полости. Однако
расправить коллабированное легкое удается
редко из-за плотных организованных шварт на
висцеральной плевре, не поддающихся лизису.
Поэтому чаще устанавливаются показания
к более сложным оперативным вмешатель­
ствам.
Задачи хирургического лечения хронической
эмпиемы плевры сводятся к устранению очага
инфекционного процесса и ликвидации стой­
кой остаточной плевральной полости.
Декортикация легкого при хро­
нической эмпиеме по сравнению с острой зна­
чительно затруднена в связи с плотными сра­
щениями фиброзных шварт с висцеральной
плеврой. Техника декортикации и особенности ее
выполнения в зависимости от срока заболева­
ния изложены в разделе о лечении острой эмпие­
мы плевры.
После декортикации, пневмолиза и диафрагмолиза обязательно выполняется плеврэктомия, т. е. удаление париетальной плевры и фиб­
розных напластований на ней. Удаляются не
только фиброзные напластования с поверхно­
сти плевры, но и фиброзно-измененная, имбибированная гноем плевра. Необходимость уда­
ления резко утолщенной плевры при хрониче­
ской эмпиеме доказана в работах Л. К. Бо­
гуша (1961 ), В. И. Маслова (1970, 1976), М. Wil­
liams (1950), р. Herzog (1967) и др. Плеврэктомия может быть полной или частичной.
Отслаивание шварты при полной плеврэктомии производится широко во всех направлениях,
плотные сращения рассекаются ножницами или
скальпелем. Во многих случаях отделение плев­
ры и фиброзных шварт облегчается гидравли­
ческой препаровкой. Особенно осторожно необ­
ходимо манипулировать на месте перехода
париетальной плевры в висцеральную, чтобы
избежать повреждения легкого, а также при
выделении шварт у купола плевральной полости,
где велика опасность повреждения подключич­
ных сосудов.
Удаление эмпиемного мешка без вскрытия
его, т. е. идеальная плеврэктомия и декортика­
ция легкого, удается редко. Чаще производит­
ся планируемое вскрытие полости эмпиемы с ас­
пирацией всего содержимого, очищением и про­
мыванием стенок полости, обработкой их 3-5 %
спиртовым раствором йода или первомуром,
а после этого выполняются поэтапная декорти­
кация легкого, плеврэктомия и диафрагмолиз.
Удаление париетальной шварты через полость
эмпиемы безопаснее, так как доступ к опасным
зонам у средостения и купола плевры шире,
чем при удалении эмпиемного мешка целиком.
При наличии гнойно-деструктивных очагов в
легком (абсцесс, бронхоэктазии, множествен­
ные бронхиальные свищи), поддерживающих
хронический гнойный процесс в плевре, плевр­
эктомия сочетается с частичной резекцией лег­
кого. Чаще всего производится лобэктомия с
декортикацией остающихся отделов легкого.
При периферически расположенных неболь­
ших участках деструкции легкого может быть
выполнена атипичная клиновидная резекция с
помощью аппарата УКЛ.
У больных с остеомиелитом ребер, а также
при наличии инородных тел в остаточной поло­
сти эффективная санация и ликвидация поло­
сти возможны только после удаления этих оча­
гов инфекционного процесса.
В некоторых случаях при обострении хрони­
ческой эмпиемы с резкой гнойной интоксика­
цией и особенно при наличии бронхиального
свища, затрудняющего санацию полости через
дренаж, показано открытое дренирование гной­
ной полости с резекцией фрагментов ребер и
части париетальных шварт, формированием
широкой торакостомы путем подшивания кожи
к надкостнице ребра или к внутригрудной фас­
ции.
При длительном существовании хронической
эмпиемы плевры происходят необратимые из­
менения в коллабированных отделах легкого
(карнификация), и оно теряет способность к рас­
правлению даже после декортикации. В таких
214
случаях ликвидировать остаточную полость
можно лишь торакопластикой или мышечной
пластикой.
Экстраплевральная
торако­
пластика, предложенная J. Estlander (1879),
модифицированная М. С. Субботиным (1888),
А. В. Лекторским (1893), Вубгк (1956) и др.,
в настоящее время практически не применяется
из-за недостаточной эффективности, так как
при этом не иссекаются париетальная и висце­
ральная шварты и после операции, как правило,
сохраняется щелевидная гнойная полость.
Экстраплевральная торакопластика может
быть эффективной только при небольших оста­
точных полостях боковой локализации без
значительного изменения плевральных листков,
и то при условии обязательного дренирования
эмпиемной полости отдельным разрезом в самом
низком ее отделе.
Интраплевральная торакопла­
стика (Schaede, 1890] предусматривает резек­
цию не только ребер, но и париетальной швар­
ты с межреберными мышцами, сосудами и нер­
вами.
Техника операции состоит в том, что разре­
зом от края большой грудной мышцы на уровне
IV ребра вниз до X ребра, затем по ходу X реб­
ра до лопаточной линии и поворачивая кверху
рассекают все мягкие ткани по внутреннему
краю лопатки; огромный кожио-мышечный
лоскут отпрепаровывают и отворачивают квер­
ху, Обнаженные ребра вместе с тканями межре­
берных промежутков и париетальной швартой
иссекают единым блоком. После тщательного
гемостаза кожно-мышечный лоскут помещают
на свое место, фиксируя отдельными швами
к висцеральной шварте, особенно в зоне брон­
хиального свища. Под лоскут подводят не­
сколько дренажей, и рану послойно ушивают
с наложением давящей повязки с пелотом.
Эта операция позволяет успешно ликвидиро­
вать полость даже при запущенной хрониче­
ской эмпиеме, однако высокая летальность
(от 20 до 50 % по данным В. 14. Колесова, 1955),
чрезвычайная травматичность и неизбежная
инвалидизация больных из-за резкой дефор­
мации скелета значительно сократили показа­
ния к этому вмешательству. Некоторые хирур­
ги (Ратнер Ю. А., 1935; Богуш Л. К., Громо­
ва Л. С., 1961] для уменьшения травматичности
предложили расчленить операцию на несколько
этапов, выполняемых через 1—2 мес. Это поз­
волило сократить летальность до 10,9 % [Мас­
лов В. И., 1976], однако длительное лечение
и частые рецидивы плеврокожных свищей при
сохранении небольших щелевидных полостей
не удовлетворяют клиницистов.
Лестничная торакопластика по Heller (1912)
и Б. Э. Линбергу (1945) является одной из
разновидностей интраплевральной торакопла­
стики.
При этой операции обнажают и поднакостнично резецируют ребро над полостью эмпие­
мы. Через ложе резецированного ребра вскры­
вают полость. Определяют размеры эмпиемы
и резецируют остальные ребра, заходя за край
полости на 2—3 см. Рассекают надкостницу и
вскрывают полость по ходу резецированных
ребер, иссекают париетальную шварту, выскаб­
ливают внутреннюю стенку эмпиемного мешка.
Образовавшиеся «перекладины» тканей меж­
реберных промежутков при глубокой полости
(свыше 3 см) рассекают поочередно: одну спе­
реди, другую сзади. Образовавшиеся лоскуты
погружают до висцеральной плевры.
После тщательною гемостаза в каждый раз­
рез рыхло вводят тампон, не подводя его под
«перекладины». Кожно-мышечный лоскут фик­
сируют швами и накладывают давящую по­
вязку.
А. Н. Кабанов и соавт. (1972, 1978) сочетают
торакопластику с перемещением диафрагмы.
Это уменьшает объем костно-пластического
вмешательства и улучшает косметический ре­
зультат, но в условиях эмпиемы перемещение
диафрагмы опасно в связи с возможностью
инфицирования брюшной полости.
Большое распространение получили методы
мышечной пластики полости эмпиемы, пред­
ложенной F. Konig (1878) для ликвидации вер­
хушечной остаточной полости и А. А. Абражановым (1899) для закрытия легочно-плевраль­
ного свища. В зависимости от локализации
эмпиемной полости и состояния мышц грудной
стенки можно использовать большую грудную
мышцу, широчайшую мышцу спины, реже —
ромбовидную, зубчатую или длинные мышцы
спины. Техника таких вмешательств разнооб­
разна в зависимости от расположения, вели­
чины и характера остаточной полости. Сущность
операции заключается в выкраивании мышеч­
ного лоскута па ножке соответственно крово­
снабжению и с таким расчетом, чтобы величина
лоскута соответствовала размеру полости, а
при повороте его для заполнения остаточной
полости не нарушалось кровоснабжение мы­
шечной ткани.
Во всех случаях оперативное вмешательство
заканчивается активным дренированием полости
и раны мягких тканей, что наряду с герметич­
ным ушиванием раны и давящей повязкой обес­
печивает хорошее соприкосновение тканей и
облитерацию полости.
Выбор метода пластики определяется в зави­
симости от локализации, размеров и формы
остаточной плевральной полости, от величины
и характера бронхоплевральных свищей. Все
же большинство костно-пластических операций
215
на грудной стенке имеют существенные недо­
статки, связанные с резкой деформацией груд­
ной клетки, снижением функции плечевого поя­
са и нарастающими необратимыми функциональ­
ными расстройствами дыхания и сердечно­
сосудистой деятельности (Сергеев В. М., 1967],
В связи с этим заслуживают внимания попытки
ликвидации стойкой остаточной плевральной
полости с помощью биологической пломбы. По
нашему мнению, наиболее эффективной, про­
стой и безопасной является антибактериаль­
ная фибринная пломбировка полости, так как
фибрин является хорошим стимулятором ре­
паративных процессов, а депо антибиотиков в
пломбе предупреждает развитие рецидива
эмпиемы, если устранен источник повторного
инфицирования плевры (бронхиальные свищи,
инородные тела, остеомиелит ребер). Техника
пломбировки эмпиемной полости изложена
выше, в разделе «Острая эмпиема плевры».
Оперативные вмешательства при хронической
эмпиеме в большинстве случаев являются очень
травматичными, что требует определенного опы­
та и достаточной ориентировки хирурга в изме­
нениях топографии органов грудной полости,
вызванных длительно существующим гнойным
процессом. Плотные сращения и значительное
смещение органов груди нередко являются веду­
щей причиной развития грозных осложнений во
время операций.
Наиболее частым из них является кровоте­
чение из сращений и сосудов грудной стенки,
иногда из сосудов легкого, средостения и диа­
фрагмы.
Кровотечение из множественных мелких со­
судов сращений напоминает паренхиматозное
и может приводить к значительной кровопотере
(700—1000 мл).
При повреждениях непарной вены, подклю­
чичных сосудов, сосудов корня легкого необ­
ходимо прижать кровоточащий сосуд пальцем
или тупфером, затем продолжать мобилизацию
легкого или отделение шварты для обеспече­
ния достаточного доступа к поврежденному
сосуду.
При повреждении вен малого круга кровооб­
ращения возможно поступление воздуха в сосу­
дистое русло из остаточной плевральной поло­
сти или полости в легком, особенно при поло­
жительном давлении воздуха в этих полостях.
Это чаще встречается во время промывания
полости или при выделении легкого из сраще­
ний. Воздух поступает в левую половину серд­
ца, откуда разносится по сосудам большого
круга. Наиболее опасна воздушная эмболия
сосудов мозга.
Опасным осложнением во время оперативных
вмешательств является острая дыхательная
недостаточность вследствие закупорки брон­
хиального дерева гноем, слизью или кровью.
Меры предупреждения сводятся к санации
бронхиального дерева и гнойных полостей в
легких, правильному положению больного на
операционном столе, своевременной эвакуации
мокроты через интубационную трубку.
Повреждение легкого во время пневмолиза
и декортикации диагностируется сразу же по уси­
лению кровотечения и прохождению воздуха
из мест разрыва легочной паренхимы. Крово­
течение останавливается диатермокоагуляцией
или лигированием сосудов, а зона повреждения
легкого ушивается атравматичными швами или
же герметизируется с помощью медицинского
клея (МК-6, МК-7 и др,). При недостаточной
герметизации легочной ткани возникают труд­
ности в расправлении легкого после операции.
Повреждение диафрагмы, перикарда, пище­
вода встречаются редко. В связи с опасностью
проникновения инфекции из плевральной поло­
сти и развития тяжелых гнойных осложнений
(перитонит, перикардит, медиастинит) очень
важно своевременно диагностировать эти по­
вреждения и восстанавливать целость повреж­
денного органа тщательным ушиванием его.
В первые часы и дни после операции наиболее
частым осложнением является кровотечение.
Как правило, оперативное вмешательство закан­
чивается дренированием плевральной полости.
Диагностика продолжающегося кровотечения
основана на оценке клинической картины, а
также количества и характера аспирируемой
через дренаж жидкости. Важное значение в
постепенном уменьшении кровотечения из раны
и стенок полости после травматичных вмеша­
тельств имеют рациональное дренирование без
чрезмерного разрежения в первые часы, конт­
роль за проходимостью дренажей и тугая по­
вязка с пелотом над областью торакопластики.
Опыт нашей клиники показал, что проходи­
мость дренажей легче сохранить при исполь­
зовании двухпросветных трубок.
Если же в течение 2—3 ч после операции
количество геморрагического экссудата и его
гематокритное число не уменьшаются, то диаг­
ностируется продолжающееся или возобновив­
шееся кровотечение. В таких случаях продол­
жается гемостатическая терапия (в том числе
переливание свежеконсервированной крови) и
делается повторное оперативное вмешательство.
Иногда через дренаж выделяется мало ге­
моррагического экссудата и гематокритное
число его может быть небольшим (меньше
0,05—0,1 л/л), однако определяются все кли­
нические признаки внутренней кровопотери (на­
растающая тахикардия,- падение артериального
давления, бледность, жажда и др.). В таких
случаях следует думать о свернувшемся гемо­
тораксе.
216
Тяжелым осложнением послеоперационного
периода является аррозионное кровотечение
из-за некроза и разрушения стенки культи со­
суда под действием ферментов гноя в условиях
эмпиемы (чаще гнилостной). Обычно аррозион­
ное кровотечение наступает на 3—4-й неделе
.после операции из культи артерий, так как ор­
ганизация тромба в артерии происходит мед­
леннее, чем в вене, а иногда они в них совсем
не образуются [Ярушевич А. Д., 1955]. Пред­
вестником аррозионного кровотечения служит
кровохарканье, так как разрушение культи
сосуда часто сочетается с образованием брон­
хиального свища. Нередко массивное кровоте­
чение развивается после кашля или перевязки
со сменой тампонов или дренажа. В большин­
стве случаев аррозионное кровотечение закан­
чивается летальным исходом. Лишь иногда
удается при срочном оперативном вмешатель­
стве найти и перевязать кровоточащий сосуд.
Опасным осложнением послеоперационного
периода являются кровотечение и затекание
крови в бронхиальное дерево в зоне ушитого
свища или мышечной пластики его. Кровоте­
чение в таких случаях может быть небольшим
и диагностируется на основании нарастающей
дыхательной недостаточности и кровохарканья.
Если санация бронхиального дерева и гемоста­
тическая терапия неэффективны, то необходимы
бронхоскопия и окклюзия бронха поврежден­
ной доли или сегмента поролоновой губкой.
Через 1—2 дня после остановки кровотечения
(о чем свидетельствует отсутствие выделения
крови из полости через дренаж) и стабилиза­
ции гемодинамических показателей пломба уда­
ляется, проводится осторожная санация брон­
хиального дерева.
Ателектаз легкого и пневмония, развиваю­
щиеся после оперативных вмешательств по по­
воду хронической эмпиемы, значительно удли­
няют послеоперационный период, а нередко и
угрожают жизни больного. Причиной ателекта­
за является, в основном, закупорка бронхиаль­
ного дерева мокротой, слизью или кровью.
Профилактика пневмонии заключается преж­
де всего в санации бронхиального дерева перед
операцией, обязательно перед завершением ее
и в послеоперационном периоде. Важное значе­
ние имеют энергичное откашливание мокроты,
дыхательная гимнастика.
Остаточные полости плевры и рецидив эмпие­
мы являются частыми осложнениями после
оперативного лечения хронической эмпиемы
плевры. Предупреждение образования остаточ­
ной полости зависит от особенностей опера­
тивного вмешательства. После декортикации
и плеврэктомии необходимо тщательное выпол­
нение мероприятий, обеспечивающих расправ­
ление легкого (герметизация легкого перед
завершением операции, тщательная санация
стенок полости, вакуумное дренирование плев­
ральной полости с рациональным разрежением
в течение 3—5 дней после операции, пневмоперитонеум, санация бронхиального дерева,
дыхательная гимнастика, хорошая аналгезия и
др.). После торакопластики и мышечной пла­
стики большое значение имеют заполнение всех
отделов полости жизнеспособными тканями и
дренирование полости и раны мягких тканей
грудной стенки для аспирации экссудата, а так­
же давящая повязка с пелотом для соприкосно­
вения тканей со стенками полости. Повязка
должна быть сохранена в течение 2—3 нед
после операции.
Иногда и после этих мероприятий полость
не удается ликвидировать полностью, а остает­
ся щелевидное или другой формы простран­
ство, в котором может рецидировать эмпиема.
Наличие стойкой остаточной полости без брон­
хоплеврального или плеврокожного свища, без
инородного тела, остеомиелита, хондрита или
другого очага, поддерживающего хронический
гнойный процесс, не является показанием к
повторному оперативному вмешательству. По
данным клиники, в таких случаях необходимо
после пункционной санации заполнить полость
антибактериальной фибринной пломбой для
предупреждения рецидива эмпиемы и стиму­
ляции репаративных процессов.
При рецидиве эмпиемы необходимо тщатель­
ное обследование с целью выявления причины
рецидива. Повторное оперативное вмешатель­
ство должно быть направлено на устранение
очага хронического гнойного процесса с одно­
временной тщательной санацией и ликвида­
цией полости одним из методов мышечной или
торакопластики. Иногда оперативное лечение
при рецидиве эмпиемы должно быть проведено
в два этапа: 1) устранение очага инфекции,
поддерживающего хронический гнойный про­
цесс (удаление инородного тела, осколков,
фрагментов ребер при остеомиелите, хондри­
те); 2) ликвидация полости с помощью торакомиопластики или пломбировка ее.
Редкими осложнениями после оперативных
вмешательств при хронической эмпиеме плевры
являются тромбозы и эмболии легочных сосу­
дов, метастатические септические гнойники
мозга, почек и других органов. Течение этих
осложнений при эмпиеме такое же, как и при
других гнойных заболеваниях.
К поздним осложнениям хронической эмпие­
мы плевры следует отнести бронхиальные сви­
щи, сопутствующие изменения в поджатом швар­
тами легком (абсцедирование, бронхоэктазии,
карнификация легкого), а также амилоидоз
внутренних органов, тяжелое истощение, «ле­
гочное» сердце.
217
БРОНХИАЛЬНЫЕ СВИЩИ
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Бронхиальный свищ — стойкое сообщение
бронха с плевральной полостью, внутренним
органом или с поверхностью грудной стенки,
развившееся в результате повреждения или
патологического процесса в легком. Крайне
редко встречаются врожденные бронхопище­
водные или трахеопищеводные свищи (0,03—
0,04 % от числа новорожденных). Приобретен­
ные бронхиальные свищи после проникающих
повреждений груди развиваются примерно у
0,9 % раненых (Джанелидзе Ю. Ю., 1948]. В
мирное время наиболее часто встречаются брон­
хиальные свищи после оперативных вмеша­
тельств на легких (в среднем около 7—15 %).
Различают несостоятельность культи бронха,
бронхоплевральные или легочно-плевральные
сообщения и бронхиальные свищи. Бронхиаль­
ный свищ — это стойкое сообщение, состоящее
из фиброзной ткани, покрытой грануляциями
или эпителием. Выделение бронхиальных сви­
щей как самостоятельной нозологической еди­
ницы обусловлено тем, что стойкие свищевые
ходы, в отличие от несостоятельности бронха
или легочной ткани, значительно труднее подда­
ются консервативным лечебным мероприятиям
и требуют, как правило, оперативного лечения.
Говоря о терминологии, следует подчеркнуть,
что классическое определение «бронхиальный
свищ» подразумевает лишь те случаи, когда пато­
логический процесс в легком и в плевральной
полости в основном уже закончен, а сохраня­
ется стойкое непосредственное бронхокожное
сообщение. Если же бронхиальный свищ откры­
вается в плевральную полость или в полость
легкого, следует говорить об эмпиеме плевры
или абсцессе легкого с бронхиальным свищом.
По опыту клиники госпитальной хирургии,
наиболее рациональной является классифика­
ция бронхиальных свищей, в которой учтены
лишь те факторы, которые имеют важное зна­
чение в выборе лечебной тактики.
Патогенез бронхиальных свищей после ране­
ний груди представляется следующим образом.
Проникающие ранения груди, как правило,
сопровождаются повреждением легкого с нару­
шением целости более или менее крупных брон­
хов. Подтверждением этого являются почти
неизбежное кровохарканье, спадение легкого
и иногда подкожная эмфизема, а при открытом
пневмотораксе — и прохождение воздуха из
поврежденного легкого через рану грудной стен­
ки. Некоторые авторы [Джанелидзе Ю. Ю.,
1948, и др.] называют такие повреждения воз­
духоносных путей первичными бронхиальными
свищами. Более оправданно мнение М. С. Гри­
горьева (1955), считающего, что бронхиальный
свищ и свежее повреждение бронхиального
дерева представляют собой два различных пато­
логических состояния и не могут быть отожде­
ствлены. Известно, что в большинстве случаев
отверстия в поврежденном небольшом бронхе
и раневой канал в легочной ткани заполняются
сгустками крови и герметизм поврежденного
легкого восстанавливается. При асептическом
течении процесса и хорошей резистентности
организма кровяные сгустки уплотняются,
раневой канал рубцуется. В легком при этом
некоторое время могут сохраняться полости
(«травматические каверны»), которые зажи­
вают [Колесников И. С., 1949].
В патогенезе бронхиальных свищей ведущее
значение имеет инфекция. Микробное загряз­
нение плевры и поврежденных участков легкого
происходит извне по ходу раневого канала или
из поврежденных бронхов. Развитию инфекци­
онного процесса в значительной степени спо­
собствуют инородные тела в легком и в плев­
ральной полости (пули, осколки, костные отлом­
ки, обрывки одежды, занесенные с ранящим
снарядом). Чаще инфекция развивается в плев­
ральной полости как нагноение гемоторакса.
В некоторых случаях эмпиема развивается как
Классификация бронхиальных свищей
Определяющий фактор
Количество
свищей
Сообщение с внешней
средой
Наружные:
бронхокожные
бронхоплеврокожные
Внутренние:
бронхоплевральные
бронхолегочные
бронхоорганные
(бронхопищеводные,
бронхожелудочные,
бронхокишечные,
бронхопеченочные)
Характер изменений легочной
ткани
Одиночные
Без значительных изменений
Множественные
С резкой инфильтрацией легочной ткани
С гнойно-деструктивным процессом в
легком
С карнификацией легкого
218
следствие нагноения раны грудной стенки и
вторично открывшегося пневмоторакса. Эмпие­
ма плевры ведет к распространению гнойного
процесса в зону раневого канала легкого и спо­
собствует возникновению сообщения бронха с
плевральной полостью. Образующийся сви­
щевой ход постепенно покрывается многослой­
ным эпителием из бронха, и формируется брон­
хиальный свищ. Нередко гной из плевральной
полости, особенно при эмпиеме с бронхиальным
свищом, прорывается наружу через рану груд­
ной стенки, и формируется бронхоплеврокож­
ный свищ.
Развитие бронхиальных свищей зависит,
кроме инфекционного процесса в плевре и ране­
вом канале легкого, от степени разрушения
легочной паренхимы, диаметра поврежденного
бронха, состояния бронхиального дерева (брон­
хит), а также от особенностей лечения развив­
шейся эмпиемы плевры и сопротивляемости
организма больного.
Бронхиальные свищи нетравматического
происхождения чаще всего развиваются при
абсцессах и гангрене легкого. Абсцессы легкого
в большинстве случаев вскрываются в бронхиаль­
ное дерево с последующим формированием
внутреннего бронхолегочного свища. Большие
абсцессы могут дренироваться через несколько
бронхиальных свищей. Множественные брон­
холегочные свищи чаще образуются при гангре­
нозных абсцессах.
Иногда бронхоплевральный свищ развивается
как осложнение эмпиемы плевры, которая про­
текает с вторичной деструкцией перифериче­
ских участков легкого. В редких случаях брон­
хиальный свищ возникает как следствие рас­
падающегося рака легкого, спонтанного пнев­
моторакса, актиномикоза, прорыва в бронх эхи­
нококковой или другой кисты, туберкулезной
каверны.
Бронхиальные свищи являются одним из
наиболее тяжелых осложнений после операций
на легких. Частота послеоперационных брон­
хиальных свищей колеблется, по данным оте­
чественных и зарубежных авторов, от 3 до 15 %
[Раков А. И., Вагнер Р. И., 1965; Амбатьелло Г. П., 1973; Цыбырнэ К. А. и др., 1975; Акжигитов Г. Н. и др., 1982; Roy S. et al., 1971;
Bazelly В. et al., 1981; Aubert M., Latreille R„
1981]. Это зависит прежде всего от характера
патологического процесса, явившегося пока­
занием к оперативному вмешательству. Так, по
данным клиники госпитальной хирургии, после
операций по поводу острых гнойно-деструктив­
ных заболеваний легких (гангрена, множе­
ственные абсцессы, осложненные абсцессы)
бронхиальный свищ развился у 9 % больных,
при хронических нагноительных заболеваниях
легких — у 2 %, а при раке легкого — у 6,6 %,
причем бронхиальные свищи после лобэкто­
мий наблюдались чаще, чем после пневмонэкто­
мий.
Послеоперационные бронхиальные свищи
являются следствием несостоятельности культи
бронха, которая может быть первичной или
вторичной. Основными причинами первичной
несостоятельности культи бронха являются
следующие: 1) некроз стенки бронха в связи
с чрезмерным раздавливанием браншами аппа­
рата при наложении механического шва или
из-за нарушения питания стенки культи после
скелетирования бронха; 2) тяжелые патологи­
ческие изменения стенки бронха в зоне шва при
гнойно-деструктивных заболеваниях легких,
раке бронха; 3) наложение механического шва
на утолщенную или склерозированную стенку
бронха без дополнительных узловых швов
и плевризации культи; 4) другие технические
погрешности ушивания культи бронха; 5) нару­
шение репаративных процессов у истощенных
больных.
Первичная несостоятельность культи обра­
зуется обычно в течение первых дней после опе­
рации, а в более поздние сроки может наблю­
даться вторичная несостоятельность в условиях
уже развившейся эмпиемы плевры. Из работ
Л. Л. Дорфман (1938), Ю. А. Муромского (1963)
известно, что танталовые скрепки и швы сохра­
няют герметизм культи бронха в течение 10—
14 дней. В дальнейшем они могут прорезаться,
но герметичность бронха обычно сохраняется
благодаря фибринным напластованиям поверх
культи и прорастания в них фибробластов. Под
воздействием ферментов гнойного экссудата
при эмпиеме фибрин лизируется, репаративные
процессы нарушаются, возникает вторичная
несостоятельность культи. И первичная, и вто­
ричная несостоятельности культи бронха под­
держивает гнойный процесс в плевральной поло­
сти и чаще всего заканчивается формированием
бронхиального свища.
В зависимости от состояния первичного пато­
логического процесса, вызвавшего образование
свища, и степени вторичных изменений окру­
жающих тканей различные формы бронхиаль­
ных свищей отличаются особой патоморфологической характеристикой.
Наружный бронхокожный свищ
может образоваться после ранения или после
вскрытия абсцесса легкого при облитерирован­
ной плевральной полости. Различают [Джане­
лидзе Ю. Ю., 1948; Григорьев М. С., 1955] два
вида бронхокожных свищей: губовидный и труб­
чатый или каналовидный. Губовидный брон­
хиальный свищ открывается или непосредствен­
но на кожу, или при помощи короткого канала,
стенки которого выстланы многослойным ци­
линдрическим и плоским эпителием, развившим­
219
ся за счет метаплазии эпителия бронха, пере­
ходящего в эпителиальный покров кожи. Труб­
чатый бронхиальный свищ сообщает просвет
бронха с внешней средой через более длинный
и извилистый канал, покрытый грануляцион­
ной тканью. Наличие грануляционной ткани,
не покрытой эпителием, при благоприятных
условиях дает возможность окончательного
заживления свища без оперативного вмеша­
тельства. Трубчатый бронхокожный свищ мо­
жет сформироваться как исход бронхоплев­
рального свища, если плевральная полость по­
степенно облитерируется вплоть до свищевого
хода, проходящего через плевральные шварты.
Бронхокожные свищи могут быть и множе­
ственными, если в результате ранения или пато­
логического процесса произошла значительная
деструкция легочной ткани с повреждением
многих ветвей бронхиального дерева. В таких
случаях может образоваться и «решетчатое
легкое» [Sauerbruch, 1934], когда бронхиаль­
ные свищи открываются не на кожу, как при
множественных бронхокожных свищах, а в
углубления, бухты и карманы, выстланные мно­
гослойным плоским эпителием из бронхов
и разделенные гребешковыми перекладинами
из сосудов, бронхов и соединительнотканных
элементов легкого.
Бронхоплевральные свищи могут
быть наружными (бронхоплеврокожными) и
внутренними, сообщающимися лишь с остаточ­
ной плевральной полостью. Бронхоплевраль­
ные свищи также бывают одиночными и мно­
жественными. Эпителий, выстилающий брон­
хоплевральные свищи, как и при бронхокож­
ных свищах, метаплазируется в многослойный
плоский, который выходит на поверхность лег­
кого и покрывает его на небольшой площади
вокруг свища. При множественных бронхо­
плевральных свищах на ограниченном участке
легкого эта поверхность иногда вся покрыва­
ется многослойным плоским эпителием, кото­
рый препятствует облитерации плевральной
полости. Как показали исследования П. П. Движкова (1945), С. С. Вайля (1948), М. С. Гри­
горьева (1955), многослойный эпителий брон­
хиальных свищей расположен на плотной сое­
динительнотканной основе, так как изменения
в бронхах при свищах носят характер хрониче­
ского воспалительного процесса по типу пан­
бронхита. Стенка бронха значительно утолщена
за счет инфильтрации лейкоцитами и лимфоид­
ными элементами, которая распространяется
и на легочную паренхиму. Мышечный слой
бронха из-за воспалительной инфильтрации
разъединяется на отдельные волокна, которые
затем атрофируются. Хрящ бронха подверга­
ется дегенеративным изменениям. В результате
перибронхита и развития соединительной тка­
ни стенки бронхиального свища становятся
ригидными, не спадаются. В окружающей свищ
легочной ткани, особенно при множественных
бронхиальных свищах, развивается интерстици­
альный процесс с утолщением альвеолярных
перегородок, разрастанием соединительной
ткани, утолщением стенок сосудов и сужением
их просвета, в дальнейшем с исходом в пнев­
москлероз (карнификацию легкого). Во многих
случаях в легочной ткани развиваются неболь­
шие гнойные полости, сливающиеся между
собой и открывающиеся в просвет бронхов по
типу бронхоэктазий.
Бронхолегочные свищи представ­
ляют собой сообщение бронха с одной или не­
сколькими полостями в легких, образовавши­
мися или в результате абсцесса, или по ходу
раневого канала, или вокруг инородного тела.
Стенки длительно существующих полостей в
легком иногда покрыты метаплазированным
эпителием бронха, что препятствует их облите­
рации. Изменения в легочной ткани вокруг по­
лости и бронхиального свища могут быть раз­
личными: от воспалительной инфильтрации до
пневмосклероза или даже до гнойно-деструк­
тивного процесса в легком. Это имеет важное
значение в выборе лечебной тактики.
М. С. Григорьев (1955) различает наружные
и внутренние бронхолегочные свищи, а также
бронхолегочно-плевральные наружные и внут­
ренние свищи. По опыту клиники, свои специ­
фические особенности имеют только внутренние
бронхолегочные свищи. Наружные бронхолегоч­
ные и бронхолегочно-плевральные свищи прак­
тически не отличаются соответственно от брон­
хокожных и бронхоплеврокожных свищей с
гнойно-деструктивным процессом в легком, а
внутренний бронхолегочно-плевральный свищ
идентичен внутреннему бронхоплевральному с
распадом в легком.
В очень редких случаях, преимущественно
после торакоабдоминальных ранений, бронхо­
легочные свищи могут соединяться с полост­
ными и неполостными органами и образуются
бронхоорганные
свищи
(бронхо­
желудочные, бронхокишечные, бронхопище­
водные, бронхопеченочные). Встречаются при­
обретенные бронхопищеводные свищи после
операций на пищеводе.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
И ДИАГНОСТИКА
Клиническая картина складывается из общих
проявлений заболевания, обусловленных вос­
палительными и гнойно-деструктивными из­
менениями в плевре и легком, и из местных
симптомов, определяющихся видом брон­
хиального свища, размером дренируемой им
220
полости, а также степенью воспалительных изме­
нений стенок полости и тканей грудной стенки.
Общие клинические проявления могут быть
следствием острой или обострения хрониче­
ской эмпиемы плевры и выражаются призна­
ками гнойной интоксикации и дыхательной
недостаточности (высокая температура тела,
ознобы, общая слабость, плохой аппетит, голов­
ные боли, раздражительность, боли в груди,
одышка, кашель с выделением гнойной мокро­
ты, иногда кровохарканье). Это наблюдается
при образовании бронхоплеврального или брон­
холегочного свища в результате прорыва содер­
жимого полости эмпиемы в бронхиальное
дерево или гноя из абсцесса легкого в бронх
или в плевральную полость. В дальнейшем фор­
мируется бронхиальный свищ, полость очища­
ется от гноя и общие проявления уменьшаются.
В большинстве случаев бронхиальный свищ
представляет собой хроническое страдание
и диагностируется преимущественно на осно­
вании местных симптомов и специальных мето­
дов исследования в зависимости от вида свища.
Наружные бронхиальные свищи (бронхокож­
ные, бронхоплеврокожные) диагностируются
прежде всего на основании жалоб больного
(наличие торакального свища со слизисто-гной­
ным или слизистым отделяемым, прохожде­
ние воздуха через свищ при кашле, натуживании, иногда и при дыхании, усиление кашля
в положении больного на здоровом боку из-за
затекания содержимого полости в бронхиаль­
ное дерево, невозможность купаться из-за по­
падания воды в свищ с резким приступом кашля
вплоть до удушья).
При больших наружных бронхиальных сви­
щах больные плохо переносят снятие повязки,
так как у них усиливается кашель, нарастают
одышка, цианоз, иногда наступает афония изза невозможности создания повышенного дав­
ления в бронхиальном дереве, необходимого
для вибрации голосовых связок. Кашель, одыш­
ка и нарастающий цианоз обусловлены спазмом
бронхов вследствие раздражения их слизистой
оболочки холодным воздухом, проникающим
через свищ. Эти явления развиваются не у всех
больных. У некоторых при открытом наружном
бронхиальном свище и закрытой носоглотке
возможно даже дыхание через свищ.
При бронхокожных трубчатых свищах из-за
извитого и узкого свищевого хода, частично
выполненного грануляциями, не всегда наблю­
дается прохождение воздуха при кашле. Иног­
да это удается определить простыми приемами:
запотеванием зеркала, приставленного к отвер­
стию свища, колебанием пламени свечи или
горящей спички, поднесенными к наружному
отверстию бронхиального свища, выхождением
дыма через свищ у курящего больного. Если
эти данные недостаточно убедительны, то ха­
рактер наружного бронхиального свища необ­
ходимо подтвердить специальными методами
исследования.
Зондирование свища (лучше тонким резино­
вым катетером) иногда позволяет дифференци­
ровать бронхиальный свищ от плеврокожного
или свища грудной стенки, так как возникно­
вение кашлевого рефлекса свидетельствует о
связи свища с бронхиальным деревом. Однако
при извилистых свищевых ходах зондом не
всегда можно достигнуть бронха. В таких слу­
чаях целесообразно через катетер ввести в свищ
2—3 мл водного раствора метиленового синего.
Откашливание окрашенной мокроты сразу или
через некоторое время после введения раствора
подтверждает наличие бронхиального свища.
У многих больных проводится промывание сви­
щевого хода или дренируемой им полости ан­
тисептическими растворами. Это имеет и диагно­
стическое значение, так как появление кашля
и привкуса лекарства свидетельствует о несо­
стоятельности легочной ткани или небольшом
бронхиальном свище. При большом размере
свища больной откашливает мокроту с приме­
сью антисептического раствора. Следует пом­
нить, что отрицательная проба с введением кра­
сящего раствора или отсутствие кашля при про­
мывании не исключают наличия бронхиаль­
ного свища, который в момент исследования
может быть закрыт слизью или гноем.
Фистулография является ценным методом
исследования при наружных свищах, так как
позволяет уточнить характер свищего хода, на­
личие и конфигурацию полостей, выявляет связь
с ребрами, пораженными остеомиелитом. Во
многих случаях удается получить также селек­
тивную бронхограмму и уточнить локализацию
и размеры бронхиального свища, что имеет важ­
ное значение в выборе плана и объема опера­
тивного вмешательства.
Техника фистулографии проста. Через сви­
щевой ход вводится катетер соответственно
диаметру свища. Для герметизации свищевого
хода накладывается кисетный шов вокруг кате­
тера. С целью предупреждения кашля в свищ
через катетер вводятся 1—2 мл раствора тримекаина или смесь Гирша. Через 2—3 мин под
контролем рентгеноскопии вводится контрастное
вещество и делаются полипозиционные рент­
генограммы. Герметизация свищевого хода
иногда может быть достаточной и без наложе­
ния кисетного шва, если после введения конт­
растного вещества сразу удалить катетер и в
наружное отверстие свища ввести плотную мар­
левую пробку, пропитанную вазелиновым мас­
лом. Эта методика герметизации показана тогда,
когда поверхность вокруг наружного отверстия
свища легкоранима и швы прорезаются.
221
По опыту клиники, наиболее выгодны для
фистулографии водорастворимые контрастные
вещества (кардиотраст, уротраст, верографин
и др.), однако в некоторых случаях можно ис­
пользовать и масляные контрастные растворы
(йодолипол), подогретые до температуры тела.
При фистулографии и ретроградной селек­
тивной бронхографии не всегда удается выяс­
нить состояние бронхиального дерева и легоч­
ной ткани вокруг свища. Поэтому в ряде слу­
чаев для определения плана лечения необхо­
дима бронхография.
Важное диагностическое значение имеет
бронхоскопия, предпринимаемая для оценки
состояния слизистой оболочки бронхиального
дерева, так как при выраженном гнойном брон­
хите ушивание или пластика свища, как пра­
вило, обречены на неудачу.
Торакоскопия допустима в тех случаях,
когда через свищ в грудной стенке можно вве­
сти в полость торакоскоп. Использование фиброторакоскопа иногда позволяет уточнить коли­
чество бронхиальных свищей, их локализацию,
диаметр, а также оценить характер изменений
стенок полости [Сергеев В. М., Катковский Г. Б.,
1975].
Внутренние бронхиальные свищи диагности­
руются на основании клинической картины и
специальных методов исследования. Так, для
бронхолегочных и внутренних бронхоплев­
ральных свищей характерно увеличение коли­
чества откашливаемой мокроты при изменении
положения больного. Важное значение имеют
рентгенологические методы исследования для
оценки состояния легкого, в том числе и томо­
графия. Особенно ценны данные бронхографи­
ческого исследования.
Наличие внутренних бронхоплевральных сви­
щей определяется при пункции и манометрии
плевральной полости. Для манометрии исполь­
зуется пневмотораксный аппарат. Невозмож­
ность создания отрицательного давления при
отсасывании воздуха из плевральной полости
указывает на наличие сообщения ее с бронхи­
альным деревом. Манометрия плевральной
полости особенно важна для ранней диагности­
ки послеоперационных бронхиальных свищей.
Если полость дренирована, то диагностика брон­
хиальной несостоятельности основывается на
невозможности создания разрежения в плев­
ральной полости при подключении дренажа
к вакуумному устройству. Очень удобен в этом
отношении послеоперационный отсасыватель
ОП-1 Лавриновича — Каншина, так как нали­
чие индикаторной лампочки позволяет ориен­
тировочно судить о диаметре открывающегося
в плевральную полость бронха.
Бронхо органные свищи имеют специфические
особенности клинической картины: кашель или
поперхивание при приеме пищи укажут на
бронхопищеводный свищ, а при изменении по­
ложения больного — на бронхожелудочный
или бронхокишечный свищ. Окончательная диа­
гностика их становится возможной благодаря
селективной бронхографии, контрастным рентге­
нологическим исследованиям желудочно-ки­
шечного тракта, а также по данным эзофагогастроскопии.
ЛЕЧЕНИЕ
В большинстве случаев одновременно с об­
следованием больного проводится общее лече­
ние, направленное на ликвидацию или значи­
тельное уменьшение гнойной интоксикации,
коррекцию важнейших нарушений, вызванных
основным патологическим процессом. Следует
помнить, что нередко свищевой ход является
дренажем для оттока гноя из патологических
полостей. Преждевременные попытки закрытия
этих свищей приводят лишь к неоправданной
деформации грудной клетки. Нельзя закрывать
бронхиальные свищи при наличии инородных
тел, поддерживающих гнойный процесс. Удале­
ние таких инородных тел может привести к са­
мопроизвольному заживлению свища.
Наиболее благополучное течение наблюдается
при бронхокожных трубчатых свищах, которые
могут заживать самостоятельно или после не­
сложного консервативного лечения. Губовидные свищи более стойкие и, как правило, тре­
буют настойчивого консервативного или. даже
оперативного лечения. Наружные бронхоплев­
рокожные. свищи под воздействием консерва­
тивного лечения в результате облитерации плев­
ральной полости могут превращаться в труб­
чатые бронхокожные свищи сложной конфигу­
рации, при которых чаще всего показано опе­
ративное закрытие свища.
Известные способы консервативного лече­
ния наружных бронхиальных свищей следует
разделить на две группы: способствующие са­
нации гнойных полостей и стенок свищевых
ходов и разрушающие эпителиальную выстилку
свищей, стимулирующие разрастание соедини­
тельной ткани.
К первой группе относится промывание гной­
ной полости антисептическими растворами. Как
правило, это делается через свищевой ход. При
значительной задержке гноя в полости и пло­
хом дренировании через свищ проводятся торакоцентез и активное вакуумное дренирование
плевральной полости в наиболее выгодном ниж­
нелатеральном отделе ее. Систематическая
санация полости через свищ или через дре­
наж приводит к быстрому уменьшению инток­
сикации, очищению стенок полости и свище­
вого хода, что очень важно в плане подготовки
222
к оперативному лечению. Антибиотики в плев­
ральную полость целесообразно вводить только
с учетом чувствительности к ним микроорганиз­
мов. В результате такой санации небольшие
остаточные полости иногда облитерируются за
счет фибринных напластований, сохраняется
лишь бронхокожный трубчатый извилистый
свищевой ход. Если он поддерживается сооб­
щением с маленьким бронхом, то устье его мо­
жет закрыться и свищ заживает.
При больших бронхиальных свищах эффек­
тивное промывание гнойной полости затрудне­
но или невозможно из-за аспирации раствора
в бронхиальное дерево. В таких случаях целе­
сообразно выполнить временную окклюзию
бронха, имеющего свищ, поролоновой плом­
бой. Последующий фракционный лаваж и по­
стоянная активная аспирация из полости позво­
ляют за сравнительно короткое время подгото­
вить больного к оперативному закрытию брон­
хоплеврального свища и остаточной плевраль­
ной полости.
Консервативные мероприятия второй группы
применяются в более отдаленные сроки при
сформировавшихся наружных бронхиальных
свищах и удовлетворительном состоянии боль­
ных. К этим мероприятиям относятся: прижи­
гание свища химическими компонентами, физи­
ческими средствами, лучевое и механическое
воздействие на свищ.
Из химических компонентов в разное время
применялись палочки, кристаллы и растворы
нитрата серебра, спиртовой раствор йода, кар­
боловая кислота, протаргол в комбинации с
генцианвиолетом и др. Наибольшее распростра­
нение получили 30—50 % растворы нитрата
серебра.
Электрокоагуляция свища, прижигание аппа­
ратом Пакелена также приводит к разрушению
эпителиальной выстилки бронхиального сви­
ща, что способствует развитию грануляцион­
ной ткани и при благоприятных условиях может
закончиться выздоровлением. М. Iselin (1944)
при небольших бронхокожных свищах реко­
мендовал электроножом освободить устье сви­
ща от окружающих тканей, а сам свищ после
этого прижигал электроножом. Иногда при­
жигание повторяется многократно до оконча­
тельного закрытия свища.
Благоприятные результаты рентгенотерапии
при наружных бронхиальных свищах отмечал
Б. Э. Линберг (1945), а С. Garre еще в 1904 г.
описал успешное заживление стойкого брон­
хиального свища введением радия в свищевой
ход. Клинические наблюдения лучевого воз­
действия на бронхиальный свищ единичны.
Несколько чаще применяется выскабливание
свища острой ложечкой [Джанелидзе Ю. Ю.,
1948 и др.] с последующими асептическими
перевязками на фоне общеукрепляющего лече­
ния (анаболическими гормонами, пиримидино­
выми производными, витаминами).
Сроки заживления наружных бронхиальных
свищей при консервативном лечении длитель­
ные — в среднем 3—4 мес. Примерно в поло­
вине случаев различные методы консерватив­
ного лечения не приводят к стойкому заживле­
нию, и требуется оперативное лечение [Джа­
нелидзе Ю. Ю„ 1948; Муромский Ю. А., 1963].
Сроки оперативного закрытия наружных
бронхиальных свищей колеблются от 4—6 нед
до 5—6 мес от момента образования свища.
Некоторые хирурги советуют еще больше выжи­
дать с оперативным вмешательством в расчете
на стойкое заживление свища под влиянием
консервативного лечения. По опыту клиники
оперативное закрытие наружных бронхиальных
свищей следует предпринимать тогда, когда нет
признаков гнойной интоксикации и задержки
гноя в полости, стихли воспалительные явле­
ния в легком и окружающих свищ тканях,
нет инородных тел или остеомиелита ребер,
поддерживающих гнойный процесс, а также
отсутствует дальнейшая положительная дина­
мика, несмотря на продолжающееся консерва­
тивное лечение. Чрезмерное затягивание кон­
сервативного лечения приводит лишь к уплот­
нению рубцовой ткани в легком и вокруг сви­
щевого хода и затрудняет выполнение операции.
Объем хирургического вмешательства опре­
деляется в зависимости от вида наружного сви­
ща, его локализации, наличия и величины стой­
кой остаточной плевральной полости, а также от
характера изменений тканей, окружающих сви­
щевой ход. Различают три группы способов опе­
ративного закрытия наружных бронхиальных
свищей: 1) ушивание бронхиального свища;
2) свободная пластика бронхиального свища
различными тканями; 3) пластика бронхиаль­
ного свища мышечным лоскутом на ножке.
Ушивание бронхиального с в ищ а может быть без иссечения и с иссечением
его. Менее всего оправдано наложение швов на
склеротически измененные ткани бронхиального
свища, так как плохое кровоснабжение этих тка­
ней способствует развитию инфекции и реци­
диву свища. Более эффективно ушивание свища
после иссечения рубцово-измененных тканей.
Это возможно при бронхокожных свищах.
По ходу операции свищ отсепаровывают от
окружающей рубцовой ткани, слизистую обо­
лочку бронха в области устья выскабливают
острой ложечкой или выжигают электрокоагу­
ляцией, бронх перевязывают у основания, и
свищевой ход отсекают. Бронх, освобожденный
от фиксирующих его рубцовых тканей, после
этого частично втягивается в легочную ткань.
Рану легкого и грудную стенку ушивают.
223
Свободная пластика различными
тканями при бронхиальных свищах имеет лишь
историческое значение. Для этих целей исполь­
зовали раньше надкостницу из соседних ребер
[Mayer W., 1909], фасцию [Hirano J., 1913],
мышцы [Смирнов С. А., 1924]. Наиболее впе­
чатляющие результаты получил Н. Neuhof
(1937), который применил свободную пересад­
ку жиром при множественных бронхиальных
свищах у 17 больных: у 11 из них получено пол­
ное излечение.
Мышечная пластика на ножке
для лечения бронхиальных свищей предложена
отечественным хирургом А. А. Абражановым
(1899). Автор описал технику своего способа
мышечной пластики свищей и подчеркнул, что
для успеха операции необходимы два условия:
объем полости должен быть невелик, и секве­
стры, омертвевшая клетчатка, поддерживаю­
щие гнойный процесс, следует удалить. Длина
свищевого хода не является противопоказанием
к операции, так как его можно заполнить двумя
мышечными лоскутами через отдельные отвер­
стия.
В последующие годы пластика различных
бронхиальных свищей мышечным лоскутом на
ножке с успехом использовалась многими отече­
ственными и зарубежными хирургами. Следует
подчеркнуть важное предложение А. П. Кры­
мова (1924): не разъединять сращения легкого
с грудной стенкой, если они имеются, а лишь
подвести мышечный лоскут к просвету брон­
хиального свища и закупорить его (как горлыш­
ко бутылки пробкой), укрепив сверху несколь­
кими швами.
В зависимости от локализации бронхиального
свища и состояния окружающих свищевой ход
тканей для пластики могут быть использованы
mm. pectoralis, latissimus dorsi, serratus anterior,
romboideus, erector spinae и др. Мышечный лос­
кут следует выкраивать на широком основании,
сохраняя ветви основных артерий мышцы. Сле­
дует помнить, что мышечный лоскут после пере­
сечения дистального конца сокращается почти
вдвое. Нельзя допускать значительного натя­
жения и перегиба лоскута в момент перемеще­
ния для пластики или поворота его по плоскости
до прямого угла [Богуш Л. К., Диденко В. Ф.,
1975]. При длинном бронхоплеврокожном свище
и отсутствии остаточной плевральной полости
можно использовать неизмененные межребер­
ные мышцы после поднадкостничной резек­
ции фрагментов двух соседних ребер. При нали­
чии остаточной полости плевры мышечный ло­
скут должен полностью заполнить все ее карма­
ны, причем мышцу фиксируют не только в зоне
бронхиального свища, но и ко дну и стенкам
полости швами, не нарушая ее кровоснабже­
ния (швы накладываются не поперек, а по ходу
сосудистого пучка мышечного лоскута). Опе­
рация заканчивается дренированием полости
и раны мягких тканей через отдельные контра­
пертуры, герметичным ушиванием раны мяг­
ких тканей и наложением давящей повязки с
пелотом (ватно-марлевым, а лучше — из поро­
лоновой губки).
Наиболее трудная хирургическая задача сто­
ит при лечении больных с «решетчатым» лег­
ким. Предложены различные оперативные вме­
шательства, которые можно объединить в 4 груп­
пы: 1) мышечная пластика «решетчатого» лег­
кого с иссечением или без иссечения его эпите­
лиальной выстилки; 2) торакопластика или ее
сочетание с мышечной пластикой «решетчатой»
поверхности легкого; 3) резекция «решетчатого»
легкого в сочетании в торакопластикой; 4) пнев­
монэктомия.
Объем операции определяется прежде всего
характером изменений легочной паренхимы
вокруг множественных бронхиальных свищей,
а также состоянием мышц и других тканей груд­
ной стенки, которые могут быть использованы
для пластики. Пластическое закрытие «решет­
чатой» поверхности возможно лишь при не­
значительных патологических изменениях лег­
кого. При наличии гнойно-деструктивного про­
цесса в легком и бронхах по типу бронхоэкта­
зий или хронических абсцессов, как правило,
необходима резекция легкого в сочетании с
торакопластикой, а также удаление всего лег­
кого. Для закрытия «решетчатого» легкого или
множественных бронхоплевральных свищей
применяется несколько модификаций способа
А. А. Абражанова.
При операции Лебше [Lebsche М., 1925]
окаймляющим разрезом рассекают ткани на
границе между кожей и «решетчатой» поверх­
ностью легкого, проникают вглубь до плевры
и хорошо распознаваемой легочной ткани. Уп­
лотненный край тканей отсепаровывают со всех
сторон и срезают вокруг свищей. Частыми
швами тонким шелком легкое погружают так,
чтобы швы не проникали в просвет инвагинируемого слизистого мешка. Рана покрывается
лоскутом жира или мышцы на ножке, под лос­
кутом оставляется дренаж на 1—2 дня, кото­
рый вводится через отдельный разрез. Кожа
мобилизуется на достаточном протяжении и
ушивается с оставлением нескольких насечек
для предупреждения образования гематомы.
При операции Ниссена [Nissen R., 1932] окай­
мляющим разрезом обнажают и резецируют
фрагменты ребер для полного открытия «ре­
шетчатой» поверхности легкого. Отсепаровы­
вают и отсекают только рубцовые края полости, ,
эпителиальную выстилку на легком не удаляют.
Мобилизуют мышечный лоскут на широком
основании, покрывают им «решетчатую» по-
224
верхность легкого и фиксируют кетгутовыми
швами. Полость под лоскутом дренируют, рану
ушивают.
Приживление мышечного лоскута к «решет­
чатой» поверхности легкого происходит мед­
ленно. Вначале значительно увеличивается ко­
личество отделяемого по дренажу, что обуслов­
лено, вероятно, слущиванием эпителиального
покрова. Через 14—28 дней восстанавливается
герметизм легкого, и постепенно рана оконча­
тельно заживает.
При аналогичной операции в модификации
Лециуса [Lezius А., 1938] резецируют фраг­
менты ребер не только над «решетчатым» лег­
ким, а значительно шире — на 7—10 см от
свищей. Кроме того, иссекаются краевые спай­
ки и соединительнотканные тяжи. Этим умень­
шается напряжение рубцов на висцеральной
плевре и сокращаются размеры «решетчатой»
поверхности легкого.
Операция Л. К. Богуша [Богуш Л. К., Ди­
денко В. Ф., 1975], наоборот, заключается в
наиболее полном выделении латеральной по­
верхности легкого со свищами, иссечении руб­
цовых и нежизнеспособных тканей, выскабли­
вании «решетчатой» поверхности легкого. Устья
свищей обрабатываются 80 % раствором три­
хлоруксусной кислоты и зашиваются отдельны­
ми П-образными капроновыми швами. После
этого выделенная поверхность легкого с гер­
метично ушитыми свищами «гофрируется» по­
перечными кисетными швами на расстоянии
1 —1.5 см один от другого, а сверху плевризуется дополнительным рядом узловых швов.
Ушитая поверхность легкого покрывается мы­
шечным лоскутом на ножке с фиксацией его
не только по краям, но и в центре несколькими
толстыми капроновыми лигатурами, предва­
рительно проведенными достаточно глубоко
под линией швов легкого и выведенными через
подкожно-кожный массив наружу. Под мышеч­
ным лоскутом оставляют микроирригатор для
введения антибиотиков в течение 2—3 дней после
операции. Рану ушивают. Свободные концы кап­
роновых лигатур туго завязывают над марле­
выми валиками на коже, плотно придавливая
кожно-подкожно-мышечный массив к поверх­
ности легкого.
Торакопластика и ее сочетание с мышечной
пластикой «решетчатого» легкого применяются
при больших размерах остаточной плевраль­
ной полости.
При значительных патологических измене­
ниях легочной ткани и бронхов, когда клини­
ческая картина обусловлена не столько на­
личием бронхоплевральных или бронхокожных
свищей, сколько гнойно-деструктивным процес­
сом в легких, пластическое закрытие свищей
может лишь ухудшить состояние больного.
15 Зак. 0517
В этих случаях показана резекция доли
или всего легкого.
Консервативное лечение внутренних брон­
хиальных свищей начинается, как правило, с
мероприятий, которые преследуют две основ­
ные задачи: санацию полостей, очагов гной­
ного процесса и ликвидацию свищей, патоло­
гических полостей.
Следует подчеркнуть, что при наличии внут­
реннего бронхоплеврального свища санация
гнойной полости значительно затруднена, иног­
да невозможна без оперативного вмешательства.
Так, при эмпиеме с бронхоплевральным сви­
щом, сопровождающейся выраженной гнойной
интоксикацией, эффективная санация полости
возможна лишь при открытом дренировании
ее одним из методов торакостомии с последую­
щим ведением как при наружных бронхоплев­
рокожных свищах. При бронхолегочных сви­
щах наличие стойкого сообщения бронхиаль­
ного дерева с полостью абсцесса в легком позво­
ляет санировать ее через дренирующий бронх.
Вопрос о ликвидации стойких внутренних
бронхиальных свищей должен решаться только
после тщательной санации полости и основного
очага гнойного процесса.
За последние годы возросла роль эндоскопи­
ческих мероприятий с целью ликвидации внут­
ренних бронхиальных свищей, особенно при не­
состоятельности или свище культи бронха после
операций на легких. Различают три группы ме­
роприятий, которые могут быть выполнены
через бронхоскоп [Белкин В. Р., 1973]. К 1-й
группе относится удаление лигатур из культи
бронха, так как они при развившемся бронхиаль­
ном свище поддерживают хроническое воспа­
ление в стенке бронха. Удаление лигатур иногда
ведет к заживлению культи. 2-я группа меро­
приятий — прижигание слизистой оболочки
культи бронха в области свищевого отверстия
химическими препаратами (30—50 % раство­
ром нитрата серебра, 40—50% раствором гид­
рата окиси натрия и др.), разрушающими эпи­
телиальную выстилку свища и стимулирующими
рост грануляционной ткани. Манипуляции по­
вторяются через 3—4 дня, всего 5—7 и более
сеансов за курс лечения. При небольших отвер­
стиях (2—3 мм в диаметре) эти мероприятия
нередко ведут к заживлению свища. 3-я группа
мероприятий направлена на эндобронхиаль­
ное закрытие дефекта культи бронха с помощью
цианакрилатного клея и биологических пла­
стических материалов.
В клинике госпитальной хирургии для этих
целей использовали клеевые композиции МК-6
или МК-7 и коллагеновые пломбы, приготов­
ленные в Центральной научно-исследователь­
ской лаборатории по изучению и применению
коллагена в медицине I Московского медицин­
225
ского института имени И. М. Сеченова. Циана­
крилатные клеевые композиции, по данным
В. Р. Белкина (1969), А. Я. Акимовой и соавт.
(1973), обладают адгезией к тканям в условиях
относительной влажности, нетоксичны, не пре­
пятствуют нормальному течению репаративных
процессов, имеют антибактериальные свойства,
подвергаются постепенному гидролизу и расса­
сыванию в тканях. Коллагеновые пломбы яв­
ляются пористыми губками, которые прора­
стают фибробластами из краев дефекта и по­
степенно рассасываются. Добавление антибио­
тиков (мономицина) и стимуляторов репара­
тивных процессов (метилурацила) в процессе
приготовления коллагеновых пломб усиливает
их благоприятное воздействие на ткани.
При любой методике заклеивания культи
бронха большое значение имеет строгое соблю­
дение ряда условий. Во-первых, необходима
заблаговременная подготовка вспомогательных
инструментов и пломбы, размер которой дол­
жен быть несколько большим, чем диаметр де­
фекта культи. Во-вторых, надо тщательно под­
сушить слизистую оболочку культи и быстро
выполнить все последующие манипуляции. Втретьих, клеевую композицию необходимо на­
носить тонким слоем и лишь в зоне дефекта
культи. В-четвертых, коллагеновую пломбу
необходимо в течение 30—40 с плотно прижи­
мать к дефекту.
Перед удалением бронхоскопа повторяется
анестезия слизистой оболочки культи, карины
и подсвязочного пространства для подавления
кашля. В последующем кашель желательно по­
давлять приемом противокашлевых средств —
глауцина, текодина, кодеина и др. После заклеи­
вания дефекта культи обязательно продолжа­
ется санация остаточной плевральной полости
с введением антисептиков и антибиотиков для
подавления инфекционного процесса. Нельзя
допускать задержки гноя в полости, однако
промывание ее должно быть очень осторож­
ным, лучше через двухпросветный дренаж.
В клинике использовали эту методику у боль­
ных с послеоперационными свищами культи
долевых (у 11) и главного (у 9) бронхов. Окон­
чательно ликвидировать свищ удалось у 16 боль­
ных. У остальных наступило отторжение или
расплавление пломбы раньше, чем в нее прора­
стала грануляционная ткань культи. Однако и
в этих неудачных случаях временное закрытие
дефекта культи способствовало лучшей сана­
ции полости эмпиемы, снятию интоксикации,
уменьшению дыхательной недостаточности.
У некоторых больных эндобронхиальное закры­
тие дефекта культи бронха проводили повтор­
но, а у трех его сочетали с широкой торако­
стомией. Открытое ведение полости эмпиемы
у этих больных позволило хорошо очистить ее
стенки и способствовало окончательному закры­
тию культи бронха грануляциями и фибринными напластованиями со стороны полости.
Анализ этого материала позволяет выделить
следующие основные причины неудачных по­
пыток эндобронхиального заклеивания дефек­
тов культи бронха: 1) большие дефекты куль­
ти — более 5 мм в диаметре; 2) недостаточно
разрушенная эпителиальная выстилка бронхи­
ального свища и отсутствие грануляционной
ткани в зоне дефекта; 3) выраженный гнойный
или эрозивный эндобронхит; 4) недостаточное
просушивание слизистой оболочки в зоне куль­
ти и несоблюдение других принципов эндоброн­
хиального заклеивания дефектов бронха; 5)
плохая санация эмпиемы до момента заклеи­
вания культи и задержка гноя в полости в первые
дни после окклюзии свища; 6) очень активное,
неосторожное промывание полости через дренад после заклеивания культи до заживления
ее дефекта. Можно предположить, что раз­
работка новых клеевых композиций с лучшими
адгезивными свойствами в условиях относи­
тельной влажности живых тканей, создание бо­
лее совершенных инструментов и усовершенст­
вование методики позволят чаще с успехом ис­
пользовать эндобронхиальное закрытие внут­
ренних бронхиальных свищей.
Оперативное лечение внутренних бронхиаль­
ных свищей. Задачей оперативного вмеша­
тельства является не только устранение брон­
хиального свища, но и ликвидация остаточной
плевральной полости.
При небольших бронхоплевральных свищах,
удовлетворительном состоянии легочной ткани,
не очень плотных фибринных напластованиях
на висцеральной плевре, хорошо санированной
полости операцией выбора является декор­
тикация легкого с ушиванием и
инвагинацией
бронхиального
свища. Если же декортикация невозможна,
выполняется торакопластика, нередко в
сочетании с одним из методов
мышечной
пластики
бронхиального
свища. Оперативное вмешательство при множе­
ственных бронхоплевральных свищах осуще­
ствляется по тем же принципам, что и при «ре­
шетчатом» легком. Наличие бронхиального
свища и выраженного гнойно-деструктивного
процесса в легком по типу хронических абсцес­
сов, бронхоэктазий является показанием к р езекции доли или всего легкого.
Наиболее сложная задача стоит при лече­
нии больных со свищом культи бронха после
пневмонэктомии. При первичной несостоятель­
ности культи в первые 1—2 дня (до развития
эмпиемы) выполняются реторакотомия и пов­
торное ушивание культи главного бронха с обя­
зательной тщательной плевризацией ее. При
226
длинной культе целесообразно произвести вы­
деление ее до карины и ушить повторно аппа­
ратом УКБ с иссечением периферических
краев культи и дополнительным ушиванием
П-образны'ми или узловатыми швами. В ряде
случаев, особенно после пневмонэктомии по
поводу рака главного бронха, культи бронха
нет, а швы подчас наложены прямо на стенку
трахеи. Ушить дефект у таких больных не­
возможно, хотя описаны единичные успешные
жйждани? цррхуляряр» розотщии трахеи с
наложением анастомоза между трахеей и глав­
ным бронхом другого легкого [Харченко В. IL,
Чхиквадзе В. Д., 1981].
Если же диагностирована вторичная несо­
стоятельность культи главного бронха, ушива­
ние ее и тем более операции на трахее в усло­
виях острой эмпиемы плевры бесперспективны.
В таких случаях необходимо срочное дрениро­
вание плевральной полости для обеспечения
оттока экссудата (гноя) и предупреждения
аспирации его в бронхи другого легкого. При
выраженной гнойной интоксикации и недо­
статочном опорожнении полости через дре­
наж показано открытое дренирование с резек­
цией фрагментов 1—2 ребер в нижнелатераль­
ном отделе плевральной полости. Оперативное
закрытие свища культи главного бронха пред­
принимается только после тщательной санации
полости эмпиемы и значительного улучшения
состояния больного.
Известны три группы оперативных вмеша­
тельств на главных бронхах при бронхиальных
свищах после пневмонэктомии: 1) операции на
культе бронха через полость эмпиемы: 2) опе­
рации на главных бронхах через средостение;
3) операции из контралатерального доступа
со стороны другой плевральной полости.
Большинство хирургов при вмешательствах
через полость эмпиемы производят
реампутацию и ушивание культи главного брон­
ха в сочетании с 7—10-реберной торакопласти­
кой [Богуш Л. К. и др., 1963; Бабашев Б. С.,
Нуркабаев Ч., 1970, и др.], Учитывая чрезмер­
ную травматичность этого вмешательства и рез­
кую деформацию грудной клетки с инвалиди­
зацией больного даже при успешном закрытии
бронхиального свища, И. С. Колесников и ф. И.
Горелов (1965) разработали метод реампута­
ции и ушивания культи бронха через полость
эмпиемы с одномоментным частичным или пол­
ным удалением эмпиемного мешка без торако­
пластики. Плевральную полость затем продол­
жают санировать пункционно или через дренаж
до купирования инфекционного процесса с по­
следующей облитерацией полости за счет по­
степенной организации экссудата.
Операции на главных бронхах через сре­
достение
осуществляют трансстерналь­
15*
ным доступом [Перельман М. И., Богуслав­
ская Т. Б., 1963; Богуш Л. К. и др., 1972; Abruzzini Р., 1963]. В большинстве случаев при этом
вскрывают перикард, выделяют и перевязы­
вают культю легочной артерии, а после этого
тупым и острым путем выделяют основание
культи главного бронха и ушивают его аппара­
том У О или УКБ. Ушитую культю бронха отсе­
кают от трахеи, затем дренируют средостение
двумя дренажами: от бифуркации трахеи через
полость перикарда и через отдельный прокол
около мечевидного отростка.
Контралатеральный доступ, по
мнению М. И. Перельмана и Г. П. Амбатьело
(1968), несколько проще трансстернального
доступа к культе левого главного бронха, а к
правому главному бронху он сложнее из-за
необходимости мобилизации дуги аорты. Само
вмешательство на главных бронхах заключается
в выделении и ушивании аппаратом основания
культи, отсечении ушитой культи от трахеи и
ушивании отверстия в периферическом отделе
культи. Линию швов на трахее плевризируют.
Бронхолегочные свищи могут ликвидиро­
ваться самостоятельно в процессе комплекс­
ного консервативного лечения острых абсцессов
легкого, дренирующихся через бронх. В таких
случаях речь идет не о стойком бронхиальном
свище, а о сообщении полости абсцесса с брон­
хом без характерной для свища эпителиальной
выстилки свищевого хода и стенок полости.
Лишь у 10 % больных острые сообщения по­
лостей деструкции в легком с бронхиальным де­
ревом превращаются в стойкие бронхолегочные
свищи, которые поддерживаются хроническим
гнойно-деструктивным процессом в легком (мно­
жественные абсцессы, бронхоэктазии).
Задачей оперативного лечения у таких боль­
ных является не закрытие бронхолегочного сви­
ща, а удаление гнойного очага, т. е. выполня­
ются частичная резекция легко­
го или же пневмонэктомия. В еди­
ничных случаях из-за крайне тяжелого состоя­
ния больного может быть выполнена широкая
пневмотомия с раскрытием и наружным дре­
нированием гнойных полостей в легком. В по­
следующем, при улучшении состояния боль­
ного, выполняется радикальное оперативное
вмешательство: резекция легкого или же мышеч­
ная пластика образовавшихся множественных
бронхиальных свищей («решетчатого» легкого).
При бронхоорганных свищах патологический
процесс в легком поддерживается и нарастает
из-за попадания содержимого желудочно-ки­
шечного тракта или желчных путей в бронхиаль­
ное дерево. Поэтому при длительном суще­
ствовании бронхоорганных свищей
произво­
дится не только разъединение свища, но и ре­
зекция части легкого вплоть до пневмонэктомии.
227
10
Глава
ПЛЕВРЫ
ОПУХОЛИ
Опухоли плевры относятся к числу относи­
тельно редких заболеваний: примерно один боль­
ной на 100 больных раком легкого [Богда­
нов А. В. и др., 1970|. По секционным данным
[Давыдовский И. В., 1940; Палешников Г. С.,
1966; Бондаренко Б. Б., Бойкова Н. В., 1975. и
др.], они встречаются от 0,024 до 0,4 % от всех
вскрытий. Частота опухолей в правой и левой
плевральной полости одинаковая. Двусторон­
няя локализация встречается очень редко, од­
нако у 2 из 5 больных с мезотелиомой, наблю­
давшихся в клинике госпитальной хирургии за
последние годы, была поражена не только плев­
ра обеих половин грудной клетки, но и перикард,
а у одного пациента — и брюшина. По данным
литературы, несколько чаще опухоли плевры
наблюдаются у мужчин пожилого возраста, но
описаны случаи заболеваний и у детей [Чепик О. Ф„ Журавлев А. В., 1979].
Различают первичные и вторичные опухоле­
вые поражения плевры. В данной главе будут
рассмотрены преимущественно первичные опу­
холи, так как вторичными являются метастати­
ческие поражения плевры при злокачественных
процессах в легких, молочной железе и других
органах.
В зависимости от источника опухолевого роста
различают два вида первичных опухолей [В. М.
Сергеева, 1967]: 1) мезотелиальные и 2) ме­
зенхимальные. Мезотелиальные опухоли чаще
всего развиваются из мезотелия, значительно
реже — из соединительнотканной стромы плевры
и ее сосудистых элементов. Мезенхимальные
опухоли происходят из тканей субмезотелиаль­
ного слоя плевры. Большинство мезотелиаль­
ных опухолей являются злокачественными,
мезенхимальные опухоли плевры, как правило,
доброкачественные. Некоторые авторы все опу­
холи из субмезотелиального слоя относят к
опухолям грудной стенки, а опухолями плев­
ры считают лишь мезотелиомы [Fojanini G.,
Picciocchi А., 1960].
Классификацию опухолей плевры можно
представить следующим образом (см. ниже).
МЕЗОТЕЛИАЛЬНЫЕ
ОПУХОЛИ ПЛЕВРЫ
По гистогенетическому принципу большин­
ство первичных опухолей плевры объединяют
в один вид — мезотелиомы. Известны много­
численные синонимы (злокачественная эпите­
лиома плевры, карциноматозная эндотелиома,
саркоматозная эндотелиома, целетелиома, рак
плевры и др.— всего около 40, по данным В. М.
Сергеева 1967), что обусловлено чрезвычай­
ным полиморфизмом их микроструктур. Мезо­
телиальные клетки, покрывающие серозные
оболочки, в процессе роста способны разви­
ваться как в эпителиальном, так и в соедини­
тельнотканном направлении. Некоторые авто­
ры признают возможность перехода соедини­
тельнотканных клеток в мезотелиальные. Раз­
личают диффузную и локализованную (узло­
ватую) формы мезотелиом.
Локализованные или фиброзные мезотелио­
мы относят к условно доброкачественным опу­
холям, так как они отличаются медленным
ростом в виде четко отграниченного узла, заклю­
ченного в богато васкуляризованную капсулу.
Опухоли плевры
Первичные
Мезотелиальные
(чаще злокачественные)
Локализованные мезотелиомы (условно-доброкачест­
венные)
Тератомы
Мезенхимальные
(преимущественно доброкаче­
ственные)
Диффузные мезотелиомы
(злокачестве иные)
Фибромы, липомы,
невриномы, хондромы, ос­
теофибромы, ангиомы
228
Вторичные
( метастатические
поражения плевры
при опухолях лег­
ких, молочных же­
лез и других орга­
нов)
Обычно эти опухоли не дают метастазов, однако
нередко встречаются местные рецидивы после
удаления опухоли [Benoit Н. et al., 1953]. Фиб­
розные мезотелиомы могут исходить из любого
листка плевры, однако из париетальной плевры
они развиваются в 3 раза чаще, чем из висце­
ральной [Clagett О. et al., 1952]. Эти опухоли
могут возникать у людей обоего пола и в любом
возрасте. Иногда узловатые мезотелиомы до­
стигают больших размеров и массы. Ю. Н. Коно­
валовым (1976) описана мезотелиома разме­
рами 21X 14X9 см и массой 2200 г. Макроско­
пически различают две формы локализованных
мезотелиом: 1) свободно расположенные в плев­
ральной полости — обычно доброкачественные;
2) сращенные с легочной тканью — чаще зло­
качественные. Последние имеют менее выражен­
ную капсулу. Ткань опухоли чаще плотная, на
разрезе — слоистая, белого, желтоватого или
красноватого цвета, иногда дольчатого строения
или кистозная. Злокачественные узловатые мезо­
телиомы обычно мягкой тестоватой консистен­
ции.
Гистологический диагноз локализованных
мезотелиом затруднен, так как опухоль пред­
ставлена фиброзной тканью, иногда местами
гиалинизированной, с очагами некроза. Строе­
ние ее напоминает многокамерную фиброму,
и только в культуре ткани удается доказать
мезотелиальное происхождение клеток опухоли.
Злокачественные мезотелиомы отличаются
большим полиморфизмом клеток, их митоза­
ми. Опухолевые клетки иногда образуют бес­
порядочные пучки, иногда приобретают округ­
лую или звездчатую форму. Многие авторы
подчеркивали чрезвычайную вариабельность
гистологических структур злокачественных
мезотелиом плевры по сравнению со злока­
чественными опухолями легких.
Диффузные опухоли плевры являются более
злокачественными и встречаются в 10 раз чаще,
чем локализованные мезотелиомы. Сведения
о частоте этих опухолей трудно считать досто­
верными, так как деление на злокачественные
и доброкачественные мезотелиомы в известной
мере условно. Кроме того, многие опухоли плев­
ры без достаточных оснований были отнесены
к диффузным мезотелиомам, а в действитель­
ности они являлись вторичными метастатиче­
скими поражениями плевры [Willis R., 1953].
Нередко диффузная мезотелиома разрастается
по обоим плевральным листкам, иногда про­
растает в перикард, брюшину. Описан даже слу­
чай инфаркта миокарда, вызванного прораста­
нием мезотелиомы в сердце и сдавлением венеч­
ной артерии [Бабушкин Г. А., 1971].
Макроскопически для этого вида мезотелиом
характерным является диффузное утолщение
париетального, реже — висцерального (иногда
и того и другого) листков, достигающих тол­
щины нескольких сантиметров и окружающих
легкое или сердце в виде плотного панциря.
Серозная полость также может быть выпол­
нена мягкими, сочными опухолевыми массами.
Если серозная полость не подверглась облите­
рации, то в ней скапливается экссудат, быстро
возобновляющийся после пункции и удаления
его. Экссудат в ранние сроки заболевания сероз­
ный или серозно-фибринозный, но вскоре ста­
новится серозно-геморрагическим вследствие
десквамации пораженного мезотелия и частич­
ного распада опухоли. L. Borek и соавт. (1965)
выделяют три стадии развития диффузной
мезотелиомы: I — проявляется возникновением
специфического экссудативного плеврита;
II — неравномерным или пластинчатым утолще­
нием плевры; III — агрессивным распростра­
нением опухоли в окружающие органы, сопро­
вождающимся сморщиванием периферических
отделов легкого и деформацией тканей груд­
ной стенки.
Злокачественная мезотелиома склонна к
быстрой диссеминации по лимфатическим со­
судам. В результате этого возможны возник­
новение опухолевого лимфангита, образование
мелкоузелковых высыпаний и возникновение
метастазов в регионарных лимфатических
узлах. Опухоль часто прорастает в подлежа­
щий орган (легкое, диафрагму) с образованием
мелких узелков и тяжистой опухолевой ткани.
При образовании в плевре или легком одиноч­
ного крупного узла всегда возникает подозре­
ние на метастаз опухоли из другого органа.
При гистологическом исследовании мезоте­
лиом обнаруживается весьма разнообразное
их строение. Наиболее частой формой мезоте­
лиом следует считать эпителиоподобную (пер­
вичный рак плевры). Клетки таких мезоте­
лиом имеют разнообразную величину, упло­
щенную кубическую, реже — низкопризматиче­
скую форму, чаще неправильную, • весьма
склонны к дискомплексации. Эпит лиоподобная форма мезотелиом часто имее преимуще­
ственно тубулярное или сосочк .вое строение.
По гистологической классификации [Чепик
О. Ф., Журавлев А. В., 1979] различают: 1) монофазные злокачественные мезотелиомы —
а) из эпителиоподобных клеток; б) из фибро­
бластоподобных клеток; 2) бифазные злока­
чественные мезотелиомы, в которых сочета­
ются эпителио- и фибробластоподобные клетки.
Описаны мезотелиомы саркоматозного, ангиоматозного строения. Среди первичных зло­
качественных опухолей некоторые авторы вы­
деляют самостоятельную подгруппу — первич­
ные саркомы, которые происходят из субмезо­
телиальной ткани или из мезотелия вследствие
его трансформации в соединительнотканном
229
направлении [Головин Д. И.. 1953]. В. М. Сер­
геев (1967) на основании данных литературы
и собственных наблюдений описал 20 случаев
первичной саркомы плевры и считает, что их
соотношение к первичным ракам плевры равно
1:6,4. Отличительной особенностью сарком
плевры является диффузное распространение
бластоматозного процесса по ходу сосудов
плевры и легкого с прорастанием в их просвет
[Рыжкова Е. В., 1958], а также более интенсив­
ный рост опухоли, что ведет к смещению сре­
достения в здоровую сторону, сглаженности меж­
реберий и выбуханию соответствующей поло­
вины грудной клетки.
Гистологический диагноз мезотелиом и пер­
вичной саркомы плевры возможен на основа­
нии изучения материалов биопсий и безуслов­
ного исключения первичной опухоли легкого.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
И ДИАГНОСТИКА
Клинические проявления в начальный период
заболевания отсутствуют или имеют стертый
характер. Общее состояние больных при первич­
ных опухолях плевры, в отличие от метаста­
тических поражений ее, длительное время оста­
ется удовлетворительным. Это затрудняет
диагностику опухолей плевры в ранних стадиях
развития заболевания, так как больные позд­
но обращаются к врачу.
Наиболее частыми признаками поражения
плевры являются боли в груди, одышка при
небольшой физической нагрузке и скопление
жидкости в плевральной полости. Боли при опу­
холях плевры в начале заболевания не связаны
с дыхательными экскурсиями грудной клетки,
что отличает их от болей другого происхож­
дения. Чаще всего боли постоянные, ноющего
характера. В некоторых случаях болевой синд­
ром проявляется по типу межреберной неврал­
гии, иногда с иррадиацией в плечо; реже быва­
ют приступообразные, опоясывающие боли.
Характерно усиление болей после пункции
плевры, что, по мнению А. Я. Могилевича (1929),
обусловлено тракцией утолщенной плевры или
трением плевральных листков после аспирации
экссудата.
Одышка у больных мезотелиомой, в отличие
от экссудативного плеврита, не уменьшается
после эвакуации плеврального выпота. Она уси­
ливается в вертикальном положении больного.
Развитие одышки обусловлено не только скоп­
лением экссудата в плевральной полости и кол­
лапсом легкого, но и раздражением рецепторов
плевры, имеющих важное значение в механизме
дыхательных движений. Нередко наблюдаются
также сухой, болезненный кашель, чувство сдав­
ления в груди.
Очень характерным симптомом мезотелиомы
является специфический экссудативный плев­
рит, особенно при диффузных опухолях. Опи­
саны случаи скопления в плевральной полости
одномоментно до 10 л геморрагического экссу­
дата [Baylac М„ 1924]. Важным признаком опу­
холевого генеза экссудата является также его
быстрое накопление после аспирации [Марморштейн С. Я. и др., 1976]. Узловатые мезо­
телиомы могут протекать без экссудата.
При локализации опухоли в области купола
плевры, как и при раке верхушки легкого, может
быть триада Панкоста [Pancoast Н., 1924]: боли
с иррадиацией в плечо, иногда отек руки, синд­
ром Горнера, связанные с поражением плече­
вого сплетения, верхнего грудного и нижнего
шейного симпатических ганглиев.
У одной из наблюдавшихся нами больных
первыми проявлениями мезотелиомы был
упорно рецидивирующий спонтанный пневмо­
торакс.
Данные физикального обследования таких
больных различны в зависимости от локализации
и распространенности опухолевого процесса,
интенсивности экссудации в полость плевры.
При осмотре может быть выявлено отставание
пораженной половины грудной клетки в акте
дыхания, иногда западение и сужение межре­
берных промежутков, в запущенных случаях —
сколиоз из-за обширного рубцового процесса,
сопутствующего опухолевому росту. В редких
случаях при саркоматозных поражениях плевры
и тканей грудной стенки наблюдается, наоборот,
сглаженность или выбухание межреберий. Голо­
совое дрожание, как правило, ослаблено. Перкуторно определяется значительное притуп­
ление легочного звука на стороне поражения,
сохраняющееся и после аспирации экссудата
из плевральной полости. Дыхание над этим
легким ослаблено. По мере прогрессирования
процесса физикальные данные нарастают, по­
являются общие признаки злокачественного
бластоматозного поражения
(значительное
недомогание, быстрая утомляемость, потли­
вость, похудание, бледность, субфебрильная
температура тела и др.). Иногда из-за распро­
странения опухоли на окружающие органы и
ткани могут определяться признаки легочной
и сердечно-сосудистой недостаточности, реже—
симптомы сдавления верхней полой вены (набу­
хание шейных вен, одутловатость лица и др.),
признаки распространения процесса на брюшину
(боли в животе, асцит).
Диагностика мезотелиомы на основании кли­
нических признаков возможна преимуществен­
но в поздней стадии заболевания. Лишь тща­
тельная оценка всех проявлений его, особенно
притупления легочного звука в отделах, не
характерных для экссудативного плеврита,
230
Рис. 107. Локализованная мезотелиома плевры.
Рис. 108. Диффузная мезотелиома плевры.
а — прямая рентгенограмма; б — боковая рентгенограмма.
а — прямая рентгенограмма; б — боковая рентгенограмма.
231
и быстрое накопление экссудата в плевральной
полости позволяют в более ранние сроки за­
подозрить наличие опухоли плевры.
Большое диагностическое значение имеют
рентгенологические исследования, особенно
после аспирации плеврального экссудата, когда
на полипозиционных рентгенограммах опреде­
ляются утолщенная плевра или патологические
тени разной величины и формы в перифериче­
ских отделах грудной клетки (рис. 107, 108).
В большинстве случаев тень средостения сме­
щается в здоровую сторону, причем это смеще­
ние не исчезает и после удаления плеврального
экссудата. Для установления топического диаг­
ноза внутригрудного пристеночного пораже­
ния Л. С. Розенштраух и М. Г. Виннер (1968),
Ю. Н. Соколова и П. А. Спасская (1971) реко­
мендуют тщательно оценить характер перехода
патологического образования в контур смежных
с ним отделов органов грудной стенки и легкого.
Так, тупой или прямой угол, образующийся в
этой переходной зоне, свидетельствует о внелегочной локализации патологического процес­
са, а острые углы дают основание предполагать
наличие пристеночной опухоли в легком. Со­
гласно наблюдениям Ю. А. Романычева (1977),
определение характера углов переходных зон
имеет относительное значение, а в диагностике
опухолей плевры следует учитывать особенности
их роста и распространения. Г. И. Варновицкий и Ю. А. Романычев (1981) подчеркивают
значение так называемого симптома «кулис»
в дифференциальной диагностике пристеноч­
ных плевритов и опухолей плевры. Так, при
плевритах интенсивность затенения латераль­
ного отдела становится меньшей в горизонталь­
ном положении больного из-за смещения жид­
кости, причем при экссудативном плеврите
симптом «кулис» имеет ровные стенки, а при
опухолях плевры контуры тени волнистые,
особенно если опухоль дольчатого строения.
По данным Б. Г. Шустерова и соавт. (1977),
важную роль в дифференциальной диагностике
между доброкачественными и злокачественными
мезотелиомами имеет оценка контуров тени
опухоли в оптимальной для каждого случая
проекции: четкие, ровные контуры опухоли при
отсутствии перифокальных воспалительных
изменений свидетельствуют о ее экспансивном
росте. При злокачественных опухолях плевры
определяется выраженное утолщение плевры
без четких границ из-за инфильтрирующего
роста опухоли и реактивных изменений окру­
жающих тканей [Варновицкий Г. М., Романы­
чев Ю. А., 1981].
Иногда применяются рентгенопневмографи­
ческие методы исследования для исключения
связи патологического образования с органами
средостения (пневмомедиастинография) и ор­
ганами брюшной полости (пневмоперитонеография), а также для более точной оценки рас­
пространенности опухоли по плевральным лист­
кам (исследование в условиях диагностиче­
ского пневмоперитонеума, плеврография с по­
мощью йодсодержащих контрастных веществ),
но эти исследования результативны лишь при
отсутствии сращений в плевральной полости.
Важнейшее значение в ранней диагностике
опухолей плевры имеет исследование плевраль­
ного экссудата. Экссудат в большинстве слу­
чаев геморрагического характера, содержит
обилие эритроцитов. Серозный экссудат по
клеточному составу является лимфоцитарно­
эозинофильным. Количество эозинофилов
в нем достигает 60 %, а нейтрофилов — не пре­
вышает 27 % [Ожогина Е. П., Комарова Н. Г.,
19751. Несомненным признаком опухолевого
процесса является обнаружение атипичных кле­
ток в экссудате с выраженным полиморфизмом
ядер и патологическими митозами. Часто клетки
больших размеров (до 40—60 мкм, т. е. в 2 раза
больше неизмененных мезотелиальных клеток),
имеют округлую форму и большое ядро, окай­
мленное протоплазмой в виде узкого ободка.
Эти клетки способны к фагоцитозу неповреж­
денных клеток, нередко содержат вакуоли, об­
разуя так называемые «перстневидные клетки».
3. Ф. Климанова (1971) описала три типа цито­
логических картин экссудата, характерных для
мезотелиомы: 1) клеточный состав экссудата
сходен с таковым при раке; 2) клетки имеют
сходство с мезотелием при регенеративно-про­
лиферативных процессах; 3) смешанный тип.
Однако и в настоящее время следует признать
справедливым замечание W. Giese (1960) о том,
что цитологическая картина не является не­
сомненным признаком наличия или отсутствия
опухоли плевры. Нередко требуются трансто­
ракальная пункционная биопсия и гистологи­
ческое исследование полученного материала.
Если пункционная биопсия была сомнительной, а
плевральная полость не облитерирована, то
выполняются торакоцентез и плевроскопия
[Богуш Л. К. и др., 1975], при которой может
быть выявлена опухолевая ткань бархатистого
вида на висцеральной плевре с более выражен­
ным утолщением париетальной плевры. В слож­
ных случаях решающее диагностическое значе­
ние имеет эксплоративная торакотомия, произ­
водимая с таким расчетом, чтобы ее можно было
расширить для радикальной операции с удале­
нием опухоли.
ЛЕЧЕНИЕ
Наиболее радикальным методом лечения ло­
кализованных фиброзных мезотелиом является
хирургическое удаление опухоли. При диффуз­
232
ных мезотелиомах это возможно лишь в редких
случаях ранней диагностики их. Первым из оте­
чественных хирургов успешное удаление мезо­
телиомы выполнил С. И. Спасокукоцкий в 1925 г.
По сводным данным отечественных и зарубеж­
ных хирургов [Сергеев В. М., 1967], лишь около
10 % больных мезотелиомами были опериро­
ваны, остальные признаны неоперабельными
из-за значительного распространения опухоле­
вого процесса. За последние годы процент опе­
рабельности этих больных и результаты лечения
существенно не изменились.
Объем оперативного вмешательства опреде­
ляется в зависимости от распространенности
процесса. При фиброзных мезотелиомах чаще
всего прибегают к резекции опухоли с приле­
жащим участком грудной стенки и частичной
резекцией легкого.
Резекция грудной стенки производится под
наркозом. Разрез проводится через все мягкие
ткани грудной стенки до ребер. Отсепаровывается овальный кожно-мышечный лоскут,
который поднимается над местом расположе­
ния опухоли кверху или кзади. Производится
резекция двух ребер, лежащих выше и ниже
опухоли. Пересекаются ребра и межреберные
ткани кпереди от опухоли и кзади от нее. Об­
разовавшийся «реберный» лоскут откидывается
кзади. Если опухоль париетальной плевры не
сращена с ребрами и межреберными мышцами,
то ее удаляют вместе с плеврой и внутригрудной фасцией, а «реберный» и кожно-мышеч­
ный лоскуты укладывают на место, дренируют
плевральную полость и рану грудной стенки
зашивают. Если опухоль прорастает в ткани «ре­
берного» лоскута, то его удаляют вместе с опу­
холью. При переходе опухоли на висцераль­
ную плевру и легкое производят одновремен­
но соответствующую резекцию легкого, иногда
выполняют лобэктомию или пневмонэктомию.
Размеры радикальной операции определяются
в зависимости от площади распространения
опухолевого процесса с обязательным соблюде­
нием современных принципов абластичности
вмешательства.
Следует отметить, что при диффузных мезо­
телиомах большие операции по типу плевро­
пневмонэктомии с обширной резекцией груд­
ной стенки не всегда оправданны из-за высокой
послеоперационной летальности и плохих отда­
ленных результатов [Богуш Л. К. и др., 1976].
Рекомендовавшиеся ранее операции по типу
декортикации легкого и плеврэктомии в боль­
шинстве случаев нерадикальны, и все больные
погибают в течение 2—5 мес от местных реци­
дивов опухоли [наблюдения Brunner W., 1953;
Lob А., 1953, и др.].
Лучевая терапия при мезотелиомах тоже мало
эффективна. Лишь при саркоматозной форме
описан очевидный лечебный эффект после воз­
действия радиоактивного золота [Miilly К.,
1956]. О перспективности лучевой терапии писа­
ли Л. С. Розенштраух и Л. А. Гуревич (1973).
В подавляющем большинстве случаев при
злокачественных мезотелиомах показано только
симптоматическое лечение, направленное на
уменьшение болей, удаление плеврального экс­
судата, а также химиотерапия внутриплевраль­
ным введением тиофосфамида или эмбихина,
5-фторурацила, хинакрина, делагила, дегранола и других цитостатических препаратов [Брац­
лавский И. Ф. и др., 1966; Бычков М. Б., 1978;
Groy F. et al., 1962; Dollinger M. et al., 1967, и
др.]. X. А. Абисатов и У. Ш. Шайхиева (1971)
показали возможность получения благоприят­
ных результатов комбинированной химиоте­
рапии при злокачественных опухолях плевры:
общей (внутривенно) и местной (внутриплев­
рально). Сочетанное применение дегранола или
5-фторурацила внутривенно и тиофосфамида
внутриплеврально при одновременном симпто­
матическом лечении дает возможность облег­
чить страдания больных, замедляя или прекра­
щая накопление плеврального экссудата. М. Б.
Бычков (1978), подводя итоги лечения 28 боль­
ных, показал преимущество внутриплеврального
введения делагила при раковых плевритах, так
как он не угнетает кроветворения, а по эффек­
тивности в основном не уступает другим хи­
миопрепаратам.
Прогноз при диффузной мезотелиоме пло­
хой. Опухоль быстро распространяется по плев­
ре и окружающим тканям, рано дает мета­
стазы в регионарные лимфатические узлы и
в лимфатические узлы средостения. Трудности
ранней диагностики этих опухолей в настоящее
время не разрешены, поэтому радикальное ле­
чение у большинства больных невозможно.
Отдаленные результаты хирургического лечения
редко превышают 6—12 мес. Даже при опера­
тивном удалении фиброзной мезотелиомы 5летний срок жизни после операции отмечен лишь
в единичных случаях [Савицкий А. М., 1967;
Stoebner Р. et al., 1970]. Необходимо стремиться
к более ранней диагностике опухолей плевры,
когда имеется возможность радикального опе­
ративного вмешательства и предупреждения
рецидива и метастазирования после операции
при комплексном лечении в послеоперацион­
ном периоде (химиотерапия, лучевая терапия).
Глава
JL X
БРОНХОЭКТАЗИИ
К бронхоэктазиям следует отнести заболе­
вание легкого с преимущественным поражением
бронхов тяжелого воспалительно-деструктив­
ного характера, распространяющимся на всю
толщу бронха, окружающую клетчатку, кро­
веносные и лимфатические сосуды, ведущим
к расширению просвета бронхов, утрате ими
дренажной функции. Бронхоэктазии имеют
достаточно четко очерченную клиническую
картину.
Известны наблюдения, когда расширение
бронхов, даже значительное, ничем себя кли­
нически не проявляет. Об этом свидетельствуют
данные патологоанатомических вскрытий, пока­
завших, что расширения бронхов у умерших
встречаются значительно чаще, чем диагности­
руются при жизни. Есть наблюдения, когда рас­
ширения бронхов обнаруживались случайно
при обследовании больных, страдавших какимлибо другим легочным заболеванием (например,
бронхиальной астмой). Однако такое расши­
рение бронхов — не более чем аномалия раз­
вития бронхиального дерева, но не болезнь.
К бронхоэктазиям как к нозологической фор­
ме его отнести нельзя.
Бронхоэктазии могут сопровождаться дру­
гой самостоятельной патологией легких. Они
могут возникать на фоне какого-либо другого
легочного заболевания, например туберкулеза,
острого или хронического абсцесса, опухоли,
инородного тела бронха. С другой стороны,
бронхоэктазии могут осложниться каким-либо
другим легочным страданием, к примеру абс­
цессом. В связи с этим некоторые авторы рас­
сматривали особо вторичные и осложненные
бронхоэктазии. Однако, строго говоря, исходя
из приведенного определения, бронхоэктазии
всегда вторичны, они всегда являются след­
ствием воспаления бронхиального дерева.
Существует мнение, что бронхоэктазии —
форма течения или стадия развития хрониче­
ской пневмонии или бронхита. Однако большин­
ство хирургов считают, что руководствоваться
этой точкой зрения в практической работе
нельзя [Горовенко Г. Г., Брусиловский Б. М.,
1973; Колесов А. П., Гаджиев С. А., 1973; Коро­
лев Б. А., 1973; Путов Н. В., 1973, и др.]. Хро­
ническая пневмония и бронхоэктазии, как пола­
гает большинство, являются самостоятельными
заболеваниями, имеющими самостоятельную
клиническую картину и течение. Наблюдения
М. Р. Рокицкого (1972) показали, что, скрыва­
ясь под неопределенным диагнозом хронической
пневмонии, значительная часть больных брон­
хоэктазиями (до 15 %) долго и безуспешно
лечатся консервативными методами, тогда как
им показано хирургическое вмешательство.
Таким образом, бронхоэктазии следует рас­
сматривать как самостоятельную патологию,
которая возникает вторично и может сочетать­
ся с другими заболеваниями легких или ослож­
няться ими.
ЧАСТОТА
Существующие противоречивые взгляды в
вопросе определения бронхоэктазий как нозо­
логической формы, отсутствие единой общепри­
нятой классификации хронических неспецифи­
ческих воспалительных заболеваний легких
затрудняют выявление истинной частоты брон­
хоэктазий.
Статистические данные, основанные на кли­
нико-рентгенологическом обследовании (вклю­
чавшем флюорографию) больших групп насе­
ления, проведенные в 50-е годы [Куприя­
нов П. А., Колесов А. П., 1960; Колесников И. С.,
Ермолаев В. Р., 1969], свидетельствовали о том,
что бронхоэктазии встречаются у 0,1—0,13 %
взрослых и у 0,5—0,6 % детей. Авторы считают
эти цифры преуменьшенными, поскольку в то
время еще недостаточно широко применялся
основной метод диагностики бронхоэктазий —
бронхография.
Оценить частоту бронхоэктазий в настоящее
время с учетом данных бронхографии можно
косвенно, зная частоту заболеваемости хро­
ническими неспецифическими воспалитель­
ными процессами (хроническими пневмония­
ми, бронхитом), с одной стороны, и частоту
бронхоэктазий, выявляемых у них при углуб­
ленном обследовании, включающем бронхогра­
фию,— с другой.
По данным ВНИИ пульмонологии М3 СССР
[Волкова Л. П. и др., 1971], хронические неспе­
234
цифические воспалительные заболевания легких
среди населения выявляются в 4,08 %; из них
хроническая пневмония составляет 1,4 % и хро­
нический бронхит— 1,7 %. Углубленное обсле­
дование этого контингента показало, что брон­
хоэктазии среди них в виде типичных цилинд­
рических и мешотчатых форм, По наблюдениям
А. Я. Цигельника (1971), выявляются у 36,7 %
больных, а по данным Н. П. Чернобрового
(1976) — у 38,7 %. Следовательно, при тща­
тельном обследовании клинически проявляю­
щиеся расширения бронхов могут быть выяв­
лены примерно у 0,5 % населения. По сообще­
нию Б. И. Давыдова (1964), при обследовании
20 672 детей хроническая пневмония обнаружи­
вается у 1,53 %, а бронхоэктазии после углуб­
ленного обследования — у 0,15 %.
Таким образом, данные как прежних, так и
более современных авторов говорят о том, что
бронхоэктазии — заболевание нередкое.
Частоту бронхоэктазий может характери­
зовать также процент оперированных больных
бронхоэктазиями к числу оперированных с хро­
ническими неспецифическими воспалитель­
ными заболеваниями легких вообще. Он доста­
точно высок: по материалам А. П. Колесова,
С. А. Гаджиева (1971, 1973), охватывающим
более 3000 наблюдений, составляет 61,9 %, по
материалам Я. У. Булгакова (1975) — 52,5 %.
Аналогичные цифры приводят и другие авторы
[Дорофеева А. И., Бойков Г. А., 1969; Черно­
бровый Н. П., 1971; Коваленко П. П., Аниси­
мова А. Т., 1972, и др.].
Частоту бронхоэктазий характеризует еще
одна цифра: по данным экспертизы трудоспо­
собности больных с хроническими заболева­
ниями легких в восьми ВТЭК Ленинграда боль­
ные бронхоэктазиями составляют 20 % [Цигельник А. Я., 1971].
Согласно многочисленным литературным
данным, бронхоэктазии чаще наблюдаются у
мужчин, чем у женщин. По наблюдениям кли­
ники госпитальной хирургии, среди находив­
шихся на обследовании 624 больных мужчин
было 385 (61,7 %), женщин — 239 (38,3 %).
Довольно закономерна локализация бронхоэк­
тазий в легких. По материалам клиники, брон­
хоэктазии слева наблюдались у 55,1 % больных,
справа — у 44,9 %. Самой частой локализацией
бронхоэктазий слева является нижняя доля
(94 %). Справа нижняя доля также поражается
чаще других долей — в 63 % наблюдений; од­
нако справа чаще, чем слева, поражаются и
другие доли. Распространенные, поражающие
все легкое бронхоэктазии слева отмечены в
34,7 % случаев, справа — в 19,2 %.
Двустороннее поражение среди больных
клиники наблюдалось у 26,1 % человек. С такой
же частотой двусторонние бронхоэктазии отме­
чали и другие авторы [Колесов А. П., Гаджи­
ев С. А., 1971; Цуман В. Г. и др„ 1976; Cooper J.,
Grillo Н„ 1969; Pineyro 1. et al., 1975].
Существенно важным обстоятельством, часто
определяющим объем оперативного вмеша­
тельства по поводу бронхоэктазий, является
весьма частое одновременное поражение ниж­
ней доли и язычка слева (у 74,6 % больных)
и нижней и средней долей справа (у 50,5 %
больных). По мнению Ф. Г. Углова и соавт.
(1971), средняя доля или язычок легкого (IV —
V сегменты) при хронической пневмонии и брон­
хоэктазиях поражаются практически всегда.
Более того, авторы считают, что именно с этих
сегментов легкого начинается всякое хрониче­
ское неспецифическое воспаление. На основа­
нии этой концепции рекомендуется широкое
удаление язычка и средней доли легкого, даже
тогда, когда они внешне кажутся неизменен­
ными.
Следует отметить также, что при воражении нижних долей страдают преимуществен­
но сегменты базальной пирамиды, тогда как
верхушечный (VI) сегмент в большинстве слу­
чаев остается интактным.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Бронхоэктазии — заболевание полиэтиологичное.
Вероятно, у некоторой части больных имеется
врожденная предрасположенность к заболе­
ванию бронхоэктазиями на почве аномалий раз­
вития бронхов. Такие бронхоэктазии называ­
ют дизонтогенетическими (постнатальными).
В качестве подтверждения этой точки зрения
приводят случаи семейных наследственных
бронхоэктазий, сообщения о которых нередки.
Имеются сведения о бронхоэктазиях в трех
поколениях одной семьи — у дедушки, отца и
детей; есть наблюдения бронхоэктазий у близ­
нецов, в том числе однояйцевых [Рыжков Е. В.,
1968; Стручков В. И. и др., 1969]. Подобные на­
блюдения касаются отнюдь не только поликистоза легких. В случаях семейных бронхоэкта­
зий выявлялись расширения бронхов самого
разнообразного характера — цилиндрические,
мешотчатые и смешанные. Следует отметить,
что, во-первых, различный характер расширения
бронхов наблюдался у членов одной и той же
семьи; они бывали разными даже у однояйце­
вых близнецов и даже у одного и того же чело­
века — в одних отделах легкого были мещотчатые (или кистоподобные) бронхоэктазии, а
в других отделах — цилиндрические; во-вторых,
как правило, семейные наследственные бронхо­
эктазии проявлялись клинически не в первые
дни и месяцы после рождения ребенка, а, как
правило, в первые годы жизни, часто спустя 5—
235
10 лет и более; в-третьих, семейные бронхоэк­
тазии нередко сочетались с другими пороками
развития, которые в этих семьях также пере­
давались по наследству и наследственная при­
рода их не оспаривается: с добавочными доля­
ми легкого, аномалиями сосудов (легочных
артерий и вен), воздушными кистами (пузы­
рями) легкого, трапециевидной формой груд­
ной клетки, гиперкератозом, инверсией внут­
ренних органов.
Врожденный характер расширения бронхов
подтверждается сочетанием его с заболева­
ниями, врожденное происхождение которых
не вызывает сомнений. Классическим приме­
ром этого служит триада Картагенера: расши­
рение бронхов, хронический синусит и обратное
расположение внутренних органов. Описано
расширение бронхов в сочетании с врожденным
расширением в других органах (кисты в почках,
дивертикулы мочевого пузыря, кишечника), с
врожденными пороками развития легкого (дер­
моидные кисты, тератомы, агенезия, аплазия),
с врожденными заболеваниями пищевода (атре­
зия, мегалия), пороками сердца и крупных со­
судов, скелета (череп, позвоночник, конечности,
грудная клетка), аномалиями мягких тканей
(расхождение мышц живота), недоразвитием
половых органов, крипторхизмом, добавоч­
ными сосками молочной железы [Рыжков Е. В.,
1968; Стручков В. И. и др., 1969; Гаджиев С. А.
и др., 1974]. Нередко при таких расширениях
бронхов выявлялись врожденные наследствен­
ные болезни обмена веществ — ксантоматоз,
фиброз печени, дисгаммаглобулинемия (врож­
денная недостаточность иммуноглобулинов
класса G), муковисцидоз [Валентинович А. А.,
1973, и др.]. По мнению ряда авторов, при тща­
тельном обследовании больных бронхоэкта­
зиями врожденные заболевания могут быть
выявлены у каждого 4—5-го больного.
Приведенное перечисление врожденных забо­
леваний, сопутствующих расширению бронхов,
не только представляет интерес для уточнения
природы происхождения бронхоэктазий, но
также преследует цель обратить внимание на
своевременное выявление этих заболеваний и
их лечение, коль скоро они обнаружены. Осо­
бенно настойчиво надо искать патологию обме­
на веществ, иммунодефицитные состояния, без
коррекции которых (а такая возможность име­
ется) окажется недостаточно эффективным
местное лечение бронхоэктазий, в том числе
оперативное.
К патогистологическим признакам врожден­
ной предрасположенности к заболеванию брон­
хоэктазиями Е. В. Рыжков (1968) относил нали­
чие облитерированных крупных бронхов, гипо­
плазию, отсутствие хрящевой ткани при правиль­
но сформированных элементах других тканей
бронха, беспорядочное расположение хряще­
вых клеток в хрящевых пластинках (как в хонд­
ромах), гипоплазию эластической ткани, пере­
мычки бронхов, наличие жировой ткани между
ними. Такие признаки автор обнаружил в 12
случаях из 311
мертворожденных детей
(в 3,7%). Однако весьма сходные патогистологические данные были получены рядом иссле­
дователей у больных бронхоэктазиями явно при­
обретенного характера — после пребывания
в бронхах взрослых инородного тела, при после­
операционных рецидивных бронхоэктазиях
в долях, где они до того не обнаруживались
[Колесов А. П., 1960; Ермолаев В. Р., 1965,
и др.].
Врожденную предрасположенность к заболе­
ванию бронхоэктазиями полностью отвергнуть
невозможно, но надо полагать, что такая пред­
расположенность наблюдается все же не часто.
По разным авторам, она с большей или меньшей
вероятностью может быть констатирована не
больше чем у 0,5—5 % больных [Цигельник А. Я., 1948; Гланцберг Н. А., 1970; Коро­
лев Б. А., Корепанова Н. В., 1972, и др.].
Для возникновения бронхоэктазий, как сви­
детельствуют клинические наблюдения и экспе­
риментальные данные, необходимо два основ­
ных условия: нарушение вентиляции легкого
и инфекция [Куприянов П. А., Колесов А. П.,
1960; Колесников И. С., Ермолаев В. Р., 1969;
Струков А. И., Колодова И. М., 1970, и др.].
Существенно важным является также наруше­
ние крово- и лимфообращения [Логинов А. П.,
Головин Ю. А., 1971]. Сочетание этих условий
наиболее часто возникает при ателектазах лег­
кого различного происхождения.
Возникновение бронхоэктазий при жизни
чаще всего наблюдается в детском возрасте,
особенно в раннем детстве. Согласно данным
литературы, подтвержденным материалами
клиники, больше чем у 2 / з больных заболева­
ние началось до 20 лет, у '/г — до 5 лет и у
'/з из них — на первом году жизни. Это обстоя­
тельство объясняется тем, что, с одной сторо­
ны, легкое в первые годы жизни ребенка еще
не завершило своего развития, в нем еще не
окончательно сформирована соединительная
ткань, недоразвиты эластические структуры
и оно представляет собой сравнительно легко
ранимый орган, склонный, в частности, к ате­
лектазам, а с другой стороны, сопротивляемость
к инфекциям в детском возрасте, как известно,
понижена.
Говоря о значении неполного развития лег­
кого ребенка в возникновении бронхоэктазий,
уместно привести данные Б. И. Ищенко и соавт.
(1972), согласно которым рецидивы бронхоэк­
тазий после резекции легкого у детей младше
10 лет (т. е. у лиц, у которых постнатальное
236
развитие этого органа егце не закончено) бывает
при прочих равных условиях в 2 раза чаще,
чем у детей, оперированных в возрасте старше
10 лет.
Наиболее частой причиной бронхоэктазий
детского возраста (85 %) являются острые
бронхопневмонии, бронхиты и катары верхних
дыхательных путей, особенно повторные [Гланцберг Н. А., 1970; Пугачев А. Г. и др., 1970, 1974;
Гауян Я. К. и др., 1976]. Для пневмоний дет­
ского возраста характерны стойкие ателектазы,
которые возникают даже при сравнительно
легком клиническом течении болезни более чем
в 20 % случаев. Этому способствуют не только
анатомо-физиологические особенности дет­
ского легкого, но и часто наблюдавшиеся у де­
тей бронхоадениты, нарушающие проходи­
мость бронхиального дерева сдавлением его
извне.
Часто выявляющиеся в анамнезе у детей
предшествующие пневмониям или сопутствую­
щие им острые респираторные заболевания,
синуситы, аденоиды, тонзиллиты нарушают
вентиляцию легких, способствуют возникнове­
нию и поддержанию бронхита и пневмонии, ре­
цидивирующему их течению. Рецидивирую­
щая пневмония, со своей стороны, поддержи­
вает воспалительный процесс в верхних дыха­
тельных путях. Создается своеобразный пороч­
ный круг. А. Я. Цигельник (1971) важную
роль в возникновении бронхоэктазий при ин­
фекции верхних дыхательных путей отводит сен­
сибилизации бронхиального дерева и парен­
химы легкого.
Среди пневмоний детского возраста особо
выделяют коревые и коклюшные пневмонии,
а в последнее время также пневмонии другой
вирусной природы, после которых бронхоэкта­
зии развиваются особенно часто (у 15 % боль­
ных). Предполагается, что в этих случаях важ­
ную роль в возникновении бронхоэктазий игра­
ют интоксикация, токсические нервно-сосуди­
стые расстройства, токсическое поражение
бронхиального дерева.
Довольно частой причиной бронхоэктазий
у детей служат инородные тела бронхов (у 0,3—
0,5 % больных). Даже сравнительно непродол­
жительное пребывание инородного тела в брон­
хе (от нескольких дней до 2—3 нед) может
привести к возникновению бронхоэктазий
вследствие присоединения инфекции [Либов
С. Л. и др., 1963].
Определенную роль в возникновении брон­
хоэктазий играет туберкулез, при котором пер­
вичное нарушение вентиляции легкого связано
со сдавлением бронхов увеличенными лимфа­
тическими узлами, а в последующем — склеро­
зированными перибронхиальными тканями;
имеет значение также и существенное нару­
шение при первичном туберкулезе лимфообра­
щения и кровоснабжения бронхиального де­
рева [Эртли А. А., Агкацев Т. В., 1973]. Веро­
ятно, важную роль играет также присоединяю­
щаяся вторичная инфекция. Бронхоэктазии
после туберкулеза обнаруживаются обычно в пе­
реднем сегменте верхней доли или в переднем
и язычковых сегментах слева, среднедолевых
сегментах справа [Ермолаев В. Р., 1965]. Брон­
хоэктазии в верхней доле легкого чаще всего
бывают посттуберкулезной этиологии.
Инфекция дыхательных путей и легкого игра­
ет важную роль в возникновении бронхоэкта­
зий и у взрослых, однако на первый план в этом
возрасте выступает хроническое воспаление,
особенно бронхит. Н. П. Чернобровый и соавт.
(1976) наблюдали 106 больных с хроническими
воспалительными процессами в бронхах в те­
чение 7 лет, используя периодически бронхо­
скопию и бронхографию. Авторами установле­
но, что при недостаточно регулярном лечении
бронхит рецидивировал в виде гнойно-язвенной
формы с постепенным переходом в склероти­
ческую форму с образованием бронхостено­
зов, с возникающими на этой почве рецидивами
пневмонии. При 3—4-летнем наблюдении у
41 больного (в 38,6 /о) с таким неблагоприят­
ным течением развились типичные цилиндри­
ческие и смешанные бронхоэктазии, а у 14 —
мешотчатые.
По наблюдениям Ф. Г. Углова и соавт. (1971 —
1976), существенную роль в возникновении
бронхоэктазий у взрослых играет неспецифи­
ческое поражение бронхолегочных лимфати­
ческих узлов. В силу особенностей анатомиче­
ского взаимоотношения бронхов средней доли
или язычка с расположенными в этой области
узлами, а также особенностями вентиляции
этих отделов нарушение дренажной функции
и воспаление начинаются прежде всего в IV—
V сегментарных бронхах, приобретают хрони­
ческое рецидивирующее течение и приводят к
склеротическому процессу, распространяюще­
муся на близлежащие отделы, в первую оче­
редь на бронхи базальной пирамиды. Посте­
пенно вовлекаются последовательно VII, VIII,
IX и X сегменты. По степени вовлечения в про­
цесс сегментов базальной пирамиды авторы
выделяют стадии бронхоэктазий, именуемые
ими хронической деструктивной пневмонией.
Стадийность нарушения дренажной функции
бронхов при ней прослежена в динамике с по­
мощью кинобронхографии и подтверждена
авторами при исследовании препаратов уда­
ленных легких, высокой эффективностью хирур­
гического лечения бронхоэктазий, обязательно
включающего удаление средней доли и язычка,
даже тогда, когда они внешне казались неиз­
мененными.
237
Распространение бронхоэктазий по такому
типу, по-видимому, действительно встреча­
ется нередко. Об этом свидетельствует частое
сочетание поражения бронхоэктазиями ниж­
них долей и IV—V сегментов. Однако такой
тип распространения нельзя считать универ­
сальным. Бронхоэктазии, как было изложено
выше, не так уж редко поражают только лишь
нижние доли (или отдельные сегменты базаль­
ной пирамиды), а бронхи IV—V сегментов оста­
ются интактными. Нередко встречаются также
бронхоэктазии средней доли и язычка (особен­
но средней доли) при совершенно здоровых
нижних долях. В клинике госпитальной хирур­
гии Б. П. Лапиным изучена в динамике бронхо­
графическая картина при бронхоэктазиях сред­
ней доли у 34 больных на протяжении 5—10 лет.
Ни у одного из них (это были взрослые люди)
распространения воспалительного процесса
(в том числе в деструктивной форме) на брон­
хи других отделов не наблюдалось. Не наблю­
далось также изменения характера бронхоэк­
тазий в пораженных отделах. Аналогичные
данные приводят М. Л. Шулутко и соавт. (1970).
Склонность к распространению бронхоэкта­
зий более характерна для детского возраста,
когда для этого имеются соответствующие пред­
посылки, о которых говорилось выше.
У взрослых, в отличие от детей, бронхоэк­
тазии в сочетании с другими заболеваниями
легких или после них наблюдаются чаще. Р. Keszler (1969) у больных, среди которых более
50 % были пожилые люди, бронхоэктазии та­
кого происхождения выявил в 70 %. Р. И. Плишко (1973) у лиц старше 20 лет такие бронхо­
эктазии отметил в 25 % случаев. Бронхоэкта­
зии после острых абсцессов зарегистрированы
Н. П. Чернобровым (1971) у 28,9 % человек.
Б. А. Королев и Н. В. Корепанова (1972) со­
общают о бронхоэктазиях у взрослых после
абсцесса легкого у 3,6 %, после гнойного плев­
рита — у 1,7 %, после хронического фиброзно­
кавернозного туберкулеза — у 1 %. Довольно
частой причиной (у 3 % больных), по их данным,
были инородные тела.
О механизме развития бронхоэктазий и их
патогенезе можно говорить лишь предполо­
жительно. Механизм их возникновения при
различных причинах имеет много общего. Выше
говорилось, что он обязательно включает вос­
паление, нарушение вентиляции легкого, а так­
же крово- и лимфообращения. В зависимости от
преобладания того или иного фактора, степени
их выраженности и распространенности в каж­
дом конкретном случае в конечном итоге возни­
кают разнообразные патоморфологические
изменения в бронхах.
Возникновение бронхоэктазий с учетом кли­
нико-экспериментальных данных разных авто­
ров и наблюдений клиники можно представить
следующим образом.
При ателектазе легкого, будь он обтурацион­
ного, пневмонического, токсического или иного
происхождения, с самого начала нарушаются
дренажная функция бронхов, кровоснабжение
и лимфоотток. В просвете бронхов скапливается
секрет. Стенка кровеносных сосудов постепен­
но гипертрофируется, просвет их суживается,
они начинают напоминать сосуды замыкаю­
щего типа. Лимфатические щели расширяются
с образованием лимфатических узелков — лим­
фом. Нарушение кровообращения и оттока
лимфы ведет к частичной атрофии элементов
стенки бронха и легочной паренхимы с после­
дующей частичной резорбцией и организацией
этих участков. В бронхе разрастается соеди­
нительная ткань, эпителий приобретает склон­
ность к аденоматозному росту, т. е. возника­
ют изменения, напоминающие таковые при
гипоксии. Они обратимы полностью или частич­
но, если не присоединяется инфекция.
Воспалительный процесс в ателектазированном легком может возникать как в бронхе, так
и в паренхиме, захватывать всю долю или сег­
мент или располагаться гнездно. Следствием
воспаления является стойкий склероз, а при
уменьшении объема органа — цирроз. Склеро­
зированный расширенный бронх навсегда утра­
чивает дренажную функцию.
Расширения бронхов могут быть самыми раз­
нообразными по форме (рис. 109). Они могут
заканчиваться слепо или частично сообщаться
с воздушной тканью легкого. Если наряду с вос­
палением в бронхе имело место длительное
воспаление и в паренхиме, она равномерно скле­
розирована. Если воспаление ограничилось
преимущественно бронхом, то в паренхиме име­
ется обычно более или менее выраженная
равномерная эмфизема. Доля (или сегмент) при
таких бронхоэктазиях резко уменьшены в раз­
мерах.
Несколько другой, по-видимому более ча­
стый, механизм развития бронхоэктазий на­
блюдается при первоначальном лишь частичном
нарушении проходимости дренирующего брон­
ха, без распространенного ателектаза, например
при сдавлении его лимфатическими узлами,
рубцами, частичной закупорке инородным те­
лом, слизью, гноем, что часто бывает при хро­
ническом бронхите. При этом воспаление, как
правило,- начинается в бронхе и преобладает
над воспалением в паренхиме; в последней оно,
как и нарушение крово- и лимфообращения,
носит вторичный характер. Вследствие такого
механизма стенки расширенного бронха всегда
резко утолщены, вокруг них имеется массив­
ное разрастание соединительной ткани, а в
паренхиме — зоны склероза чередуются с зона-
238
Рис. 109. Коррозионные слепки бронхов при бронхоэктазиях,
а
мешотчатые бронхоэктазии; б — мешотчатые и цилиндриче­
ские (смешанные) бронхооктазии.
ми эмфиземы, участками ателеказа, а также
нормальной легочной тканью. Частично она
может вентилироваться. Пораженная доля или
сегмент при таком механизме могут иметь нор­
мальные размеры, резкого уменьшения нет.
Отличить их при наружном осмотре от непо­
раженных отделов бывает подчас затрудни­
тельно. Обращается внимание на то, что пора­
женное легкое имеет более светлую, розовую
или с вишневым оттенком окраску, зависящую
от измененных условий кровообращения, а
также отсутствие пигментации пылью как след­
ствие нарушения вентиляции.
Развитие бронхоэктазий после абсцесса
легкого или на его фоне, при фиброзно-кавер­
нозном туберкулезе, при длительном сдавле­
нии легкого извне (например, при длительно
существующем спонтанном пневмотораксе,
при эмпиеме) может идти по тому или друго­
му из изложенных механизмов с преоблада­
нием какого-нибудь из них.
Эти (схематично изложенные) механизмы
патогенеза бронхоэктазий в комбинации дают
довольно пеструю морфологическую картину,
которая еще более усложняется по мере перио­
дических обострений воспалительного процесса.
Для практики сохраняет свое значение под­
разделение бронхоэктазий по форме расшире­
ния на цилиндрические, мешотчатые и смешан­
ные. П. А. Куприянов, А. П. Колесов (1960)
разделяют бронхоэктазии на ателектатиче­
ские и неателектатические. И. С. Колесников.
В. Р. Ермолаев (1969) рассматривают следую­
щие морфологические формы: кистоподобные,
преимущественно встречающиеся в верхних
долях, бронхоэктазии с преимущественным
перибронхиальным склерозом и бронхоэкта­
зии с истонченной склеротической стенкой на
фоне выраженной эмфиземы. Кистоподобные
бронхоэктазии от истинных кист отличаются
тем, что при истинных кистах, как правило,
сохраняется более или менее нормальное брон­
хиальное дерево. Для бронхоэктазий с выра­
женной эмфиземой характерно наиболее тя­
желое клиническое течение; они часто сопро­
вождаются картиной легочного сердца.
Изменения в органах при бронхоэктазиях
касаются прежде всего изменений в легких во­
обще, а не только в пораженных отделах. Эти
изменения выражаются в виде вторичного диф­
фузного пневмосклероза и эмфиземы на почве
прогрессивно нарастающей легочной гипер­
тензии, ведущей к системному сосудистому
поражению малого круга (или являющейся
ее следствием). По мере прогрессирования
страдание приводит в конце концов к хрониче­
239
ской правожелудочковой сердечной недоста­
точности, к «легочному сердцу», что и является
основной причиной смерти больных бронхо­
эктазиями при несвоевременно предпринятых
мерах профилактики и лечения.
Изменения в других органах — печени, поч­
ках — развиваются в связи с возникающим
амилоидозом, хотя амилоидоз сейчас встре­
чается редко.
КЛИНИЧЕСКАЯ КАРТИНА, ДИАГНОСТИКА
Первые признаки заболевания, как указыва­
лось, появляются преимущественно в детском
и даже раннем детском возрасте. В настоящее
время оно в детском возрасте обычно и диагно­
стируется. Больные в зрелом и пожилом возрасте
в хирургические стационары поступают сейчас
все реже и реже. Это объясняется более ранней,
чем прежде, диагностикой бронхоэктазий и свое­
временно предпринятым еще в детском возрасте
хирургическим лечением в показанных слу­
чаях.
Основными жалобами при бронхоэктазиях
являются кашель с мокротой и периодически
возникающее ухудшение общего состояния,
зависящее от обострения инфекционного про­
цесса и связанной с этим интоксикацией.
Характерен постоянный, упорный, персисти­
рующий кашель. Лишь изредка он бывает су­
хим. Чаще это кашель со слизистой, слизисто­
гнойной и гнойной мокротой до 50—200 мл/сут.
Какое-то количество мокроты больной может
откашлять по просьбе в любое время, но наи­
большее количество выделяется по утрам, во
время утреннего туалета. После этого в тече­
ние дня кашель может особенно не беспокоить
больного.
У некоторых больных, чаще при поражении
передних сегментов, средней доли, кашель бес­
покоит по ночам, в положении лежа на спине.
Больные даже без специальных расспросов
часто обращают внимание на то, что для более
эффективного откашливания мокроты им при­
ходится принимать вынужденное положение:
свесившись с кровати вниз головой, перегнув­
шись через спинку стула, край ванны. Особенно
характерно такое положение для поражения
бронхоэктазиями нижних долей. Как правило,
больные хорошо знают положение тела, при
котором мокрота отходит лучше всего, и это
имеет определенное значение для предваритель­
ной топической диагностики.
Мокроты бывает то больше, то меньше. Ха­
рактернее тоже меняется. Слизистого характера
мокрота периодически делается гнойной, при­
обретает неприятный запах, становится обиль­
ной. Такое состояние может продолжаться до­
вольно долго, месяцами. Из-за неприятного
запаха изо рта больные нетерпимы в коллек­
тивах, что весьма их угнетает. Относительно
большое количество мокроты с гнилостным
запахом в настоящее время встречается неча­
сто, это свойственно главным образом распро­
страненным мешотчатым бронхоэктазиям.
Довольно частым симптомом является кро­
вохарканье. На небольшое кровохарканье (на
наличие примеси, прожилок крови в мокроте)
жалуются примерно треть больных. Нередко
наблюдается также легочное кровотечение —
у 10 % больных. Однако обильные легочные
кровотечения в общем для бронхоэктазий не
характерны. Жизни они, как правило, не угро­
жают. Тем не менее кровохарканье и, особенно,
кровотечение часто являются именно тем симп­
томом, который приводит больного к врачу.
Причину кровохарканий и легочных крово­
течений при бронхоэктазиях усматривают в
гиперемии рыхлой, гипертрофированной и легко
райимой слизистой оболочки в области пора­
жения, в ее изъязвлениях, наличии грануляций,
сосуды которых местами имеют варикозные
изменения.
В отдельных случаях кровохарканье — един­
ственный симптом наличия бронхоэктазий («су­
хие бронхоэктазии» по А. Я. Цигельнику, 1948).
На боли в груди жалуются половина больных.
Обычно боли соответствуют области (стороне)
поражения. Они более или менее постоянны,
тупого характера, умеренные по интенсивности.
Наличие болей объясняют спаечным процессом.
Отмечается также, что боли становятся мень­
ше после того, как больной хорошо откашли­
вает мокроту.
К постоянным жалобам надо отнести также
одышку. Обычно она появляется при нагрузке.
Особенно характерна одышка для детей. Именно
одышка у них может вызвать беспокойство ро­
дителей в первую очередь, так как на боли ма­
ленькие дети часто пожаловаться неспособны,
а мокроту проглатывают. Одышка является
характерным симптомом и для стариков. У них
она является следствием не только дыхатель­
ной, но и сердечно-сосудистой недостаточности.
Сильная одышка — неблагоприятный признак,
свидетельствующий о распространенном и да­
леко зашедшем процессе.
В любом возрасте может присоединиться
астматическое состояние по типу бронхита
с астматическим компонентом: приступы
одышки с затрудненным выдохом. Этот компо­
нент при бронхоэктазиях выявляется доволь­
но часто — у 25 % больных [Виноградов В. Н.,
Лейзеровская Э. Г., 1962]. Иногда такое состоя­
ние требует оказания неотложной помощи.
Однако истинная аллергическая бронхиаль­
ная астма бронхоэктазиям сопутствует редко:
по данным клинки, на 624 больных она наблю­
240
далась у 3 человек (0,02 %). Другие авторы
[Углов Ф. Г. и др., 1971; Seely W. et al., 1966]
приводят более высокие цифры. Существует
даже теория инфекционно-аллергического про­
исхождения бронхиальной астмы, обусловлен­
ной, в частности, хронической деструктивной
пневмонией, т. е. бронхоэктазиями [Углов Ф. Г.
и др., 1971].
Периодические обострения при бронхоэкта­
зиях характеризуются прежде всего ухудше­
нием общего состояния: появляются слабость,
вялость, быстрая утомляемость, расстраивается
внимание. Нередко больные отмечают, что в
период обострений у них «все валится из рук».
Дети становятся адинамичными, взрослые —
нетрудоспособными. Как правило, в этот период
увеличивается количество мокроты и она при­
обретает гнойный характер. Для периода обост­
рения характерно также учащение кровохар­
канья. Усиливается одышка.
Закономерной в период обострения является
температурная реакция. Однако высокой (до
38 °C и больше) температура тела бывает редко
и чаще наблюдается в начальной стадии разви­
тия бронхоэктазий, особенно у детей. Это обус­
ловлено тем, что у детей при еще сохраненной
в значительной части легочной паренхиме обо­
стрения протекают с явлениями интерстициаль­
ной пневмонии. У взрослых температура тела
в основном носит субфебрильный характер,
с отдельными температурными «свечками»,
или даже характер так называемого «субнор­
мального субфебрилитета» — значительных, в
пределах градуса, колебаний, но не выше нор­
мальных цифр.
Такое состояние обострения может длиться
довольно долго — неделю, месяц, два и больше.
Оно отчетливо носит сезонный характер —
начинается в предвесенний и послеосенний
периоды. Иногда основные симптомы заболе­
вания проявляются только в периоды обостре­
ния.
В основе обострений бронхоэктазий лежит
интоксикация, связанная с воспалением в брон­
хах (реже — в паренхиме легкого). Поскольку
бронхоэктазиям свойственно более или менее
выраженное отграничение местного очага, обо­
стрения бурно не проявляются.
Тем не менее в периоды обострений обыч­
ным является диагноз пневмонии, затянувшей­
ся пневмонии, обострения хронической пнев­
монии.
Своеобразное начало заболевания, которое,
как говорилось, относится к детскому, а чаще
раннему детскому возрасту, связь начала забо­
левания с пневмонией, особенно послекоревой
или послекоклюшной, характерные изложен­
ные жалобы, волнообразное течение с довольно
типично протекающими обострениями позво­
16 Зак. 0517
ляют с довольно большой вероятностью поста­
вить правильный диагноз. Этому помогают не­
которые дополнительные сведения, а также
данные физикального обследования, которые
выявляют отдельные характерные особенности.
Детям, больным бронхоэктазиями, свой­
ственно отставание в физическом и умственном
развитии. Для взрослых более характерна
склонность к худобе, чем к полноте.
Из анамнеза у детей можно установить, что
ребенок сравнительно поздно начал ходить, раз­
говаривать, читать. Можно выяснить отстава­
ние от других детей при занятиях в школе. По
данным клиники, эти признаки установлены у
25 % больных детей.
Очень часто (у 1 /3 больных) масса тела детей
меньше нормальной возрастной, вторичные
половые признаки у них не соответствуют воз­
расту. При осмотре можно отметить некоторую
бледность кожных покровов и слизистых обо­
лочек, легкую одутловатость век, шелушение
на груди, локтях, коленях, голенях.
Патогномоничным признаком считалось
наличие деформации пальцев кистей и стоп в
виде «барабанных палочек». При бронхоэкта­
зиях этот симптом сейчас встречается сравни­
тельно редко. Не менее часто он наблюдается
при других хронических заболеваниях, сопро­
вождающихся интоксикацией и гипоксией,—
туберкулезе, хроническом абсцессе, пороках
сердца, остеомиелите. У взрослых он нередок
при хроническом бронхите. Генез этого симпто­
ма не вполне ясен. Обращается внимание на
возможность обратного развития этого симптома
в случае своевременно предпринятого и успеш­
ного лечения.
Отставание грудной клетки при дыхании, за­
падение ее на стороне поражения, деформация
позвоночника могут наблюдаться при тяжелых
распространенных формах, особенно когда за­
болевание началось в раннем детстве и прогрес­
сировало по мере развития ребенка.
При опросе, осмотре и пальпации не надо
забывать о возможности встретить явные приз­
наки какой-либо наследственной патологии —
деформацию скелета, добавочные соски молоч­
ной железы, крипторхизм, ксантоматоз и др.
Аускультативные данные могут быть весьма
характерными, но полностью зависят от фор­
мы, распространенности бронхоэктазий, от
фазы течения заболевания. Наиболее типичны
постоянные звучные разнокалиберные хрипы
на фоне жесткого дыхания на стороне пора­
жения, над пораженными отделами легких.
Важно отметить, что хрипы можно выслушать
не только в фазе обострения, но и в фазе ремис­
сии. В общем, степень выраженности аускуль­
тативных данных отчетливо коррелирует с ко­
личеством отделяемой мокроты.
241
Рис. 110. Кистозные бронхоэктазии верхней доли правого
легкого. Прямая рентгенограмма.
Рис. 111. Бронхоэкта ши нижнем доли левого легкого. Брон­
хография под местной анестезией
Однако следует помнить, что данные физи­
кального объективного обследования представ­
ляют для врача меньшую ценность, чем жалобы
и анамнез. Очень нередко больной обращается
к врачу, будучи внешне совершенно здоровым.
При рентгеноскопии и рентгенографии в
большинстве случаев только при очень внима­
тельном исследовании и известном опыте можно
выявить некоторые косвенные признаки брон­
хоэктазий. Исключение составляют кистоз­
ные бронхоэктазии и бронхоэктазии с выра­
женным пневмосклерозом, которые на рентге­
нограммах видны довольно хорошо: в первом
случае виден ячеистый рисунок, во втором —
долевое или сегментарное затенение (рис. 110).
К косвенным рентгенологическим признакам
бронхоэктазий относят усиленный легочный
рисунок или, напротив, обедненный рисунок
(как бы «пустота»— свидетельство эмфиземы
или кист без выраженного склероза), смещение
тени сердца, диафрагмы, средостения (в резуль­
тате цирроза легкого, уменьшения его в разме­
рах), нечеткость контуров сердца, сглаженность
сердечно-сосудистых дуг (указывающее на
шварту). При рентгеноскопии можно видеть
дыхательную деформацию диафрагмы, легоч­
ного рисунка, что бывает при плевральных сра­
щениях.
Рентгенотомография добавляет для диагно­
стики бронхоэктазий немного. Она показана
у пожилых больных, у которых имеется ате­
лектаз (или сегментарный склероз, трудно
отличимый от ателектаза) и у которых в связи
с этим возникают подозрения на опухоль. Томо­
графия показана при подозрении на инородное
тело.
Диагноз ставится окончательно только после
бронхографического исследования.
Бронхография выполняется под местной ане­
стезией или под наркозом, используются раз­
личные контрастные вещества. Поднаркозную
бронхографию одномоментно с двух сторон
рекомендуется делать детям. У взрослых многие
предпочитают бронхографию под местной ане­
стезией с помощью управляемого катетера,
поочередно для каждого из легких. Опыт кли­
ники госпитальной хирургии, где использованы
различные методы, говорит, что любые из них
приемлемы и дают хорошие результаты при
известном навыке. Бронхография под местной
анестезией проще. Она более пригодна в повсе­
дневной практической работе. При ней, однако,
невозможно получить одномоментно хоро­
шие двусторонние бронхограммы. Одномомент­
ная двусторонняя поднаркозная бронхогра­
фия сложнее организационно. Тем не менее
такая бронхография делалась в клинике
амбулаторно 3—4 больным за амбулаторный
утренний прием. При поднаркозной бронхогра­
242
фии, имеющей целью контурное контрастиро­
вание всего бронхиального дерева, не всегда
удается хорошо заполнить бронхи поражен­
ных долей, так как они плохо вентилируются;
однако ориентировочная картина выявляется
достаточно хорошо (рис. 111, 112). В послед­
ние годы в клинике используется метод под­
наркозной контурной бронхографии, дополня­
емой при надобности тугой наливкой поражен­
ных отделов бронхиального дерева с помощью
управляемого катетера (рис. 113). Рентгеногра­
фию производят в прямой и косой проекциях,
а также с выведением пораженных отделов в
наиболее выгодное для обзора положение; дела­
ются снимки на вдохе и на выдохе, позволяю­
щие судить о степени податливости бронхов
разных отделов.
По-видимому, перспективным методом иссле­
дования бронхиального дерева является кино­
бронхография [Углов Ф. Г. и др., 1972]. Воз­
можно, получит признание метод бронхографии
воздушной взвесью танталовой пыли. Некото­
рые ценные данные можно, вероятно, получить
при использовании так называемой терминаль­
ной бронхографии жидкими контрастными
смесями |Феофилов Г. Л. и др., 1973], при ко­
торой, надо полагать, создаются возможности
для выявления степени сообщения бронхоэкта­
тических полостей с вентилируемой легочной
паренхимой, чего при обычной бронхографии
сделать никогда не удается.
Какой бы метод бронхографии при диагно­
стике бронхоэктазий ни использовался, должно
быть соблюдено основное правило: надо полу­
чить достоверные сведения о состоянии брон­
хов всех отделов легких с обеих сторон.
Противопоказанием к бронхографии служат
тяжелое состояние, выраженная дыхательная
недостаточность. Не следует делать бронхо­
графию при легочном кровотечении — кашель
во время исследования или после него может
усилить кровотечение. При большом количе­
стве мокроты перед исследованием надо про­
вести курс санации бронхиального дерева —
наличие мокроты снижает качество бронхо­
грамм, служит причиной ложных заключений.
Следует отметить, что бронхография — не
безопасное для больного исследование. Даже
если она выполнена в наиболее щадящем ва­
рианте и на высоком профессиональном уров­
не, после нее всегда наступает обострение вос­
палительного процесса в легких, повышается
температура тела, усиливается дыхательная
недостаточность. Поэтому другие исследова­
ния, направленные на уточнение диагноза или
предпринимаемые для оценки общего состоя­
ния больного, следует делать прежде бронхо­
графии или спустя некоторый промежуток вре­
мени после нее, когда спровоцированное обо­
lb *
Рис. 112. Бронхоэктазии нижнем доли левого легкого. Брон­
хография под наркозом.
113. Бронхография под наркозом с селективным заполне­
нием пораженных бронхоэктазиями отделов легких.
243
стрение стихает, что обычно происходит не
ранее чем через 1—2 нед.
Ценным дополнительным диагностическим
методом является бронхоскопия. Она абсолют­
но показана при подозрении на опухоль или
наличие инородного тела в бронхе. Бронхоско­
пия проясняет картину при бронхолитах, яв­
ляясь при этом часто решающим диагностиче­
ским (а иногда и лечебным) мероприятием.
По данным бронхоскопии оценивается состоя­
ние слизистой оболочки доступных обозрению
бронхов, выявляются воспаление и его особен­
ности, локализация поражения, распространен­
ность его. Кроме того, при бронхоскопии мож­
но оценить подвижность устьев сегментарных
бронхов. Согласно данным Г. К. Орджоникидзе,
В. М. Матасова (1971), отсутствие подвижно­
сти устья бронха, его сокращения при дыха­
нии и кашле — один из ранних диагностиче­
ских признаков бронхоэктазий данного отде­
ла; он указывает на то, что бронх уже утратил
свою дренажную функцию.
До недавнего времени существовало мне­
ние, что лабораторное и функциональное обсле­
дование больных бронхоэктазиями для диагно­
стики заболевания не имеет большого значе­
ния. С этим нельзя согласиться. Круг этих ис­
следований в специализированных стационарах
и поликлиниках в последнее время существенно
расширен и, как показал опыт, является важным
подспорьем в уточнении диагноза, а главное —
прогноза заболевания, что имеет большое значе­
ние для выбора метода лечения. Данные лабо­
раторного обследования становятся особенно
ценными, если они делаются систематически,
когда больной находится под постоянным вра­
чебным наблюдением. По мнению В. И. Кукоша, С. Н. Захарова (1976), лабораторная и функ­
циональная диагностика на современном этапе
имеет не меньшее значение, чем топическая.
Общеклинический анализ крови в большин­
стве случаев довольно характерен: это умерен­
ная анемия и умеренное повышение СОЭ. Уг­
лубление анемии при динамическом исследова­
нии — свидетельство нарастающей интоксика­
ции, даже если анемия сравнительно невелика.
СОЭ бывает существенно увеличена при рас­
пространении воспаления на легочную парен­
химу; чаще это бывает у детей.
Анализ мочи долгое время остается нормаль­
ным. Стойкое появление в ней белка — небла­
гоприятный признак, свидетельствующий о
поражении почек. Следует обратить внимание
и на плотность мочи, при необходимости про­
вести пробу Зимницкого.
Общий белок сыворотки при бронхоэктазиях
изменяется мало. Чаще имеет место диспротеинемия — уменьшение альбуминов в крови
и повышение глобулиновых фракций. Это на­
стораживает, так как гипоальбуминемия всег­
да является отражением нарушения белковосин­
тетической функции печени. Это может быть
ранним признаком амилоидоза, однако чаще
является следствием хронической гипоксии.
Гиперглобулинемия за счет a-фракций отража­
ет степень реакции организма на воспаление;
об этом же свидетельствуют гипергаммаглобулинемия и повышение содержания фибрино­
гена в крови [Вакалюк П. М. и др., 1971].
Углубленное исследование глобулиновых
фракций белка представляет большую ценность
для выявления иммунодефицитных состояний,
особенно дефицита иммуноглобулинов класса
А. Это укажет на целесообразность иммуно­
терапии, которая в ряде случаев может оказать­
ся весьма эффективной [Штейнгард Б. П.
и др., 1975].
Дефицит IgA может быть обнаружен и в слю­
не, и в мокроте, даже тогда, когда их уровень
в сыворотке крови нормальный.
Многое, как говорилось выше, может прояс­
нить исследование основных электролитов слю­
ны и пота. При этом может быть выявлен скры­
то протекающий муковисцидоз.
Исследование изоферментов лактатдегидро­
геназы сыворотки (ЛДГ) способствует диффе­
ренцировке форм бронхоэктазий: повышение
ЛДГз говорит о преимущественно деструктив­
ных процессах в легких, ЛДГ4 5—о пораже­
нии печени, ЛД1\ 2—об интоксикации, про­
текающей в скрытой форме.
Много внимания уделялось в последнее вре­
мя изучению неспецифического и специфиче­
ского иммунитета [Луценко С. М., Рыбаков А. И.,
1970; Невецкая Л. М. и др., 1971]. Стойкое
снижение титра комплемента, фагоцитарной
активности нейтрофилов, изо- и гетерофильных
антител, стрепто- и стафилолизинов, антипневмококковых антител является неблагоприятным
признаком, указывающим на то, что заболева­
ние имеет склонность к обострениям, которые,
если не были частыми в прошлом,— участятся
в будущем. Такие состояния укажут на целе­
сообразность применения в процессе лечения
(в том числе оперативного) средств стимуля­
ции иммунных механизмов защиты — продигиозана, антистафилококкового глобулина,
анатоксина и др.
Весьма неблагоприятным прогностическим
признаком, даже при общем кажущемся вполне
удовлетворительном состоянии, служит обнару­
жение в сыворотке противолегочных антител.
Выше указывалось, что противолегочная ауто­
иммунизация является существенно важным
звеном патогенеза заболевания: при ней возни­
кает угроза распространения деструктивного
процесса [Китаев М. И., Морозов В. Л., 1970;
Невецкая Л. М., Прозоровская К. Н., 1970].
244
Выделение и идентификация микробной рия, при бронхоэктазиях мало что добавляют
флоры бронхиального дерева в настоящее вре­ к данным простых методик, по крайней мере
мя уже не рассматриваются как дополнитель­ в тех вариантах, в которых бронхоспиромет­
ный метод — сейчас это делается повсеместно рия предлагалась до сих пор,— уточнение пока­
в обязательном порядке, особенно в хирурги­ зателей внешнего дыхания непораженного лег­
ческих стационарах; обязательным является кого по сравнению с пораженным с целью уточ­
определение чувствительности выделенной нения функциональной полноценности легкого
микрофлоры к наиболее распространенным здоровой стороны [Помелов В. С. и др., 1971].
антибиотикам. При сборе мокроты для посева Этот метод, кстати, может быть заменен более
важно, чтобы она не была загрязнена микро­ простым определением степени участия в дыха­
флорой полости рта. Рекомендуют делать посе­ нии каждого из легких с помощью известного
вы смыва с бронхов через бронхоскоп; доста­ латерального теста Бергена. Бронхоспиромет­
точным средством является также полоскание рия могла бы быть более информативной, если
полости рта перед сбором мокроты растворами бы она была использована для оценки степени
сохранения функции не интактных, а поражен­
антисептиков (перманганат калия и др.).
Важным этапом обследования больных яв­ ных отделов легкого в случаях, когда в них
ляется определение показателей внешнего ды­ имеются цилиндрические бронхоэктазии с час­
хания, центральной и легочной гемодинамики. тично сохранившейся вентилируемой легочной
Изучение внешнего дыхания, несмотря на ■ паренхимой. Вероятно, иногда это помогло бы
простоту исследования, дает много ценной ин­ воздержаться от хирургического лечения в ва­
формации, особенно если это делается система­ рианте, когда показания к операции представ­
тически в период поликлинического наблюдения ляются спорными, способствовало бы сбере­
(1—2 раза в год) и во время санации брон­ гательному направлению в данном разделе хи­
хиального дерева (до и после курса лечения). рургии. В этом отношении может представить
Наибольшую ценность из общедоступных пока­ интерес разработка селективной долевой и сег­
ментарной бронхоспирометрии с газовым ана­
зателей представляет определение дыхательных
объемов легких (жизненной емкости), макси­ лизом.
Изменения со стороны сердечно-сосудистой
мальной вентиляции и пневмотахометрия [Антелава Н. В. и др., 1970; Хлопотова Г. П., Лиф­ системы служат в основном для оценки функ­
шиц Н. А., 1973; Углов Ф. Г., Джафаров Ч. М., циональной операбельности. В этом отношении
главным общепризнанным критерием является
1974; Ермолаев В. Р. и др., 1976; Pande J. et al.,
степень легочной гипертензии. Стойкое увели­
1971, и др.]. Для бронхоэктазий характерны
чение среднего давления в легочной артерии
преимущественно рестриктивные нарушения,
довольно четко коррелирующие со степенью выше 35 мм рт. ст. свидетельствует о далеко
распространенности процесса, развитием скле­ зашедших диффузных изменениях, о развитии
роза и эмфиземы, т. е. со степенью выражен­ легочного сердца, о большом операционном
риске. Наиболее надежным методом опреде­
ности необратимых изменений. Сдвиги в пока­
ления давления в легочной артерии является
зателях обструктивных изменений отражают
метод прямого измерения его при зондирова­
в основном степень воспаления слизистой обо­
нии сердца, к которому следует прибегать в сом­
лочки, гипертрофию ее, а также бронхоспасти­
ческий копонент, обычно связанный с воспали­ нительных случаях [Кукош В. И., Захаров С. Н.,
1976].
тельным процессом.
В последние годы для оценки степени нару­
Правильная оценка рестриктивных изме­
шений
легочного кровообращения стали более
нений возможна вне фазы обострения воспале­
ния и после снятия бронхоспазма. Прогрессиру­ широко применять метод сканирования легких
ющее снижение дыхательных объемов, опре­ и ангиопульмонографию [Маневич В. Л. и др.,
деленное при этих условиях, свидетельствует 1971, 1972; Сергеев В. М., Стахов С. Н., 1972].
о, продолжающемся распространении основ­ По данным авторов, при его использовании, как
ного патологического процесса и может являть­ правило, выявляются более распространенные
ся одним из показаний к операции. Вместе с изменения в легких, чем обнаруженные при
тем при выраженных изменениях (уменьше­ бронхографии. Вопрос о том, должно ли это
ние ЖЕЛ более чем на 50 % от должной вели­ служить показанием к расширению объема
чины) могут возникнуть противопоказания к вмешательства, если таковое предпринимается,
вмешательству. По степени уменьшения сдви­ пока остается открытым.
Оценка нарушений функции сердечно-сосу­
гов в показателях обструктивных нарушений
судят об эффективности консервативной те­ дистой системы и дыхания у больных бронхо­
эктазиями производится в клинике в последнее
рапии.
Более сложные исследования аппарата внеш­ время с использованием метода интегральной
него дыхания, в частности бронхоспиромет­ реографии тела по М. И. Тищенко (1970). Этот
245
метод дает возможность выявить одновременно становиться мешотчатыми, могут появляться
и бескровно функциональные резервы сердца, расширения бронхов в ранее не пораженных
степень гемодинамической обеспеченности долях, что для бронхоэктазий вообще не харак­
дыхательной недостаточности, оценить подат­ терно. Именно у больных этой клинической
ливость легких и ориентировочно судить о сте­ группы чаще, чем у больных других групп, воз­
пени легочной гипертензии. Важно, что это мо­ никают рецидивы заболевания после оператив­
жет быть сделано в динамике и с дозированной ного лечения.
Легкая форма клинического течения заболе­
нагрузкой. При использовании метода сравни­
тельно легко и без какого-либо вреда для боль­ вания постепенно может перейти в более тяже­
ного можно рассчитать весьма информативный лую с выраженными клиническими симптома­
«индекс сократительной способности миокарда» ми, что может быти, однако, и с самого начала
[Кукош В. И., Захаров С. Н., 1976], представ­ возникновения бронхоэктазий. Эта группа
ляющий отношение процента прироста удар­ больных с выраженными клиническими проявле­
ного объема крови к проценту учащения пульса ниями является самой многочисленной в хи­
после стандартной нагрузки. Отставание уве­ рургических стационарах пульмонологического
личения ударного объема от частоты пульса, профиля.
Для больных этой группы характерны все
снижение индекса, по данным этих авторов, сви­
детельствуют о низких функциональных ре­ клинические признаки бронхоэктазий — посто­
зервах; уменьшение его до 0,3 и меньше может янный кашель, постоянное выделение мокроты,
служить одним из противопоказаний к опера­ которой периодически становится много, она
приобретает гнойный характер, наблюдается
тивному вмешательству.
Бронхоэктазии могут возникнуть, как указы­ кровохарканье; обострения становятся регу­
валось, сравнительно быстро. Однако течение лярными, сезонными, а иногда возникают и
заболевания длительное, обострения бывают чаще чем 2—3 раза в год. Дети школьного воз­
сначала легкими, непродолжительными, а пе­ раста с данной формой течения заболевания
риоды ремиссии, напротив, продолжаются ме­ подолгу не посещают школьные занятия, взрос­
сяцы и годы. Большинство пациентов на про­ лые часто нетрудоспособны по нескольку меся­
тяжении многих лет может сохранять вполне цев в году.
Для больных этой формы характерна посто­
удовлетворительное состояние и быть трудо­
янная дыхательная недостаточность, выражен­
способными, не меняя образа жизни.
Постепенно все же наступает ухудшение. ная в большей или меньшей степени в зависи­
Обострения становятся более частыми, более мости от фазы обострения или ремиссии. По­
тяжелыми и более продолжительными, а в пе­ являются и признаки интоксикации — голов­
риоды ремиссий полного благополучия уже ная боль, раздражительность, слабость, потли­
нет — продолжается кашель, выделяется мок­ вость.
При рентгенологическом исследовании, как
рота, периодически она становится гнойной,
правило, обнаруживаются заканчивающиеся
может наблюдаться кровохарканье.
При обследовании больных с таким относи­ слепо цилиндрические и мешотчатые брон­
тельно благоприятным течением обычно обна­ хоэктазии. Степень их распространения может
руживаются преимущественно цилиндрические быть различной, но именно у этой группы боль­
бронхоэктазии, часто еще вентилируемые, с ных часто (примерно у 25 %) выявляются дву­
сохраненными периферическими ветвями. В сторонние поражения. Изменения легочной
большинстве случаев они ограничиваются од­ паренхимы — фиброз, ателектаз, эмфизема —
ной-двумя долями и лишь редко бывают с двух имеют место всегда.
сторон. Клинически дыхательной недостаточ­
Данные лабораторных и специальных иссле­
ности нет. Она может быть выявлена при опре­ дований весьма характерны. Они описаны выше.
делении показателей внешнего дыхания.
Особенно характерны сдвиги со стороны внеш­
По И. С. Колесникову, В. Р. Ермолаеву (1969), него дыхания. В фазе ремиссии отчетливо вы­
такую форму течения можно назвать началь­ являются признаки рестриктивной дыхатель­
ной и легкой. Обычно она бывает у детей, осо­ ной недостаточности; в фазе обострения недо­
бенно в подростковом возрасте. Называя эту статочность рестриктивного типа углубляется,
форму, «начальной», авторы подчеркивают воз­ присоединяется недостаточность обструктивного
можное стадийное развитие бронхоэктазий, типа.
протекающих в таком варианте, что подтверж­
Консервативное лечение больных этой груп­
дается клиническим анализом течения заболе­ пы дает обычно лишь временный эффект. Не­
вания и данными повторных обследований смотря на достаточно интенсивную терапию,
больных. При несвоевременно предпринятом заболевание постепенно прогрессирует. Ухудше­
или нерегулярном лечении цилиндрические ние состояния, как правило, не является след­
бронхоэктазии у больных этой группы могут ствием распространения бронхоэктазий или
246
изменения их патоморфологической формы,
а является результатом все более нарастаю­
щих диффузных изменений в легких, хрониче­
ской гипоксии и интоксикации.
Постепенно заболевание приобретает тяже­
лую и очень тяжелую формы течения, для кото­
рых характерна сердечно-легочная недостаточ­
ность по типу легочного сердца, высокая легоч­
ная гипертензия, дистрофические изменения
внутренних органов, прежде всего почек. Может
развиться амилоидоз. Прогноз у подавляюще­
го большинства больных этой группы неблаго­
приятный.
Таким образом, по клиническому течению
можно выделить три основные типичные фор­
мы заболевания: легкую, форму выраженных
(умеренных и более отчетливых) клинических
проявлений и тяжелую.
В числе особых клинических форм выделяют
так называемые «сухие бронхоэктазии» [Цигельник А. Я., 1948], для которых характерны
постоянный персистирующий кашель, крово­
харканье и легочные кровотечения, а также
нарастающая одышка, дыхательная недоста­
точность.
Другой своеобразной формой заболевания
являются бронхоэктазии с выраженным астма­
тическим компонентом. В клиническом тече­
нии у этих больных преобладает дыхательная
недостаточность по типу бронхиальной астмы.
Такое течение бронхоэктазии могут приобрести
в любом возрасте и при любой форме перво­
начальных проявлений. Природа его, по-види­
мому, инфекционно-аллергическая. Астмати­
ческие приступы особенно часты в периоды обо­
стрений.
Своеобразной клинической формой течения
бронхоэктазий являются бронхоэктазии, ослож­
ненные язвой желудка или двенадцатиперст­
ной кишки, склонной к кровотечениям. Подоб­
ные формы течения хронических неспецифи­
ческих воспалительных заболеваний легких не­
редки, служат предметом обсуждения в литера­
туре [Иоселиани Г. Д., Ефремов А. В., 1976,
и др.].
Как отмечалось ранее, для бронхоэктазий
детского возраста в общем характерны сравни­
тельно частые, но кратковременные обострения,
протекающие с выраженной общей реакцией.
У детей особенно часто бронхоэктазиям сопут­
ствуют синуситы. Бронхоэктазии у пожилых
людей протекают с более выраженными явле­
ниями дыхательной и сердечно-сосудистой не­
достаточности, у них чаще бывают кровохар­
канья и легочные кровотечения. Эти особенно­
сти у пожилых лиц обусловлены не только са­
мим заболеванием, но также возрастной эмфи­
земой, пневмосклерозом, возрастными измене­
ниями сердечно-сосудистой системы.
Из осложнений течения бронхоэктазий сле­
дует упомянуть о спонтанном пневмотораксе,
абсцессе легкого, эмпиеме плевры, метастати­
ческом абсцессе мозга и раке. Спонтанный
пневмоторакс иногда бывает при кистоподоб­
ных бронхоэктазиях. На 624 больных, находив­
шихся под наблюдением в клинике, он возник
у 1 больного.
Абсцесс легкого — более частое осложне­
ние: он отяготил течение бронхоэктазий у 9
больных этой группы. Абсцесс обычно разви­
вался в здоровых долях или сегментах, не по­
раженных бронхоэктазиями; нередко он лока­
лизуется в VI сегменте. Причину абсцесса сле­
дует усматривать в затекании мокроты в здо­
ровые отделы бронхиального дерева.
Эмпиема плевры как следствие нагноения
выпотного плеврита наблюдалась у 6 больных.
Абсцесс мозга возник у 1 человека.
Рак легкого как осложнение течения брон­
хоэктазий у пожилых больных не так уж редок
[Брауде В. И., 1971; Arrigoni М. et al., 1971, и
др.]. Здесь надо подчеркнуть, что речь идет не
о раке, вызвавшем бронхоэктазии, а об опухоли,
возникшей на фоне длительно протекавшего
хронического воспаления с преимуществен­
ным исходом в пневмосклероз. Такие опухоли
иногда являются случайной находкой при ре­
зекции легкого по поводу бронхоэктазий. Про­
исхождение опухоли в этом случае, по-видимому,
близко к известному из литературы «раку из
рубца» [Robe R., 1966].
Дифференцировать бронхоэктазии у детей
и лиц молодого возраста приходится прежде
всего от туберкулеза легких: особенности те­
чения бронхоэктазий у детей весьма напоми­
нают туберкулез. Неудивительно, что почти
половина детей, больных бронхоэктазиями,
сначала длительное время наблюдаются и ле­
чатся у фтизиатров [Кухаренко С. Д., 1972,
и др.].
В пользу бронхоэктазий говорят отсутствие
эпидемиологического анамнеза, сравнительно
длительное течение, характерные сезонные
обострения, постоянное выделение гнойной
мокроты, а также преимущественно нижнедо­
левая локализация процесса. Физикальные
аускультативные данные при туберкулезе обыч­
но скудны, тогда как при бронхоэктазиях до­
вольно ярко выражены, особенно в периоды
обострений. Важны в дифференциальной диа­
гностике результаты туберкулиновых проб,
наличие (или отсутствие) при повторных иссле­
дованиях микобактерий туберкулеза в мокроте.
О бронхоэктазиях с наибольшей достоверно­
стью свидетельствуют результаты бронхогра­
фического исследования, хотя и при установ­
ленных бронхоэктазиях исключить туберку­
лез бывает трудно, так как туберкулез может
247
предшествовать бронхоэктазиям, быть их при­
чиной, сопутствовать им.
Посттуберкулезные бронхоэктазии у взрос­
лых требуют исключения активного специфи­
ческого процесса. Это подчас тоже трудная за­
дача, решить которую сразу удается далеко не
всегда. В таких случаях наряду с лечением
бронхоэктазий проводят полный курс противо­
туберкулезной терапии.
Дифференцировать бронхоэктазии у взрос­
лых часто приходится с хроническим бронхи­
том. При этом надо иметь в виду, что хрониче­
ский бронхит — частое заболевание, а бронхо­
эктазии — значительно более редкое, что хрони­
ческий бронхит имеет совсем другое клиниче­
ское течение. Для бронхита более характерны
постоянный кашель со скудной мокротой, по­
степенно нарастающая одышка, а периоды обо­
стрений протекают по типу воспаления лег­
кого, т. е. совершенно не так, как при бронхо­
эктазиях. Решить вопрос помогает бронхогра­
фия, хотя и после нее могут остаться сомне­
ния, так как при деформирующем бронхите
могут быть обнаружены отдельные расширен­
ные бронхи. Два важных рентгенологических
признака более характерны для бронхита: рас­
пространенность, диффузность поражения
легких и сохранение вентилируемой легочной
паренхимы; последняя претерпевает эмфизе­
матозные изменения, но не склеротические, а
тем более не цирротические.
Довольно частым при бронхоэктазиях явля­
ется диагноз хронической пневмонии. Он отпа­
дает сразу же после бронхографического ис­
следования, устанавливающего типичное рас­
ширение бронхов. При отсутствии же брон­
хоэктазий у таких больных, как правило, выяв­
ляются признаки бронхита. Таким образом,
для хронической пневмонии как самостоятель­
ной нозологической формы в легочной патоло­
гии практически не остается места [Коле­
сов А. П., Гаджиев С. А., 1973; Ржаницин В. В.,
1975, и др.].
Бронхоэктазии иногда по течению трудно
отличить от хронического абсцесса легких, осо­
бенно от более или менее хорошо дренирую­
щейся полости (или полостей). При абсцессе
правильной диагностике способствуют типич­
ные анамнестические данные — острое начало,
эпизод внезапного отхождения большого коли­
чества мокроты и др. Полости абсцесса хорошо
выявляются при томографическом исследова­
нии, они имеют типичную для абсцесса лока­
лизацию — в задних сегментах легкого. При
бронхографии эти полости часто не заполня­
ются контрастным веществом, а если запол­
няются, то видны дренирующие абсцесс брон­
хи, как правило, небольшого диаметра; боль­
шая часть бронхиального дерева при этом из­
менена незначительно, т. е. бронхи не расши­
рены, лишь деформированы; отсутствует типич­
ный для бронхоэктазий сегментарный харак­
тер поражения.
При обследовании больных нередко встает
вопрос: бронхоэктазии или локальный пневмо­
склероз? Локальный пневмосклероз бывает
различного происхождения, а следовательно,
дифференцировать необходимо от бронхоэкта­
зий пневмосклероз разного характера.
Одним из таких склерозов является склероз
средней доли (или язычка) легкого — форма
так называемого среднедолевого синдрома. При
такого рода пневмосклерозе обычно выявля­
ются и бронхоэктазии IV—V сегментарных
бронхов. Клиника, течение, последствия и ме­
тоды лечения при этом совершенно аналогич­
ны бронхоэктазиям (легкой форме). Поэто­
му пневмосклероз средней доли следует считать
одной из форм течения бронхоэктазий.
Другого характера пневмосклероз наблюда­
ется после перенесенного абсцесса легкого. Ес­
ли при этом сохраняется полость (как правило,
сухая), но есть угроза рецидива абсцесса в хро­
нической форме (особенно когда эта угроза
в той или иной степени реализуется) — эту
форму следует отнести к хроническому абс­
цессу [Колесников И. С., Вихриев Б. С., 1973].
В случае, когда сухая полость после абсцесса
протекает бессимптомно, можно говорить о лож­
ной кисте; в этом случае нет возражений также
против термина «пневмосклероз после абсцесса».
Локальный пневмосклероз в легком может
быть следствием полностью зажившего абсцес­
са или пневмонического очага с исходом в ру­
бец. Иными словами, это результат благоприят­
ного течения острого воспаления. Однако, как
всякий рубец, такой склероз может причинять
некоторые беспокойства, становясь уже сам по
себе болезнью. Клиника госпитальной хирургии
имеет опыт наблюдения за такими больными.
Чаще всего они поступали с диагнозом рака,
а иногда и оперировались с подозрением на
это заболевание.
Обычно это были пожилые пациенты, склон­
ные к диффузному пневмосклерозу вообще,
который у них, наряду с локальным, и выявля­
ется. Они жаловались на одышку; это была наи­
более частая жалоба. Другим проявлением
было кровохарканье, изредка довольно обиль­
ное, типа кровотечений. Третьей жалобой была
жалоба на боль в груди. Боли в груди, по-видимому, были следствием спаечного процесса
в плевральной полости. При бронхографии у
таких пациентов бронхоэктазии не обнаружи­
ваются, но находят изменения, напоминающие
хронический деформирующий бронхит, хотя
клиники бронхита у них нет. Поскольку нет
ни клиники бронхита, ни клиники бронхоэкта­
248
зий, ни к тому ни к другому заболеванию эту
патологию отнести нельзя. Оперативному ле­
чению такие больные не подлежат. Случайно
оперированные (с подозрением на рак), осо­
бенно которым сделаны обширные резекции,
послеоперационный период из-за распростра­
ненного пневмосклероза переносили, как пра­
вило, тяжело, а в отдаленном периоде у них
выявлялась выраженная дыхательная недо­
статочность.
Бронхоэктазии с астматическим компонен­
том иногда принимают за бронхиальную аст­
му и наоборот. Несмотря на общность этиоло­
гического фактора (инфекционного) — это раз­
ные болезни. Астматические приступы при брон­
хоэктазиях могут быть совершенно идентич­
ны приступам при астме. Однако в промежут­
ках между ними клиника бронхоэктазий все
же сохраняется. При астме же ее нет. Разное
у этих категорий больных и течение заболе­
вания. Анализ клиники и течения, а также дан­
ные бронхографического исследования позво­
ляют разграничить эти страдания. Бронхогра­
фия при длительно текущей бронхиальной аст­
ме может дать картину периферического рас­
ширения бронхиол (бронхиолэктазий Лешке).
Но они совершенно не похожи ни на одну из
патоморфологических форм типичных бронхо­
эктазий.
Иногда возникает необходимость дифферен­
циальной диагностики нагноившихся кист лег­
кого и кистозных бронхоэктазий, а также на­
гноившихся полостей при внутридолевой сек­
вестрации и при других врожденных анома­
лиях. Дифференцировать эти заболевания ча­
сто можно только на основании данных брон­
хографии, при которой в случае кист бронхи­
альное дерево может иметь практически нор­
мальный вид. При аномалиях типа секвестра­
ции поможет ангиография, которая выявит ати­
пичное (из болыцого круга кровообращения)
артериальное кровоснабжение пораженного
участка.
Не всегда бывает легко дифференцировать
бронхоэктазии и рак легкого
[Шеляховский М. М., 1960; Воропаев М. М., Адамян А. А.,
1971]. Бронхоэктазии, с одной стороны, могут
быть следствием опухоли, а с другой стороны,
опухоль может возникнуть на фоне бронхоэкта­
зий. При диагностических трудностях такого
рода в ходе диагностики у пожилых больных,
особенно у мужчин, надо идти по пути исклю­
чения рака. Особенно трудна дифференциаль­
ная диагностика опухоли средней доли (или
язычка) и бронхоэктазий этой области. От­
правными пунктами для суждений являются
данные томографии, бронхоскопии, бронхоско­
пической биопсии и исследований мокроты (про­
мывных вод бронхов) на атипичные клетки;
данные бронхографии здесь не являются ре­
шающими. И все же окончательно диагноз без
операции иногда установить не удается. В сом­
нительных случаях показана эксплоративная
торакотомия.
ЛЕЧЕНИЕ
Учитывая, что при бронхоэктазиях имеют
место необратимые изменения, а течение забо­
левания характеризуется в основном прогрес­
сирующим ухудшением состояния, развитием
тяжелых расстройств, приводящих в конеч­
ном итоге к глубокой инвалидности и прежде­
временной смерти, основным методом лечения
бронхоэктазий следует считать хирургический.
В этом вопросе сейчас противоречивых мне­
ний нет. Однако существуют разные взгляды
на показания и противопоказания к операции,
выбор метода оперативного лечения при раз­
личных формах заболевания, при различных
вариантах течения. Не решен окончательно
также вопрос о том, какой возраст при брон­
хоэктазиях у детей и у взрослых является наи­
более подходящим для хирургического вме­
шательства.
Показания к операции, очевидно, должны
прежде всего учитывать прогноз в разных груп­
пах больных, особенности течения заболева­
ния у них, а также возможности консерватив­
ной терапии.
Показания к операциям неотложного харак­
тера могут возникнуть при осложнениях, преж­
де всего при легочном кровотечении. Профуз­
ное легочное кровотечение, как указывалось, в
общем для бронхоэктазий не характерно. Од­
нако оно все же бывает и среди больных хрони­
ческими неспецифическими заболеваниями
легких занимает не последнее место. Согласно
сводным данным литературы [Семенова Л. П.,
1960; Абдуллаев Г. И. и др., 1974; Домбаев М. Д.,
1975; Чернобровый Н. П. и др., 1976], массив­
ное легочное кровотечение, требующее неот­
ложных мероприятий, при хронических неспе­
цифических воспалениях наблюдается в 6—8 %
случаев; из них почти половина (20—42 %) —
больные бронхоэктазиями.
Опыт показал, что консервативное лечение
(переливание крови, гемостатические препа­
раты, лекарства, угнетающие кашель, и др.)
в такой ситуации малоэффективны. Кровоте­
чение удается остановить лишь у немногих па­
циентов, причем в большинстве случаев не окон­
чательно. Летальность при консервативной те­
рапии достигает 50 % и более [Палиашви­
ли В. А., 1972; Juhasz L., Ungar J., 1970, и др.].
Причиной смерти лишь отчасти является кро­
вотечение как таковое; главным образом — это
дыхательная недостаточность и пневмония,
249
развивающиеся вследствие аспирации крови
в здоровые участки легкого.
В случае профузного легочного кровотече­
ния (при потере крови до 0,5 л/сут и более)
показания к операции могут быть неотложны­
ми (на высоте кровотечения), срочными (в бли­
жайшие несколько дней, при стихающем кро­
вотечении) и поздними (после остановки кро­
вотечения). Наилучшие результаты получены
при операциях, выполненных по срочным пока­
заниям: кровотечение удавалось остановить
практически всегда, ближайшие исходы у 95 %
больных оказались хорошими. У большинства
больных при этом было достигнуто и полное
выздоровление. Исключение составляли слу­
чаи, когда операции с целью остановки крово­
течения производились при двусторонних брон­
хоэктазиях.
Основным видом операции является резек­
ция пораженных отделов легкого, которые на
операции хорошо видны, так как пропитаны
кровью. Перед операцией необходимо точно
установить, из какого легкого происходит кро­
вотечение, а также дифференцировать, не яв­
ляются ли источником кровотечения верхние
дыхательные пути, желудочно-кишечный тракт.
В решении этих вопросов помогают простей­
шее рентгенологическое исследование и брон­
хоскопия. При бронхоскопии в некоторых слу­
чаях в качестве временной меры, предупрежда­
ющей затекание мокроты и крови в здоровые
отделы легких, целесообразна тампонада брон­
хов. Для остановки кровотечения рекомендовали
и более сложные приемы, например временную
окклюзию легочной артерии на стороне пора­
жения с помощью специальных сердечных зон­
дов с манжеткой [Натадзе Д. А. и др., 1973];
данное предложение пока имеет немного сто­
ронников. Бронхоскопия после операции явля­
ется обязательной.
Другим показанием к срочному оператив­
ному вмешательству при бронхоэктазиях слу­
жат гнойные осложнения — острые абсцессы,
особенно склонные к гангрене, пиопневмоторакс, а также спонтанный пневмоторакс с яв­
лениями напряженного пневмоторакса или
выраженного гемоторакса. При бронхоэкта­
зиях такие осложнения встречаются редко.
Лечение их описано в соответствующих раз­
делах монографии.
Для оценки прогноза в разных группах боль­
ных бронхоэктазиями наибольшую ценность
представляют материалы о судьбе пациентов,
находившихся под наблюдением длительное
время и лечившихся консервативно, а также
материалы о судьбе больных, которые находи­
лись в хирургических стационарах и которым
была предложена операция, но они были выпи­
саны по тем или иным причинам.
По данным Н. П. Чернобрового (1973), при
диспансерном наблюдении за 612 больными
бронхоэктазиями в течение 10 лет периодиче­
ски проводившееся консервативное лечение
оказалось эффективным у 487 человек (у
81,2 %). Обострения у них либо прекратились,
либо стали редкими и кратковременными, а пе­
риоды ремиссии, наоборот, продолжительными;
заболевание стало мало беспокоить, они зани­
мались обычным для себя трудом. В эту группу
входили в основном больные с умеренным рас­
ширением бронхов, однако какое-то число и со
значительным расширением тоже — со смешан­
ными и мешотчатыми формами. Независимо
от характера расширения бронхов заболевание
у этой группы больных с самого начала проте­
кало в сравнительно легкой форме или в фор­
ме выраженных клинических проявлений, но
без тяжелой клинической картины. У 16,8 %
больных либо не наблюдалось улучшения, либо
отмечалось ухудшение состояния. У этих боль­
ных, как правило, выявлялись мешотчатые фор­
мы, заболевание с самого начала протекало
с выраженными клиническими проявлениями
и часто тяжело. У некоторых из них наблюда­
лись осложнения в виде легочных кровотече­
ний, абсцедирования, развития легочного серд­
ца, амилоидоза. Автор считает, что именно эта
вторая, меньшая группа больных подлежит
хирургическому вмешательству.
С. В. Сахаров и соавт. (1970) при длитель­
ном наблюдении и интенсивной терапии отка­
зались от операции у 58,2 % больных. Это также
были пациенты в основном с относительно
легким клиническим течением.
Результаты отдаленных наблюдений (в те­
чение более чем 10 лет) за больными, выписан­
ными из клиники госпитальной хирургии по
разным причинам, показали [Ермолаев В. Р.,
1972], что среди отказавшихся от операции
улучшение состояния или состояние без изме­
нений (бронхоэктазии с относительно легким
течением и с выраженной клинической фор­
мой) наблюдались у 37 % больных, ухудше­
ние — у 31 %; остальные были в последующем
оперированы. Среди выписанных в связи с пред­
полагавшейся неоперабельностью из-за тяже­
сти состояния и распространенности процесса
(бронхоэктазии с выраженной и тяжелой фор­
мами клинического течения) улучшение или
относительно удовлетворительное состояние без
ухудшения отмечено у 27 % больных, умерли
57 %; остальные находились на момент осмот­
ра в крайне тяжелом состоянии.
Приведенные данные свидетельствуют о том,
что настойчивая консервативная терапия может
быть определенным объективным критерием
оценки показаний к операции. При этом выяв­
ляется, что, с одной стороны, почти у половины
250
больных в операции настоятельной необходи­
мости нет и вопрос о ней может вообще отпасть,
а с другой стороны, у второй половины опера­
ция оказывается безусловно необходимой. Как
в той, так и в другой группах могут находить­
ся пациенты и с относительно легким клиниче­
ским течением, и с выраженной, а также тяже­
лой формой заболевания.
Учитывая эти данные и принимая во внима­
ние то, что больные бронхоэктазиями в подав­
ляющем большинстве не требуют оказания сроч­
ной хирургической помощи, вопрос о показа­
ниях к хирургическому лечению должен ре­
шаться только после достаточно длительного
курса интенсивного терапевтического лечения.
Терапевтическое лечение включает обяза­
тельную санацию верхних дыхательных путей
и полости рта (зубов). Больные должны соблю­
дать строгий режим поведения, «следить за сво­
им здоровьем». Этот режим отрабатывается
индивидуально, но предусматривает в каче­
стве необходимого компонента дыхательную
гимнастику с постуральным дренажем, дози­
рованную физкультуру.
В предвесенний и послеосенний периоды (пе­
ред обычными в это время обострениями, но
независимо от них) они проходят курс эндо­
бронхиальной санации. В относительно легких
случаях это делается амбулаторно — прово­
дится ежедневное промывание (лаваж) трахео­
бронхиального дерева через назотрахеальный
катетер. В более тяжелых случаях показано
стационарное лечение в специализированных
пульмонологических отделениях, где при необ­
ходимости делается также санация через брон­
хоскоп. Курс санации занимает обычно 10—14
дней.
При лаваже используются теплый изотони­
ческий раствор натрия хлорида, фурацилин,
йодинол, новокаин, натрия бикарбонат (5 %)
с последующим введением протеолитических
ферментов, разжижающих мокроту (ацетил­
цистеин, химопсин, рибонуклеаза и др.), гидро­
кортизона, а в особо упорных случаях — анти­
биотиков с учетом чувствительности к ним
микрофлоры бронхов [Углов Ф. Г., Джафа­
ров Ч. М., 1974; Чернобровый Н. П., 1972; Бул­
гаков Я. У., 1975; Ramizer R., 1966, и др.].
После лаважа и в промежутках между сеан­
сами его (а также в амбулаторных условиях
и при необходимости дома) делаются систе­
матические паровые ингаляции.
Из лекарственных препаратов больные полу­
чают эуфиллин, витамины, экстракт алоэ, пентоксил. При наклонностях к бронхоспазму
назначаются бронхолитики.
В борьбе с инфекцией, наряду с антибиоти­
ками и местными антисептическими средства­
ми, могут использоваться также такие препара­
ты специфического действия, как аутовакцина,
приготовленная из микрофлоры бронхов [Маль­
цев А. М. и др., 1971], стафилококовый ана­
токсин, антистафилококковая сыворотка [Недвецкая Л. М. и др., 1973]. Для стимуляции не­
специфического иммунитета рекомендуют
пирогенал, продигиозан [Луценко С. М. и др.,
1970; Чекин С. Т., Рыбалко С. И., 1974] и пр.
У пожилых больных с сопутствующей пато­
логией, например с сердечно-сосудистыми за­
болеваниями, она требует лечения и этих забо­
леваний по соответствующим показаниям.
Для всех больных желательно санаторнокурортное лечение не реже одного раза в год.
Условия климата решаются индивидуально.
Интенсивная терапия проводится в течение
2—3 лет. Контроль эффективности ее осущест­
вляется как по клиническим данным, так и по
данным лабораторного и специального обсле­
дования, предпринимаемого периодически. Ла­
бораторное и специальное обследование дела­
ется обычно перед курсом санации бронхов и
после него.
В обязательном порядке делается общеклини­
ческий анализ крови и мочи, определяется со­
держание белка в сыворотке. Желательна про­
ба на С-реактивный белок. При использовании
для лечения антибиотиков каждый раз опреде­
ляется чувствительность к ним микрофлоры
мокроты и ставятся аллергические пробы.
Важным показателем эффективности прово­
димой терапии является исследование внеш­
него дыхания; крайне желательно иметь дан­
ные об изменениях давления в малом круге
кровообращения.
Контрольная бронхография делается по весь­
ма ограниченным показаниям. Она показана
у больных с выраженными проявлениями забо­
левания, у которых не удается добиться улуч­
шения состояния, или при ухудшении его. Как
правило, повторная бронхография показана в
предвидении оперативного лечения.
Интенсивно проводимое терапевтическое
лечение является одновременно хорошим (и
необходимым) методом подготовки к операции,
коль скоро таковая предстоит. В этом случае
средства терапии могут быть расширены за
счет использования некоторых новых специаль­
ных методов. С. А. Гаджиев и соавт. (1966),
Ф. Г. Углов и соавт. (1969), С. X. Авдакбелян
и соавт. (1970), Р. А. Галкин (1970), С. Т. Че­
кан, Л. И. Рыбалко (1974) и мн. др. настойчиво
рекомендуют введение антибиотиков в ветви
легочной артерии и санацию трахеобронхиаль­
ного дерева через микротрахеостому.
И. И. Неймарк, Ю. К. Норкайтис (1973)
установили, что при введении антибиотиков
в ветви легочной артерии в легком создается
концентрация их, превышающая в 4,5 раза кон-
251
Рис. 114. Трансторакальное дренирование бронхов.
центрацию, когда антибиотики вводятся внутри­
венно. Правда, аналогичная концентрация на­
блюдается при инфузии их через катетер, вве­
денный в устье полой вены через подключич­
ную. Вероятно, для практики этот последний
метод более приемлем.
Микротрахеостомия осуществляется путем
чрескожного прокола трахеи на шее толстой
иглой с введением через нее микроирригатора.
С помощью бронхоскопа конец ирригатора уста­
навливается в области устья пораженных брон­
хов. Через ирригатор осуществляется ороше­
ние (промывание) бронхов 4—5 раз в день.
По мнению С. X. Авдалбекяна и соавт. (1970),
такое лечение особенно эффективно именно
при бронхоэктазиях. Эффект даже в тяжелых
случаях отмечается уже через 2—3 дня.
В госпитальной хирургической клинике ис­
пользуется оригинальная методика санации
бронхиального дерева через ирригатор (кате­
тер), установленный в пораженном долевом
(сегментарном) бронхе трансторакально, через
грудную стенку (рис. 114). Методика установ­
ки такого ирригатора предложена И. С. Колес­
никовым и В. Т. Плешаковым [Плешаков В. Т.
и др., 1979|. Она состоит в следующем.
Через бронхоскоп (лучше двухпросветный)
вводится в нужный бронх направляющий полужесткий катетер; через него проводится длин­
ная игла, прокалывающая периферические от­
делы легкого, плевру и мягкие ткани стенки
груди (кожа надсекается скальпелем); после
извлечения направляющего катетера и укреп­
ления к игле ирригатора последний протягива­
ется через трубку бронхоскопа и бронх вслед
за иглой; конец его под контролем гла за уста­
навливается у устья бронха или непосредственно
за устьем; выведенная через грудную стенку
часть ирригатора фиксируется к коже швом.
Промывание бронхов, введение в бронхиальное
дерево лекарственных средств производятся
в течение дня многократно (5—6 раз). При
достаточном диаметре ирригатора (3—4 мм)
он может выполнять дренажную функцию: у
некоторых наших больных бронхоэктазиями
через него за сутки отходило до 150 мл гнойной
мокроты.
Указанные новые методы санации трахео­
бронхиального дерева существенно расширя­
ют возможности терапевтического лечения
бронхоэктазий, способствуют наиболее эффек­
тивной подготовке к операции и создают усло­
вия для наиболее благоприятного течения пос­
леоперационного периода.
Неэффективность всех основных средств
консервативной терапии в течение 2—3 лет
является показанием к операции. При этом воз­
никает необходимость решения вопросов, свя­
занных с ее проведением: оптимальный срок
в зависимости от возраста, оптимальный объем
резекции легкого и противопоказания к вмеша­
тельству.
Что касается возраста, то, по мнению боль­
шинства авторов, наиболее подходящим воз­
растом для детей является возраст после 7—
10 лет [Колесов А. П„ Чухловина М. Г., 1962;
Ищенко Б. И. и др., 1972; Бойков Г. А., 1973; Пу­
гачев А. Г. и др., 1974, и др.]. При операциях,
сделанных в более раннем возрасте, отдален­
ные результаты оказались менее благоприятны­
ми. Это объясняется, с одной стороны, ана­
томо-физиологическими особенностями лег­
252
кого у детей младшей возрастной группы, кото­
рые обусловливают склонность к послеопера­
ционным ателектазам, инфекции и возникно­
вению рецидива заболевания, а с другой сторо­
ны, у маленьких детей часто трудно достаточ­
но четко отграничить зону поражения, что яв­
ляется причиной остаточных (резидуальных)
бронхоэктазий. Нельзя не считаться также
с тем мнением, что у части детей при интенсив­
ном терапевтическом лечении некоторые формы
бронхоэктазий в процессе роста ребенка как
бы подвергаются обратному развитию с восста­
новлением нормальной картины бронхов — так
называемые «динамические формы бронхо­
эктазий» |Рошаль М. Н., 1969; Макаров И. А.,
1969; Никулин К. Г. и др., 19701. Показания к
операции у детей раннего возраста могут быть
расширены только при тяжелом течении, при
отсутствии эффекта от терапевтического лече­
ния и при четко ограниченных смешанных и
мешотчатых формах поражения [Пугачев А. Г.
и др., 1974|.
Возрастные ограничения у взрослых менее
определенны. Здесь применима формула: «чем
раньше оперируется больной — тем лучше».
Отдаленные функциональные результаты в об­
щем у больных старше 40 лет хуже, чем у лиц
более молодого возраста. Однако после опе­
раций, сделанных по правильным показаниям,
с хорошо проведенной предоперационной под­
готовкой, функциональные показатели в отда­
ленном периоде после вмешательства всегда
выше, чем до него, даже у больных, опериро­
ванных в весьма преклонном возрасте — 60—
74 года |Избинский А. Л. и др., 1971; Ермо­
лаев В. Р. и др., 1975|. Следует подчеркнуть,
что преклонный возраст больных не исключает
у них необходимости длительной предопера­
ционной консервативной терапии, а, напротив,
предполагает ее.
Вопрос об объеме резекции легкого при брон­
хоэктазиях обсуждался в течение многих лет.
Вполне понятно стремление к ограничению
объема операции, к максимальному сохране­
нию функционирующей легочной паренхимы
[Ермолаев В. Р., 1962; Герасименко Н. И., Пи­
рогов А. И., 1967; Пугачев А. Г. и др., 1970,
1972; Исаков Ю. Ф. и др., 1973, и др.|. Особен­
но важно это при двусторонних поражениях.
Стремление к таким «сберегательным» опера­
циям реализовалось в расширении показаний
к комбинированным сегментарным резекциям —
удалению базальной пирамиды и одного из сег­
ментов (V) средней доли, одного или двух сег­
ментов язычка с оставлением VI сегмента, уда­
лению средней доли и отдельных сегментов
базальной пирамиды (VII, например). Отда­
ленные результаты показали, однако, что такие
сберегательные операции довольно часто были
недостаточно оправданны, так как оставление
участков легкого с измененными в виде де­
формирующего бронхита и даже пневмоскле­
роза, распространившегося с соседних сегмен­
тов (с X на VI, например), практически неми­
нуемо вело к рецидиву заболевания, необходи­
мости повторных вмешательств.
Другой крайностью являются недостаточно
оправданное расширение объема операции,
удаление участков легкого, которые, по дан­
ным предварительного обследования и при ос­
мотре во время операции, кажутся здоровыми,
но в которых часто наблюдается рецидив. По
мнению Л. М. Рошаля (1969), Ф. Г. Углова
(1976), удаление базальной пирамиды, как пра­
вило, должно сочетаться с удалением IV—V
сегментов, если даже они кажутся здоровыми.
По мнению многих, оставлять кажущийся здо­
ровым VI сегмент при удалении сегментов ба­
зальной пирамиды нецелесообразно. Вряд ли
такая точка зрения может быть оправдана. В ука­
занных сегментах действительно часто наблю­
дается рецидив заболевания, но лишь при не­
достаточной предоперационной подготовке,
при дефектах, допущенных во время операции
и в послеоперационном периоде.
При определении объема резекции, по-види­
мому, наиболее правильной тактикой будет
стремление к максимальному удалению пора­
женной части легкого, необратимо утратив­
шего свою функцию, и в то же время стремле­
ние к максимальному сохранению малоизмененных отделов [Ермолаев В. Р., 1971; Гаджи­
ев С. А. и др., 1972; Кухаренко С. Д., 1973; Гауен Я. К. и др., 1976: Thumann Н. et al„ 1971,
и др.].
Для уточнения размеров и локализации по­
раженных участков во время операции В. А. Климанский [Климанский В. А., Ревис М. Г., 1971J
предложил пробу на эластичность легочной
ткани: после раздувания легкого с помощью
наркозного аппарата делается резкая аспира­
ция содержимого бронхов; пораженные отде­
лы при этом не спадаются. Во время операции
допустима и срочная биопсия периферических
отделов участков легкого, сомнительных в мор­
фологической и функциональной полноцен­
ности. Удалению подлежат сегменты, в кото­
рых обнаруживаются выраженные необрати­
мые (склеротические) изменения: они всегда
указывают на необратимые изменения в брон­
хах. Участки с обратимыми изменениями в виде
остаточных явлений воспаления паренхимы
сохраняются. По данным В. А. Климанского
(1971), благодаря такой методике удалось су­
щественно сократить объем резекции у 22 боль­
ных из 131.
Важную роль в успешности таких операций
играет оперативная техника. Резекция долж­
253
на производиться строго анатомично. Приме­
нение сшивающих аппаратов для ткани легкого
должно быть исключено [Колесников И. С.
и др., 1965]. Свободные межсегментарные
плоскости желательно прикрыть лоскутом плев­
ры (можно использовать лоскут с удаляемой
части легкого). Длинные культи бронхов остав­
лять нельзя. Герметизация швов обязательна.
Последнее контролируется раздуванием легкого
в жидкости, налитой в плевральную полость.
Успех операции может быть обеспечен только
тогда, когда после зашивания раны грудной
стенки остаток легкого полностью расправится
без перерастяжения легочной ткани, перегибов
бронхов, сдавления отдельных участков. Рас­
правление легкого обеспечивается в первую
очередь соответствием его эластичности и объе­
ма объему полости плевры. Важно, чтобы были
сохранены хорошая вентиляция, хороший
крово- и лимфоток. Для предупреждения пере­
гибов бронхов, перекручивания их иногда при­
ходится зафиксировать периферические отде­
лы: сегменты язычка и средней доли имеют
склонность завернуться кзади, в задний кост­
но-диафрагмальный синус; поэтому их следует
фиксировать спереди к перикарду. При явном
несоответствии объема остатка легкого объему
плевральной полости рекомендуются френикоалкоголизация, френикоэкзерез. В таких слу­
чаях показано также наложение искусственного
пневмоперитонеума немедленно по оконча­
нии операции.
Лечение в ближайшем послеоперационном
периоде проводится как обычно у торакальных
больных. Предупреждение послеоперацион­
ных осложнений — важнейшее условие про­
филактики послеоперационных рецидивов.
Другое, не менее важное, условие — лечение
в период реабилитации.
Оно, в основном, проводится по той же схеме,
как и в период предоперационной подготовки.
Сопутствующие заболевания редко являются
противопоказанием к операции. Среди них могут
быть, например, болезни сердца, в том числе
приобретенные и врожденные пороки. Опера­
ция на легком противопоказана, как выясни­
лось, только в случаях тяжелого декомпенси­
рованного порока, при котором терапия любы­
ми средствами бесперспективна. Если порок
подлежит хирургическому лечению и показана
резекция легкого по поводу бронхоэктазий,
то возникает вопрос: какую операцию раньше
делать? Вопрос этот решается строго индиви­
дуально. Как свидетельствует опыт, допустимы
и одномоментные вмешательства на сердце
и легком [Колесников И. С., Ермолаев В. Р.,
1969]: У больных, которым предстоит коррек­
ция сердечного порока в условиях экстракорпо­
рального кровообращения, лучше сначала сде­
лать операцию на легком [Колесов А. П., Ку­
тушев Ф. X., 1963].
У больных бронхоэктазиями с тяжелой и
очень тяжелой формой течения решить вопрос
о противопоказаниях к операции нелегко.
С одной стороны, это больные, которым ника­
кое другое лечение не поможет, а с другой сто­
роны, риск операции слишком велик; к тому
же операция у такого рода пациентов в боль­
шинстве не облегчает их страдания. Нефропа­
тия и амилоидоз как осложнения течения брон­
хоэктазий рассматривать в качестве абсолют­
ных противопоказаний нельзя, так как в на­
чальных фазах и нефропатия, и даже амилои­
доз, по-видимому, обратимы. Главным противо­
показанием является такое течение бронхоэкта­
зий, при котором имеют место диффузные
поражения легкого в виде пневмосклероза,
эмфиземы, органической формы легочной ги­
пертензии («легочного сердца»). При этом надо
ориентироваться на показатели внешнего ды­
хания и данные измерения давления в малом
круге. Снижение дыхательных объемов (ЖЕЛ)
ниже 50 % от должных величин со стойким
повышением давления в легочной артерии (вы­
ше 25 мм рт. ст.) говорит о том, что риск плани­
руемой операции превышает возлагаемые на нее
надежды.
Наличие двусторонних бронхоэктазий уже
само по себе настораживает. Однако, значитель­
ная часть больных с такой формой заболева­
ния могут быть успешно оперированы. К этой
категории относятся больные бронхоэктазиями,
поражающими лишь нижние отделы обоих лег­
ких, а также больные выраженными и распро­
страненными бронхоэктазиями с одной стороны
и незначительными и ограниченными — с дру­
гой. В первом варианте операция может быть
сделана сначала на одной стороне, а потом, по
выздоровлении, через несколько месяцев,— на
другой (одномоментные двусторонние операции
сейчас уже не практикуются). Бывает так, что
после операции на одной стороне (с большим
поражением) больные чувствуют себя настолько
хорошо, что вопрос о повторном вмешательстве
уже не возникает. Во втором варианте допустимы
так называемые паллиативные вмешатель­
ства — резекции легкого только на стороне
наибольшего поражения. Такая операция за­
ведомо не излечит больного, но может значи­
тельно облегчить его состояние. Принято счи­
тать, что допустимым объемом "резекции при
таких двусторонних операциях является резек­
ция не более 11 —13 сегментов легких у детей
и не более 8 сегментов у взрослых при усло­
вии сохранения в целости верхних долей.
У больных с противопоказаниями к операции
остается единственный путь облегчения стра­
дания — упорная санирующая терапия.
Глава -L
ПНЕВМОМИКОЗЫ
АКТИНОМИКОЗ
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Актиномикоз — хроническое инфекционное
неконтагиозное заболевание человека и живот­
ных, вызываемое лучистыми грибами.
Актиномицеты устойчивы к различным не­
благоприятным условиям внешней среды —
споры их сохраняются жизнеспособными в те­
чение 15—20 лет, выдерживают высушивание,
прямое воздействие солнечных лучей, нагрева­
ние до 60 °C. Среди огромного количества видов
актиномицетов, распространенных в природе,
лишь немногие патогенны. Вначале была дока­
зана роль актиномицета в развитии заболевания
у крупного рогатого скота, затем у человека
[Israel, 1878].
Различают два вида патогенных актиноми­
цетов: аэробный (тип Бострема, имеющий длин­
ный разветвленный мицелий, легко образую­
щий споры) и анаэробный (тип Вольф — Израеля, состоящий из палочек со слабым ветвле­
нием, способный образовывать друзы). Наибо­
лее патогенной является анаэробная форма,
приспособившаяся к паразитированию в орга­
низме. Аэробная форма обычно бывает сапро­
фитной. Возможен переход одной формы в дру­
гую, а у больных актиномикозом чаще всего
выделяют обе формы гриба.
Экзогенная теория заражения утратила к на­
стоящему времени доминирующее признание.
В развитии актиномикоза у человека основное
значение придается эндогенному способу зара­
жения, так как патогенные штаммы возбу­
дителя часто обнаруживаются у здоровых людей
в полости рта, желудочно-кишечном тракте,
верхних дыхательных путях и т. д. Инкубаци­
онный период актиномикоза точно не установ­
лен. Экспериментальные исследования и отдель­
ные клинические наблюдения показывают, что
он колеблется в очень широких пределах — от
1—3 нед до нескольких лет.
Внедрение актиномицета в ткани и развитие
типичного патологического процесса возмож­
ны лишь при травме, в том числе и в определен­
ных условиях. Твердо установлена роль неспе­
цифической микрофлоры, которая, вызывая
нагноительный процесс, как бы создает «почву»
для развития специфического процесса. Изредка
возможно развитие актиномикоза и без уча­
стия неспецифической микрофлоры. Несом­
ненно также, что течение заболевания и харак­
тер патологических изменений определяются,
наряду с биологическими свойствами возбуди­
теля, местными и общими защитными реакция­
ми организма.
Актиномикозом могут поражаться почти все
органы и ткани. Поражение легких встречается
в 15—33 % по отношению ко всем формам
актиномикоза. Обычно патологический про­
цесс в легких является вторичным вследствие
распространения его через клетчатку средосте­
ния при первичной локализации на шее в забрю­
шинном пространстве, через диафрагму из
брюшной полости, а также гематогенным или
лимфогенным путем, причем очаги первичного
поражения часто остаются скрытыми и не вы­
являются при клиническом, а иногда даже и
патологоанатомическом исследовании.
Характерной особенностью актиномикоза
является способность гриба поражать прежде
всего соединительную ткань. Развивающиеся
при этом изменения имеют много общего с теми,
которые наблюдаются при туберкулезе, что рас­
сматривается как одно из доказательств био­
логической близости возбудителей этих забо­
леваний. Однако, в отличие от туберкулеза,
при актиномикозе более выражена тенденция
к распространению патологического процесса на
соседние ткани и органы контактным путем.
На месте внедрения гриба развивается спе­
цифическая гранулема — узелок, состоящий из
грануляционной ткани с круглыми эпителиоид­
ными клетками, участком гнойного расплав­
ления и друзами актиномицета в центре. Пери­
ферические отделы гранулемы образованы руб­
цующейся грануляционной тканью разной сте­
пени зрелости. Для актиномикоза довольно ти­
пично появление в очагах поражения клеток
соединительной ткани, имеющих мелкие липо­
идные включения,— так называемых ксантомных клеток. Если количество клеток становится
значительным, то пораженные ткани приобрета­
ют желтую окраску, что дает возможность оп­
ределить природу заболевания по внешнему
255
виду измененных тканей даже без их гистоло­
гического исследования. Обычно преобладают
пролиферативные процессы, а очаги распада
имеют небольшие размеры. Значительно реже
более выражены экссудативные явления и рас­
пад, что сопровождается образованием крупных
гнойников.
Возможны регрессии и спонтанное исчезно­
вение специфических актиномикотических
гранулем. В таких случаях друзы гриба импрегнируются солями кальция или отделяются
через свищи с гноем, а полость заполняется
рубцовой тканью. Наряду с изменениямй в лег­
ких, имеющими характер специфической брон­
хопневмонии, часто возникает серозно-фибри­
нозный или гнойный плеврит, а позднее обра­
зуются очень прочные, толстые шварты. При
переходе процесса на грудную стенку формиру­
ются множественные свищи и натечные абсцес­
сы. При гематогенном поражении легкого об­
разуется множество мелких очагов, наряду
с наличием крупных узлов и гнойников. Почти
постоянное участие в патологическом процессе
неспецифической инфекции объясняет наблюда­
емый иногда выраженный вторичный распад
пораженных тканей и гангренозный характер
изменений. В зависимости от механизма раз­
вития актиномикоза и особенностей течения
заболевания следует различать: 1) стадию акти­
номикотического бронхита, 2) начальную фор­
му легочного или легочно-плеврального актино­
микоза, 3) распространенную, инфильтратив­
но-пневмоническую форму и, наконец, 4) фор­
му, протекающую с метастазами в другие орга­
ны и ткани.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
И ДИАГНОСТИКА
Бронхиальная
форма
легочного
актиномикоза, или, как ее иногда называют,
поверхностный актиномикоз, рассматривается
и как самостоятельная форма, и как стадия в
развитии заболевания.
Клинические и рентгенологические симпто­
мы в таких случаях не отличаются от обычного
бронхита. Есть указания, что при этом отмеча­
ется наклонность к кровохарканьям и разви­
тию воспалительного стеноза бронхов. Диагноз
устанавливается лишь на основании длительного
многократного обнаружения патогенных грибов
в мокроте.
Начальная форма легочного актино­
микоза крайне редко является следствием аэро­
генного заражения. При этом обычно в легком
выявляется образование, напоминающее по
рентгенологической картине опухоль легкого.
Чаще всего начальная форма развивается вслед­
ствие распространения процесса из брюшной
полости или забрюшинной клетчатки. Заболе­
вание начинается постепенно. Появляются
общее недомогание, субфебрильная темпера­
тура тела, боли в пораженной половине грудной
клетки, постепенно разрастающие и достигаю­
щие значительной интенсивности. При рентге­
нологическом исследовании выявляется обли­
терация реберно-диафрагмального синуса.
Обычно в это время заболевание расценивается
как плеврит или туберкулез. Картина стано­
вится более ясной при появлении воспалитель­
ного инфильтрата в мягких тканях грудной
стенки, в особенности после формирования
свищей. Иногда диагноз облегчает обнаруже­
ние патогенных форм гриба в пунктате из плев­
ральной полости.
Клинические и рентгенологические проявле­
ния распространенной
инфиль­
тративно-пневмонической
форм ы легочного/ актиномикоза во многом опре­
деляются сопутствующей неспецифической
инфекцией. Заболевание начинается обычно
постепенно, с появлением общего недомогания,
похудания, субфебрильной температуры тела,
болями в грудной клетке. При распростране­
нии процесса на париетальную плевру боли
становятся особенно интенсивными. При рент­
генологическом исследовании выявляется более
или менее распространенный инфильтрат в лег­
ком, локализация которого в известной мере
позволяет судить о первичной локализации
очага, из которого процесс распространился
на легкое.
В ряде случаев актиномикоз с самого начала
протекает по типу хронической интерстици­
альной пневмонии. Наступают резкое выражен­
ный склероз легочной паренхимы и деформа­
ция бронхиального дерева, развиваются вто­
ричные бронхоэктазии, не достигающие, однако,
очень значительной степени.
Такие больные предъявляют жалобы на ка­
шель с небольшим количеством мокроты и час­
тым кровохарканьем, иногда бывают легочные
кровотечения.
При рентгенологическом исследовании опре­
деляется грубосетчатый рисунок легочной стро­
мы, на фоне которого могут выявляться мно­
жественные мелкие очаги деструкции, окру­
женные зоной инфильтрации. Довольно типич­
ны плевродиафрагмальные сращения в случаях
вторичного поражения трансдиафрагмальным
путем или парамедиастинальные шварты при
распространении процесса из средостения.
В случаях аэрогенного заражения поражаются
периферические отделы легкого.
При преобладании экссудативного процесса
с распадом ткани и образованием гнойника
в легком клиническая и рентгенологическая
картина не отличается от обычного абсцесса
256
легкого, и лишь микологические исследования
мокроты позволяют распознать природу забо­
левания в ранние сроки. И в этих случаях нель­
зя исключить, что актиномицет является, либо
вторичной инфекцией, осложнившей обычный
абсцесс, либо сапрофитом, не оказывающим
влияния на течение процесса.
Поражение легких специфическим процес­
сом может быть вторичным, когда наиболее
выражены клинико-рентгенологические про­
явления актиномикоза органов средостения
(медиастинальной клетчатки, перикарда, пище­
вода) . В ряде случаев на первый план выступают
признаки сдавления органов средостения. В этих
случаях при рентгенологическом исследовании
обнаруживаются расширение тени средостения
и инфильтративные изменения в легких. Диаг­
ноз облегчается при выявлении очага первич­
ного поражения на лице, шее или в брюшной
полости, а также при наличии типичных сви­
щей.
Актиномикоз легких может быть как вторич­
но-метастатического характера, так и сопровож­
даться гематогенным и лимфогенным метаста­
зированием в другие органы и ткани. Метастастатические поражения легких при актиноми­
козе характеризуются инкапсуляцией, четкой
очерченностью очага, изредка с мелкопятни­
стым обсеменением обоих легких. Нередко
наблюдается перифокальное воспаление вокруг
гематогенно развившихся очагов.
Обычно поражение легких сопровождается
выраженным воспалительным процессом в плев­
ральной полости с образованием грубых шварт.
Тем не менее наблюдается прорыв актино­
микотического очага в свободную плевраль­
ную полость с развитием типичного пневмото­
ракса или эмпиемы.
При далеко зашедшем процессе, распростра­
нившемся на грудную стенку, диагностика об­
легчается характерными рентгенологическими
симптомами поражения скелета (декальцина­
ция и остеопороз, иногда изменения позвоноч­
ника, для которых характерно отсутствие сек­
вестров и деформации тел позвонков). Патоло­
гический процесс в этих случаях никогда не
распространяется на межпозвоночные диски.
Следует отметить, что распознавание актино­
микоза на ранних стадиях развития заболева­
ния представляет большие трудности. Диаг­
ноз обычно ставится методом исключения и до
подтверждения специальными исследованиями
остается лишь предположительным.
Наибольшие трудности возникают в диффе­
ренциальной диагностике с туберкулезом лег­
ких, опухолями и неспецифическим нагноительными процессами. Однако, в отличие от туберку­
леза легких, в мокроте при актиномикозе почти
никогда не бывает эластических волокон.
17 Зак. 0517
Не следует переоценивать данные лаборатор­
ного исследования. Отсутствие в мокроте выяв­
ляемых при бактериоскопии друз и мицелия
гриба, а также отрицательные результаты по­
севов могут быть обусловлены дегенеративными
изменениями мицелия гриба в тканях. Наряду
с этим грибковая флора может обнаруживаться
вследствие попадания ее из полости рта. Кроме
того, в ряде случаев она может находиться
в очагах нагноения как сапрофит. Наконец,
лабораторные данные следует считать доста­
точно достоверными лишь в тех случаях, когда
они получены в учреждениях, имеющих спе­
циальную квалификацию и опыт в проведении
таких исследований.
Диагностика облегчается нахождением в мок­
роте типичных для актиномикоза ксантомных
клеток. Получение анаэробной культуры при
посеве, в особенности если в ней выражены яв­
ления лизиса,— весьма ценное доказательство
ее патогенной природы. Выделение же нелизирующихся спороносных анаэробных культур
имеет диагностическую ценность лишь при мно­
гократном их обнаружении.
В ряде случаев правильный диагноз может
быть поставлен на основании данных, получен­
ных при пункционной биопсии легкого.
ЛЕЧЕНИЕ
До недавнего времени прогноз при легочном
актиномикозе был крайне неблагоприятным
и смертность достигала 90—95 %. В настоящее
время большинство больных актиномикозом
легких стойко излечиваются даже при тяжелых,
запущенных формах. Успехи в лечении акти­
номикоза достигнуты благодаря применению
антибиотиков и сульфаниламидных препара­
тов. Наилучшие результаты достигаются при
инфильтративных, очаговых или диссеминиро­
ванных поражениях. Лечебный эффект объяс­
няется как подавлением неспецифической гной­
ной микрофлоры, так и прямым воздействием
антибиотиков на актиномицеты.
Учитывая биологическую близость актиномицета к микобактериям туберкулеза, рекомен­
дуют применять специфическую антибактери­
альную терапию фтивазидом в течение 1—3 мес,
лучше в комплексе с антибиотиками. Иммуно­
терапия при легочном актиномикозе, прово­
димая актинолизатом, малоэффективна. Актинолизотерапию целесообразно применять и пос­
ле клинического излечения, чтобы предупре­
дить рецидив заболевания.
Независимо от метода лечения огромное
значение имеет общеукрепляющая терапия —
полноценное, богатое витаминами питание.
Велика роль систематических переливаний крови
или эритроцитной массы, позволяющих ликвиди­
257
ровать анемию и истощение, стимулировать
иммунобиологические защитные реакции.
Оперативные методы лечения этого заболе­
вания сейчас занимают скромное место. Из­
редка приходится прибегать к вскрытию и дре­
нированию изолированных гнойников, в частно­
сти при актиномикозе, осложненном эмпиемой
плевры или пиопневмотораксом. При ограничен­
ных поражениях операция обычно производится
в случаях, когда ошибочно диагностируются
хронический нагноительный процесс или опу­
холь легкого, а природа патологического про­
цесса выясняется после изучения препарата.
У таких больных после операции необходима
энергичная антибактериальная терапия для
профилактики рецидива.
КАНДИДОЗ
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Кандидоз легких вызывается дрожжеподоб­
ными грибами рода Candida. В виде первичного
заболевания он встречается, как правило, при
различных иммунодефицитных состояниях,
а также на фоне лечения больных антибиоти­
ками, глюкокортикостероидами, антиметабо­
литами и цитостатиками. Однако в большинстве
случаев кандидоз легких является вторичным
и возникает как осложнение имеющегося пато­
логического процесса в этом органе. В том и дру­
гом случае кандидоз легких может протекать
остро и носить затяжной характер.
Первичный кандидоз легких локализуется
в нижних и средней долях легких, однако про­
цесс может распространяться и на верхние
доли. При остром кандидозе легких, который
развивается вслед за поражением бронхов
и распространением процесса по протяжению
или гематогенно, в патологических очагах, в
альвеолах образуется лейкоцитарный экссудат
с примесью фибрина или наблюдаются фибри­
нозно-некротические изменения.
Морфологические изменения при затяжном
кандидозе разделяют на три стадии: при I ста­
дии в центре пораженного участка легкого об­
наруживают лейкоциты, окруженные эпителио­
идными, плазматическими и единичными ги­
гантскими клетками; для II стадии характерно
разрастание грануляционной ткани в очагах
поражения; в III стадии превалируют фиброз­
ные изменения.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
Клинически кандидоз легких может проте­
кать в легкой и тяжелой формах. Тяжесть те­
чения зависит от распространенности деструк­
тивных изменений в легких. В начальной стадии
болезни и в легко протекающих случаях канди­
доз легких напоминает бронхит (бронхомикоз).
Отмечаются сухие хрипы, мучительный кашель
со скудной, сероватого цвета мокротой, иногда
имеющей запах дрожжей. Больные жалуются
на слабость, недомогание, понижение рабо­
тоспособности, головную боль. Температура
тела, как правило, нормальная. Однако в ряде
случаев заболевание начинается внезапно с
подъема температуры до высоких цифр. Затем
появляется кашель, обычно сухой, «царапаю­
щий», сопровождающийся болями в груди. Рент­
генологически при этом определяется неболь­
шое усиление легочного рисунка.
В поздние стадии и при тяжелом течении кан­
дидоз легких проявляется очаговой или лобар­
ной пневмонией. Общее состояние больных
обычно тяжелое, наблюдается высокая или
умеренно повышенная температура тела, почти
всегда постоянный кашель, сопровождающийся
отделением обильной мокроты, кровохарканьем
и часто болями в груди. В затяжных случаях
кандидоза пневмония осложняется плевритом
с соответствующей симптоматикой.
Рентгенография при затяжном течении про­
цесса выявляет неясную пятнистость, неболь­
шие пневмонические очаги и ателектазы. Более
крупные очаги локализуются, как правило,
в нижних долях легких. Нередко при кандидопневмОнии рентгенологически определяются
милиарные затенения («снеговые хлопья»),
тяжистые тени от очагов затенения к бронхо­
легочным (корневым) лимфатическим узлам,
нередки случаи распада инфильтратов с обра­
зованием единичных крупных или множествен­
ных мелких полостей. В этом случае рентгено­
логическая картина напоминает кавернозный
туберкулез легких. Однако для нее характерны
быстрое возникновение тонкостенных полостей,
увеличивающихся в размерах, и сравнительно
быстрая их регрессия вплоть до полного исчез­
новения под влиянием противомикотической
терапии. Рентгенологические данные о распаде
легочной ткани, связанные с действием самого
гриба, должны всегда подкрепляться исследо­
ванием всего «микробного пейзажа», так как
распад может быть обусловлен другими микро­
организмами, ассоциирующимися с грибом.
Изменение картины крови при кандидозе
может отсутствовать. В тяжелых случаях вы­
являются лейкопения, базофилия, эозинофи­
лия, нейтрофилез, лимфопения с моноцитозом,
увеличение СОЭ.
При вторичном кандидозе легких, несмотря
на терапию основного заболевания, измене­
ния в легких прогрессируют, температура тела
становится гектической, возникает озноб, ноч­
ные поты, общее состояние больных резко
ухудшается.
258
Для постановки диагноза кандидоза недо­
статочно одних клинических симптомов. Не­
обходимы микроскопические, культуральные и
серологические исследования.
ЛЕЧЕНИЕ
Лечение кандидоза легких проводят амфоглюкамином, микогептином, нистатином. При
тяжелом течении применяют натриевую соль
леворина и амфоглюкамина в виде ингаляций.
В ряде случаев применяется хирургическое ле­
чение.
АСПЕРГИЛЛЕЗ
Аспергиллез легких — наиболее частая вис­
церальная форма аспергиллеза. Заражение про­
исходит при вдыхании спор грибка. Первичный
аспергиллез легких встречается редко, вторич­
ный развивается у ослабленных больных на фоне
других легочных болезней (туберкулез и рак
легкого, бронхоэктазии и т. д.), а также при
длительном лечении антибиотиками, глюкокор­
тикостероидами, цитостатиками.
Первичный острый бронхолегочный аспергил­
лез может протекать по типу тяжелой пневмо­
нии, бронхита. На легочную ткань процесс пере­
ходит вследствие радиарного роста концевых
отделов мицелия гриба, который проникает
через стенки бронхов, межальвеолярные пере­
городки, стенки капилляров, артерий и вен. В
участках секвестрации аспергиллезной пневмо­
нии иногда формируется аспергиллома лег­
кого, которая представляет собой шарообраз­
ное распространение гриба (Fungus boll) с по­
следующим образованием полости. Внедрение
мицелия в стенку полости, сопровождающееся
фиброзно-гнойной экссудацией, обозначается
как инвазивная аспергиллома.
В начале заболевания наблюдаются сухой,
мучительный кашель, одышка, озноб и лихо­
радка. В дальнейшем присоединяется крово­
харканье, нарастают слабость, астения, анорек­
сия. Над поверхностью легких выслушиваются
множественные разнокалиберные хрипы. Рент­
генологически определяются участки инфильтра­
ции легочной ткани, склонные к распаду с обра­
зованием полостей, увеличиваются бронхоле­
гочные лимфатические узлы.
При отсутствии лечения заболевание прини­
мает хроническое течение с ремиссиями и обо­
стрениями. Постепенно увеличивается количе­
ство мокроты, которая становится кровянисто­
гнойной. Периоды обострения сопровождают­
ся гектической лихорадкой, ознобом, ночными
потами, похуданием. Перкуторно определяют
коробочный звук и его притупление при суб­
17 *
плевральном расположении очага поражения,
аускультативно — сухие и влажные хрипы.
При вторичном аспергиллезе легких довольно
часто (в 70 % случаев) развивается аспергил­
лома, которая формируется в санированных
туберкулезных кавернах, бронхоэктазиях, по­
лостях, образовавшихся после абсцессов, ганг­
рены легких, вскрывшейся эхинококковой кисты.
Аспергиллома представляет собой полость,
сообщающуюся с просветом бронха и содержа­
щую плотные сплетения нитей гриба в виде
тяжей серого цвета и грануляционную ткань,
легко кровоточащую при перемещении.
Заболевание проявляется постепенным на­
растанием слабости, понижением аппетита, не­
правильной лихорадкой, ознобом и повышенной
потливостью. Характерный признак — при­
ступообразный кашель с отделением обильной
мокроты без запаха, содержащей зеленовато­
серые хлопья (скопления мицелия гриба) и про­
жилки крови. Могут возникать повторное кро­
вохарканье, иногда значительное, боли в груди,
одышка. При отсутствии бронхолегочного
дренажа характерные симптомы не наблюда­
ются.
Физикальное обследование больного выявля­
ет признаки имеющейся в легком полости.
Рентгенологически вначале определяется
утолщение стенок полости, затем секвестро­
подобное затенение, окруженное серповид­
ным просветлением («нимб», «ореол», «полу­
месяц»), которое может смещаться при пере­
мещении тела больного (симптом «погремуш­
ки») или всплывать при заполнении полости
рентгенконтрастным веществом (симптом «по­
плавка») .
Аспергиллез легких может протекать с по­
ражением плевры. Иногда разросшийся мице­
лий гриба выполняет плевральную полость.
В других случаях развивается выпотной плеврит.
При постоянном вдыхании спор гриба может
наблюдаться аспергиллезный аллергический
альвеолит.
Для лечения аспергиллеза легких применяют
амфотерицин В, препараты йода в постоянно
возрастающих дозах, нистатин, леворин в виде
ингаляций.
При локализованных формах бронхолегочного
аспергиллеза общепризнанным является опера­
тивное удаление очагов деструкции в виде кли­
новидной резекции, сегментэктомий, лобэктомий
или пневмонэктомии в случаях обширных пора­
жений. Непосредственные результаты таких
вмешательств многими авторами оцениваются
как хорошие, несмотря на довольно частые
осложнения в виде бронхиальных свищей, эмпие­
мы плевры, кровотечений. Что касается отдален­
ных результатов, то данные литературы очень
немногочисленны. А. X. Керимов и А. Ф. Мали­
259
новский (1985) обследовали 17 больных в сроки
от 1 года до 10 лет после оперативного вмеша­
тельства по поводу первичного аспергиллезного
поражения легких. У всех обследованных в ука­
занные сроки были обнаружены различные
осложнения или рецидивы заболевания: аспергиллезная мицетома с наличием бронхиального
свища в области бывшей операции (3), хрони­
ческий бронхит (10), поликистоз на фоне диф­
фузных изменений оставшейся части легкого
(3). Один больной умер от легочного кровоте­
чения через 6 лет после операции.
Авторы отмечают, что у 10 больных в мокроте
и смывах из просвета бронхов обнаружены
Aspergillus fumigatus, а у 6 — ассоциации Asper­
gillus niger, Mucor и Candida albicans. Следова­
тельно, оперативное вмешательство позволило
устранить очаги деструкции, но не предотвратило
обсеменения грибами оставшихся участков лег­
кого. Поэтому больные, подвергающиеся опе­
ративному лечению по поводу аспергиллезных
поражений легких, в дальнейшем должны не
менее 3 лет находиться под диспансерным
наблюдением, включающим повторные клинико­
рентгенологические и микологические обследо­
вания, а также консервативную терапию антифунгальными препаратами.
которая может быть удалена при резекции ча­
сти или доли легкого.
Макроскопически гистоплазмома представ­
ляет собой шаровидный плотный очаг, обычно
расположенный под висцеральной плеврой.
Размеры этого опухолевидного очага варьиру­
ют от 0,5 до 3,5 см в диаметре, плотной, упру­
гой консистенции. На разрезе ткань очага сло­
истая, она четко отграничена от почти неизмен­
ной легочной паренхимы. Центральная часть
гистоплазмомы мягковатая, зернистая, иногда
с наличием творожистых масс.
Микроскопически гистоплазмома по пери­
ферии окружена плотной коллагеновой тканью,
в которой обнаруживаются отдельные фибро­
циты. Ближе к центру располагается тонкий
слой из эпителоидных клеток. Внутри него
имеется широкая капсула из коллагеновых воло­
кон, которая окружает некротические массы
с отложением солей извести. В некоторых гистоплазмомах среди казеозных масс выявляется
сохранившийся альвеолярный каркас. Гисто­
логически диагностика гистоплазмомы бывает
достоверной только при обнаружении дрожже­
вых клеток гриба в центральной части очага.
Первичный гистоплазмозный комплекс яв­
ляется источником лимфогематогенной диссеминации.
ГИСТОПЛАЗМОЗ
ЛЕЧЕНИЕ
Г истоплазмоз
(ретикулоэндотелиальный
цитоплазмоз, болезнь Дарлинга) — глубокий
микоз, протекающий в виде ограниченного про­
цесса или генерализованного заболевания.
Первично поражаются клетки ретикулоэндо­
телиальной системы органов и тканей.
Гистоплазмоз легких может быть первичным,
связанным с вдыханием спор гриба, и вторич­
ным — в результате лимфогематогенного рас­
пространения гриба из других органов.
Исследование резецированных легких позво­
лило изучить динамику ранних гистопатологи­
ческих изменений при гистоплазмозе. Очаги
поражения в легких чаще бывают двусторон­
ними, расположенными в нижних долях.
В настоящее время выделяют особую фор­
му гистоплазмоза легких — гистоплазмому,
Этиотропная терапия гистоплазмоза легких
состоит в применении сульфаниламидных пре­
паратов (норсульфазол 4—6 г в сутки), нистати­
на (4—6 млн ЕД в сутки), амфотерицина Б
(1,0—1,5 мг на 1 кг массы тела в сутки) и его
дериватов (амфоглюкамин по 200—500 тыс. ЕД
2 раза в сутки, микогепин — по 280 мг 2 раза
в сутки). В качестве общеукрепляющей терапии
показаны гемотрансфузии, введение плазмы кро­
ви, донорског.о гамма-глобулина. Оперативное
лечение может оказаться необходимым при
непреодолимых трудностях этиологического
диагноза в случаях гистоплазмомы, рентгено­
логическая картина при которой трудноотличима
от таковой при раке легкого, а также при стойком
или рецидивирующем синдроме средней доли,
вызванным гистоплазмозным лимфаденитом.
Глава ±
ПАРАЗИТАРНЫЕ
ЗАБОЛЕВАНИЯ ЛЕГКИХ
ЭХИНОККОКОЗ ЛЕГКИХ
Однокамерный или гидатидозный эхино­
кокк — объект хирургического лечения при
развитии его в легких человека — является
личиночной стадией развития червя Echinococcus
granulosus. Поражение им внутренних органов
человека носит название эхинококкоза.
Эхинококкоз относят к одной из тяжелей­
ших форм антропозоонозов. Он распростра­
нен в Южной Америке, Австралии, Турции, Ал­
бании, а в нашей стране — в республиках с пре­
имущественно сухим и жарким климатом, где
интенсивно развито скотоводство: в Молдавии,
Азербайджане, Киргизии и др. [Цыбырнэ К. А.
и др., 1979; Манафов С. С., 1974; Ахунбаева Н. И.,
1972].
Легкие стоят на втором месте после печени
по частоте поражения эхинококком, и легоч­
ный эхинококкоз встречается от 6 до 35 % по
отношению к другим локализациям этого пара­
зита. Наряду с множественным поражением
эхинококковыми пузырями одного легкого,
встречаются и двусторонние формы заболева­
ния, а также с одновременным поражением
других органов, чаще всего — печени [Вахи­
дов В. В., Исламбеков Э. С., 1972].
Паразит существует в двух формах — лен­
точной и личиночной. В ленточной форме он
обитает в кишечнике собак, волков, шакалов,
лисиц и других хищных млекопитающих, являю­
щихся для глиста окончательным хозяином.
Личиночная (гидатидозная) форма гельминта
паразитирует во внутренних органах и тканях
более чем у 60 видов млекопитающих (круп­
ный и мелкий рогатый скот, свиньи, олени,
обезьяны и др.), а также в организме человека,
являющегося для него промежуточным хозяи­
ном. Известны два цикла развития эхинококка.
Полный жизненный цикл совершается со сме­
ной двух хозяев: промежуточного и оконча­
тельного.
Неполный (бесполый) цикл развития пара­
зита происходит только в органах промежуточ­
ного хозяина в результате загрязнения органов
и тканей носителя зародышевыми элементами
эхинококка.
Пути загрязнения внешней среды — с кало­
выми массами больного животного. Обладая
способностью к самостоятельному передвиже­
нию, зародыш — онкосфера — забирается на
стебельки растений или располагается в шерсти
животного и благодаря выделяемому клейкому
веществу прочно прикрепляется. Заражение
травоядных животных происходит на пастби­
щах.
Проникновение онкосфер в организм чело­
века возможно двумя основными путями: при
употреблении в пищу зараженных яйцами пара­
зита овощей, фруктов, воды или путем переноса
яиц паразита с шерсти зараженных эхинокок­
ком собак при несоблюдении правил личной
гигиены.
Доказана также возможность непосредствен­
ного попадания онкосфер в дыхательные пути
с вдыхаемой зараженной пылью [Потапов В. Г.,
1938; Ганжулевич Т. Ф., 1947]. При благопри­
ятных условиях — достаточной влаге и опти­
мальной температуре — в яйцах паразита про­
исходит рост зародыша. Это создает повышен­
ное внутри скорлупы давление. Она разруша­
ется, и шестикрючный зародыш выходит наружу
[Скрипниченко Д. Ф., Цыбырнэ К. А., 1959].
Онкосферы, лишенные оболочки, обладают
подвижностью и при помощи трех пар крючьев
проникают в толщу слизистой оболочки верх­
них отделов тонкой кишки. Внедрившись в кро­
веносные капилляры через систему воротной
вены, они проникают в печень, легкие и разно­
сятся по всему организму. Застряв в капилля­
рах органа, онкосферы проникают в окружаю­
щую ткань, где продолжают развитие в форме
гидратидозного эхинококка.
Взрослый, сформировавшийся эхинококковый
пузырь имеет вид кисты, окруженной фиброз­
ной капсулой (капсула носителя), которая об­
разуется в результате постоянного давления
растущим паразитом и реактивных изменений
в окружающих тканях легкого. Оболочка са­
мого паразита состоит из двух слоев — внут­
реннего, или зародышевого (герминативного),
и наружного, или хитинового (кутикулярного);
фиброзная капсула не имеет прочной связи
с хитиновой оболочкой. От последней она отде­
261
лена щелевидным перипаразитарным простран­
ством, заполненным тканевой жидкостью. Через
фиброзную оболочку происходит обмен веществ
между организмом человека и паразитом. Рост
эхинококка связан с герминативной оболочкой.
Ее клетки имеют беспредельную способность
к размножению и образуют выводковые капсу­
лы и сколексы. Последние, попав в кровенос­
ные капилляры (при нарушении целости мате­
ринской кисты), свободно проходят через их
стенки и, внедрившись в окружающие ткани,
развиваются в виде пузыря. Этот путь распро­
странения паразита называют вторичным, или
метастатическим.
Полость эхинококковой кисты наполнена
питательной жидкостью, в которой плавают до­
черние пузыри, выводковые капсулы и сколексы.
Встречаются и бесполые формы эхинококковых
кист, не содержащие зародышевых элементов.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
Симптоматика и течение заболевания при
эхинококкозе зависят от стадии развития, из­
менений в паразитарной кисте и характера рас­
стройств в легком и организме больного. В кли­
нической картине неосложненного эхинококко­
за легкого нет ни единого патогномоничного
симптома, основываясь на котором можно было
бы установить достоверный диагноз [Манафов С. С., 1974]. Вопрос о сроках появления
основных клинических признаков для диагно­
стики болезни до последнего времени остается
не уточненным. По мнению В. С. Гамова (1960),
Н. И. Ахунбаевой (1972), своеобразием пато­
генеза заболевания при развитии эхинококка
в легком является то, что рост паразита про­
исходит здесь гораздо быстрее, чем в печени
и других органах. Это обусловлено более высо­
кой податливостью и эластичностью паренхимы
легкого, вследствие чего при своем росте эхино­
кокковый пузырь встречает относительно не­
большое сопротивление.
Изучение патологических изменений в орга­
низме больных эхинококкозом легких, своеобра­
зия клинического течения и особенностей хирур­
гического лечения позволяет выделять 4 ста­
дии заболевания [Ахунбаева Н. И., 1972]:
1. Латентная стадия, которая может
продолжаться до 5 лет. В этой стадии развития
паразит не причиняет заметных расстройств,
которые могли бы проявляться какими-либо
клиническими признаками, свидетельствующими
о наличии эхинококкового паразита в легком.
2. Стадия начала клинических
проявлений. Клинические признаки воз­
никают как следствие прогрессирующего роста
эхинококковой кисты, механического давления
ее на ткань легкого: альвеолы, бронхи, висцераль­
ную плевру. Чаще всего одним из первых симп­
томов бывают боли в груди различной интен­
сивности и характера, напоминающие межре­
берную невралгию или вызывающие чувство
необъяснимой «тяжести в груди». Спустя не­
продолжительное время к этим ощущениям при­
соединяется кашель, чаще всего сухой или с
небольшим количеством мокроты слизистого
вида. Деструкция тканей в зоне формирова­
ния фиброзной капсулы паразита может сопро­
вождаться нарушением целости капилляров,
мелких кровеносных сосудов. Тогда в отделяе­
мой мокроте можно отметить прожилки изме­
ненной и свежей крови. В этот период развития
болезни возможно появление общих расстройств
в виде недомогания, слабости, потливости, пе­
риодического повышения температуры тела до
субфебрильных цифр, изредка — аллергиче­
ской крапивницы.
Обследование, проведенное в период началь­
ных клинических проявлений эхинококкоза
легких, может выявить патологические изме­
нения лишь при значительных размерах эхино­
кокковой кисты, обычно при периферическом
ее расположении. При этом в зоне локализа­
ции паразита можно отметить укорочение пер­
куторного звука и ослабленное дыхание, а при
воспалительном процессе в легочной паренхи­
ме — крепитирующие и влажные мелкопузыр­
чатые хрипы. У детей и больных молодого воз­
раста иногда появляется асимметрия — выпя­
чивание отдельных участков грудной стенки.
Межреберные промежутки на стороне пора­
женного легкого несколько сглаживаются, и
эта половина груди отстает в акте дыхания. При
выслушивании над зоной «выпячивания» слы­
шен шум трения плевры. Гораздо реже могут
появиться признаки, характеризующие смеще­
ние органов средостения в здоровую сторону.
3. Стадия
развитых
клиниче­
ских проявлений. Этот период харак­
теризуется дальнейшим нарастанием клиниче­
ских расстройств: усилением болей в груди,
более постоянным кашлем, часто с отделением
крови. Возникает и прогрессивно нарастает
одышка, более выраженными становятся гемо­
динамические расстройства, обусловленные
сдавлением и смещением органов средостения.
Многое определяется при этом локализацией
паразита в том или ином участке легкого.
4. Стадия
возникновения
ос­
ложнений. Возникновение различных ос­
ложнений, к которым почти неотвратимо при­
водят прогрессирующее развитие эхинококко­
вой кисты в легком, характеризуется тяже­
лым течением заболевания и наиболее выра­
женными его клиническими проявлениями.
Наиболее частыми из этих осложнений яв­
ляются прорыв и опорожнение эхинококковой
262
кисты в бронх. Как правило, в бронх прорыва­
ются центрально расположенные кисты и зна­
чительно реже — из периферических отделов
легкого. Прорыв эхинококковой кисты сопро­
вождается отхождением с кашлем значитель­
ного количества прозрачной жидкости. В ней
могут содержаться элементы хитиновой обо­
лочки паразита, иногда — дочерние кисты. Если
прорыву предшествовало нагноение кисты, то
отделяемая жидкость может быть гнойной,
зловонной. Нарушение фиброзной капсулы при­
водит к появлению в жидкости небольшого ко­
личества крови.
Опорожнение большой эхинококовой кисты,
значительные размеры соустья ее с просветом
бронхиального дерева могут вызвать быстрое
и одномоментное поступление большого коли­
чества жидкости с явлениями тяжелой асфик­
сии. Возможно и постепенное опорожнение в
бронх содержимого эхинококковой кисты через
небольшое отверстие. Тогда это происходит
почти незаметно для больного, лишь увеличи­
вается количество отделяемой мокроты.
У части больных всасывание эхинококковой
жидкости из просвета дыхательных путей со­
провождается появлением аллергических реак­
ций — крапивницы.
С момента сообщения эхинококковой кисты
с просветом дыхательных путей данные, полу­
чаемые при физикальном обследовании боль­
ных, становятся более многочисленными и мно­
гообразными. Это объясняется тем, что про­
рыв эхинококкового пузыря в бронх сопровож­
дается периодом воспаления легкого вокруг
кисты, формированием участков гиповентиля­
ции, иногда — ателектазом сегмента или доли
в результате закрытия дренирующего бронха
кусочком хитиновой оболочки. Кровохарканье
может достигать интенсивности легочного кро­
вотечения [Ахунбаева Н. И., 1972].
Самостоятельное заживление полости в лег­
ком после вскрытия эхинококковой кисты в
бронх и самоизлечение наступают редко. По
данным В. С. Гамова (1960), подобный исход
отмечен не более чем у 1 /5 части больных. Обыч­
но в сформировавшейся полости развивается
нагноительный процесс. Тогда последующее
течение заболевания, клиническая и рентгено­
логическая симптоматика приобретают черты
абсцесса легкого.
При нарушении целости эхинококкового
паразита всегда следует иметь в виду возмож­
ность бронхогенной диссеми нации сколексов с
развитием множественных эхинококковых
пузырей в других отделах легких, а при их про­
никновении в кровеносное русло — выход про­
цесса за пределы грудной полости.
Прорыв в плевральную полость относится
к более редким осложнениям течения эхино­
коккоза легких. Однако клинические прояв­
ления при этом характеризуются значительной
тяжестью. Это обусловлено коллабированием
легкого, нарастающей дыхательной недоста­
точностью, которая при одновременном сооб­
щении кисты с просветом дыхательных путей
нарастает. Тогда появляется симптоматика,
характерная для пневмоторакса, часто — на­
пряженного. Быстрая резорбция эхинококко­
вой жидкости плевральными листками может
привести к тяжелому анафилактическому шоку.
Опорожнение в плевральную полость нагноив­
шейся эхинококковой кисты усугубляет тече­
ние болезни клиническими проявлениями, ха­
рактерными для тяжелого пиопневмоторакса.
В числе нередких осложнений эхинококкоза
легких отмечают гибель паразита, его разло­
жение и нагноение. Процесс нагноения явля­
ется следствием попадания гноеродной инфек­
ции гематогенным или бронхогенным путями
внутрь хитиновой оболочки и вокруг нее. Кли­
ническая картина нагноения отличается отно­
сительной «доброкачественностью», но может
протекать по типу блокированного абсцесса
легкого.
Множественное поражение одного или обоих
легких эхинококковыми кистами наблюдается
в 8—22 % случаев. Большое количество кист
является результатом одновременного инвазирования в легкое значительного количества
онкосфер — первично-множественный эхино­
коккоз.
При развитии в одном или обоих легких боль­
шого количества эхинококковых кист клиниче­
ские проявления заболевания выражены ярче,
а состояние больных бывает тяжелее. Это объ­
ясняется в первую очередь уменьшением дыха­
тельной поверхности легкого, явлениями легоч­
ной гипертензии. Ведущими жалобами таких
больных являются одышка, кашель, различ­
ные проявления гипоксии.
Латентная стадия течения болезни при мно­
жественном эхинококкозе легких имеет более
короткий период. Паразитарные кисты редко
достигают огромных размеров. Прорыв кист
при множественном эхинококкозе происходит
довольно часто, несмотря на небольшие их
размеры. Это объясняется тем, что дыхатель­
ная поверхность легкого резко уменьшается
в результате развития в нем нескольких кист.
Больные вынуждены затрачивать больше уси­
лий для обеспечения нормального газообмена,
делать глубокие вдохи. Это приводит к сдавле­
нию кист и вызывает их прорыв. Возможно,
для этого имеются и другие, более глубокие
изменения взаимосвязи между человеком и па­
разитом.
При обследовании больных множественным
эхинококкозом легких обращает на себя вни­
263
мание то, что данные объективного исследо­
вания у них чаще всего не отражают тех выра­
женных изменений, которые развиваются в лег­
ких. Между тем изучение показателей функ­
ции внешнего дыхания, гемодинамики почти,
во всех случаях множественного эхинококко­
за свидетельствует о значительных наруше­
ниях.
Как показали исследования К. А. Цыбырнэ
и соавт. (1979), до 50 % больных легочным
эхинококкозом имеют одновременное пораже­
ние печени. Естественно, патология этого орга­
на вносит дополнительные черты в клиниче­
ское течение заболевания, что следует учиты­
вать при решении вопросов диагностики рас­
пространенности болезни, выборе лечебной
тактики.
ДИАГНОСТИКА
Своеобразие клинических проявлений эхи­
нококкоза легких, особенно в ранних стадиях
развития заболевания, дает мало патогномонич­
ных симптомов, которые могут быть выявлены
с помощью физикальных приемов обследова­
ния.
Это определяет значение и роль рентгено­
логического исследования для диагностики и
решения вопросов лечебной тактики (рис. 115,
116).
Из специальных методов диагностики эхино­
коккоза легких широкую известность получила
кожная аллергическая проба — реакция Каццони [Cacconii L., 1912]. Она сводится к внут­
рикожному введению на предплечье 0,1—0,2 мл
эхинококковой жидкости, полученной из пара­
зита, выращенного во внутренних органах экспе­
риментального животного. Для контроля в кожу
другого предплечья вводится такое же количе­
ство изотонического раствора натрия хлорида.
Появление красноты на месте введения антиге­
на в период до 6 ч может свидетельствовать
о наличии в организме больного паразита. Ю. А.
Волох (1953, 1959), И. Г. Гурбаналиев (1970)
считают, что с помощью этой пробы правиль­
ный диагноз может быть установлен в 80,5 %
наблюдений. Определенное значение имеет
постановка этой реакции в эозинофильно-ал­
лергическом варианте: с подсчетом числа эози­
нофилов в крови больного до и спустя 24 ч пос­
ле введения антигена. Увеличение их процент­
ного содержания патогномонично для эхино­
коккоза.
Следует иметь в виду, что проба Каццони
может сопровождаться тяжелыми аллергиче­
скими реакциями, а также активизацией про­
цесса с прорывом эхинококкового пузыря в
бронх.
В последние годы стали отдавать предпочте­
ние методам иммунологической диагностики
эхинококкоза — постановке реакции непрямой
микрогемагглютинации. Реакция проводится
между эритроцитарным эхинококковым диагностикумом (очищенным антигеном из эхино­
кокковой жидкости QT овцы) и СЫВ£фОТ£рЙ боЛЬного. Она исключает неблагоприятные ответ­
ные реакции в организме больного и, по мнению
К. А. Цыбырнэ и соавт. (1979), при положи­
тельном результате позволяет поставить точ­
ный диагноз эхинококкоза.
ЛЕЧЕНИЕ
В последние годы проводятся интенсивные
работы в области изыскания препаратов, дей­
ствующих на личиночную форму Echinococcus
granulosus. Появились отдельные сообщения о
возможности консервативного лечения эхино­
коккоза с помощью препарата вермокса.
Однако, по общему признанию, в настоящее
время единственным методом, решающим про­
блему лечения больных эхинококкозом легких
в социальном аспекте, остается хирургический
[Милонов О. Б. и др., 1983].
Оперативный метод лечения легочного эхи­
нококкоза должен применяться возможно рань­
ше, как только установлен диагноз. Лишь абсо­
лютные противопоказания, ■ обусловленные тя­
жестью общего состояния больного при нали­
чии сопутствующих заболеваний, могут быть
причиной отказа от операции.
Оптимальной операцией, к выполнению ко­
торой следует стремиться во всех случаях, яв­
ляется удаление паразита без вскрытия пузыря.
Такое удаление, вылущивание из фиброзной
капсулы паразита в хитиновой оболочке, не на­
рушая ее целости, называют «идеальной эхинококкэктомией».
Легочная ткань надсекается в месте наиболее
поверхностного залегания кисты, и пузырь тупо
вылущивается. Как правило, он легко отслаи­
вается от фиброзной капсулы, для чего удобно
использовать тупую ложку (чайную или столо­
вую — в зависимости от размеров паразита),
а также периодически создавать повышенное
давление газовой смеси в замкнутой системе
«наркозный аппарат — легкие». После удале­
ния пузыря полость дважды обрабатывается
5 % раствором формалина в глицерине, дваж­
ды 96 % этанолом и промывается антисептиче­
ским раствором. Это делается для того, чтобы
уничтожить сколексы, которые могут находить­
ся в фиброзной капсуле или попасть в нее из
небольших надрывов пузыря, оставшихся не­
замеченными при его выделении.
Нередко при крупных эхинококковых пузы­
рях удалить их без опорожнения не представ­
ляется возможным, так как имеется реальная
опасность разрыва капсулы при выделении.
264
б
Рис. 116. Множественные эхинококковые кисты легких.
Рис. 115. Эхинококковая киста легкого.
а прямая рентгенограмма; б
вление стенок кисты.
боковая рент1енограмма. Видно обызвест­
Тогда осуществляется пункция пузыря тол­
стой иглой с краником и аспирация содержи­
мого в замкнутую систему. При этом следует
всячески предупредить попадание жидкости из
пузыря в плевральную полость, что может при­
вести к развитию тяжелого анафилактического
шока вплоть до смертельного исхода и, вслед­
ствие попадания сколексов, к возникновению
эхинококка плевры. Для предупреждения попа­
а
прямая рентгенограмма; о
ооковая рентгенограмма.
дания жидкости из пузыря в рану перед пункцией
следует дополнительно ограничить этот участок
легкого салфетками (сухими или смоченными
гипертоническим раствором или раствором ка­
кого-либо антисептика). После завершения
максимально возможного освобождения кисты
паразита от содержимого в нее вводят
5 % раствор формалина в глицерине на срок
не менее 5 мин — достаточный для уничтоже­
265
ния оставшихся сколексов. После этого рассе­
кается фиброзная капсула и предпринимается
попытка удалить опорожненный эхинококко­
вый пузырь. В случае невозможности это сде­
лать — рассекается хитиновая оболочка, по­
лость паразита осушается, он отделяется от
фиброзной капсулы и удаляется. Фиброзная
капсула дополнительно обрабатывается фор­
малином и спиртом.
При невозможности отделить хитиновую обо­
лочку от фиброзной капсулы паразит удаля­
ется вместе с ней, т. е. выполняется так назы­
ваемая «радикальная эхинококкэктомия»
[Волох Ю. Н., 19651. При этом необходимо
тщательно обрабатывать все мелкие сосуды и
бронхи, идущие в капсулу. Особенно тщательно
следует выделить и обработать бронх, находя­
щийся в наиболее глубоко расположенной части
капсулы — в области ее «дна».
Полость, оставшаяся после удаления пузыря,
может ликвидироваться самостоятельно, если
она небольших размеров. Однако лучше про­
извести ее облитерацию путем наложения ки­
сетных кетгутовых швов в несколько этажей,
начиная с наиболее глубоких отделов. После
завязывания они обеспечивают тесное сопри­
косновение стенок полости.
При значительных по размеру полостях,
остающихся после удаления гигантских эхино­
кокковых кист, возможно использование при­
ема, предложенного А. А. Вишневским (1956).
Производится частичное иссечение фиброзной
капсулы, а затем ее края обшиваются непре­
рывным кетгутовым швом. После расправле­
ния легкого стенка полости, составляющая ее
«дно», несколько растягивается, выпрямляется,
как бы превращаясь в поверхность легкого, со­
прикасается с париетальной плеврой, а в даль­
нейшем — припаивается к ней.
Эти методы оперативных вмешательств обыч­
но применяются либо при закрытых кистах,
либо после вскрытия их в бронх, до развития
гнойных осложнений.
В последнее время, с появлением новых анти­
бактериальных средств, эхинококкэктомия с
ушиванием полости используется и в случаях,
осложненных нагноением.
Если органосохраняющая операция невоз­
можна, то выполняются клиновидные резекции,
удаление доли или всего легкого [Львов А. Н.,
1956].
Хирургические вмешательства по поводу мно­
жественного эхинококкоза имеют существен­
ные особенности, но наибольшие трудности
возникают при оказании помощи больным с
двусторонним поражением.
Одновременное двустороннее оперативное
вмешательство по поводу эхинококкоза лег­
ких, впервые выполненное в СССР С. Л. Либо-
вым, правомочно. Однако риск его слишком
велик. Большая часть хирургов, имеющих опыт
лечения эхинококкоза легких [Гамов В. С.,
1960; Ахунбаев И. К., 1972, и др.], полагают,
что предпочтительнее последовательное удале­
ние паразитов сначала из одного, а затем из
другого легкого. Интервал между операциями
определяется общим состоянием больных, вос­
становлением и стабилизацией функциональ­
ных показателей систем дыхания и кровообра­
щения. В среднем он составляет I1 /г—2 мес.
Определяя очередность оперативного лече­
ния при двустороннем эхинококкозе, учитывают
распространенность поражения. Вначале сле­
дует оперировать со стороны наиболее изме­
ненного легкого. Тогда больные легче пере­
носят послеоперационный период: основная
нагрузка по обеспечению газообмена ложится
на наименее пораженное легкое. Затем пред­
принимается второй этап операции.
АЛЬВЕОКОККОЗ ЛЕГКИХ
Многокамерный эхинококк — личиночная
стадия развития другого самостоятельного вида
эхинококка — Alveococcus multilocularis. Забо­
левание, вызываемое им при поражении вну­
тренних органов, называют альвеококкозом.
Альвеококкоз распространен в южных рай­
онах ФРГ, Австрии, Швейцарии. В нашей стра­
не — главным образом в районах Сибири, Яку­
тии, Алтая и Дальнего Востока [Брегадзе И. Л.,
1961; Коган А. С., 1962; Кузнецов Ю. В., 1966].
Несмотря на то, что альвеолярный эхинококк
известен в медицине уже более 125 лет [Vir­
chow R., 1956], лишь относительно недавно —
в 60-х годах — был окончательно решен вопрос
о самостоятельности этого вида паразита и осо­
бенностях его эпидемиологии.
Цикл развития Alveococcus multilocularis во
многом повторяет развитие Echinococcus granu­
losus. При этом постоянным хозяином полово­
зрелой — ленточной — формы паразита явля­
ются песцы, лисы, собаки. Промежуточным
хозяином, в организме которого происходит
формирование личиночной (альвеолярной) ста­
дии паразита, служат мышевидные грызуны.
Человек заболевает альвеококкозом при упот­
реблении в пищу ягод, грибов, овощей, зара­
женных экскрементами больных животных,
носителей онкосфер, а также при обработке
их шкур.
Активно проникая из кишечника в кровенос­
ную систему, зародыш паразита всегда первично
закрепляется в печени, где находит оптималь­
ные условия для дальнейшего роста.
Личиночная стадия альвеолярного эхино­
кокка представляет большое количество мелких
266
Дифференциальная диагностика альвеоккоза с бластоматозным процессом даже при ла­
пароскопии, а нередко и при лапаротомии пред­
ставляет большие трудности вследствие свое­
образия изменений как в самом паразите, так
и близлежащих тканях.
Возможности серологической диагностики с
использованием антигена, полученного от одно­
камерных форм эхинококка (реакция Каццони),
по данным В. С. Семенова (1960), не превы­
шает 70—73 %.
Прогноз лечения альвеококкоза, особенно
при вторичном поражении легких, неблагоприя­
тен. При невозможности выполнить резекцию
из-за обширности распространения паразита
в организме используют консервативные мето­
ды лечения. Наряду с симптоматическими,
с 1958 г. предпринимаются попытки патогене­
тического воздействия — препаратами тимола.
Препарат «тэпаль» (тимоловый эфир пальмити­
новой кислоты) вводится внутримышечно по
1 мл через день, 5 инъекций на цикл. Курс лече­
ния включает 5 циклов, проводимых с интер­
валами от 6 до 14 дней. Установлено, что лече­
ние «тэпалем» снижает паразитарную актив­
ность при альвеококкозе.
Г. А. Моргунов (1962) отметил у больных
альвеококкозом, не подлежавших оператив­
ному лечению, улучшение под влиянием тера­
пии «тэпалем».
круглых пузырьков, расположенных в соедини­
тельнотканной капсуле. Оболочка альвеоляр­
ного эхинококка чаще всего состоит из одного
слоя. На разрезе паразит имеет ячеистое стро­
ение. Альвеолы-ячейки достигают 1—5 мм в
поперечнике. В них содержится желтоватая
или коричневато-желтая студенистая масса.
При микроскопическом изучении видно, что
альвеолы имеют кутикулярную оболочку, а в их
содержимом обнаруживаются выводковые кап­
сулы и сравнительно редко — сколексы и крю­
чья. В личиночной стадии паразит размножа­
ется почкованием по типу «неукротимого ро­
ста». Дочерних пузырей альвеолярный эхино­
кокк не имеет. Метастатическое распростране­
ние может происходить как гематогенным, так
и лимфогенным путем, а также по желчным
протокам. Метастазы возникают в легких, мозге,
почках и других органах.
Изменения в тканях, пораженных альвеококком, по внешнему виду напоминают бластома­
тозное поражение с очень плотными участками
неправильной конфигурации. На разрезе видны
очаги некроза, чередующиеся с фиброзными
прослойками. Распад тканей сопровождается
образованием полостей, которые содержат гно­
евидную жидкость, детрит, желчные пигменты
и т. д., а также мелкие пузырьки альвеококка.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
Альвеолярный эхинококкоз наблюдается
почти одинаково часто у мужчин и женщин
в возрасте от 20 до 50 лет. В очень редких слу­
чаях бывает инвазия в детском возрасте.
Первые признаки заболевания скудны и не­
определенны, причем даже при значительном
поражении печени боли и общие расстройства
могут отсутствовать длительное время.Жалобы
сводятся к нерезким болевым ощущениям, чув­
ству тяжести в надчревной области. Непосред­
ственной причиной обращения к врачу обычно
является обнаружение самим больным плотной
«опухоли» в правом подреберье.
Вследствие медленного развития и много­
летнего бессимптомного течения диагностика
альвеококкоза трудна. Поражение легкого обыч­
но происходит путем перехода процесса с пе­
чени, диафрагмы или заносом метастазов. К это­
му времени в клинической картине преоблада­
ют симптомы, более характерные для пораже­
ния органов брюшной полости. Имеются уве­
личение печени, изменение ее конфигурации.
Одним из ранних и сравнительно частых симпто­
мов альвеококкоза является желтуха (по дан­
ным И. Д. Даниляк, Ю. А. Волоха — в 85—
90 %), в основе которой лежат поражение пе­
ченочной паренхимы и нарушение оттока желчи
по внутрипеченочным желчным ходам.
ЦИСТИЦЕРКОЗ ЛЕГКИХ
Поражение внутренних органов человека
цистицерками (финнами) — личиночной фор­
мой развития свиного (Taenia solium) или
бычьего (Taenia saginata) цепней — носит на­
звание цистицеркоза.
Широкого распространения заболевание не
имеет, но наблюдается всюду, где развито ско­
товодство. В СССР цистицеркоз встречается
в Белоруссии, Западной Украине, на Дальнем
Востоке [Коновалова Л. М„ 1964], а также в
Армении, Азербайджане, Якутии, Бурят-Монголии, Тувинской автономной области [Плотни­
ков Н. Н„ 1965].
В стадии половой зрелости цепень паразити­
рует только в тонкой кишке человека. Свиньи,
крупный рогатый скот являются промежуточ­
ными хозяевами паразита и заражаются фин­
нозом (цистицерками), поедая корм, загряз­
ненный фекалиями инвазированного цепнем
человека.
В организм человека цистицерки попадают
при употреблении в пищу сырого или недоста­
точно термически обработанного финнозного
мяса. В просвете тонкой кишки они развиваются
в половозрелого ленточного гельминта.
267
Формирование взрослого гельминта проис­
ходит в течение 3 мес. В кишечнике человека
паразиты могут жить более 10 лет. По мере
созревания зрелые членики, располагающиеся
в терминальной части глиста, отделяются и пас­
сивно выделяются наружу. Возможно их актив­
ное выползание из анального отверстия и пере­
мещение по телу, белью.
За сутки больной выделяет до 28 члеников,
а с ними каждый раз до 5 млн. яиц (онкосфер)
цестод [Бердыев X. Б., Мухамадиев М. М„
1983].
При несоблюдении правил личной гигиены,
проглатывании с продуктами питания, загряз­
ненными выделениями больного кишечным
тениозом или тениаринхозом онкосфер свиного
или бычьего цепней, а также проникновения
онкосфер из кишечника в желудок ретроград­
ным путем — с рвотными движениями — про­
исходит их освобождение от оболочки. После
перехода вместе с содержимым желудка в тон­
кую кишку онкосферы внедряются в ее стенку
и током крови разносятся по всему организму,
поражая внутренние органы. Формирующиеся
здесь цистицерки приводят к появлению различ­
ных клинических расстройств. Цистицеркоз
относится к числу тяжелых осложнений тениоза и тениаринхоза.
Излюбленной локализацией цистицерков
являются головной мозг, глаза. Значительное
их количество продолжает развитие в подкож­
ной клетчатке, мышцах, в языке, сердце, легких.
Цистицерки, развивающиеся в легких, длитель­
ное время не приводят к выраженным клиниче­
ским расстройствам. Когда они достигнут раз­
меров 1—2 см, их рост останавливается, проис­
ходит гибель паразитов с омелотворением кап­
сулы. Этот признак при проведении рентгено­
логического обследования позволяет отличить
цистицеркоз от эхинококкоза и от развития
метастазов опухоли в легких. На рентгенограм­
ме видны множественные, четко очерченные
образования до 2 см в поперечнике, многие из
которых содержат включения извести.
Одновременное обнаружение цистицерков
в глазу при офтальмоскопии, а также клиниче­
ские проявления поражения центральной нерв­
ной системы (эпилептиформный, неопластиче­
ский, психический, менингеальный симптомокомплексы) дают возможность установить
точный диагноз.
В качестве специальных методов лаборатор­
ной диагностики цистицеркоза в клинической
практике получили распространение реакция
непрямой гемагглютинации и реакция флюо­
ресцирующих антител с антигеном из цисти­
церков. Разрешающие возможности этих реак­
ций, по данным Л. М. Коноваловой (1964),
являются весьма высокими.
В большинстве наблюдений при локализо­
ванной форме легочного цистицеркоза как хи­
рургическое, так и терапевтическое лечение не
требуется.
Осложнения со стороны других внутренних
органов — головного мозга, глаза, развиваю­
щиеся при цистицеркозе, являются показанием
к выполнению оперативных вмешательств.
Для профилактики осложнений кишечного
тениоза цистицеркозом основное значение
имеют ранняя диагностика и лечение этого гель­
минтоза.
ПАРАГОНИМОЗ ЛЕГКИХ
Парагонимоз — заболевание, возникающее
при поражении организма человека гельминтом
трематодой — легочной двуусткой (Paragonimus westermani). Эндемические очаги болезни
расположены главным образом на территории
Японии, Китая, Кореи, Индии. В СССР параго­
нимоз встречается среди населения, проживаю­
щего в районах Дальнего Востока: в низовье
Амура, на Южном побережье Охотского моря.
Цикл развития парагонимуса сложен. Он
включает двух промежуточных и окончатель­
ного хозяина. Последним чаще всего являют­
ся кошки, собаки, свиньи, лисицы, барсуки,
выдры, а также человек. Являясь строгим аэро­
филом, в теле окончательного хозяина, в том
числе и у человека, парагонимус может до­
стичь полного развития только в легких. В дру­
гих органах вследствие отсутствия доступа
кислорода воздуха цикл развития парагони­
муса приостанавливается на различных ста­
диях.
Оплодотворенные яйца паразита, выделяю­
щиеся с мокротой больного животного или че­
ловека, для своего дальнейшего развития
должны обязательно попасть в воду. Здесь из
них при благоприятных температурных условиях
через месяц выходят личинки — мирацидии. Мирацидии активно внедряются в тело первого про­
межуточного хозяина — речных моллюсков — и
в них проходят несколько фаз развития, превра­
щаясь в церкарии. Церкарии покидают тело мол­
люсков и свободно плавают в воде, проникая в
организм второго промежуточного хозяина —
пресноводных крабов или раков. Здесь церкарии
превращаются в цисты.
Заражение происходит при употреблении
в пищу сырых или недостаточно термически
обработанных крабов, раков, а также с питьевой
водой.
В организме человека для выхода парагони­
муса из цист важное значение имеет сочетанное
воздействие температуры тела, влажности и
щелочной реакции кишечного содержимого.
268
Под их влиянием происходит активация, выход
незрелых форм паразита из цист. Вышедшие
в просвет тонкой кишки незрелые парагонимусы перфорируют ее стенку и проникают в
свободную брюшную полость. Обладая спо­
собностью к активному передвижению, парагонимусы мигрируют в забрюшинное пространство,
печень, селезенку, заднее средостение. Подав­
ляющее число паразитов проникает в диафрагму
и достигает плевральных полостей. Здесь часть
парагонимусов может задержаться, а большин­
ство через висцеральную плевру достигает пери­
ферических отделов легкого, где и паразитирует,
завершив полный цикл развития. Длина зрелого
парагонимуса достигает 8—16 мм, ширина —
4—8 мм [Даниленко М. В., 1963].
Сравнительно крупные размеры, которых
паразит достигает в организме человека после
выхода из цисты, активная миграция на пути
к легкому с повреждением кишок, органов брюш­
ной полости, плевральной полости, а также ле­
гочной ткани, приводят к возникновению свое­
образных морфологических изменений в этих
органах.
В тканях по ходу миграции молодых гель­
минтов образуются паразитарные ходы с не­
крозом и кровоизлияниями.
С течением времени в легких — на конечном
этапе миграции паразита — формируются сооб­
щающиеся с бронхами кисты, «каверны». Иногда
эти образования могут быть закрытыми. Диаметр
этих образований — 1—6 см и больше; внутри
кисты обнаруживается 1—2 гельминта. Одиноч­
ные каверны и кисты располагаются обычно
в верхней и язычковой долях левого легкого
(правое легкое поражается реже), множествен­
ные — в нижней.
Микроскопически ранние каверны напомина­
ют геморрагический инфаркт, в центре которого
имеется участок расплавления. Зрелые имеют
гладкие стенки серо-красного цвета, обычно они
располагаются субплеврально. Паразитарные
каверны первично возникают в паренхиме легко­
го и только с течением времени вскрываются в
бронх и эпителизируются. Каверны, сообщаю­
щиеся с мелкими бронхами, напоминают мешот­
чатые бронхоэктазии. Стенка каверны имеет зо­
ны некроза, грануляций и инфильтратов. Про­
свет каверны заполнен казеозной массой серо­
белого цвета или жидкостью шоколадного, крас­
новатого цвета, иногда слизью, в которой имеется
примесь гноя. При благоприятном течении парагонимоза каверны и кисты замещаются соедини­
тельной тканью. В плевральной полости часто
развиваются спайки.
Вокруг яиц гельминта и продуктов их распада
в тканях легкого образуются гигантоклеточные
гранулемы.
КЛИНИЧЕСКОЕ ТЕЧЕНИЕ
Несмотря на то, что клиническая картина
парагонимоза описана еще в прошлом столе­
тии, современные представления об этом забо­
левании расширились мало. Наиболее часто
встречаются лишь отдельные наблюдения с
описанием признаков хронического парагони­
моза легких [Постников В. В., 1956].
Детальные представления о морфологиче­
ских и клинических проявлениях парагонимо­
за сформировались на основании работ Ю. Д.
Бацуро (1958, 1964), М. В. Даниленко (1963),
показавших все многообразие симптомов забо­
левания, обративших внимание нередкими не­
благоприятными исходами его течения.
Парагонимозом чаще болеют взрослые люди
в возрасте до 45 лет, т. е. наиболее трудоспо­
собная часть населения. Относительно высока
заболеваемость и в детском возрасте (более
20 % из всех больных имеют возраст до 16 лет).
Своеобразие патогенеза заболевания, миг­
рации паразита в человеческом организме опре­
деляют последовательность появления и разви­
тия его клинических симптомов.
Принято выделять 4 основные клинические
формы парагонимоза: 1) острую абдоминаль­
ную, 2) острую плевролегочную, 3) хрониче­
скую легочную, 4) осложненную легочную.
Нередко последовательность развития каж­
дого из периодов развития заболевания может
являться основой для распознавания болезни.
Однако строго разграничить каждый из перио­
дов парагонимоза не всегда удается ввиду того,
что выход генераций паразитов из цист проис­
ходит в несколько этапов. Абдоминальные рас­
стройства наслаиваются на плевролегочные.
Клинические проявления абдоминаль­
ной фазы парагонимоза включают
симптомы, более характерные для энтерита,
гепатита. Перитониты парагонимозного про­
исхождения нередки, но они протекают зна­
чительно легче, чем бактериальные, так как в
большинстве наблюдений являются асептиче­
скими.
При проникновении паразитов в плевральную
полость возникают клинические признаки ост­
рой плевролегочной фазы пара­
гонимоза. При этом симптоматика плев­
рита мало отличается от парапневмонического.
Клиника острого легочного парагонимоза
характеризуется повышением температуры
тела, возникновением болей в груди, появле­
нием кашля. Вначале кашель сопровождается
отделением небольшого количества слизистой
мокроты, которая вскоре становится гнойной,
часто содержит примесь измененной и свежей
крови. По истечении 3—4 мес такого острого
или подострого течения парагонимоз перехо­
дит в фазу хронического поражения легкого.
269
К этому времени все паразиты покидают кишеч­
ник, достигают внутренних органов — печени,
селезенки, средостения (где ввиду отсутствия
доступа воздуха прекращают свое развитие)
и легких, в которых имеются благоприятные
условия для роста паразита.
При хроническом легочном па­
рагонимозе клинические проявления за­
болевания обусловлены главным образом раз­
витием паразита в паренхиме легкого. Плеврит
в этот период встречается сравнительно редко,
а если бывает, то имеет слабо выраженные приз­
наки, не сопровождается болями и повышением
температуры тела. Как показали исследования
Б. Зографски и Г. Тезиева (1957), в происхож­
дении плеврита в этот период, наряду с ответ­
ной реакцией плевры на поражение легкого,
определенное значение имеет ремиграция парагонимусов в плевральную полость.
Течение хронического легочного парагонимоза медленное, с периодами обострения и от­
носительной ремиссии. Прогрессивно ухудша­
ется состояние больных.
Наряду е расстройствами, обусловленными
разрушением парагонимусом ткани легкого,
определенное значение имеют инфекционно ­
аллергические изменения в организме, явления
интоксикации продуктами жизнедеятельности
паразитов.
В период обострения повышается темпера­
тура тела, достигая 38—39 °C. Усиливаются
боли в груди, кашель. При этом значительно
увеличивается количество отделяемой гнойной
мокроты, в ней появляется примесь крови. Кро­
вохарканье — весьма характерный симптом
парагонимоза — может достигать значительной
интенсивности, переходить в кровотечения,
которые нередко обильны и угрожают жизни
больных. Наряду с легочными кровотечениями
возможно развитие пиопневмоторакса вслед­
ствие нарушения целости паразитарной кисты.
В периоды ремиссий температура тела сохра­
няется на субфебрильных цифрах, может быть
нормальной. Больные обычно отмечают тяжесть
и подострые боли в груди, кашель с отделением
гнойной мокроты.
Инфекционно-аллергические
признаки и
интоксикация проявляются в виде поражения
преимущественно центральной нервной систе­
мы и сопровождаются головной болью, голово­
кружениями, рассеянностью, снижением памяти.
Астенический синдром включает нарушение
сна и аппетита, снижение работоспособности,
развитие быстрой утомляемости.
При хроническом парагонимозе легких отме­
чают также остаточный абдоминальный синд­
ром, выражающийся болями в животе, увеличе­
нием и болезненностью печени. Известны эндо­
кринные расстройства — увеличение щитовид­
ной железы или ее долей, нарушение менстру­
ального цикла у женщин.
Ухудшение состояния, обострения хрониче­
ского легочного парагонимоза наступают вес­
ной и осенью, и их можно считать сезонными.
Тяжелые физические нагрузки, прием алко­
голя также приводят к декомпенсации состоя­
ния больных парагонимозом.
В терминальном периоде заболевания при
осложненном легочном парагонимозе имеется
метастатическое поражение других органов.
Наиболее часто и закономерно в процесс вовле­
кается головной мозг. Сюда заносятся яйца
паразита из легких.
Клиническое течение мозгового парагони­
моза тяжелое, сопровождается слепотой, пара­
личами, судорожными приступами с потерей
сознания.
ДИАГНОСТИКА
До настоящего времени диагностика параго­
нимоза легких представляет большие трудно­
сти. Важное место при этом отводят учету дан­
ных анамнеза, особенностей быта, питания,
пребывания на территориях, относимых к эн­
демическим очагам парагонимоза.
Наряду со своеобразием клинических прояв­
лений в разные периоды заболевания, диагно­
стическую ценность представляет характер
экссудата, полученного из плевральной поло­
сти: в острой плевролегочной фазе он содер­
жит примесь измененной и свежей крови. В экс­
судате и мокроте при микроскопическом ее
изучении возможно обнаружение парагонимусов.
Экссудат в фазе хронического течения ле­
гочного парагонимоза желтовато-мутноватый.
При его центрифугировании в осадке имеются
большое количество кристаллов холестерина,
капель жира, лейкоциты и эритроциты.
Как показали исследования Ю. Д. Бацура
(1962), в мокроте больных хроническим пара­
гонимозом легких закономерно обнаружива­
ются ромбовидные кристаллы, являющиеся
продуктом распада яиц гельминтов. Напоминая
по внешнему виду кристаллы Шарко — Лейдена,
они отличаются от последних не только тем.
что возникают в связи с непосредственным пре­
быванием половозрелого гельминта в тканях
окончательного хозяина при его жизни, но и
значительной устойчивостью к воздействию
хлороформа, спирта, эфира, бензола, раство­
ров щелочей и кислот. Выявление ромбовидных
кристаллов в мокроте считается достоверным
признаком парагонимоза, даже при отсутствии
яиц гельминта.
Серологические реакции в диагностике пара­
гонимоза еще не нашли широкого практиче­
270
ского применения. R. Ando (1916) предложил
для этой цели реакцию связывания компле­
мента. По мнению М. В. Даниленко (1963),
внутрикожная проба с антигеном, полученным
из легочных двуусток (1:100), может облег­
чить раннюю диагностику заболевания при мас­
совых обследованиях населения. Реакция ста­
вится и оценивается аналогично реакции Каццони.
ЛЕЧЕНИЕ
Большинство больных легочным парагонимозом может быть излечено консервативными
методами.
С наибольшим эффектом лечение больных
парагонимозом проводится эндотрахеальным
и внутривенным введением гидрохлорида эмитина с антибиотиками и раствора кальция хло­
рида. Пятидневные курсы с перерывами в 10
сут повторяются 2—3 раза.
Показанием к оперативному лечению парагонимоза легких является отсутствие эффекта
при использовании консервативных средств,
особенно при одностороннем расположении
паразитарной кисты. Частые и тяжелые легочные
кровотечения также являются основанием для
выполнения резекции легкого.
Формирование больших кист, содержащих
значительное количество гноя, угрожающих
инфицированием здоровых участков легкого,
прорывом в плевральную полость, является
показанием к оперативному лечению. Известно,
что первая операция при парагонимозе легкого
была выполнена L. Amreino (1923) в связи с
прорывом большой нагноившейся кисты в плев­
ральную полость.
При выборе объема и характера предприни­
маемой резекции легкого всегда руководству­
ются данными о распространенности процесса.
Своеобразие проникновения парагонимуса в
легкое — через висцеральную плевру в перифе­
рические его отделы с формированием субплев­
ральных полостей — позволяет у большинства
больных предпринять экономные операции:
удаление сегмента, выполнение краевой резек­
ции.
При значительных изменениях объем вмеша­
тельства может быть расширен до резекции доли
и даже всего легкого.
Глава ±
■
РАК ЛЕГКОГО
Среди всех опухолей легких рак встречается
наиболее часто — в 90—95 % наблюдений. Со
времени первых сведений о частоте этого забо­
левания [Bayle К., 1805; Laennec R.-T., 1837]
заболеваемость раком легкого быстро и про­
грессивно увеличивалась.
В США только в 1980 г. зарегистрировано
117 000 новых заболеваний раком легкого и
101 300 случаев смерти от него [Hardy J. et al.,
1981]. За 70-е годы в СССР число ежегодно
заболевающих злокачественными заболевания­
ми возросло с 430,2 тыс. в 1970 г. до 530,4 тыс.
в 1979 г. При этом значительный рост частоты
опухолей среди населения нашей страны, опре­
деляющий увеличение этого общего показателя,
связан в первую очередь со значительным уча­
щением рака легкого [Напалков Н. П., 1982].
В 70-е годы показатель заболеваемости раком
легкого на 100 000 человек населения составил
в среднем 24,5.
ЭТИОЛОГИЯ
К настоящему времени накоплено значитель­
ное количество данных, свидетельствующих
о том, что злокачественная трансформация
клеток может наступить от воздействия раз­
личных причин. Установлено, что в одинаковых
условиях один и тот же канцерогенный фактор
может вызвать развитие опухоли в значитель­
ном числе случаев, но может и не вызвать: многое
зависит от реакции организма в целом. Опре­
деление понятия «канцерогенные факторы», их
разнообразные классификации (по происхож­
дению, механизму действия, делению на хими­
ческие, физические, биологические и др.) весьма
условны. Однако это не мешает считать доказан­
ной способность многих хорошо идентифици­
рованных агентов самим по себе и в сочетании
с другими факторами достоверно повышать
вероятность развития злокачественных ново­
образований [Напалков Н. П., 1982]. Много­
численные наблюдения позволяют установить
причины возникновения так называемых «про­
фессиональных раков». По данным A. Huper
(1956), если среди 1000 мужчин, занятых в сель­
ском хозяйстве, смертность от рака легкого
составляет всего 0,82, то среди занятых в про­
изводстве железа и стали — 2,18, пластмасс и
резины — 2,34, графита — 2,91, цветных ме­
таллов — 3,22.
Высока заболеваемость раком легкого у работ­
ников шахт и рудников, асбестовых предприятий.
Достоверно доказано, что в городах рак лег­
кого встречается гораздо чаще, чем среди жите­
лей сельской местности. Источниками загряз­
нения атмосферы городов являются отопитель­
ные системы, выхлопные газы автомобилей,
пыль асфальтовых дорог, выброс в воздух хими­
ческих продуктов производственными пред­
приятиями. Среди канцерогенных веществ,
содержащихся в атмосферном воздухе про­
мышленных городов и областей, наиболее важ­
ную роль приписывают 3,4-бензпирену. Не­
сомненно, неблагоприятное воздействие оказы­
вают на эпителий слизистой оболочки дыха­
тельных путей такие канцерогенные вещества,
как радиоактивные соединения, производные
хрома, мышьяка, никеля. Развитие очагов воспа­
ления в дыхательных путях вокруг отложив­
шихся механических частиц в присутствии кан­
церогенов создает условия для взаимодействия
их со структурными элементами клеток, избы­
точной клеточной пролиферации и атипии эпи­
телия, с последующей их опухолевой трансфор­
мацией.
Одним из факторов, нарушающих, угнетаю­
щих процессы самоочищения бронхов, является
табачный дым. Канцерогенное действие та­
бачного дыма и его конденсата доказано в опы­
тах на животных. При исследованиях, проведен­
ных на секционном материале, установлено, что
у курящих в бронхах развиваются обширные
метапластические изменения, степень выражен­
ности которых находится в прямой зависимо­
сти от интенсивности курения. У больных раком
легкого эти изменения выражены особенно
сильно. С этих позиций хронический бронхит
курильщиков можно рассматривать как пред­
раковое состояние — тот фон, на котором часто
возникает рак легкого. Заболеваемость раком
легкого у длительно курящих людей примерно
в 20 раз выше, чем у некурящих.
272
Трудности эпидемиологического или клини­
ческого выявления агентов вирусной природы,
канцерогенных для человека, во многом понят­
ны, учитывая существующие представления
о механизме вирусного канцерогенеза. Автор
вирогенетической теории Л. А. Зильбер, начи­
ная с рабочей гипотезы, разработал стройную
систему, подтвержденную в настоящее время
многочисленными экспериментальными дан­
ными.
Вирусы широко распространены в природе.
Их известно более 600 видов. Считается, что
примерно 150 из них обладают онкогенным
действием и могут вызвать в организме жи­
вотных особый вид клеточной пролиферации,
ведущей к развитию опухолевого роста.
Экспериментальные данные свидетельствуют
о том, что вирусный онкогенез — сложный мак­
ромолекулярный процесс, протекающий в не­
сколько стадий с участием как вирусных, так и
клеточных генов и их ферментных систем.
Хронические воспалительные процессы, со­
провождающиеся образованием очагов избы­
точной пролиферации с атипией эпителия, под­
готавливают слизистую оболочку бронхов к раз­
витию злокачественной опухоли. Отмечено, что
рост заболеваемости раком и хроническими вос­
палительными заболеваниями дыхательных пу­
тей происходит параллельно.
При тщательном исследовании слизистой
оболочки бронхов у лиц, болевших хроническими
заболеваниями легких, нередко обнаруживают
начальные признаки рака легкого. Сходные
изменения отмечены у лиц, болевших тубер­
кулезом. В то же время у больных, погибших
от рака легкого, очень часто в слизистой обо­
лочке бронхов выявляются отчетливые призна­
ки хронического воспаления, а также пневмо­
склероз.
К числу заболеваний, имеющих известное
значение в этиологии рака легкого, относят так­
же грипп [Doll R„ 1955].
Все изложенное позволяет определить основ­
ные направления профилактики рака легкого.
Они сводятся к устранению причин, ведущих
к нарушению гигиены дыхания. Можно выде­
лить три направления: 1) социальное — борьба
за чистоту атмосферы городов, перевод на но­
вые, менее вредные для организма человека
виды энергетического обеспечения предприятий,
автомобильного транспорта, создание высокоэф­
фективных очистных сооружений; 2) гигиени­
ческое — отказ от курения, использование мер
индивидуальной защиты при выполнении спе­
циальных работ в помещениях с высокой сте­
пенью загазованности, запыленности; 3) клини­
ческое — выявление, своевременное и полно­
ценное лечение и учет лиц, болеющих хрониче­
скими воспалительными заболеваниями легких.
18 Зак. 0517
ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ
Рак легкого развивается из метаплазированного эпителия бронхов и бронхиальных желез.
Возникновение опухолевого роста из респира­
торного эпителия не доказано. Формы рака,
которые раньше называли паренхиматозными
или альвеолярными, по мнению многих иссле­
дователей, возникают не из метаплазированных
альвеолярных клеток, а их эпителия мельчай­
ших, терминальных бронхов, бронхиол.
Степень анаплазии клеток опухоли является
морфологическим выражением ее злокачествен­
ности — различий в темпе роста, взаимоотно­
шения с анатомическими образованиями лег­
кого, интенсивностью лимфогенного и гемато­
генного метастазирования [Петерсон Б. Е.,
1971; Пирогов А. И. и др., 1978]. Поэтому клас­
сификация гистологических типов рака легкого
имеет большое практическое значение при ре­
шении вопросов лечебной тактики.
Учитывая исследования ряда авторов [Чистович А. Н„ 1963; Малая Л. Т„ 1965; Weiss W.
et al., 1970], а также опыт многолетней работы
клиники госпитальной хирургии, в практическом
отношении оправдано выделение трех основных
гистологических типов рака легкого: эпидермо­
идного, недифференцированного и аденокар­
циномы. Так как рак легкого является органо­
специфической опухолью и степень его диф­
ференцировки определяется сохранением приз­
наков эпителиальной ткани, входящей в его
состав, то подобное распределение вполне обо­
снованно. К дифференцированным опухолям
относятся аденокарцинома и плоскоклеточный
рак с ороговением и без него. В этих опухолях
сохранен ряд признаков зрелой ткани: слизообразование в аденокарциноме, стратификация
и образование кератина — в плоскоклеточных
раках. Утрата этих свойств указывает на сни­
жение дифференцировки опухоли.
Наиболее удобной для клинической практики
является гистологическая классификация рака
легкого, разработанная в 1966 г. академиком
АМН СССР Н. А. Краевским и его сотрудни­
ками [Краевский Н. А., 1969, 1976; Ягубов А. С.,
1969, 1971]. Эта классификация выделяет:
1) плоскоклеточный рак (с ороговением и без
ороговения); 2) аденокарциному (высокодиф­
ференцированную, железисто-солидную, мало­
дифференцированную) ; 3) недифференциро­
ванный рак (мелкоклеточный «овсяно-клеточ­
ный», мелкоклеточный «лимфоцитоподобный»,
крупноклеточный).
Каждый гистологический тип рака легкого
характеризуется своеобразными чертами кли­
нического развития. Плоскоклеточный рак рас­
тет относительно медленно, не склонен к ран­
нему и обширному метастазированию. Адено-
273
карциномы развиваются сравнительно медленно,
но отличаются ранней гематогенной диссеминацией. Недифференцированные раки рано и ши­
роко метастазируют.
Своеобразием рака легких является нередко
встречающийся полиморфизм их гистологи­
ческого строения. Так, опухоль, имеющая в
основной своей массе строение, характерное
для плоскоклеточного рака, в отдельных участ­
ках может быть сходна с мелкоклеточными его
типами. При низкодифференцированных раках
встречаются зоны, более характерные по строе­
нию для плоскоклеточных типов опухоли, ме­
стами — для аденокарциномы. Это подтверж­
дает известное положение об условности границ
разделения отдельных гистологических типов
рака легкого, обусловливает трудности, с кото­
рыми встречаются при проведении патогистологической диагностики, ответственность при
установлении морфологической принадлежности
опухоли.
Аденокарциномы встречаются
наиболее
редко, составляя 10—-12 % от всех наблюдений.
Лишь в последние годы отмечено некоторое
увеличение числа больных аденокарциномой.
Одной из причин этого явления считают увели­
чение заболеваемости раком легкого среди жен­
щин, у которых аденокарциномы развиваются
более чем в 3 раза чаще, чем у мужчин.
Раки легкого плоскоклеточного типа заметно
преобладают у мужской части больных, направ­
ляемых в хирургические стационары, составляя
до 60 %. Недифференцированные раки легкого
встречаются примерно у 30% хирургических
больных, распределяясь, в равном соотношении
среди мужчин и женщин.
Важным критерием при решении вопросов
лечебной тактики признается величина первич­
ной опухоли в легком. Все современные клас­
сификации рака легкого учитывают этот пока­
затель как составной элемент общей характе­
ристики распространенности бластоматозного
процесса.
О состоянии и возможностях диагностики
заболевания, ее своевременности нередко судят
по частоте выявления небольших по размерам
раковых опухолей [Вагнер Р. И. и др., 1967;
Jashar J., 1975]. Принято считать, что с увели­
чением размеров опухоли исходы хирургическо­
го лечения ухудшаются. Однако, как показы­
вают многочисленные наблюдения, взятый
изолированно, этот признак не всегда позво­
ляет достоверно определить прогноз заболе­
вания. Нередки случаи успешного удаления
огромных опухолей с благоприятным исходом и
множественного гематогенного и лимфогенного
метастазирования так называемых «маленьких
раков», сводящего на нет все попытки помочь
больным [Шеляховский М. В., 1964].
На объем и вид оперативных вмешательств
у больных раком легкого, особенности хирур­
гической техники оказывает влияние характер
роста и развития первичной опухоли в легком.
По данным П. А. Куприянова и соавт. (1963),
Л. Т. Малой (1965), Р. И. Вагнера, А. С. Бар­
чука (1978), каждой опухоли легкого присуща
анатомическая форма и направленность роста:
относительно ограниченная с выраженными
границами (узловато-эндобронхиальная) или
инфильтративная без четких границ (преи­
мущественно перибронхиальная и перивазальная). Встречаются и смешанные, имеющие чер­
ты каждой из двух крайних типов, формы роста
раковой опухоли.
Вовлечение в бластоматозный процесс при
перибронхиально и перивазально растущих
раках различных внелегочных анатомических
образований грудной полости и средостения
во многом определяет своеобразие резекции
при выполнении оперативных вмешательств.
Большинство современных классификаций
бронхогенных раков делит их на центральные
и периферические [Ганул В. Л., 1963; Савиц­
кий А. И., 1967; Гарин Н. Д. и др., 1968; Albertini А., 1951, 1955]. Как показали исследования
А. С. Барчука (1967), периферические раки
склонны рано прорастать висцеральную плев­
ру, выходить за пределы легкого. Скрытое те­
чение заболевания при периферических фор­
мах роста опухоли определяет, как полагает
И. А. Максимов (1967), поступление в хирур­
гические стационары примерно каждого треть­
его больного с III стадией развития рака лег­
кого. Это дало основание В. И. Варгузиной
(1972) заключить, что в силу особенностей
местного роста периферических раков резектабельность при них выше, а техника операций
проще, но отдаленные результаты хуже, чем при
центрально расположенных опухолях. Своеоб­
разие роста и развития центральных, прикор­
невых раков легкого и периферических, исхо­
дящих из эпителия слизистой оболочки мель­
чайших бронхов, находит свое отражение в осо­
бенностях и возможностях диагностики каж­
дой из этих форм. В хирургические клиники
примерно в два раза чаще направляются боль­
ные с центральными формами опухоли, отно­
сительно рано проявляющими себя развитием
сопутствующих ателектазов или воспалитель­
ных процессов в легких.
Значительные изменения при развитии опу­
холи в легком претерпевает его регионарный
лимфатический аппарат. К моменту обращения
за помощью лимфогенные метастазы рака име­
ются у 65—70 % больных. При этом процессы
метастазирования центральных и перифериче­
ских раков легкого происходят по общим пра­
вилам и одинаково часто.
274
Детальное изучение характера и направлен­
ности лимфогенного метастазирования рака
легкого позволило установить некоторые зако­
номерности этого процесса, которые положены
в основу разработки расширенных оператив­
ных вмешательств.
Как показали исследования сотрудников
клиники С. А. Шалаева (1969, 1983) и Д. Сухээ
(1972), в начальном периоде развития заболе­
вания распространение лимфогенных метастазов
происходит в наибольшем соответствии с пред­
ставлениями о нормальном движении лимфы
от каждой из долей легкого.
Как правило, вначале поражаются распо­
ложенные ближе к опухоли внутрилегочные
группы узлов, затем — корневые, медиасти­
нальные и, наконец, надключичные. Процесс
метастазирования рака легкого имеет общую
тенденцию — от периферических отделов лег­
кого к средостению. Правда, наличие прямых
связей между отдельными участками регионар­
ных лимфатических коллекторов, а также фор­
мирование коллатеральных сосудов допускают
возможность поражения метастазами лимфа­
тических узлов последующих порядков, минуя
предыдущие. Такое метастазирование носит
название «скачущего». Так как основная масса
лимфатических узлов регионарных лимфа­
тических коллекторов легких сосредоточена в
средостении, это определяет особенно частое
поражение их метастазами — в 46—52 % на­
блюдений.
В пределах средостения с восходящим током
лимфы, по хорошо развитым лимфатическим
сосудам метастазы достигают лимфатических
коллекторов надключичных областей.
В практическом отношении важно, что дли­
тельное время, до полного поражения лимфа­
тических узлов, регионарных для легкого, в ко­
тором развивается опухоль, процесс метастази­
рования в пределах средостения происходит
по одноименной его стороне. Лишь при обшир­
ном метастазировании,
сопровождающимся
полной блокадой лимфатических коллекто­
ров средостения со стороны пораженного
легкого и при полной дезорганизации оттока
лимфы из этой области, метастазы развиваются
и на противоположной стороне средостения.
Распространяясь в восходящем направлении,
метастазы рака легкого достигают лимфатиче­
ских коллекторов надлючичных областей, по­
ражая расположенные здесь группы лимфати­
ческих узлов. Детальные исследования сотруд­
ника клиники Д. Сухээ (1972) показали, что
поражение метастазами надключичных регио­
нарных лимфатических коллекторов всегда
происходит вслед за медиастинальными.
С наибольшим постоянством лимфатические
узлы надключичных областей поражаются
18 *
метастазами рака легкого одноименной с опу­
холью стороны. Наиболее часто в бластоматоз­
ный процесс вовлекаются группы лимфатиче­
ских узлов надключичных областей при пора­
жении опухолью верхних долей, что обуслов­
лено их анатомической близостью и полностью
соответствует существующим представлениям
о направлении тока лимфы из этих отделов
легких.
Распространение рака легкого по лимфати­
ческим коллекторам средостения и надключич­
ных областей взаимосвязано. Метастазирова­
ние в надключичные группы лимфатических
узлов с закономерным постоянством проис­
ходит вслед за поражением наиболее верхних
участков лимфатических коллекторов, распо­
ложенных в средостении.
Поражение метастазами надключичных лим­
фатических узлов противоположной опухоли
в легком стороны или с двух сторон всегда
свидетельствует о далеко зашедшем, двусторон­
нем развитии лимфогенных метастазов рака
в пределах средостения.
Весьма важными в практическом отношении
являются неспецифические воспалительные
параканкрозные изменения, выявляемые при
патоморфологическом изучении в легком и груд­
ной полости у больных раком легкого. Так,
В. И. Ляшенко (1974, 1978), детально изучив
распространенность опухолевого процесса при
вскрытии у 100 больных раком легкого, кото­
рым были выполнены пробные торакотомии,
установил, что среди них в 11,2 % наблюдений
причиной отказа от радикальной операции яви­
лись увеличенные, спаянные в конгломераты
лимфатические узлы средостения, которые были
расценены как проявление множественного
метастазирования. При гистологическом изу­
чении в этих группах лимфатических узлов были
установлены только воспалительные измене­
ния. В 15 % наблюдений спаяние легкого с со­
седними образованиями также было расценено
как прорастание опухоли, в то время как про­
цесс не распространялся за пределы органа
и больные могли бы быть радикально опери­
рованы.
Параканкрозные изменения возникают как
в непосредственной близости к первичной опу­
холи, так и в более удаленных отделах легкого
и в регионарных лимфатических коллекторах,
пораженных и не пораженных ее метастазами.
Особое значение имеет гистологическое изу­
чение пограничных зон опухолевого роста
в легком [Гуревич М. А., 1967; Onuigbo W., 1973].
Согласно данным А. В. Григоряна (1962),
вокруг опухоли в легком вначале формируется
довольно толстый фиброзный слой, который
постепенно, по мере приближения к терминаль­
ной стадии заболевания замещается раковой
275
тканью. М. Д. Моисеенко (1966) также показал,
что при развитии опухолевого узла даже в глу­
бине легкого висцеральная плевра всегда отве­
чает реактивным процессом; при этом границы
бластоматозных изменений не доходят до нее
подчас на 2—3 см. Происходит утолщение са­
мой плевры за счет разрастания соединительной
ткани, образование вначале рыхлых, а затем
более грубых сращений между ее листками.
Развитие раковой опухоли в легком, как пра­
вило, сопровождается изменениями в регио­
нарных лимфатических коллекторах. Как пока­
зали наши исследования, эти изменения харак­
теризуются поражением лимфатических узлов
не только метастазами, но и воспалительным
процессом. Установлено, что примерно в каж­
дом 10-м лимфатическом узле, внешне неиз­
мененном, формируется метастаз опухоли.
В то же время в лимфатических узлах, достига­
ющих иногда значительных размеров и даже
спаянных в конгломераты, в трети наблюдений
при самом тщательном гистологическом иссле­
довании установлено лишь воспаление.
Процессы, происходящие в лимфатических
узлах при поражении их метастазами рака,
весьма своеобразны. Небольшой метастаз, фор­
мирующийся в лимфатическом узле под капсу­
лой, в краевом синусе, растет главным образом
в направлении к его центру, за счет паренхимы.
Капсула лимфатического узла длительное вре­
мя является своеобразным барьером для его
роста. Она претерпевает воспалительные из­
менения, несколько утолщается, формируется
зона периаденита, лимфатические узлы слива­
ются между собой и с расположенными рядом
бронхами, сосудами. Лишь в поздней фазе раз­
вития, при прогрессирующем увеличении, когда
метастаз почти полностью выполняет собой
пораженный лимфатический узел, происходит
его выход за пределы соединительнотканной
капсулы, прорастание рядом расположенных
анатомических образований.
Гематогенное метастазирование рака легкого
проявляет себя формированием очагов бласто­
матозного роста чаще всего в печени, почках,
надпочечниках, головном мозге, костях и реже—
в других органах.
При распознавании такого обширного, вы­
ходящего за пределы грудной полости, рас­
пространения опухоли пребывание больных
в хирургических стационарах не оправданно.
КЛАССИФИКАЦИЯ РАКА ЛЕГКОГО
Для классификации рака легкого детальное
патогистологическое изучение операционного
и секционного материала требует особого вни­
мания. На основании полученных данных скла­
дываются наиболее полные и точные представ­
ления о характере и распространенности опу­
холевых изменений, что определяет как воз­
можности и эффективность предпринятого
лечения, разработку и совершенствование хи­
рургических приемов и методов, так и общее
решение задачи оказания помощи этой кате­
гории онкологических больных.
Это решается путем тщательной маркировки
в ходе оперативных вмешательств всех удаля­
емых образований, отделов регионарных лим­
фатических коллекторов по отношению к основ­
ным топографо-анатомическим ориентирам
грудной полости, средостения, с последующим их
патогистологическим исследованием.
Полученные при таком исследовании сведения
дают возможность с высокой степенью досто­
верности распределить оперированных больных
по стадиям развития заболевания.
При этом руководствуются общепризнан­
ными в стране классификациями: по клиниче­
ским стадиям (утвержденной Президиумом
Ученого совета М3 СССР в 1956 г.) и между­
народной — по системе TNM (разработанной
Всемирным комитетом по классификациям
в 1965 г. и согласованной Программой коопе­
ративного изучения рака легкого в рамках СЭВ
в 1975 г.). Значения символов TNM общеизвест­
ны. Ниже приведены основные критерии оценки
опухолевого роста, определяющие принадлеж­
ность больных к каждой из принятых стадий
рака легкого.
Следует отметить, что нередко степень рас­
пространения процесса у больных раком лег­
кого принято определять до начала лечения,
сохраняя ее неизменной в течение всего периода
дальнейшего наблюдения. При установлении
стадий развития заболевания у хирургических
больных более правильным является, сохранив
их структуру и градации, руководствоваться
результатами патогистологического изучения
операционного материала. Такой подход дает
возможность более точно характеризовать рас­
пространенность рака легкого и в наибольшей
степени отвечает потребностям хирургической
кл