2 | 13
реклама

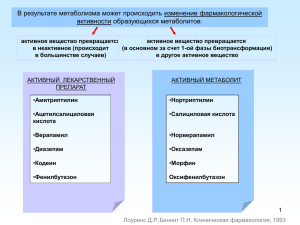
Роль масс-спектрометрии высокого разрешения в идентификации метаболитов синтетических каннабиноидов Тимофей Соболевский, к.х.н. ФГУП «Антидопинговый центр» 2 | 13 ФГУП АДЦ Аккредитация • ГОСТ Р ИСО/МЭК 17025 • одна из 32 антидопинговых лабораторий в мире, аккредитованных ВАДА Производительность • одно из первых мест в мире среди антидопинговых лабораторий по количеству проанализированных проб (18600 в 2013 году) • скрининговый анализ включает более 400 соединений (анаболические стероиды, β2-агонисты, антиэстрогены, диуретики, стимуляторы, наркотики, каннабиноиды, кортикостероиды, β-блокаторы) в трех аналитических процедурах Методы анализа • GC-MS, GC-MS/MS, GC-C-IRMS, UPLC-MS/MS, UPLC-OrbitrapMS 3 | 13 ФГУП АДЦ Оборудование приборный парк – один из самых больших в РФ, что позволяет разрабатывать методики и выполнять анализы не только для национального антидопингового агентства (РУСАДА), но и ряда других антидопинговых организаций, а также выполнять иные потоковые анализы (научные исследования, тестирование персонала и т.д.) 4 | 13 Синтетические каннабиноиды в ФГУП АДЦ JWH-018, начало работы, 2009 год Forensic Sci Int. 2010, 200(1-3), 141 Sobolevsky T, Prasolov I, Rodchenkov G. Detection of JWH-018 metabolites in smoking mixture post-administration urine. JWH-210, AM-2233, UR-144, AM-2201, 2012 год Drug Test Anal. 2012, 4, 745 Sobolevsky T, Prasolov I, Rodchenkov G. Detection of urinary metabolites of AM-2201 and UR-144, two novel synthetic cannabinoids. APICA, STS-135, 2014 год Drug Test Anal. (в печати) Sobolevsky T, Prasolov I, Rodchenkov G. Study on the phase I metabolism of novel synthetic cannabinoids, APICA and its fluorinated analog. AB-PINACA, 5F-AB-PINACA, PB-22F, AB-CHMINACA, MDMBCHMINACA, MMB2201, 2014 год … 5 | 13 Методология Детектируемые соединения все синтетические каннабиноиды полностью метаболизируют в организме! Выделение активного компонента из курительных смесей с использованием препаративной ВЭЖХ Проведение ферментативных реакций in vitro метаболизм с помощью микросомальной фракции печени человека (первая фаза метаболизма) Идентификация метаболитов • • высокоэффективная жидкостная хроматография в сочетании массспектрометрией высокого разрешения – поиск метаболитов высокоэффективная жидкостная хроматография в сочетании с тандемной масс-спектрометрией низкого разрешения – изучение фрагментации, выбор характеристичных SRM-переходов Анализ образцов мочи выбор диагностически значимых метаболитов 6 | 13 Масс-спектрометрия Орбитальная ионная ловушка Тройной квадруполь (Q) Exactive, Thermo Fisher Scientific TSQ Vantage, Thermo Fisher Scientific разрешение 100,000 @ 200 Да, точность масс < 5 ppm изучение фрагментации, выбор характеристичных SRM-переходов поиск метаболитов внедрение в методику скринингового анализа 7 | 13 Пробоподготовка и типовые условия анализа Пробоподготовка образца мочи • • • • • ферментативный гидролиз β-глюкуронидазой (Escherichia Coli) в фосфатном буфере создание слабощелочной среды карбонатным буфером жидкостно-жидкостная экстракция диэтиловым эфиром упаривание органического экстракта перерастворение в смеси метанол/вода Условия инструментального анализа • • • • • • хроматографическая колонка Waters Acquity C18 BEH (100 мм x 2.1 мм, 1.7 мкм) градиентное элюирование элюенты: вода/метанол с добавлением муравьиной кислоты электрораспылительная ионизация методика включает 120 соединений различных классов длительность анализа 10 мин 8 | 13 Поиск метаболитов STS-135 расчетное значение [MH]+ = 383.2493 Да F F O + гидроксилирование моно/ди/три дезалкилирование окислительное дефторирование … и их комбинации • • • • COOH HN O NH N O OH N NH OH NH 415.2392 395.2329 F F O OH O HN N O OH 399.2442 O N NH NH HN OH OH NH NH OH 431.2341 295.1805 311.1754 9 | 13 Профиль метаболитов STS-135 ВЭЖХ-МСВР 6.07 30000000 6.07 m/z 399.2442 m/z 399.2442 20000000 20000000 10000000 6.43 6.54 0 20000000 in vitro 0 5.80 m/z 415.2392 15000000 10000000 10000000 5.52 3000000 5.26 m/z 431.2341 5.19 2000000 5.04 1000000 5.65 0 in vivo 5.40 0 5.28 m/z 431.2341 200000 5.54 5000000 5.41 0 400000 5.79 m/z 415.2392 4.88 4.97 5.51 5.0 5.5 0 4.5 5.0 5.5 Time (min) 6.0 6.5 7.0 4.5 6.0 6.5 7.0 Time (min) 6.63 6.61 m/z 381.2537 m/z 381.2537 600000 6.51 100000 400000 50000 200000 6.52 0 1000000 6.77 4.95 0 5.69 m/z 397.2486 1000000 500000 5.67 m/z 397.2486 500000 6.14 6.35 6.15 0 150000 0 5.36 3000000 m/z 413.2435 5.31 m/z 413.2435 2000000 100000 1000000 50000 4.99 5.94 6.10 0 0 6.47 m/z 295.1805 300000 4000000 6.47 m/z 295.1805 200000 2000000 100000 4.35 0 4000000 m/z 311.1754 30000000 10000000 5.42 0 6.00 5.51 0 4.85 m/z 327.1703 400000 5.98 4.85 m/z 327.1703 6000000 4000000 200000 2000000 300000 5.60 5.32 m/z 311.1754 20000000 2000000 0 4.86 0 5.32 4.57 4.57 0 6.55 150000 m/z 395.2329 200000 100000 100000 50000 5.60 m/z 395.2329 6.54 5.73 4.51 5.78 0 0 4.5 5.0 5.5 Time (min) 6.0 6.5 7.0 4.5 5.0 5.5 Time (min) 6.0 6.5 7.0 10 | 13 Масс-спектры метаболитов STS-135 ВЭЖХ-МС/МС 133.1 100 F 90 232 90 O 80 Relative Abundance N 60 91.2 NH 232.1 OH 50 40 151 151.2 30 Relativ e Abundance 206 80 70 232.1 100 F 70 O N OH 60 NH 50 131.1 OH 40 206.1 30 167 105.2 20 206.1 10 118.2 144.1 155.2 399.3 10 249.2 0 415.4 149.2 20 93.2 121.1 144.2 167.2 249.2 0 100 150 200 250 300 350 400 100 150 200 250 m/z m/z 248.2 100 90 222 70 O N 60 OH NH 50 OH 40 30 149.1 20 222.1 244 NH 50 40 135 395.3 30 218.1 200.1 93.0 107.2 244.2 317.2 226.2 0 0 150 60 10 321.2 O N 70 20 204.1 91.2 105.1131.1 144.2 100 431.4 400 218 80 Relative Abundance Relative Abundance 90 248 350 COOH OH 80 10 135.0 100 F 300 200 250 m/z 300 350 400 100 150 200 250 300 m/z выбор характеристичных и селективных SRM-переходов 350 400 11 | 13 STS-135 в образце спортсмена 12 | 13 Газовая хроматография Основные сложности • структура малопригодна для анализа методом ГХ • низкая летучесть метаболитов • малопредсказуемые спектры ЭИ • низкая концентрация в образце • интерференция с эндогенными соединениями (кортикостероиды) CH 3 CH3 N O Масс-хроматограмма моногидроксилированных метаболитов JWH-018, полученная методом ГХ-МС/МС после триметилсилилирования Si H3C O CH3 13 | 13 Заключение • использование микросомальной фракции ферментов печени человека для реакций in vitro позволяет получить широкий спектр потенциальных метаболитов синтетических каннабиноидов • принимая во внимание особенности структуры этого класса соединений, метод высокоэффективной жидкостной хроматографии является предпочтительным • масс-спектрометрия высокого разрешения позволяет однозначно идентифицировать метаболиты на фоне биологической матрицы • используя данные, полученные методом ВЭЖХ-МСВР, возможно охарактеризовать потенциальные метаболиты методом тандемной масс-спектрометрии, установив характеристичные SRM-переходы для каждого из них • анализ образцов, полученных в условиях in vivo, позволит установить, какие из метаболитов являются диагностически значимыми 14 | 13 Спасибо за внимание Тимофей Соболевский [email protected] +7 (916) 624-4389