Независимое расследование по теме « Галогены».
реклама

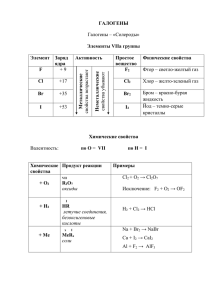
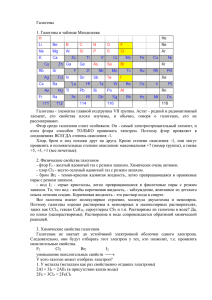
Независимое расследование по теме «Галогены». Цель урока: систематизировать и углубить знания о галогенах на основании их сравнительной характеристики; уметь сравнивать свойства простых веществ, работать с учебником. План урока. Строение атомов. Следственный эксперимент физиков. Следственный эксперимент химиков. Следственный эксперимент биологов. Следственный эксперимент историков. Выводы. Закрепление. На дом. Спасибо за урок. Строение атома F+9)2)7 Cl +17)2)8)7 Br +35)2)8)18)7 I +53)2)8)18)18)7 Следственный эксперимент физиков Вещество Агрегат ное состояние Цвет Запах t пл. ºС t кип. ºС Фтор F2 Газ Светложелтый Резкий, раздражающий -220 -188 Хлор Cl2 Газ Желтозеленный Резкий, удушлевый -101 -34 Резкий, зловонный -7 +58 Резкий +114 +186 Бром Br2 Жидкост Буроватоь коричневый Иод I2 Твердое веществ о Чернофиолетовый с металлическ им блеском. Следственный эксперимент химиков Химические свойства С металлами: F 2+ Zn = ZnF2 2Sb +3 Cl2 = 2SbCl3 2 Sb + 5 Cl2 = 2SbCl5 2Fe + 3Cl2 = 2Fe Cl 3 Cu + Br2 = CuBr2 2Al + 3I2 = 2AlI3 H2 + Cl2 = 2HCl Со сложными веществами: Сl2 + 2NaBr = 2NaCl + Br2 Br2 +2KI = 2KBr + I2 2F2+2H 2O= 4HF + O2 Следственный эксперимент биологов. Фтор, хлор - простые вещества, газы, ядовиты. Элемент фтор входит в состав зубной эмали Участвует в обмене веществ в железах, мышцах, нервных клетках. Ионы хлора важнейшие элементы для живых клеток. Бром для медицинских препаратов.Регулирует процессы возбуждения и торможения ЦНС. Иод входит в состав гормона тироксина,которую вырабатывает щитовидная железа. Следственный эксперимент историков F получен в 1866г. фр. химиком Анри Муассан. Cl открыт в 1774г. швед. химиком К. Шееле. Br открыт в 1826г. фр. химиком А. Баларом. I открыт в 1811г. фр. Химиком Б. Куртуа. Выводы Все галогены – неметаллы. В реакциях с металлами или менее электроотрицательными неметаллами галогены являются окислителями. Окислительная способность галогенов падает от фтора к иоду, это связано с увеличением порядкового номера элемента, заряда ядра атома и радиуса атома. Закрепление: Дайте сравнительную характеристику хлора и брома, указав: а) сходство; б) различие.Ответ поясните уравнениями реакции. Напишите уравнения химических реакций: Cl2 + ? = HCl Cl2 + ? = AlCl3 HCl+ ? = AlCl3+ ? Составьте электронные формулы хлороводорода и хлора.Укажите вид химической связи. На дом: §17, упр. 7,8.