Осциллятор гармонического осциллятора, гамильтониан гармонического осциллятора, причём потенциальная энергия W
реклама

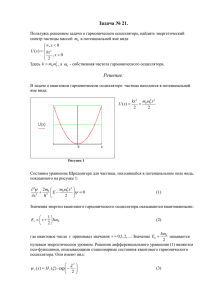
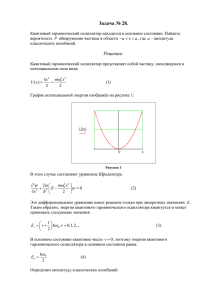
Осциллятор в квантовой механике представляет собой квантовый аналог простого гармонического осциллятора, при этом рассматривают не силы, действующие на частицу, а гамильтониан , то есть полную энергию гармонического осциллятора, причём потенциальная энергия W предполагается квадратично зависящей от координат. Wk(x,y,z). Так как энергия E — материальная величина, гамильтониан являться Эрмитовым оператором (т.е. самосопряжённым) . будет Средняя энергия квантового осциллятора Распределение Максвелла - Больцмана было получено в классической физике, но оно оказалось верным и в квантовой механике. Классическая энергия системы, моделирующей колебания атомов в молекуле дается формулой и может принимать любые значения в зависимости от амплитуды колебаний. Как нам известно из квантовой механики, энергия колебаний квантуется, то есть принимает дискретный ряд значений (по гипотезе М.Планка), определяемых формулой: . Для нахождения среднего колебательного квантового числа п при некоторой температуре T, мы должны подсчитать сумму: => => , отсюда средняя энергия: где функция cth - гиперболический котангенс будет определяться соотношением Средняя энергия квантового ротатора В квантовой механике ротатор - система, совершающая вращательное движение (вращающаяся молекула, электрон в поле атомного ядра). Его главной характеристикой является момент импульсa I, который может принимать дискретные значения, описываемые соотношением . Энергия вращательного движения классического ротатора будет иметь вид: , отсюда энергия вращения молекулы: . В квант. Мехе квадрат момента импульса будет квантоваться и энергия вращ. Движения молекулы будет равна: . Используя это соотношение и распределение Максвелла - Больцмана, можно получить выражение для средней энергии квантового ротатора. При низких температурах ротатор будет находиться в основном состоянии, соответствующем значению J=0 (отсутствие вращения). «Переход» между двумя этими предельными случаями осуществляется, очевидно, при такой температуре ТВР когда тепловое движение способно возбудить вращательные степени свободы. Минимальная (отличная от нуля) энергия вращения равна . Влияние температуры на скорость хим. Реакций. Объяснение влияния температуры на скорость хим. Реакций можно дать, используя распределение Максвелла – Больцмана. Для протекания большинства хим. реакций необходимо, чтобы энергия частиц превышала определенный порог, т.е, чем больше таких частиц, тем выше скорость реакций (N частиц ~ V реакции). Выразим скорость одной частицы через ее кин. Энергию: Уровням: , в результате получим расп-е частиц по энерг. , отсюда количество частиц с большей пороговой энергией: Используя значения комнатной температуры, можно сделать вывод, что повышение температуры на мизерное значение привело к увеличению на 60% числа частиц, энергия которых превышает пороговое значение.