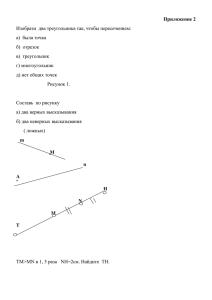
Bexterevax
реклама

Министерство общего и профессонального образования свердловской области Государственное бюджетное образовательное учреждение Среднего профессионального образования Свердловской области «Сухоложский многопрофильный техникум» Методические указания по выполнению лабораторных работ (практикум) для УП.01 учебная практика по профессиональному модулю ПМ.01 Хранение и подготовка сырья для специальности СПО 240111 «Производство тугоплавких неметаллических и силикатных материалов и изделий» Номинация: «Учебно-методическая продукция» Вид методической продукции: методические разработки и рекомендации по проведению лабораторных работ Автор: Бехтерева Ольга Юрьевна, Преподаватель спецдисциплин 624804, Свердловская область, г. Сухой Лог, ул. Юбилейная, 10 телефон 8(34373) 4-27-91 [email protected] Екатеринбург, 2015 Рассмотрена на заседании ПЦК технического профиля ГБОУ СПО СО «Сухоложского многопрофильного техникума» Председатель цикловой комиссии _____________________/Н.А. Шурова «____»______________________2014г. Методическое пособие - Сборник лабораторных работ (практикум) составлен на основе Федерального государственного образовательного стандарта (далее – ФГОС) по специальности среднего профессионального образования (далее СПО) 240111 «Производство тугоплавких неметаллических и силикатных материалов и изделий», приказ Минобрнауки РФ № 437 от 20 октября 2009 г, с учетом запросов регионального рынка труда, учебного плана и рабочей программой УП.01 УЧЕБНАЯ ПРАКТИКА по профессиональному модулю ПМ.01 ХРАНЕНИЕ И ПОДГОТОВКА СЫРЬЯ Организация-разработчик: ГБОУ СПО СО «Сухоложский многопрофильный техникум». Разработчик: Бехтерева Ольга Юрьевна, преподаватель первой квалификационной категории, ГБОУ СПО СО «Сухоложский многопрофильный техникум», г. Сухой Лог. Рецензент: Ситчихина Любовь Арсентьевна,методист высшей квалификационной категории, ГБОУ СПО СО «Сухоложский многопрофильный техникум», г. Сухой Лог. 2 СОДЕРЖАНИЕ 1 ПОЯСНИТЕЛЬНАЯ ЗАПИСКА 2 ОБЩИЕ ПОЛОЖЕНИЯ 3 ТЕМАТИЧЕСКИЙ ПЛАН 4 УЧЕБНО-МЕТОДИЧЕСКОЕ ОБЕСПЕЧЕНИЕ ЛАБОРАТОРНОГОПРАКТИКУМА 5 ТЕХНИКА ВЫПОЛНЕНИЯ ЛАБОРАТОРНЫХ РАБОТ 5.1 Общие правила работы в лаборатории 5.2 Химическая посуда и обращение с ней 5.3 Посуда общего назначения 5.4 Посуда специального назначения 5.5 Фарфоровая посуда 5.6 Металлическое оборудование 5.7 Электрическое оборудование 6 ЛАБОРАТОРНЫЕ РАБОТЫ Лабораторная работа 1-Взятие навески материала для определения потерь при высушивании Лабораторная работа 2-Определение потерь при прокаливании лабораторная работа 3-Определение общего содержания серного ангидрида методом осаждения хлорида бария Лабораторная работа 4-Приготовление стандартного раствора соляной кислоты Лабораторная работа 5-Определение общей щелочности соды Лабораторная работа 6-Приготовление стандартного раствора трилона Б Лабораторная работа 7-Определение процентного содержания кальция в кальците Лабораторная работа 8-Определение качества извести Лабораторная работа 9-Ситовой анализ зернистых материалов Лабораторная работа 10-Определение качества глинистого шликера Лабораторная работа 11-Определение водопоглощения шамота Лабораторная работа 12-Определение количества шамота в шамотной массе Лабораторная работа 13-Определение плотности огнеупорный материалов Лабораторная работ 14-Химическая стойкость керамических изделий Лабораторная работа 15-Определение распушки асбеста Лабораторная работа 16-Определение нормальной густоты цементного теста Лабораторная работа 17-Определение сроков схватывания цемента 7 ИНФОРМАЦИОННОЕ ОБЕСПЕЧЕНИЕ ОБУЧЕНИЯ 3 4 5 7 8 9 9 10 12 20 23 24 28 30 32 37 40 43 45 48 52 54 57 59 62 65 68 71 74 77 1 ПОЯСНИТЕЛЬНАЯ ЗАПИСКА Методические рекомендации по выполнению лабораторных работ для УП.01 УЧЕБНАЯ ПРАКТИКА по профессиональному модулю ПМ.01 ХРАНЕНИЕ И ПОДГОТОВКА СЫРЬЯ является составной частью основной профессиональной образовательной программы и составлены в соответствии с требованиями федерального государственного образовательного стандарта СПО по специальности 240111 Производство тугоплавких неметаллических и силикатных материалов и изделий,учебным планом и рабочей программой. Сборник предназначен для подготовки специалистов среднего звена в области производства тугоплавких неметаллических и силикатных материалов и изделий целью овладения соответствующих компетенций, умений и знаний, необходимых для обеспечения конкурентоспособности выпускника. В каждой теме сборника определены цели работы, приведен перечень необходимого оборудования, инструментов, аппаратуры, материалов, даны теоретические основы по теме занятия, раскрыт порядок проведения работы. При составлении пособия было учтено, что большинству современных пред -приятий в настоящей момент требуются специалисты с хорошо развитыми навыками. Выполнение заданий лабораторного практикума поможет Вам быстрее адаптироваться к условиям профессиональной деятельности. Лабораторные работы проводятся в лаборатории техникума, оснащенной всем необходимым технологическим оборудованием. В процессе проведения лабораторных работ студенты должны: иметь практический опыт: - распознавания основных и вспомогательных сырьевых материалов; - проведения расчетов сырья; - проведения анализа сырья и сырьевых смесей; - приготовления сырьевых смесей; уметь: - выбирать метод анализа; - выбирать технологию обработки сырьевых материалов; - работать с лабораторным оборудованием; знать: - методики анализа химического и гранулометрического состава сырьевых материалов и шихты; - физико-химические свойства сырьевых материалов; - технические требования к химическому составу сырья; - технические требования к гранулометрическому составу сырья; - условия хранения отдельных видов сырья; - нормативный запас каждого вида сырья. Тематика лабораторных работ, содержащихся в данном сборнике, может быть изменена или дополнена, в зависимости от пожеланий социальных партнеров (работодателей), возможностей материальной базы учебного заведения, наличия необходимого оборудования и других факторов. 4 2 ОБЩИЕ ПОЛОЖЕНИЯ УВАЖАЕМЫЙ СТУДЕНТ! Настоящие методические пособие определяют цели и задачи, а также конкретное содержание заданий , особенности организации и порядок выполнения работ. К выполнению лабораторно-практических работ допускаются обучающиеся, которые: прошли инструктаж по технике безопасности; сдали допуск к выполнению лабораторной работы; составили отчеты и защитили выполненные работы (имеют не более двух незащищенных работ); защитили теоретический и практический материал по всем предыдущим темам. Лабораторные работы по качественному химическому анализу считаются успешно выполненными, если обучающийся верно идентифицировал все компоненты пробы. Лабораторные работы по количественному химическому анализу считаются успешно выполненными, если полученный студентом результат соответствует истинному значению с допустимой погрешностью. При получении ошибочного результата студент выполняет работу еще раз, заново взяв контрольную пробу. После выполнения каждого цикла работ проводится проверка усвоения теоретического и практического материала в форме индивидуального устного собеседования с преподавателем, письменного ответа с последующей защитой либо компьютерного тестирования. К защите темы допускаются обучающиеся, которые выполнили все лабораторные и расчетные задания по ней. Обучающиеся, полностью выполнившие программу лабораторного практикума, допускаются к сдаче зачета по УП.01, который проводится в устной или письменной форме. При выставлении зачета учитывается вся работа студента на протяжении учебной практики: выполнение лабораторных работ и расчетных заданий, знание теоретического и практического материала. Отчеты о выполненных лабораторных работах оформляются в электронном виде ,а затем с распечатываются для проверки преподавателем. После защиты работ отчеты подписываются преподавателем и служат документом, подтверждающим успешное выполнение лабораторного практикума. При выполнении работ по количественному анализу обязательным является соблюдение правил записи результатов измерения и указание единиц измерения. Точность измерения основных величин и правила записи результатов измерения приведены в таблице 2.1, а точность расчета величин - в таблице 2.2. 5 ТАБЛИЦА 2.1-ТОЧНОСТЬ ИЗМЕРЕНИЯ ОСНОВНЫХ ВЕЛИЧИН И ПРАВИЛА ЗАПИСИ РЕЗУЛЬТАТОВ Пример Точность Измеряемая величина Средство измерения записи измерения Пипетка 25,00 ± 0,05 V, мл (при использовании Бюретка мерная 12,45 ± 0,05 точной мерной посуды) Колба 100,0 ± 0,1 V, мл (при использовании Мерный стакан 200 мерной посуды с ориентиМерный цилиндр 15 ±1 ровочными делениями) Мензурка 30 Технические весы 0,10 ± 0,01 m, г Аналитические весы 0,1023 ± 0,0001 Таблица 2.2-Точность расчета величин Рассчитываемая величина Точность расчета m, г ± 0,0001 V, мл ± 0,05 Атомная масса, С точностью, указанной в Молярная таблице Д. И. Менделеева Масса, г/моль С, моль/л 4 значащие цифры (цифры, Т, г/мл начиная с первуй N, моль, ммоль Пример записи 0,1200 12,35 126,033 0,1025 0,0052 6,728 Структура лабораторной работы: Наименование темы лабораторной работы. Цель лабораторной работы. Материалы, реактивы и оборудование. I. Теоретическая часть. II. Методика выполнения работы. III. Расчетная часть. IV. Заключение. Обращаем Ваше внимание ,что по окончании каждого занятия студенты составляют отчет по предложенной форме,защищают свою работу и получают оценку.Завершается обучение проведением дифференцированного зачёта. Желаем Вам успехов! 6 3 ТЕМАТИЧЕСКИЙ ПЛАН Тема Инструктаж Техника безопасности при выполнении работ по химическому анализу Техника безопасности при использовании приборов, химической посуды, инструментов. Вводный инструктаж по ТБ. Техника безопасности на рабочем месте.Заполнение нормативно-технической документации Общие правила при работе с оборудованием, материалами,химическими веществами Учебно-производственные работы Определение потерь при высушивании Определение потерь при прокаливании Определение общего содержания серного ангидрида методом осаждением хлористым барием Приготовление стандартного раствора соляной кислоты Определение общей щелочности соды Приготовление стандартного раствора трилона Б Определение процентного содержания кальция в кальците Определение качества извести Проведение ситового анализа зернистого материала Определение водопоглащения шамота Определение количества шамота в шамотной массе Определение качества глинистого шликера Определение кислотоустойчивости керамических изделий Определение плотности огнеупорных материалов пикнометрическим способом Определение степени распушки асбеста Определение нормальной густоты цементного теста Определение сроков схватывания цементного теста Зачет Всего 7 Кол-во часов 6 2 2 2 70 6 6 6 2 2 2 4 4 4 4 6 4 4 4 4 4 4 4 80 4 УЧЕБНО-МЕТОДИЧЕСКОЕ ОБЕСПЕЧЕНИЕ ЛАБОРАТОРНОГО-ПРАКТИКУМА Для изучения и успешного выполнения лабораторно-практических работ необходимо использовать учебную литературу, издания на электронных носителях, программное обеспечение и т. п. Список рекомендуемой литературы и учебно-методических материалов приведен в конце методического пособия. Литературу можно получить в библиотеке ГБОУСПОСО «СМТ», в т. ч. материалы на электронных носителях. Кроме того, разработку можно записать на флэш-карту в учебной лаборатории Химического анализа. Для самостоятельной работы рекомендуется использовать следующие учебно-методические материалы: 1) для изучения теории: учебники [1-3,5-8,10,16,17,19,21,22 доп.ист. 2,3]; конспекты лекций и их электронные версии; учебно-методическое пособие [7,9доп.ист.1] и его электронная версия; 2) для выполнения лабораторных работ и составления отчетов о выполненных лабораторных работах: настоящее издание лабораторного практикума и его электронная версия; действующие стандарты на методы испытаний и оформление технической документации [1-7]; 3) для решения расчетных задач: задачники [11, 13, 14]; учебно-методическое пособие [13]; 4) для поиска справочной информации: справочник [18]; справочное издание [доп.ист. 4] и его электронная версия; 5) для выполнения проблемного задания: печатное издание [16] и его электронная версия; лабораторные практикумы [4,12,20]; 6) компьютерные программы, презентации и видеоматериалы. 8 5 ТЕХНИКА ВЫПОЛНЕНИЯ ЛАБОРАТОРНЫХ РАБОТ 5.1 Общие правила работы в лаборатории Приступая к практическим занятиям в лаборатории, необходимо помнить, что малейшая неаккуратность в работе приводит к искажению результатов анализов, на которые затрачивается много труда и времени. Следует внимательно следить за тем, чтобы рабочее место всегда было чисто и сухо. Нельзя загромождать его посторонними предметами. На столе должно находиться только то, что необходимо для проведения текущей операции, все лишнее надо убирать. При выполнении отдельных количественных определений следует тщательно соблюдать установленную методику работы. Нужно помнить, что результаты анализа могут быть хорошими только тогда, когда строго соблюдаются все условия, при которых данный метод был разработан и проверен. Не менее тщательно должны соблюдаться также правила, касающиеся техники выполнения отдельных операций, например фильтрования, промывания, высушивания и прокаливания осадков и т.д. Важное значение имеет ведение лабораторных записей. Ни в коем случае не разрешается делать эти записи на отдельных листках или кусках бумаги, а следует обязательно завести тетрадь. При ведении электронного лабораторного практикума следует все необходимые данные заносить в него сразу, избегая переписываний. Каждому определению отводят особую страницу. Оборудование рабочего места. Помимо общего оборудования, имеющегося в лаборатории качественного анализа, на каждом рабочем месте должны быть: металлический штатив для колец и зажимов, штатив для пробирок. маленькая коническая колба или химический стакан,. Кроме того, на рабочем месте должен находиться набор реактивов, посуда: стеклянная воронка, фарфоровая чашка, тигель часовое стекло, бюкс, промывалка, бюретка, стеклянная палочка или шпатель. 5.2 Химическая посуда и обращение с ней Важным значением в работах по химическому анализу имеет стеклянная посуда. Кроме нее применяют также посуду и приборы из фарфора и других материалов. Стекло. Стекло по своему составу бывает различным, не всякое стекло пригодно для химических работ. Лучшим сортом является жаростойкое стекло, отличающееся сравнительно малым коэффициентом расширения, высокой температурой размягчения и большой химической устойчивостью. Наиболее сильно разрушают стекло щелочные растворы; кислые растворы (кроме содержащих плавиковую кислоту) действуют на него даже слабее, чем чистая вода. При нагревании всех стеклянных изделий необходимо избегать резкого изменения температуры, а также неравномерного нагревания их в разных частях. Нагре9 вать стеклянные сосуды следует только на асбестированной сетке, но не на открытом огне. Термостойкая посуда имеет мутный или закрашенный значок (круг, прямоугольник) на своей поверхности. 5.3 Посуда общего назначения Пробирки рисунок 5.1- представляют собой узкие цилиндрической формы сосуды с закругленным дном; они бывают различной величины и диаметра и из различного стекла. Обычные лабораторные пробирки изготовляют из легкоплавкого стекла, но для особых работ, когда требуется нагревание до высоких температур, пробирки изготовляют из тугоплавкого стекла или кварца. Для хранения пробирок, находящихся в работе, служат специальные деревянные, пластмассовые или металлические штативы рисунок 52. Рисунок 5.1- Простая и градуированная пробирки Рисунок 5.2-Штатив Пробирки применяют для проведения главным образом аналитических или микрохимических работ. При проведении реакций в пробирке реактивы не следует применять в слишком большом количестве. Совершенно недопустимо, чтобы пробирка была наполнена до краев. Реакцию проводят с небольшими количествами веществ; достаточно бывает 1/4 или даже 1/8 емкости пробирки. Иногда в пробирку нужно ввести твердое вещество (порошки, кристаллы и т. п.), для этого полоску бумаги шириной чуть меньше диаметра пробирки складывают вдвое по длине и в полученный совочек насыпают нужное количество твердого вещества. Пробирку держат в левой руке, наклонив ее горизонтально, и вводят в нее совочек почти до дна. Затем пробирку ставят вертикально и слегка ударяют по ней. Когда все твердое вещество высыплется, бумажный совочек вынимают. Для перемешивания налитых реактивов пробирку держат большим и указательным пальцами левой руки за верхний конец и поддерживают ее средним пальцем, а указательным пальцем правой руки ударяют косым ударом по низу пробирки. Этого достаточно, чтобы содержимое ее было хорошо перемешано. Совершенно недопустимо закрывать пробирку пальцем и встряхивать ее в таком виде; при этом можно не только ввести что-либо постороннее в жидкость, находящуюся в пробирке, но иногда и повредить кожу пальца, получить 10 ожог. Если Пробирка наполнена жидкостью больше чем на половину, содержимое перемешивают стеклянной палочкой. Если пробирку нужно нагреть, ее следует зажать в держателе. При неумелом и сильном нагревании пробирки жидкость быстро вскипает и выплескивается из нее, поэтому нагревать нужно осторожно. Когда начнут появляться пузырьки, пробирку следует отставить и, держа ее не в пламени горелки, а около него или над ним, продолжать нагревание горячим воздухом. Следует помнить! При нагревании открытый конец пробирки должен быть обращен в сторону от работающего и от соседей по столу. Когда не требуется сильного нагрева, пробирку с нагреваемой жидкостью лучше опустить в горячую воду. Если работают с маленькими пробирками (для полумикроанализа), то нагревают их только в горячей воде, налитой в стеклянный стакан соответствующего размера (емкостью не больше 100 мл). Воронки служат для переливания - жидкостей, для фильтрования и т. д. Химические воронки выпускают различных размеров, верхний диаметр их составляет 35, 55, 70, 100, 150, 200, 250 и 300 мм. Обычные воронки имеют ровную внутреннюю стенку, но для ускоренного фильтрования иногда применяют воронки с ребристой внутренней поверхностью. Воронки для фильтрования всегда имеют угол 60° и срезанный длинный конец. При работе воронки устанавливают или в специальном штативе, или в кольце на обычном лабораторном штативе рисунок 5.3. Рисунок 5.3-Штатив с воронкой Для фильтрования в стакан полезно сделать простой держатель для воронки рисунок 5.4. Рисунок 5.4-Держатель для воронки Для этого из листового алюминия толщиной около 2 мм вырезают полоску длиной 70—80 мм и шириной 20 мм. На одном из концов полоски просверливают отверстие диаметром 12—13 мм и полоску сгибают так, как показано на рисунке 5.4. Как укрепить воронку на стакане, показано на рисунке 5.5. 11 Рисунок 5.5- Приспособление для крепления воронки на стакане При переливании жидкости в бутыль или колбу не следует наполнять воронку до краев. Если воронка плотно прилегает к горлу сосуда, в который переливают жидкость, то переливание затрудняется, так как внутри сосуда создается повышенное давление. Поэтому воронку время от времени нужно приподнимать. Еще лучше сделать между воронкой и горлом сосуда щель, вложив между ними, например, кусочек бумаги. При этом нужно следить, чтобы прокладка не попала в сосуд. Для аналитических работ при фильтровании лучше пользоваться аналитическими воронками рисунок 5.6. Рисунок 5.6- Аналитическая воронка Особенность этих воронок заключается в том, что они имеют удлиненный срезанный конец, внутренний диаметр которого в верхней части меньше, чем в нижней части; такая конструкция ускоряет фильтрование. Кроме того, бывают аналитические воронки с ребристой внутренней поверхностью, поддерживающей фильтр, и с шарообразным расширением в месте перехода воронки в трубку. Воронки такой конструкции ускоряют процесс фильтрования почти в три раза по сравнению с обычными воронками. 5.4 Посуда специального назначения Круглодонные колбы рисунок 5.7 -изготовляют из обыкновенного и из специального стекла. Все, что сказано об обращении с плоскодонными колбами, относится и к круглодонным; их применяют при многих работах. Некоторые круглодонные колбы имеют короткое, но широкое горло. Для нагревания круглодонных колб на голом пламени применяют асбестированные сетки с полушаровидным углублением. Круглодонные колбы, так же как и плоскодонные, бывают самой разнообразной емкости; со шлифом на горле и без него. 12 Круглодонные колбы удобно ставить в подставки из дерева, имеющие углубление рисунок 5.8. Применяют также подставки в виде колец разного диаметра, изготовленные из различных материалов, например из резины, резиновых трубок и др. Рисунок 5.7-Круглодонные Рисунок 5.8-Подставка для круглоколбы донных колб Эксикатор - это специальный сосуд, служащий для защиты предметов от поглощения влаги из воздуха. В нижней части эксикатора находится осушающее вещество. Эксикатор снабжен притертой крышкой, шлиф которой смазан вазелином. Для того чтобы открыть или закрыть крышку эксикатора, ее сдвигают в сторону. Если в эксикатор помещают сильно нагретый тигель, то не следует сразу плотно закрывать крышку, нужно слегка сдвинуть ее для выхода воздуха, а затем уже плотно закрыть.. Эксикаторы закрывают стеклянными крышками, края которых притерты к верхней части цилиндра. Различают два основных типа эксикаторов: обыкновенные рисунок 5.9 и вакуум-эксикаторы рисунок 5.10. Рисунок 5.9-Обыкновенный эксикатор Рисунок 5.10- Вакуум-эксикаторы Последние имеют отверстие, в которое на резиновой пробке вставляют трубку с краном или же в крышке имеется тубус с притертой пробкой, к которой припаяна стеклянная трубка с краном; это дает возможность соединять эксикатор с вакуум-насосом и, создавая внутри эксикатора уменьшенное давление, вести высушивание под вакуумом. Если в эксикатор ставят горячие тигли на фарфоровые вкладки рисунок 5.11, то вследствие нагревания воздуха крышка иногда приподнимается, при этом она может соскользнуть и разбиться. Рисунок 5.11- Фарфоровые вкладки для эксикаторов 13 Поэтому, поместив горячий тигель в эксикатор и накрыв его крышкой, ее некоторое время притирают, т. е. двигают вправо и влево. При остывании тигля внутри эксикатора создается небольшой вакуум и крышка держится очень плотно. Перенося эксикатор с места на место, необходимо придерживать крышку большими пальцами обеих рук рисунок 5.12, так как она может упасть и разбиться.Чтобы открыть эксикатор, нужно не поднимать крышку, а сначала сдвинуть ее в сторону, после чего она легко снимается рисунок 5.13. Для того чтобы облегчить снимание крышки с вакуум-эксикатора, рекомендуется помещать полиэтиленовую прокладку между фланцами крышки и эксикатора. Прокладка приклеивается к фланцу эксикатора вакуумной смазкой. Смазывать крышку не следует. В эксикаторе с такой прокладкой вакуум удерживается до 3 дней. Рисунок 5.12-Положение рук при переноске эксикатора Рисунок 5.13-Открывание эксикатора В качестве водопоглощающих средств для снаряжения эксикаторов применяют различные поглотители.Силикагель и окись алюминия(безводная). Для удобства наблюдения за состоянием адсорбентов к ним прибавляют немного хлористого кобальта. Поэтому безводне силикагель и окись алюминия окрашены в синий цвет, при поглощении влаги они приобретают розовую окраску. Насыщенные водой поглотители регенерируют нагрева нием: силикагеля при температуре не выше 200 0 С, окиси алюминия-не выше 175 0 С. Характеристики поглотителей, применяемых для снаряжения эксикаторов, приведены в таблице 5.1. Таблица 5.1-Поглатители для эксикаторов Высушивающее вещество Температура, С 0 Хлористый кальций СаСl2 Серная кислота Н2SО4 Силикагель SiО2 Оксид алюминия Аl2О3 Хлорнокислый барий Ва(СlО4)2 Гидроксид натрия NaОН Гидроксид калия КОН Оксид кальция СаО 25,0 25,0 30,0 30,5 30,5 30,5 30,5 30,5 14 Количество воды, остающееся в 1л воздуха, мг 0,3600 0,0300 0,0300 0,0050 0,8200 0,8000 0,0140 0,0030 Оксид бария ВаО 30,5 0,0007 Мерные цилиндры — стеклянные толстостенные сосуды с нанесенными на наружной стенке делениями, указывающими объем в миллилитрах рисунок 5.14. Они бывают самой разнообразной емкости: от 5—10 мл до 1 л и больше. Чтобы отмерить нужный объем жидкости, ее наливают в мерный цилиндр до тех пор, пока нижний мениск не достигнет уровня нужного деления. Иногда встречаются цилиндры, снабженные притертыми пробками. Обычно их применяют только лишь при специальных работах. Кроме цилиндров, для той же цели употребляют мензурки рисунок 5.15. Это сосуды конической формы, на стенке которых имеются деления. Они очень удобны для отстаивания мутных жидкостей, когда осадок собирается в нижней, суженной части мензурки. Рисунок 5.15-Мензурка а- обыкновенный; б-с притертой пробкой Рисунок 5.14-Мерные цилиндры Пипетки служат для точного отмеривания определенного объема жидкости. Различают пипетки для жидкостей и газовые пипетки. Пипетки для жидкостей рисунок 5.16. Обычные пипетки (пипетки Мора) представляют собой стеклянные трубки небольшого диаметра с расширением посредине. Пипетки служат для отмеривания и переноса точного объема раствора из одного сосуда в другой, они бывают двух видов: градуированные и с одной меткой (пипетки Мора) вместимостью от 1 до 100 мл. Градуированные пипетки менее точны, чем пипетки Мора. Существуют микропипетки вместимостью 0,1-0,2 мл. Пипетки калибруют на выливание. Объем свободно вытекающей жидкости, которой предварительно заполнена пипетка, является номинальным объемом. Согласно ГОСТ 29169-91, ISO 9002-94, ISO 835-81, ISO 648-77, пределы допускаемой погрешности номинальной вместимости пипеток не должны превышать значений, указанных в таблице 5.2. 15 Таблица 5.2-Допускаемые погрешности номинальной вместимости пипеток Вместимость, Допускаемая погрешность, см3, Допускаемая погрешность, см3 Для градуированных пипеток см3, для пипеток мора 1 ±0,01 ±0,015 2 ±0,02 ±0,02 5 ±0,05 ±0,03 10 ±0,1 ±0,04 20 ±0,06 25 ±0,06 50 ±0,1 100 ±0,15 В системе СИ объем выражают в кубических метрах или его кратных долях (см3, дм3). Однако мерная посуда и приборы для измерения объема, применяемые до настоящего времени в лабораториях, градуированные пипетки во внесистемных единицах — миллилитрах (мл) или литрах (л), поэтому в данном пособии оказалось более целесообразным выражать объем в этих единицах. Для наполнения пипетки нижний конец ее опускают в жидкость и втягивают последнюю при помощи груши или ртом, но лучше при этом пользоваться специальными приспособлениями. Засасывание жидкости нужно научиться делать отрывистыми сосательными движениями языка (или губами), но только не вдыхая воздух из пипетки (обычная ошибка начинающих). Проводя засасывание, нужно совершенно свободно дышать через нос и следить, чтобы кончик пипетки все время находился в жидкости. Жидкость набирают так, чтобы она поднялась на 2— 3 см выше метки, затем быстро закрывают верхнее отверстие указательным пальцем правой руки, придерживая в то же время пипетку большим и средним пальцами. Очень полезно указательный палец слегка увлажнить, так как влажный палец более плотно закрывает пипетку. Когда пипетка наполнена, ослабляют нажим указательного пальца, в результате чего жидкость будет медленно вытекать из пипетки; как только нижний мениск жидкости окажется на одном уровне с меткой, палец снова прижимают рисунок 5.17. Если на конце пипетки после этого будет висеть капля, ее следует осторожно удалить. Введя пипетку в сосуд, отнимают указательный палец и дают жидкости стечь по стенке сосуда. После того как жидкость вытечет, пипетку держат в течение еще 5 сек (считая до 5) прислоненной к стенке сосуда, слегка поворачивая вокруг оси, после чего удаляют пипетку, не обращая внимания на оставшуюся в ней жидкость. Выливание раствора из пипетки в коническую колбу показано на рисунок 5.18. Очень важно, чтобы раствор стекал именно по стенке конической колбы и не разбрызгивался, так как при этом часть выливаемого раствора мо- 16 жет попасть на стенку колбы и при последующем титровании не вступит в реакцию с раствором, выливаемым из бюретки. а- простая; б-градуированная Рисунок 5.16-Пипетки Рисунок 5.17Рисунок 5.18-Положение Выливание раствора пипетки при установлении из пинетки мениска на уровне метки Следует помнить, что объем жидкости, вытекающей из пипетки, зависит от способа вытекания и последний должен быть таким же, как и применяемый при калибровании пипеток. Поэтому, никогда не следует стремиться выгонять остатки жидкости из пипетки выдуванием или нагреванием рукой расширенной части пипетки. Для отмеривания малых объемов жидкостей применяют микропипетки емкостью 1, 2, 3 и 5 мм. Микропипетки часто градуируют, они имеют деления 0,01 мл, что позволяет делать отсчет с точностью 0,002—0,005 мл. Градуированной пипеткой можно отбирать не только один определенный объем жидкости (как обыкновенными пипетками), но любой в пределах ее емкости. Жидкость набирают в пипетку до нужной метки (нижний мениск жидкости находится на уровне последней) и затем выливают ее, как обычно. Пипетки должны быть всегда чисто вымытыми; их следует ставить в особый штатив рисунок 5.19 и закрывать сверху маленькими пробирками или куском чистой фильтровальной бумаги. 17 5.19-Штатив для хранения пипеток Если штатива в лаборатории нет, пипетки можно хранить в стеклянном цилиндре, на дно которого предварительно кладут несколько слоев чистой фильтровальной бумаги, вырезанной кружками; После работы пипетку ополаскивают несколько раз дистиллированной водой и помещают в стеклянный цилиндр, каждый раз заменяя верхний слой фильтровальной бумаги свежим. Следует помнить! Обычными пипетками нельзя отмеривать жидкости, вязкость которых заметно отличается от вязкости воды, например концентрированные кислоты, щелочи и т. п., так как объем отобранной жидкости не будет соответствовать указанному. Для отбора таких жидкостей пользуются специально прокалиброванными пипетками. При обращении со всеми видами пипеток нужно обязательно придерживаться следующих правил: 1. Пипетка при отборе жидкости всегда должна находиться в строго вертикальном положении. 2. При установке нижнего мениска на уровне черты глаз наблюдателя должен быть расположен в одной плоскости с меткой (метки на передней и задней стенках должны при этом сливаться в одну). Бюретки применяют при титровании, для измерения точных объемов. Объемные бюретки. Это — стеклянные трубки с несколько оттянутым нижним концом или снабженные краном. На наружной стенке по всей длине бюретки нанесены деления в 0,1 мл, так что отсчеты можно вести с точностью до 0,02 мл. Б ю р е т к и представляют собой цилиндрические трубки с суженным концом, к которому при помощи резиновой трубки присоединена оттянутая стеклянная трубочка указанная на рисунке 5.20 б, г. Для титрования растворами веществ, которые разрушают резину, используют бюретки со стеклянными кранами указанными на рисунке 5.20 а. Бюретку закрепляют строго вертикально рисунок 20 д в штативе и заполняют раствором титранта до уровня, превышающего нулевую отметку. Наполняют бюретку через воронку. Необходимо внимательно следить за тем, чтобы в бюретке и ее нижней узкой трубке ( к а п и л л я р е ) не оставалось пузырьков воздуха. Для их удаления отгибают капилляр кверху как показано на рисунке 5.20 г и, подставив под него пустую коническую колбу или стакан, выпускают жидкость до тех пор, пока весь воздух не будет удален. Воронку обязательно снимают, после чего устанавливают уровень жидкости в бюретке на нулевое деление. Если воронку не снять, то во время титрования с н е е м о г у т с те ч ь о с та в ши е с я к а п л и р а с тв о р а , и и з м е р е н и е о б ъ е м а о к а ж е т с я н е то ч н ым . Уровень прозрачных растворов устанавливают по нижнему краю мениска, а непрозрачных - по верхнему краю. 18 абв г д Рисунок 5.20- Бюретка с краном (а); зажимом (б); оливой (в); удаление воздуха из носика бюретки (г); правильно собранная установка для титрования Бюретки и правила работы с ними (д) Бюретки применяются для измерения точных объемов при титровании при других операциях. Все они предназначаются для измерения вылитой из них жидкости, поэтому калиброваны на выливание. Существуют макро- и микробюретки. Употребляемые в макроанализе бюретки на 50 мл отградуированы на миллилитры и доли миллилитра с ценой наименьшего деления 0,1 мл, а бюретки на 25 мл отградуированы либо аналогично, либо с ценой деления 0,05 мл. Отсчет сотых долей миллилитра производится на глаз с точностью, не большей, чем половина цены деления. Микробюретки имеют вместимость 1, 2, 5, 10 мл с ценой наименьшего деления 0,01-0,02 мл. Бюретки изготавливают в соответствии с ГОСТ 29251-91, ISO 9002-94, ISO 385-84. Пределы погрешности для бюреток 2-го класса точности вместимостью 25 и 50 см при температуре 20°С не должны превышать ±0,1 см . После охлаждения отрезают кусок длиной 8 мм, для этого проводят на палочке черту, помещают палочку в отверстие в пробке до черты и отламывают. Острые края в месте излома проще всего сгладить напильником. После этого отрезанный кусок вставляют в резиновую трубку закругленным концом вниз.Для наполнения бюретки раствором сжимают то место резиновой трубки, куда заложена бусина. Мерные колбы —необходимейшая посуда для большинства аналитических работ рисунок 5.21; они представляют собой плоскодонные колбы различной емкости; в большинстве случаев мерные колбы имеют пришлифованные стеклянные пробки. Однако часто применяют мерные колбы без пришлифованных стеклянных пробок. В таких случаях для закрывания мерных колб используют пробки из полиэтилена и полипропилена соответствующего размера. 19 Рисунок 5.21- Мерные колбы Мерные колбы применяют для приготовления стандартных растворов, точного отмеривания объемов, разбавления растворов и т. п. Мерные колбы изготавливают вместимостью 5-2000 мл и калибруют на вливание. На колбе указываются номинальный объем, температура калибрования и класс точности. Мерные колбы изготавливают в соответствии с ГОСТ 1770-74, ISO 1042-83, ISO 4788-80. Их допускаемые погрешности от номинальной вместимости при температуре 20 0С для 2-го класса точности не должны превышать указанных в таблице 5.3. Таблица 5.3-Допускаемые погрешности номинальной вместимости мерных колб Вместимость мерной колбы, см3 Допускаемая погрешность, см3 25 ±0,08 50 ±0,12 100 ±0,20 Различают узкогорлые и широкогорлые мерные колбы. Диаметр горла последних приблизительно в полтора раза больше по сравнению с узкогорлыми. На горле колбы имеется кольцевая метка, а на самой колбе вытравлено число, указывающее ее емкость в миллилитрах при определенной температуре. Приведенная емкость означает, что при данной температуре объем воды, налитой в колбу до метки, точно соответствует указанному. Объем вылитой из колбы воды будет несколько меньше помеченного, так как часть ее останется на стенках. Поэтому обычные мерные колбы не пригодны для отмеривания точного объема воды с последующим выливанием ее. Мерные колбы, предназначенные для выливания, имеют две метки. Верхняя метка предназначена «для выливания», т. е. если наполнить колбу до этой метки и вылить содержимое, вылитая жидкость будет иметь объем, указанный иа колбе. Мерные, колбы служат для разбавления всякого рода растворов до определенного объема или же для растворения какого-нибудь вещества в определенном объеме соответствующего растворителя. Мерные колбы всегда должны быть чисто вымыты. Когда минует надобность в находящемся в мерной колбе растворе, последний должен быть тотчас вылит, а колба, вымыта. При хранении пустой колбы во избежание «заедания» стеклянной пробки последнюю, обернув фильтровальной или чистой писчей бумагой, вставляют в горло колбы. При работе бумагу, конечно, снимают. Если в мерной колбе готовят какой-либо раствор, то вначале насыпают или наливают через воронку растворяемое вещество и остатки его в воронке тщательно, без потерь, смывают небольшими порциями воды. Затем наполняют колбу до половины водой, осторожно встряхивая, перемешивают ее содержимое до полного растворения и доливают воду, как указано выше. При пересыпании через воронку измельченных твердых веществ следует применять только сухую воронку, причем высыпать всю навеску сразу не рекомендуется. Лучше высыпать понемногу, слегка встряхивая воронку легкими ударами пальцев. При быстром высыпании всей навески может случиться, что 20 порошок застрянет в трубке воронки и перевести его в колбу будет труднее. Никогда не следует начинать обмывание воронки прежде, чем вся навеска из нее не высыпается в колбу. Для введения в мерную колбу измельченных веществ удобно применять химическую воронку с укороченным концом. Воду или другую жидкость наливают в мерную колбу до тех пор, пока нижний мениск не достигнет уровня метки. Добавление последних капель жидкости затруднительно, то сперва наливают ее на 0,1—1 мл ниже метки, после чего доводят до метки, добавляя жидкость по каплям рисунок 5.22. Рисунок 5.22- Добавление последних капель в мерную колбу Следует помнить! что раствор в мерной колбе нужно перемешивать очень осторожно многократным переворачиванием. Прежде всего следует убедиться, прочно ли закрыта колба и не будет ли при переворачивании ее вытекать жидкость. Мерную колбу можно держать только за горлышко, придерживая большим и средним пальцами правой руки, одновременно прижимая пробку указательным пальцем. Совершенно недопустимо держать мерную колбу за шар, так как это вызывает нагревание колбы с жидкостью и изменение объема последней. Начинающим работать в лаборатории рекомендуется вначале попрактиковаться наливать в мерную колбу воду. 5.5 Фарфоровая посуда Ассортимент фарфоровой посуды, применяемой в обычных лабораториях, не так многочислен, как стеклянной. Фарфоровая посуда имеет ряд преимуществ перед стеклянной: она более прочная, не боится сильного нагревания, в нее можно наливать горячие жидкости, не опасаясь за целость посуды, и т. д. Недостатком изделий из фарфора является то, что они тяжелы, непрозрачны и значительно дороже стеклянных. Стаканы — тех же видов и емкостей, что и стеклянные. Выпарительные чашки широко применяются в лабораториях. Они бывают самых разнообразных емкостей, с диаметром от 3—4 до 50 см и больше. Фарфоровые выпарительные чашки с носиком выпускаются следующих размеров: Емкость, мл 28,8 65,0 140,0 311,0 471,0 1010,0 2106,0 4600,0 Высота, мм 56 72 93 120 156 202 260 366. 21 Чашки служат для выпаривания разного рода растворов; хотя фарфоровые чашки можно нагревать на голом пламени. Тигли фарфоровые сосуды с фарфоровыми крышками. Тигли для прокаливания рисунок 5.23. В тиглях прокаливают разного рода вещества, сжигают органические соединения при определении зольности и т. д. В большинстве случаев нагревание тиглей проводят прямо на горелке без применения асбестированных сеток или бань. Для нагревания тигля его нужно ставить в фарфоровый треугольник рисунок 5.24. Последний делают из трех насаженных на проволоку фарфоровых трубок. Подогрев ведут постепенно. Вначале тигель нагревают над пламенем горелки (только горячим воздухом), затем постепенно его вводят в бесцветное пламя горелки и, наконец, помещают в ту или иную зону пламени в зависимости от требуемой температуры прокаливания. При этом рекомендуется с самого начала нагревания укрепить тигель на такой высоте, на которой он должен находиться в последний наиболее длительный период прокаливания. Вначале же, держа горелку в руке, регулируют расстояние пламени от дна тигля. Такой способ подогрева в особенности важен при сжигании органических веществ. В большинстве случаев работы с тиглем последний должен быть закрыт крышкой на все время работы. Для наблюдения за ходом прокаливания или сжигания крышку периодически снимают при помощи тигельных щипцов или пинцета. После окончания прокаливания или сжигания горелку отставляют или гасят, дают тиглю остыть некоторое время, а затем помещают его в эксикатор. Рисунок 5.23- Фарфоровый тигель Рисунок 5.24-Фарфоровый треугольник для тиглей Фарфоровые тигли можно нагревать до температуры не выше 1200° С; такую температуру возможно получить, если прокаливание вести в муфельной печи. В фарфоровом тигле нельзя проводить сплавление с щелочным веществом, например с углекислым натрием, а также работать с фтористоводородной кислотой, так как фарфор при этом разрушается. Следует помнить, что новые, еще не разу не использованные тигли полезно предварительно промыть и прокалить. Это необходимо потому, что при использовании новых фарфоровых тиглей, например для озоления природных органических веществ с целью количественного определения в их золе кальция, всегда получаются повышенные результаты. Это объясняется тем, что кальций из тигля переходит в золу, причем в зависимости от метода озоления (с применением окислителей или без них) ошибка может достигать 3—4 мг. Для того чтобы уменьшить ошибку и 22 сделать ее постоянной, для подобных работ лучше использовать фарфоровые тигли, длительное время бывшие в употреблении, предварительно прокипятив их последовательно в разбавленной соляной кислоте (1 : 1), в 5 н. растворе NaOH и в дистиллированной воде. Таким же путем обрабатывают новые тигли. Когда приходится работать с большим количеством тиглей, их необходимо предварительно переметить или пронумеровать специальной огнестойкой краской. При проведении массовых анализов бывает необходимым прокаливать одновременно несколько тиглей, например 8—10 штук. В подобных случаях следует применять подставки, рассчитанные на прокаливание одновременно до 10 тиглей. Эти подставки изготовляют из жароупорных материалов. Из металлов для этой цели пригоден никель и жароупорные стали, из других материалов — огнеупорные глины, шамот и т. п. Подставку можно смонтировать также из фарфоровых трубок и толстой нихромовой проволоки. Каждое гнездо для тигля должно иметь предохранительное устройство из проволоки в форме треугольника. Прокаливаемые тигли помещают именно в эти треугольники. Размеры подставок по высоте должны быть такими, чтобы в зоне устойчивой температуры печи 850±25°С расстояние от дна тигля до пода муфельной печи было около 20 мм. Тигли, только что вынутые из муфельной печи или снятые с горелки, нельзя ставить на деревянную, линолевую или пластмассовую поверхность стола или вытяжного шкафа. Около муфельной печи нужно положить кирпич из шамота, керамическую плитку, на которые помещают раскаленные тигли. После того как тигель немного остынет и исчезнет красный цвет раскаленного фарфора, тигель ставят в эксикатор для полного охлаждения. Для получения правильных результатов анализа очень важным является продолжительность охлаждения фарфоровых тиглей в эксикаторе. В случае, когда эксикатор заполнен тиглями, охлаждение их до момента взвешивания должно проводиться не менее 2 ч, так как при меньшем охлаждении возникает ошибка из-за разницы температуры весов и тиглей. Чтобы свести ошибку до минимума (0,16 мг), тигли в эксикаторе необходимо охлаждать не менее 1 ч, даже когда в эксикаторе находятся только два тигля. Если тигли выдерживать в эксикаторе 25—40 мин, как это обычно рекомендуют, разница в температуре весов и тиглей достигает 10° С, а ошибка взвешивания составляет 2—3 мг. Сократить время охлаждения тиглей можно: 1) охлаждением их на воздухе перед помещением в эксикатор; 2) уменьшением количества тиглей, одновременно устанавливаемых в эксикаторе, 3) выдерживанием тиглей в витрине весов перед взвешиванием. Ложки-шпатели рисунок 5.25 применяют в химических лабораториях для отбора вещества, для снятия осадков с фильтров и т. п, Лодочки для прокаливания. Фарфоровые лодочки для прокаливания веществ при анализе рисунок 5.26 бывают различных размеров. Их не покрывают глазурью. На одном бортике лодочки имеется кольцо, за которое можно зацепить крючком при вытаскивании лодочки из печи. 23 Рисунок 5.25-Фарфоровая ложкаРисунок 5.26-Фарфоровая лодочка для шпатель прокаливания Фарфоровые трубки, применяемые для лабораторных целей, также не бывают покрыты глазурью. Они имеют различные диаметры — от 2 до 50 мм и больше. Тонкие трубки применяют как изоляторы проводов и для приготовления термопар. В последнем случае часто пользуются трубками с двумя каналами небольшого диаметра. Более широкие трубки выдерживают температуру до 1200° С, их применяют в качестве реакторов при синтезах Ниже перечислены наиболее употребительные инструменты и материалы, которые полезно иметь в лабораториях. Ножницы. Ножи — желательно иметь минимум два ножа: один малый, перочинный, и один большой. Молоток. Стальная щетка (кордовая) — для чистки металлических предметов Проволока — нужно иметь небольшой запас звонковой, железной, медной и алюминиевой проволоки, жилки от электрического шнура и немного самого шнура. 5.6 Металлическое оборудование В лабораториях широко применяют разнообразное металлическое оборудование, преимущественно стальное рисунок 5.27. 1-лапки малые; 3, 4 — лапки большие; 5, 6, 7 — кольца; 8 — вилка; 9муфты для лапок и колец Рисунок 5.27-Железный штатив 24 Штатив представляет собой стальной стержень, укрепленный на тяжелой стальной подставке, чаще всего имеющей форму четырехугольника. Обычно стержень укрепляют почти у самого края меньшей стороны подставки Пинцеты рисунок 5.28 служат для взятия небольших предметов. Например, пинцетами следует пользоваться при работе с металлическим натрием, при работе с разновесом, чтобы не касаться его руками Тигли металлические бывают медные, чугунные, стальные, из чистого никеля, из чистого серебра, платиновые и из сплавов платины, из чистого золота. Все они применяются при разного рода химических анализах, исследовательских работах и пр. Рисунок 5.28-Пинцеты Рисунок 5.29-Тигельные типцы Чашки металлические. Для выпаривания многих растворов применяют чашки из платины, золота и других металлов. Обращение с ними то же, что и с тиглями. Они бывают различного диаметра и емкости. а-деревянный; б-металлический Рисунок 5.30-Чашка металлическая Рисунок 5.31- Держатели для пробирок: Держатели для пробирок бывают металлические и деревянные рисунок 5.31. Держателями пользуются при нагревании пробирок. Следует помнить, что за лабораторными металлическими предметами следует постоянно следить и предохранять их от ржавления. Поэтому, например, штативы, муфты, лапки следует иногда, хотя бы раз в год, покрывать специальным негорючим черным лаком. Такие предметы как треноги, зажимы, тигельные щипцы рисунок 5.31, пинцеты, металлические тигли, которые нельзя лакировать, следует очищать от ржавчины. Чистить можно наждачной бумагой разных номеров (в зависимости от назначения предмета) или песком. 5.7 Электрическое оборудование Электропечи лабораторные. Электропечь лабораторная SNOL 8,2/1100 представленная рисуноке 5.32 предназначена для термообработки веществ при температуре от 50 до 1100°С. 25 Рисунок 5.32-Электропечь лабораторная Работа с ней требует предельной собранности, осторожности и соблюдения всех правил безопасностиво избежание получения термических ожогов. Студенты могут пользоваться печью только после обучения приемам безопасной работы и под контролем преподавателя. Печь включается нажатием тумблера на передней панели, при этом загорится сигнальная лампа. Управление температурным режимом производится с помощью кнопок «больше» или «меньше», расположенных на пульте управления. Нажимая на них, устанавливают на нижнем дисплее необходимую температуру. На верхнем дисплее высвечивается значение текущей температуры в камере электропечи. Следует помнить,что после окончания работы необходимо отключить печь нажатием тумблера. Весы лабораторные электронные представленные на рисунке 5.33 а,б это точные измерительные приборы, предназначенные для статического взвешивания материалов. Принцип действия весов основан на компенсации веса груза электромагнитной силой, которая создается системой автоматического уравновешивания. б-технические а-аналитические Рисунок 5.33- Весы В зависимости от требуемой точности в лабораториях используют аналитические указанные на рисунке 5.33, а) или технические на рисунке 5.33, б) весы. Погрешность взвешивания на аналитических весах составляет ±0,0001 г, предельная нагрузка - 210 г. Аналитические весы имеют защитный кожух Погрешность взвешивания на технических весах составляет ±0,01 г, предельная нагрузка - 510 г. 26 Для обеспечения воспроизводимости результатов взвешивания весы должны стоять ровно и устойчиво. Горизонтальное выравнивание весов проводится по встроенному уровню вращением двух задних ножек. При этом пузырек воздуха устанавливается по центру встроенного уровня между двумя концентрическими окружностями представленными на рисунке 5.34. Правильное положение пузырька воздуха Рисунок 5.34- Горизонтальное выравнивание весов по встроенному уровню Включение весов осуществляется кратковременным нажатием клавиши «ON/ OFF». На дисплее появится индикация массы: «0,00» (технические весы) или «0,0000» (аналитические весы). Для выключения следует нажать и удерживать клавишу «ON/ OFF»до появления на дисплее индикации «OFF». Правила работы с весами 1. Не нагружать весы выше предельной нагрузки. 2. Не ставить на чашку весов теплые предметы. 3. Не облокачиваться на стол, на котором установлены весы. 4. Взвешиваемый предмет помещать на центр чашки весов. 5. Взвешивать вещества в чистой, сухой таре ( бюксы, тигли) . 6. Нельзя помещать вещества непосредственно на чашку весов или взвешивать их на кусочке бумаги. 7. Дверцы аналитических весов во время взвешивания должны быть закрыты. 8. При выполнении лабораторной работы все взвешивания нужно производить на одних и тех же весах. 9. Нельзя подсыпать и отсыпать вещество и непосредственно на аналитических весах. 27 6 ЛАБОРАТОРНЫЙ ПРАКТИКУМ ЛАБОРАТОРНАЯ РАБОТА 1-ВЗЯТИЕ НАВЕСКИ МАТЕРИАЛА ДЛЯ ОПРЕДЕЛЕНИЯ ПОТЕРЬ ПРИ ВЫСУШИВАНИИ Цель работы: определение влажности материала. Оценка правильности полученных результатов Материалы и оборудование: Материалы: исследуемое вещество (глина). Оборудование: аналитические весы, бюкс, щипцы, эксикатор, сушильный шкаф. I. Теоретическая часть. Гигроскопичность это способность материала поглощать и конденсировать влагу из окружающего воздуха. Оценивается влажностью. Влажность – это содержание влаги в материале в данный момент времени. Гигроскопическая вода (влага) - это вода, которая адсорбируется из воздуха частицами твердого вещества. Содержание ее в веществе непостоянно, оно изменяется при изменении температуры и влажности воздуха. Изменение количества гигроскопической воды влияет на массовые доли всех других составных частей вещества. Для устранения колебаний состава вещества в зависимости от колебаний влажности результаты анализа веществ, содержащих заметные количества гигроскопической влаги, пересчитывают на абсолютно сухое вещество. Для этого предварительно определяют содержание гигроскопической воды - влажность в испытуемом образце. Такое определение выполняют при анализе самых разнообразных материалов (глины,гипс др.). Высушивание проводят при температуре 105-110 0С. II. Методика выполнения работы: 1. Хорошо моют бюкс, насухо вытирают его снаружи полотенцем и помещают на 30 минут в сушильный шкаф при 105-110 оС. Горячий бюкс охлаждают в эксикаторе. Взвешивают бюкс на аналитических весах. Результаты взвешивания записывают в тетрадь. После первого взвешивания бюкс вновь ставят в сушильный шкаф на 20 минут при той же температуре. Охладив бюкс в эксикаторе, снова взвешивают и записывают результат. Если масса бюкса не изменяется или изменяется незначительно (не более чем на ± 0,0002 г), высушивание считается законченным. 2. Высушенный и взвешенный бюкс насыпают 2-3 грамма глины, взвешивают его и записывают в тетрадь массу бюкса с веществом. 3. Бюкс с веществом ставят на 1,5 часа в сушильный шкаф. Температура в шкафу должна быть 105-110 оС. 4. Бюкс охлаждают в эксикаторе и взвешивают. Высушивание повторяют при тех же условиях в течение 30 минут и после охлаждения в эксикаторе 28 вновь взвешивают бюкс с веществом. Высушивание повторяют до тех пор, пока масса бюкса с веществом не будет постоянной (разница не более ± 0,0002г). ПРОТОКОЛ АНАЛИЗА Взвешивание глины до высушивания: Масса бюкса после первого высушивания-_________, г; Масса бюкса после второго высушивания-__________, г; Масса бюкса после третьего высушивания-__________, г; Постоянная масса бюкса-________, г; Масса бюкса с навеской-_________, г; Масса глины-______________, г; Взвешивание глины после высушивания: Масса бюкса с навеской после первого высушивания-__________, г; Масса бюкса с навеской после второго высушивания-__________, г; Масса бюкса после третьего высушивания-___________, г; Масса бюкса после четвертого высушивания-_________, г; Постоянная масса бюкса с глиной-____________, г; III. Расчетная часть: По формуле 1.1 расчитываем процентное содержание влажности вещества %вл= 𝑚0− 𝑚1 𝑚0 ∙ 100, (1.1) где % вл-процентное содержание влажности вещества,% m0-масса навески до высушивания, г; m1-масса навески после высушивания, г; m0-______, г; m1-_______, г. %вл = − ∙100% =__ % Ответ IV. Заключение: Полученные результаты по влажности (не) входят в стандартные значения. Подпись преподавателя:_____________ Вопросы для самоконтроля 1. Что такое «постоянный вес»? 2. Для чего бюкс доводится до постоянного веса? 3. Как определяют содержание влаги в анализируемом образце? 4. Что такое влажность для чего ее определяют? 5. Почему взвешивание навески образца до и после высушивания проводят в бюксе с закрытой крышкой? 29 ЛАБОРАТОРНАЯ РАБОТА 2-ОПРЕДЕЛЕНИЕ ПОТЕРЬ ПРИ ПРОКАЛИВАНИИ Цель работы: изучить методику определения потерь при прокаливании (ППП).Закрепить навыки пользования аналитическими весами и приобрести навыки работы с муфельной печью. Материалы и оборудование: Материалы: исследуемое вещество глина. Оборудование: аналитические весы, тигель, щипцы, эксикатор, муфельная печь. I. Теоретическая часть. Потери при прокаливании (П.П.П .). При прокаливании глин до 900° С из них удаляются химически связанная вода, углекислота карбонатов, выгорают органические примеси и сера. В глинах с незначительным содержанием органических веществ и обычным количеством. Примесей п. п. п. зависят в основном от присутствия в них глинистого вещества. В связи с этим по потере при прокаливании, которая определяется быстро и легко, можно косвенно судить о количестве каолинита. П.П.П (%) определяют весовым методом на пробе массой 1 г, предварительно высушенных при 105 — 110°С. Газы образуются при испарении конституционной воды, сгорании органических веществ, разложения карбонатов II. Методика выполнения работы: 1. Хорошо моют и вытирают полотенцем тигель. Помещают его на 20 минут в муфельную печь t=1000 оС. Затем тигель охлаждают в эксикаторе и взвешивают, после чего снова помещают в печь на 10 минут при той же температуре. Такую операцию повторяют до тех пор, пока масса тигля не будет постоянной. 2. В доведенный до постоянной массы тигель, насыпают предварительно высушенное исследуемое вещество 1-2г. и точно взвешивают на аналитических весах. Тигель с навеской ставят в муфельную печь на 2 часа t=1000 оС. Затем тигель с навеской охлаждают в эксикаторе и взвешивают. Прокаливание повторяют при тех же условиях в течение 30 мин. и после охлаждения вновь взвешивают. Такую операцию повторяют до тех пор, пока масса тигля с навеской не будет постоянной. ПРОТОКОЛ АНАЛИЗА Взвешивание исследуемого вещества до прокаливания: Масса тигля после первого прокаливания-_________, г; Масса тигля после второго прокаливания-_________, г; Масса тигля после третьего прокаливания-_________, г; Масса тигля постоянная-_________, г; Масса тигля с навеской-__________, г; 30 Масса навески-___________, г; Взвешивание исследуемого вещества после прокаливания: Масса тигля с навеской после первого прокаливания-__________, г; Масса тигля с навеской после второго прокаливания-__________, г; Масса тигля с навеской постоянная-_________, г; Масса тигеля с навеской постоянная-________, г; Масса прокаленного остатка-___________, г; III. Расчетная часть: По формуле 2.1 определяем процентное содержание петерь при прокаливании %ППП = 𝑚сух.н −𝑚прок 𝑚сух.н ∙100, (2.1) где mсух.н.-масса сухой навески, г; mпрок-масса прокаленной навески, г; mсух.н.=________,г; mпрок=_______, г. %ппп= − ∙ 100% = ________ % Ответ IV. Заключение: Полученные результаты по процентному содержанию петерь при прокаливании (не) входят в стандартные значения Подпись преподавателя:_____________ Вопросы и задачи для самоконтроля 1. Какую цель преследует прокаливание до постоянной массы пустого тигля и тигля с навеской? 2. Почему вес прокаленного осадка меньше высушенного при 105 0С? Задача 1. Определите содержание оксида кремния, если известно масса тигля с осадком 2г, масса пустого тигля 0,83 г исходная навеска при сплавлении 1,8г. Задача 2. Определите потери после прокаливания, если масса пробы до прокаливания была 1,5г , масса навески после 1г. Сколько процентов потери? Задача 3.Сколько кирпича получится из 2,5 м3 глины,если средняя плотность кирпича равна 1700 кг/м3, насыпная плотностькарьерной глины 1600 кг/м3, влажность глины 12 %, потери при обжиге (потери при прокаливании) – 8 % от массы сухой глины. 31 ЛАБОРАТОРНАЯ РАБОТА 3-ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ СЕРНОГО АНГИДРИДА МЕТОДОМ ОСАЖДЕНИЯ ХЛОРИДА БАРИЯ Цель работы: Научиться применять метод осаждения для определения массы вещества в растворе путем получения в качестве осаждаемой формы кристаллического осадка и прокаливания последнего до постоянной массы Приобрести навыки растворения, осаждения, декантации, прокаливания. Материалы и оборудование: Материалы и реактивы: исследуемое вещество, дистиллированная вода, 2 нормальная соляная кислота, фильтр, 0,2 н. хлорид бария. Оборудование: аналитические весы, тигель, щипцы, эксикатор, муфельная печь. I. Теоретическая часть. Осаждение проводят для выделения того или иного компонента образца из раствора в виде малорастворимого соединения. Осаждение считают к о л и ч е с т в е н н ым в том случае, если остаточная концентрация иона в растворе не превышает 10-6 моль/л. Осадитель приливают в стакан с раствором по палочке, перемешивая раствор после добавления каждой порции. Потом проверяют п о л н о ту о с а жд е н и я: дают осадку собраться на дне стакана и к прозрачному раствору ( ф и л ь тр а ту ) добавляют несколько капель осадителя, наблюдая, не появится ли муть в местах падения этих капель. Если муть не появляется, то можно считать, что полнота осаждения достигнута. Фильтрование и промывание осадка проводят для отделения осадка от раствора и очистки его от адсорбированных примесей. А м о р ф н ые о с а дк и отфильтровывают через 5-10 мин после осаждения, дав осадку собраться на дне стакана. Отделять осадок от раствора можно с помощью ф и л ьтр у ю щи х ти г л е й или ф и л ь т р о в а л ь н о й б у м а г и . В гравиметрии чаще всего применяют специальные бумажные фильтры, которые называются б е з з о л ьн ым и . После сжигания фильтра остается зола, масса которой мала и указана на упаковке, поэтому при необходимости в результат взвешивания можно внести поправку. Размер фильтра выбирают не по объему жидкости, которую нужно профильтровать, а по объему осадка - он должен занимать не более половины сложенного конусом фильтра. Чаще всего употребляются фильтры, имеющие диаметр 6, 9 и 12 см. Подготовка воронки с фильтром для фильтрованияуказана на рисунке 3.1. Выбранный фильтр перегибают по диаметру пополам, затем полученный полукруг перегибают еще раз пополам (рисунок 3.1а). После этого разворачивают фильтр, чтобы образовался конус (рисунок 3.1б), и вставляют его в воронку (рисунок 3.1в). 32 а - складывание фильтра б- конус в - подготовленная к работе воронка с фильтром Рисунок 3.1- Подготовка воронки с фильтром для фильтрования Смачивают фильтр дистиллированной водой и осторожно прижимают его края к стенкам воронки так, чтобы фильтр плотно, без зазоров прилегал к ней. Край фильтра должен быть н и ж е к р а я в о р о н к и на 5-8 мм. Воронку с фильтром вставляют в кольцо штатива. Под нее подставляют стакан или коническую колбу для сбора фильтрата так, чтобы носик воронки касался внутренней стенки стакана. После подготовки и установки в кольцо воронки с фильтром можно приступать к фильтрованию методом д е к а н та ц и и . Осадок должен находиться на дне стакана, его не следует взмучивать. Если взмутить осадок, то после внесения на фильтр первых порций жидкости с осадком, фильтрование сильно замедлится, так как частицы осадка забьют поры фильтра. Стакан с осадком подносят к воронке, осторожно вынимают палочку из стакана, чтобы ни одна капля раствора не попала мимо фильтра. Ставят палочку почти вертикально над воронкой в той части фильтра, где он сложен втрое ( п а л о ч к а н е до л ж н а к а с а тьс я ф и л ь тр а ! ) , подносят стакан и по палочке сливают жидкость на фильтр рисунок 3.2. Уровень жидкости на фильтре должен быть на 4-5 мм н и ж е е г о к р а я . Стеклянная палочка должна быть или в руке над воронкой, или стакане. Н е л ьз я к л а с ть е е н а с то л ! Рисунок 3.2-Фильтрование После этого приступают к п р о м ыв а н и ю осадка методом декантации. Наливают в стакан промывную жидкость, перемешивают осадок палочкой, 33 дают ему отстояться несколько минут. Затем прозрачную жидкость сливают по палочке на фильтр, оставляя основную часть осадка в стакане. Операцию повторяют несколько раз. После каждой промывки проверяют п о л н о ту п р о м ыв а н и я осадка. Для этого в пробирку отбирают несколько капель промывной жидкости, вытекающей из воронки, и проводят качественную реакцию на отмываемый ион. Промывку прекращают только в случае отрицательной реакции. После этого с помощью небольших порций промывной жидкости, взмучивая осадок и не давая ему отстаиваться, переносят его на фильтр. Для п е р е н е с е н и я н а ф и л ь тр осадка, оставшегося на стенках стакана и палочке, поступают следующим образом. В стакан наливают промывную жидкость небольшими порциями и сдвигают в нее осадок со стенок стакана резиновым наконечником стеклянной палочки. Затем ополаскивают палочку промывной жидкостью над стаканом, берут четвертинку беззольного фильтра и протирают им палочку и стакан, снимая частицы осадка. Потом этот кусочек фильтра с частицами осадка присоединяют к собранному на фильтре основному осадку. После этого фильтр с осадком и з в л е к а ю т и з в о р о н к и . С помощью стеклянной палочки отделяют край фильтра от стенок воронки в той части, где он сложен в три слоя (рисунок 3.3, а), и загибают их над осадком, полностью закрывая последний (рисунок 3.3, б). Пакетик с осадком извлекают из воронки, складывают, как показано (на рисунке 3.3,в ) , помещают в фарфоровый тигель (рисунок 3.5 г) и озоляют. а - отделение фи- б - извлечение фильтра от края во- льтра из воронки ронки в - складывание фильтра с осадком г - перенос фильтра с осадком в тигель Рисунок 3.3- Перенос фильтра с осадком в тигель Для фильтрования осадков, которые разлагаются при высокой температуре, Озоление и прокаливание проводятся с целью перевода осаждаемой формы в гравиметрическую. Фильтр с осадком о з о л я ют при температуре 400 °С в э л е к тр о п е ч и . При этом бумага превращается в золу, минуя стадию горения. Бумага не должна гореть, поскольку пламя может унести частицы осадка. Когда бумага полностью обуглится, приступают к п р ок а л и в а н и ю осадка при более высокой температуре. Затем тигель с помощью тигельных щипцов переносят в эксикатор. тигель захватывают щипцами за края, а не обхватывают его. после охлаждения тигля до комнатной температуры его взвешивают 34 Затем повторяют прокаливание в течение 30 мин и помещают тигель в эксикатор, ждут, пока он не охладится до комнатной температуры, и вновь взвешивают. Операцию повторяют до тех пор, пока два последних взвешивания не будут отличаться друг от друга не более чем на 0,0002 г. Такая операция называется п р о к а л и в а н и е м до п о с то я н н о й м а с с ы . В процессе работы тигель с осадком должен находиться либо в печи, либо в эксикаторе. Хранить его на воздухе недопустимо! Тигель вынимают из эксикатора только для взвешивания. II. Методика выполнения работы: 1. Подготовка раствора к анализу. Навеску сульфата 0,15-0,2 г. взятую на аналитических весах растворяют в 100 мл. (50 мл.) дистиллированной воды в хим. стакане емкостью 250 мл. (100 мл.). К полученному раствору приливают 3 мл. 2 н. соляной кислоты. 2. Приготовление раствора осадителя. В другой хим. стакан наливают 5 мл. 0,2 н. раствора хлорида бария. 3. Осаждение. Подготовленный раствор сульфата нагревают до кипения (но не кипятят) на электроплитке. К горячему раствору сульфата прибавляют горячий раствор 0,2 н. хлорида бария 5 мл. медленно по каплям. Полученный раствор с осадком кипятят не более 10 мин. Дают осадку осесть из горячего раствора и проверяют полноту осаждения раствором хлорида бария. Для этого осторожно прибавляют в раствор 2-3 капли осадителя (хлористого бария), если в месте падения капель осадителя не образуется мути (допускается легкое взмучивание осадка со дна стакана) осаждение считается законченным. Na2SO4+BaCl2=BaSO4+2NaCl 4. Промывание и фильтрование осадка Через несколько часов с отстоявшегося осадка сливают прозрачный раствор через плотный фильтр (синяя лента). Осадок в стакане промывают несколько раз декантацией дистиллированной холодной водой, каждый раз фильтруя промывную воду. Осадок из стакана количественно переносят на фильтр. Промывают на фильтре 2 раза 1% раствором нитрата аммония. Фильтр с осадком, не вынимая из воронки, подсушивают в сушильном шкафу при t=100-105 оС. 30 мин. Слегка влажный фильтр с осадком осторожно вынимают из воронки, завертывают краями внутрь, прикрывая ими осадок. Полученный «пакет», перевернутый конусом вверх, помещают в прокаленный до постоянной массы фарфоровый тигель. Фильтр с осадком осторожно сжигают при возможно низкой температуре. Затем прокаливают тигель при t=500-600 оС. (слабо-красное каление) в муфельной электрической печи. После охлаждения тигля в эксикаторе его взвешивают и прокаливают повторно до установления постоянной массы при t=900-1000 о С. При более высокой температуре сульфат бария разлагается. 35 ПРОТОКОЛ АНАЛИЗА Масса навески сульфата-________, г; Масса тигля с навеской после первого прокаливания-________, г; Масса тигля с навеской после второго прокаливания-_________, г; Масса тигля с навеской после третьего прокаливания-_________, г; Постоянная масса тигля с навеской-_________, г; Масса прокаленного остатка-________, г. III. Расчетная часть: По формуле 3.1 определяем процентное содержание SO3 %SO3= 𝑚х.соед∙Мопр.части Мн ∙Мх.соед ∙ 100 , (3.1) где mx.coeд-масса химического соединения, г; Мопр.часть-масса определяемой части, г; Мн-масса навески, г; Мч.соед-масса части соединения, г. mx.coeд=______, г; Мопр.часть=____, г; Мн=______, г; Мч.соед=_____, г. %SO3= ∙100=________ % Ответ IV. Заключение: Подпись преподавателя:_____________ Вопросы и задачи для самоконтроля 1. В чем заключается сущность гравиметрических определений по методу осаждения? Приведите примеры. 2. Какие операции включает метод осаждения? 3. Какие природные примеси удаляются фильтрованием? 4. Какие компоненты осадка удаляются прокаливанием? 5. Для удаления, каких примесей предусматривается промывка осадка при фильтровании? Задача 1.Определить содержание чистого BaCl2∙2H2O в образце технического хлорида бария. Навеска составляет 0,5956 г. Масса осадка сульфата бария BaSO4 после прокаливания равна 0,4646 г. 36 ЛАБОРАТОРНАЯ РАБОТА 4-ПРИГОТОВЛЕНИЕ СТАНДАРТНОГО РАСТВОРА СОЛЯНОЙ КИСЛОТЫ Цель работы:научиться готовить стандартные растворы. Оценка правильности полученных результатов Материалы и оборудование: Реактивы: концентрированная соляная кислота, дистиллированная вода, бура (тв.), метилоранж. Оборудование: аналитические весы, бюкс, воронка, мерная колба на 100мл, электроплитка, мерный цилиндр, колба на 500мл, мерная пипетка на 2025мл, колба для титрования. I. Теоретическая часть. Исходные вещества, применяемые для приготовления стандартных (титрованных) растворов кислот и оснований. Для титрования оснований необходимо иметь стандартный раствор кислоты. Чаще всего применяют хлористоводородную кислоту. Ей отдают предпочтение перед другими кислотами главным образом потому, что хлористоводородная кислота является сильной кислотой и почти все ее соли хорошо растворимы в воде. В тех случаях, когда приходится нагревать или кипятить растворы, лучше брать серную и хлорную кислоты. При титровании неводных растворов применяют преимущественно хлорную кислоту. Для титрования кислот необходимо иметь стандартный раствор сильного основания. Наиболее широкое применение находят титрованные водные растворы едкого натра или неводные растворы едкого кали, этилата натрия, гидроокиси тетраэтил аммония. Концентрации стандартных растворов могут изменяться от 0,01 н. до 0,2 н. Иногда применяют 0,5 и 1 н. растворы II. Методика выполнения работы: 1. Приготовление раствора соляной кислоты. В колбу наливают 500мл. дистиллированной воды и добавляют 5-6мл. концентрированной соляной кислоты. Хорошо перемешивают. 2. Приготовление раствора буры. (Na2B4O7 x 10H2O).На аналитических весах взвешивают навеску буры примерно 2-3гр. И растворяют ее в горячей воде. Горячий раствор буры аккуратно переливают в мерную колбу через воронку. После полного растворения навески раствор охлаждают и доводят объем колбы до метки дистиллированной водой. 3. Определение нормальности раствора соляной кислоты по буре. Пипеткой отмеряют 20-25мл. раствора буры и переносят в колбу для титрования и прибавляют 1 каплю метилоранжа. Титруют раствором соляной кислоты до появления бледно-розовой окраски. Na2B4O7+2HCl+5H2O=2NaCl+4H3BO3 37 ПРОТОКОЛ АНАЛИЗА Масса буры-________, г; Объем буры общий-_____, мл; Объем буры титр.-______, мл; Объем HCl титрования-ср. =________, мл. 3 III. Расчетная часть: По формуле 4.1 определяем Титр буры По формуле 4.2 определяем нормальность HCl По формуле 4.3 определяем нормальность буры Тбуры = 𝑚б (4.1) , 𝑉б.общ где mб-массса буры, г; Vб.общ- обьем буры общий, мл. mб=_______, г; Vб.общ=______, мл. Тбуры = = _______, г/мл; NHCl = 𝑁б∙𝑉б.𝑚𝑢𝑚𝑝 𝑉𝐻𝐶𝑙ср , (4.2) где Nб-нормальномть буры, г∙э/л; Vб.титр- обьем буры пошедшее на титрование, мл; VHClср.-обьем соляной кислоты среднее, мл. Nб-_____, г∙э/л; Vб.титр-___, мл; VHClср-_____, г∙э/л. NHCL = = _____, г∙э/л; Nбуры = 𝑇б∙ 1000 Эб , где Тбуры- титр буры, мл; Эб- эквивалент буры, г/моль; Тбуры-______, мл; Эб-______, г/моль. Nбуры = = ________, г∙э/л Ответ 38 (4.3) IV. Заключение: Подпись преподавателя:_____________ Вопросы и задачи для самоконтроля 1. Какие способы выражения концентраций вам известны? Что такое эквивалент, фактор эквивалентности, молярная масса эквивалента, титр, титр по определяемому веществу? 2. Что такое титрование? Дайте определение понятиям точка эквивалентности, конечная точка титрования. 3. Что такое кривые титрования и для чего они строятся? Что такое скачок титрования? Задача 1.На титрование смеси, состоящей из карбонатов натрия и калия массой 0,4 г. израсходовали 22,00 мл 0,3М HCl. Вычислить массовую долю (%) Na2CO3 и К2СО3 в смеси. Задача 2.Навеску хлорида аммония обработали избытком щелочи. Выделившийся аммиак поглотил 50 мл 0,5120 М HCl и раствор разбавили до 250 мл. На титрование 50 мл полученного раствора израсходовали 23,73 мл 0,05М КОН (К = 0,9740). Вычислить массу NH3, которая содержалась в хлориде аммония. 39 ЛАБОРАТОРНАЯ РАБОТА 5-ОПРЕДЕЛЕНИЕ ОБЩЕЙ ЩЕЛОЧНОСТИ СОДЫ Цель работы:Научиться определять щелочность соды. Оценка правильности полученных результатов Материалы и оборудование: Материалы и реактивы: карбонат натрия (тв), дистиллированная вода, метилоранж, стандартный раствор соляной кислоты. Оборудование: аналитические и химические весы, бюкс, воронка, мерная колба на 100мл., колба для титрования, пипетка на 10мл. I. Теоретическая часть. Наряду с минеральными кислотами и удобрениями содопродукты кальцинированная сода, каустическая сода и бикарбонат натрия относятся к важнейшим видам продукции основной химической промышленности, стекольной, металлургической, нефтеперерабатывающей, легкой и пищевой. В настоящее время в мире производство соды базируется на четырех способах ее получения: аммиачный, из нефелинов, карбонизация гидроксидов натрия и из природной соды. Кальцинированная сода Na2CO3 - белый порошок плотностью 2,5 г/см. Насыпная плотность так называемой легкой соды 0,5 - 0,6 г/см3, тяжелой соды 0,9 - 1,0 г/см3, температура плавления углекислого натрия 854°С. Кроме того, кальцинированная сода способна образовывать термически неустойчивые кристаллогидраты различной степени водности: сода химический хлористый натрий Na2CO3∙H2O; Na2CO3∙1,5H2O; Na2CO3∙4H2O; Na2CO3∙7H2O; Na2CO3∙10H2O Согласно ГОСТ 5100 - 64, кальцинированная сода, получаемая аммиачным методом, должна отвечать следующим требованиям к химическому составу: содержание Na2CO3 в прокаленном продукте, не менее 99,0% (что соответствует содержанию Na2CO3 в чистом виде) 96,8% II. Методика выполнения работы: Навеску карбоната натрия (соды) примерно 2гр. Взвешивают на технических весах, а затем более точно на аналитических весах в предварительно во взвешенном бюксе. Навеску через воронку переносят в мерную колбу, полностью растворяют, доливают дистиллированную воду до метки, и тщательно перемешивают. В колбу для титрования переносят пипеткой 10мл. исследуемого раствора карбоната натрия и добавляют 2 капли индикатора метилоранжа. Титруют стандартным раствором соляной кислоты до появления бледнорозовой окраски. При титровании идут реакции: Na2CO3+HCl=NaHCO3+NaCl I ст NaHCO3+HCl=H2CO3+NaCl II ст 40 ПРОТОКОЛ АНАЛИЗА Масса исследуемого-______, г; Объем исследуемого общий-_____, мл; Объем исследуемого на титрование-_____, мл; Объем HCl-ср. =_____, мл. 3 III. Расчетная часть: По формуле 5.1 определяем нормальность исследуемого вещества По формуле 5.2 определяем Титр исследуемого вещества По формуле 5.3 определяем массу NaOH По формуле 5.4 определяем процентное содержание NaOH Nиссл.= 𝑁HCl ∙ VHCl.mump. Vuccл.𝑚𝑢𝑚𝑝. , (5.1) где NHCl –нормальность соляной кислоты, г∙э/л; VHCl.mump-обьем соляной кислоты пошедшей на титрование, мл; Vuccл.mump-обьем исследуемого вещества пошедшее на титрование, мл. NHCl-______, г∙э/л; VHCl.mump-______, мл; Vuccл.mump-_____, мл. N иссл= = _______, г∙э/л; (5.2) Tиссл.= Nuccл ∙ Э𝑁𝑎𝑂𝐻 1000 , Nиссл-нормальность исследуемого раствора, г∙э/л; ЭNaOH-эквивалент гидроксида натрия, г/моль; Nиссл-_______, г∙э/л; ЭNaOH-_____, г/моль. Tислл= = _______, мл; mNaOH= Tиссл. ∙ Vиссл.общ, где Тиссл-титр исследуемого вещества, мл; Vиссл.общ-обьем иследуеммого вещества общий, мл. Тиссл-_______, мл; Vиссл.общ-_______ мл. mNaOH=________=________, г/мл; 41 (5.3) %NaOH= 𝑚𝑁𝑎𝑂𝐻 𝑚иссл ∙ 100 , (5.4) где mNaOH-масса гидроксида натрия, г; mиссл-масса исследуемого вещества, г. mNaOH=______, г; mиссл=_______, г. %NaOH= ∙100%=______, % Ответ IV. Заключение: Подпись преподавателя:_____________ Вопросы и задачи для самоконтроля 1. Какие способы получения соды Вы знаите? 2. Техническое название Na2CO3? 3. Применение соды в промышленности? Задача 1. В 500 мл раствора содержится 25 г кальцинированной соды Na2СО3 (карбоната натрия). Чему равны процентная и нормальная концентрации, если плотность раствора равна ρ = 1,03 г/см Задача 2.Химический контроль за очисткой судовых парогенераторов от отложений осуществляют, титруя пробу моющего раствора 0,1 н раствором NaOH в присутствии метилоранжа. Как приготовить 3 л 0,1 н раствора щелочи и 100 мл индикатора (С % = 1 %, ρ = 1,05 г/см3 )? 42 ЛАБОРАТОРНАЯ РАБОТА 6-ПРИГОТОВЛЕНИЕ СТАНДАРТНОГО РАСТВОРА ТРИЛОНА Б Цель работы: Закрепление навыков по приготовлению, стандартизации растворов. Реактивы и оборудование: Реактивы: трилон Б (т.в), дистиллированная вода Оборудование: аналитические весы, бюкс, мерная колба на 250мл, электроплитка. I. Теоретическая часть. Стандартные растворы готовят различными способами. 1. Из химически чистого вещества. Берут навеску точно на аналитических весах и растворяют ее в мерной колбе. Концентрацию рассчитывают математическим путем. 2. Из нехимически чистого вещества. Берут навеску на технохимических весах и растворяют в воде, объем которой измеряют цилиндром или мензуркой. Концентрацию такого стандартного раствора определяют титрованием исходного раствора. 3.Из фиксанала. Фиксанал — это стеклянная, герметически запаянная ампула с точным количеством раствора или сухого вещества. Чаще всего из одного фиксанала можно приготовить 1л 0,1 н. или 1 л 0,01 н. раствора, если растворять в мерной колбе вместимостью 1 л. Беря различное количество фиксаналов и мерные колбы разной вместимости, можно готовить растворы различной концентрации. Чаще всего стандартные растворы готовят вторым способом. Для работы удобнее всего использовать 0,1 и. стандартные растворы. II. Методика выполнения работы: Навеску Трилона Б≈ 2,5, г. Взвешивают на аналитических весах растворяют в мерной колбе при нагревании. Объем колбы доводят до метки. ПРОТОКОЛ АНАЛИЗА Масса трилона Б-________, г; Объем трилона Б общий-_______, мл; Эквивалент трилона Б-_______, г/моль. III. Расчетная часть: По формуле 6.1 определяем нормальность трилона Б Nтр.Б= 𝑚𝑚𝑝.б ∙100 𝑉𝑚𝑝.Бобщ ∙Э𝑚𝑝.Б 43 , (6.1) где mmp.Б-масса трилона Б, г; Vmp.Б-обьем трилона Б общий, мл; Эmp.Б-эквивалент трилона Б, г/моль; mmp.Б=________, г; Vmp.Б=_______, мл; Эmp.Б=_______, г/моль. Nтр.Б= =______, г∙э/л Ответ IV. Заключение: Подпись преподавателя:_____________ Вопросы и задачи для самоконтроля 1. Каким способом приготовлен раствор Задача1. Определить массу соли и объем дистиллированной воды, необходимых для получения 230г 12% поваренной раствора. Задача 2.Какую массу соли и объем воды необходимо взять для приготовления: 50 г 0,5 %-ного раствора; 60 г 1 %-ного раствора; 70 г 2 %-ного раствора. 44 ЛАБОРАТОРНАЯ РАБОТА 7-ОПРЕДЕЛЕНИЕ ПРОЦЕНТНОГО СОДЕРЖАНИЯ КАЛЬЦИЯ В КАЛЬЦИТЕ Цель работы: определение процентного содержания кальция в кальците Оценка качества выполненных работ и правильности полученного результата. Материалы и оборудование: Материалы и реактивы: кальцит (мел) твер., соляная кислота 2н, буферная смесь, индикатор эриохром черный, стандартный раствор раствора трилона Б Оборудование: аналит. весы, химический стакан на 50мл, колба для титрования, бюретка, пипетка, мерная колба на 100 мл. I. Теоретическая часть. Строительная воздушная известь – вяжущее вещество, получаемое умеренным обжигом не до спекания (900…1100ºС) карбонатных горных пород (известняков, мела, доломитов и т. п.), состоящих преимущественно из углекислого кальция СаСО3 и небольшого количества углекислого магния МgСО3, а также примесей кварца и глины, которые ухудшают качество строительной извести. Содержание глины в карбонатных породах не должно превышать 6 %. В результате обжига получают комовую негашеную известь, называемую «кипелкой», и состоящую в основном из оксида кальция СаО рисунок 7.1. Рисунок 7.1- Получение, гашение и твердение воздушной извести В зависимости от содержания оксида магния МgО воздушную известь разделяют на кальциевую (содержание МgО≤ 5 %), магнезиальную (МgО - от 5 до 20 %) и доломитовую (МgО от 20 до 40 %). II. Методика выполнения работы: 1 Приготовление исследуемого раствора. Исследуемый кальцит тонко растирают в ступке и взвешивают на аналит. весах в химическом стакане, предварительно взвешивают примерно 0,2гр. 45 А в этот стакан добавляют 15мл. 2н. соляной кислоты и нагревают смесь на электроплитке до растворения кальцита. Раствор охлаждают и переносят в мерную колбу. Не доводя объем колбы до метки, раствор кипятят 5 мин. для удаления углекислого газа. После охлаждения раствора объем колбы доводят до метки. Реакция при растворении: CaCO3+2HCl=CaCl2+H2O+CO2 2 Титрование. Порцию исследуемого раствора 20мл. пипеткой переносят в колбу для титрования, добавляют 15мл. буферной смеси и немного индикатора (раствор хорошо размешать до растворения индикатора) окраска должна быть вишневокрасноватой. Титруют стандартным раствором трилона Б до появления синезеленой окраски. ПРОТОКОЛ АНАЛИЗА Масса исследуемого вещества -_______, г; Объем исследуемого общий -______, мл; Объем исследуемый на титр. -_____, мл; Объем трилона Б на титрование-ср. = _______ мл. 3 III. Расчетная часть: По формуле 7.1 определяем нормальность исследуемого вещества По формуле 7.2 определяем массу Ca По формуле 7.3 определяем процентное содержание Ca 𝑁𝑚𝑝. Б∙𝑉𝑚𝑝. Бср. Nиссл. = (7.1) 𝑉иссл.𝑚и𝑚𝑝 где Nmp.Б-нормальность трилона Б, г∙э/л; Vmp.Бср.-обьем трилона Б среднее, мл; Vuccл.mump-обьем исследуемого раствора пошедшего на титрование,мл. Nmp.Б=________, г∙э/л; Vmp.Бср.=______, мл; Vuccл.mump=_____, мл Nиссл. = =______, мл; MCa= 𝑁иссл ∙ 𝑉иссл.общ ∙Э𝐶𝑎 1000 Nuccл-нормальность исследуемого раствора, г∙э/л; Vuccл.общ-обьем исследуемого раствора общий, мл; ЭCa-эквивалент Ca, г/моль. 46 (7.2) Nuccл=______, г∙э/л; Vuccл.общ=_____, мл; ЭCa=_____, г/моль. MCa= =______, г; % Ca= 𝑚𝐶𝑎 𝑚 иссл. ∙ 100, где mCa-масса Са, г; muccл-масса исследуемого расствора, г. mCa-______, г; muccл-______, г. % Ca= ∙ 100=_____, % Ответ IV. Заключение: Подпись преподавателя:_____________ Вопросы для самоконтроля 1 2 3 4 Виды воздушной строительной извести. Основные показатели качества воздушной строительной извести. Области применения воздушной извести. Что называют строительной известью? 47 (7.3) ЛАБОРАТОРНАЯ РАБОТА 8-ОПРЕДЕЛЕНИЕ КАЧЕСТВА ИЗВЕСТИ Цель работы:определение содержания в извести активных СаО+МgО, скорости гашения извести. Оценка качества выполненных работ и правильности полученного результата. Материалы и оборудование: Материалы: комовая известь негашеная, соляная кислота 1н HCl, раствор фенолфталеина,вода,метилоранж,1н NaOH. Оборудование: сито 0,2мм., стакан, термометр, коническая колба, часовое стекло, песочная баня. I. Теоретическая часть. При взаимодействии негашеной извести с водой происходит гидратация оксида кальция по реакции: СаО + Н2О = Са(ОН)2 + Q, где q – количество тепла, выделяющегося при реакции. Этот процесс называют гашением извести. Он сопровождается выделением значительного количества тепла. При этом температура гасящейся извести повышается до определенного максимума. С окончанием реакции прекращается выделение тепла, и температура смеси падает. Момент начала снижения температуры смеси является признаком прекращения реакции гашения извести. Сущность метода заключается в определении максимально высокой температуры гашения извести и времени, за которое произошло повышение температуры. Для испытаний используют сосуд Дьюара указанный на рисунке 8.1, который состоит из термосной колбы (1), термометра со шкалой на 150º (2) и пробки (3). Рисунок 8.1- Прибор для определения скорости гашения извести 48 II. Методика выполнения работы: Определение скорости гашения извести В зависимости от скорости гашения известь делят на быстрогасящуюся (скорость гашения до 10мин.), среднегасящуюся (скорость гашения от 10 до 30мин.) и медленногасящуюся (скорость гашения свыше 30мин.) Для определения скорости гашения извести пробу измельчают до прохода ее через сито 0,2 мм. Навеску 10 грамм измельченной извести помещают в сосуд Дьюара, в который предварительно наливают 20мл. воды, имеющей температуру 20 оС. Закрывают пробкой, в которую установлен термометр, и взбалтывают. Затем сосуд оставляют в покое и через каждые 30сек. отмечают температуру гасящейся извести. Наблюдения ведут до достижения максимальной температуры и начала ее падения. По полученным значениям температуры строится график t oС-𝜏, мин. (температура-время). За скорость гашения принимают время от момента добавления извести к воде до момента достижения максимальной температуры. Определение содержания активной CaO в извести. Для определения содержания активной CaO навеску примерно 0,5г абсолютно сухой жженой извести (величина зерен 0,2 мм) помещают в коническую колбу, заливают 100мл воды, прибавляют 1-2 капли фенолфталеина и титруют 1н раствором HCl до исчезновения малиново-красной окраски (титрование продолжительное). ПРОТОКОЛ АНАЛИЗА Масса извести-_____, г; Обьем исследуемого раствора общий- _____, мл; Обьем HCl титр-_______, см3; Обьем NaOH израсходованный на нейтрализацию избытка кислоты-_____, мл. III. Расчетная часть: По формуле 8.1 определяем количество активной CaO По формуле 8.2 определяем общее содержание CaO в извести CaO= 𝑎∙0,028∙100 𝑏 , где а- количество Iн HCl, пошедшей на титрование, см3; b- навеска извести, г; 0,028- титр Iн HCl по CaO a=_____, см3; b=_____, г. CaO= =______, % Определение общего содержания CaO в извести 49 (8.1) Для определения общего содержания СаО навеску 0,5г абсолютно сухой жженой извести (величина зерен 0,2мм) помещают коническую колбу, добавляют около 50мл воды и 50мл 1н HCl, прикрывают колбу часовым стеклом, нагревают на песочной бане до прекращения выделения СО2 (если в навеске присутствуют зерна неразложившегося СаСО3). После охлаждения в колбу прибавляют 1-2 капли метилоранжа и оттитровывают избыток кислоты 1н NaOH до перехода красной краски в оранжевожелтую. (а−𝑏)∙0,028∙100 (8.2) СаО= 𝑚 , где а- количество 1н HCl, прибавленной к извести, мл; в- количество lн NaOH, израсходованной на нейтрализацию избытка кислоты, мл; m- навеска извести, г; 0,028- титр 1н HCl по CaO a=___, мл;b=____, мл;m=____, г. СаО= = _____, % 𝑉𝐻𝐶𝑙𝑚𝑢𝑚𝑝 a= 𝑉𝑁𝑎𝑂𝐻𝑚𝑢𝑚𝑝 b= 𝐾𝐻𝐶𝑙 𝐾𝑁𝑎𝑂𝐻 VHCl титр-обьем соляной соляной кислоты пошедшей на титрование, мл; VNaOHтитр-обьем гидроксида натрия пошедшего на титрование, мл; KHClKNaOHСортность извести устанавливают по соответствию полученных результатов испытаний с показателями таблицы 8.1. Таблица 8.1-Технические требования к строительной извести Значение показателя Показатель 1-й 2-й Содержание активных оксидов кальция и магния в негашеной извести, не менее, % 90 80 Количество непогасившихся зерен в негашеной извести, не более, % 7 11 Скорость гашения, мин: быстрогасящаяся, менее 8 8 среднегасящаяся, не более 25 25 медленногасящаяся, более 25 25 Тонкость помола – остаток частиц, %, не более, на ситах с сеткой: № 02 1 1 № 008 10 10 50 сорта 3-й 70 14 8 25 25 1 10 Все данные по испытаниям заносять в таблицу 8.2 Таблица 8.2 -Результаты испытаний строительной извести Показатель Установлено испытанием Активность, % Скорость гашения, мин Содержание непогасившихся зерен, % Сорт IV. Заключение: Сравнивая результаты испытаний с техническими требования к строительной извести можно сказать, что известь по показателям относится к____сорту. Подпись преподавателя:_____________ Вопросы для самоконтроля 1. 2. 3. 4. Классификация воздушной извести. Какие показатели характеризуют сортность извести? Как определить активность извести? Где используется строительная воздушная известь? 51 ЛАБОРАТОРНАЯ РАБОТА 9-СИТОВОЙ АНАЛИЗ ЗЕРНИСТЫХ МАТЕРИАЛОВ Цель работы:освоить один из методов определения зернового состава огнеупорных материалов. Материалы и оборудование: Материалы: Зернистый материал (например- шамот ) Оборудование: набор сит, весы технические с разновесами, фарфоровые чашки, сушильный шкаф, щетка. I. Теоретическая часть. Определение величины зерен испытуемого материала просеиванием через стандартный набор сит, принято называть ситовым анализом. Ситовой анализ используются лишь в том случае, когда размер зерен материала больше 0,04 мм. Анализ является одним из наиболее простых и широко распространенных в лабораторной практике методом определения зернового состава. Принцип его состоит в нахождение количества материала, задерживаемого ситами с отверстиями различного размера. На сите указывается его номер или размер отверстия в сетки. Номер сетки соответствует номинальному размеру (мм) стороны ячейки, в номерах сит с размерами ячейки менее 1 мм. запятая перед десятыми долями опускается. Ситовой анализ проводят сухим способом. Для этого навеску высушенного материала помещают на верхнее наиболее крупное сито. Другие сита располагают одно под другим последовательно по мере уменьшения отверстий в ситах. Снизу набор сит закрывают сплошным металлическим поддоном. Материал рассеивают вручную или с помощью различных приспособлений. II. Методика выполнения работы: Каждое сито необходимо осмотреть внимательно, остатки предыдущего рассева тщательно удалить мягкой щеткой, хорошо промыть, высушить в сушильном шкафу при температуре 100-1100С. Из подготовленных таким образом сит собирают комплект, который вставляют в поддон. Предназначенную для анализа пробу испытуемого материала помещают в фарфоровую чашку и высушивают в сушильном шкафу при температуре 100-1100С до постоянной массы. Затем из пробы на технических весах берут навеску 200 гр. с точностью до 0,01 гр., которую помещают на верхнее сито. Комплект сит закрывают крышкой и рассеивают встряхиванием вручную в течение 20 мин. По окончании просеивания фракции собирают отдельно на бумагу, тщательно очищая дно и стенки сита щеткой. Каждый из остатков взвешивают с точностью до 0,01 гр. данные ситового анализа записывают в таблицу 9.1. Частным остатком на сите называют выражение в % отношение остатка на этом сите ко всей навеске испытуемого материала. 52 Полным остатком на сите называют выражение в % отношение суммы всех остатков как на данном, так и на всех предыдущих ситах ко всей навеске испытуемого материала. Таблицы результатов определений 9.1 Размер отверстий Частный остаток Остаток на сите, гр. в сетке, мм. на сите, %. остаток Полный на сите, %. 0 После заполнения таблицы строится график зернистости материалов . IV. Заключение: Подпись преподавателя:_____________ Вопросы для самоконтроля: 1. Какие материалы используют для изготовления сит? 2. Для каких размеров частиц(зерен) применим ситовой анализ? 3. Какая последовательность используется при сборе набора стандартных сит? 4. Вствьте недостающие слова. Ситовой анализ можно производить …….или …… 5. Закончите предложение. Для анализа крупнозернистых и кусковых материалов используют, как правило …….. 53 ЛАБОРАТОРНАЯ РАБОТА 10 - ОПРЕДЕЛЕНИЕ КАЧЕСТВА ГЛИНИСТОГО ШЛИКЕРА Цель работы:Научиться практически, определять основные параметры глинистого шликера. Материалы и оборудование: Материалы: глина,вода Оборудование стакан 500мл (коническую колбу) воронка , мерную колба объемом 100мл, стакан 100мл, технические весы, Вискозиметр Энглера I. Теоретическая часть. Для характеристики текучести шликера определяют его относительную вязкость, которая представляет отношение времени истечения шликера через отверстие заданного диаметра ко времени истечения такого же объема воды при одинаковых условиях и выражается в градусах Энглера (0Е). Текучесть-величину, обратную вязкости–определяют на вискозиметре Энглера рисунок 10.1. Прибор состоит из двух медных сосудов, вставленных один в другой. Внутренний сосуд представляет собой цилиндрический резервуар с дном. В центре дна устроено конусное отверстие , которое закрывается конусным штырем с конусным концом. К внутренним стенкам сосуда прикреплены на одном уровне три заостренных штифта, которые служат указателями высоты уровня шликера и контролируют горизонтальность прибора. Наружный сосуд служит водяной баней (термостатом) для поддержания заданной температуры вторую контр шликера, контролируют термометром . 1-внешний сосуд 2 внутренний сосуд,3-подача шликера через трубку 4термостат, 5-крепление сосудов 6- термометр. Рисунок 10.1- Вискозиметр Энглера 54 Для определения времени истечения вискозиметр устанавливают по уровню. Шликер пропускают через сито 144от .в./см2 и заливают во внутренний сосуд так, чтобы шликер покрыл все три острия. Шликер тщательно перемешивают в течении 2-3 мин, а затем оставляют в покое на 1 мин. Под выпускное отверстие ставят мерную колбу, выпускают в нее шликер, одновременно пускают в ход секундомер, по которому отсчитывают время истечения 100 мл. Аналогично (при этой же температуре) определяют время истечения воды. 0 𝑡ш E= , (1) 𝑡в где 0 E- относительная вязкость, по Энглеру; tш- время истечения шликера, секунды; tв- время истечения воды, секунды. II. Методика выполнения работы: Для приготовления шликера берут 40г глины, помещают в стакан 500мл (коническую колбу) и заливают 120мл горячей воды при непрерывном перемешивании (соотношение глины и воды должно быть 1:3). Полученный шликер переносят с помощью воронки в мерную колбу объемом 100мл (стакан 100мл) и взвешивают на технических весах. ПРОТОКОЛ АНАЛИЗА Масса навески-___, г; Обьем воды_____, мл; Обьем шликера-______, мл. III. Расчетная часть: По формуле 1 определяют количество абсолютной сухой глины в 100см3 По формуле 2 определяем плотность шликера По формуле 3 определяем относительную влажность шликера По формуле 4 определяют относительную вязкость %вл= 𝑚ш−𝑚с.о 𝑚ш 100, (1) где mшл – масса 100см3 шликера, г; mсух.ост-масса сухого остатка, г. mшл=______, г; mсух.ост=________, г. %вл= 100=% (2) 55 𝑚г+100 S= 100 𝑚г 𝑝 , где 100 – объем шликера, см3; mг-масса глины, г; p-плотность глины, г/см3. mг-_____, г;р-2,2, г/см3. S= =% Wотн = 100 𝑝−𝑠 𝑆(𝑝−1) , где p-плотность глины, г/см3; s-плотность шликера, г/см3; 100 – объем шликера, см3; mг-масса глины, г; p=_____, г/см3;s=______, г/см3. Wотн = 100 = % IV. Заключение: Подпись преподавателя:_____________ Вопросы для самоконтроля: 56 (3) ЛАБОРАТОРНАЯ РАБОТА 11-ОПРЕДЕЛЕНИЕ ВОДОПОГЛОЩЕНИЯ ШАМОТА Цель работы: Исследовать шамот, определить его водопоглащение по методике. Оценка правильности полученных результатов. Материалы и оборудование: Материалы: шамот кусковой, шамот молотый различных марок Оборудование: металлический противень, сосуд для кипячения, эксикатор, электрическая плитка, технические весы, разновес, сушильный шкаф, мешочек, часовое стекло. I.Теоретическая часть. Водопоглощение керамических материалов следует проводить согласно требованиям ГОСТ 7025-91. Существуют различные методы определения водопоглощения керамических изделий: определение водопоглощения при атмосферном давлении в воде температурой (20±5)°С; то же, под вакуумом в воде температурой (20±5)°С; то же, при атмосферном давлении в кипящей воде. Водопоглощение W – способность материала впитывать и удерживать воду. Водопоглощение – это разность между массой образца, насыщенного водой m 2 , и массой сухого образца m 1 определяется по формуле 11.1: W m2 m1 (11.1) где m 2 - масса образца, насыщенного водой, кг, г. m 1 - масса сухого образца, кг, г. Объемное водопоглощение Wоб - это разность между массой образца, насыщенного водой m 2 , и массой сухого образца m 1 отнесенная к объему образца V определяется по формуле 11.2: Wоб m2 m1 100% V или Wоб Wm ср (11.2) Массовое водопоглощение Wm - это разность между массой образца, насыщенного водой m 2 , и массой сухого образца m 1 , отнесенная к массе сухого образца m 1 определяется по формуле 11.3: m2 m1 (11.3) Wm m1 100% II.Методика выполнения работы: Основным показателем качества шамота является степень его спекания, оцениваемая по водопоглощению. Водопоглощение существенно влияет на пористость готовых изделий. Определение водопоглощения шамота по выходу из печи Пробу отбирают от кусков шамота, выходящего из печи, в количестве 100-200г. Пробу нагревают на электроплитке ( на противне) в течении 5 минут, 57 затем погружают в кипящую воду на 45 минут, после чего охлаждают и взвешивают. По формуле определяют водопоглощение. Определение водопоглощения шамота после помола Для испытания от шамота отсеивают зерна крупнее 2мм. Пробу в количестве 100г сушат в сушильном шкафу в течении 1 часа 20 минут, охлаждают в эксикаторе и взвешивают. Навеску помещают в небольшой мешочек из плотного материала, который вместе с пробой опускают в горячую воду и кипятят 1час 20минут. После кипячения зерна шамота из мешочка переносят на часовое стекло и взвешивают. По формуле определяют водопоглощение. ПРОТОКОЛ АНАЛИЗА Масса шамота общая- ______, г; Масса шамота исследуемая- ______, г. III. Расчетная часть: По формуле 11.3 определяем водопоглащение шамота где W m – водопоглащение шамота,% m 1 - массой сухого образца, г; m 2 -насыщенного водой, г; m1=_____, г; m2=_____,г. 𝑊𝑚 = − 100% = ______% IV. Заключение: Подпись преподавателя:_____________ Задачи для самоконтроля: 1.Определить среднюю плотность, массовое водопоглощение камня и его пористость, если объемное водопоглощение составляет 10%, истинная плотность 2,7г/см3, образец в сухом состоянии весил 200г, а при полном насыщении водой 210г. 2.Образец известняка имеет среднюю плотность 2100 кг/м3, его водопоглощение по массе составило 43%- Определить объемное водопоглощение. 3.Масса сухого известняка 300 г, а после насыщения водой 308г. Средняя плотность известняка 2400 кг/м3. Вычислить массовое и объемное водопоглощение известняка. 58 ЛАБОРАТОРНАЯ РАБОТА 12-ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА ШАМОТА В ШАМОТНОЙ МАССЕ Цель работы:научиться практически, определять количество шамота в шамотной массе различными способами. Материалы и оборудование: Материалы: шамотная масса Оборудование: стакан 500 мл, сито, технические весы, разновес, стеклянная палочка, сушильный шкаф, электрическая плитка. I.Теоретическая часть. Керамическая шамотная масса, применяемая в промышленности, является огнеупорной глиной, в которую добавили шамотный порошок. Благодаря введению шамота уменьшается пластичность и усадка изделий при обжиге и сушке. Сформованные изделия длительный период сушат без пропарки в формах, после чего подвергают обжигу при высоких температурах.В производстве шамотных изделий определение содержания шамота и глины в массе очень важно, т.к. соблюдение постоянства состава массы- одно из основных условий стабильности свойств изделий. Существует несколько методов определения степени отощения: ситовой ускоренный (весовой и объемный), метод отмучения и другие. II. Методика выполнения работы: Метод определения Ситовой ускоренный (весовой) метод Ситовой метод основан на том, что размеры частиц глины меньше размеров даже наиболее мелких фракций шамота. Лишь очень незначительное количество шамота проходит через сито №0063, 008, 009, тогда, как частицы глинистого вещества проходят полностью. По весовому методу берут две навески: одну для определения влажности, другую (100г) для определения степени отощения. Первую навеску помещают в фарфоровую чашечку, взвешивают и высушивают ускоренным методом. После сушки навеску вновь взвешивают. ПРОТОКОЛ АНАЛИЗА Масса навески-100, г. III. Расчетная часть: По формуле 12.1 определяют относительную влажность массы По формуле 12.2 пересчитывают массу влажной навески 100г на сухое вещество По формуле 12.3 определяют количество шамота в массе (степень отощения) 59 Wотн = 𝑚вл−𝑚𝑐𝑦𝑥 𝑚вл 100, (12.1) где mвл – масса навески до сушки, г; mсух – масса навески после сушки, г. mвл=______, г; mсух=_____, г. Wотн = 100= ______, % Вторую навеску помещают в стакан емкостью 500 мл, заливают 300см3 горячей воды и растирают комочки массы стеклянной палочкой. Суспензию процеживают через сито №0063 (008, 009), а оставшийся на сито остаток промывают слабой струей воды до тех пор, пока стекающая вода не станет прозрачной.Отстоявшийся на сите отощитель переносят в фарфоровую чашку, ставят в сушильный шкаф и сушат. Остаток охлаждают и взвешивают на технических весах. 𝑚𝑐𝑦𝑥 = 𝑚в(100−𝑊отн) 100 , (12.2) где mсух-масса навески в пересчете на сухое вещество, г; mвл–масса навески, г; Wотн–относительная влажность массы, %. mвл= _____, г; Wотн= _______, %. 𝑚𝑐𝑦𝑥 = = _______, г O= 𝑚0 𝑚сух 100% + П, (12.3) где О- степень отощения (количества шамота), %; mo – масса сухого остатка шамота, г; П – поправка, %. mо=______, г; П-_____, %; mсух=______, г. O= 100 + _______ = ________% Поправка учитывается то количество отощителя, которое проходит через сито при промывании. Поправку находят опытным путем, она зависит от вида отощителя и степени его отношения. Величина поправки берется в пределах 5-7%. Метод отмучивания Навеску массы (100г) помещают в стакан емкостью 500мл, заливают горячей водой и кипятят на плитке 3-5мин, чтобы комочки глины распустились. 60 Затем суспензию снимают с плитки, дают отстояться 2-3 минуты и осторожно декантируют (сливают мутную воду) с осадка отощителя. Затем в стакан наливают холодную (300мл), ставят на стол и оставляют в покое, 60 сек. после чего вновь декантируют воду с осадка. Эту операцию повторяют до тех пор, пока вода над осадком после 60 сек, покоя не будет прозрачной.Остаток отощителя из стакана переносят в фарфоровую чашечку, высушивают и взвешивают. Все необходимые расчеты производят точно так же, как и в предыдущем опыте. IV. Заключение: Подпись преподавателя:_____________ Вопросы для самоконтроля: 1. Перечислите метода определения степени отощения шамота? 2. При методе отмучивания можно получить большую степень ошибке результата. С чем это связано и как этого избежать. 3. При какой степени влажности навески необходимо её предварительно сушить? 4. Составьте сами вопрос проблемного характера 61 ЛАБОРАТОРНАЯ РАБОТА 13-ОПРЕДЕЛЕНИЕ ПЛОТНОСТИ ОГНЕУПОРНЫЙ МАТЕРИАЛОВ Цель работы: изучить сущность метода и научиться практически, определять плотность огнеупорных материалов. Материалы и оборудование: Материалы: образец изделия, вода дистиллированная Оборудования: пикнометр 2 штуки, весы аналитические, разновес, сушильный шкаф, фарфоровая ступка с пестиком, сито 0,5 мм, сито 0,2 мм, эксикатор, воронка, сосуд для кипячение. I.Теоретическая часть. Любой керамический материал – это, как правило, сочетание твердого вещества (кристаллического и стекловидного) с пустотами – порами. Объем пор, их размеры и характер распределения оказывает значительное влияние на ряд свойств керамических изделий и материалов. Так, например, механическая прочность керамики зависит не только от общей пористости, но и от размера пор, равномерности их распределения. Бесспорно, что с увеличением пористости механическая прочность керамики уменьшается за счет увеличения дефектности структуры и снижения прочности связей. Установлено, что объем пор, заполненных водой, определяет морозостойкость строительной керамики; количество, размер и характер распределения пор во многом определяют шлако-устойчивость огнеупорной футеровки печей; пористость влияет на теплопроводность и звукопроводность керамических материалов. Поры в керамике имеют разнообразную форму, очертания, неравномерно распределены по объему, поэтому полную характеристику пористости получить чрезвычайно трудно, даже при использовании современных поромеров. Несмотря на разнообразие форм, поры можно подразделить на закрытые поры (недоступные для проникновения в них жидкости и газа) и открытые, которые в свою очередь делятся на тупиковые (заполняемые жидкостью и газом, но не влияющие на проницаемость керамики) и каналообразующие (открытые с обоих концов поры, создающие поровые каналы). Поскольку прямые методы измерения пористости материалов чрезвычайно сложны, то в технологии керамики этот показатель часто оценивают путем определения других свойств, непосредственно зависящих от пористости. К таким показателям относятся плотность материала (истинная, кажущаяся, относительная) и водопоглощение. Истинная плотность (𝜌и ) является физической константой для индивидуального вещества и зависит от его строения. Для керамики эта величина зависит от плотности упаковки атомов в кристаллах и химического состава стекловидной фазы. Истинная плотность и определяется как отношение массы материала к его объему без учета пор и выражается в кг/м3, г/см3. 62 Кажущаяся плотность (𝜌к ) – это отношение массы тела ко всему занятому им объему, включая поры (выражают ее также в кг/м3, г/см3). Относительную плотность (𝜌отн ) определяют как отношение кажущейся плотности к истинной (выражают в долях единицы или в процентах). Она представляет объемную долю твердого вещества в материале. Плотностью называется отношение покоящейся массы материала к его объему без учета пор. Объем тела зависит от температуры, поэтому плотность керамических материалов определяют при нормальной температуре (200С). Наиболее распространенным методом определения плотности керамических материалов является пикнометрический. Его используют при испытании тонкоизмельченных порошков, и хотя он требует значительной затраты времени, но отличается высокой точностью. II. Методика выполнения работы(по ГОСТУ 2211-65): Плотность огнеупоров определяют параллельно с двумя навесками. Все взвешивания проводят с точностью до 0,0002 г. Среднюю пробу массой 200 г измельчают в фарфоровой ступке до прохождения без остатка через сито с ячейками размером в свету 0,5 мм. После тщательного смещения пробу сокращают квартованием до 50 г и дополнительно измельчают, до прохождения без остатка через сито с ячейками размером в свету 0,2 мм до исчезновения закрытых пор. Растертую пробу высушивают при 105-1100С до постоянной массы и хранят в эксикаторе. Из высушенной пробы отбирают 5-8 г материала и засыпают его через воронку и предварительно взвешенный пикнометр типа ПШМ емкостью 25 мл. Пикнометр, с пробой взвешивают, затем до половины наполняют жидкостью и подвергают кипячению в воде в течении 30 минут для удаления воздуха из материала и воды. Материалы невзаимодействующие с водой насыщают дистиллированной водой. Материалы, взаимодействующие с водой, насыщают ксиломом или толуолом. Во время кипячения пробка с пикнометра должна быть снята. После кипячения в пикнометр, с пробой добавляют прокипяченной (дистиллированной) воды до метки и взвешивают. Затем пробу из пикнометра удаляют, пикнометр промывают, заполняют прокипяченной (дистиллированной) водой до метки и взвешивают. ПРОТОКОЛ АНАЛИЗА Масса навески-_____, г; Обьем смеси- _____, мл. III. Расчетная часть: По формуле 1определяют плотность пробы вычисляют с точностью до 0,001 г/см3 По формуле 2 плотность пробы находят как среднее арифметическое двух параллельных определений 63 𝜌= 𝑚 ∙ 𝜌ж 𝑚 − (𝑚1 − 𝑚2 ) (1) где ρ -плотность пробы, г/см3; ρж - плотность жидкости при 200С (для воды ρж=0,998 г/см3) m -масса пробы, г; m1 -масса пикнометра с пробой и жидкостью, г; m2 -масса пикнометра с жидкостью, г; m3 -масса пикнометра сухого, г; m4 -масса пикнометра с пробой, г. M=____, г; p(ж)=0,998, г/см3; m1=_______, г; 𝜌= m2=______, г. =_____см3 IV. Заключение: Подпись преподавателя:_____________ Вопросы для самоконтроля: 1. Что такое истинная плотность материала? 2. Что такое средняя плотность? 3. Что такое пористость материала? 4. Какие свойства материала улучшаются с повышением пористости 5. Для чего необходимо определять плотность? 6. Какой метод является самым распространенным для тонкоизмельченных материалов? 7. В чем отличие истинной от кажущей плотности? 64 ЛАБОРАТОРНАЯ РАБОТ 14-ХИМИЧЕСКАЯ СТОЙКОСТЬ КЕРАМИЧЕСКИХ ИЗДЕЛИЙ Цель работы:изучить сущность метода и научиться практически, определять кислотоустойчивость керамических материалов. Материалы и оборудование: Материалы: испытуемый материал(керамическая плитка), 5% раствор щелочи NaOH, серная кислота концентрированная, вода дистиллированная. Оборудование: ступка с пестиком, сита №1 и №0,5, чашка фарфоровая, тигель, эксикатор, сушильный шкаф, муфельная печь, щипцы тигельные, колба коническая, воронка, электроплитка, асбестовая сетка, фильтровальная бумага. I. Теоретическая часть. Химически стойкими керамическими изделиями считается такие, которые оказывают сопротивление разрушающему действию различных химических реагентов (кислот, щелочей, солей, газов) Химическая стойкость зависит от плотности и характера структуры, химического состава изделий, содержания и вида примесей, концентрации и вида реагентов, температуры и взаимодействия и других факторов. В большинстве случаев химически стойкие керамические изделия используются в условиях взаимодействия кислых или щелочных реагентов. В соответствии с этим лабораторные методы определений химической стойкости керамики разделяет на два вида испытаний: характеризующих отношение керамики к кислым реагентам или кислотоупорность и характеризующих отношение керамики к основным реагентам, т.е. щелоустойчивость. Методы испытаний кислотоустойчивости керамических изделий делятся на две группы: - испытание целых образцов или изделий - испытание материала в измельченном состоянии По методам первой группы качество материалов оценивается лишь приблизительно, испытания громоздки и требуются большего качества реактивов и рабочего времени. Получению количественной оценки (по потере массы) часто мешает то обстоятельствам внутри образцов могут образовываться новые химические вещества, которые с большим трудом удаляются при промывке или не удаляются совсем. В результате потери массы не отражают действительной степени разрушения материала. Иногда обработанное кислотой изделие может оказаться тяжелее, чем до испытания вследствие отложения внутри керамики вновь образовавшихся солей. Поэтому методы первой группы практически не используются, а определения проводят обычно по методам второй группы. Методы определения кислотостойких материалов в измельченном состоянии различаются в основном степенью измельчения материала, видом и концентрацией применяемых для испытания кислот, характером обработки (на холоде или при нагревании). 65 Изучение влияния разнообразных факторов на растворимость керамических материалов показало, что наиболее достоверные результаты получаются при обработке зерен испытуемого материала крупностью 0,5–1мм концентрированной серной кислоты при кипячении в течение 1 часа. Этот метод принят как стандартный (ГОСТ 473.5-81). Следует отметить, что по стандартному методу требуется значительно меньшие затраты времени на измельчение испытуемого материала и к тому же не требуется идеальная очистка его от примесей железа, попадающих в испытуемый материал при измельчении его в стальной ступке. II.Методика выполнения работы: Стандартный метод определения кислотоустойчивости керамических материалов (ГОСТ 473.5-81) 1 Подготовка материала к испытанию. Испытуемый материал измельчают в ступке и просеивают через сито с сеткой №1 до полного прохождения через него всего материала. Полученный порошок пропускают через сито с сеткой 0,5. Порошок, оставшийся на этом сите, используют для определения химической стойкости. Для освобождения порошка от пыли его промывают на сите струей воды до полной прозрачности промывных вод. Промытый порошок перенося в фарфоровую чашечку и высушивают при температуре 110-120 оС. Высушенный порошок помещают в эксикатор для охлаждения и хранения. 2 Испытание Из подготовленного материала на аналитических весах берут навеску 12 грамма и помещают ее в колбу, куда затем через воронку осторожно заливают 25мл концентрированной серной кислоты. Воронку оставляют в колбе. Колбу с содержимым устанавливает на асбестовой сетке и медленно нагревают (на электроплитке) до кипения. Спокойное и равномерное кипение поддерживают в течение 1часа. Нагревание ведут под тягой. Колбе дают остыть. В остывшую колбу добавляют небольшими порциями 75см3 воды, обмывая при этом воронку, чтобы смыть зернышки испытуемого материала, которые могли попасть на воронку во время кипячения. При помутнении жидкости колбу ставят на 15-20 мин. на электроплитку. Затем прозрачный раствор декантируют на беззольный фильтр. Остаток в колбе промывают 2-3 раза небольшими процентами горячей воды. Отстоявшиеся в колбе зерна обливают 50мл 5% раствором щелочи, 15-30 минут нагревают и вновь декантируют на тот же фильтр. Осадок еще раз промывают и переносят на фильтр. Остаток вместе с фильтром на воронке подсушивают в сушильном шкафу, затем переносят в предварительно взвешенный фарфоровый тигель, озоляют и прокаливают до постоянной массы (20-30 минут). Охлажденный в эксикаторе тигель с осадком взвешивают на аналитических весах. III. Расчетная часть: По формуле 14.1 определяют кислотоустойчивость в % 66 К= 𝑚1 𝑚0 ∙ 100%, где К- кислотоустойчивость , %; m0 – масса навески вещества до испытания, г; m1- масса остатка, г; m0=____, г; m1=____, г. К= ∙ 100% =____% IV. Заключение: Подпись преподавателя:_____________ Вопросы для самоконтроля: 1. Что такое химическая стойкость материала и как её оценить? 2. Что такое коррозия? Как защитить материалы от коррозии? 3. От чего зависит химическая стойкость? 4. В каких средах работает химически стойкий материал? 67 (14.1) ЛАБОРАТОРНАЯ РАБОТА 15-ОПРЕДЕЛЕНИЕ РАСПУШКИ АСБЕСТА Цель работы: научиться практическим путем определять распушку асбеста. Оценка правильности полученного результата Материалы и оборудование: Материалы: асбест дробленый, вода Оборудование: аналитические весы, мерный цилиндр на 500 мл, фарфоровая чашечка, стеклянная палочка. I. Теоретическая часть. Асбестом (горным льном) называют волокнистые материалы , способные расщепляться на тончайшие гибкие и эластичные волокна, из которых можно также, как и из растительных (хлопок, лен) прясть нити и вырабатывать несгораемые ткани. Для изготовления асбесто- цементных изделий применяют хризотил-асбест. По химическому составу хризотил – асбест представляет собой гидросиликат магния. 3 MgO ∙ 2SiO2 ∙ 2 H2О Для тепловой изоляции применяют обычно хризотиловый асбест (ГОСТ 12871-93), обладающий высокой температуростойкостью (500 °С при длительном нагреве, 700 °С — при кратковременном). Прочность волокон асбеста на разрыв составляет до 3000 МПа и превышает прочность стальной проволоки. Асбест хорошо адсорбирует (поглощает) воду вследствие развитой удельной поверхности. Эта способность асбеста используется для образования пористости у всех асбестсодержащих теплоизоляционных изделий. Асбест залегает в породе в виде отдельных жил. Его добывают взрывным способом в основном в открытых карьерах. Добытая в карьере асбестовая руда подвергается механическому обогащению, т. е. пустую породу отделяют от асбестового волокна. В процессе обогащения волокно расщепляется и с помощью барабанных сит разделяется в зависимости от длины волокна на восемь групп — от нулевой до седьмой. Хризотиловый асбест обладает слабой кислотоустойчивостью и высокой щелочеустойчивостью. Средняя плотность асбеста зависит от степени распушки асбеста, уплотнения волокна и увеличивается с уменьшением длины волокна и с увеличением содержания пыли. Плотность асбеста 2,4—2,6 г/см3. II Методика выполнения работы: Взять навеску сухого асбеста 10 г, перенести в фарфоровую чашечку и добавить в чашечку 100 мл воды. Содержимое чашечки перемешать стеклянной палочкой 15-20 мл. для того, чтобы асбест распушился. Затем асбест отжать и перенести в другую чистую фарфоровую чашечку и взять из нее асбеста 5 г для определения влажности. Эту навеску асбеста поместить в тигель (предварительно взвешенный) и поставить сушить в сушильный шкаф ускоренным методом. Затем охладить тигель в эксикаторе, взвесить на аналитических ве68 сах.Оставшуюся массу перемешать стеклянной палочкой и перенести в мерный цилиндр с водой, объем цилиндра довести до метки 500мл. После чего содержимое цилиндра перемешать и дать отстояться 30минут. Результат определяют по делениям на цилиндре: 100мл-10% 200мл-20% 300мл-30% Распушка асбеста должна быть не менее 30%. ПРОТОКОЛ АНАЛИЗА Масса асбеста-_____, г; Обьем воды- _____, мл; Обьем раствора для распушки- _____, мл; Масса навески для сушки_____, г. III. Расчетная часть: По формуле 15.1 определяют влажность асбеста По формуле 15.2 исходя из влажности асбеста определяют массу навески асбеста для распушки %вл= 𝑚н−𝑚𝑐𝑦𝑥.𝑜𝑐𝑚 𝑚н ∙100, (15.1) где %вл– влажность асбеста,%; mн– масса навески асбеста до высушивания, г; mсух.ост. – масса навески после высушивания, г. mн=________ г; mсух.ост.=_______, г. %вл= 100%=______, % mн = 𝑚1 ∙100 100∙ 𝑚2 , где mн– масса навески асбеста для распушки, г.; m1 – масса увлажненного асбеста, взятого для определения влажности, г; m2 – полученая масса асбеста, %; m1=_____, г; m2_____ IV. Заключение: Подпись преподавателя:_____________ 69 (15.2) Вопросы для самоконтроля: 1. Какие изделия можно получитьиз асбеста 2. Вставить слово. Доля асбеста в этих …….. Может составлять от 50 до 70%. 3. Дополнить предложение смесь асбестовой крошки с силикатным клеем, обработанная затем раствором хлорида кальция, образует прекрасную…… 4. Вставить недостающие слова. Основная доля добываемого асбеста (около 80%) потребляется в …….., например, для изготовления ………. – распространенного кровельного материала. 70 ЛАБОРАТОРНАЯ РАБОТА 16-ОПРЕДЕЛЕНИЕ НОРМАЛЬНОЙ ГУСТОТЫ ЦЕМЕНТНОГО ТЕСТА Цель работы: изучить методику определения нормальной густоты цементного теста. Закрепить навыки пользования техническими и аналитическими весами, мерной посудой, приобрести навыки работы с прибором Вика. Материалы и оборудование: Материалы: цемент, вода. Оборудование: прибор Вика с иглой и пестиком, кольцо к прибору Вика, чаша для приготовления цементного теста. I. Теоретическая часть. Цементным тестом называют смесь цемента и воды. Цементным тестом нормальной густоты условно принято называть такую консистенцию его, при которой металлический цилиндр диаметром 10-0,1 мм и высотой 50 мм под нагрузкой 300 г отпускается в него за 30 секунд на глубину от 33 до 35 мм или не доходит до дна кольца на 5-7 мм. Обычно нормальная густота цементного теста характеризуется тем количеством воды, выраженным в % к массе цемента, какое необходимо для получения теста. Для различных цементов величина нормальной густоты цементного теста колеблется в некоторых пределах и составляет для портландцемента 21-27, пуццоланового портландцемента 30-45, шлакопортландцемента 26-30, глиноземистого 31-33, романцемента 30-50% и т.д. Значение нормальной густоты цементного теста опытным путем принято определять прибором называемым Вика представленным на рисунке 16.1 1 – кольцо, 2 – стальная игла (или пестик), 3 – подвижный металлический стержень, 4 – указательная стрелка, 5 – шкала с делениями, 6 – зажимной винт, 7 – станина Рисунок 16.1-Прибор Вика 71 Прибор Вика имеет цилиндрический металлический стержень 3, свободно перемещающийся в обойме станины 7. Для закрепления стержня на требуемой высоте служит зажимной винт 6. Стержень снабжен указательной стрелкой 4 для отсчета перемещения его относительно шкалы 5, прикрепленной к станине. Шкала имеет цену деления 1 мм. При определении нормальной густоты цементного теста в нижнюю часть стержня вставляют металлический цилиндр-пестик 2. При определении сроков схватывания пестик заменяют иглой 2. Пестик должен быть изготовлен из нержавеющей стали с полированной поверхностью. Игла должна быть изготовлена из стальной жесткой нержавеющей проволоки с полированной поверхностью, не должна иметь искривления. Поверхность пестика и иглы должна быть чистой.Массу перемещающейся части прибора сохраняют взаимной перестановкой пестика и иглы. Отдельные детали перемещающейся части прибор подбирают таким образом, что бы их масса находилась в пределах 300±2 г.Кольцо 1 к прибору Вика и пластинка, на которую устанавливают кольцо, должно быть изготовлены из нержавеющей стали, пластмассы или другого не впитывающего воду материала. II. Методика выполнения работы: Для приготовления цементного теста берут 400 г цемента и высыпают его в сферическую металлическую чашу, предварительно протертую влажной тканью. В цементе делают углубление, в которое в один прием выливают воду в количестве необходимом (ориентировочно) для получения теста нормальной густоты. Обычно для первого пробного затворения берут 25…26% воды от массы цемента, т.е. около 100 мл. Воду отмеряют мерным цилиндром с точностью до 0,5 мл либо отвешивают с точностью 0,5 г, а затем вливают ее в чашу, стараясь заполнить углубление в цементе. В воду насыпают цемент, находящийся на бортах чаши. В это же время включают секундомер. Через 30 сек смесь воды с цементом в чаше сначала медленно, а затем быстрее в течении 5 минут перемешивают стальной лопаткой во взаимно перпендикулярных направлениях. После этого порцию полученного цементного теста лопаткой в один прием укладывают в кольцо прибора, которое находится на металлической пластине. Последнюю вместе с кольцом и цементным тестом несколько раз встряхивают, уплотняя тесто, затем избыток его снимают вровень с краями кольца влажным штапелем (ножом), после чего перемещают под пестик на станину точно вертикально установленного прибора. Открывая винт, осторожно опускают пестик до соприкосновения с поверхностью тела и затем в таком положении закрепляют его. После этого включают секундомер и одновременно опускают винт. При этом пестик свободно погружается в тесто и через 30 сек по шкале прибора отмечают глубину его погружения.Если стрелка-указатель находится между 5-м и 7-м делениями шкалы, это значит, что пестик Тетмайера погрузился на глубину 33-35 мм и густота такого теста нормальна. Если за указанное время пестик до такой глубины не опустился-тесто слишком густо, если он опустился ниже или раньше 30 сек-тесто слишком жидкое. В обоих случаях нужно изменить количество воды. Для этого готовят новую порцию теста с 72 изменением водоцементного отношения. Так поступают до тех пор, пока не будет найдена нормальная густота цементного теста. Количество воды для получения теста нормальной густоты, выражаемое в процентах от массы цемента, определяют с погрешностью не более 0,25%. ПРОТОКОЛ АНАЛИЗА Масса навески-_______, г; Объем воды добавленный для приготовления теста-______, мл; Глубина-____мм. III. Заключение: Цементное тесто ____________ густоты, имеет цилиндр диаметром ______мм и высотой ____мм, под нагрузкой ______г опускается в него за 30секунд на глубину от ___ до ____мм или не доходит до дна кольца на _____мм. Подпись преподавателя:_____________ Вопросы для самоконтроля: 1. Охарактеризуйте минеральные вяжущие вещества. 2. Какими общими свойствами обладают минеральные вяжущие вещества? 3. К какому классу по условию твердения и эксплуатации относится портландцемент? 4. Общая технология получения портландцемента. 5. Чем мокрый способ получения портландцемента отличается от сухого? 6. Какие минералы входят в состав портландцемента? 7. Что обеспечивает портландцементу гидравлические свойства? 8. По каким показателям оценивают качество портландцемента? 9. Что такое портландцемент? 10. Понятие химического и минерального состава цемента. 11. Какими физическими и механическими свойствами обладает портландцемент и цементный камень? 12. Опишите методику определения нормальной густоты цементного теста и связи этой характеристики со свойствами цементного камня. 13. Какие виды цемента Вы знаете? 73 ЛАБОРАТОРНАЯ РАБОТА СХВАТЫВАНИЯ ЦЕМЕНТА 17-ОПРЕДЕЛЕНИЕ СРОКОВ Цель работы: изучить методику определения сроков схватывания цемента, закрепить навыки пользования техническими и аналитическими весами, мерной посудой, работы с прибором Вика. Материалы и оборудование: Материалы: цемент, вода. Оборудование: прибор Вика с иглой и пестиком, кольцо к прибору Вика, чаша для приготовления цементного теста. I. Теоретическая часть. Начало и конец схватывания вяжущего вещества в строительной технике имеет большое значение для технологии производства строительных работ. Минеральные вяжущие вещества, в том числе и цемент, обычно используют в виде теста, состоящего из вяжущего и воды, причем вода является химическим реагентом, превращающим тесто в соответствующий камень. Последний процесс условно можно разделить на два этапа – схватывание и твердение, которые должны протекать только после того, как тесто будет приготовлено, доставлено к месту укладки и уложено в бетонную конструкцию. В связи с этим при исследовании свойств вяжущих веществ всегда определяют сроки их схватывания. Сроки схватывания для цементов по началу схватывания 45минут и по концу схватывания 12часов, для гипса начало – не ранее 4 минут, конец – не ранее 6 и не позже 30минут. II. Методика выполнения работы: Сроки схватывания определяют на цементном тесте нормальной густоты с помощью прибора Вика, но вместо пестика на конце стержня закрепляют иглу, а пестик устанавливают сверху; при этом масса подвижной части остается разной 300± 2 г. Перед началом испытаний проверяют, свободно ли опускается стержень прибора, чистоту поверхности иглы и отсутствие ее искривлений, а также нулевое показание прибора. 1 Для приготовления цементного теста берут 400 г цемента и высыпают его в сферическую металлическую чашу, предварительно протертую влажной тряпкой. В цементе делают углубление, в которое в один прием выливают воду в количестве необходимом ( ориентировочно) для получения теста нормальной густоты. Обычно для первого пробного затворения берут 25…26% воды от массы цемента, то есть около 100мл. Воду отмеряют мерным цилиндром с точностью 0,5 г, а затем вливают ее в чашу, стараясь заполнить углубление в цементе. В воду насыпают цемент, находящийся на бортах чаши. В это же время включают секундомер. Через 30 секунд смесь воды с цементом в чаше сначала медленно, а затем быстрее в течении 5 минут перемешивают стальной лопаткой во взаимно перпендикулярных направлениях. После этого порцию полученного 74 цементного теста лопаткой в один прием укладывают в кольцо прибора, которое находится на металлической пластине. Последнюю вместе с кольцом и цементным тестом несколько раз встряхивают, уплотняя тесто, затем избыток его снимают вровень с краями кольца влажным шпателем( ножом).Приготовленное тесто помещают в кольцо прибора Вика и устанавливают на столик прибора. Стержень опускают до прикосновения иглы с поверхностью теста и в том положении закрепляют винтом. Затем винт освобождают, давая стержню с иглой свободно погружаться в тесто. В начале испытания, пока тесто находится в жидком состоянии, во избежание сильного удара иглы о пластину рекомендуется слегка придерживать ее при погружении в тесто. Иглу можно свободно опускать, как только тесто загустеет на столько, что опасность повреждения иглы будет исключена. Момент начала схватывания определяют при свободном опускании иглы. Иглу погружают в тесто через каждые 10 минут, при этом кольцо после каждого погружениям передвигают таким образом, чтобы игла не попадала в прежнее место. После каждого погружения иглу вытирают. Во время испытаний прибор должен находиться в затененном месте, где нет сквозняков, и не должен подвергаться сотрясениям. 2 Началом схватывания цементного теста считается время, прошедшее от начала затворения теста ( момент приливания воды) до момента, когда игла не доходит до пластины на 1-2 мм; концом схватывания – время от начала затворения до момента, когда игла опускается в тесто не более чем на 1-2мм. Результаты записывают в таблицу 1. III. Заключение: Начало схватывания цементного теста ___ минут, конец схватывания ___ часа. Подпись преподавателя:_____________ Вопросы для самоконтроля: 1. Чем свойства пуццоланового портландцемента отличаются от свойств рядового? 2. С какой целью при помоле клинкера вводят гипс? 3. Чем клинкер отличается от портландцемента? 4. Где применяют в строительстве портландцемент, шлако- и пуццолано- вый портландцементы? 5. С какой целью определяют равномерность изменения объема цементного теста при твердении? 6. Какие виды портландцемента вы знаете? 7. По каким признакам можно определить пуццолановый портландцемент? 8. Как определить среднюю (насыпную) плотность портландцемента? 9. От чего зависит насыпная плотность портландцемента? 10. Какие периоды твердения портландцемента характеризуют время начала и конца схватывания? 75 11. Какие требования предъявляет стандарт на портландцемент по срокам схватывания? 12. С какой целью определяют нормальную густоту цементного теста? 13. На каком приборе и в каких единицах определяют нормальную густоту цементного теста? 14. На смеси какого состава определяют марку цемента? 15. Какой режим твердения используют при определении марки цемента? 16. Как Вы понимаете выражение - марка портландцемента 400, 500? 17. Каким образом можно рассчитать ориентировочно марку цемента, образцы которого твердели 7 суток? 18. С какой целью при определении марки цемента предварительно определяют нормированную подвижность цементного раствора? 19. От чего зависит марка цемента? 20. Какие экспериментальные данные необходимо иметь для расчета марки цемента? Перечень ГОСТов, используемых при выполнении лабораторной работы 76 7 ИНФОРМАЦИОННОЕ ОБЕСПЕЧЕНИЕ ОБУЧЕНИЯ Перечень рекомендуемых учебных изданий, Интернет-ресурсов, дополнительной литературы Основные источники: 1. Захаров Н.Л. Начало техники лабораторных работ: учеб. пособие / Н.Л. Захаров. — Л. ; Издательство «Химия», 1981. – 192с. 2. Киреева, Ю.И. Современные строительные материалы и изделия / Ю.И. Киреева. - Ростов н/Д.: Феникс, 2010. - 256 с. 3. Горшков В.С. Методы физико-химического анализа вяжущих веществ. : учеб. пособие / В.С.Горшков, В.В. Тимашов. М., Высшая школа, 1981. –160с. 4. Булатов М.И. Практическое руководство по физико-химическим методам анализа./ М.И. Булатов, И.П. Калинкин. –Л.: Химия, 1986. –378 с. 5. Дорохова Е.Н. Аналитическая химия. Физико-химические методы анализе / Е.Н. Дорохова, Г.В.Прохорова. –М.: Высшая школа, 1991. –256 с. 6. Лайтинен Г.А. Химический анализ : учеб. пособие/ Г.А. Лайтинен, В.Е. Харрис – М. ; Издательство «Химия», 1979. – 400с. 7. Ольшакова К.М. Аналитическая химия. : учеб. пособие / Ольшакова К.М., Пискарева С.К. М., Химия, 1980. – 224с. 8. Саркисов П.Д. Технический анализ и контроль производства. : учеб. пособие / П.Д. Саркисов, А.С. Агарков. – М., Стройиздат, 1976. – 80с. 9. Попов Л. Н. Лабораторные работы по дисциплине «Строительные материалы и изделия»: Учеб. Пособие / Л. Н. Попов, Н. Л. Попов - М.: ИНФРАМ, 2003. – 219 с. 10. Белов В.В. Лабораторные определения свойств строительных материалов / В.В. Белов В.Б. Петропавловская, Ю.А. Шлапаков – М.: Издательство Ассоциации строительных вузов, 2004. 11. Васильев В. П. Аналитическая химия. Сборник вопросов,упражнений и задач / В. П. Васильев Л. А. Кочергина, Т. Д. Орлова. – М.: Дрофа, 2003. – 320 с. 12. Васильев В. П. Аналитическая химия. Лабораторный практикум / В. П. Васильев, Р. П. Морозова, Л. А. Кочергина. – М.:Дрофа, 2004. – 416 с. 13. Клещев Н.Ф. Задачник по аналитической химии / Н.Ф. Клещев [и др.]. – М.: Химия, 1993. 221 с. 14. Коренман Я. И. Задачник по аналитической химии. Титриметрические методы анализа / Я. И. Коренман [и др.]. – Воронеж: ВГТА., 2001. – 336 с. 15. Лебедева М.И. Практикум по аналитической химии / М.И. Лебедева, Б.И. Исаева [и др.]. Тамбов: Издательство ТГТУ, 2002.79 с. 16. Васильев В. П. Аналитическая химия: в 2 кн. – Кн. 1. Титриметрические и гравиметрический методы анализа. / В. П. Васильев. – М.: Дрофа, 2002.– 368 с. 77 17. Золотов Ю.А. Основы аналитической химии: в 2 кн. – Кн. 1./ Ю.А. Золотов и др. –М.: Высшая школа, 1999. – 234 с. 18. Лурье Ю. Ю. Справочник по аналитической химии /Ю. Ю. Лурье. – М.: Химия, 1989. – 448 с. 19. Аналитическая химия. Химические методы анализа / под ред. О. М. Петрухина. – М.: Химия, 1993. – 400 с. 20. Практикум по физико-химическим методам анализа / Под ред. О.М. Петрухина. – М.: Химия, 1987. 245 с. 21. Основы аналитической химии: в 2 кн. / под ред. Ю. А. Золотова. – М.: Высш. шк., 2001. – Кн. 1: Общие вопросы. Методы разделения. – 351 с. 22. Основы аналитической химии: в 2 кн. / под ред. Ю. А. Золотова. – М.: Высш. шк., 2001. – Кн. 2: Методы химического анализа. – 494 с. Действующие стандарты и технические условия на методы испытаний и оформление документации 1. ГОСТ 310.2-85 – ГОСТ 310.4-85. Портландцемент. Методы испытаний. 2. ГОСТ 22688-77. Известь строительная. Методы испытаний 3. ГОСТ 7025-91 – Кирпич и камни керамические и силикатные. Методы определения водопоглощения, плотности и контроля морозостойкости. 4. ГОСТ 27180-2001 – Плитки керамические. Методы испытаний. 5. ГОСТ 1.5 - 2001 Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Общие требования к построению, изложению, оформлению, содержанию и обозначению 6. ГОСТ 2.105—95 Единая система конструкторской документации. Общие требования к текстовым документам 7. ГОСТ 7.32.2001 Система стандартов по информации, библиотечному и издательскому делу. Отчет о научно-исследовательской работе. Структура и правила оформления Интернет-ресурсов httр://files.stroyinf.ru/ standart Gost.ru Дополнительные источники: 1. Мороз И.И. Технология строительной керамики: / И.И. Мороз учебное пособие. - М.: Кнорус, 2011. -384 с. 2. Попов К.Н. Строительные материалы и изделия/К.Н. Попов.,М.Б. Кад - до : Учеб. – М.: Высш. шк., 2002. – 367 с. 3. Микульский В.Г. Строительные материалы .Материаловедение.: Учеб. издание. / В.Г.Микульский, [и др.]. - М.: Издательство Ассоциации строительных вузов, 2004. -536 с. 4. Современные строительные материалы. Технологии работ: справочное пособие. - М.: Стройинформ, 2007. - 720 с. 78