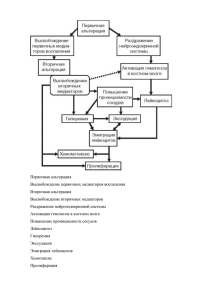
1 Лекция ВОСПАЛЕНИЕ Воспаление – это типический патологический процесс, который возникает в результате повреждения ткани и проявляется комплексом структурных, функциональных и метаболических нарушений, а также расстройствами микроциркуляции. Воспаление является наиболее распространенным типовым патологическим процессом. Оно представляет собой важную защитно-приспособительную реакцию, эволюционно сформировавшуюся, как способ сохранения целого организма ценой повреждения его части. ЭТИОЛОГИЯ ВОСПАЛЕНИЯ Причиной воспаления является любой фактор, способный вызвать повреждение тканей, - флогоген. Флогогены бывают: экзогенные и эндогенные. Внешние флогогены могут быть: биологическими (чаще всего инфекционными - бактерии, риккетсии, вирусы, грибы, простейшие, насекомые), физическими (механическая - инородные тела, давление, разрыв, термическая, лучевая энергия), химическими (кислоты, щелочи, боевые отравляющие вещества). Внутренние причины: очаг некроза ткани, гематома, образовавшиеся камни, отложение солей, иммунные комплексы и др. Так как частой причиной воспаления являются инфекционные агенты, то по этиологии может быть: инфекционное (септическое) и неинфекционное (асептическое). Признаки воспаления. Внешние (местные): покраснение (rubor) – вызвана артериальной гиперемией, припухлость (tumor) – вызвано экссудацией, повышение местной температуры, или жар (calor) – повышение обмена веществ и теплопродукции в очаге воспаления, а также артериальной гиперемие (при которой в ткань поступает много теплой артериальной крови), боль (dolor) – в результате раздражения рецепторов медиаторами воспаления, механическим давлением экссудата, ацидозом, нарушение функции (functio laesa) – вследствие повреждения и гибели клеток. Общие проявления воспаления: лихорадка, лейкоцитоз, повышенная скорость оседания эритроцитов, ускоренный обмен веществ, измененная иммунологическую реактивность, явления интоксикации организма. ПАТОГЕНЕЗ ВОСПАЛЕНИЯ Любое воспаление включает 3 основных компонента: • альтерацию (alteratio, от лат - изменять) - повреждение клеток и тканей; • расстройство микроциркуляции с экссудацией и эмиграцией; • пролиферацию - размножение клеток и восстановление целостности ткани. Стадия альтерации В ее основе лежат две группы реакций: 1.повреждение клеток и внеклеточных структур, 2.образование медиаторов воспаления. Различают первичную и вторичную альтерацию. Первичная альтерация является результатом повреждающего воздействия самого флогогенного фактора, поэтому ее выраженность при прочих равных условиях (реактивность организма, локализация) зависит от его свойств. Первичная альтерация не является компонентом воспаления, так как воспаление это реакция на повреждение, вызванное флогогеном, т.е. на первичную альтерацию. Вторичная альтерация – это повреждение ткани, возникающее в результате действия факторов, которые образовались вследствие первичной альтерации. 2 Вторичная альтерация не зависит от воспалительного агента, для ее развития необязательно дальнейшее присутствие флогогена в очаге. Это необходимый компонент воспаления как защитно-приспособительной реакции, направленный на скорейшее отграничение (локализацию) флогогена и (или) поврежденной под его воздействием ткани от остального организма. Факторы вызывающие вторичную альтерацию. 1.медиаторы воспаления 2.свободные радикалы и пероксиды 3.гипоксия, как результат местного нарушения кровообращения 4.местный ацидоз 5.повышение осмотического (выход ионов калия из поврежденных клеток) и онкотического давления в очаге воспаления (плазменный источник - поступление белков из крови при экссудации и тканевой фактор - расщепление больших белковых молекул на мелкие под действием лизосомальных ферментов). Повышение обмена веществ при воспалении («пожар обмена» - обмен веществ повышен, но «горение» идет не до конца, с образованием недоокисленных продуктов) происходит в основном за счет углеводов, усиливается их окисление и гликолиз. Увеличивается потребление кислорода воспаленной тканью. Расщепление углеводов не доходит до конечных продуктов - углекислого газа и воды. Дыхательный коэффициент снижается. В ткани накапливаются недоокисленные продукты углеводного обмена - молочная кислота. Расстройства микроциркуляции в очаге воспаления 1.Кратковременный спазм артериол, сопровождающийся побледнением ткани. Является результатом рефлекторного спазма артериол. Длится от нескольких десятков секунд до нескольких минут, так что его не всегда удается отметить. 2.Артериальная гиперемия, механизм развития. 1.нейрогенный механизм (нейротонический и нейропаралитический) имеет значение в первые минуты развития артериальной гиперемии. 2.влияние физико-химических факторов: ацидоза, увеличения содержания ионов калия в ткани, гипоксии. 3.влияние продуктов метаболизма: молочной кислоты. 4.действие медиаторов воспаления: гистамина, серотонина, брадикинина, простагландинов. 3. Венозная гиперемия. Она может развиться уже через несколько минут после воздействия флогогена и характеризуется значительной продолжительностью - сопровождает весь ход воспалительного процесса. В механизме венозной гиперемии различают 3 группы факторов: а)внутрисосудистые (нарушения реологических свойств крови) и ее циркуляции. -увеличение вязкости крови вследствие ее сгущения, обусловленного экссудацией, потери альбуминов, увеличения содержания глобулинов, изменения коллоидного состояния белков; -микротромбообразование вследствие активации свертывающей системы крови; -краевое стояние лейкоцитов, -набухания и агрегации эритроцитов; -замедление тока крови, б)изменения сосудистой стенки, 3 -потеря сосудистого тонуса (вследствие паралича нервно-мышечного аппарата сосудов); -снижение эластичности сосудистой стенки; -набухание эндотелия и повышение его адгезивности, в результате чего просвет сосудов сужается, создаются условия для прилипания лейкоцитов к эндотелию; в)внесосудистые -сдавление венозных сосудов отечной, инфильтрированной тканью; -снижение упругости соединительной ткани. Многие из перечисленных факторов являются и причинами, и одновременно следствиями развивающейся венозной гиперемии. 4.Стаз. Расстройства микроциркуляции при воспалении сопровождаются явлениями экссудации и эмиграции. Экссудация (exsudatio, от лат. - потеть) – выход жидкости и растворенных в ней компонентов плазмы крови из кровеносных сосудов в ткань. В основе экссудации лежат 3 механизма: 1)повышение проницаемости сосудистой стенки; 2)увеличение кровяного (фильтрационного) давления в сосудах очага воспаления вследствие гиперемии; 3)возрастание осмотического и онкотического давления в воспаленной ткани в результате альтерации и начавшейся экссудации. Основным фактором экссудации является повышение проницаемости сосудов, которое имеет две фазы - немедленную и замедленную. Немедленная - мимолетное увеличение проницаемости стенок микрососудов при воспалении, обнаруживают при слабом повреждении. В этом случае повышение проницаемости возникает практически сразу, достигает максимума в течение 5-10 мин и исчезает через 15-30 мин. Оно связано с высвобождением гистамина, серотонина и брадикинина. Замедленное сразу после повреждения - увеличение проницаемости стенок микрососудов при воспалении обнаруживают при глубоком повреждении микрососудов. Резкое повышение проницаемости стенок микрососудов при этом возникает сразу после повреждения, нарастает в течение 1-5 ч и сохраняется 1-5сут. И может быть замедленное (отсроченное) - пролонгированное увеличение проницаемости стенок микрососудов при воспалении характеризуется латентным периодом после повреждения с последующим быстрым увеличением проницаемости, продолжающимся несколько часов или дней. Такой тип ответа сосудов часто встречается в патологии: при легком и среднем по тяжести термическом повреждении, ионизирующем и ультрафиолетовом облучении, действии бактериальных токсинов, аллергии замедленного типа и др. В этих случаях характерного сокращения и округления эндотелиальных клеток не происходит, а нарушаются межэндотелиальные сцепления в капиллярах и венулах. Увеличение проницаемости при этом обусловлено прямым действием патогенных факторов. В зависимости от качественного состава различают следующие виды экссудатов. Серозный экссудат - характерен для воспаления серозных оболочек (серозный перитонит, плеврит, перикардит, артрит и др.), реже встречается при воспалении в паренхиматозных органах. Экссудат при серозном воспалении слизистых оболочек характе- 4 ризуется большой примесью слизи. Такое воспаление называется катаральным (катаральный ринит, гастрит, энтероколит и др.). Чаще всего серозный экссудат наблюдается при ожоговом, вирусном, аллергическом воспалении. Фибринозный экссудат. Его разновидность (крупозный и дифтеритический экссудат). Если фибринозная пленка расположена рыхло, поверхностно, легко отделяется без нарушения целостности слизистой, такое воспаление называется крупозным. Оно наблюдается в желудке, кишечнике, трахее, бронхах. В том случае, когда пленка плотно спаяна с подлежащей тканью и ее удаление обнажает язвенную поверхность, речь идет о дифтеритическом воспалении. Оно характерно для миндалин, полости рта, пищевода. Такое различие обусловлено характером эпителия слизистой оболочки и глубиной повреждения. Фибринозный экссудат может формироваться при дифтерии, дизентерии, туберкулезе. Гнойный экссудат характерен для воспалительных процессов, вызванных кокковой инфекцией, патогенными грибками или химическими флогогенами, такими как скипидар, отравляющие вещества. Гнилостный (ихорозный) экссудат отличается наличием продуктов гнилостного разложения тканей, вследствие чего имеет грязно-зеленую окраску и дурной запах. Образуется в случае присоединения патогенных анаэробов. Геморрагический экссудат характеризуется большим содержанием эритроцитов, что придает ему розовый или красный цвет. Характерен для туберкулезных поражений (туберкулезный плеврит), чумы, сибирской язвы, черной оспы, токсического гриппа, аллергического воспаления. Смешанный экссудат наблюдаются при воспалении, протекающем на фоне ослабленных защитных сил организма и присоединения вследствие этого вторичной инфекции. Биологическое значение экссудата: Положительное - сдавливает отводящие сосуды, межтканевые щели. Тем самым блокируя распространение микробов, токсических веществ по межтканевым щелям. - экссудат уменьшает (разбавляя) концентрацию токсинов и тем самым ослабляет их действие на ткань. - в экссудате содержатся ферменты, которые разрушают токсические вещества и лизируют некротизированные ткани. - экссудат выделяет в ткань иммуноглобулины, которые оказывают антитоксическое и антимикробное действие, а также оказывают и общее защитное действие в связи с наличием неспецифических факторов защиты: лизоцим, комплемент, интерферон, бетализины и др. - с экссудатом в ткань выделяется большое количество фибриногена, который переходит в фибрин и таким образом оказывает защитное действие, препятствуя распространению болезнетворного фактора, главным образом по межклеточным пространствам. Отрицательная роль экссудата. - сдавливает окружающие ткани и приводит к атрофии паренхиматозных органов. Выход лейкоцитов в воспаленную ткань (эмиграция лейкоцитов) Эмиграция - выход лейкоцитов из сосудов в ткань. Осуществляется путем диапедеза через стенку венул. 5 Пусковым моментом активации лейкоцитов является воздействие на рецепторы клеточных мембран разнообразных хемотаксических агентов, высвобождаемых микроорганизмами или фагоцитами, а также образующихся в ткани в результате действия воспалительного агента или под влиянием самих фагоцитов. Лейкоциты выходят из осевого тока крови в плазматический. Этому способствуют нарушение реологических свойств крови, замедление кровотока, изменение его характера. Прилипание лейкоцитов к эндотелию опосредовано следующими факторами: • лейкоциты в фазе инициации воспаления активируются и образуют агрегаты; в результате активации лейкоцита его отрицательный заряд снижается, что уменьшает силы взаимного отталкивания между ним и отрицательно заряженным эндотелием; • между лейкоцитами и эндотелием образуются кальциевые мостики; • в ходе активации в лейкоцитах усиливается синтез специфических гранул, некоторые компоненты которых, например лактоферрин, усиливают адгезивные свойства клеток; Первоначальный контакт лейкоцитов с эндотелием является непрочным, и под влиянием кровотока они могут перекатываться по поверхности фибриновой пленки, но контакт быстро стабилизируется, так как лейкоциты выделяют в зону слипания протеазы. Эмигрируя в ткань, лейкоциты преодолевают два барьера капиллярной стенки: эндотелий и базальную мембрану. Процесс перехода лейкоцита через стенку сосуда продолжается от 2 до 12 минут. Нейтрофилы и макрофаги проходят через эндотелий по межэндотелиальным щелям выпуская свои псевдоподии в пространства между эндотелиоцитами и «раздвигают» клетки. Преодоление базальной мембраны может быть обусловлено двумя механизмами: Первый обусловлен явлениями тиксотропии – при контакте нейтрофила с базальной мембраной ее коллоиды переходят из состояния геля в состояние золя (разжижение мембраны). Нейтрофил легко проходит через золь, после чего золь обратно превращается в гель. Второй механизм заключается в выделении нейтрофилами нейтральных протеаз (эластазы, коллагеназы), которые расщепляют волокнистые компоненты базальной мембраны. Иммигрировавшие лейкоциты отделяются от наружной поверхности сосудистой стенки и амебовидными движениями направляются к центру очага воспаления, что определяется градиентом концентрации хемотаксических веществ в очаге. Скорость движения фагоцитирующих лейкоцитов в тканях составляет около 15 мкм/мин. Она зависит от температуры тела. Максимальная скорость передвижения фагоцитов и их наивысшая функциональная активность отмечаются при температуре от +38 до +39 0 С. Первоначально среди лейкоцитов экссудата в очаге острого воспаления преобладают нейтрофилы, а затем - моноциты/макрофаги. Позже в очаге накапливаются лимфоциты. Замедление кровотока в отдельных разветвлениях микроциркуляторного русла и краевое стояние лейкоцитов могут развиваться быстро, а мигрирующему нейтрофилу достаточно 3-12 мин, чтобы пройти эндотелий, появление нейтрофилов в очаге может наблюдаться уже к 10-й мин от начала воспаления. Скорость аккумуляции нейтрофилов в очаге является наивысшей в первые 2 ч, постепенно снижаясь. Нейтрофилы фагоци- 6 тируют бактерии или другие инородные тела и частицы отмирающих клеточных элементов, параллельно осуществляют внеклеточную поставку ферментов, катионных белков, активных метаболитов кислорода. Одновременно происходит массивное разрушение нейтрофилов, останки которых являются важным стимулом расширения инфильтрации - как нейтрофильной, так и моноцитарной. Как и в норме, большинство нейтрофилов, вышедших в ткань, никогда не возвращается в кровоток. Моноциты преобладают в очаге острого воспаления через 16-24 ч и достигают пика, на третьи сутки. Миграция моноцитов из крови в ткань начинается одновременно с миграцией нейтрофилов. Но вначале меньше, чем у нейтрофилов, скорость аккумуляции моноцитов связана с торможением хемотаксиса этих клеток под влиянием продуктов жизнедеятельности нейтрофилов в течение определенного времени, необходимого для полной выраженности нейтрофильной реакции. В очаге воспаления наблюдаются постепенное превращение моноцитов в макрофаги. Моноциты и макрофаги также являются источником медиаторов воспаления (ферментов, метаболитов кислорода, цитокинов), фагоцитируют бактерии, но в основном участвуют в фагоцитозе останков погибших нейтрофилов. Воспалительная пролиферация - это размножение местных клеточных элементов в очаге воспаления. Пролиферация развивается с самого начала воспаления вместе с явлениями альтерации и экссудации, но становится преобладающей в поздний период процесса. Важным условием прогрессирования пролиферации является эффективность очищения очага воспаления от микроорганизмов, продуктов альтерации тканей, погибших лейкоцитов (раневое очищение). Основная роль в этом отводится макрофагам - гематогенного (моноциты) и тканевого (гистиоциты) происхождения. Фагоцитоз был открыт и понят как важнейший элемент воспаления и естественного иммунитета И.И. Мечниковым в 1882 г. И.И. Мечников выделил 4 фазы фагоцитоза: 1) фаза приближения: выход лейкоцита из сосуда и приближение к объекту фагоцитоза; 2) фаза прилипания (контактная); 3) фаза погружения: обволакивание и погружение объекта внутрь фагоцита; образуется особая вакуоль, где скапливаются лизосомы; 4) фаза переваривания, результатом которой могут быть 2 варианта исхода: а) адекватное дозированное освобождение лизосомальных ферментов, разрушающее только флогоген (сам фагоцит остается интактным); б) чрезмерное выделение лизосомальных ферментов, что ведет к разрушению объекта фагоцитоза и самого фагоцита. Стадия пролиферации включает: 1. Размножение клеток, собственно пролиферация, 2.синтез внеклеточных компонентов соединительной ткани – коллагена, эластина, гликопротеинов. Факторы вызывающие активацию размножения клеток в очаге воспаления: 1.уменьшение концентрации в ткани кейлонов - это вещества белковой природы, которые образуются зрелыми клетками. Кейлоны являются ингибиторами клеточного деления. При повреждении и гибели клеток в очаге воспаления концентрация кейлонов уменьшается, а следовательно снимается тормозное влияние кейлонов на малодифференцированные (камбиальные) клетки. Они начинаются делиться. Деление продолжается до тех пор, пока концентрация кейлонов не увеличится до уровня, который существовал в неповрежденной ткани. 7 2.Увеличение концентрации в ткани стимуляторов пролиферации – факторов роста, которые поступают в ткань из плазмы крови или являются продуктами клеток, находящихся в очаге воспаления (фактор роста эпидермиса, фибробластов). Пролиферация сменяется регенерацией. Регенерация не входит в комплекс собственно воспалительных явлений, однако непременно следует им и трудно от них отделима. Она состоит в разрастании соединительной ткани, новообразовании кровеносных сосудов, в меньшей степени - в размножении специфических элементов ткани. При незначительном повреждении ткани происходит относительно полная ее регенерация. При образовании дефекта он заполняется вначале грануляционной тканью молодой, богатой сосудами, которая впоследствии замещается соединительной тканью с образованием рубца. ВИДЫ ВОСПАЛЕНИЯ По характеру сосудисто-тканевой реакции различают альтеративное, экссудативноинфильтративное и пролиферативное воспаление. Вид воспаления зависит от реактивности организма, локализации процесса, вида, силы и продолжительности действия флогогена. Альтеративное воспаление характеризуется особой выраженностью явлений дистрофии (вплоть до некробиоза и некроза) и, таким образом, преобладанием их над экссудативно-инфильтративными и пролиферативными. Чаще всего альтеративное воспаление развивается в паренхиматозных органах и тканях (миокард, печень, почки, скелетные мышцы) при инфекциях и интоксикациях, поэтому называется еще паренхиматозным. Экссудативно-инфильтративное воспаление характеризуется преобладанием циркуляторных расстройств с экссудацией и эмиграцией над альтерацией и пролиферацией. Пролиферативное, или продуктивное, воспаление отличается доминированием размножения клеток и разрастания соединительной ткани. Пролиферативное воспаление характерно для хронических заболеваний - туберкулеза, сифилиса, лепры, ревматизма и др., для гранулематозных острых инфекционных процессов - брюшного и сыпного тифов, васкулитов разной этиологии и др., для длительного раздражения кожи химическими веществами. Оно наблюдается вокруг животных паразитов (трихинеллы, цистицерки и т.д.) и инородных тел. ИСХОДЫ ВОСПАЛЕНИЯ Исход воспаления зависит от его вида и течения, локализации и распространенности. Возможны следующие исходы воспаления: 1.Практически полное восстановление структуры и функции (возврат к нормальному состоянию). Наблюдается при незначительном повреждении, когда происходит восстановление специфических элементов ткани. 2. Образование рубца (возврат к нормальному состоянию с неполным восстановлением). Наблюдается при значительном дефекте на месте воспаления и замещении его соединительной тканью. Рубец может или же привести к нарушениям функций в результате: а) деформации органа или ткани (например, рубцовые изменения клапанов сердца); б) смещения органов (например, легких в результате образования спаек в грудной полости в исходе плеврита). 3. Гибель органа и всего организма - при некротическом воспалении. 8 4. Гибель организма при определенной локализации воспаления - например, от удушья вследствие образования дифтеритических пленок на слизистой оболочке гортани. Угрожающей является локализация воспаления в жизненно важных органах. 5. Развитие осложнений воспалительного процесса: а) поступление экссудата в полости тела с развитием, например, перитонита при воспалительных процессах в органах брюшной полости; б) образование гноя с развитием абсцесса, флегмоны, эмпиемы, пиемии; в) склероз или цирроз органа в результате диффузного разрастания соединительной ткани при пролиферативном воспалении. 6. Переход острого воспаления в хроническое.