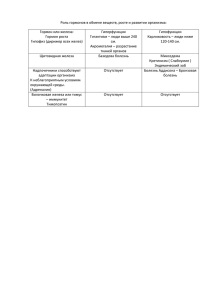
Лекция № 22. Железодефицитная анемия у детей. Выделяют несколько стадий железодефицитных состояний (ЖДС): Латентный дефицит железа (ЛДЖ) – состояние, характеризующееся снижением тканевых запасов и транспортного фонда железа при нормальном уровне гемоглобина. Железодефицитная анемия (ЖДА) – патологическое состояние, характеризующееся снижением содержания гемоглобина вследствие дефицита железа в организме в результате нарушения его поступления, усвоения или патологических потерь. Этиология. Критические возрастные периоды обмена железа в организме: антенатальный, первый год жизни, ранний и подростковый возраст. Факторы риска ЖДС в антенатальном периоде: Глубокий или длительный дефицит железа в организме матери. Нарушение маточно-плацентарного кровообращения, фето-плацентарная недостаточность. Фето-плацентарные и фето-материнские кровотечения. Внутриутробная мелена. Многоплодие. Причины ЖДС в грудном возрасте: Недоношенность. Синдром задержки внутриутробного развития плода (ЗВУР). Ускоренные темпы развития. Истощение антенатальных запасов железа к 4-5 месяцам жизни. Раннее искусственное вскармливание. Вскармливание цельным коровьим или козьим молоком, кефиром в первые 8 месяцев жизни. Непереносимость белков коровьего молока. Причины ЖДС в раннем возрасте: Манифестация аномалий конституции. Пищевая аллергия. Частые инфекционные заболевания. Грубые нарушения диететики. Рахит, гипотрофия. Причины ЖДС в подростковом возрасте: Физиологические особенности пубертата (период второго ростового скачка, быстрое увеличение мышечной массы, повышенный синтез половых гормонов и появление вторичных половых признаков). Половая принадлежность подростка. Алиментарный фактор («голодные» диеты). Чрезмерные физические нагрузки. Хронические заболевания ЖКТ, язвенная болезнь. Вредные привычки. Дополнительные причины ЖДС: Дисбактериоз кишечника (клинически выраженный). Глистные и паразитарные инфекции (особенно гематофаги). Синдром мальабсорбции. Кровотечения из желудочно-кишечного тракта (грыжа пищеводного отверстия диафрагмы, множественные дивертикулы толстой кишки, дивертикул Меккеля, болезнь Крона, опухоли и полипы желудка и кишечника). Врожденные пороки сердца. Хронические и врожденные болезни почек. Хроническая и врожденная бронхолегочная патология. Алиментарная недостаточность. Патогенез. I этап — прелатентный дефицит железа. Дефицит железа сопровождается его мобилизацией из депо. При этом депо обедняется, снижается уровень ферритина. Количество сывороточного железа, уровень гемоглобина остаются нормальными. II этап — ЛДЖ («анемия без анемии»). При прогрессирующем выведении железа из депо снижается уровень сывороточного железа. Низкое содержание ферритина. Общая железо связывающая способность сыворотки (ОЖСС) крови нормальная, уровень гемоглобина приближается к нижней границы нормы. III этап - манифестный дефицит железа или стадия анемии. Депо полностью истощено. Уровень сывороточного железа низкий. Повышается ОЖСС. Снижается количество гемоглобина и степень насыщения эритроцитов гемоглобином, при этом количество эритроцитов может оставаться нормальным. IV этап - глубокий дефицит железа. Резко снижено содержание тканевого железа. Начинается распад клеток, в результате которого железо освобождается в виде ферритина, но этого количества не хватает для полноценного эритропоэза. Показатели гемоглобина низкие, количество и степень насыщения гемоглобином эритроцитов снижены, появляются атипичные их формы. Классификация: стадии ЖДС: I. Латентный дефицит железа II. Железодефицитная анемия: 1. Легкая степень – гемоглобин 109 – 90 г/л; 2. Средняя степень тяжести – 90 – 70 г/л; 3. Тяжелая степень - < 70 г/л. Клиника ЖДА: I. Сидеропенический синдром - появляется первым и является более специфичным для ЖДА. В большей степени присуще взрослым детям. Дистрофические изменения покровного эпителия (сухость кожи, уплощение и ломкость ногтей, сухие, истонченные, ломкие волосы). Диспепсические расстройства. Извращение вкуса и обоняния. Задержка психомоторного и интеллектуального развития. Мышечная гипотония. Снижение местного иммунитета. II. Анемический синдром - появляется в клинике последним. Является менее специфичным. Ярко выражен у детей раннего возраста. Бледность кожи и слизистых оболочек (бледность кожи имеет алебастровый или зеленоватый оттенок). Снижение аппетита вплоть до анорексии. Астено-вегетативный симптомокомплекс (снижение работоспособности, быстрая утомляемость, непереносимость душных помещений). Нарушения со стороны сердечно-сосудистой системы (тахикардия, систолический шум на верхушке). Диагностика. 1. ОАК: Количество эритроцитов (RBC) = 3,66 -5,12 ×1012/л Уровень гемоглобина (Hb) = 120 – 140 г/л Цветовой показатель = 0,85 – 1,05 Среднее содержание гемоглобина в эритроците (отражает абсолютное содержание гемоглобина в одном эритроците) (MCH) = 27 – 31пг (пикограмм, 1 пг = 10-12 г) Средняя концентрация гемоглобина в эритроците (MCHC) = 32 – 36 г/л; (320 – 360%) Показатель анизоцитоза (RDV) – дает количественную оценку разброса эритроцитов по объему, оценивается степень выраженности анизоцитоза. Средний объем эритроцитов (MCV) – определяется по номограмме или автоматически в гематологических счетчиках = 72 – 94 fl (фемтолитры) 2. Описание морфологии эритроцитов: Для ЖДА характерно наличие в периферической крови эритроцитов разных по: размеру (анизоцитоз), форме (пойкилоцитоз), а также гипохромных клеток с зоной просветления в центре, напоминающих кольцо (анулоцитоз) 3. Исследование феррокинетики: Показатели транспортного и депонированного фонда железа: Сывороточное железо: новорожденные дети = 5,0 – 19,3 мкмоль/л дети старше 1 месяца = 10,6 – 33,6 мкмоль/л ОЖСС – косвенно отражает количество свободного трансферрина в плазме = 40,6 – 62,5 мкмоль/л Ферритин сыворотки крови: новорожденные = 175 мг/л в возрасте 3 месяцев = 146 мг/л в возрасте 6 месяцев = 51 мг/л в возрасте 9 месяцев = 37 мг/л в 1 год = 32 мг/л в 10 лет = 34 мг/л в 14 лет = 36 мг/л Лабораторные критерии ЛДЖ Возраст ребенка Показатели гемоглобина (г/л) 1 – 12 месяцев 125 - 110 1 – 3 года 118 - 110 3 – 5 лет 120 - 110 6 – 11 лет 125 -120 ≥ 12 лет 130 - 120 Сывороточное железо < 14 мкмоль/л Сывороточный ферритин < 20 мкг/л RBC, ЦП, MCH, MCHC, MCV, ОЖСС в норме Степень тяжести Легкая Возраст 1 мес – 5 лет 6 – 11 лет ≥ 12 лет Средняя 1 мес. ≥ 12 лет Тяжелая 1 мес. ≥ 12 лет RBC 1012/л HB (г/л) 5,0 – 3,5 10990 11990 11990 MCH (п/г) Критерии тяжести ЖДА MCHC MCV ОЖСС (г/л) (fl) (мкм/л) сыв. железо (мкм/л) Ферритин мкг/л 63 - 70 10 - 9 < 15 - 12 ≤ 77 72 ≤ 27 ≤ 32 ≤ 80 ≤ 80 3,5 – 2,5 89 70 ≤ 27 ≤ 27 ≤ 72 80 70 - 80 8-7 < 15 - 12 < 2,5 < 70 < 27 < 32 < 72 > 80 <7 < 12 Лечение: 1. Лечебно-охранительный режим: Ограничение физической нагрузки на весь период манифестного дефицита железа: временно ребенка переводят из основной физкультурной группы в подготовительную, освобождают от участия в спортивных соревнованиях, приостанавливают занятия в спортивных секциях, в плавательном бассейне. Дополнительный дневной сон (отдых). Аэротерапия – ежедневные прогулки на улице, частые проветривания и поддержание оптимального температурного режима (22о - 23оС) в жилых помещениях. 2. Диетотерапия. Самую высокую биодоступность имеет лактоферрин – железо грудного молока (40 – 50%), среднюю – гемовое железо, содержащееся в мясе и рыбе (18 – 25%), низкую – негемовое железо, содержащееся в продуктах растительного происхождения (2 –7%). Источники гемового железа (мг/ 100 г): печень (9), язык говяжий (5), мясо кролика (4,4), мясо индейки (4), мясо курицы (3), скумбрия (2,3), сазан (2,2), налим (1,4). Содержание железа в продуктах растительного происхождения (мг/100 г): грибы сушеные (35), морская капуста (16), шиповник свежий (11,5), толокно (10,7), гречка, овес (7,8), персики (4,1), груша и яблоки (2,32,2), слива и абрикосы (2,1), алыча, черешня, малина, крыжовник, укроп (1,9-1,6), свекла, капуста цветная, смородина черная, морковь, земляника, дыня (1,4-1,0). На период лечения ЖДА исключают (или ограничивают, если возраст больного не позволяет полностью исключить) употребление молока – продукта, богатого кальцием (кальций и железо находятся в конкурирующих взаимоотношениях за рецепторы для всасывания на энтероцитах), крупяных и макаронных изделий (бедны витаминами и минеральными соединениями, содержат пищевые волокна, которые неблагоприятно влияют на кишечное всасывание железа), чая, кофе, какао (содержат танин, фитин). Таким образом, в подборе лечебной диеты оптимальным является сочетание мясных и рыбных продуктов с овощными гарнирами и фруктовыми соками. «Гемовую» диету необходимо соблюдать в течение основного курса ферротерапии и желательно продолжать в период профилактического лечения. 3. Заместительная терапия препаратами железа. Принципы: Возместить дефицит железа без железосодержащих препаратов невозможно. Терапия ЖДС должна проводиться препаратами железа для энтерального приема. Гемотрансфузии при ЖДА должны выполняться только по жизненным показаниям. Терапия ЖДА не должна прекращаться после нормализации уровня гемоглобина. Современные препараты железа Названия препаратов Лекарственные формы Количество активного железа в препарате (мг) Ранний возраст (до 3 – х лет) Феррум Лек сироп Мальтофер капли Гемофер капли Актиферрин капли Дошкольный возраст (с 3 до 6 лет) Феррум Лек сироп Мальтофер сироп Актиферрин сироп Тотема раствор (для приема внутрь) Ферроплекс драже Препубертатный возраст (от 7 до 12 лет), подростки Феррум Лек жевательные таблетки Мальтофер жевательные таблетки Гемофер пролонгатум таблетки Актиферрин капсулы Тардиферон таблетки Тотема раствор (для приема внутрь) Ферроплекс драже 1 мл = 10 1 капля = 2,5 1 капля = 1,5 1 капля = 0,53 1 мл = 10 1 мл = 10 1 мл = 6,8 1 мл = 5 мг 10 100 100 105 34,5 80 1 мл = 5 мг 10 Среднесуточные дозы препаратов железа для энтерального применения: детям до 3 лет = 3-5 мг/кг детям от 3 до 7 лет = 40-120 мг детям старше 7 лет = 120-200 мг Расчет дозы препарата проводится по содержанию в нем активного железа. В первые дни лечебного курса препарат назначается в 1/3 – 1/2 терапевтической дозе и при хорошей переносимости препарата в последующие 5-7 дней доза повышается до полной возрастной. Нецелесообразно сочетать прием препаратов железа с некоторыми медикаментами: тетрациклином, левомицетином, препаратами кальция и антацидами. Показания для парентерального введения железосодержащих препаратов: ургентные состояния, синдром нарушенного кишечного всасывания, состояния после резекции желудка и тонкого кишечника, неспецифический язвенный колит, хронический энтероколит. Длительность основного курса лечения ЖДА зависит от степени тяжести и в среднем составляет 6 –10 недель. Критерии эффективности лечения ЖДА препаратами железа: купирование клинических симптомов ЖДА, появление ретикулоцитарного криза на 7-10 день лечения, ежесуточный прирост гемоглобина на 1 - 2 г/л и достоверный его прирост на 3-4 недели лечения, восстановление морфологии эритроцитов в периферической крови, нормализация показателей сывороточного железа и активности ОЖСС. После нормализации клинико-лабораторных показателей ферротерапия продолжается профилактической дозой, которая составляет ½ от суточной лечебной дозы. Проведение профилактического курса лечения позволяет ликвидировать ЛДЖ и восполнить депо. Продолжительность профилактического лечения зависит от степени тяжести ЖДА: легкая = 6 – 8 недель, среднетяжелая = 8 – 10 недель, тяжелая = 10 – 12 недель. 4. Ферментотерапия. Для увеличения всасывания алиментарного железа и железа из лекарственных препаратов в период заместительной терапии следует назначать ферменты в возрастных дозах на 7 –10 дней. Всего проводят несколько курсов с 5 – 7 - дневными интервалами. Предпочтение следует отдавать комбинированным препаратам (мезим-форте, панзинорм, ораза, абомин). Профилактика: Антенатальная – выявление беременных из групп высокого риска по развитию ЖДА и больных ЖДА и проведение им профилактического или лечебного курса препаратами железа. Постнатальная: сохранение исключительно грудного вскармливания в течение первых 4-5 месяцев жизни; своевременное введение основных прикормов, мяса и рыбы; достаточное пребывание на свежем воздухе; предупреждение и своевременное лечение рахита, гипотрофии; профилактика острых инфекционных заболеваний; для детей, находящихся на искусственном вскармливании, а также для детей, входящих в группу риска по развитию ЖДА, с профилактической целью назначают смеси, обогащенные железом. Доношенным детям смеси вводят с 3 месяцев жизни и недоношенным – с 2 месяцев. Всем детям из группы высокого риска по развитию ЖДА независимо от вида вскармливания, начиная с 2 – месячного возраста, с профилактической целью следует назначать препараты железа. К группе высокого риска по развитию ЖДА относятся дети: с низкой массой тела при рождении, недоношенные, рожденные от многоплодной беременности, с задержкой внутриутробного развития, имеющие высокие темпы физического развития, с лимфатико-гипопластическим диатезом, находящиеся на искусственном вскармливании коровьим молоком. Диспансеризация. I этап – наблюдение за больными ЖДА – 6-10 недель. Больные осматриваются участковым педиатром 1 раз в 2 недели до нормализации показателей гемограммы. Первый анализ крови выполняется не ранее 7-10 - го дня (появление ретикулоцитарного криза), последующий – через 1 месяц от начала лечения (достоверный прирост гемоглобина). Вакцинация больных проводится после нормализации уровня гемоглобина. II этап - наблюдение в стадии ЛДЖ - проводится в отношении двух категорий детей: Больные, вышедшие из состояния манифестного дефицита железа и требующие продолжения профилактического курса. Дети с впервые выявленным ЛДЖ и нуждающиеся в профилактическом лечении сидеропении. В период ЛДЖ больные осматриваются педиатром ежемесячно, исследование гемограммы проводят на 3, 4, 6 и 12 - ом месяцах от начала лечения препаратами железа. Обязательными определяемыми параметрами крови являются: гемоглобин, эритроциты, цветовые индексы, морфология эритроцитов; желательными – ОЖСС, уровень сывороточного железа, ферритин сыворотки крови. Лекция №23. Геморрагический васкулит. Тромбоцитопеническая пурпура. Геморрагический васкулит Геморрагический васкулит (болезнь Шенлейн - Геноха, капилляротоксикоз) — это системное сосудистое заболевание, характеризуется гиперэргическим воспалением капилляров и мелких сосудов. Этиология не установлена. Провоцирующие факторы: Экзогенные: Инфекционный фактор: стрептококковая инфекция (ангина, стрептодермия), острые вирусные инфекции, стафилококковая инфекция, микобактерии туберкулеза. Паразитозы – чаще простейшие. Вакцинные препараты, в первую очередь - живые вакцины. Лекарства: пенициллины, сульфаниламиды, барбитураты. Пищевые аллергены: яйца птиц, рыба, животное молоко, мед, цитрусовые, какао и кофе, шоколад, копчености. Укусы насекомых (комаров, пчел, ос). Травма. Ожоговая болезнь. Эндогенные: Аномалии конституции. Наличие очагов хронической инфекции. Очаги хронической интоксикации (энтеробиоз, лямблиоз, токсокароз и др.) Наследственная предрасположенность к: Сосудистой патологии. Аллергическим и аутоиммунным заболеваниям. Патогенез: 1. Образование в сосудистом русле циркулирующих иммунных комплексов (ЦИК), представленных комплексом АГ (бактериальные токсины, вирусы и др. белковые субстанции) и АТ (Ig всех классов). 2. ЦИК фиксируется на эндотелий капилляров и мелких сосудов, тем самым вызывает образование в ней пор или брешей (повреждение), через которые пропотевает сначала плазма, а затем выходят за переделы сосудистого русла форменные элементы крови, образуя экзантему или энантему. 3. Поврежденные компоненты эндотелия в последующем запускают механизмы аутосенсибилизации с образованием более агрессивных ЦИК против собственного поврежденного эндотелия сосудов, выступающего в роли аутоАГ. 4. Процессы антителообразования выходят из-под контроля и становятся неуправляемыми в результате нарушения клеточного (Т–лимфоцитов) и гуморальных (В–лимфоцитов) звеньев иммунитета, нарушения соотношения CD4 и CD8 потенциала. 5. При повреждении сосудистой стенки выделяются тромбопластические факторы, которые активизируют процессы гиперкоагуляции (I фаза ДВС-синдрома) - агрегацию тромбоцитов, привлечение в место повреждения сосудов плазменных белков свертывания крови. 6. Развивается - тромбообразование в системном капиллярном кровотоке, что позволяет восстановить целостность сосудистой стенки и предотвратить кровопотерю. 7. Поскольку процессы повреждения сосудов и образования ЦИК без лечения идут постоянно и непрерывно, то вскоре наступает истощение механизмов гемостаза. 8. Процессы гиперкоагуляции сменяются гипокоагуляцией (II фаза ДВС – синдрома), т.е. массивными кровотечениями по всей капиллярной сети. Клиническая классификация: Клинические формы: Кожная Кожно-суставная Кожно-абдоминальная Смешанная Степени тяжести: Легкая Среднетяжелая Тяжелая Течение: Молниеносное (3-5 дней) Острое (до 3 недель) Подострое (свыше 3 недель) Рецидивирующее Осложнения: Инвагинация Аппендицит Гломерулонефрит и хроническая почечная недостаточность Клиника. Начало острое, через 3 – 4 недели, после перенесенного инфекционного заболевания или воздействия АГ другой природы. Температура тела повышается до фебрильных цифр, другие симптомы интоксикации. Кожная форма. Типичный кожный элемент – папула, но могут быть везикулы, пузыри, пятна, некротические элементы, единичные или сливные. Часто высыпания сопровождаются зудом и отеком кистей, стоп, лица, которые проходят самостоятельно. Папула не исчезает при надавливании. Излюбленная локализация элементов – область крупных суставов, наружная поверхность ног и ягодицы. Характерна этапность и полиморфизм высыпаний (фаза желтого пятна, красно-бардового цвета, синюшно-красного цвета, пигментация, шелушение), симметричность. Кровоизлияния могут возникать не только на коже, но и слизистых оболочках. Носовые кровотечения не характерны. Кожно-суставная форма - высыпания сочетаются с поражением суставов. В патологический процесс вовлекаются крупные суставы (тазобедренные, коленные, плечевые, локтевые), характерно симметричность поражения, летучий характер болей. Поражение суставов обусловлено серозно-геморрагическим пропитыванием периартикулярных тканей. Кожа над суставом долго остается измененной, напоминающей большой синяк. Суставной синдром может рецидивировать, но исход всегда благоприятный, никогда не бывает гемартрозов и анкилозов. Абдоминальная форма всегда указывает на тяжесть васкулита и очень часто симулирует любую хирургическую патологию. Боли в животе носят интенсивный, схваткообразный характер, которые связаны с кровоизлияниями в субсерозный слой слизистой оболочки и усиленной перистальтикой воспаленного кишечника. Больные беспокойные, «мечутся» в постели, гримаса боли и страдания на лице. Появляются симптомы токсикоза и эксикоза, ацидоза – взгляд тусклый, осиплый голос, сухие слизистые оболочки ротовой полости и губ, вязкая слюна, невнятная речь, липкий пот. Возможна кровавая рвота, кровавый стул, тенезмы. Не характерен положительный симптом раздражения брюшины (симптом Щеткина – Блюмберга), т.к. никогда не бывает кровоизлияний в брюшину. Каждая из перечисленных форм может встречаться изолированно или сочетаться между собой, но всегда присутствуют кожные геморрагии. Почечный синдром - развивается только у 30 – 50% больных и по клиническим проявлениям представляет собой гломерулонефрит без экстраренальных симптомов. Типично начало почечных изменений в конце первой - начале второй неделе заболевания, но возможно и более позднее появление мочевого синдрома в виде эритроцитурии, протеинурии, цилиндрурии. Другие клинические проявления геморрагического васкулита: Заболевание носит системный характер, и весь организм вовлечен в патологический процесс, но наибольшим изменениям подвержены органы, имеющие богатую капиллярную сеть: почки, легкие, сердце, головной мозг: Пневмония не поддается антибактериальной терапии. Кардиопатия. Поражения сердца обусловлены метаболическими нарушениями, что проявляется приглушенностью тонов, лабильностью пульса, нежным систолическим шумом на верхушке сердца. Мозговой синдром проявляется эпилептиформными припадками, галлюцинациями. В основе этих клинических проявлений лежат микрососудистые нарушения и ангионевротический отек мозга. Лабораторная диагностика: 1. ОАК: нейтрофильный лейкоцитоз, увеличенная СОЭ, возможна кратковременная симптоматическая тромбоцитопения. 2. БАК: диспротеинемия, повышение γ – фракции глобулинов, повышение активности СРБ, положительные пробы на деградацию соединительной ткани (ДФА, Гесса, др.). 3. Иммунограмма: повышение концентрации Ig А, снижение количества CD4 и CD8. 4. Коагулограмма свидетельствует о гиперкоагуляции: укорочение времени свертывания крови, повышение уровня фибриногена (норма 200 – 400 мг%), снижение количества свободного гепарина (норма 5 – 7 ЕД), повышение толерантности плазмы к гепарину (норма 7 – 11 минут), уменьшение времени рекальцификации сгустка крови (норма 60 -120 сек), снижение фибринолиза (норма 15 – 26%). Следует запомнить, что длительность кровотечения, ретракция кровяного сгустка, количество тромбоцитов остаются нормальными. Эндотелиальные пробы отрицательные. Лечение комплексное в условиях стационара: 1. Режим строгий постельный продолжается в течение всего периода высыпаний и последующих 2 недель после последнего высыпания. 2. Диета. Необходимо исключить все облигатные аллергены. При абдоминальной форме назначают грудничковый стол для детей раннего возраста и стол №1 по Певзнеру для детей старшего возраста. При наличии почечных осложнений – стол №7. 3. Медикаментозная терапия: Если предшествовала бактериальная инфекция, то коротким курсом проводится антибактериальная терапия. Предпочтительны защищенные аминопенициллины, цефалоспорины II - III поколения, современные макролиды. Антигистаминные препараты показаны при легком кожном синдроме. Глюкокортикостероиды назначают при тяжелых и сочетанных вариантах геморрагического васкулита. Препаратом выбора является преднизолон (1 -2 мг/кг в сутки), но возможно использование полькорталона, метилпреднизолона, дексаметазона, гидрокортизона, триамсиналона в соответствующих дозировках, рассчитанных по преднизолону. Альтернативные средства лечения: нестероидные противовоспалительные препараты показаны при наличии противопоказаний к назначению ГК и сохранении активности при волнообразном течении: вольтарен, диклофенак, индометацин и др. Обязательно назначение антикоагулянтов. Гепарин в дозе 150 – 200 ЕД/кг в сутки, разделенного на 4 – 6 введений (под контролем коагулограммы) восстанавливает проходимость капилляров. Отмена гепарина производится постепенно за счет уменьшения разовой дозы, а не кратности введения. В последние годы предпочтение отдается современным низкомолекулярным гепариноидам – фраксипарину, варфарину, сулодексиду, кальципарину, кливарину. Достоинствами современных гепариноидов являются наличие таблетированных лекарственных форм, пролонгированный механизм действия, отсутствие при их длительном применении таких грозных осложнений как кровотечения. Энтеросорбенты связывают БАВ в просвете кишечника: полифепан, лактофильтрум, энтеросорб, полисорб, смекта. Длительность лечения от 2-4 недель до 3 месяцев, циклы энтеросорбции не должны превышать 10-14 дней (м.б. снижение уровня калия). Антиагрегантные препараты: курантил – 3-5 мг/кг/сут, трентал – 5-10 мг/кг/сут. Длительность лечения – 3-4 нед., при нефрите – 6-12 мес. Мембраностабилизаторы укрепляют сосудистую стенку: аскорбиновая кислота (500 - 700 мг/сут.), витамин Р (20 -50 мг×2-3 раза/сут.), витамин B6 (40 мг×2-3 раза/сут). Лечение почечного синдрома проводят по схеме лечения гломерулонефрита. При абдоминальном синдроме - инфузионная терапия: глюкозо-новокаиновая смесь (1:1) – 10 мл/год жизни, контрикал, трасилол, гордокс, реополиглюкин, свежезамороженная плазма. При упорном волнообразном течении, абдоминальном синдроме – плазмаферез. Прогноз чаще благоприятный. В течение месяца выздоравливают 60%, в течение года – 95% больных. Хронический гломерулонефрит развивается лишь у 1-2% детей. Летальность не превышает 3% в основном за счет молниеносной формы васкулита и развития хронической почечной недостаточности в группе больных с осложненным течением заболевания. Диспансеризация: Больные с простой (кожной) формой геморрагического васкулита подлежат наблюдению в течение 1 года. Больные с другими вариантами заболевания состоят на диспансерном учете у педиатра в течение 5 лет. Осмотры педиатра в течение первого года наблюдения осуществляются каждые 3 месяца, затем 2 раза в год, осмотры отоларинголога и стоматолога – 2 раза в год. Общий анализ мочи исследуют 1 раз в 3 месяца и обязательно на фоне интеркуррентного заболевания при вовлечении почек в патологический процесс. Обследование на энтеробиоз и паразитозы – 1 раз в 6 месяцев. Вакцинация разрешена через 2 года после выздоровления. Плановая терапия не проводится. В весенне-осенний период назначаются курсы мембраностабилизиторов. Больным запрещается купаться в открытых водоемах, принимать солнечные ванны, резко менять климат в течение нескольких лет (выезд на курорты Черного, Средиземного морей, и т.д.). Тромбоцитопеническая пурпура Идиопатическая тромбоцитопеническая пурпура (ИТП) (болезнь Верльгофа) – первичный геморрагический диатез, обусловленный количественной и качественной недостаточностью тромбоцитарного звена гемостаза. Этиология и патогенез. При тромбоцитопенической пурпуре тромбоцитопения развивается вследствие разрушения тромбоцитов посредством иммунных механизмов. Антитела к собственным тромбоцитам могут появляться спустя 1-3 нед. после перенесённых вирусных или бактериальных инфекций, профилактических прививок, приёма лекарственных препаратов при индивидуальной их непереносимости, переохлаждения или инсоляции, после хирургических операций, травм. В ряде случаев какую-либо определённую причину выявить не удаётся. Поступившие в организм антигены (например, вирусы, лекарственные средства, в том числе вакцины) оседают на тромбоцитах больного и индуцируют иммунный ответ. Антитромбоцитарные антитела относят преимущественно к IgG. Реакция «Аг-AT» происходит на поверхности тромбоцитов. Продолжительность жизни тромбоцитов снижается до нескольких часов вместо 7-10 дней в норме. Преждевременная гибель тромбоцитов происходит в селезёнке. Селезенка является не только кладбищем тромбоцитов, но одновременно и местом синтеза антитромбоцитарных АТ, направленных против поврежденных тромбоцитов. Кровоточивость при тромбоцитопенической пурпуре обусловлена: снижением количества тромбоцитов, вторичным повреждением сосудистой стенки в связи с выпадением ангиотрофической функции тромбоцитов, нарушением сократительной способности сосудов из-за понижения концентрации серотонина в крови, невозможностью ретракции кровяного сгустка (Ретракция кровяного сгустка — процесс сокращения, уплотнения и выделения сыворотки крови из начального тромба. В норме индекс ретракции — 48-64 %.). Классификация: 1. По течению: С редкими рецидивами С частыми рецидивами Непрерывно рецидивирующее течение 2. По периодам болезни: Обострение (криз) Ремиссия 3. По клинике: «Сухая» пурпура (отсутствие кровотечения) «Влажная» пурпура (наличие кровотечения) Клиника. Начало заболевания, особенно при остром течении, бурное. Внезапно появляется геморрагический синдром в виде кровоизлияний и кровотечений. Тип кровоточивости - капиллярный. Самочувствие больных существенно не страдает, иногда больные жалуются на вялость, недомогание. Нередко имеет место субфебрильная температура. Кожный геморрагический синдром - наиболее типичный. Он имеется у всех больных. Характерные черты: спонтанность возникновения кровоизлияний, преимущественно по ночам, неадекватность их степени воздействия, полиморфность (от петехиальных элементов до крупных, распространенных экхимозов), полихромность (одновременно на коже можно видеть геморрагии разной окраски – от красноватосиневатых до зеленых и желтых), несимметричность расположения. Кожа больного напоминает «шкуру леопарда». Типичным симптомом являются кровотечения (носовые, десневые, из лунки удаленного зуба, у девочек пубертатного возраста - маточные). Реже наблюдаются мелена, гематурия и другие кровотечения. Нетипичны кровоизлияния в суставы. Кровоизлияния во внутренние органы, мозг редки (2-4% больных). У 10% больных детей может быть умеренная спленомегалия (нижний край селезенки на 1-2 см выступает изпод реберной дуги). Диагностика. 1. Тромбоцитопения в общем анализе крови менее 150×109/л; 2. Увеличение времени кровотечения после стандартной травмы (по Дюке – в норме 2-4 мин.); 3. Положительные эндотелиальные пробы (симптомы «жгута» и «щипка»); 4. Резкое удлинение времени ретракции кровяного сгустка (25 – 50% в норме); 5. Увеличение количества «недеятельных» мегакариоцитов в костном мозге. Лечение. 1. Режим полупостельный, щадящий. 2. Диета, богатая кальцием, с исключением облигатных аллергенов. Отвары, настои из гемостатических фитосборов. 3. Местная терапия при носовых, десневых, желудочно-кишечных, маточных и других кровотечениях. 4. Если исключен ДВС – синдром назначают препараты, улучшающие адгезивно-агрегационные способности тромбоцитов: Σ-аминокапроновую кислоту наружно или внутрь, парентерально (0,05 – 0,1/кг массы тела × 4 раза в сутки), андроксон, пантотенат кальция, препараты магния. 5. Глюкокортикостероиды показаны при генерализованном кожном синдроме и при критически низком количестве тромбоцитов (менее 20×109/л) в общем анализе крови, сочетающимся с кровоточивостью слизистых оболочек. Преднизолон из расчета 2 мг/кг/сут на 2 – 3 недели или в дозе 1 мг/кг – три 10-дневных курса, с 10-дневным перерывом. 6. При тяжелых кровотечениях назначают ГК, внутривенный иммуноглобулин, переливание тромбомассы. 7. При отсутствии полного и стойкого эффекта от гормонотерапии в течение 4 мес. возникают показания к спленэктомии, которая у 80% больных приводит к практическому выздоровлению. 8. Если через 5 мес. после спленэктомии клинические проявления сохраняются, назначают иммунодепрессивные препараты Диспансерное наблюдение. 1. При острой форме заболевания проводится в течение 5 лет, при хронической – до перехода ребенка во взрослую поликлинику. 2. Прививки на фоне десенсибилизирующей терапии возможны через год после острого периода. Противопоказаны прививки живыми вирусными вакцинами. 3. В течение 3-5 лет нецелесообразна смена климата. 4. Диета обычная. 5. Анализы крови с подсчетом числа тромбоцитов в первые 3 мес. после выписки надо делать 1 раз в 2 недели, далее в течение 9 мес. ежемесячно и в дальнейшем раз в 2 мес., а также после каждой перенесенной инфекции. 6. При лечении детей надо избегать ацетилсалициловой кислоты, анальгина, карбенициллина, нитрофурановых препаратов, УВЧ и УФО. Прогноз. Благоприятный. Летальность не выше 2-3%. 75% больных с острой ИТП выздоравливают спонтанно, без всякого лечения. Лекция №24. Гемофилия. «Маски» лейкоза. Гемофилия Гемофилия - наследственное заболевание, сцепленное с «X» хромосомой, поэтому болеют лица мужского пола, женщины являются носителями генных мутаций. Этиология. Формы заболевания: 1. гемофилия «А» - наследственный дефицит VIII фактора; 2. гемофилия «В» - наследственный дефицит IX фактора; 3. гемофилия «С» - наследственный дефицит XI фактора (крайне редкая форма). Патогенез. При гемофилии нарушена плазменная фаза гемостаза. Сразу после травмы кровотечения может и не быть, так как нормально функционирует сосудисто-тромбоцитарный (первичный) гемостаз, который и обеспечивает образование первичного тромба. Первичный тромб не в состоянии обеспечить окончательную остановку кровотечения. При гемофилии страдает вторичный гемостаз, т. е. формирование окончательного (фибринового) тромба. Происходит возобновление кровотечения, которое возникает внезапно, чаще всего через несколько часов (иногда на следующие сутки) после травмы (вмешательства). Клиника. Первые признаки гемофилии проявляются чаще на втором году жизни, когда ребенок начинает самостоятельно ходить и получает случайные травмы. Чрезвычайно редко болезнь манифестирует в периоде новорожденности в виде кровотечений из пупочной ранки, мелены, внутричерепных кровоизлияний, что больше характерно для врожденных коагулопатий, обусловленных дефицитом К-витаминозависимых факторов. В течение первых 6 – 9 месяцев жизни больные даже с тяжелой формой гемофилии не страдают от геморрагий. Считают, что материнское молоко, содержащее тромбопластические субстанции защищает младенцев от раннего проявления болезни. Кровоизлияние в суставы – гемартрозы – характерный симптом гемофилии. Чаще поражаются коленные 42%, локтевые – 35%, голеностопные – 12%, плечевые – 5,5% суставы. Кровоизлияния в сустав возникают спустя 6 - 12 часов после травмы и ночью. Ребенок просыпается от острой боли в суставе. Объективно: сустав увеличен в размерах, кожа над ним напряжена, блестящая, несколько гиперемированная и горячая на ощупь. Ребенок занимает вынужденное положение, обеспечивающее покой пораженному суставу. Параллельно нарушается самочувствие, снижается аппетит, повышается температура тела. При повторных кровотечениях формируется фиброз синовиальной оболочки, околосуставной ткани, мышц, поддерживающих сустав, что приводит к анкилозирующей артропатии и инвалидности. Кровоизлияния в мягкие ткани – гематомы - второй по частоте встречаемости симптом гемофилии, являются следствием ударов или медицинских манипуляций. Геморрагии имеют жидкую, тестоватую консистенцию, широко проникают в ткани, как бы «стелятся» вдоль фасций, выраженность кровоизлияний и их размеры значительно превосходят степень полученной травмы. Внутритканевые гематомы могут приводить к сдавлению мышц, нервов, сосудов конечностей, что является причиной ишемии, параличей и контрактур. Особенно опасны гематомы в мягкие ткани глотки, гортани, средостения, т.к. острое развитие непроходимости дыхательных путей может привести к смертельному исходу. Гематурия чаще развивается у детей старше 5 лет. Причина почечных кровотечений: травмы поясничного отдела, провоцировать гематурию могут ОРВИ, кристаллы оксалатно-кальциевых солей, прием нестероидных противовоспалительных средств, но возможно и спонтанное начало, без всякой видимой причины. Появляется моча темно красного или коричневого цвета из-за перехода гемоглобина в гематин. У части больных появляется дизурия, боли в поясничной области, по ходу мочеточников и мочеиспускательного канала. Обычно после нескольких болезненных позывов к мочеиспусканию из мочевыделительного канала отходят сгустки крови и боль уменьшается. Неврологические нарушения. Поражение центральной нервной системы встречается реже других симптомов гемофилии, но всегда определяет особую тяжесть состояния больных. Внутричерепные кровоизлияния считаются главной причиной смерти таких больных. В клинике нарастают беспокойство, головная боль, появляются «стволовые» симптомы, расстройство ритма дыхания и сердечной деятельности. Диагностика. 1. Анамнестические сведения. 2. Нарушения общих коагуляционных показателей: удлинение общего времени свертывания крови (в норме по Дюке - 1-3 мин., по Сухареву - от 3-х до 5 мин.), удлинение времени рекальцификации, увеличение активности парциального тромбопластинового времени, снижение коагуляционной активности при нормальных показателях протромбинового и тромбинового времени (норма протромбинового индекса: 70 -120%). 3. Определение дефицита того или иного фактора свертывания крови. 4. Возможно проведение медико-генетического обследования членов семьи больного ребенка на носительство генной мутации. Лечение: 1. Всем больным в период рецидива болезни назначается диета, богатая кальцием, витаминами А, С, группы В. Возможно использование лекарственных форм кальция и витаминов, гемостатических сборов, дицинона. 2. Специфическая заместительная терапия – антигемофильная плазма, свежезамороженная человеческая плазма, материнская кровь, криопреципитаты, синтетические факторы свертывания крови. Применяются две программы лечения больных гемофилией: 1) Систематическое трансфузионное лечение - показана детям с тяжелой гемофилией: каждые 10-14 дней вводят в/в при гемофилии А криопреципитат VIII а при гемофилии В – нативную концентрированную плазму, содержащую IX фактор. Такая терапия приводит через 1,5-2 года к 4-5-кратному увеличению уровня VIII и IX факторов и уменьшению тяжести течения болезни. 2) Периодическое, симптоматическое трансфузионное лечение - предусматривает введение концентратов VIII и IX факторов в первые часы после кровоизлияния или обширной травмы. 3. При гематрозах в острый период местно используют холод, накладывают лангет на 2 недели. Затем назначают тепловые процедуры на пораженный сустав, проводят ЛФК, гормоны из расчета 1-1,5 мг/кг в сутки. 4. В периоды ремиссии показано специализированное санаторно-курортное лечение в Евпатории. Прогноз. С появлением современных синтетических факторов свертывания крови выживаемость больных значительно возросла, однако больные имеют много жизненных ограничений. Диспансерное наблюдение. Осуществляется совместно гематологом и участковым педиатром. Ребенок освобождается от прививок и занятий физкультурой в школе из-за опасности травм, им противопоказаны занятия в спортивных секциях, подвижные игры, включая катание на лыжах, коньках, санках, прыжки в воду и т.д. Однако физические нагрузки показаны, т.к. это увеличивает уровень VIII фактора. Питание обычное. При простудных заболеваниях не следует назначать ацетилсалициловую кислоту или индометацин. Противопоказаны банки. Любые инвазивные медицинские манипуляции (инъекции, операции, эндоскопические исследования) проводятся только на фоне заместительной терапии. Не делать в/м инъекций, п/к вводить не более 2 мл, держать место введения 5 мин. Регулярный осмотр стоматолога, лор-врача. «Маски» острого лейкоза у детей Острый лейкоз у детей — это системное злокачественное заболевание кроветворной ткани, морфологическим субстратом которого являются незрелые бластные клетки, поражающие костный мозг. Этиология и патогенез. Этиология окончательно не установлена. Предполагают, что это различные эндо- и экзогенные факторы (онкогенные вирусы, неблагоприятные факторы внешней среды, ионизирующая радиация и т. д.), которые приводят к мутацим соматических или зародышевых клеток, относящихся к системе кроветворения. При этом клетки реагируют неудержимым ростом, невозможностью дифференцировки и изменением скорости нормального созревания. Клиника. 1. Начальный период протекает под видом заболеваний - «масок». Варианты: 1) Острое начало (приблизительно у 50 % больных), высокая лихорадка, проявления интоксикации, болями в суставах, животе, горле. Это состояние обычно трактуют как грипп, ангину, острую ревматическую лихорадку, аппендицит. В таких случаях правильный диагноз устанавливают лишь спустя 2-3 недели от появления первых симптомов. 2) Начало заболевания с выраженным геморрагическим синдромом (приблизительно у 10 % больных) проявляется кровотечениями различной локализации: носовыми, желудочно-кишечными, церебральными, кровоизлияниями в кожу, слизистые оболочки, склеры. 3) Постепенное начало (приблизительно у 35-37 % больных) характеризуется не специфическим симптомокомплексом: прогрессирующая слабость, снижение работоспособности, боли в костях, мышцах, суставах, увеличение лимфатических узлов, появление небольших геморрагии на коже. В таких случаях правильный диагноз устанавливается лишь через 4-6 недель, ведущая роль принадлежит исследованию периферической крови. 4) Бессимптомное (скрытое) начало у детей встречается редко. В этом случае общее состояние не нарушено, самочувствие может быть удовлетворительным. При объективном исследовании можно выявить незначительное увеличение лимфоузлов, печени и селезенки. Заболевание выявляется при случайном исследовании клинического анализа крови. Трудности ранней диагностики острого лейкоза обусловлены отсутствием симптомов, патогномоничных для данного заболевания, а также должной онкологической настороженности практикующих врачей-педиатров. 2. Острый период – развернутые клинические проявления. Синдромы: 1) Гиперпластический синдром - обусловлен лейкозной инфильтрацией тканей. Увеличиваются периферические лимфатические узлы, печень, селезенка, небные миндалины. Возможно значительное увеличение лимфоузлов средостения вплоть до сдавления верхней полой вены с развитием характерной симптоматики (одышки, цианоза, отека шеи, выбухания шейных вен). Одно из проявлений этого синдрома - гиперплазия десен с развитием тяжелого язвенно-некротического стоматита. 2) Геморрагический синдром - обусловлен тромбоцитопенией, повышением проницаемости и снижением резистентности сосудистой стенки, дефицитом факторов свертывания, повышением фибринолитической активности. Проявляется кровоизлияниями в кожу и слизистые оболочки, носовыми, желудочнокишечными, почечными, легочными, маточными, церебральными кровотечениями, которые могут быть профузными и угрожать жизни пациента. 3) Анемический синдром - развивается у всех больных лейкозом, обусловлен резким угнетением красного ростка кроветворения, интоксикацией, кровотечениями. Степень анемии четко коррелирует с активностью опухолевого процесса. 4) Интоксикационный синдром характеризуется общей слабостью, высокой температурой тела, потливостью (особенно ночью), головными болями, отсутствием аппетита, исхуданием, атрофией мышц, оссалгиями, тошнотой, рвотой. 5) Иммунодефицитный синдром - нейтропения, резкие нарушения клеточного и гуморального звеньев иммунитета, фагоцитоза, снижение активности комплемента. Складываются благоприятные условия для развития инфекционно-воспалительных поражений с тяжелым течением вплоть до септического состояния, что может привести к гибели больного. Лихорадка вследствие самого лейкоза (неопластическая) отличается от инфекционно-воспалительной лихорадки следующими особенностями: температура тела ежедневно выше 38,7°С, продолжительность лихорадки более 2 недель, отсутствие проявлений инфекции, отсутствие положительной реакции на эмпирическую антибактериальную терапию, положительный эффект от нестероидных противовоспалительных препаратов. 3. Период ремиссии. При полной ремиссии отсутствуют клинические симптомы, показатели периферической крови в пределах возрастной нормы. При неполной ремиссии клинических симптомов нет, а в показателях периферической крови имеется лишь улучшение. 4. Рецедив характеризуется возвратом клиники лейкозного процесса и изменений со стороны крови. 5. Терминальный период - резко выражены все основные проявления заболевания, обусловленные необратимыми изменениями во внутренних органах, приводящими к смерти. Чаще всего дети погибают от кровотечений. Лабораторная диагностика. 1. ОАК: бластные клетки, анемия, тромбоцитопения, высокая СОЭ; количество лейкоцитов вариабельно: чаще выявляют лейкоцитоз различной степени, реже - лейкопению. Характерным диагностическим критерием служит «лейкемический провал - отсутствие промежуточных форм между бластными и зрелыми клетками. 2. Исследование красного костного мозга обычно проводят после исследования периферической крови. Достоверный диагностический критерий острого лейкоза - обнаружение бластных клеток в стернальном пунктате в количестве более 30% клеточного состава красного костного мозга. Лечение: Терапию острого лейкоза проводят только в специализированных гематологических клиниках. Группы препаратов и способы лечения: 1. Цитостатики 2. Глюкокортикоиды 3. Лучевая терапия 4. Тансплантация гемопоэтических стволовых клеток 5. Иммунотерапия Этапы лечения: 1. Индукция (достижение) ремиссии 2. Консолидация (закрепление) ремиссии 3. Поддерживающая терапия. Однако ни интенсивная, ни поддерживающая терапия у большинства больных не в состоянии сдержать прогрессирование процесса, поэтому необходима 4. Реиндукция - периодическая интенсификация лечения. К настоящему времени отработаны различные схемы лечения острого лейкоза у детей, используемые с учетом особенностей кинетики лейкозных клеток. Название схем состоит из первых букв препаратов: Пример, ВАМП (винкристин, аметоптерин, 6-меркаптопурин, преднизолон). В лечении острых лейкозов с успехом используется метод синхронизирующей полихимиотерапии. Он заключается в том, что под влиянием некоторых цитостатических препаратов (циторабин, метотрексат) клеточный цикл задерживается, клетки блокируются в определенной стадии митотического цикла, происходит их накопление, а затем вводятся препараты, воздействующие на клетки в этой фазе. Метод способствует повышению результативности противолейкозной терапии. Диспансерное наблюдение осуществляется гематологом специализированного центра и участковым педиатром. 1. Учитывая, что больной практически все время получает цитостатическую терапию, необходимо 1 раз в 2 нед. делать ОАК. При поддерживающей терапии назначают цитостатики. Необходимо подсчитать число лейкоцитов, т.к. если их менее 1×109/л то препараты не назначают. Дают медикаменты, способствующие увеличению количества лейкоцитов (экстракт элеутерококка по 1 капле на год жизни 3 раза в день, нуклеинат натрия, дибазол, пентоксил, метацил), и лишь при увеличении количества лейкоцитов более 1,5×109/л возобновляют цитостатическую терапию. 2. Миелограмму делают перед и после каждого курса реиндукции, который проводят в стационаре. 3. Не показано изменение климатическизх условий. 4. Ребенок освобождается от профилактических прививок, занятий физкультурой. Его надо оберегать от физических нагрузок, психических травм, охлаждения, случайных инфекций. Занятия по школьной программе не противопоказаны, но лучше заниматься дома, т.к. в школе, особенно в зимне-весенний период, часты ОРЗ среди детей. Прогноз при остром лимфоидном лейкозе в случае рано начатой интенсивной терапии в последние несколько лет существенно изменился: в 15-25% случаев, а по мнению отдельных авторов - и еще чаще выздоровление кажется окончательным. Приблизительно в 40% случаев миелобластного лейкоза можно достигнуть ремиссии, но окончательный прогноз все еще плохой.