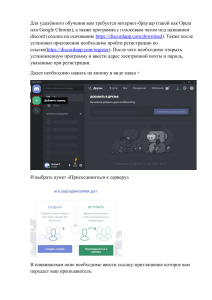
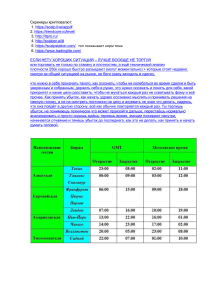
S-элементы Группа → 1 ↓ Период 1 1 2 8 Водород H 2 He4,0026 1,008[1 1 1s2 1s 3 2 Li Литий 4 Бериллий [2] 6,94 4 Be 9,0122 2 1 3 Гелий [Не]2s 2s 11 12 Натрий Магний Na 22,989 Mg 24,305 [Nе]3s1 3s2 19 20 Кальций K Калий 39,098 [Ar]4s1 Ca 40,078 4s2 37 Рубидий 38 Стронций 5 6 Rb 85,467 Sr 1 [Kr]5s 5s 55 Цезий 56 Cs 132,90 1 Ba [Rn]7s1 137,32 6s 87 Франций 88 Fr Барий 2 [Xe]6s 7 87,62 2 (223) Ra Радий (226) 7s2 s-Элементы в периодической таблице элементов — химические элементы, электронная оболочка которых включает в себя первые два s-электрона. Такие элементы объединяются в группу, называемую s-блок. К s-элементам относятся: щелочные металлы, щелочноземельные металлы, водород и гелий. S-элементы отличаются тем, что в невозбужденном состоянии высокоэнергетичный электрон атомов находится на s-орбитали. Исключая водород и гелий, эти электроны очень легко отщепляются и формируются в положительные ионы при химической реакции. Конфигурация гелия химически стабильна; за счёт этого его относят к инертным газам. S-элементы (кроме гелия) являются сильными восстановителями и поэтому в свободном виде в природе не встречаются. Элемент в металлическом виде может быть получен только с помощью электролиза расплава соли. Гемфри Дэви, в 1807 и 1808 году, стал первым, кто выделил s-металлы из их солей, за исключением лития, бериллия, рубидия и цезия. Бериллий был впервые выделен из солей независимо двумя учёными: Ф. Вулером и А. А. Бази в 1828 году, в то время как литий был выделен Р. Бунзеном только в 1854 году, который, после изучения рубидия, выделил его спустя 9 лет. Цезий не был выделен в чистом виде вплоть до 1881 года, до того, как Карл Сеттерберг подверг электролизу цианид цезия. Твёрдость s-элементов в компактном виде (при обычных условиях) может варьироваться от очень малой (все щелочные металлы — их можно разрезать ножом) до довольно высокой (бериллий). Исключая бериллий и магний, металлы очень реакционноспособны и могут быть использованы в сплавах со свинцом в малых количествах (<2 %). Бериллий и магний, ввиду их высокой стоимости, могут быть ценными компонентами для деталей, где требуется твёрдость и лёгкость. Эти металлы являются чрезвычайно важными, поскольку позволяют сэкономить средства при добыче титана, циркония, тория и тантала из их минеральных форм; могут находить своё применение как восстановители в органической химии. Опасность и хранение Все элементы, имеющие s-оболочку, являются опасными веществами. Они пожаро(взрыво-)опасны, требуют особого пожаротушения, исключая бериллий и магний. Храниться должны в инертной атмосфере аргона или углеводородов. Бурно реагируют с водой, продуктом реакции является водород, например: , исключая магний, который реагирует медленно, и бериллия, который реагирует только когда его оксидная плёнка снята с помощью ртути. Литий имеет схожие свойства с магнием, так как находится, относительно периодической таблицы, рядом с магнием. Примечания 1. Atomic weights of the elements 2013 (IUPAC Technical Report) (англ.) — IUPAC, 1960. — ISSN 0033-4545 (https://www.worldcat.org/issn/0033-4545) ; 1365-3075 (https://www.w orldcat.org/issn/1365-3075) ; 0074-3925 (https://www.worldcat.org/issn/0074-3925) — doi:10.1515/PAC-2015-0305 (https://dx.doi.org/10.1515/PAC-2015-0305) 2. Meija J., Coplen T. B., Berglund M., Brand W. A., Bièvre P. D., Gröning M., Holden N. E., Irrgeher J., Loss R. D., Walczyk T. et al. Atomic weights of the elements 2005 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry — IUPAC, 2016. — Vol. 88, Iss. 3. — ISSN 0033-4545 (https://www.worldcat.org/issn/0033-4545) ; 1365-3075 (https://www.w orldcat.org/issn/1365-3075) ; 0074-3925 (https://www.worldcat.org/issn/0074-3925) — doi:10.1515/PAC-2015-0305 (https://dx.doi.org/10.1515/PAC-2015-0305) Литература Дикерсон Р., Грей Г., Хейт Дж. Основные законы химии: В 2-х томах. Пер. с англ. — М.: Мир, 1982. 652 с., ил. — Т. 1. — С. 432—437. Источник — https://ru.wikipedia.org/w/index.php?title=Sэлементы&oldid=116957775 Последняя правка сделана 3 месяца назад участником OneLittleMouse