RuBisCO - Институт фундаментальной биологии и биотехнологии
реклама

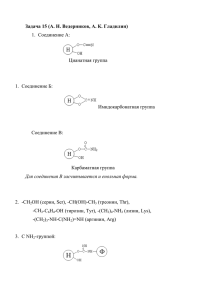
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ Федеральное государственное автономное образовательное учреждение высшего профессионального образования «СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ» Институт фундаментальной биологии и биотехнологии Кафедра биофизики RuBisCO Рибулозобисфосфаткарбоксилаза EC 4.1.1.39 Выполнил: Чижова Анастасия ФБ 09-01С Красноярск 2014 RuBisCO (PDB ID: 8RUC)— глобулярный белок состоит из двух типов белковых субъединиц: Большая цепь (L, массой 55 000 Да) Малая цепь (S, массой 13 000 Да) RuBisCO — фермент катализирующий присоединение углекислого газа к рибулозо-1,5-бифосфату на первой стадии цикла Кальвина, а также реакцию окисления рибулозобифосфата на первой стадии процесса фотодыхания. Является одним из важнейших ферментов в природе, поскольку играет центральную роль в основном механизме поступления неорганического углерода в биологический круговорот. Рибулозобисфосфаткарбоксилаза является основным ферментом листьев растений и поэтому считается наиболее распространённым ферментом на Земле. Одним из наиболее перспективных направлений использования RuBisCO в генной инженерии видится трансплантация генов данного фермента из красной водоросли Galdieria partita, рибулозобисфосфаткарбоксилаза которой обладает естественной высокой специфичностью к CO2, в высшие культурные растения. Это, предположительно, может увеличить их урожайность. 2 АКТИВНЫЙ ЦЕНТР ФЕРМЕНТА Активный центр фермента находится на больших цепях, объединённых в димеры. Все 8 димеров больших цепей и 8 малых цепи объединены в единый комплекс массой 540 000 Да. У некоторых протеобактерий малых цепей в составе рубиско не обнаружено. При этом большие цепи кодируются в ДНК хлоропласта, а малые — в ядре и транспортируются в хлоропласт перед сборкой всего белка Рисунок с сайта: http://www.uic.edu/classes/bios/bios100/lectures/ps01.htm 3 СТРУКТУРА ФЕРМЕНТА Рисунок с сайта: http://www.rcsb.org/pdb/explore/remediatedSequence.do?structureId=1RLC&bionumber=1 4 3D модель белка Различимы все атомы белка. Белые – углерод Синие – азот; Красные – кислород; Желтые – сера. 5 Рибон диаграмма 6 ВАН–ДЕР-ВААЛЬСОВА МОДЕЛЬ ПОВЕРХНОСТИ 7 ВОДОРОДНЫЕ СВЯЗИ 8 Карта Рамачандра На карте показаны углы между аминокислотами. За синей чертой – область недопустимых значений. Между синей и желтой – допустимы, но с напряжением. Внутри желтой границы – допустимы. 9 КЛАССИФИКАЦИЯ ПО РАДИКАЛУ Полярные заряженные положительно – голубые Полярные заряженные отрицательно – красные Полярные незаряженные( заряды скомпенсированы) при pH=7 – желтые Неполярные – серые 10 Доступность для молекул воды 11