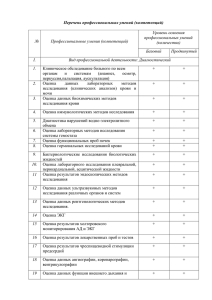
Л.И. Крикунова ЛУЧЕВАЯ ТЕРАПИЯ РАКА ШЕЙКИ МАТКИ
реклама

ГУ- Медицинский радиологический научный центр РАМН Директор академик РАМН А.Ф. ЦЫБ ЦЕЛЕСОООБРАЗНОСТЬ И ЭФФЕКТИВНОСТЬ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ профессор Л.И. КРИКУНОВА г. ОБНИНСК Ежегодно в Российской Федерации выявляется 400 тыс. больных со злокачественными новообразованиями различных локализаций. Реальный показатель запущенности заболевания составляет 37,1%, смертности в течение года – 35,7%. В поздних стадиях (III-IV) наиболее часто выявляются опухоли ротоглотки, прямой кишки, молочной железы, шейки матки, яичников и опухоли щитовидной железы С 90-х годов в России значительно увеличилось количество многоцентровых клинических исследований новых лекарственных препаратов, используемых при различных заболеваниях, включая и злокачественные опухоли ЦЕЛЬ ИССЛЕДОВАНИЙ Повышение эффективности и результативности лечения онкологических заболеваний с сохранением качества жизни больного ПРОЦЕСС ИЗЫСКАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ИЗЫСКАНИЕ ЭКСПЕРИМЕНТАЛЬНАЯ РАЗРАБОТКА ПЕРСПЕКТИВНЫЕ КЛИНИЧЕСКИЕ ИСПЫТАНИЯ РЕГИСТРАЦИЯ И ОДОБРЕНИЕ ПОСТМАРКЕТИНГОВЫЕ СТРАТЕГИИ В среднем на разработку нового лекарственного средства со стадии изыскания до полного одобрения необходимо потратить более 12-15 лет. Примерно 1 из 15 лекарственных средствкандидатов переходящих в стадию РАЗРАБОТКИ, исследуется на III Фазе и получает одобрение регулирующих органов. Ограниченное число лекарственных веществ успешно проходит доклинические испытания. Как показано на рисунке, из сотен тысяч химических соединений, протестированных в начале процесса по изысканию лекарственных средств, только 10-20 соединений в год будут подвергнуты дальнейшей разработке. Из них только 5-10 переходят в следующую стадию разработки лекарственного средства (первая фаза клинических испытаний). «Планирование и проведение клинических исследований лекарственных средств». Под редакцией Ю.Б. Белоусова, Москва-2000 Клинические испытания лекарственных средств проходят несколько ФАЗ: Задачи I фазы: установить переносимость, безопасность, наличие терапевтического действия, фармакокинетические и фармакодинамические характеристики, а иногда и первоначальные показатели эффективности I фаза проводится на 100 здоровых добровольцах. Исключением являются испытания онкологических лекарственных средств. С точки зрения медицинской этики, в связи с потенциальной токсичностью противораковых лекарственных средств, предпочтительнее испытывать их на онкологических больных Задачи II фазы: доказательство клинической эффективности лекарственного средства при испытании на группе пациентов и определение терапевтического уровня дозирования лекарственного средства. Обычно эти испытания плацебо-контролируемые Задачи III фазы: Оценка безопасности и эффективности лекарственного средства, дозировка которого определена терапевтическими целями, а форма является наиболее оптимальной Проводится в условиях, приближенных к тем, в которых препарат будет использован в случае получения разрешения и выпуска на фармацевтический рынок. В исследования включаются тысячи пациентов. РЕКОМЕНДАЦИЯ К ШИРОКОМУ КЛИНИЧЕСКОМУ ПРИМЕНЕНИЮ СЧИТАЕТСЯ ОБОСНОВАННОЙ, ЕСЛИ НОВЫЙ ПРЕПАРАТ: • Более эффективен, чем известные препараты, аналогичного действия; • Обладает лучшей переносимостью при равной эффективности с известными препаратами; • Эффективен в тех случаях, когда лечение известными препаратами безуспешно; • Экономически более выгоден; • Прост в применении; • Имеет более удобную лекарственную форму; • Обладает синергидным действием при комбинированной терапии, не увеличивая токсичности ОТРИЦАТЕЛЬНЫЕ ВОЗДЕЙСТВИЯ Нежелательная лекарственная реакция Токсический эффект Вторичное действие Нежелательное явление Побочное действие ВИДЫ ТОКСИЧНОСТИ • Гематологическая • Гастроинтестинальная • Гепатотоксичность • Нейротоксичность • Ототоксичность • Нефротоксичность • Кардиотоксичность • Развитие вторичных опухолей ПРИЧИНЫ ТОКСИЧНОСТИ • НЕСЕЛЕКТИВНЫЙ механизм действия: Повреждаются активно делящиеся клетки, что приводит к разнообразным видам токсичности Токсичность химиотерапии создает следующие проблемы • Ограничение по разовой дозе • Ограничение по кумулятивной дозе • Удлинение интервалов между циклами химиотерапии • Невозможность сочетания эффективных препаратов из-за перекрестной токсичности Клинические исследования на основании апробации противоопухолевых препаратов позволяют оценить целесообразность и эффективность применения их в лечении больных с первично-выявленными и рецидивирующими злокачественными опухолями в качестве первой и второй линии химиотерапии.