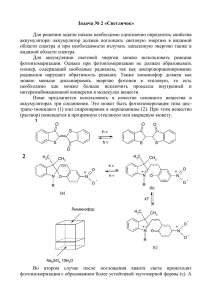
Лекция 8. Гидроксикислоты. Оптическая изомерия
реклама

ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксикислоты) ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксикислоты) – карбоновые кислоты, в которых одновременно содержатся карбоксильная (СООН) и гидроксильная (ОН) группы δ-ГИДРОКСИКИСЛОТЫ и т.д. O β-ГИДРОКСИКИСЛОТЫ γ O HO β HO α-ГИДРОКСИКИСЛОТЫ α γ OH γ-ГИДРОКСИКИСЛОТЫ O O HO α β OH β HO γ α OH α OH ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) НОМЕНКЛАТУРА O O HO OH HO O OH HO OH OH трив.: гликолевая кислота сист.: гидроксиэтановая кислота гидроксиуксусная кислота соли: гликолят O CH3 трив.: молочная кислота сист.: 2-гидроксипропановая кислота соли: лактат трив.: глицериновая кислота сист.: 2,3-дигидроксипропановая кислота соли: глицерат OH O O O HO OH O O OH OH OH HO трив.: яблочная кислота сист.: 2-гидроксибутандиовая кислота соли: малоат OH HO OH O OH трив.: винная кислота сист.: 2,3-дигидроксибутандиовая кислота соли: тартрат трив.: лимонная кислота сист.: 2-гидроксипропантрикарбоноаая кислота соли: цитрат ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) МЕТОДЫ СИНТЕЗА ОБЩИЕ МЕТОДЫ СИНТЕЗА 1. Нуклеофильное замещение галогена O O Br HO OH - HO OH t CH3 CH3 2. Диазотирование аминокислот CH3 H2N O + - Na O OH N O N HCl O CH3 Cl + - HO OH N CH3 H2O íåóñòîé÷. 3. Гидролиз нитрилов CH3 HO N CH3 O + H2O H t HO OH O OH ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) МЕТОДЫ СИНТЕЗА ОБЩИЕ МЕТОДЫ СИНТЕЗА 4. Гидролиз эфиров, амидов, солей O O O + H3C O - H2O H + H3C OH H2O H H3C OH OH OH X X=RO, NH 2 5. Синтез дигидроксикислот O O OH HO O [O] OH OH HO OH [O] = 1% KMnO 4, H2O2 O ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) МЕТОДЫ СИНТЕЗА СПЕЦИАЛЬНЫЕ МЕТОДЫ СИНТЕЗА 1. α-ГИДРОКСИКИСЛОТЫ. ЦИАНГИДРИННЫЙ СИНТЕЗ O O HCN/CN H3C CN H3C - + H3C H2O/H /t OH OH H OH 2. β-ГИДРОКСИКИСЛОТЫ. СИНТЕЗ РЕФОРМАТСКОГО R 1 R + OR + O R 3 1 R Zn Br OC2H5 OH + H2O/H /t OR 2 H3C R 3 O OH 2 OH + H2O/H /t OC2H5 O 1 R OH O H O Zn Br O H3C OH O 2 H3C O OH ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) МЕТОДЫ СИНТЕЗА Механизм реакции Реформатского H3C H OZnBr O O O Zn Br OC 2H5 + BrZn O _ H3C OC 2H5 OH OC 2H5 O H3C OH CH3 CH3 O O Br H3C OC 2H5 H CH3 CH3 OH + H2O/H /t H3C O OH ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) ХИМИЧЕСКИЕ СВОЙСТВА 1. Реакции по карбоксильной группе H3C O NaOH HO NaHCO 3 H3C HO O OH H3C HO H3C RNH 2 HO + ROH/H /t H3C HO ONa O ONa O -+ O NH 3R O OR ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) ХИМИЧЕСКИЕ СВОЙСТВА 2. Реакции по гидроксильной группе (CH 3)2SO 4/OH H3C - O (CH 3)2SO 4/OH H3CO OH - H3C O H3CO OCH 3 àëêèëèðîâàíèå C6H5SO 3CH 3/OH H3C HO O OH - H3C O C6H5SO 3CH 3/OH H3CO OH H3C (CH 3COO) 2O O O O H3C HBr H3C Br OH àöèëèðîâàíèå O OH - H3C H3CO O OCH 3 ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксикислоты) ХИМИЧЕСКИЕ СВОЙСТВА 3. Реакции по гидроксильной и карбоксильной группе PCl 5 H3C HO O SOCl 2 OH CH 2N2 H3C O Cl Cl H3C O Cl Cl H3C HO O CH 2N2/BF3 OCH 3 H3C H3CO O OCH 3 ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксикислоты) H3C HO Нуклеофильность выше O OH ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) ХИМИЧЕСКИЕ СВОЙСТВА 4. Дегидратация. Влияние расположения ОН-группы 4.1. Дегидратация α-гидроксикислот O OH .. HO CH3 O O CH3 H3C O O 0 150 C H3C OH HO .. O 4.2. Дегидратация β-гидроксикислот O O 0 HO OH CH3 150-160 C -H 2O H2C OH CH3 ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) ХИМИЧЕСКИЕ СВОЙСТВА 4. Дегидратация. Влияние расположения ОН-группы 4.3. Дегидратация γ-гидроксикислот H2O/H + OH HO H2O/OH - OH t .. OH HO O O O - O 0 O O t NH3 γ-Бутиролактон OH H2N O CH 3OH O OH H3CO 0 N H O ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ (гидроксикислоты, оксокислоты) ХИМИЧЕСКИЕ СВОЙСТВА 4.4. Дегидратация δ-гидроксикислот t .. OH HO 0 δ-Валеролактон O O O O 5. Окисление O 3+ H2O2, Fe H3C OH OH H3C OH O 6. Восстановление O O HI/t H3C OH OH H3C OH СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ АКТИВНОСТЬ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ СТЕРЕОХИМИЯ (от греч. stereos – пространственный) – раздел химии, изучающий пространственное строение молекул и влияние его на физические, химические свойства (статическая стереохимия) и на направление и скорость реакций (динамическая стереохимия) Вещества, способные поворачивать плоскость поляризации проходящего через них света, называют ОПТИЧЕСКИ АКТИВНЫМИ Важное структурное свойство веществ - ХИРАЛЬНОСТЬ (от греч. chéir – рука) - явление, свойственное любым объектам, которые несовместимы со своим отображением в плоском зеркале. В химии зеркально асимметричные молекулы называются оптическими L- и Dизомерами (от лат. levo – левый и dextro – правый), R- и S-изомерами или ЭНАНТИОМЕРАМИ. В природе встречаются L-аминокислоты и D-сахара. ХИРАЛЬНОСТЬ. ЗЕРКАЛЬНОЕ ОТОБРАЖЕНИЕ СТЕРЕОХИМИЯ И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ. ВЗАИМОДЕЙСТВИЕ С РЕЦЕПТОРАМИ СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) ПРОСТРАНСТВЕННАЯ ИЗОМЕРИЯ (СТЕРЕОИЗОМЕРИЯ, ОПТИЧЕСКАЯ ИЗОМЕРИЯ) - изомерия возникает в результате различий в пространственной конфигурации молекул, имеющих одинаковое химическое строение. Этот тип изомеров подразделяют на энантиомерию (оптическую изомерию) и диастереомерию. КОНФИГУРАЦИЯ СТЕРЕОХИМИЧЕСКАЯ — характеризует относительное пространственное расположение атомов или групп атомов в молекуле химического соединения. ЭНАНТИОМЕРАМИ (оптическими изомерами, зеркальными изомерами) являются пары оптических антиподов — веществ, характеризующихся противоположными по знаку и одинаковыми по величине вращениями плоскости поляризации света при идентичности всех других физических и химических свойств (за исключением реакций с др. оптически активными веществами). Необходимая и достаточная причина возникновения оптических антиподов — наличие асимметрического атома углерода - sp3-гибридного атома углерода, связанного с четырьмя разными заместителями. Эквимолярная смесь энантиомеров не обладает оптической активностью. Такая смесь называется РАЦЕМИЧЕСКОЙ СМЕСЬЮ или РАЦЕМАТОМ . ДИАСТЕРИОМЕРЫ – оптические изомеры, характеризующиеся наличием хотя бы одного асимметрического атома углерода с одинаковой конфигурацией и хотя бы одного с различной. Диастериомеры характеризуются различными физическими свойствами и одинаковыми химическими СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) Количество стериоизомеров определяется по формуле: N=2 n N-количесвто стериоизомеров, n- количество ассиметрических атомов углерода O H O H HO H H OH CH 2OH Проекции Э. Фишера CH 2OH 1 O 1 и 2 – энантиомеры (оптитические антиподы) 2 OH O OH O H H OH OH H OH HO H CH3 1 Энантиомеры – Диастериомеры - CH3 2 OH O OH HO H H OH HO H HO H CH3 CH3 3 4 СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) O OH O OH O H H OH H OH H O OH O HO 1 Количество изомеров - ? Ответ - 3 2 OH O OH HO H H OH OH HO H HO OH O OH 3 H O OH 4 Количество оптически активных изомеров - ? Ответ - 2 Но, почему - ?, ведь асимметрических атомов углерода 2, значит количество изомеров должно быть 4 Соединения 2 и 3 это МЕЗОФОРМА – структура не обладающая оптической активностью (внутримолекулярный рацемат). Таким образом, 2 и 3 – это одно и то же. СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) L-, D- номенклатура оптических изомеров. Система Фишера-Розанова. ЭТАЛОН – ГЛИЦЕРИНОВЫЙ АЛЬДЕГИД O H O H HO H H OH CH 2OH CH 2OH 1 2 L-глицериновый альдегид (-) –левовращающий изомер D-глицериновый альдегид (+) –правовращающий изомер Было условно принято правовращающий (+) изомер глицеринового альдегида отнести к D-ряду, а левовращающий (-) – к L-ряду . Для названия других оптически активных соединений их сравнивали с глицериновым альдегидом и относили к D или L-ряду. При этом сторона вращения (право (+) или лево (-) не связана с буквой D- или L-). L-изомер может быть правовращающим или левовращающим. Тоже относится и к D-изомерам. СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) L-, D- номенклатура оптических изомеров. Система Фишера-Розанова. O OH O OH HO H H OH H3C CH3 H3C CH3 L-2-гидрокси-3-метилбутановая кислота D-2-гидрокси-3-метилбутановая кислота L-, D- номенклатура оптических изомеров применяется только для соединений схожих с глицериновым альдегидом (аминокислоты, сахара). Для оптически активных веществ, имеющих 2 и более асимметрических атома Углерода используется R-, S-номенклатура (система Кана-Ингольда-Прелога, CIP) СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) R-, S-НОМЕНКЛАТУРА (СИСТЕМА КАНА-ИНГОЛЬДА-ПРЕЛОГА, CIP) СИСТЕМА КАНА-ИНГОЛЬДА-ПРЕЛОГА использует символы R (от лат. rectus-правый) или S (от лат. sinister-левый) для обозначения каждого хирального центра в зависимости от его конфигурации. В основе большинства стереохим. обозначений лежит правило старшинства заместителей, которое определяется атомным номером или массой атома, связанного с асимметрическим центром. Чем больше номер, тем старше заместитель. Если эти атомы одинаковы по старшинству, то рассматривают "ВТОРОЙ СЛОЙ", в который входят атомы, связанные с атомами "ПЕРВОГО СЛОЯ", и т.д., до появления первого различия; номера атомов, связанных двойной связью, при определении старшинства удваивают. Обозначение R получает тот из энантиомеров, в к-ром при рассмотрении модели со стороны, противоположной младшему заместителю, старшинство остальных заместителей уменьшается по часовой стрелке. Падение старшинства против часовой стрелки соответствует S-обозначению R,S-изомеры можно определять и по проекционной формуле Фишера. Если в ней младший заместитель расположен в нижней части формулы, а старшинство заместителей a–>b–>c уменьшается по часовой стрелке, то конфигурацию обозначают знаком R, а если против часовой стрелки, то знаком S. СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) R-, S-НОМЕНКЛАТУРА (СИСТЕМА КАНА-ИНГОЛЬДА-ПРЕЛОГА, CIP) A>B>C>D Против часовой стрелки – S-изомер 1 1 OH 4 2 4 H OHC H 3 HOH 2C 2 CHO R OH S 3 CH2OH СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) R-, S-НОМЕНКЛАТУРА (СИСТЕМА КАНА-ИНГОЛЬДА-ПРЕЛОГА, CIP) 1 1 OH 4 2 4 H OHC H 3 HOH 2C 2 CHO R O H 2 H OH OH S 3 O CH2OH 2 H 1 CH 2OH 3 D-глицериновый альдегид R-глицериновый альдегид 1 HO H CH 2OH 3 L-глицериновый альдегид S-глицериновый альдегид СТЕРЕОХИМИЯ. ОПТИЧЕСКАЯ ИЗОМЕРИЯ (стереоизомерия) R-, S-НОМЕНКЛАТУРА (СИСТЕМА КАНА-ИНГОЛЬДА-ПРЕЛОГА, CIP) O 2 OH 1 HO 3 H OH H 3 (2S,3S) O H 1 OH 1 HO H H H OH 3 HO H 3 HO O 1 HO H 2 OH H OH (1) O (2) OH 3 2 OH 1 OH H (3) O 2 OH H 1 OH 1 HO H OH (1) 3 HO (1) O (2) OH OH (2R,3R) (2S,3R) (3) 2 O (2) OH O (2) OH (2R,3S) (3) (3) 3 2 OH O (2) OH O (2) OH O O O 2 OH H H O (2) OH O 2 OH H 3 HO (1) 1 OH H O (2) OH (3) (3) O 1 HO 3 H 2 OH H OH (1) O (2) OH (2S,3S) 3 (3) (3) O 2 OH O H 1 OH 1 HO H OH (1) 3 HO (1) O (2) OH (2R,3S) 2 OH H H O H 3 HO (1) 2 OH 1 OH H O (2) OH O (2) OH (2S,3R) (2R,3R) СИНТЕЗ ОПТИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ. ИЗМЕНЕНИЕ КОНФИГУРАЦИИ O HCN/CN - H3C CN CN H H OH + HO H CH3 CH3 R S рацемат COOH HO H COOH + H OH CH3 CH3 (S) (R) рацемат COOH - OH (ðàçá) SN1 H Br CH3 (R) COOH - OH (êîíö) SN 2 HO H CH3 (S) обращение конфигурации ОБРАЩЕНИЕ КОНФИГУРАЦИИ (SN2) РАЦЕМИЗАЦИЯ (SN1) ОБРАЩЕНИЕ КОНФИГУРАЦИИ СОХРАНЕНИЕ КОНФИГУРАЦИИ СИНТЕЗ ОПТИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ. ИЗМЕНЕНИЕ КОНФИГУРАЦИИ COOH H OH CH3 SOCl2 O Cl H Cl SN i CH3 (R) (R) без обращение конфигурации РАЗДЕЛЕНИЕ РАЦЕМИЧЕСКОЙ СМЕСИ COOH COOH H H OH O CH3 (R) COOH HO Br (S) рацемат O H H2O H (R,R) OH CH3 Br (R) CH3 оптически чистое CH3 (R) H CH3 CH3 Cl H O COOH COOH COOH O O оптически чистое H Br CH3 H CH3 (S,R) диастериомеры H2O HO H CH3 (S) оптически чистое ИЗМЕНЕНИЕ ОПТИЧЕСКОЙ АКТИВНОСТИ, КОНФИГУРАЦИИ АТОМОВ УГЛЕРОДА, КОЛИЧЕСТВА ИЗОМЕРОВ O OH H OH OH H OH OH O OH O OCH 3 H OH H O H2O/H + Изменится ли кол-во оптических изомеров и конфигурация атомов углерода O OH H OH CH3 (CH 3)2SO4/OH 1:1 O OH H OCH 3 - CH3 АМИНОКАРБОНОВЫЕ КИСЛОТЫ (АМИНОКИСЛОТЫ) АМИНОКИСЛОТЫ – карбоновые кислоты, в которых одновременно содержатся карбоксильная (СООН) и амино (NH2) группы НОМЕНКЛАТУРА В природе встречаются α-аминокислоты L-ряда 1 NH2 O H2N α OH Глицин (аминоуксусная кислота) 3 HOOC O 2 H CH3 2 H2N 1 OH H CH3 3 L-Аланин 2(S)-Аминопропановая кислота МЕТОДЫ СИНТЕЗА 1. Амминолиз галогенокарбоновых кислот O O NH3 H3C OH H3C OH Cl NH2 2. Синтез Габриэля O O NH HO - O O Br - N OC 2H5 H2O/OH N OC 2H5 O O O O - O H2N O - МЕТОДЫ СИНТЕЗА 3. Синтез Штреккера-Зелинского O O KCN+NH 4Cl+H 2O H3C OH H3C NH2 H KCN+NH 4Cl+H 2O HCN+NH 3+KCl O O H3C HCN/CN CN - H3C H OH NH3 CN H O/H + 2 OH H3C H3C NH2 + NH3 МЕТОДЫ СИНТЕЗА 4. Из малонового эфира NH2 NO OC 2H5 H5C2O HNO 2 O O OC 2H5 H5C2O O O O O CH3 C2H5O OC 2H5 H5C2O - CH3 HN - RBr OC 2H5 C H5C2O O O O O HN (CH 3COO) 2O OC 2H5 H5C2O [H] O O O CH3 HN OC 2H5 H5C2O O O R H2O/H O NH2 + OH HO O O R t R OH NH2 МЕТОДЫ СИНТЕЗА 4. Из ненасыщенных кислот O NH2 O NH3 H3C OH H3C ONH 4 5. Синтез Родионова R O + R H5C2O H OC 2H5 O H5C2O OC 2H5 O O O R R OH NH2 O NH3 R OH O HO OH O O