Лекция 13 ВОСПАЛЕНИЕ • Воспаление — один из самых
реклама

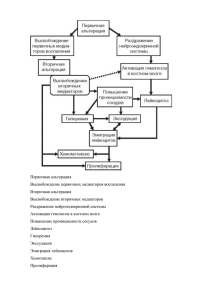
Лекция 13 ВОСПАЛЕНИЕ • Воспаление — один из самых распространенных общепатологических процессов и лежит в основе многих заболеваний (воспалительные заболевания). Неудивительно поэтому, что со времен Гиппократа взгляды на воспаление исторически отражали взгляды на сущность болезни вообще. Поэтому воспаление испытало груз всех течений в медицине — гуморализма, целлюляризма, нервизма, физиологизма, а в конце XX столетия — влияние достижений иммунологии, генетики и молекулярной биологии. ИСТОРИЧЕСКАЯ СПРАВКА Клинические признаки воспаления были впервые описаны римским энциклопедистом Цельсом 2000 лет назад. Он относил к ним красноту (rubor), припухлость ткани — опухоль (tumor), жар (calor) и боль (dolor). В начале нашей эры греческий врач Гален дополнил эти четыре признака пятым — нарушением функции (functio laesa). В довирховский период все многочисленные исследования воспаления проводились путем визуальных наблюдений, хотя и предпринимались попытки выделения различных его форм — катаральное, флегмонозное, гнойное, острое, хроническое воспаление (К.Рокитанский, 1846). Р.Вирхов в "целлюлярной патологии" (1858) смог раскрыть механизмы каждого из классических признаков воспаления: краснота и жар связаны с воспалительной гиперемией, припухлость — со скоплением в ткани экссудата, боль — с повреждением (альтерацией) ткани. Отстаивая свою нутритивную (питательную) теорию воспаления, Р.Вирхов противопоставляет паренхиматозный тип воспаления отделительному (экссудативному). Важным этапом изучения воспаления в XIX веке явились исследования Ю.Конгеймом (1878) сосудистого компонента воспалительной реакции, позволившие выдвинуть сосудистую теорию воспаления. Подтверждением этой теории послужило открытие А.С.Шкляревским краевого стояния лейкоцитов и В.В.Подвысоцким (1899) межэндотелиальной миграции лейкоцитов в очаге воспаления. К концу прошлого столетия сущность воспалительной реакции стала достаточно ясной: это защитно-приспособительная реакция, а назначение ее заключается как в уничтожении агента, вызвавшего повреждение, так и в восстановлении повреж146 денной ткани. Такое толкование воспаления определяет необходимость изучения его в филогенезе. Этот труд взял на себя И.И.Мечников, показавший, что основой воспалительной реакции является фагоцитоз, осуществляющийся с помощью клеточных "цитаз", названных впоследствии лизосомами. Появляется фагоцитарная теория воспаления И.И.Мечникова (1892), наиболее аргументированная в "Сравнительной патологии воспаления" (1917). Теория Мечникова убеждает в совершенствовании механизмов воспаления по мере эволюции организмов, но она касается лишь фагоцитоза, направленного на уничтожение повреждающего агента; репаративная функция воспаления, ее эволюционное совершенствование оказались вне поля зрения исследователя. Репаративный компонент воспаления был раскрыт лишь в середине нашего столетия исследователями, показавшими роль медиации и клеточной рецепции в кинетике воспалительного процесса. H.Dale и P.Luidow (1909) первыми открыли первый медиатор воспаления гистамин, a V.Menkin (1948) выделяет из экссудата вещество — лейкотаксин, влияющий на состояние сосудистой стенки и движение лейкоцитов в очаг воспаления. В дальнейшем среди медиаторов воспаления были выделены биогенные амины, плазменные системы, производные арахидоновой кислоты, кислородные радикалы и гидропероксидазы липидов, а также многочисленные медиаторы нейтрофилов, моноцитов, лимфоцитов и фибробластов [Серов В.В., Пауков B.C., 1995]. Эти исследования позволили дать наиболее полное, раскрыкающее сущность процесса, определение воспаления. СУЩНОСТЬ И ЭТИОЛОГИЯ ВОСПАЛЕНИЯ • Воспаление — наиболее древняя и сложная сосудисто-мезенчимальная реакция на повреждение, направленная не только на ликвидацию повреждающего агента, но и на восстановление поврежденной ткани. Уникальность воспаления в его многоликости. Биологическое его назначение — сохранение вида. Как категория медицинская, воспаление — это и проявление болезни, и патологический процесс, направленный на устранение повреждающего начала и репарацию, т.е. на исцеление от болезни. Этиология воспаления многообразна. Оно может быть вызвано разнообразными э н д о г е н н ы м и и э к з о г е н н ы м и о и о л о г и ч е с к и м и (вирусы, бактерии, грибы, животныепаразиты, антитела и иммунные комплексы), ф и з и ч е с к и м и (лучевая и электрическая энергия, высокие и низкие температуры, пыли и аэрозоли, различные травмы) и х и м и ч е с к и м и ( химические вещества, в том числе лекарства, токсины, яды) фа к т о р а м и . 147 Определение воспаления предусматривает тесную его связь как с иммунитетом (становление иммунитета осуществляется "посредством воспаления" — достаточно вспомнить постинфекционный иммунитет), так и с регенерацией (третья фаза воспаления — фаза репарации). Связь воспаления с иммунитетом и регенерацией хорошо объясняет ставшее аксиомой положение: иммунологический гомеостаз — это структурный гомеостаз. ВОСПАЛЕНИЕ И ИММУНИТЕТ КИНЕТИКА ВОСПАЛИТЕЛЬНОГО ПРОЦЕССА Сопряжение воспаления с иммунитетом для репарации обес печивается участием всех систем защиты организма в уникал ной реакции терминальных сосудов и соединительной ткан„, которая составляет сущность воспаления. Как известно, защиту организма определяют неспецифические факторы и иммунологическая реактивность, или иммунный ответ. Неспецифические факторы защиты и иммунологическая реактивность [по Петрову Р.В., 1982] Неспецифические факторы защиты Иммунологическая реактивность (иммунный ответ) Фагоцитоз Антитела Система комплемента Гиперчувствительность немедленного типа (ГНТ) Гиперчувствительность замедленного типа(ГЗТ) Иммунологическая память Иммунологическая толерантность Идиотипы — антиидиотипы Фагоцитоз Система комплемента Интерферон Лизоцим Пропердин Гидролитические фрагменты Бактерицидные субстанции тканей Непроницаемость покровов В становлении иммунитета при воспалении велика роль ка фагоцитоза, так и системы комплемента. Место фагоцитоза, осуществляемого полиморфно-ядерными лейкоцитами (ПЯЛ) и моноцитарными фагоцитами (макрофаги), в системе иммунитета определяется тем, что, несмотря на неспецифичность самого акта фагоцитоза, фагоциты, особенно макрофаги, принимают участие в очищении антигенов, переработке их в иммуногенную форму, которую воспринимает Т-хелпер. Место макрофагов 148 системе иммунитета определяется и участием в кооперации Т- и В-лимфоцитов, необходимой для становления иммунного ответа. Поэтому фагоцитоз дополняет формы реакций иммунологической реактивности. Система комплемента участвует в специфических реакциях, присоединяя свои компоненты к молекулам антител, что обеспечивает лизис антигенных субстанций, против которых выработаны антитела. Из этого следует, что комплемент как один из неспецифических факторов защиты принимает участие в иммунном ответе, поэтому он, как и фагоцитоз, дополняет формы иммунологической реактивности. Как видно, включение иммунного ответа при воспалении обеспечивается двумя клеточными системами неспецифической защиты: системой моноцитарных фагоцитов, а также плазменной системой — системой комплемента. Кинетика воспалительной реакции для достижения конечной цели — элиминации повреждающего агента и репарации ткани — характеризуется сменой взаимоотношений клеточных систем защиты между собой и с системой соединительной ткани, что определяется медиаторной регуляцией. Из этого, однако, не следует, что в воспалительной реакции участвуют лишь ПЯЛ, макрофаги, лимфоциты и фибробласты. Клетки — носители вазоактивных аминов (лаброциты, базофилы, тромбоциты), как и сдерживающие их функциональную активность эозинофилы, имеют огромное значение для развития собственно сосудистой реакции воспаления. Но они непричастны к основному назначению воспалительной реакции — элиминации повреждающего начала и репарации повреждения. Как цепная, в значительной мере саморегулирующаяся, воспалительная реакция укладывается в универсальную схему: повреждение -+ медиация ► рецепция ► кле точная кооперация > клеточные трансформации ► репарация (схема 16). Воспалительная реакция определяет и последовательно развивающиеся фазы: 1) повреждения, или альтерации, 2) экссудации, 3) пролиферации и дифференцировки клеток. П о в р е ж д е н и е ( а л ь т е р а ц и я ) — обязательный компонент воспаления. Это изначально то, на что возникает сосудисто-мезенхимальная реакция, составляющая сущность воспаления. Можно ли считать альтерацию фазой воспаления? Вопрос этот не решается однозначно. Одни современные патологи IRobbins S. et al., 1981] не выделяют альтерацию как таковую, подменяя ее нарушениями микроциркуляции и реологических свойств крови. А.М.Чернух в монографии "Воспаление" (1979) первой стадией воспаления называет сосудистую, выделяя в ней две фазы. Д.С.Саркисов и В.Н.Галанкин (1988) рассматривают альтерацию как неспецифический компонент воспаления, причем не всегда обязательный (В.Н.Галанкин) для развития после149 150 дующей экссудации и пролиферации. Иными словами, допускается возможность развития воспаления без повреждения, причем альтерация в такой ситуации подменяется функциональной недостаточностью полиморфно-ядерных лейкоцитов. Эта позиция, даже условно допускаемая, исключает понимание воспаления как сосудисто-мезенхимальной реакции на повреждение. Многие патологи [Струков А.И., 1972; Серов В.В., Пауков B.C., 1995; Cottier H„ 1980] отстаивают необходимость выделения альтеративной фазы воспаления, характеризующей инициальные процессы (дистрофия, некроз) и выделение медиаторов. Вероятно, у патологоанатома есть все основания для сохранения этой фазы, имеющей конкретное морфологическое и биохимическое выражение. ■ Следует заметить, что сохранение альтеративной фазы воспалительной реакции не оправдывает выделения альтеративной формы воспаления, при которой сама сосудистомезенхимальная реакция на повреждение практически отсутствует. Поэтому необходимо согласиться с большинством современных патологов в том, что признание альтеративного воспаления, выделяемого классической патологией прошлого, противоречит сути воспалительной реакции в ее современном толковании. Повреждение и медиация — неразрывные компоненты морфогенеза воспаления, поскольку медиаторы "рождаются" в самом повреждении (альтерации). Принято выделять плазменные (циркулирующие) медиаторы, представленные прежде всего калликреин-кининовой системой, системой комплемента и системой свертывания крови, а также клеточные (локальные) медиаторы, связанные со многими клетками: лаброцитами, тромбоцитами, базофилами, ПЯЛ, макрофагами, лимфоцитами, фибробластами и др. Однако и плазменные, и клеточные медиаторы тесно взаимосвязаны и работают при воспалении как аутокаталитическая система, использующая принципы "обратной связи", "дублирования", "необходимого разнообразия" и"антагонизма". Эти принципы системы позволяют циркулирующим медиаторам обеспечить повышение сосудистой проницаемости и активацию хемотаксиса ПЯЛ для фагоцитоза, а внутрисосудистую коагуляцию в отводящих из очага воспаления сосудах — для отграничения возбудителя и самого очага воспаления (барьерная функция очага воспаления). При этом основные этапы сосудистой реакции — повышение проницаемости, активация хемотаксиса ПЯЛ и фактора Хагемана — дублируются несколькими медиаторами. Те же принципы системы в аутокаталитической реакции клеточных медиаторов обеспечивают не только повышение сосудистой проницаемости, фагоцитоз и вторичную деструкцию, но и включение иммунного ответа для элиминации повреждающего агента и продуктов повреждения и, наконец, репарацию ткани путем пролиферации и дифференцировки клеток в очаге воспаления. Наиболее ярко принцип дублирования выражен среди клеток — носителей вазоактивных веществ — лаброцитов, базофи-лов, тромбоцитов, а антагонистические начала — между этими клетками и эозинофильными лейкоцитами: медиаторы лаброцитов и базофилов стимулируют хемотаксис эозинофилов, последние же способны инактивировать эти медиаторы и фагоцитировать гранулы лаброцитов (схема 17). Среди клеток, несущих медиаторы сосудистой проницаемости, возникает "антагонистическое равновесие", определяющее своеобразие морфологии сосудистой фазы воспаления, особенно при аллергических реакциях. Клеточные медиаторы — лейкокины, монокины (интерлейкин-1), лимфокины (интерлейкин-2) и фиброкины — являются локальными регуляторами кооперации клеток на "поле" воспаления — ПЯЛ, макрофага, лимфоцита и фибробласта [Серов В.В., Шехтер А.Б., 1981]. Другими словами, клеточные медиаторы определяют последовательность и долю участия в воспалении фагоцитарной и иммунной систем, с одной стороны, и системы соединительной ткани — с другой. "Дирижером" ансамбля клеточных медиаторов следует считать м о н о к и н ы м а к р о ф а г о в (схема 18). Макрофаги, 151 поддерживаемые медиаторной ауторегуляцией, способны управлять с помощью монокинов дифференцировкой гранулоцитов и моноцитов из стволовой клетки, пролиферацией этих клеток, т.е. являются регуляторами фагоцитоза. Макрофаги не только влияют на функциональную активность Т- и В-лимфоцитов, принимают участие в их кооперации, но и секретируют 6 первых компонентов комплемента, т.е. являются посредниками привлечения иммунной системы в воспалительную реакцию. Макрофаги индуцируют рост фибробластов и синтез коллагена, т.е. являются стимуляторами завершающей фазы репаративной реакции при воспалении. Вместе с тем сами макрофаги испытывают регулярное влияние лимфокинов и фиброкинов, т.е. теснейшим образом связаны в локальной клеточной регуляции с лимфоцитом и фиб-робластом [Серов В.В., Шехтер А.Б., 1981; Маянский А.Н., Ма-янский Д.Н., 1983]. 152 К л е т о ч н а я р е ц е п ц и я играет огромную роль в локальной клеточной регуляции при воспалении. С нею связаны межклеточное взаимодействие и привлечение в очаг воспаления компонентов иммунных реакций, так как у всех эффекторных клеток воспаления обнаружены Fc-рецепторы иммуноглобулинов и С-рецепторы комплемента. Становятся понятными неразрывная связь и неравнозначное во времени сопряжение фагоцитарной системы, иммунной системы и системы соединительной ткани в реализации конечной цели воспалительной реакции (схема 19). Варианты этого сопряжения, зависящие от особенностей как повреждающего агента, так и организма, реагирующего на повреждение, должны, вероятнее всего, определять развитие той или иной формы воспаления. Так, гнойное воспаление (вид экссудативного воспаления) отражает, вероятно, особую форму сопряжения функционально несостоятельной системы ПЯЛ с макрофагами. При этом макрофаги, усиленно фагоцитирующие распадающиеся ПЯЛ, становятся устойчивыми к возбудителю. В.Е.Пигаревский (1978), изучающий это особое взаимоотношение двух систем фагоцитоза, называет его резорбтивной клеточной резистенцией. Как видно, оно отражает вторичную несостоятельность фагоцитарной функции макрофагов при первичной несостоятельности фагоцитоза ПЯЛ. Первичная и избирательная несостоятельность системы моноцитарных фагоцитов, разобщение ее с системой ПЯЛ лежат в основе гранулематозного воспаления (вид продуктивного воспаления). Фагоцитарная недостаточность макрофагов определяет образование из них эпителиоидных и гигантских клеток, теряющих фагоцитарные функции. Фагоцитоз подменяется отграниче154 нием, персистенцией возбудителя. Незавершенный фагоцитоз делает незавершенной и несовершенной саму воспалительную реакцию. Она становится выражением реакции гиперчувствительности замедленного типа (ГЗТ). Очевидно также, что наследственные дефекты каждой из систем защиты, как и системы самой соединительной ткани, делают дефектной и воспалительную реакцию как по форме ее проявления и течению, так и по возможности реализации конечной цели. Достаточно вспомнить наследственную недостаточность бактерицидных систем ПЯЛ и моноцитов, наиболее ярко представленную при хронической гранулематозной болезни детей, наследственные и врожденные иммунные дефициты и фатальность развивающейся при них гнойной инфекции, врожденную несостоятельность соединительной ткани и упорство хронического воспаления. Нельзя не сказать и о наследственных дефицитах системы комплемента, особенно СЗ- и С5-компонснтов ее. Эти дефициты проявляются либо рецидивирующей гнойной инфекцией, либо волчаночноподобным синдромом. При воспалении, особенно вызываемом различными агентами, пошлются как циркулирующие в крови, так и локальные гетсрологичные иммунные комплексы, при хроническом течении воспалении они могут быть и аутологичными. Так, при воспалении возникают иммунокомплексные реакции — наиболее частые среди реакций гиперчувствительности немедленного типа (ГНТ). ВОСПАЛЕНИЕ И ГИПЕРЧУВСТВИТЕЛЬНОСТЬ ИММУННОЕ ВОСПАЛЕНИЕ Связь воспаления и иммунных реакций в сенсибилизированном организме известна давно, со времени формирования C.F.Pirquet и B.Schick (1905) самого понятия "аллергия". Тот же C.F.Pirquet предложил выделять среди аллергических реакций немедленную (ускоренную) и замедленную (растянутую) формы. Однако лишь после работ R.Rossle (1914) и А.И.Абрикосова (1933) стала понятна гиперергическая сущность аллергического воспаления. Ими было показано, что для гиперергического воспаления характерны не только выраженная экссудация, но и дистрофические и некротические (фибриноидный некроз) изменения соединительной ткани, микротромбы в сосудах, кровоизлияния. Потребовалось несколько десятков лет поисков и находок иммунологии и морфологии для того, чтобы показать, что немедленная и замедленная аллергия в своей основе имеет иммунопатологические реакции, а последние представлены своеобразным в о с п а л е н и е м , которое не без оснований стали называть 155 и м м у н н ы м [ Струков А.И., 1979]. Важно отметить, что характер иммунного воспаления, т.е. морфология реакций гиперчувствительности, целиком зависит от особенностей иммунопатологического механизма (подробнее см. лекцию 17 "Реакции гиперчувствительности") . КЛАССИФИКАЦИЯ ВОСПАЛЕНИЯ Классификация воспаления учитывает характер течения процесса и морфологические формы в зависимости от преобладания экссудативной или пролиферативной фазы воспаления. По х а р а к т е р у т е ч е н и я воспаление подразделяют на острое, подострое и хроническое. Следует заметить, что критерии выделения подострого воспаления весьма условны. О хроническом воспалении говорят тогда, когда оказывается несостоятельной репаративная фаза. Поэтому хроническое воспаление и является основным проявлением дисрегенерации (подробнее см. лекцию 16 "Воспаление, регенерация и дисрегенерация"). По п р е о б л а д а н и ю ф а з ы в о с п а л е н и я различают э к с с у д а т и в н о е и п р о л и ф е р а т и в н о е (продуктивное) воспаление; каждое из них подразделяется на несколько видов. О несостоятельности выделения альтеративной формы воспаления уже упоминалось. Не обосновано и бытующее еще деление воспаления на "банальное" и "специфическое", так как любая форма воспаления, развивающаяся в результате воздействия того или иного повреждающего агента, может быть названа специфической. Недостаточно оправдано и выделение геморрагического вида экссудативного воспаления, критерии отличия которого от кровоизлияния практически отсутствуют. Многие вопросы, касающиеся классификации воспаления, его взаимодействия с другими реакциями организма, биологической сущности — состоятельность защитно-приспособительной реакции, клинического значения и др., подлежат дальнейшему изучению и обсуждению.