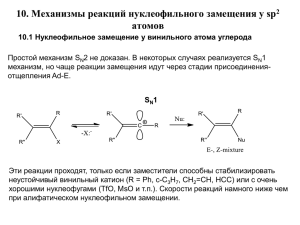
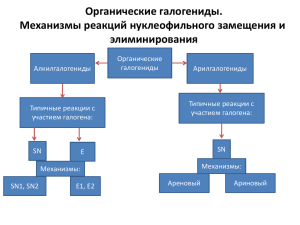
Программа лекций, «Биоорганическая химия
реклама

Программа лекций по курсу «Биоорганическая химия» Весенний семестр 2012 г. Неделя 1 2 3 4 5 6 7 8 9 10 Лекция Введение. Предмет органической химии. Углерод. Источники выделения и получения органических веществ. Основные классы органических веществ. Рациональная и IUPAC номенклатура – основные положения. Методы исследования органических соединений. Химическая связь в органических соединениях. Методы молекулярных орбиталей (МО) и резонансных структур (РС). Индуктивные эффекты. Энергия сопряжения. Мезомерные эффекты. Делокализованные связи в методе РС. Предельные резонансные структуры. Химическая связь в органических соединениях (продолжение). Ароматические соединения, ароматичность. Правило Хюккеля. Бензол и другие ароматические циклы. Водородная связь в органических соединениях. Слабые межмолекулярные взаимодействия. Пространственная изомерия органических соединений – основные понятия. Физикохимические и биологические свойства стереоизомеров. Стереоспецифичность в биологических системах: стереоспецифичность лекарственных веществ, биологически активных веществ, ферментативных реакций, взаимодействия «рецептор-лиганд». Классификация органических реакций. Электрофильные и нуклеофильные реагенты. Нуклеофильное замещение при насыщенном атоме углерода. Моно- и бимолекулярный механизмы нуклеофильного замещения. Влияние на скорость нуклеофильного замещения и на реализацию SNI-, SN2-механизмов строения субстрата, природы уходящей группы, пространственных эффектов, нуклеофильного агента. Соотношение между нуклеофильностью и основностью. Зависимость скорости нуклеофильного замещения от полярности растворителя. Стереохимия нуклеофильного замещения. Вальденовское обращение. Электрофильное присоединение к кратным связям. Механизмы электрофильного присоединения. -Комплексы. Неклассические циклические карбкатионы как промежуточные продукты электрофильного присоединения. Стереохимия присоединения. Влияние на скорость электрофильного присоединения строения субстрата. Электрофильное замещение в ароматических системах. Механизм электрофильного замещения. - и σ-Комплексы. Влияние строения субстрата на скорость электрофильного замещения. Ориентирующее влияние заместителей. Нуклеофильное присоединение к кратным связям углерод-гетероатом. Механизм нуклеофильного присоединения. Кислотно-основной катализ. Зависимость скорости присоединения от строения субстрата. Типичные реакции присоединения: гидратация, получение ацеталей, взаимодействие альдегидов и кетонов с азотосодержащими нуклеофилами. Нуклеофильное присоединение к кратным связям углерод-гетероатом (продолжение). Типичные реакции присоединения: реакции карбоновых кислот и их производных. Гидролиз сложных эфиров и амидов, реакция переэтерификации, реакция этерификации, взаимодействие карбонильных соединений с металлоорганическими соединениями и карбанионами. Реакции β-элиминирования. Моно- и бимолекулярное отщепление. Стереохимия отщепления. Влияние на соотношение реакций замещения и отщепления внутренних и 11 12 13 14 15 16 внешних факторов. Аминокислоты. Классификация аминокислот. Протеиногенные и непротеиногенные аминокислоты. Стереохимия аминокислот. Кислотно-основные свойства, цвиттерионы, изоэлектрическая точка. Химические реакции для открытия и определения аминокислот в гидролизатах белков. Незаменимые аминокислоты. Белки и пептиды. Функции белков в клетке и организме. Классификация белков (глобулярные и фибриллярные белки, простые и сложные белки). Белки-рецепторы. Пептидная связь, ее свойства. Пептидомиметики. Белки (продолжение). Физико-химические свойства белков. Денатурация белка. Изоэлектрическая и иозоинная точки белков. Структурная организация белковых молекул. Первичная, вторичная третичная и четвертичная структура белков. Принципы определения первичной структуры. Современные методы выделения, очистки исследования структуры и свойств белков. Методы определения концентрации белка. Ферменты. Понятие о ферментах. Классификация и номенклатура ферментов. Химическая природа ферментов. Основные свойства ферментов. Строение ферментов, понятие активного центра. Регуляция активности ферментов. Мультимолекулярные ферментные системы. Коферменты. Применение ферментов в биологии и медицине. Проблемы медицинской энзимологии. Нуклеиновые кислоты. Азотистые основания. Таутомерное равновесие. Понятие нуклеозида и нуклеотида. Роль свободных моно- и динуклеотидов в клетке. ДНК и РНК. Химический состав нуклеиновых кислот. Структура нуклеиновых кислот. Правила Чаргаффа. Вторичная и третичная структура нуклеиновых кислот. Роль ДНК и РНК в клетке. Химия углеводов. Классификация углеводов. Моносахариды, их основные типы. D-ряд углеводов. Циклические формы сахаров. Проекции Хедорса. Конформация сахаров. Основные реакции моносахаридов. Олиго-и полисахариды (гомои гетерополисахариды). Биологическая роль углеводов. Основные представители (крахмал, гликоген, целлюлоза, хитин, гликозаминогликаны). Химия липидов. Классификация липидов. Жирные кислоты. Глицериды. Фосфолипиды (глицерофосфолипиды, сфинголипиды). Гликолипиды. Стероиды. Биологическая роль липидов. Перекисное окисление липидов.