Любое вещество может находиться в ... газообразном. Возможен переход из одного ... ТЕМА: СТРОЕНИЕ И КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ И СПЛАВОВ
реклама

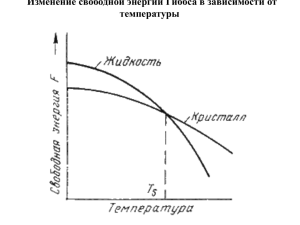
ТЕМА: СТРОЕНИЕ И КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ И СПЛАВОВ Лекция 3 3.1. Строение металлов и сплавов Любое вещество может находиться в трех агрегатных состояниях: твердом, жидком, газообразном. Возможен переход из одного состояния в другое, если новое состояние в новых условиях является более устойчивым, обладает меньшим запасом энергии. С изменением внешних условий свободная энергия изменяется по сложному закону различно для жидкого и кристаллического состояний. Характер изменения свободной энергии жидкого и твердого состояний с изменением температуры показан на рис. 3.1. Рис. Изменение свободной энергии в зависимости от температуры В соответствии с этой схемой выше температуры ТS вещество должно находиться в жидком состоянии, а ниже ТS – в твердом. При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго. Температура ТS – равновесная или теоретическая температура кристаллизации. Рассмотрим переход металла из жидкого состояния в твердое. При нагреве всех кристаллических тел наблюдается четкая граница перехода из твердого состояния в жидкое. Такая же граница существует при переходе из жидкого состояния в твердое. Кристаллизация – это процесс образования участков кристаллической решетки в жидкой фазе и рост кристаллов из образовавшихся центров. Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура. Кривая охлаждения чистого металла представлена на рис. 3.2. Рис. Кривая охлаждения чистого металла – теоретическая температура кристаллизации; .– фактическая температура кристаллизации. 1 3.2. Механизм и закономерности кристаллизации металлов При соответствующем понижении температуры в жидком металле начинают образовываться кристаллики – центры кристаллизации или зародыши. Механизм кристаллизации представлен на рис.3.4. Рис.3.4. Модель процесса кристаллизации Центры кристаллизации образуются в исходной фазе независимо друг от друга в случайных местах. Сначала кристаллы имеют правильную форму, но по мере столкновения и срастания с другими кристаллами форма нарушается. Рост продолжается в направлениях, где есть свободный доступ питающей среды. После окончания кристаллизации имеем поликристаллическое тело. 3.3. Понятие об изотропии и анизотропии Свойства тела зависят от природы атомов, из которых оно состоит, и от силы взаимодействия между этими атомами. Силы взаимодействия между атомами в значительной степени определяются расстояниями между ними. В аморфных телах с хаотическим расположением атомов в пространстве расстояния между атомами в различных направлениях равны, следовательно, свойства будут одинаковые, то есть аморфные тела изотропны В кристаллических телах атомы правильно располагаются в пространстве, причем по разным направлениям расстояния между атомами неодинаковы, что предопределяет существенные различия в силах взаимодействия между ними и, в конечном результате, разные свойства. Зависимость свойств от направления называется анизотропией 3.4. Аллотропия или полиморфные превращения Способность некоторых металлов существовать в различных кристаллических формах в зависимости от внешних условий (давление, температура) называется аллотропией или полиморфизмом. Каждый вид решетки представляет собой аллотропическое видоизменение или модификацию. Примером аллотропического видоизменения в зависимости от температуры является железо (Fe). Fe: – ОЦК ; – ГЦК - ; – ОЦК ; (высокотемпературное ) Превращение одной модификации в другую протекает при постоянной температуре и сопровождается тепловым эффектом. Видоизменения элемента обозначается буквами греческого алфавита в виде индекса у основного обозначения металла. 2 Примером аллотропического видоизменения, обусловленного изменением давления, является углерод: при низких давлениях образуется графит, а при высоких – алмаз. 3.5. Магнитные превращения Некоторые металлы намагничиваются под действием магнитного поля. После удаления магнитного поля они обладают остаточным магнетизмом. Это явление впервые обнаружено на железе и получило название ферромагнетизма. К ферромагнетикам относятся железо, кобальт, никель и некоторые другие металлы. При нагреве ферромагнитные свойства металла уменьшаются постепенно: вначале слабо, затем резко, и при определ¨нной температуре (точка Кюри) исчезают (точка Кюри для железа – ). Выше этой температуры металлы становятся парамагнетиками. Магнитные превращения не связаны с изменением кристаллической решетки или микроструктуры, они обусловлены изменениями в характере межэлектронного взаимодействия. 3.6. Понятие о сплавах и методах их получения Под сплавом понимают вещество, полученное сплавлением двух или более элементов. Возможны другие способы приготовления сплавов: спекания, электролиз, возгонка. В этом случае вещества называются псевдосплавами. Сплав, приготовленный преимущественно из металлических элементов и обладающий металлическими свойствами, называется металлическим сплавом. Основные понятия в теории сплавов. Компоненты – вещества, образующие систему. В качестве компонентов выступают чистые вещества и химические соединения. Фаза – однородная часть системы, отделенная от других частей системы поверхностного раздела, при переходе через которую структура и свойства резко меняются. 3.7. Особенности строения, кристаллизации и свойств сплавов: механических смесей, твердых растворов, химических соединений Строение металлического сплава зависит от того, в какие взаимодействия вступают компоненты, составляющие сплав. Почти все металлы в жидком состоянии растворяются друг в друге в любых соотношениях. При образовании сплавов в процессе их затвердевании возможно различное взаимодействие компонентов. В зависимости от характера взаимодействия компонентов различают сплавы: 1. механические смеси; 2. химические соединения; 3. твердые растворы. Сплавы механические смеси образуются, когда компоненты не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. Образуются между элементами значительно различающимися по строению и свойствам, когда сила взаимодействия между однородными атомами больше чем между разнородными. Сплав состоит из кристаллов входящих в него компонентов (рис. 4.1). В сплавах сохраняются кристаллические решетки компонентов. 3 Рис. Схема микроструктуры механической смеси Сплавы химические соединения образуются между элементами, значительно различающимися по строению и свойствам, если сила взаимодействия между разнородными атомами больше, чем между однородными. Особенности этих сплавов: 1. Постоянство состава, то есть сплав образуется при определенном соотношении компонентов, химическое соединение обозначается Аn Вm/ 2. Образуется специфмческая, отличающаяся от решеток элементов, составляющих химическое соединение, кристаллическая решетка с правильным упорядоченным расположением атомов (рис. 4.2) 3. Ярко выраженные индивидуальные свойства 4. Постоянство температуры кристаллизации, как у чистых компонентов Рис. Кристаллическая решетка химического соединения Сплавы твердые растворы – это твердые фазы, в которых соотношения между компонентов могут изменяться. Являются кристаллическими веществами. Характерной особенностью твердых растворов является:наличие в их кристаллической решетке разнородных атомов, при сохранении типа решетки растворителя. Твердый раствор состоит из однородных зерен (рис. 4.3). Рис. Схема микроструктуры твердого раствора 3.7. Кристаллизация сплавов Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. В сплавах в твердых состояниях, имеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз, когда растворимость компонентов в твердом состоянии меняется с изменением температуры. Эти превращения называют фазовыми превращениями в твердом состоянии. При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост. 4 Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы, в течение некоторого времени, имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз. Нарушение когерентности и обособления кристаллов наступает, когда они приобретут определенные размеры. Процессы кристаллизации сплавов изучаются по диаграммам состояния. 5