ЛЕКЦИЯ ГЕМОРРАГИЧЕСКИЙ ИНСУЛЬТ ЗАДНЕЙ ЧЕРЕПНОЙ ЯМКИ
реклама

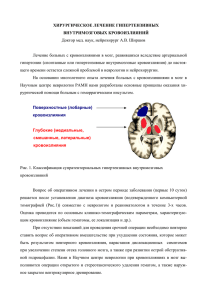
НЕЙРОХИРУРГИЯ, № 4, 2006 ЛЕКЦИЯ © КОЛЛЕКТИВ АВТОРОВ, 2006 ГЕМОРРАГИЧЕСКИЙ ИНСУЛЬТ ЗАДНЕЙ ЧЕРЕПНОЙ ЯМКИ В.В. Крылов, В.Г. Дашьян, А.А. Мурашко, С.А. Буров 1 НИИ скорой помощи им. Н.В. Склифосовского, Московский государственный медико-стоматологический университет В лекции рассматриваются современные взгляды на этиологию и патогенез нетравматических кровоизлияний в мозжечок и ствол мозга, варианты клинического течения заболевания, построение диагностического комплекса, вопросы выбора тактики лечения и вида хирургического вмешательства в зависимости от тяжести состояния больных, локализации и объема гематомы, наличия вентрикулярного кровоизлияния, наличия и выраженности окклюзионной гидроцефалии. Уделено внимание применению малоинвазивных методик хирургического лечения геморрагического инсульта задней черепной ямки (пункционная аспирация и локальный фибринолиз кровоизлияний, эндоскопическая аспирация, наружное дренирование желудочков), вопросам прогнозирования исхода заболевания. Отмечена тенденция к использованию более активной хирургической тактики при мозжечковых и стволовых кровоизлияниях. Ключевые слова: геморрагический инсульт задней черепной ямки The paper reviews modern concepts of the etiology and pathogenesis of non-traumatic intracranial cerebellar and brainstem hemorrhages, the variants of clinical course of the disease, the diagnostic algorithms and the management and the type of surgical intervention that is determined by the degree of severity of the patient’s clinical status, by the localization and the volume of haematoma and by the presence of ventricular hemorrhage together with the presence and the degree of severity of obstructive hydrocephalus. Special attention is drawn to the application of less invasive surgical techniques in the course of treatment of hemorrhagic stroke located in the posterior cerebral fossa (puncture aspiration and local fibrinolysis of hemorrhages, endoscopic aspiration, external ventricular drainage) together with the items concerning the prognosis of the outcome of the disease. The tendency towards the application of more active surgical approach in case of cerebellar and brainstem hemorrhages has been detected. Key words: hemorrhagic stroke in the posterior cerebral fossa. В структуре острых нарушений мозгового кровообращения геморрагический инсульт (ГИ) составляет 8—13%. Субтенториальная локализация кровоизлияния встречается у 9—20% больных. Патогенез. По своей этиологии первичные внутримозжечковые кровоизлияния не отличаются от супратенториальных. У 60% больных основной причиной кровоизлияния в мозжечок является артериальная гипертензия. У 40% кровоизлияние обусловлено разрывом сосудистых мальформаций и осложнениями антикоагулянтной терапии. У детей причиной первичных внутримозжечковых кровоизлияний чаще всего являются ангиомы, у пожилых — церебральная амилоидная ангиопатия. Для инсульта мозжечка характерно развитие кровоизлияний по типу гематомы (рис. 1). В первые часы кровоизлияния не происходит значительного разрушения мозгового вещества. Излившаяся кровь раздвигает ткань мозга, что сопровождается смещением отдельных его участков. При таком механизме формирования гематомы ее размеры намного превышают объем разрушенной ткани мозга. Гематомы чаще располагаются в области зубчатого ядра мозжечка, в бассейне ветвей верхней мозжечковой артерии, которые наиболее часто поражаются при гипер1 6 Россия, 129090, Москва, Большая Сухаревская площадь, 3. тонической болезни и являются источником кровоизлияния [3]. Определяющим фактором в патогенезе заболевания при геморрагическом инсульте мозжечка имеет масс-эффект и связанный с ним дислокационный процесс, приводящий к сдавлению ствола и IV желудочка. Размер гематомы при первичных внутримозжечковых кровоизлияниях определяет клиническое течение и исход заболевания [4, 6]. Проникновение крови в желудочковую систему наблюдается у 66—75% больных с ГИ задней черепной ямки (ЗЧЯ) [7]. Наиболее высокая вероятность прорыва крови в IV желудочек отмечается при медиальных гематомах мозжечка. Обычно это сопровождается развитием окклюзионной гидроцефалии (рис. 2). Геморрагический инсульт стволовой локализации чаще всего возникает в мосту, а в других отделах ствола встречается редко. Основную роль в генезе этих кровоизлияний играет артериальная гипертония и кавернозные ангиомы. В отличие от кавернозных ангиом другой локализации, повторные кровоизлияния из этого вида мальформаций ствола встречаются чаще. Другие этиологические факторы ГИ данной локализации менее значимы [11]. Кровоизлияния в ствол чаще развиваются по типу геморрагического про- ЛЕКЦИЯ а б в Рис. 1. Компьютерные томограммы больных c инсультами мозжечка различной локализаци: а — гематома левого полушария мозжечка. Сдавление и дислокация IV желудочка; б — гематома верхних отделов червя мозжечка; в — гематома правого полушария и червя мозжечка. Гемотампонада IV желудочка. Рис. 2. Компьютерные томограммы больных c кровоизлиянием в заднюю черепную ямку. Гематома полушарий и червя мозжечка, гемотампонада IV желудочка, кровоизлияние в III и боковые желудочки, вентрикуломегалия. питывания. По этой причине непосредственно в момент кровоизлияния и в ближайшее время после него происходит выраженное повреждение нервной ткани ствола в месте локализации кровоизлияния (рис. 3). Отек ствола, приводящий к деформации ликворопроводящих путей, и часто наблюдаемый прорыв крови в четвертый желудочек являются причиной развития окклюзионной гидроцефалии. Токсическое действие компонентов крови, а также механическая компрессия жизненно важных образований ствола мозга, приводит к нарушению сознания, развитию острой сердечно-сосудистой недостаточности, что и обусловливает высокую летальность. Диагностика кровоизлияний в заднюю черепную ямку Для геморрагического инсульта структур ЗЧЯ характерно острое и реже подострое течение заболевания. Клиническая картина обусловлена локализацией кровоизлияния, развитием дислокации ствола или окклюзионной гидроцефалией. Специфические клинические проявления поражения структур задней черепной ямки (изменение координации и мышечного тонуса, поражение ядер и проводящих путей ствола, нистагм) у больных без нарушения сознания позволяют локализовать патологический процесс. Среди больных с выраженным угнетением сознания это удается только у 23% [10]. С внедрением в клиническую практику рентгеновской компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) значительно возросла выявляемость кровоизлияний в структуры ЗЧЯ. Эти методы позволяют установить как сам факт кровоизлияния, так и его локализацию, а также объем, выявить наличие окклюзионной гидроцефалии, ее выраженность, наличие и степень сдавления ствола головного мозга, характер дислокационного процесса. Компрессия IV желудочка является главным томографическим признаком сдавления ство7 НЕЙРОХИРУРГИЯ, № 4, 2006 ла. Было установлено, что наличие деформации IV желудочка коррелирует с частотой выявления стволовой симптоматики. Этот признак рассматривается как основное показание к операции, а также является неблагоприятным прогностическим фактором исхода при ГИ мозжечка [2, 9]. Компрессия околостволовых цистерн связана как с наличием гидроцефалии, так и с масс-эффектом гематомы. У больных с выраженной дизрезорбтивной гидроцефалией иногда наблюдается деформация околостволовых цистерн, однако при наличии объемного образования в ЗЧЯ деформация четверохолмной и обходной цистерн рассматривается как признак восходящей транстенториальной дислокации. Рентгеновская КТ является методом выбора в остром периоде внутримозжечкового кровоизлияния (ВМК) из-за ее высокой чувствительности к кровоизлияниям в этой фазе и небольшой длительности исследования. Для ранней диагностики кровоизлияний МРТ традиционно считается менее чувствительным и специфичным методом, чем рентгеновская КТ. В силу того, что в первые сутки в области гематомы дезокси- и метгемоглобин практически отсутствуют, кровоизлияние имеет изоплотностные характеристики и его четкая визуализация затруднена. МРТ более информативна при диагностике подострого и хронического кровоизлияний, а также особенностей дислокационных процессов. МРангиография в ряде случаев позволяет обнаружить причину внутримозгового кровоизлияния, например сосудистую мальформацию [1]. Церебральную ангиографию проводят для исключения сосудистой аномалии (мальформации, аневризмы) у больных молодого возраста, при отсутствии гипертонического анамнеза и при сочетании внутримозгового кровоизлияния с базальным субарахноидальным кровоизлиянием. Частота выявления сосудистых аномалий, связанных с кровоизлияниями в заднюю черепную ямку, составляет не более 25%, а у пожилых больных, страдающих артериальной гипертонией, встречается крайне редко. В связи с этим целесообразность обязательного выполнения ангиографии при данной патологии обсуждается [8]. Регистрация акустических стволовых вызванных потенциалов позволяет проводить оценку состояния стволовых структур при кровоизлияниях в ствол и мозжечок. Выявление нарушения проведения звуковых сигналов в виде увеличения латентности пиков, снижение их амплитуды (особенно III и V), увеличение межпиковых интервалов (I—III, III—V, I—V) рассматривается как один из признаков повреждения стволовых структур и играет важную роль в определении тактики дальнейшего лечения больного. б а 8 Рис. 3. Компьютерные томограммы больных с гематомами ствола мозга: а — гематома продолговатого мозга, моста и среднего мозга, окклюзия водопровода мозга, вентрикуломегалия; б — гематома моста, сдавление и дислокация IV желудочка. ЛЕКЦИЯ Все больные с кровоизлиянием в ЗЧЯ подлежат госпитализации. При тяжелом течении заболевания, развитии бульбарного синдрома, дыхательных нарушений и острой сердечно-сосудистой недостаточности необходима госпитализация больного в реанимационное отделение, раннее протезирование дыхания, проведение противоотечной терапии. Хирургическое лечение Впервые об успешном хирургическом лечении геморрагического инсульта сообщил Macewan в 1883 г. На протяжении многих лет мнения о целесообразности хирургического лечения ГИ остаются неоднозначными. Но в отношении кровоизлияний в мозжечок хирургическая активность всегда оставалась выше, чем при инсультах другой локализации. Так, по данным популяционного исследования Greater Cincinnati за 1988 г. из 188 больных с внутримозговыми кровоизлияниями 29% оперированы по поводу внутримозжечковых кровоизлияний и 10% — по поводу кровоизлияний в мост, в то время как частота операций при лобарных кровоизлияниях составила 24% [8]. Высокая хирургическая активность при мозжечковых гематомах обусловлена тем, что в большинстве случаев заболевание протекает бурно, сопровождается острой окклюзионной гидроцефалией и необходимость операции, как правило, не вызывает сомнений. Кроме того, при своевременно выполненной операции и благоприятном течении заболевания в послеоперационном периоде, грубого неврологического дефицита, в отличие от подкорковых кровоизлияний, как правило, не остается. При геморрагическом инсульте мозжечка большинство нейрохирургов и неврологов являются сторонниками экстренного хирургического лечения, а при геморрагическом инсульте ствола до последнего времени была принята тактика консервативного лечения [9]. Имеются четкие патогенетические предпосылки для обоснования раннего (в течение первых 12 ч после начала заболевания) хирургического лечения. Удаление гематомы в этот период позволяет устранить масс-эффект кровоизлияния, предупредить развитие острой окклюзионной гидроцефалии и токсическое влияние компонентов крови на перифокальную мозговую ткань. Однако удаление гематомы в течение первых 4—6 ч после начала заболевания, как и при инсультах другой локализации, сопряжено с повышением риска развития повторных кровоизлияний. Хирургическое лечение при гематоме мозжечка показано при ее объеме более 10—15 мл или максимальном диаметре более 3 см, угнетении сознания до 13 баллов и менее по шкале комы Глазго, наличии стволовой симптоматики, деформации и смещении IV желудочка, деформации четверохолмной и обходной цистерн, гемотампонаде IV желудочка, развитии окклюзионной гидроцефалии (вентрикуломегалия с вентрику- ло-краниальным коэффициентом (ВКК2) более 20%) [2,5]. Абсолютными противопоказаниями для хирургического лечения больных с ГИ мозжечка являются: глубокая или запредельная кома, отсутствие стволовых рефлексов, вялая тетраплегия, нестабильная гемодинамика, КТ-признаки выраженного разрушения ствола головного мозга. Относительными противопоказаниями являются тяжелая коагулопатия, декомпенсированный сахарный диабет, сердечно-сосудистая, легочная, почечная недостаточность и другие тяжелые сопутствующие заболевания, пожилой возраст больного (более 70—75 лет). Несмотря на то что геморрагический инсульт моста чаще характеризуется тяжелым или крайне тяжелым течением и высокими показателями летальности, имеются серии наблюдений, показывающие эффективность хирургического лечения при данной патологии. Возможность хирургии гематом ствола связана с развитием нейронавигации и появлением новых, малоинвазивных методов вмешательств. Хирургическое лечение может оказаться эффективным при лечении больных с угнетением сознания от оглушения до комы, и приводит не только к снижению летальности, но и к улучшению функциональных исходов. Консервативное лечение коматозных больных малоэффективно. У больных в стабильно компенсированном состоянии, как правило, течение заболевания благоприятное и необходимости в хирургическом лечении нет [12, 13, 15]. Открытые операции Наиболее распространенным на сегодняшний день методом хирургического лечения геморрагического инсульта субтенториальной локализации является трепанация ЗЧЯ и удаление гематомы. Речь идет о мозжечковых кровоизлияниях. Операция позволяет быстро удалить гематому, при необходимости создать декомпрессию задней черепной ямки, выявить и удалить возможную мальформацию. К недостаткам такой операции можно отнести ее относительную длительность и травматичность, а следовательно, более высокую частоту развития послеоперационных осложнений. Тем не менее у больных с компрессией ствола, в том числе с глубоким угнетением сознания, неотложная декомпрессия ЗЧЯ и удаление гематомы мозжечка является операцией выбора. Классические арбалетный (Кушинга) и подковообразный (Денди) доступы к ЗЧЯ сейчас практически не используют в связи с высокой травматичностью. Наиболее распространены срединный доступ по Наффцигеру—Тауну и парамедианные по Геймановичу и Егорову. При отсутствии показаний к созданию декомпрессии можно выполнять костно-пластическую краниотомию затылочной кости без резекции дужки атланта, а при наличии хорошего увеличения и освещения нет необходимости в создании большого трепанационного окна. Для обзора труднодоступных мест можно использовать ассисти9 НЕЙРОХИРУРГИЯ, № 4, 2006 а б Рис. 4. Компьютерные томограммы больных с кровоизлияниями в мозжечок: а — до операции, гематома объемом 22 см3 полушарий и червя мозжечка. Окклюзионная гидроцефалия — ВКК2 — 26%; б — гематома удалена. Вентрикуло-цистерностомия по Торкильдсену. рующую эндоскопию. При сочетании гематомы с вентрикуломегалией возможно выполнение операции Торкильдсена (рис. 4). При инсульте ствола в настоящее время используют только пункционные вмешательства. С учетом относительных противопоказаний, открытая операция может быть заменена менее травматичной (пункционной или эндоскопической аспирацией, с использованием метода локального фибринолиза), но только при компенсированном состоянии больного и отсутствии необходимости в быстром создании наружной декомпрессии структур ЗЧЯ. Малоинвазивные операции В последние 20 лет в лечении геморрагического инсульта, особенно глубинной, подкорковой локализации, получили распространение малоинвазивные методики удаления гематом: пункционная аспирация с использованием метода стереотаксиса или видеоэндоскопии, локального фибринолиза и их сочетания. Эффективность и относительная безопасность пункционных методов и локального фибринолиза хорошо известны [13, 14, 16]. К их преимуществам относят: минимальное повреждение мозга во время вмешательства, возможность удалять глубоко расположенные гематомы малого объема, в том числе гематомы ствола, внутрижелудочковые кровоизлияния, незначительную длительность операции, возможность применения местной анестезии, возможность оперировать пожилых больных и в тяжелом соматическом состоянии. Недостатками этих методов являются: невозможность удаления сосудистых мальформаций, риск инфекционных осложнений, обусловленных длительным дренированием гематомы. Повторные кровотечения, связанные с локальным фибринолизом, не превышают 15%. В силу описанных ранее особенностей клинического течения при инсультах мозжечка малоинвазивные операции распространены меньше, чем при кровоизлияниях супратенториальной локализации, хотя при мостовых кровоизлияниях применяют только пункционные методики. Развитие рамной и безрамной КТ- и МРТ-навигации, интраопера10 ционной томографии позволило чаще использовать малоинвазивные вмешательства (рис. 5). Эндоскопическая аспирация не имеет доказанных преимуществ над стереотаксической, и выбор вида вмешательства в основном определяется традициями клиники. В большинстве случаев и та и другая операция заканчивается дренированием гематомы и проведением, при необходимости, локального фибринолиза оставшегося объема кровоизлияния. Приверженцы эндоскопии относят к ее преимуществам возможность более полного интраоперационного опорожнения гематомы, а соответственно сокращение сроков ее последующего дренирования, возможность удаления вентрикулярных сгустков и визуального контроля интраоперационного кровотечения. Однако это признается не всеми исследователями. После пункционных операций пациентам можно проводить раннее реабилитационное лечение, что особенно важно у пожилых и ослабленных больных, сокращая длительность интенсивной терапии и пребывания их в стационаре. У больных с гематомой моста пункционная аспирация является операцией выбора, и, как указывалось ранее, у тяжелых больных приводит к снижению летальности и улучшению функциональных исходов. При пункции мозжечка трефинацию выполняют в проекции кровоизлияния. При гематомах моста применяют ретромастоидальный доступ. Возможна также трансводопроводная эндо скопическая аспирация гематомы моста [15]. При окклюзионной гидроцефалии с помощью эндоскопа возможно проведение вентрикулостомии III желудочка. Дренирование желудочков Раннее лечение острой окклюзионной гидроцефалии снижает летальность и улучшает степень восстановления больных при кровоизлиянии в ЗЧЯ. Наиболее распространенным методом лечения этого грозного осложнения является наружное вентрикулярное дренирование (НВД), однако оно не всегда эффективно и безопасно. При наличии гематомы мозжечка более 10—15 см3 и аксиальной дислокации НВД без удаления ге- ЛЕКЦИЯ а Рис. 5. Компьютерные томограммы больного с кровоизлиянием в полушарие мозжечка: а — до операции, гематома объемом 12 см3 левого полушария и червя мозжечка; б — пункция гематомы с использованием безрамной навигации. Светлая линия соответствует направлению пункции гематомы; в — через 12 ч после операции, гематома дренирована, проводится локальный фибринолиз; г — через 2 сут после операции, гематома полностью лизирована. б в матомы чревато усугублением мозжечково-тенториального вклинения. В таком случае только раннее удаление гематомы и декомпрессия ЗЧЯ могут способствовать улучшению исхода заболевания. При кровоизлиянии в IV желудочек небольшая по объему гематома может не приводить к сдавлению ствола, но сопровождаться гемотампонадой IV и/или даже III желудочка. В этом случае НВД эффективно, так как в течение нескольких суток позволяет контролировать гидроцефалию, а за это время ликвороток через IV желудочек, как правило, восстанавливается. Возможно проведение эндоскопической вентрикулостомии III желудочка. Введение фибринолитика в боковые желудочки при гемотампонаде г IV желудочка неэффективно, поскольку терапевтическая доза препарата разводится церебро-спинальной жидкостью боковых желудочков и его концентрация в IV желудочке становится недостаточной для растворения сгустка. При сочетании большой гематомы и вентрикулярного кровоизлияния показано как удаление гематомы, так и отведение церебро-спинальной жидкости из желудочков. В этом случае открытое удаление гематомы дополняют вентрикуло-цистерностомией по Торкильдсену, либо наружным дренированием желудочков. При проведении НВД большинству больных показан мониторинг внутричерепного давления, для чего используют специальные датчики, под11 НЕЙРОХИРУРГИЯ, № 4, 2006 ключаемые к дренажам по принципу сообщающихся сосудов. Они позволяют регулировать давление ликвора по уровню столба жидкости и производить его своевременный сброс при появлении гипертензии [5]. Наружное вентрикулярное дренирование, как основной метод хирургического лечения ГИ мозжечка, показано при вентрикуломегалии в сочетании с гемотампонадой IV желудочка, угнетением сознания (менее 13 баллов по ШКГ), деформацией околостволовых цистерн, при отсутствии в задней черепной ямке субстрата, приводящего к прямому сдавлению ствола. Противопоказанием к НВД является наличие гематомы мозжечка более 10—15 см3 (более 3 см в диаметре), приводящее к мозжечково-тенториальному вклинению, нестабильная гемодинамика. сочетание паренхиматозного кровоизлияния с вентрикулярным, развитие окклюзионной гидроцефалии, что определяет тяжелое состояние больных и необходимость экстренного хирургического вмешательства. В последнее время отмечена тенденция к использованию более активной хирургической тактики при мозжечковых и стволовых кровоизлияниях. Однако эти данные основаны на оценке результатов лечения малого числа больных и ретроспективном анализе исхода заболевания [7, 8]. Возможность хирургического лечения больных с геморрагическим инсультом моста дискутабельна. До настоящего времени крупные, рандомизированные, мультицентровые исследования, посвященные хирургии геморрагического инсульта задней черепной ямки, отсутствуют. Л И Т Е РА Т У РА Прогноз при кровоизлияниях в мозжечок и ствол мозга Общая летальность при геморрагическом инсульте мозжечка колеблется от 20 до 75%. Проведение консервативного лечения эффективно в случаях небольших кровоизлияний (до 10 см3), не сопровождающихся нарушением сознания, дислокацией ствола и гидроцефалией (ВКК2 менее 20%). Послеоперационная летальность составляет 24—45% [2, 9]. При своевременном вмешательстве, до развития развернутой картины дислокации ствола, возможно полное выздоровление более чем у половины больных. Риск неблагоприятного исхода значительно возрастает при угнетении сознания до сопора и более, объеме гематомы более 27 см3, локализации гематомы в черве, наличии вентрикулярного кровоизлияния, аксиальной дислокации, выраженной вентрикуломегалии (ВКК2 более 29%) [2]. При геморрагическом инсульте ствола общая летальность составляет 40—57%. По данным F. Eelco и соавт. (1997) [11], при геморрагическом инсульте моста летальность составила 55%, нуждались в постоянном уходе 24% больных и хорошее восстановление наблюдалось у 21% больных. К прогностически неблагоприятным факторам у больных с ГИ ствола относят: угнетение сознания до комы; распространение кровоизлияния на обе половины ствола, основание моста и покрышку, средний мозг, таламус; поперечный диаметр гематомы более 20 мм или более 25% поперечного сечения ствола; фиксированные глазные яблоки, отсутствие фотореакции зрачков, их расширение или анизокория, отсутствие корнеальных рефлексов, вентрикулярное кровоизлияние, острую окклюзионную гидроцефалию, тахикардию (более 110 уд/мин), раннюю центральную гипертермию, дыхательные расстройства, децеребрационную ригидность. Выводы Основными особенностями внутримозговых кровоизлияний в ЗЧЯ являются первичное или дислокационное поражение ствола мозга, частое 12 1. Гайдар Б.В., Свистов Д.В., Щеголев А.В. и др. // Практическая нейрохирургия. — 2002. — С. 276—282. 2. Дашьян В.Г., Мурашко А.А., Крылов В.В. // Выбор тактики лечения гипертензивных гематом мозжечка. Материалы IV съезда нейрохирургов России. — М., 2006. — С. 258. 3. Закарявичюс Ж., Никифоров Б.М. // Гипертонические кровоизлияния в мозжечок: диагностика и лечение // Нейрохирургия. — 2000. — № 4. — С. 22—27. 4. Лебедев В.В., Иоффе Ю.С., Островская И.М. Хирургия острых мозговых инсультов. — М.: Медицина, 1970. 5. Скворцова В.И., Крылов В.В. Геморрагический инсульт. — М.: «ГЭОТАР-Медиа», 2005. 6. Чеботарева Н.М. Хирургическое лечение внутримозговых кровоизлияний, обусловленных артериальной гипертонией. — М.: Медицина, 1984. 7. Alvarez-Betancourt L., Ramirez-Mendoza A., Lopez-Ortega S.J., Caldera-Duarte A. // Spontaneous cerebellar haematoma. Diagnosis, management and follow-up in 18 patients // Gac Med Mex. — 2005. — May-Jun; 141(3). — P. 191—194. 8. Broderick J.P., Adams H.P., Jr, Barsan W. et al. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage. A Statement for Healthcare Professionals From a Special Writing Group of the Stroke Council, American Heart Association // Stroke. — 1999. — 30. — P. 905—915. 9. Da Pian R., Bazzan A., Pasqualin A. Surgical versus medical treatment of spontaneous posterior fossa hematomas: a cooperative study on 205 cases. // Neurol Res. — 1984, Sep. — Vol. 6, № 3. — P. 145—151. 10. Dunne J.W., Chakera T., Kermode S. Cerebellar haemorrhagediagnosis and treatment: a study of 75 consecutive cases // Q. J. Med. — 1987, Sep. — 64 (245). — P. 739—754. 11. Eelco F.M. Wijdicks, St Louis Er. Clinical profiles predictive of outcome in pontine hemorrhage // Neurology. — 1997. — Vol. 49. — P. 1342—1346. 12. Hara T., Nagata K., Kawamoto S. et al. Functional outcome of primary pontine hemorrhage: conservative treatment or stereotaxic surgery // No Shinkei Geka. — 2001, Sep. — Vol. 29, № 9. — P. 823—829. 13. Myung-Hyun Kim, Jun-Hyeok Song, Sung-Hak Kim et al. A new trend in operative technique for intracerebral hemorrhage: a comparative study of stereotactic endoscopic removal and stereotactic catheter drainage // Neurosurg. Focus. — 1996. — Vol. 16. — P. 184—192. 14. Takanashi Y., Shinonaga M. Usefulness of aspiration surgery for elderly patients with hypertensive cerebellar hemorrhage // No To Shinkei. — 1998. Aug; 50(8): 751—754. 15. Takimoto H., Iwaisako K., Kubo S. et al. Transaqueductal aspiration of pontine hemorrhage with the aid of a neuroendoscope. Technical note // J. Neurosurg. — 2003. — Apr; 98(4): 917—919. 16. Teernstra O.P.M., Evers S.M.A.A., Lodder J. et al. Stereotactic Treatment of Intracerebral Hematoma by Means of a Plasminogen Activator. A Multicenter Randomized Controlled Trial (SICHPA) // Stroke. — 2003. 34 — P. 968—974.