Электронная структура атома углерода в органических
advertisement
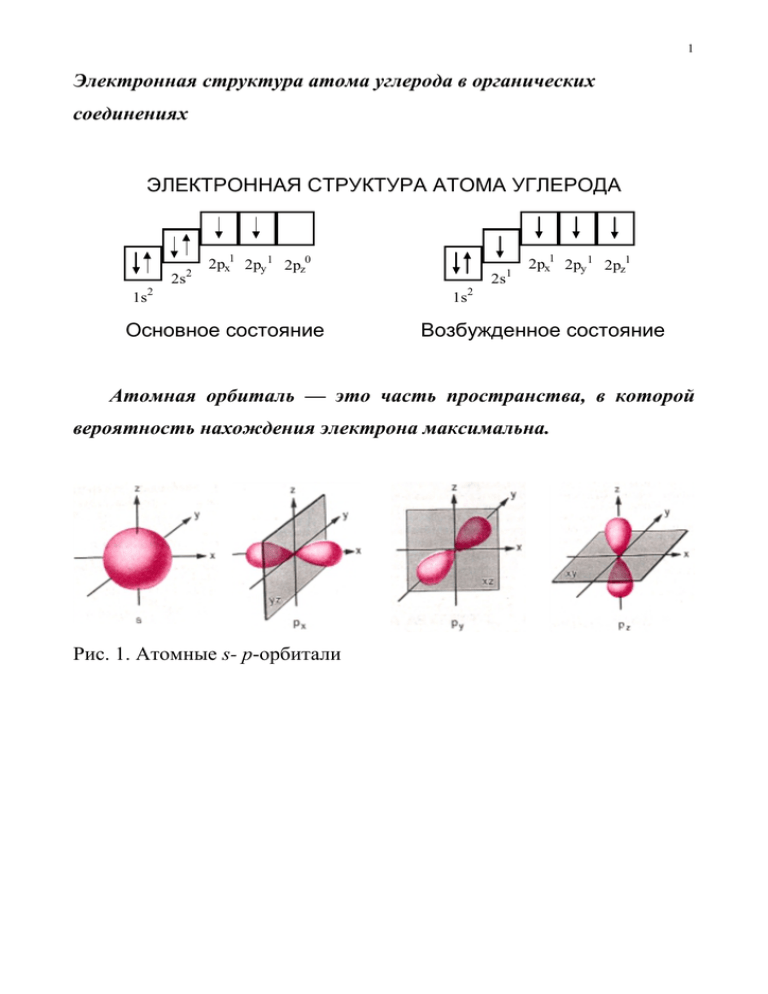
1 Электронная структура атома углерода в органических соединениях ЭЛЕКТРОННАЯ СТРУКТУРА АТОМА УГЛЕРОДА 1s2 2s 2 2px1 2py 1 2pz0 Основное состояние 1s2 2s 1 2px1 2py 1 2pz1 Возбужденное состояние Атомная орбиталь — это часть пространства, в которой вероятность нахождения электрона максимальна. Рис. 1. Атомные s- p-орбитали 3 2 sp -Гибридизация Рис. 2. Схема образования четырех sp3-гибридных орбиталей: а негибридизованные орбитали атома углерода; б - орбитали атома углерода в состоянии sp3-гибридизации sр2-Гибридизация Рис. 3. Схема образования трех sр2-гибридных орбиталей: a негибридизованные орбитали атома углерода; б - орбитали атома углерода в состоянии sp2-гибридизации. 3 sp-Гибридизация Рис. 4. Схема образования двух sp-гибридных орбиталей: а негибридизованные орбитали атома углерода; б - орбитали атома углерода в состоянии sp-гибридизации Таблица 1. Гибридные орбитали и характер углеродных атомов Орбитали Валентное состояние атома углерода 2s 2px 2py 2pz – Состояние углеродного атома Возбужденное, исходное состояние Возбужденное, в алканах 2sp 2sp 2sp 2sp 3 Возбужденное, в алкенах 3 2sp 2sp 2sp 2 Возбужденное, в алкинах 3 2 2 3 2p 2sp 2sp 2p 2p I Тип гибридизации и строение молекулы – (sp3) Тетраэдрическое II (sp2) Тригональное (плоскостное) III (sp) Дигональное (линейное) 4 Типы химической связи. Ковалентная связь Ионная (электровалентая) связь Na Na + Cl + Cl - Ковалентная (неэлектровалентная) связь A + B A:B Молекулярная орбиталь H:H H + H H H C H H 4H + C H H водород H или H C H метан H H H C :: C H или H : C ::: C : H или H H H или C H C H H C C H этилен ацетилен 5 σ (сигма)-связь Рис. 5. Различные виды перекрывания орбиталей при образовании (σ-связей: а - перекрывание двух sр3-гибридных орбиталей атомов углерода (С-С); б - перекрывание 1s-ор6италей атома водорода с sр3-гибридной орбиталью атома углерода (С-Н)) π(пи)-связь Рис. 6. Перекрывание двух негибридизованных 2р-орбиталей в молекуле этилена: а - объемное изображение двух перекрывающихся негибридизованных 2р-орбиталей; б - области максимальной электронной плотности лежат над и под плоскостью расположения σсвязей атомов углерода. 6 а) б) Рис. 7. Перекрывание четырех негибридизованных 2р-ор6италей в молекуле ацетилена: а - объемное изображение четырех перекрывающихся 2р-орбиталей; 6 - схематическое изображение этих орбиталей в двух взаимно перпендикулярных плоскостях π-связь менее прочна, чем σ-связь, а ее электроны легче смещаются в сторону одного из углеродных атомов. Полярность связи F > O > С1 > N > Вг > С > Н 7 Электроотрицательность Рис 8. Изменение электроотрицательности (по Полингу) элементов в зависимости от их положения в таблице Д.И. Менделеева С ( sp ) > C ( sp2 ) > C ( sp3 ) + δ H3C − δ Cl Электрический момент диполя (дипольный момент) µ=e⋅r где µ — электрический момент диполя (векторная величина), Кл⋅м (или дебаях (D); 1D = 3.34⋅10-30 Кл⋅м); е — элементарный заряд; r — расстояние между центрами тяжестей всех зарядов. 8 Поляризуемость — способностью изменять свою полярность, например, под влиянием внешнего воздействия Таблица 2. Некоторые параметры ковалентных углерод-углеродных связей Тип Ковалентн ая связь Угол между Энергия гибриди- Длина гибридными связи, зации связи, орбиталями кДж/мо атома нм (межвалентные ль* молекулы углы)- углерода 3 Форма 350 Тетраэдричес 0,154 109° 28' sp2 0,134 120° 610 Плоскостная sp 0,120 180° 830 Линейная C C sp C C C C кая * Приведены средние значения энергий. Направленность Координационная связь, или донорно-акцепторная донор акцептор A: + B неподеленная пара электронов A:B 9 H + H H N : + H+ H N:H H H ион аммония Семиполярная связь (от англ. semi — наполовину) CH3 H3C N CH3 + CH3 H3C N+ O- O CH3 или H3C N CH3 CH3 триметиламин O оксид триметиламина Водородная связь (H-связь) :O H :O H H H :O H :O H H H 12,5—20 кДж/моль Понятие о пространственном строении органических молекул Конформации ациклических соединений Проекция Ньюмена H C H H H C H H H HH H H H H Заслоненная конформация H H C C H H H H H H H H H Заторможеная конформация Рис. 9. Заслоненная и заторможенная конформации молекул этана и их ньюменовские проекционные формулы. 10 Торсионным, или диэдральным, углом называется угол между связями (в проекции Ньюмена), исходящими от атомов, связь между которыми является осью внутреннего вращения. Так, например, торсионный угол заслоненной конформации молекулы этана равен 0°, а заторможенной — 60°. Рис. 10. Зависимость энергии конформации молекулы этана от торсионного угла. CH3 H H H H CH3 CH3 H3C CH3 CH3 H H H H H H H H анти син гош (антиперипланарная) (синперипланарная) (синклинальная) 11 H H H H H H H H C C C C C C C C H H H H H H H H Рис. 11. Наиболее стабильная, так называемая зизгзагообразная конформация неразветвленных алканов Конформационный анализ Заторможенное вращение вокруг простой связи R R R R Пространственная изомерия, стереоизомерия Цис-транс-изомерия Оптическая изомерия Оптическая, или зеркальная, изомерия Био (1815) 12 Рис. 12. Схематическое изображение электромагнитных колебаний в луче обыкновенного и поляризованного света; 1 – в обыкновенном свете; 2 – в поляризованном свете; 3 – плоскость поляризации; 4 - призма Николя Антиподы или энантиомеры противоположный). Рацемическая смесь, или рацемат (от греч. enantio — 13 Рис. 13. Изменение плоскости поляризации при прохождении поляризованного света через оптически активные вещества: 1 – оптически активное вещество, 2 – первоначальная плоскость поляризации, повернутая на угол α после прохождения света через оптически активное вещество. Тетраэдрическая теория Я. Вант-Гоффа и А. Ле-Беля (1874) Асимметрический атом углерода Рис. 14. Модели асимметрического атома углерода: а тетраэдрическая; б - шаростержневая 14 H C HO Cl Br бромхлорметанол Рис. 15. Несовместимость оптических изомеров 15 Хиральный (от греч. хейрос — рука, рукоподобие) Оптическая изомерия — это явление, обусловленное хиральностью. Проекционные формулы (Э. Фишер) CH3 CH COOH Молочная кислота OH α-гидроксикоричная кислота COOH H * OH COOH HO * H CH3 CH3 D(–)-молочная кислота L(+)-молочная кислота М.А. Розанов, 1906 O H C H C OH CH2OH D(+)–глицериновый альдегид O H C HO C H CH2OH L(–)–глицериновый альдегид 16 Л. Пастер, 1848 Рис. 16. Энантиоморфные формы кристаллов CH2 CH2 COOH OH β гидроксипропионовая кислота N = 2n COOH H C OH HO C H COOH COOH HO C H COOH H C OH HO C H H C OH H COOH I II D(+)-винная L(-)-винная C OH HO C H COOH III мезовинная кислота виноградная кислота 1) + + 2) – – COOH IV кислота кислота COOH 3) + – 4) – + 17 Стереоизомеры, которые, не являются энантиомерами, называются диастереомерами. Относительная и абсолютная конфигурация. Определение абсолютной конфигурации по системе Кана — Ингольда — Прелога R (от латинского rectus — правый) S (от латинского sinister — левый) Рацемическую модификацию обозначают R, S Рис. 17. Определение абсолютной конфигурации хирального центра после установления старшинства заместителей 18 Правила старшинства: 1. Атом с большим атомным номером является старшим (т.е. имеет относительное старшинство) относительно атома с меньшим атомным номером. 2. Большее массовое число имеет преимущество перед меньшим. Этот пункт относится к изотопам. 3. Несвязанные электроны уступают старшинство атомам и имеют более низкий порядок, чем, например, атом водорода. Br направление взгляда C F Cl (R)-бромхлорфторметан H 19 CH3 CH3 C H C H Br направление взгляда C H CH3 H (R)-3-бром-2-метилпентан Br > (CH3)2CH > CH3CH2 > H цис-транс- Изомерия в кольце CH3 CH3 CH3 CH3 CH3 транс-1,3диметилциклобу транс-1,4-диметилциклогексан тан CH3 цис-1,4диметилциклогексан 20 цис-транс- Изомеры относительно двойной связи (E/Zизомерия) H3C C C H H3C CH3 H CH3 транс-бутен-2 F Br C C Cl C C H цис-бутен-2 Br H I C C I Cl F (Z)-1-бром-1-хлор-2-фтор-2- (E)-1-бром-1-хлор-2-фтор-2- иодэтен иодэтен Е (от нем. entgegen—напротив) Z (от нем. zusammen—вместе). N N анти-азобензол hv N N син-азобензол




