ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ ТЕСТ-СИСТЕМА «АБ-ГРАМОТР» МИКРООРГАНИЗМОВ
реклама
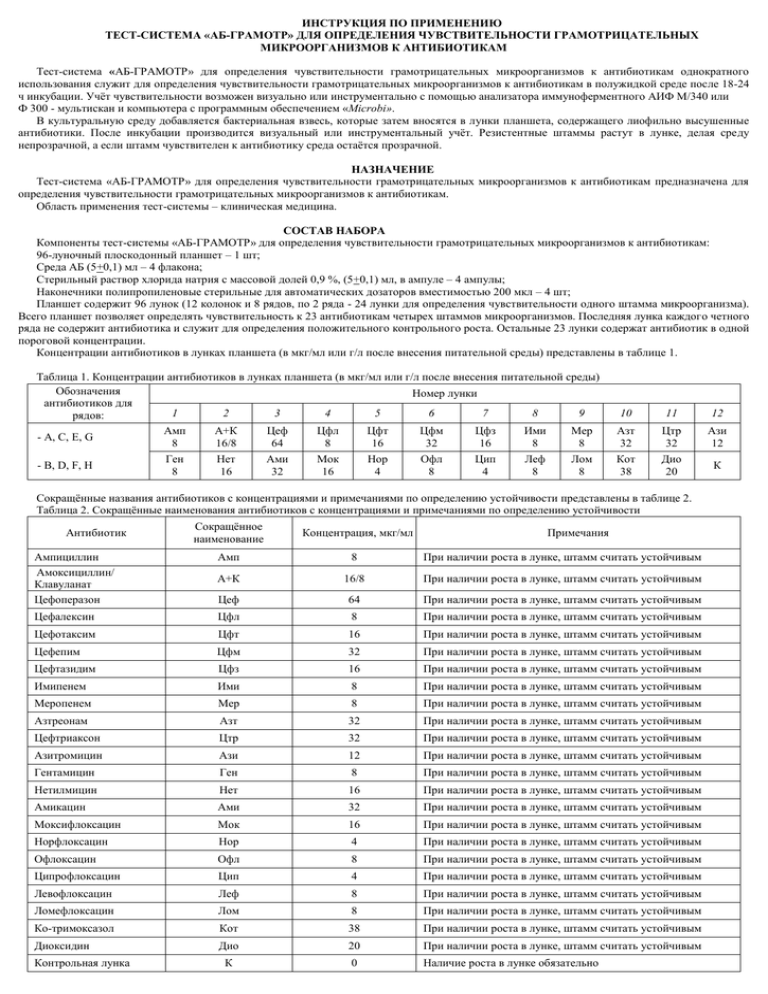
ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ ТЕСТ-СИСТЕМА «АБ-ГРАМОТР» ДЛЯ ОПРЕДЕЛЕНИЯ ЧУВСТВИТЕЛЬНОСТИ ГРАМОТРИЦАТЕЛЬНЫХ МИКРООРГАНИЗМОВ К АНТИБИОТИКАМ Тест-система «АБ-ГРАМОТР» для определения чувствительности грамотрицательных микроорганизмов к антибиотикам однократного использования служит для определения чувствительности грамотрицательных микроорганизмов к антибиотикам в полужидкой среде после 18-24 ч инкубации. Учѐт чувствительности возможен визуально или инструментально с помощью анализатора иммуноферментного АИФ М/340 или Ф 300 - мультискан и компьютера с программным обеспечением «Мicrobi». В культуральную среду добавляется бактериальная взвесь, которые затем вносятся в лунки планшета, содержащего лиофильно высушенные антибиотики. После инкубации производится визуальный или инструментальный учѐт. Резистентные штаммы растут в лунке, делая среду непрозрачной, а если штамм чувствителен к антибиотику среда остаѐтся прозрачной. НАЗНАЧЕНИЕ Тест-система «АБ-ГРАМОТР» для определения чувствительности грамотрицательных микроорганизмов к антибиотикам предназначена для определения чувствительности грамотрицательных микроорганизмов к антибиотикам. Область применения тест-системы – клиническая медицина. СОСТАВ НАБОРА Компоненты тест-системы «АБ-ГРАМОТР» для определения чувствительности грамотрицательных микроорганизмов к антибиотикам: 96-луночный плоскодонный планшет – 1 шт; Среда АБ (5+0,1) мл – 4 флакона; Стерильный раствор хлорида натрия с массовой долей 0,9 %, (5+0,1) мл, в ампуле – 4 ампулы; Наконечники полипропиленовые стерильные для автоматических дозаторов вместимостью 200 мкл – 4 шт; Планшет содержит 96 лунок (12 колонок и 8 рядов, по 2 ряда - 24 лунки для определения чувствительности одного штамма микроорганизма). Всего планшет позволяет определять чувствительность к 23 антибиотикам четырех штаммов микроорганизмов. Последняя лунка каждого четного ряда не содержит антибиотика и служит для определения положительного контрольного роста. Остальные 23 лунки содержат антибиотик в одной пороговой концентрации. Концентрации антибиотиков в лунках планшета (в мкг/мл или г/л после внесения питательной среды) представлены в таблице 1. Таблица 1. Концентрации антибиотиков в лунках планшета (в мкг/мл или г/л после внесения питательной среды) Обозначения Номер лунки антибиотиков для 1 2 3 4 5 6 7 8 9 рядов: 10 11 12 - A, С, E, G Амп 8 А+К 16/8 Цеф 64 Цфл 8 Цфт 16 Цфм 32 Цфз 16 Ими 8 Мер 8 Азт 32 Цтр 32 Ази 12 - B, D, F, H Ген 8 Нет 16 Ами 32 Мок 16 Нор 4 Офл 8 Цип 4 Леф 8 Лом 8 Кот 38 Дио 20 К Сокращѐнные названия антибиотиков с концентрациями и примечаниями по определению устойчивости представлены в таблице 2. Таблица 2. Сокращѐнные наименования антибиотиков с концентрациями и примечаниями по определению устойчивости Антибиотик Сокращѐнное наименование Концентрация, мкг/мл Примечания Ампициллин Амоксициллин/ Клавуланат Цефоперазон Амп 8 При наличии роста в лунке, штамм считать устойчивым А+К 16/8 При наличии роста в лунке, штамм считать устойчивым Цеф 64 При наличии роста в лунке, штамм считать устойчивым Цефалексин Цфл 8 При наличии роста в лунке, штамм считать устойчивым Цефотаксим Цфт 16 При наличии роста в лунке, штамм считать устойчивым Цефепим Цфм 32 При наличии роста в лунке, штамм считать устойчивым Цефтазидим Цфз 16 При наличии роста в лунке, штамм считать устойчивым Имипенем Ими 8 При наличии роста в лунке, штамм считать устойчивым Меропенем Мер 8 При наличии роста в лунке, штамм считать устойчивым Азтреонам Азт 32 При наличии роста в лунке, штамм считать устойчивым Цефтриаксон Цтр 32 При наличии роста в лунке, штамм считать устойчивым Азитромицин Ази 12 При наличии роста в лунке, штамм считать устойчивым Гентамицин Ген 8 При наличии роста в лунке, штамм считать устойчивым Нетилмицин Нет 16 При наличии роста в лунке, штамм считать устойчивым Амикацин Ами 32 При наличии роста в лунке, штамм считать устойчивым Моксифлоксацин Мок 16 При наличии роста в лунке, штамм считать устойчивым Норфлоксацин Нор 4 При наличии роста в лунке, штамм считать устойчивым Офлоксацин Офл 8 При наличии роста в лунке, штамм считать устойчивым Ципрофлоксацин Цип 4 При наличии роста в лунке, штамм считать устойчивым Левофлоксацин Леф 8 При наличии роста в лунке, штамм считать устойчивым Ломефлоксацин Лом 8 При наличии роста в лунке, штамм считать устойчивым Ко-тримоксазол Кот 38 При наличии роста в лунке, штамм считать устойчивым Диоксидин Дио 20 При наличии роста в лунке, штамм считать устойчивым К 0 Наличие роста в лунке обязательно Контрольная лунка ПОДГОТОВКА РЕАГЕНТОВ Флаконы со средой и планшеты должны быть выдержаны при температуре 18 – 30 °С 20 минут. Работа с планшетом должны проводиться в стерильном боксе после 30 минут обработки ультрафиолетовым облучением. Необходимое лабораторное оборудование: - холодильник; - термостат электрический с автоматической регулировкой и поддержанием температуры в пределах (37±1)°С; - спиртовая или газовая горелка; - дозаторы автоматические с погрешностью 1 % объѐмом от 5 до 50 мкл и от 20 до 200 мкл; - денситометр, спектрофотометр или стандартный образец оптической плотности 0,5 оптических единиц McFarland ; - Анализатор иммуноферментный АИФ М/340 или Ф 300 - мультискан; - программное обеспечение «Мicrobi»; - IBM совместимый компьютер. МЕТОДИКА ПОСТАНОВКИ В стерильный флакон внести 2 мл стерильного раствора хлорида натрия с массовой долей 0,9 %. Приготовить взвесь бактерий. Для этого бактериологической петлей внести одну или более колоний бактерий, выращенных в течение 18-24 ч при 37°С на мясо-пептонном агаре или селективной среде для грамотрицательных бактерий, например, цетилпиридиний-хлориде, в стерильном флаконе с 2 мл стерильного раствора хлорида натрия с массовой долей 0,9 %. Оптическая плотность взвеси в пробирке после внесения микроорганизма должна соответствовать 0,5 оптических единиц McFarland. Этого можно достичь путем: - измерения на денситометре или на спектрофотометре при длине волны 550 нм - 0,125 OD (составляет 1,5х 108 КОЕ/мл); - сравнения со стандартом оптической плотности 0,5 McFarland; Перенести в ампулу с питательной АБ средой 7 мкл приготовленной взвеси бактерий и тщательно перемешать. Внести в каждую лунку планшета по 135 мкл питательной среды АБ с микроорганизмами (106 КОЕ/мл). Планшет накрыть крышкой. Инкубировать 18-24 ч при 37 °С в термостате. УЧЕТ РЕЗУЛЬТАТОВ Резистентные штаммы растут в лунке, делая среду непрозрачной, а если штамм чувствителен к антибиотику среда остаѐтся прозрачной. При отсутствии роста в контрольной лунке – тест считается недействительным, и его необходимо повторить. Визуальный учет Интерпретация: прозрачная Ч (S) чувствительный штамм мутная + Р (R) устойчивый или резистентный штамм Инструментальный учет Измерение оптической плотности проводят на иммуноферментном анализаторе АИФ М/340 или Ф300 - мультискане с помощью программного обеспечения «Мicrobi» при длине волны 570 нм. Положительным считается результат при оптической плотности ≥0,4 OD, а отрицательным <0,23 OD. «Серая зона» располагается в интервале от <0,4 до ≥0,23 – тест считается спорным и требуется для учѐта визуальное подтверждение. При отсутствии роста в контрольной лунке – тест считается недействительным, и его необходимо повторить. УСЛОВИЯ ХРАНЕНИЯ И ПРИМЕНЕНИЯ НАБОРА Тест-система должна храниться при температуре плюс (4+2) °С на протяжении всего срока годности, указанного на упаковке. Флаконы со средой и планшеты перед постановкой опыта должны быть выдержаны при 20-30 0С 20 минут. Для исследования необходимо использовать только 18-24 ч культуру микроорганизма. Количество вносимого инокулята должно быть стандартным. Поэтому обязательно необходимо пользоваться денситометром или стандартом оптической плотности. Для отбора и добавления реагентов необходимо использовать полуавтоматические пипетки со сменными наконечниками, аттестованные на точность по значению средней дозы и воспроизводимость результатов пипетирования. Инкубация планшета должна производиться только в температурном режиме 36 -38 0С. При повышении или понижении температуры возможен некорректный результат. Большое количество пузырьков в культуральной среде может изменить результаты автоматического учѐта чувствительности. Собранный материал и бактериальные культуры следует считать потенциально опасными, что требует опытного и квалифицированного обращения. После использования все планшеты, флаконы и наконечники должны быть простерилизованы в паровом стерилизаторе при температуре (120+2) °С давлении (0,11+0,02) мПа (1,1+0,2) кгс/см2 в течении (45+3) мин, сожжены или дезинфицированы погружением в раствор хлорамина Б с массовой долей 0,5 % с экспозицией 30 мин. Для получения надежных результатов необходимо строгое соблюдение инструкции по применению набора. ФОРМА ВЫПУСКА Планшет позволяет определять чувствительность к 23 антибиотикам четырех штаммов микроорганизмов. Компоненты тест-системы в виде комплекта, включающего 1 планшет с антибиотиками, 1 пакетик с силикагелем, 4 флакона питательной среды АБ (5+0,1) мл, 4 флакона стерильного раствора хлорида натрия с массовой долей 0,9% (5+0,1) мл, 4 наконечника стерильных для автоматических дозаторов вместимостью 200 мкл, лист с комплектностью (таблица 2) и инструкция по применению помещаются в коробку из картона коробочного. В тару с тест-системами, направлением в каждый адрес по требованию заказчика вкладывается 1флакон стандартного образца оптической плотности 0,5 оптических единиц McFarland, объемом (4+0,1) мл. УСЛОВИЯ ХРАНЕНИЯ И ТРАНСПОРТИРОВАНИЯ Хранение тест-системы должно производиться при температуре плюс (4+2) °С на протяжении всего срока годности. Транспортирование тест-системы осуществлять при температуре плюс (4+2) °С в сухих, чистых, крытых транспортных средствах (ГОСТ 17768). Срок годности тест-системы - 12 месяцев с даты изготовления. При нарушении условий хранения, транспортирования и схемы постановки опыта рекламации не принимаются. В остальных случаях рекламации на качество тест-системы направляются по адресу учреждения изготовителя: 211309, Республика Беларусь, Витебская обл., Витебский р-н, д. Должа, ул. Советская, 26А. Тел/факс +375212-20-94-10. Открытое акционерное общество «БелВитунифарм».