влияние цинка и меди на распределение кадмия в организме
реклама

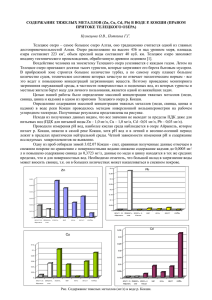
ВЛИЯНИЕ ЦИНКА И МЕДИ НА РАСПРЕДЕЛЕНИЕ КАДМИЯ В ОРГАНИЗМЕ Чужакин Н.Л., Колесников В.А. Красноярский государственный аграрный университет, Красноярск, Россия The Cadmium is a rare element, gained together with zinc. Opened in 1817 it back did not find broad using half a century ago. Presently cadmium is broadly used in production of different goods: in galvanic elements, as dying material in paint and plastic, in charging nickel-cadmium battery, in special alloy and solder. Кадмий – редкий элемент, добываемый вместе с цинком. Открытый в 1817 году, он ещё полвека назад не находил широкого применения. Сейчас кадмий широко используется в производстве различных товаров: в гальванических элементах, как красящее вещество в красках и пластмассах, в заряжаемых никель-кадмиевых батареях, в специальных сплавах и припоях. Влияние на здоровье: считают, что вдыхание кадмия приводит к раку легких. Этот металл классифицируют как возможный канцероген. Постоянный контакт с кадмием, пусть в небольших количествах, может привести к болезням легких, например, хронический бронхит и эмфизема. Постоянное заражение кадмием также связывают с рядом других болезней, включая сердечные болезни, анемию, хрупкость скелета, подавление деятельности иммунной системы, а также болезни печени и почек. В большинстве случаев накопление кадмия в мягких тканях органов не влияет на их деятельность, пока содержание металла не достигнет критического уровня. Имеющиеся в литературе данные указывают на то, что на токсичность, всасывание и распределение кадмия в организме, по-видимому, может оказывать влияние содержание цинка, меди и других эссенциальных микроэлементов в пищевом рационе, однако эти данные крайне противоречивы[8, 9]. Согласно [7], медь и особенно цинк ингибируют процессы всасывания и депонирования кадмия. В настоящее время известно 15 эссенциальных микроэлементов, которые не синтезируются в организме животного, но крайне необходимы для нормальной жизнедеятельности. Одними из ведущих являются цинк (Zn), железо (Fe) и медь (Cu). Так, цинк, являясь составной частью более 300 энзимов, принимает активное участие во всех видах обмена, необходим для нормальной работы иммунной системы. Медь - это микроэлемент, необходимый для формирования клеток крови, соединительной и костной ткани [1, 4, 5]. Изучение распределения и накопления кадмия в различных органах и тканях в зависимости от дозы цинка в рационе показало, что наиболее характерные изменения обнаруживаются в печени, почках и поджелудочное железе, в других органах и тканях они менее выражены [3]. Обращает на себя внимание антагонистический характер динамики депонирования меди и кадмия, соответствуя исследованиям некоторых авторов, свидетельствующим об обратно пропорциональной корреляции между медью и рядом макроэлементов [2]. При проведении мониторинговых исследований г. Красноярска по тяжелым металлам и их влиянию на организм животного не выявлено четкой картины антагонизма во взаимовлиянии элементов цинк-кадмий и медькадмий. Антагонистический характер взаимодействия меди и кадмия, с высокой степенью вероятности, обнаруживался в крови и некоторых кроветворных органах. Так, непосредственно в крови, коэффициент корреляции составил -0,50, в лимфатическом узле -0,73, в селезенке -0,51. Между тем, в одном из самых главных кроветворных органов, в костном мозге, корреляционная зависимость составила малозначимые 0,11. В остальных органах и системах соотношение меди и кадмия не превышало 0,2, что говорит о незначительной корреляционной связи медьсодержащих соединений организма к соединениям кадмия (Табл. №1). Как уже отмечалось выше, данные о влиянии цинка на распределение кадмия часто противоречивы[8,9]. Орган Почки Печень Сердце Легкие Диафрагма Прямая кишка Слепая кишка Мышцы Трубчатая кость Ребро r 0,10 0,13 0,19 -0,14 0,17 0,09 0,07 -0,25 -0,09 0,04 Орган Селезенка Поджелудочная железа Ободочная кишка Желудок Головной мозг Язык Костный мозг Лимфатический узел Тонкий кишечник Кровь Таблица №1 r -0,51 -0,10 -0,09 0,15 0,09 -0,07 0,11 -0,73 -0,005 -0,50 По нашим данным соотношение кадмия и цинка проявляет в печени антагонистический характер (Табл. №2). Между тем в ряде исследований отмечалось, что при отсутствии цинка в рационе, в печени не синтезируется цинк- тионеин, являющийся одним из основных рецепторов кадмия, и как следствие снижается накопление кадмия в этом органе [3]. Это подтверждается данными [6], указывающими, что под воздействием цинка увеличивается количество кадмия в цитозоле печени, большая часть которого связана с тионеином, но только при экспериментальном введении повышенных доз кадмия и цинка, часто в сублетальных и летальных дозах. Наша модель эксперимента заключалась в изучении животных, изъятых из естественных условий среды обитания. При фоновом содержании кадмия в организме и естественном уровне содержания цинка в рационе на коэффициент корреляции влияют и другие эссенциальные элементы, давая отрицательные значения ответа. При изучении биотрансформации цинка и кадмия характерная корреляционная зависимость просматривается в желудочно-кишечном тракте. Так в ободочной, слепой и прямой кишке характер этих отношений отрицательный, а в желудке и тонком кишечнике положительный (Табл. №2). В клетках крови, лимфатических узлах и кроветворных органах цинк отчетливо ингибирует процессы накопления кадмия. В костной ткани процессы антагонизма цинка и кадмия не просматривается, что можно объяснить возрастом изучаемых животных, так как активных биохимических процессов синтеза к этому времени в костях скелета животного уже не происходит. Орган Почки Печень Сердце Легкие Диафрагма Прямая кишка Слепая кишка Мышцы Трубчатая кость Ребро r 0,29 -0,39 0,005 -0,001 -0,03 -0,33 -0,03 -0,16 -0,03 0,02 Орган Селезенка Поджелудочная железа Ободочная кишка Желудок Головной мозг Язык Костный мозг Лимфатический узел Тонкий кишечник Кровь Таблица №2 r -0,08 0,17 -0,02 0,25 0,08 0,05 -0,28 -0,31 0,17 -0,29 На последнем этапе анализа накопленных данных были проведены параллели взаимодействия между суммарными значениями концентраций тяжелых металлов всех органов и систем. Полученные результаты показали отрицательные значения корреляции между кадмием и медью -0,07, а также между кадмием и цинком -0,14. Обобщая полученные данные, можно высказать предположение, что различные экспериментальные модели изучения взаимодействия тяжелых металлов не всегда корректные, что подтверждается противоречивыми данными различных авторов. Представленная модель отражает состояние микроэлементозного статуса животного находящегося в естественных условиях. Литература: 1.Авцын А.П., Жаворонков А.А., Риш М.А., Строчкова Л.С. Микроэлементозы человека. - М.: Медицина, 1991. - 496 с. 2. Белан М.Г. О метаболизме некоторых микроэлементов в длинных трубчатых костях при общих заболеваниях скелета // Ортопед., травматол. и протезир., 1964, № 3. С.141—148. 3. Богомазов М.Я., Гарибян Г.М. Влияние содержания цинка в рационе экспериментальных животных на всасывание, распределение и накопление хлорида кадмия в организме при различных путях его введения. // Вопросы питания. -1992. -№4 -с.51-53. 4.Лаврова А.Е. Клиническое значение изменений содержания цинка и их коррекция у детей с хроническим гастродуоденитом при пищевой аллергии: Дисс.канд.мед.наук.: 14.00.09. - Н.Новгород, 1998. - 167 с. 5.Цинк в педиатрической практике: Учебное пособие / под ред. Щеплягиной Л.А. - Москва, 2001. - 83 с. 6. Goering P.L., Klaassen D.G. // Toxicol appl. Pharmacol.-1984.- Vol.74, #3P.299-307. 7. Hill C., Matrone G., Payne W., Barber C. In vivo interactions of Cd with Cu, Zn and Iron // J. Nutr., 1963., Vol. 80, № 3. P. 227—235. 8. Jacobs R., Jones A., Fry B., Fox M.//J.Nutr.-1978.-Vol.108.#6.-P.901-910.; 9. Nakamura K., Suzuki E., Sugiura I., Torat T. //Industr. Hlth.-1979.-Vol.17, #1.P. 1-9.