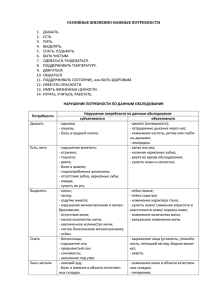
Мочевая система
реклама
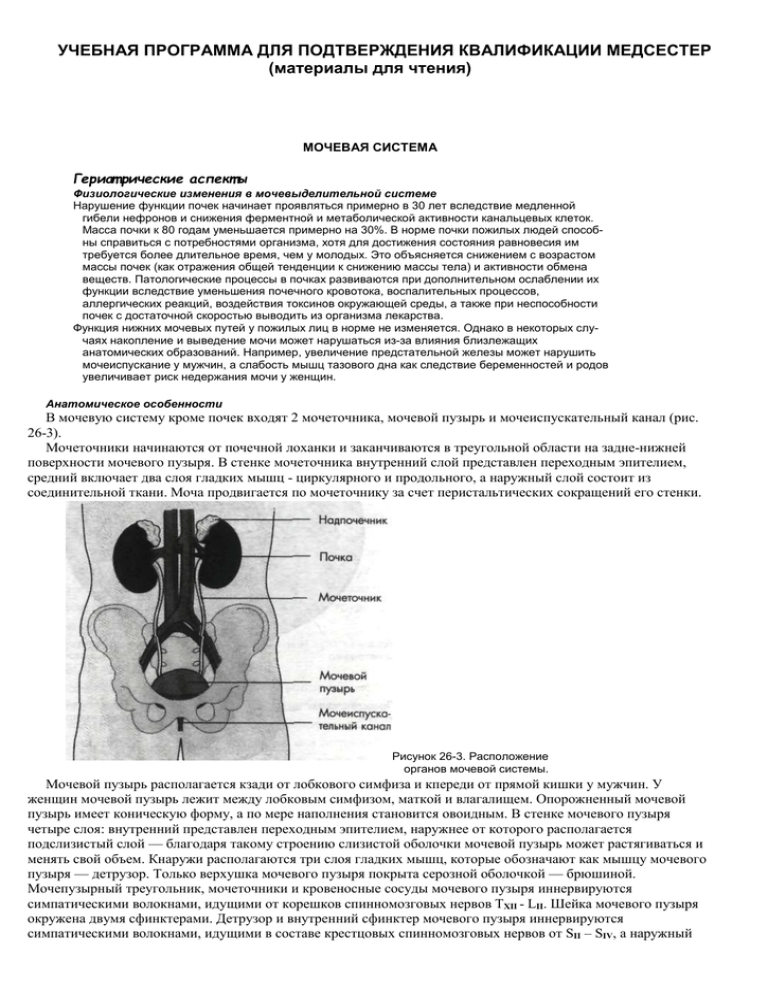
УЧЕБНАЯ ПРОГРАММА ДЛЯ ПОДТВЕРЖДЕНИЯ КВАЛИФИКАЦИИ МЕДСЕСТЕР (материалы для чтения) МОЧЕВАЯ СИСТЕМА Гериат рические аспект ы Физиологические изменения в мочевыделительной системе Нарушение функции почек начинает проявляться примерно в 30 лет вследствие медленной гибели нефронов и снижения ферментной и метаболической активности канальцевых клеток. Масса почки к 80 годам уменьшается примерно на 30%. В норме почки пожилых людей способны справиться с потребностями организма, хотя для достижения состояния равновесия им требуется более длительное время, чем у молодых. Это объясняется снижением с возрастом массы почек (как отражения общей тенденции к снижению массы тела) и активности обмена веществ. Патологические процессы в почках развиваются при дополнительном ослаблении их функции вследствие уменьшения почечного кровотока, воспалительных процессов, аллергических реакций, воздействия токсинов окружающей среды, а также при неспособности почек с достаточной скоростью выводить из организма лекарства. Функция нижних мочевых путей у пожилых лиц в норме не изменяется. Однако в некоторых случаях накопление и выведение мочи может нарушаться из-за влияния близлежащих анатомических образований. Например, увеличение предстательной железы может нарушить мочеиспускание у мужчин, а слабость мышц тазового дна как следствие беременностей и родов увеличивает риск недержания мочи у женщин. Анатомическое особенности В мочевую систему кроме почек входят 2 мочеточника, мочевой пузырь и мочеиспускательный канал (рис. 26-3). Мочеточники начинаются от почечной лоханки и заканчиваются в треугольной области на задне-нижней поверхности мочевого пузыря. В стенке мочеточника внутренний слой представлен переходным эпителием, средний включает два слоя гладких мышц - циркулярного и продольного, а наружный слой состоит из соединительной ткани. Моча продвигается по мочеточнику за счет перистальтических сокращений его стенки. Рисунок 26-3. Расположение органов мочевой системы. Мочевой пузырь располагается кзади от лобкового симфиза и кпереди от прямой кишки у мужчин. У женщин мочевой пузырь лежит между лобковым симфизом, маткой и влагалищем. Опорожненный мочевой пузырь имеет коническую форму, а по мере наполнения становится овоидным. В стенке мочевого пузыря четыре слоя: внутренний представлен переходным эпителием, наружнее от которого располагается подслизистый слой — благодаря такому строению слизистой оболочки мочевой пузырь может растягиваться и менять свой объем. Кнаружи располагаются три слоя гладких мышц, которые обозначают как мышцу мочевого пузыря — детрузор. Только верхушка мочевого пузыря покрыта серозной оболочкой — брюшиной. Мочепузырный треугольник, мочеточники и кровеносные сосуды мочевого пузыря иннервируются симпатическими волокнами, идущими от корешков спинномозговых нервов ТХII - LII. Шейка мочевого пузыря окружена двумя сфинктерами. Детрузор и внутренний сфинктер мочевого пузыря иннервируются симпатическими волокнами, идущими в составе крестцовых спинномозговых нервов от SII – SIV, а наружный сфинктер, сформированный поперечно-полосатыми мышечными волокнами, иннервируется мотонейронами полового нерва. Мочеиспускание — рефлекторный акт, направленный на опорожнение мочевого пузыря. Этот процесс запускается в тот момент, когда рецепторы растяжения стенки мочевого пузыря раздражаются в результате его наполнения. Центр рефлекса мочеиспускания располагается в крестцовом отделе спинного мозга (Sn—Srv). Парасимпатические импульсы способствуют сокращению детрузора и расслаблению внутреннего сфинктера мочевого пузыря. У младенцев отсутствует произвольный контроль мочеиспускания. У взрослых непроизвольное мочеиспускание наблюдается при снижении тонуса наружного сфинктера мочевого пузыря, регулируемого волокнами полового нерва. Мочеиспускательный канал представляет собой трубку, по которой моча из мочевого пузыря выводится наружу. У женщин мочеиспускательный канал короткий (2,5—4 см) и по нему поступает только моча. У мужчин мочеиспускательный канал значительно длиннее (18-20 см), проходит через предстательную железу (рис. 26-4) и половой член, поэтому по нему во время эякуляции поступает сперма. ■ СЕСТРИНСКОЕ ОБСЛЕДОВАНИЕ АНАМНЕЗ Заболевания почек и мочевых путей проявляются характерными симптомами. Возможно нарушение функции почек в результате травмы, недостаточного кровообращения в связи с гипотензией, воздействия нефротоксичных агентов, а также в результате образования камней в почках и развития инфекции мочевых путей. Приведенные в рамке симптомы могут наблюдаться у пациентов с заболеваниями мочевых путей. Кроме выявления этих симптомов необходимо уточнить, не было ли у пациента камней в почках, почечной недостаточности, частых или хронических инфекций мочевых путей, нефротического синдрома, гломерулонефрита, нарушений свертывания крови (гемофилия), гемолитико-уремического синдрома, серповидно-клеточной анемии, ВИЧ-инфекции, сахарного диабета, застойной сердечной недостаточности, артериальной гипертензии, злокачественных опухолей, а также сведения о предшествующих исследованиях (экскреторная урография, УЗИ, цистоуретрография, цистоскопия и др.) почек или мочевого пузыря. Симптомы заболеваний почек Аменорея Анурия (прекращение выделения мочи) Одышка Дизурия (болезненное или затрудненное мочеиспускание) Отеки Быстрая утомляемость Лихорадка Боль в боку Учащенное мочеиспускание Гематурия Недержание мочи Тошнота и рвота Никтурия (обильное выделение мочи ночью) Олигурия (уменьшение количества мочи при нормальном приеме жидкости) Полиурия (увеличение количества мочи) Кожный зуд Сыпь Боль в надлобковой области Императивные позывы к мочеиспусканию (ощущение сильного позыва к мочеиспусканию, при котором, однако, выделяется небольшое количество мочи) Увеличение массы тела Определение характера дополнительных исследований зависит от знаний медсестры в области патофизиологии, терапии, а также от симптомов сопутствующих заболеваний. Например, пациент может жаловаться на примесь крови в моче (гематурия). Макрогематурия может наблюдаться при травме, инфекциях мочевых путей, опухоли почки или мочевого пузыря, нефролитиазе, а также при проведении химиотерапии по поводу рака, поэтому медсестра опрашивает пациента с учетом симптомов других заболеваний. Если пациент отмечал сильную боль в боку, напоминающую колику и распространяющуюся в нижние отделы живота, половые губы или мошонку, то можно заподозрить камень в мочеточнике. Если женщина жалуется на учащенное мочеиспускание с императивными позывами, жжением после недавнего полового акта, можно предположить инфекцию мочевых путей. Учащенное мочеиспускание с императивными позывами у пациента, принимающего циклофосфамид по поводу лейкоза, свидетельствует о геморрагическом цистите, вызванном этим препаратом. Если мужчина старше 50 лет отмечает макрогематурию, то можно думать о раке почки или мочевого пузыря. Собирая анамнез, следует также выяснить привычки пациента, какие заболевания он перенес, был ли госпитализирован, выполнялись ли ему операции, были ли у него травмы, делалась ли ему вакцинация, принимал ли он недавно какие-либо препараты и наблюдались ли аллергические реакции. Гематурия может быть обусловлена приемом варфарина. Нестероидные противовоспалительные препараты у некоторых пациентов могут вызвать нарушение функции почек. Оценивая семейный анамнез пациента при обследовании мочевой системы, выясняют, не было ли у коголибо из членов семьи нефролитиаза, поликистоза почек, агенезии почки, опухоли почки или мочевого пузыря, нарушения свертывания крови (гемофилия), гемолитико-уремического синдрома, серповидно-клеточной анемии, гломерулонефрита, почечного канальцевого некроза. В случае положительного ответа указывают заболевание в семейном анамнезе и прямого родственника пациента (например, у деда -нефролитиаз; у сестры поликистоз почек). Собирают сведения о родителях, дедушках и бабушках, тетях и дядях, сестрах и братьях, супруге, детях. ОБЪЕКТИВНОЕ ОБСЛЕДОВАНИЕ Физикальное исследование мочевой системы обычно предполагает исследование живота. Важно знать также количество принятой пациентом (введенной пациенту) жидкости и выделенной мочи. Следует исследовать половую систему. У всех пациентов оценивают общее состояние. Оценка общего состояния При оценке общего состояния учитывают рост, массу тела, показатели гемодинамики и дыхания, соответствие физиологического возраста паспортному, качество и режим питания, общий вид, самочувствие.c аспекты Гериат рические аспект ы Исследование мочевыделительной системы ОБЩИЙ ПОДХОД : Необходимо больше времени, чем при обследовании молодых пациентов Инструкции пожилому пациенту нужно произносить четко, так как у него может быть нарушен слух Из-за возможных нарушений зрения, интеллекта или подвижности пожилым пациентам труднее выполнять инструкции врача Инструкции должны быть понятными и краткими СБОР АНАМНЕЗА Может потребоваться повторение вопросов Некоторые ответы могут оказаться неадекватными, так как пожилые пациенты могут неправильно понять вопрос из-за нарушений слуха или интеллекта Вновь появившееся недержание мочи может быть признаком инфекции мочевых путей ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ Методика физикального исследования не меняется, но его следует провести таким образом, чтобы получить необходимую диагностическую информацию, не вызывая дискомфорта или смущения у пациента Исследовать нужно в спокойной обстановке, чтобы не отвлекать пациента и не прерывать исследования Скорость клубочковой фильтрации с возрастом уменьшается Клиренс креатинина с возрастом уменьшается Кожные покровы Осматривают и пальпируют кожу, обращают внимание на ее температуру, цвет, влажность, тургор, дефекты, васкуляризацию, возможные высыпания, их цвет, характер и расположение, смотрят, нет ли периферических отеков и отеков век. Осматривают область сердца, обращают внимание на выпячивания грудной стенки, ее движения придыхании, пульсацию. Пальпируют область сердца, верхушечный толчок, отмечают, нет ли шумов. При аускультации стетоскопом и фонендоскопом отмечают частоту сердечных сокращений, ритм, I (S1) и II (S2) тоны сердца, дополнительные тоны (S3, S4), шумы. Сердечно-сосудистая система Дыхательная система Осматривают грудную клетку, обращают внимание на ее симметричность, конфигурацию, характер дыхания - глубину, ритмичность и дополнительные усилия при дыхании. При перкуссии грудной клетки оценивают качество перкуторного звука и сравнивают его в симметричных отделах грудной клетки. При аускультации грудной клетки отмечают основные и побочные дыхательные шумы (сухие и влажные хрипы, шум трения плевры). Живот Осматривают живот, отмечая рубцы, стрии, расширенные вены, состояние пупка, контуры живота, его симметричность. Обращают внимание на перистальтику, видимую пульсацию. При аускультации живота выявляют кишечные шумы и жужжащий шум над венами. Далее проводят перкуссию всех отделов живота, затем переходят к перкуссии отдельных органов. С помощью перкуссии определяют границы печени, селезенки и иногда мочевого пузыря. При перкуссии желудка уточняют место расположения газового пузыря. Наполненный мочевой пузырь при перкуссии определяется в виде притупления звука над лобком. Болезненность реберно-позвоночного угла выявляют с помощью легкого поколачивания кулаком — это делают при исследовании задней поверхности грудной клетки, а результаты отмечают в разделе карты пациента, посвященном исследованию живота. Возможно прямое и непрямое поколачивание. При отсутствии поражения почек, например, пиелонефрита или камня почки, поколачивание не вызывает болевых ощущений. Если предполагается поражение почки и ранее отмечена болезненность реберно-позвоночного угла, то поколачивание не производят. Для выявления болезненности реберно-позвоночного угла пациента следует усадить. Распластанную ладонь недоминирующей руки помещают на область реберно-позвоночного угла (рис. 26-5). Локтевой поверхностью кулака доминирующей руки наносят легкие удары по тыльной поверхности недоминирующей руки. Болезненность реберно-позвоночного угла оценивают с обеих сторон (рис. 26—6). Сначала пальпируют брюшную стенку, затем отдельные органы и объемные образования, выявленные в брюшной полости. Начинают с поверхностной пальпации. Если пациент не может расслабиться, ему рекомендуют согнуть ноги в коленях. Таким образом достигается расслабление мышц живота. После поверхностной пальпации переходят к глубокой, отмечая участки болезненности и напряжения, а также объемные образования. Пальпируют нижний край печени, селезенки, почек. Правую почку пальпируют, уложив пациента на спину. Расположившись справа от него, помещают левую руку ладонью вверх под его правый бок. Левой рукой стараются сместить правую почку кпереди. Положив правую руку на живот пациента ниже края реберной дуги, пытаются «захватить» правую почку в то время, как пациент делает глубокий вдох, как показано на рис. 26—7. В норме правую почку удается пропальпировать у худощавых пациентов при расслабленных мышцах живота. Чтобы пальпировать левую почку, становятся справа от пациента, помешают левую руку под левый реберно-позвоночный угол. Правую руку укладывают на край левой реберной дуги пациента. Просят его глубоко вдохнуть. Проводят глубокую пальпацию во время глубокого вдоха пациента. В норме левая почка не пальпируется, так как расположена в забрюшинном пространстве достаточно высоко (рис. 26—8). Мужские половые органы Уретрит (воспаление мочеиспускательного канала) у мужчин начинается с расстройств мочеиспускания. Заболевание может быть вызвано возбудителем, передающимся половым путем (но не только), например, хламидиями. Следует осмотреть мочеиспускательный канал и взять материал для бактериологического исследования. При простатите и доброкачественной гиперплазии предстательной железы могут также возникать нарушения мочеиспускания, например, его затруднение, уменьшение струи мочи, трудности в начале мочеиспускания. Если выявлены такие симптомы, необходимо исследовать предстательную железу. Женские половые органы При нарушении мочеиспускания у женщин необходимо исследовать наружные половые органы, чтобы исключить их воспаление. Если при нарушении мочеиспускания дизурия усиливается при прохождении мочи через зону промежности, отмечаются обильные или патологические выделения из влагалища, можно предположить вульвовагинит. При симптомах вульвовагинита необходимо влагалищное исследование, взятие цервикального секрета на бактериологическое исследование для выявления хламидий, гонококков, дрожжеподобных грибов, трихомонад или бактерий. ЛАБОРАТОРНЫЕ И ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ АНАЛИЗ МОЧИ Анализ мочи (общий анализ мочи) — важное диагностическое исследование, которое дает информацию о состоянии почек и мочевых путей, а также о состоянии всего организма (табл. 26—1). Для этого анализа необходимо иметь порцию мочи объемом не менее 15 мл. Предпочтительнее исследовать утреннюю мочу. Женщинам перед мочеиспусканием следует тщательно обработать антисептическим раствором промежность и наружные половые органы, чтобы в мочу не попали выделения из влагалища и фекалии. Полученную порцию мочи отсылают в лабораторию, а если невозможно исследовать мочу в течение 1 ч, то ее замораживают. Если оставить мочу при комнатной температуре на 5 ч, она становится непригодной для бактериологического исследования, а форменные элементы в ней распадаются. Используя тест-полоску Multistix, медсестра может сразу получить информацию о кетоновых телах, рН мочи, протеинурии, глюкозурии и эритроцитурии. Пригодна для исследования только та тест-полоска, которая находится в плотно закрытой таре. До использования тест-полоски медсестра должна проверить срок годности тары и инструкцию производителя. Чтобы получить достоверные результаты исследования, контейнеры, в которых хранятся тестполоски, таблетки или ленты-реактивы, необходимо плотно закрывать и хранить в сухом месте. Для получения точных результатов исследования необходимо соблюдать время экспозиции реактива или тест-полоски, а также тщательно сравнивать полученный цвет со шкалой, обозначенной на таре. БАКТЕРИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ МОЧИ Посев мочи — стандартное исследование в диагностике инфекции мочевых путей. Обычно определяют также чувствительность выявленных микроорганизмов к антибиотикам. Новые методы исследования позволяют определить наличие бактерий в моче быстрее и надежнее. Например, с помощью фотометрии по изменению светового пучка, проходящего через питательную среду с бактериями, можно выявить выраженный рост бактерий. Биолюминесценция позволяет выявить микроорганизмы по содержанию бактериального аденозинтрифосфата в среде. В настоящее время проводятся испытания новых автоматизированных бактериологических методов, например, с использованием веществ, меченных углеродом-14, с последующей микрокалориметрией. Число бактериальных колоний менее 10 000 в 1 мл является недостаточным для установления диагноза, а при числе колоний от 10 000 до 100 000 в 1 мл невозможно сделать вывод о виде инфекции. При числе колоний 100 000 в 1 мл посев считается положительным, а если эти изменения сопровождаются клиническими признаками — лихорадкой и болью в боку, то можно говорить о пиелонефрите. Положительные результаты посева мочи в сочетании с болезненным учащенным мочеиспусканием, императивными позывами свидетельствуют о цистите. Положительный результат посева мочи без клинических признаков инфекции мочевых путей может указывать на загрязнение пробы мочи при сборе или на хронический пиелонефрит в неактивной фазе. Наличие двух или более видов микроорганизмов, принадлежащих к вагинальной или кожной микрофлоре — признак загрязнения пробы мочи. Подготовка пациента Пациентов информируют о том, что исследование позволяет выявить инфекцию мочевых путей и правильный сбор мочи необходим для получения достоверных результатов. Медсестра выдает стерильный сосуд для мочи, предупреждает пациента, чтобы он не прикасался к внутренней поверхности этого сосуда и старался не касаться сосудом ног, гениталий и одежды. Пациентам объясняют необходимость тщательно помыть половые органы перед сбором мочи. Женщинам следует развести половые губы и как минимум тремя тампонами, смоченными антисептическим раствором, обработать наружные половые органы в направлении спереди назад, а во время мочеиспускания немного наклониться вперед, чтобы струя мочи попадала прямо в сосуд и не касалась кожи. Мужчинам рекомендуют обнажить головку полового члена и обработать ее по меньшей мере тремя тампонами с антисептическим раствором. Мужчина начинает мочиться, таким образом смывая микроорганизмы со слизистой оболочки задней уретры, затем прекращает мочеиспускание и далее продолжает мочиться в сосуд для сбора мочи. Пробы мочи для посева можно получить с помощью катетеризации мочевого пузыря. Мочу, находящуюся в мочеприемнике, не следует использовать для бактериологического исследования. Медсестра записывает антибактериальные препараты, принимаемые пациентом, на специальном лабораторном бланке и немедленно относит пробы мочи в лабораторию. Если транспортировка мочи откладывается, то сосуд с мочой необходимо положить в холодильник (кроме тех случаев, когда мочу исследуют на цитомегаловирус, так как при замораживании он погибает). СЛОЖНЫЕ АНАЛИЗЫ МОЧИ Для сложных анализов (например, определение уровня электролитов, 17-кетостероидов, креатинина) мочу собирают в течение 2-24 ч (табл. 26-2). Пациент должен помочиться в унитаз и отметить время (это время соответствует началу исследования). В дальнейшем мочу при мочеиспускании собирают в специальный сосуд. По окончании заранее определенного времени медсестра просит пациента помочиться и добавляет полученный объем к общему количеству мочи в сосуде. КЛИРЕНС КРЕАТИНИНА Клиренс креатинина — общепринятый и точный показатель скорости клубочковой фильтрации. Креатинин, небелковый продукт обмена веществ в поперечно-полосатых мышцах, в норме выводится из организма почками. При нарушениях клубочковой фильтрации уровень креатинина в сыворотке повышается, а клиренс креатинина падает. Повышение клиренса креатинина не имеет клинического значения. Из-за меньшего объема мышечной массы (источника циркулирующего в крови креатинина) у женщин клиренс креатинина ниже (74-130 мл/мин), чем у мужчин (82—162 мл/мин). Важно точно соблюдать время взятия мочи и собрать мочу полностью. Обычно собирают суточную мочу, хотя можно исследовать и мочу, выделенную за 2,6 или 12 ч. Креати-нин сыворотки можно определить за любой интервал времени, так как уровень этого вещества в крови постоянен в течение 24 ч. Подготовка пациента Пациентам объясняют, что определение клиренса креатинина позволяет оценить функцию почки и что, хотя оно не требует придерживаться особой диеты, но тем не менее перед исследованием и во время него желательно воздержаться от мясной пиши. Следует выяснить, не принимает ли пациент такие препараты, как фуросемид, L-дофа, гентамицин или тиазидные диуретики — они могут повлиять на результат исследования. Медсестра также предупреждает пациента, чтобы он избегал интенсивной физической нагрузки во время исследования. Пациенту подробно объясняют, как собирать мочу. ПРИМЕНЕНИЕ РАДИОФАРМПРЕПАРАТОВ ДЛЯ ОЦЕНКИ ПОЧЕЧНОГО КЛИРЕНСА Скорость клубочковой фильтрации можно определить, измеряя уровень йода-125 в моче и плазме крови после подкожной инъекции йоталамовой кислоты (йоталамат), меченной йодом-125. Изотоп попадает в почечные канальцы в результате канальцевой секреции и клубочковой фильтрации. Пациенту объясняют, что это исследование позволяет определить функцию почек и не требует ограничений в диете. ВЗЯТИЕ СЫВОРОТКИ КРОВИ Для оценки функции почек и мочевых путей, а также электролитного обмена разработано множество исследований сыворотки крови (табл. 26-3). Таблица 26-1. Результаты анализа мочи Показатель ОБЩЕЕ ИССЛЕДОВАНИЕ Цвет Нормальное значение Отклонения от нормы От бледно-желтого до темно-золотистого Цвет может меняться в зависимости от приема лекарств Цвет меняется в связи с концентрацией мочи Серьезный симптом — коричневый или черный цвет мочи Запах Ароматический Внешний вид Удельная плотность Прозрачная 1001-1025 РН 5,0-8,0 Белок Глюкоза Отсутствует или обнаруживаются следы Отсутствует Кетоновые тепа Отсутствует Скрытая кровь Отсутствует Эстераза лейкоцитов Отсутствует Гнилостый запах при инфекции Фруктовый запах при сахарном диабете, голодании, дегидратации Характерный запах отмечается при приеме лекарств, например, паральдегида, витаминов и антибиотиков Мутность может свидетельствовать об инфекции мочевых путей Высокая удельная плотность указывает на повышенную концентрацию мочи Удельная плотность увеличивается при введении рентгеноконтрастных веществ, альбумина, декстрана, при дегидратации, застойной сердечной недостаточности и печеночной нецостаточности Снижение удельной плотности указывает на снижение концентрации мочи, возникает при несахарном диабете, почечном канальцевом некрозе или ограниченном употреблении повареной соли Щелочная реакция характерна для инфекции мочевых путей, метаболического или дыхательного алкалоза, повышенного содержания овощей и фруктов в диете, введения бикарбоната натрия или цитрата калия Кислая реакция мочи наблюдается при метаболическом или дыхательном ацидозе, лихорадке, голодании, фенилкетонурии, диете с повышенным содержанием белка, введении аскорбиновой кислоты и метенамина Протеинурия может свидетельствовать о гломерулонефрите, преэклампсии у беременных, множественной миеломе Тест-полоска может не показывать выраженную протеинурию при очень малой концентрации мочи или при миеломе Глюкоэурия в норме отмечается после приема пищи, богатой углеводами, после стресса, при беременности, на фоне приема лекарств, например, кортикостероидов, карбоната лития, аспирина, тиазидных диуретиков Глюкоэурия может быть признаком некорригируемого диабета, заболеваний ЦНС, синдрома Кушинга, инфекций, внутривенного введения растворов, содержащих глюкозу Уровень глюкозы можно проверить тест-полосками Tes-Tape, Clinistix, Clinitesl При беременности, приеме аскорбиновой кислоты, кефлина и стрептомицина возможны ложноположительные результаты исследования тест-полоской Clinitest Кетоновые тела появляются при недостаточной коррекции гипергликемии, дегидратации, голодании или чрезмерном употреблении аспирина Гемоглобинурия возможна при гемолитической анемии, приеме некоторых лекарств (мышьяк, кумадин), посттрансфузионных осложнениях, интоксикации Проба на скрытую кровь положительна при наличии в моче миоглобина (пигмент мышечной ткани), что возможно при инфаркте мышцы, травме, ожогах, судорогах Проба на эстеразу лейкоцитов положительна при наличии нейтрофилов, обычно при инфекции мочевых путей При загрязнении пробы мочи выделениями из влагалища возможен ложноположительный результат Ложноотрицательный результат возможен при массивной Нитриты Отсутствует протеинурии, высоком содержании аскорбиновой кислоты в моче, когда исследование выполняют с помощью тест-полоски Положительный результат свидетельствует о наличии бактерий в моче Ложноотрицательный результат возможен при исследовании только что выпущенной мочи и при наличии в моче грибов или грамположительных бактерий Исследование проводят с использованием тест-полоски МИКРОСКОПИЧЕСКОЕ ИССЛЕДОВАНИЕ Лейкоциты 0-5 в поле зрения Эритроциты 0-5 в поле зрения Цилиндры Отсутствуют или выявляются единичные гиалиновые цилиндры Повышение количества лейкоцитов может указывать на инфекцию верхних или нижних мочевых путей Повышение количества эритроцитов может свидетельствовать о микрогематурии — при нефролитиазе, опухолях мочевых путей, остром гломерулонефрите Гиалиновые цилиндры, или белковые слепки, встречаются в концентрированной моче, и их небольшое количество еще не означает заболевания почек Лейкоцитарные цилиндры указывают на пиелонефрит Эритроцитарные цилиндры встречаются при гломерулонефрите, поражениях сосудов, коллагенозах, подостром бактериальном эндокардите, инфаркте почки; наличие этих цилиндров — признак тяжелого заболевания, требующий тщательного обследования Кристаллы оксалата кальция и фосфатов отмечаются при гиперпаратиреозе или нарушениях всасывания Кристаллы уратов присутствуют в моче при высоком уровне мочевой кислоты в сыворотке крови (подагра) ДИАГНОСТИЧЕСКИЕ МЕТОДЫ ВИЗУАЛИЗАЦИИ Обычное рентгенологическое исследование почек, мочеточников и мочевого пузыря Обзорный снимок живота и таза в прямой проекции позволяет определить форму, размеры и расположение почек, выявить камни, опухоли и аномалии развития почек. Пациенту объясняют, что рентгенологическое исследование позволяет определить анатомические особенности почек. Обычно не требуется особой подготовки, хотя для большей информативности можно назначить слабительные или клизму, чтобы очистить кишечник. Исследование противопоказано при беременности. Таблица 26-2. Результаты сложного анализа мочи Показатель Нормальные значения (СИ) Минимальное количество Альдостерон Нормальное потребление соли: 100-200 мэкв/сут (100-200 ммоль/сут) — 2-26 мкг/сут (8,3-52,7 нмоль/сут) за 24 часа Амилаза 24-76 ЕД/мл Повышение при остром панкреатите Кальций Не более 300 мг/сут (7,5 ммоль/сут) Повышение при гиперпаратиреозе Снижение при гипопаратиреозе или недостаточности витамина D Катехоламины Адреналин: до 20 мкг/сут (менее 109 нмоль/сут) Норадреналин: до 100 мкг/сут (менее 590 нмоль/сут) Хорионический Гонадотропин (тест на беременность Медь Тест отрицательный 0-100 мкг/сут (0-1,6 мкмоль/сут) за 24 часа Повышение при циррозе печени и нефрозе Копропорфирин 50-250 мкг/сут (80-380 нмоль/сут) за 24 часа Креатинин М: менее 40 мг/сут (менее 0,30 нмоль/сут) Ж: менее 80 мг/сут (менее 0,61 нмоль/сут) за 24 часа Повышение при полиомиелите или печеночной порфирии Повышение при лихорадке, беременности, раке печени Клиренс креатинина До 40 лет: М: 90-139 мл/мин/1,73 м3 (0,87-1,34 мл/с/м2) Ж: 80-125 мл/мин/1,73 м3 (0,77-1,20 мл/с/м2) После 40 лет значения уменьшаются на 6,5 мл/мин/1,73 м3 (0,06 мл/с/м2) 2,12 или 24 часа за 24 часа Клиническое значение Повышение при первичном и вторичном (в результате злокачественной гипертензии, застойной сердечной недостаточности, цирроза печени) альдостеронизме Снижение при болезни Аддисона, повышенном приеме натрия, гипокалиемии, беременности Повышение при феохромоцитоме Положительный тест при беременности или пузырном заносе Повышение при сальмонеллезе и столбняке Уменьшение при падении скорости клубочковой фильтрации в сочетании с повышением уровня креатинина плазмы Уменьшение при анемии, лейкозе, мышечной атрофии Цистин или цистеин 0 менее 38,1 мг/сут (менее 317 мкг/сут) Гемоглобин; миоглобин Отсутствует - . ■ -.:,--■• :■ :- Гидроксииндолуксусная кислота 2-6 мг/сут (10,4-31,2 мкмоль/сут) за 24 часа Повышение при карциноидных опухолях Свинец менее 80 мкг/л (менее 0,39 мкмоль/л) 50-1400 мосм/кг 300-900 ммоль/кг (на фоне нормального приема жидкости) за 24 часа Повышение при отравлении свинцом Произвольно за 24 часа Снижение осмоляльности мочи и повышение осмоляльности сыворотки крови при сахарном диабете Повышение при олигурии, обусловленной гиповолемией Фосфор (неорганический) В зависимости от потребления; в среднем 1г/сут i (32 нмоль/сут) за 24 часа Повышение при лихорадке, рахите, туберкулезе Снижение при острых инфекциях, гломерулонефрите Порфобилиноген 0 за 24 часа Белок 1-14 мг/дл (10-140 мг/л) за 24 часа Повышение при острой порфирии или заболеваниях печени Повышение при гематурии, лихорадке, сердечной недостаточности, нефрите Натрий 40-220 мэкв/л (40-220 ммоль/л) за 24 часа Снижение при рвоте, диарее и преренальной анурии Стероиды 17-кетостероиды Возра ст 20 л 30 л 50 л 70 л за 24 часа Повышение при гиперплазии надпочечников и синдроме Кушинга Снижение при болезни Аддисона и гипертензии 17гидроксистероиды 3-8 мг/сут (8-22 мкмоль/сут) за 24 часа Повышение при синдроме Кушинга Снижение при болезни Аддисона Глюкоза 0,5 г/сут (менее 2,78 мкмоль/сут) за 24 часа Повышение при сахарном диабете Клиренс мочевины 12-20 г/сут (0,42-0,71 моль/сут) Азот мочевины следует определять во время сбора мочи за 24 часа Повышение при повышенном катаболизме белка Снижение при нарушении функции почек Осмоляльность мг/сут М Ж 6-21 4-16 8-26 4-14 5-18 3-9 2-10 1-7 мг/сут М 21-73 28-90 17-62 7-35 Ж 14-56 14-49 10-31 3-24 Повышение при цистинурии 10 мл за 24 часа Повышение при переливании несовместимой крови, обширных ожогах, синдроме длительного сдавления . Объем мочи Взрослые: М: 800-1800 мл/сут Ж: 600-1600 мп/сут После 60 лет: 250-2400 мл/сут Уробилиноген До 1,0 ЕД Эрлиха (до 1,0 усл. ЕД) за 2 часа менее 50 мкг/сут за 24 часа Уропорфирины Ванилилминдальная (менее 60 нмоль/сут) 2-7 мг/сут кислота (10,1-35,4 мкмоль/сут) за 24 часа Повышение при несахарном диабете, приобретенных заболеваниях почек, инфузии маннитола, введении рентгеноконтрастных веществ, надпочечниковой недостаточности, белковой недостаточности, после менструации, при употреблении некоторых лекарств. Снижение при дегидратации, кровопотере, шоке, ХПН, циррозе печени, нефролитиазе, почечной недостаточности Повышение при заболеваниях печени Снижение при диарее или почечной недостаточности Повышение при порфирии Повышение при феохромоцитоме Экскреторная урография Экскреторная урография (внутривенная пиелография) — рентгенологическое исследование, позволяющее визуализировать мочевые пути на всем протяжении; оно информативно для диагностики аномалий развития и заболеваний мочевого пузыря, опухолей и кист почек, повреждений почек, опухолей забрюшинного пространства, обструкции мочевых путей. Исследование начинают с внутривенного введения рентгеноконтрастного вещества, после чего производят несколько рентгеновских снимков. Снимок, сделанный в конце исследования после мочеиспускания, позволяет оценить опорожнение мочевого пузыря. При повременном проведении экскреторной урографии снимки делают каждые 5 мин после введения рентгеноконтрастного вещества. Такой вариант экскреторной урографии более надежен в диагностике одностороннего поражения мочевых путей, но не позволяет исключить стеноз почечной артерии. Исследование занимает примерно 45 мин. Подготовка пациента. Пациенту следует объяснить суть исследования, сказав, что оно позволяет уточнить строение мочевых путей на всем протяжении и не вызывает болезненных ощущений. Медсестра проверяет, нет ли в анамнезе указаний на повышенную чувствительность к морепродуктам и йод-содержащим контрастным веществам, на застойную сердечную недостаточность, сахарный диабет, гипертиреоз, бронхиальную астму, сенную лихорадку и артериальную гипертензию. Оценивают степень гидратации пациентов, так как на фоне обезвоживания может проявиться нефротоксичность рентгено-контрастных веществ. Пациента предупреждают, что во время введения рентгеноконтрастного вещества возможны прилив крови, жар и солоноватый привкус во рту, но эти ощущения самостоятельно пройдут. Медсестра указывает на необходимость голодания в течение 8 ч до исследования, чтобы добиться умеренной дегидратации, при которой достигается большая концентрация рентгеноконтрастного вещества; после исследования рекомендуется прием жидкости без ограничений, чтобы способствовать его быстрому выведению. Вечером перед исследованием назначают клизму или слабительное, поскольку скопление кала и газов в кишечнике затрудняет визуализацию мочевых путей. Медсестра должна получить у пациента согласие на исследование. Остатки бария в кишечнике могут затруднить визуализацию мочевых путей, поэтому исследование кишечника с барием следует проводить после экскреторной урографии. Почечная ангиография Ангиография почек позволяет визуализировать почечные сосуды, информативна при стенозе почечной артерии и добавочных или отсутствующих почечных сосудах, реноваскулярной гипертензии, объемных образованиях почки. Во время исследования пациента укладывают на спину, сосудистый катетер вводят через бедренную артерию в аорту до уровня почечных сосудов. Вводя по катетеру контрастное вещество, делают серию рентгеновских снимков. При выполнении дигитальной субтракционной ангиографии требуется меньшее количество рентгеноконтрастного вещества. Таблица 26-3. Биохимические показатели крови Норма (единицы СИ) Показатель Альдостерон нг/дл нмоль/л В положении лежа на спине: Повышение в результате увеличения активности 3-10 ренина в плазме, при застойной сердечной 0,08-0,28 В положении стоя: М: Ж: Азот мочевины Кальций, общий Креатинин Клиническое значение 5-30 6-22 недостаточности, нефротическом синдроме, 0,24-0,83 0,17-0,61 При умеренном потреблении натрия 100 мэкв/сут (100 ммоль/сут) 8-25 мг/дл (2,9-8,9 ммоль/л) гиповолемии Снижение при назначении гепарина Повышение при сниженной клубочковой фильтрации, усиленном приеме белка, повреждениях 8,4-10,2 мг/дл (2,10-2,55 ммоль/л) после 60 лет: 8,8-10,0 мг/дл Повышение при гиперпаратиреозе или гл оме рул о нефрите с уремией (2,20-2,50 ммоль/л) Снижение при поносе, нефрозе, хронической почечной недостаточности или гипопаратиреозе Взрослые нг/дл нмоль/л Повышение при сниженной скорости клубочковой М: 0,6-1,2 53-106 фильтрации; малочувствительный показатель Ж: 0,5-1,1 44-97 ранних стадий заболеваний почек Осмоляльность 275-295 мосм/кг воды (275-295 ммоль/кг воды) после 60 лет:280-301 мосм/кг воды (280-301 ммоль/кг воды) Повышение при дегидратации Калий 3,5-5,0 мэкв/л (3,5-5,0 ммоль/л) Повышение при анурии, олигурии, болезни Аддисона Снижение при диарее, рвоте, диабетическом ацидозе Ренин (активность Обычная диета: Повышение при нефротическом синдроме, хрони- ренина плазмы) Лежа: 1,6 ± 1,5 нгА1/мл/ч 1,6 ± 1,5 мкгА1 ческой почечной недостаточности, злокачественной гипертензии, стенозе почечной артерии, за- Стоя (4 ч): 4,5 ± 2,9 нгА1/мл/ч стойной сердечной недостаточности, кровотече- 4,5 ± 2,9 мкгА1 нии, болезни Аддисона Диета с ограничением соли: Снижение при первичном альдостеронизме, повы Лежа: 3,2 ± 1,1 нгА1/мл/ч шенном приеме соли, употреблении лакрицы 3,2 ± 1,1 мкгА1 Стоя (4 ч): 9,3 ± 4,3 нгА1/мл/ч 9,3 ± 4,3 мкгАГ (*А1 — Ангиотензин 1) Мочу собирают в охлажденный шприц с антикоагулянтом, кладут в лед и немедленно доставляют в лабораторию Натрий 135-145 мэкв/л (135-145 ммоль/л) Повышение при нефрите или при пилоростенозе Снижение при болезни Аддисона или микседеме Подготовка пациента. Медсестре следует объяснить пациенту, что исследование обычно проводится под местной анестезией и что оно позволяет визуализировать сосудистую сеть почек. Ему рекомендуют голодать после полуночи накануне процедуры; некоторые рентгенохирурги предпочитают, чтобы пациент накануне процедуры пил достаточное количество жидкости во избежание гемоконцентрации, повышающей риск послеоперационного тромбоза артерии. Медсестра уточняет чувствительность пациента к пищевым продуктам, йодсо-держащим контрастным веществам, выясняет, получает ли пациент антикоагулянты. Получают письменное согласие пациента на исследование. Медсестра по назначению врача делает клизму или дает слабительное накануне вечером. Определяют ЧСС, АД, частоту дыхания, после введения катетера определяют пульсацию артерий дистальнее места катетеризации. Перед исследованием пациента просят помочиться, по назначению врача вводят седативные препараты. Уход за пациентом после исследования. На 8-12 ч после исследования назначают строгий постельный режим, а в течение 24 ч не разрешают ходить. В течение первых 2 ч каждые 15 мин оценивают пульсацию артерий ниже места катетеризации, кровенаполнение капилляров, ЧСС, АД, частоту дыхания, затем эти же показатели оценивают каждый час, в соответствии с протоколом и результаты сравнивают с результатами, полученными до исследования. Медсестра должна периодически осматривать место пункции бедренной артерии (опасность кровотечения!), измерять диурез. Изотопное сканирование почек Изотопное сканирование почек - информативный метод исследования в диагностике отторжения пересаженной почки, опухолей, абсцессов, кист, сосудистых поражений почек, травмы почек. Радиоактивный изотоп, например, 99mmТс-диэтилентетрамин-пентаацетат (ДТПА), 99mm Тс-димеркаптоянтарную кислоту (ДМЯК) или глюкогептонат вводят внутривенно и измеряют радиоактивность над каждой почкой с помощью гамма-камеры или специального датчика. Уровень радиоактивности сначала быстро повышается, а затем уменьшается по мере того, как радиоактивная метка выводится почками. Форма получаемой кривой выведения радиоизотопа зависит от состояния почек. Иногда проводят двойное исследование — с помощью второго изотопа выполняют серию исследований, а затем, через 4 ч, когда радионуклиды выведены из мочевой системы, получают статические изображения. Изотопное сканирование почек занимает примерно 1,5 ч. Подготовка пациента. Пациенту сообщают, что исследование позволяет оценить функцию почки и что доза радиоактивности минимальна, а радионуклиды полностью выводятся из организма в течение 24 ч. Медсестра просит пациента не двигаться во время сканирования, которое проводят в положении пациента лежа на животе. Исследование не требует ограничений в диете. Необходимо письменное согласие пациента. Компьютерная томография в диагностике заболеваний почек Компьютерная томография (КТ) позволяет получить высококачественное изображение почки и по сравнению с УЗИ выявляет более тонкие различия в плотности тканей. КТ особенно информативна в дифференциальной диагностике между простой кистой и кистозной опухолью почки, при выявлении опухоли почки, надпочечника, гидронефроза и забрюшинного кровотечения из почки. Медсестра должна объяснить пациенту, что исследование дает изображение почек, проводится в положении лежа на спине, при этом сканер вращается вокруг тела обследуемого. Необходимо предупредить пациента о шуме, который издает сканер, и о необходимости снять все металлические предметы перед исследованием. Ультразвуковое исследование почек Ультразвуковое исследование (УЗИ) почек особенно информативно в дифференциальной диагностике простых кист и плотных опухолей почки, при выявлении камней почек, обструкции мочевых путей. Исследование не требует специальной подготовки пациентов, поэтому его можно проводить при почечной недостаточности. Небольшой датчик прикладывают к спине пациента. Ультразвуковые волны проходят через анатомические структуры, а датчик воспринимает волны, отраженные от этих структур. Компьютер обрабатывает отраженные волны и создает изображения. Медсестре следует предупредить пациента, что исследование длится около 30 мин и что во время процедуры врач может попросить сделать форсированный вдох или выдох. СПЕЦИАЛЬНЫЕ ИССЛЕДОВАНИЯ Цистоскопия Цистоскопия обеспечивает возможность непосредственного осмотра слизистой оболочки мочевого пузыря и мочеиспускательного канала с помощью специального инструмента — цистоскопа (рис. 26-9). Она эффективна в диагностике опухолей, воспалительных процессов, анатомических изменений, увеличения соседних органов, например, предстательной железы. Во время этой процедуры можно взять биопсию подозрительных участков, удалить из мочевого пузыря небольшие камни, попавшие в него из почек. Цистоскопия противопоказана при острой инфекции мочевых путей, при выраженной инфравезикальной обструкции, обусловленной увеличением предстательной железы. Во время цистоскопии можно установить катетер в один из мочеточников и собрать мочу из почки или ввести рентгеноконтрастное вещество и получить рентгеновское изображение чашечнолоханочной системы. Ретроградная пиелография информативна при выявлении причин обструкции мочевых путей. Для цистографии в мочевой пузырь через цистоскоп или уретральный катетер вводят раствор, содержащий рентгеноконтрастное вещество. При выполнении микционной цистограммы производят снимки в момент мочеиспускания. Для получения цисто-уретрограмм рентгеноконтрастное вещество вводят в мочеиспускательный канал и мочевой пузырь, а для уретрографии контрастное вещество вводят только в мочеиспускательный канал. Цистография показана при рецидивирующих инфекциях мочевых путей; она информативна при пузырно-мочеточниковом рефлюксе, опухолях, дивертикулах и свищах мочевого пузыря, увеличении предстательной железы. Подготовка пациента. Пациенту объясняют, что исследование выполняют для осмотра слизистой оболочки мочевого пузыря и оно длится от 30 мин до 1 ч, что его уложат в цистоскопическое кресло в положение Тренделенбурга, а бедра, промежность и половые органы закроют операционным бельем. ■ Рисунок 26-9. Цистоскопия у мужчины. Желательно, чтобы пациент высказал все свои опасения и выяснил интересующие его вопросы. Если процедура планируется под наркозом, то необходимо голодание после полуночи перед цистоскопией, для достаточного образования мочи внутривенно вводят растворы. Если исследование планируется под местной анестезией, то перед цистоскопией пациенту разрешают позавтракать. Медсестра объясняет пациенту методику глубокого дыхания, которая позволяет уменьшить ощущения давления или жжения во время цистоскопии, уточняет, нет ли у него повышенной чувствительности к пищевым продуктам или йодсодержащим рентгеноконтрастным веществам, оценивает мочеиспускание, пульс, АД, частоту дыхания, при необходимости, по назначению врача, дает седативные препараты. Перед цистоскопией необходимо получить письменное согласие. Уход за пациентом после исследования. Медсестра наблюдает за функциональными показателями в соответствии с принятой в клинике методикой ведения послеоперационного периода. Пациента предупреждают, что в течение 1 -2 дней после цистоскопии возможно розоватое окрашивание мочи и жжение при мочеиспускании. Для уменьшения дискомфорта после процедуры рекомендуют обильный прием жидкостей, прикладывание теплой грелки к нижним отделам живота, слабые анальгетики, сидячие ванны. Пациенту рекомендуют воздерживаться от приема алкогольных напитков в течение 2 дней после исследования. Макрогематурия, боль, ощущение переполнения мочевого пузыря, лихорадка и тахикардия могут свидетельствовать об осложнениях — перфорации мочевого пузыря, острой задержке мочи, инфекции мочевых путей, аритмии. Медсестра должна знать об этих симптомах и сообщить о них врачу. Если в связи с этим предполагаются дополнительные исследования, то медсестра должна информировать о них пациента; при необходимости она отменяет прием лекарств, например, спазмолитиков или холинолитиков, которые могут помешать исследованию. После цистоскопии для облегчения или устранения некоторых симптомов, в частности, дизурии, гематурии, учащенного мочеиспускания медсестра рекомендует сидячие ванны, теплую ванну, обильное питье. Биопсия почки Чрескожную биопсию почки выполняют путем введения иглы в нижний сегмент почки и взятия с ее помощью столбика почечной ткани. Полученный материал отправляют на гистологическое исследование, чтобы определить характер заболевания почки и его динамику. Биопсия почки — наиболее информативное исследование, позволяющее верифицировать диагноз. Обычно выполнению биопсии предшествует экскреторная урография или УЗИ. Введение иглы в почку часто осуществляют под контролем рентгеноскопии или ультразвукового сканирования. Подготовка пациента. Пациенту объясняют, что биопсия почки позволяет уточнить диагноз, ее выполняют под местной анестезией и что во время процедуры он должен лежать на животе. Пациенту рекомендуют ограничить прием пищи и жидкостей за 8 ч до исследования, предупреждают, что во время процедуры, когда иглу вводят в почку, его могут попросить задержать дыхание и не двигаться. Медсестра уточняет, нет ли в анамнезе нарушения свертывания крови, проверяет результаты коагулографии, при необходимости проверяет группу крови, резус-фактор и наличие необходимого оснащения для переливания крови. Биопсию выполняют после получения письменного согласия пациента. По назначению врача вводят слабое седативное средство. Уход за пациентом после биопсии почки. На 4— 12 ч после исследования назначают постельный режим. Пульс, АД, частоту дыхания, температуру тела контролируют в течение первых 4 ч каждые 15 мин, в течение следующих 4ч — каждые 30 мин, следующие 4ч — каждый час, затем в течение суток 1 раз каждые 4 ч. Часто осматривают место биопсии, чтобы своевременно выявить признаки кровотечения, исследуют мочу на макроили микрогематурию. Рекомендует обильное питье, чтобы уменьшить вероятность почечной колики и избежать ге-моконцентрации. Пациента просят в течение последующих нескольких дней избегать физической нагрузки, связанной с сотрясением тела, и сообщать о появлении жжения при мочеиспускании, боли в боку, лихорадки, гематурии. Уродинамические исследования Уродинамические исследования используются для оценки мочеиспускания и включают цистометрию (цистометрографию), урофлоуметрию, электромиографию и определение профиля уретрального давления. Для цистометрии в мочевой пузырь вводят катетер, соединенный с цистометром. Последний регистрирует давление и объем при наполнении мочевого пузыря стерильной водой, физиологическим раствором или углекислым газом, а также при опорожнении мочевого пузыря. Пациента просят сообщить, когда появится первое ощущение наполнения (обычно при объеме 150-200 мл) и возникнет позыв к мочеиспусканию (обычно при объеме, примерно равном 300 мл). Результаты исследования позволяют планировать время для стимуляции мочеиспускания или проведения периодической катетеризации мочевого пузыря, а также могут оказаться полезными для диагностики интерстициального цистита. Необходимо получить информированное согласие пациента на исследование. Непосредственно перед исследованием пациента просят помочиться. При урофлоуметрии определяют скорость тока мочи. При этом исследовании пациент садится на специальный унитаз и нажимает на кнопку в начале и конце мочеиспускания. В воронке, в которую мочится пациент, находится урофлоуметр, определяющий скорость тока мочи, непрерывность струи. Скорость тока мочи зависит от возраста, пола и объема мочи. В возрасте 14—45 лет средняя скорость тока мочи составляет 21 мл/с у мужчин и 18 мл/с у женщин. В возрасте 46—65 лет средняя скорость тока мочи равна 9 мл/с у мужчин и 10 мл/с у женщин. Повышение скорости тока мочи обусловлено уменьшением уретрального сопротивления, а уменьшение скорости тока мочи вызвано инфравезикальной обструкцией или гипотонией детрузора. Медсестра просит пациента не мочиться в течение нескольких часов перед исследованием. Пациенту также рекомендуют обильное питье перед исследованием, так как для достоверного результата необходим объем мочи не менее 200 мл. Пациенту объясняют, что можно мочиться в том положении, которое наиболее удобно, и он сможет оставаться в уединении во время процедуры. Исследование занимает 10—15 мин. Электромиография — запись электрической активности поперечно-полосатых мышц во время мочеиспускания — позволяет оценить координацию деятельности нейромышечных элементов мочевого пузыря. Электрическую активность измеряют посредством накожных или игольчатых электродов, установленных в области мочеиспускательного канала и промежности, а также электродов, введенных в задний проход с тампоном. Во время исследования пациента просят попеременно напрягать и расслаблять наружный сфинктер мочеполовой диафрагмы. Электромиография особенно информативна в установлении причин недержания мочи. Медсестра объясняет пациенту цель исследования, а также роль и расположение каждого типа используемых электродов. Исследование профиля уретрального давления позволяет оценить активность гладких мышц, окружающих мочеиспускательный канал, что важно для диагностики стриктур и повышенного тонуса мышц, связанного с инфравезикальной обструкцией. Во время исследования устанавливают уретральный катетер, по которому вводят углекислый газ или воду. Затем катетер медленно удаляют — при этом измеряют сопротивление, оказываемое катетеру стенками мочеиспускательного канала. • ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ 1. Что такое скорость клубочковой фильтрации? Какие факторы влияют на образование клубочкового фильтрата? 2. Какое значение имеют жалобы пациентов? 3. Почему важно выяснить, какие лекарства назначены пациенту с заболеваниями почек и мочевых путей? 4. Как оценивают болезненность в области реберно-позвоночного угла, каково значение этого симптома? 5. Расскажите о подготовке пациента к экскреторной урографии, ретроградной пиелографии и цистоскопии, а также о ведении пациентов после этих исследований. 6. Объясните методику сбора мочи для сложных исследований так, как это объясняют пациентам. ИНФЕКЦИОННЫЕ И ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ ПОЧЕК. АНОМАЛИИ РАЗВИТИЯ ПОЧЕК ПОЛИКИСТОЗ ПОЧЕК ■ ОПРЕДЕЛЕНИЕ Поликистоз почек — врожденное заболевание почек, характеризующееся образованием кист внутри нефронов и передающееся аутосомно-доминантным путем (рис. 27-1). У взрослых заболевание обычно проявляется примерно в 40 лет. ЭТИОЛОГИЯ И ЭПИДЕМИОЛОГИЯ Поликистоз почек поражает одинаково часто мужчин и женщин. Проявления этой болезни отмечаются более чем у одного члена семьи и наблюдаются в последующих поколениях. От поколения к поколению симптомы возникают примерно в одном и том же возрасте. Наличие в семье больных поликистозом почек обычно отмечают 75—85% пациентов с этим заболеванием. Хотя симптомы, как правило, возникают примерно в 40 лет, заболевание может проявиться и в 20 лет, и в 80. До появления симптомов при УЗИ можно выявить кисты. Поражаются обычно обе почки, возможно сочетание с кистозными изменениями других органов — поджелудочной железы, селезенки, яичек, яичников, легких, щитовидной железы и матки. Примерно в 40-60% случаев поликистоз почек сочетается с кистами печени. Хотя при этом размеры печени увеличиваются, ее функция не нарушается. Поликистоз почек часто сочетается с дивертикулезом кишечника и аортальной регургитацией, а также с аневризмами мозговых артерий. Примерно у 10% пациентов с аневризмами мозговых артерий случаются субарахноидальные кровоизлияния. Поликистоз почек занимает третье место среди причин терминальной почечной недостаточности и отмечается не менее чем у 12% пациентов, которым проводят диализ или выполняют трансплантацию почки. ПАТОФИЗИОЛОГИЯ Множественные кисты напоминают грозди винограда, растущие из нефронов. Эти тонкостенные кисты наполнены жидкостью, но могут содержать кровь или гной. По мере роста кист почка увеличивается в 2—5 раз по сравнению с нормальными размерами — это приводит к сдавлению внутри- и внепочечных анатомических структур. Возможны разрывы и инфицирование кист, приводящие к рубцеванию почечной ткани и уменьшению количества функционирующих нефронов. В конце концов возникает почечная недостаточность. Уремия обычно развивается в течение 16 лет после появления симптомов заболевания. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ Частый симптом — боль в животе или боку, которая носит постоянный тупой характер, но иногда напоминает колику. Примерно в 50% случаев отмечается гематурия из-за кровотечения в полость кист. Характерно повышение АД, так как теряется способность почек регулировать концентрацию натрия в крови. В 2/3 случаев при поликистозе можно пропальпировать объемные образования в проекции почек, смещающие органы брюшной полости. Пальпировать следует осторожно, чтобы не вызвать боль и кровотечение. Поликистоз почек часто сопровождается рецидивами инфекции мочевых путей. Изначально у таких пациентов может быть сепсис, вызванный грамотрицательной флорой. Уремия нарастает медленно, в течение длительного периода; уменьшить эти проявления можно с помощью ограничений в диете и приема жидкостей, а в терминальной стадии заболевания прибегают к диализу или трансплантации почки. Рис. 27-1. Вид почки при поликистозе РАБОТА МЕДИЦИНСКОЙ КОМАНДЫ При поликистозе не существует специфического лечения. Все мероприятия направлены на уменьшение боли и других симптомов заболевания. Тепловые процедуры и ненаркотические анальгетики позволяют уменьшить боль, обусловленную увеличением почек. При возникновении кровотечения отменяют тепловые процедуры и назначают строгий постельный режим. В случае выраженного кровотечения может потребоваться переливание крови, а также эмболизация сегментарной почечной артерии или даже резекция почки. Артериальная гипертензия поддается лечению гипотензивными препаратами, диуретиками, коррекцией диеты и количества принимаемой жидкости. В связи с инфекцией мочевых путей часто назначают антибиотики. У пациентов с поликистозом почек может не быть эффекта от обычной антибактериальной терапии; следовательно, может потребоваться чрескожная пункция и аспирация содержимого кист. При тяжелых гнойных осложнениях выполняют нефрэктомию. По мере прогрессирования заболевания возникает необходимость в диализе. Разрывы кист могут произойти от сдавления ремнем безопасности в автомобилях и самолетах. Пациентам не запрещают пользоваться этими защитными приспособлениями, но советуют не затягивать их слишком туго вокруг живота. Как женщинам, так и мужчинам не следует туго застегивать одежду. Необходимо избегать контактных видов спорта. Поскольку поликистоз почек — наследственное заболевание, пациентам показано генетическое консультирование и скрининг членов семьи. У каждого ребенка, родитель которого страдает поликистозом почек, риск наследования дефектного гена составляет 50%. Иногда поликистоз почек диагностируют у пациентов, уже перешагнувших рубеж репродуктивного возраста. Если для лечения терминальной почечной недостаточности у пациента с поликистозом почек планируется трансплантация почки, то членов семьи, несущих дефектный ген, необходимо исключить из числа потенциальных доноров. СТАДИИ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ Течение острой почечной недостаточности (ОПН) делят на четыре стадии: начальную, олигурическую, диуретическую, восстановления. Первая стадия, начальная, соответствует началу повреждения почечной ткани. Важность этой стадии заключается в том, что немедленные вмешательства могут привести к обратному развитию изменений почечной паренхимы и предотвращению дальнейших нарушений функции почек. В олигурическую фазу, которая продолжается от 8 до 14 дней, образование мочи значительно снижается (менее 400 мл в сутки). В норме процесс старения сопровождается снижением способности нефронов концентрировать мочу, поэтому у пожилых людей возможно нарушение функции при большем объеме суточной мочи (600-700 мл). Выраженность азотемии, возникающей в эту фазу, в значительной степени зависит от количества мочи и интенсивности катаболизма белков. Остается неясным, является ли почечная недостаточность без олигурии самостоятельным синдромом или фазой олигурической формы ОПН. Почечная недостаточность без олигурии возникает главным образом после назначения нефротоксичных антибиотиков, а иногда после ожогов, анестезии или травматических повреждений. Почечная недостаточность без олигурии обычно сопровождается меньшей летальностью и меньшим количеством осложнений по сравнению с олигурической формой почечной недостаточности. Это может быть обусловлено меньшей выраженностью и меньшей длительностью азотемии. Диуретическая фаза ОПН обычно продолжается около 10 дней и отражает восстановление нефронов и их способности выделять мочу. Эта фаза протекает на фоне неполного восстановления функции нефронов, поэтому азотемия все еще сохраняется. Фаза восстановления отражает улучшение функции почек и может продолжаться до 6 мес. В последнюю очередь восстанавливается способность почек концентрировать мочу. Часто впоследствии сохраняется некоторое нарушение функции почек. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ Клинические проявления ОПН могут отсутствовать в течение недели после повреждающего воздействия. Симптомы ОПН появляются, как правило, внезапно, и состояние пациента становится критическим. Возникают нарушения регуляции водно-электролитного и белкового обмена с последующей полиорганной недостаточностью. Олигурическая стадия Наиболее частый симптом ОПН — уменьшение суточного количества мочи. Во время олигурической фазы суточный диурез не превышает 400 мл. В некоторых случаях возникает анурия (суточный диурез менее 50 мл). При ОПН без олигурии у пациентов может выделяться около 2 л мочи. Олигурическая фаза продолжается от 8 до 14 дней, и чем она длительнее, тем хуже прогноз. Удельная плотность мочи снижается и стабилизируется на уровне 1010 (в норме 1025), а по осмоляльности моча приближается к плазме крови (примерно 300 мосм/кг). Во время этой фазы в крови накапливаются продукты азотистого обмена. Уровень креатинина в крови возрастает приблизительно на 1 мг/дл в сутки, а уровень мочевины в крови — примерно на 20 мг/дл в сутки (табл. 27—1). Экскреция кислых продуктов обмена веществ с мочой уменьшается, поэтому нарастает метаболический ацидоз. Дыхание становится частым, глубоким (дыхание Куссмауля) и направлено на удаление избытка углекислого газа и компенсацию метаболического ацидоза. Олигурия приводит к задержке жидкости в тканях, возникновению отеков и артериальной гипертенз'ии. Увеличение массы тела на 1 кг соответствует задержке 1 л жидкости. Перегрузка жидкостью может вызвать застойную сердечную недостаточность и отек легких. Уменьшение экскреции калия с мочой и обусловленный ацидозом выход калия из клеток приводят к гиперкалиемии. Признаки гиперкалиемии определяются на ЭКГ - высокий, пикообразный зубец Т, исчезновение зубцов Р, расширение комплекса QRS, эктопический сердечный ритм. Значительная гиперкалиемия (более 6,5 мэкв/л) может вызвать остановку сердца. Гиперкалиемия встречается реже при ОПН без олигурии, так как в этом случае частично сохраняется экскреция калия с мочой. При ОПН могут возникнуть потери натрия с мочой. Эти потери в сочетании с гемодилюцией приводят к гипонатриемии. В результате повышается возбудимость нервных клеток, что проявляется головной болью, спутанностью сознания, судорогами и развитием комы. Эти неврологические расстройства могут быть также результатом воздействия уремических токсинов на центральную нервную систему. Таблица 27-1. Изменения лабораторных показателей при острой почечной недостаточности Показатель Преренальная ОПН Ренальная ОПН Постренальная ОПН Остаточный азот мочевины Повышается Повышается Повышается Креатинин Отношение мочевина/креатинин В норме 20:1 или больше (повышено) Повышается 10:1 или меньше (не повышено, так как увеличены оба показателя) Повышается В норме или незначительно повышено Мочевина Креатинин Удельная плотность Снижается = В норме 1020 или более (повышена) Снижается Снижается Стабильная, может быть высокой Снижается Снижается Может быть как повышенной, так и сниженной Количество ОЛИГУРИЯ Возможна олигурия Олигурия/полиурия Анурия Осмоляльность 400 мосм/кг или более 250-350 мосм/кг (низкая и стабильная, как у плазмы) Повышена или такая же,как у плазмы КРОВЬ МОЧА Если длительность ОПН превышает несколько дней, то у пациентов развивается анемия. Она обусловлена сниженной продукцией эритропоэтина поврежденными почками и токсическим воздействием уремии на кроветворение. Накопление мочевины в крови приводит к снижению адгезивной способности тромбоцитов и уменьшению продолжительности жизни эритроцитов. Клинически анемия проявляется в повышенной утомляемости, слабости, одышке, тахикардии. Накопление продуктов азотистого обмена в крови вызывает различные симптомы, которые объединяют в так называемый уремический синдром. Этот синдром включает тошноту, рвоту, анорексию, понос, икоту и неврологические симптомы, указанные ранее. Мочевина также раздражает перикард и может вызвать уремический перикардит, который может осложниться тампонадой сердца. При уремии нарушается как гуморальный, так и клеточный иммунитет, поэтому у пациентов с ОПН высок риск инфекционных осложнений. Диуретическом стадия Диуретическая фаза ОПН начинается примерно через 14 дней после действия повреждающего фактора на почки и продолжается около 10 дней. Эта фаза характеризуется увеличением суточного диуреза (более 1000 мл). Оно отражает частичное восстановление функции почек; однако уровни креа-тинина и остаточного азота мочевины продолжают повышаться в течение первых дней диуретической фазы. Мочевина и другие продукты обмена веществ играют роль осмотических диуретиков. Все эти факторы вызывают дегидратацию и могут привести к смерти. В эту фазу погибают 25% пациентов с ОПН. Утех, кто выживает, лабораторные показатели начинают возвращаться к норме. Во время диуретической фазы отмечаются значительные водно-электролитные нарушения, и поэтому пациентам может потребоваться диализ. Стадия восстановления Фаза восстановления продолжается до 12 мес. Обычно у пациентов сохраняются нарушения функции почек (табл. 27-2). Таблица 27-2. Сравнение олигурической и диуретической фаз острой почечной недостаточности Физиологические Показатели Симптомы эффекты ОЛИГУРИЧЕСКАЯ ФАЗА Нарушение экскреции продуктов обмена веществ Повышение уровня мочевины и креатинина в крови Нарушение регуляции уровня электролитов Гиперкалиемия Гипонатриемия Ацидоз Нарушение экскреции жидкости Перегрузка жидкостью Гиперволемия Тошнота Рвота Сонливость Спутанность сознания Кома Желудочно-кишечное кровотечение Порхающий тремор Перикардит Тошнота Рвота Аритмии сердца Дыхание Куссмауля Сонливость Спутанность сознания Кома Отеки Застойная сердечная недостаточность Отек легких Артериальная гипертензия ДИУРЕТИЧЕСКАЯ ФАЗА Увеличение образования мочи Гиповолемия Потери натрия Потери калия Медленно повышается экскреция продуктов обмена веществ Высокий начальный уровень остаточного азота мочевины постепенно возвращается к норме Количество мочи до 4-5 л в сутки Постуральная гипотензия Тахикардия Улучшается функция нервной системы, восстанавливается сознание РАБОТА МЕДИЦИНСКОЙ КОМАНДЫ Как при любом заболевании, на первом месте с ит профилактика ОПН. Очень важно обеспечить достаточное поступление жидкости для поддержания перфузии почечной ткани у пациентов с высоким риском ОПН. К ним относятся пожилые люди, все пациенты с нестабильной гемодинамикой и лица, которых лечат препаратами, обладающими нефротоксическим действием, или которым вводят большие дозы рентгеноконтрастных веществ. Для профилактики преренальной почечной недостаточности необходимо улучшить кровоток в почках путем внутривенного введения жидкостей и лекарственных препаратов. Например, если преренальная почечная недостаточность вызвана снижением сердечного выброса вследствие аритмии или нарушения сократительной функции миокарда, то лечение должно быть направлено на улучшение сердечной деятельности — введение антиаритмических средств или сердечных гликозидов. Для восстановления перфузии почечной ткани следует улучшить работу сердца. Врач может назначить болюсное внутривенное введение жидкостей, чтобы увеличить скорость клубочковой фильтрации и диурез. Можно назначить осмотический диуретик маннитол, который увеличивает объем внутрисосудистой жидкости и перфузию почечной ткани. Такие диуретики, как фуросемид, буметанид, этакриновая кислота, у этих пациентов могут использоваться селективно. Раннее введение диуретиков (в первые 4—8 ч после действия повреждающего фактора на почки) может перевести олигурическую форму ОПН в неолигурическую и улучшить прогноз. Олигурическая стадия Лечение при олигурической фазе ОПН направлено на восстановление водно-электролитного обмена, кислотно-щелочного равновесия, профилактику токсических эффектов уремии и инфекционных осложнений, а также на обеспечение адекватного питания. Проводят тщательный мониторинг количества введенной и выделенной жидкости, а также других показателей водного баланса — ЦВД, ДЗЛА, массы тела. После восстановления водного баланса продолжают введение жидкостей в объеме 400—600 мл в сутки для восполнения потерь (с потом и дыханием плюс некоторое количество мочи, выделенной за предшествующие сутки). Следует также учитывать потери жидкости при рвоте, промывании желудка и поносе. Перегрузка жидкостью вследствие олигурии может привести к временной гипонатриемии, что требует соответствующей коррекции водного баланса. В связи с нарушением почечной экскреции фосфора можно назначить внутрь препараты, связывающие фосфор, например, гидроксид алюминия. Это позволит удалить избыток фосфатов с калом, обеспечить нормальный уровень фосфора в сыворотке без изменения уровня кальция. Гиперкалиемия (см. вставку) опасна для жизни, поэтому должна быть устранена. При уровне калия в сыворотке ниже 6 мэкв/л можно обойтись неинвазивными методами: ограничение поступления калия с пищей; прием внутрь или ректальное введение ионо-обменных смол, например, полистирола натрия сульфоната (Kayexalate) для выведения калия через желудочно-кишечный тракт. Сорбитол является осмотическим слабительным. Его назначают вместе с полистиролом натрия сульфоната, чтобы предотвратить каловый завал и удалить натрий, выделяемый ионообменными смолами. При повышении уровня калия в сыворотке до 6,5 мэкв/л можно отметить изменения на ЭКГ — это показание к более интенсивному лечению. К экстренным мероприятиям, уменьшающим кардиотоксические эффекты выраженной гиперкалиемии, относятся: внутривенное введение лекарств, в том числе 50% глюкозы и простого инсулина, бикарбоната натрия, глюконата кальция. Метаболический ацидоз вызван снижением почечной экскреции кислот и нарушением регуляции обмена бикарбоната и калия. Компенсаторная функция дыхательной системы, направленная на преодоление метаболического ацидоза посредством гипервентиляции и экскреции углекислого газа, становится неэффективной и возникает потребность в диализе для устранения ацидемии. Уменьшить количество продуктов метаболизма можно с помощью коррекции питания. Диета, бедная белком и богатая жирами и углеводами, дает достаточное количество энергии и сохраняет запасы белка в организме, таким образом уменьшая образование небелковых азотистых метаболитов. Мочевина утилизируется в организме при синтезе аминокислот, необходимых для образования белков и построения тканей, даже если потребление белка сведено к минимуму. В диете также следует ограничить количество натрия и калия. Желудочно-кишечные расстройства, такие как тошнота и рвота, обусловленные уремией, лучше всего устранить с помощью диализа. Противорвотные средства лишь незначительно уменьшают эти симптомы. Если с пищей поступает недостаточное количество питательных веществ, то прибегают к парентеральному введению питательных растворов или к зондовому кормлению. Введение интралипида в качестве добавки к основному рациону — хороший источник калорий небелкового происхождения. Главная цель коррекции диеты — уменьшить распад белка в организме и предотвратить кетоз, обусловленный расшеплением тканевых жиров. Лечение гиперкалиемии Катионообменные смолы (например, каэксалат), назначаемые внутрь или ректально. Внутривенное введение глюконата или хлорида кальция, 5-10 мл 10% раствора, чтобы воспрепятствовать падению сердечной деятельности. Бикарбонат натрия, 1 -2 ампулы внутривенно, для коррекции ацидоза и перемещения калия обратно в клетки. Простой инсулин 10-15 ЕД в 250-500 мл 10% глюкозы внутривенно в течение 30-60 мин для перемещения калия обратно в клетки. Терапия диуретиками для выведения калия с мочой. Диализ для восстановления электролитного баланса и коррекции ацидоза. Значительное число пациентов, особенно пожилых, погибают при ОПН от вторичной инфекции. Очень важно тщательно соблюдать правила асептики, а также изолировать этих пациентов от тех, у кого выявлены инфекционные заболевания. Следует избегать постановки постоянного уретрального катетера Фо-лея, чтобы не внести инфекцию. Пациента необходимо наблюдать для своевременного выявления симптомов инфекции (лихорадка, припухлость, покраснение, боль и лейкоцитоз). Оправдана антибактериальная терапия, при этом нужно учитывать, что многие антибиотики и их метаболиты выделяются почками. У многих пациентов возникает уремический перикардит. Его симптомами являются боль, усиливающаяся при дыхании, которая может уменьшиться в вертикальном положении тела, шум трения перикарда, тахикардия и лихорадка. Лечение направлено на уменьшение воспалительного процесса и включает использование стероидов или нестероидных противовоспалительных препаратов. При нарушениях системной гемодинамики показаны перикардиоцентез или перикардэктомия. Наиболее приемлемый вид диализа выбирается исходя из клинической ситуации. Цели диализа — восстановление водно-электролитного баланса, коррекция ацидоза и устранение симптомов уремии. Диуретическом стадия У пациента, выздоравливающего после ОПН, диуретическая фаза возникает в период от нескольких дней до нескольких недель после начала лечения. Повышение количества мочи свидетельствует о том, что некоторые нефроны восстанавливаются, но функция почек еще не восстановилась. Канальцевые нарушения сохраняются, о чем свидетельствуют большие потери натрия и калия с мочой. В течение первых нескольких дней диуретической фазы уровень креатинина и азота мочевины продолжают повышаться — эти вещества играют роль осмотических диуретиков. Возможна дегидратация, поэтому в течение диуретической фазы необходимо восполнять потери жидкости и электролитов. Может потребоваться диализ, чтобы очистить кровь от уремических токсинов и поддержать оптимальный водный баланс. ХРОНИЧЕСКАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ ОПРЕДЕЛЕНИЕ И ЭТИОЛОГИЯ Хроническая почечная недостаточность (ХПН) возникает в результате многих заболеваний и характеризуется прогрессирующим, необратимым повреждением нефронов и почечных клубочков. Рецидивирующие воспалительные процессы в почке, поражения сосудов при диабете или гипертензии могут привести к Рубцовым изменениям почечной ткани и представляют собой относительно редкую группу причин ХПН. Неразрешившаяся острая почечная недостаточность также может перейти в ХПН. Патологический процесс может поражать диффузно обе почки или локализоваться в одной из них. Первично поражается почечная паренхима. Независимо от причины ХПН приводит к постепенному снижению клубочковой фильтрации, ухудшению функции почечных канальцев и падению их реабсорбирующей способности — это вызывает нарушения водно-электролитного баланса, кислотно-основного равновесия и другие системные изменения. В целом, состояние прогрессивно ухудшается вплоть до уремии. По мере снижения функции почек возникает необходимость в диализе. Патогенез ХПН или терминальной стадии заболеваний почек характеризуется прогрессирующим, необратимым разрушением нефронов. Функция почек снижается, конечные продукты белкового обмена накапливаются в крови (азотемия). Согласно гипотезе интактных нефронов, некоторые нефроны не вовлекаются в процесс, тогда как другие подвергаются прогрессирующему разрушению. Интактные нефроны максимально увеличивают свою функцию по мере адаптации к возрастающей на них нагрузке. Эти адаптационные изменения поддерживают функцию почек до тех пор, пока не наступит разрушение примерно 3/4 всех нефронов. Однако по мере гипертрофии нефронов теряется их способность концентрировать мочу. В результате выделяется значительный объем мочи низкого удельного веса, и пациент теряет большое количество жидкости. Один из самых ранних признаков почечной недостаточности — выделение мочи, которая практически изотонична плазме крови (осмолярность ее составляет примерно 300 мосм/л). Постепенно теряется способность канальцев к реабсорбции электролитов — это приводит к «солевому истощению» и усиливает полиурию. По мере того, как заболевание прогрессирует и почки перестают справляться с удалением метаболитов, нарастают клинические проявления уремии. В конце концов, водно-электролитные нарушения начинают влиять на другие системы органов. Причины хронической почечной недостаточности Инфекции: - Пиелонефрит - туберкулез Метаболические нарушения: - амилоидоз - гипероксалурия Врожденные и наследственные заболевания: - поликистоз - поликистоз почек - гипоплазия почки Обструкции мочевых путей: - доброкачественная гиперплазия предстательной железы - мочекаменная болезнь - опухоли мочевых путей Поражение почечных клубочков: - гломерулонефрит - нефротический синдром Стеноз мочевых путей: - врожденные аномалии развития Поражения почечных канальцев: - почечный канальцевый ацидоз - хронические электролитные нарушения Диффузные болезни соединительной ткани: - склеродермия - системная красная волчанка - узелковый периартериит Иммунологические нарушения: - сахарный диабет - синдром Гудпасчера Болезни крови и сосудов: - серповидно-клеточная анемия - артериальная гипертензия - тромбоз Инфаркт почки Рак Лучевой нефрит Нефротоксичность КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ При ХПН происходит задержка натрия и воды в организме, в результате наступает «пропитывание тканей водой». Клинические признаки такого состояния — отеки, артериальная гипертензия, возможность застойной сердечной недостаточности и отека легких. Активация ренин-ангиотензин-альдостероновой системы может усугубить водно-электролитные нарушения и артериальную гипертензию. У некоторых пациентов отмечается потеря соли, приводящая к потере воды и гиповолемии. Тошнота, рвота и диарея также могут усилить водноэлектролитные нарушения. Наиболее часто возникают нарушения обмена таких электролитов, как натрий, хлориды, калий, кальций, магний и фосфор. При ХПН нарушается экскреция натрия, которая является причиной гипернатриемии. Гипонатриемия может возникать в результате истощения, диареи или рвоты. Калий экскретируется в основном почками; однако гиперкалиемия возникает не всегда — лишь на поздних стадиях заболевания, когда нарушается регуляция водного баланса и наступает метаболический ацидоз. Гиперкалиемия — характерная черта терминальной стадии заболеваний почек. При гиперкалиемии снижается сократительная способность миокарда, возникают изменения на ЭКГ. Между концентрацией кальция и фосфора в плазме крови существует обратно пропорциональная зависимость. При ХПН теряется способность почек к экскреции фосфата, который является буфером для ионов водорода. Повышение уровня фосфата в плазме приводит к снижению концентрации ионизированного кальция в ней, что влечет за собой усиление секреции паратгормона. Это стимулирует высвобождение кальция и фосфора из костей — возникает почечная остеодистрофия с потерей поддерживающего костного матрикса. Такое состояние у детей иногда называют почечным рахитом. Почечная остеодистрофия может также усиливаться в результате хронического метаболического ацидоза, так как минеральные вещества кости используются в качестве буфера, препятствующего снижению рН крови. Под влиянием паратгормона в почках в норме происходит превращение витамина D в 1,25-дигидроксихолекальцифе-рол, наиболее активную форму, необходимую для всасывания кальция в желудочно-кишечном тракте. При ХПН в результате вторичного гиперпаратиреоза, обусловленного дисбалансом между уровнями кальция и фосфора, нарушается обмен витамина D. В терминальной стадии заболеваний почек прием магния может вызвать повышение уровня фосфора и привести к остановке сердца или дыхания. Метаболический ацидоз — характерный признак заболеваний почек. При поражении почек нарушается способность почек выделять кислые метаболиты и сохранять ионы бикарбоната. В целом, снижение экскреции иона водорода пропорционально уменьшению скорости клубочковой фильтрации. Метаболические изменения при почечной недостаточности также проявляются в накоплении продуктов обмена веществ, в частности, возрастает уровень креатинина и остаточного азота мочевины. Снижение толерантности к глюкозе при ХПН возникает в результате нарушения утилизации инсулина периферическими тканями. При почечной недостаточности период полувыведения инсулина увеличивается, однако существенного клинического значения это не имеет. Почти всегда при ХПН обнаруживают повышение уровня триглицеридов, приводящее к гиперлипидемии IV типа. Эти изменения, по-видимому, обусловлены усилением образования липидов в печени в ответ на повышение уровней глюкозы и инсулина, а также на уменьшение утилизации липидов периферическими тканями. Кроветворная система также поражается при ХПН, так как почка вырабатывает эритропоэтин, который стимулирует образование эритроцитов в красном костном мозге. Снижение секреции эритропоэтина приводит к анемии. На возникновение анемии также влияют следующие факторы: 1) накопление в крови токсинов, которые дополнительно подавляют образование эритроцитов в красном костном мозге; 2) вторичный гиперпаратиреоз, при котором происходит стимуляция соединительной ткани, возникает фиброз костной ткани, костномозговые полости зарастают; 3) укорочение жизни эритроцитов в результате токсического действия мочевины; 4) токсическое действие мочевины снижает адгезивные свойства тромбоцитов, вызывая повышенную кровоточивость и развитие пурпуры, а также создает опасность стрессовой язвы желудка и желудочнокишечного кровотечения. Неврологические осложнения ХПН — головная боль, повышенная утомляемость, раздражительность и депрессия — обычно развиваются медленно; их можно охарактеризовать как уремическую энцефалопатию и периферическую нейропатию. При уремической энцефалопатии нарушение функции центральной нервной системы по своим проявлениям напоминает токсические или метаболические поражения мозга. К первым признакам уремической энцефалопатии относятся снижение реактивности и подавленное состояние, так как пациенты осознают наличие у себя тяжелого почечного заболевания. Постепенно нарушаются способность концентрировать внимание, кратковременная память, появляются ошибки восприятия, способность узнавать людей и предметы. В терминальной фазе может возникнуть делирий или кома. Эти расстройства центральной нервной системы, повидимому, вызваны накоплением уремических токсинов, недостатком ионизированного кальция в спинномозговой жидкости, задержкой калия и фосфатов, эпизодами ги-пертензии и нарушением водного баланса. Симптомы периферической нейропатии возникают на ранних стадиях уремии. Более часто поражаются нижние конечности, нарушаются и двигательные и чувствительные функции — возникают ощущения жжения и онемения в голенях и ступнях. Поражение обычно симметричное. Нарушения периферической иннервации голеней и ступней обычно отмечаются в 40% случаев уремии — возникает ощущение ползания мурашек, зуд, покалывание, обычно более интенсивные ночью. Движения ногами несколько облегчают эти ощущения — отсюда название «синдром беспокойных ног». Даже при отсутствии периферической нейропатии возможны нарушения вегетативной иннервации, например, артериальная гипертензия или импотенция. Наиболее распространенные желудочно-кишечные расстройства при ХПН — тошнота, рвота, ано-рексия и икота. Распад мочевины, содержащейся в слюне, до аммиака вызывает характерный уремический запах. Возникает металлический привкус во рту, что все больше снижает аппетит у таких пациентов. Выдыхаемый воздух в этих случаях может пахнуть рыбой, гнилью или аммиаком. Причины тошноты и рвоты не совсем ясны, но могут быть связаны с выработкой аммиака, раздражающего слизистую желудка, при разложении мочевины микрофлорой тонкой кишки. Кроме того, под влиянием паратгормона усиливается секреция соляной кислоты в желудке. Эти симптомы в сочетании с кровоточивостью, вызванной нарушением функции тромбоцитов, могут стать причиной желудочно-кишечных кровотечений. Частота язвенной болезни желудка при уремии составляет от 40 до 60%. Нередко возникает стоматит с изъязвлением слизистой оболочки щек. Большие трудности вызывают также запоры, вызванные ограничением приема жидкостей, снижением физической активности и использованием лекарств, связывающих фосфаты. Как было указано ранее, ХПН приводит к нарушению водного баланса, артериальной гипертензии и застойной сердечной недостаточности. Кроме того, накопление уремических токсинов примерно в 50% случаев ХПН может вызвать перикардит, симптомами которого являются боль, шум трения перикарда, лихорадка и тахикардия. У пациентов, которым проводится диализ, перикардит возникает в результате стресса, инфекции или гепаринизации. Перикардит может осложниться тампонадой сердца. Вероятно, 50—65% причин смерти при ХПН обусловлено сердечно-сосудистыми осложнениями. ХПН ускоряет развитие атеросклероза из-за нарушения липидного и углеводного обмена, гиперпаратиреоза и дефектов фибринолиза, приводящих к возникновению микроэмболов. В артериях таза, голеней, ступней, кистей, предплечья и в брюшном отделе аорты можно обнаружить обызвествления. Хроническая почечная недостаточность сопровождается изменениями кожи. Вторичный гиперпаратиреоз и отложение кальция в коже приводят к выраженному зуду. На поздних стадиях почечной недостаточности зуд усиливается из-за появления уремического «инея» — кристаллов мочевой кислоты, которая выделяется через кожу, компенсируя нарушенное выведение ее почками. Длительное расчесывание приводит к появлению экскориаций. Кровоточивость, обусловленная нарушением функции тромбоцитов, становится причиной петехий, пурпуры и легкого образования синяков. Кожа приобретает желтовато-бледный оттенок из-за анемии и отложения урохромных пигментов. Таблица 27-3. Проявления хронической почечной недостаточности Система Причины поражения Признаки/Симптомы Контролируемый показатель Кроветворение Подавление образования Анемия Гематокрит эритроцитов Снижение продолжительности жизни эритроцитов Кровопотеря из-за кровотечений Лейкоцитоз Гемоглобин Нарушение функции тромбоцитов Количество тромбоцитов Кровопотеря при диализе Тромбоцитопения Синяки, рвота кровью, Сердечнососудистая Желудочнокишечный тракт Незначительная тромбоцитопения Снижение активности тромбоцитов Перегрузка жидкостью Ренин-ангиотензиновый механизм Перегрузка жидкостью, анемия Гиперволемия Гипертензия Тахикардия Пульс, АД, ЧД Масса тела ЭКГ Хроническая гипертензия Аритмии Тоны сердца Обызвествление мягких тканей Застойная сердечная недостаточ- Электролиты крови Уремические токсины в перикарди- ность Перикардит Боль Анорексия Контроль за количеством принимаемой пищи и жидкости, физиологическими выделениями Гематокрит альной жидкости Отложения фибрина на эпикарде Уремические токсины в сыворотке крови мелена Электролитные нарушения Изменения активности тромбоцитов Нервная система Опорнодвигательная Кожа Желудочно-кишечные кровотечения Гемоглобин Тошнота и рвота Гваяковая проба на Мочевина превращается в аммиак Вздутие живота под действием слюны Диарея Запор скрытую кровь Вид каловых масс Боль в животе Уремические токсины Электролитные нарушения Уремический запах Сонливость, спутанность сознания Уровень ориентации Уровень сознания Отек мозга из-за перерохпределе- Судороги Рефлексы ния жидкости Ступор, кома ЭЭГ Нарушения сна Уровень электролитов, сыворотки Уменьшение всасывания кальция Необычное поведение «Хлопающий» тремор Повышенная мышечная возбудимость Уменьшение экскреции фосфатов Остеодистрофия Кальций сыворотки Почечный рахит Боль в суставах Боль в суставах Бледность Синяки Цвет кожи Анемия Пигментация Уменьшение размеров потовых желез Пигментация Фосфор сыворотки Целостность кожи Мочеполовая Уменьшение активности сальных желез Сухая кожа; отложения фосфатов Повреждение нефронов Зуд Расчесы Экхимозы Экскориации Уремический «иней» Уменьшение диуреза Уменьшение удельного веса мочи Протеинурия Цилиндры и клетки в моче Контроль за количеством принимаемой жидкости и выделяемой мочи Креатинин сыворотки Мочевина сыворотки Электролиты сыворотки Удельный вес мочи Электролиты мочи Также меняется цвет ногтевых лож: появляется темная кайма у свободного края ногтя и за ней — белая полоска. Такое изменение ногтей известно как «ногти Терри». Возможны также другие изменения ногтей, например, появление красных полос (линии Мюрке). Ногти тонкие и ломкие, волосы также ломкие и часто выпадают. Влияние ХПН на дыхательную систему проявляется отеком легких от перегрузки жидкостью; плевритом, особенно на фоне перикардита; и компенсаторным учащением дыхания, направленным на удаление углекислого газа и уменьшение метаболического ацидоза. Отмечается снижение уровней эстрогенов и тестостерона, приводящее к аменорее, бесплодию, уменьшению яичек, импотенции. Снижается либидо, что может быть следствием как физиологических, так и психологических факторов. Нарушение половой функции может стать источником сильных эмоциональных переживаний для пациентов и их партнеров. В табл. 27—3 собраны проявления почечной недостаточности. ч РАБОТА МЕДИЦИНСКОЙ КОМАНДЫ Комплексная помощь пациенту ХПН включает как консервативные мероприятия, так и инвазивные вмешательства, например, диализ, гемофильтрацию и трансплантацию почки. Консервативные мероприятия направлены на облегчение симптомов нарушения водно-электролитного баланса, поражения различных систем организма, а также на назначение оптимальной диеты и поддержание приемлемого качества жизни. Нарушения водного баланса — наиболее ранние проявления почечной недостаточности. У многих пациентов отмечается задержка натрия и воды в тканях, и поэтому возникают симптомы «перегрузки жидкостью» — артериальная гипертензия, застойная сердечная недостаточность и отеки; однако у части пациентов происходит повышенная потеря натрия с мочой и развивается дегидратация. Лечение направлено на поддержание нормального объема циркулирующей плазмы, нормального артериального давления. При перегрузке жидкостью ограничивают прием натрия и воды, применяют диуретики и гипотензивные препараты. Необходимость строго регулировать прием жидкости обычно возникает на поздних стадиях заболевания. В начале заболевания используют тиазидные диуретики, чтобы усилить выделение воды, но эти лекарства становятся неэффективными при скорости клубочковой фильтрации менее 20 мл/мин и приходится назначать петлевые диуретики, например, фуросемид (лазикс). Можно применять многие гипотензивные препараты, в том числе бета-адреноблокаторы, например, пропрано-лол, который может уменьшить выделение ренина. Необходимо устранить электролитные нарушения, такие как гиперкалиемия, чтобы предотвратить аритмии и возможность остановки сердца. На ранних стадиях заболевания, пока суточный диурез составляет не менее 1 л, достаточно ограничить поступление калия с пищей. Пациентов следует предупредить, что многие заменители соли содержат хлорид калия, поэтому от их применения следует воздержаться. Когда уровень калия в сыворотке достигает критического, начинают медикаментозную терапию или диализ (см. обсуждение этого вопроса в главе об ОПН). При почечной недостаточности нарушается экскреция фосфатов и возникает гиперфосфатемия. Так как между уровнем фосфатов и кальция в плазме существует обратная зависимость, то гипокальциемия, обусловленная гиперфосфатемией, стимулирует выделение паратгормона, который приводит к деминерализации костей с поступлением кальция и фосфора в кровоток. Этот порочный круг, включающий гипер-фосфатемию, стимуляцию парашитовидных желез и деминерализацию костей, приводит к остеодистро-фии и возможности вторичного гиперпаратиреоза. В этом случае лечение направлено на поддержание уровня фосфатов, чтобы избежать возникновения порочного круга. Один из методов лечения — назначение гидроксида алюминия в виде геля с пищей. Это средство связывает фосфор в кишечнике и выводит его с калом. Так как гидроксид алюминия может вызвать запор, препарат принимают вместе со слабительным. При продолжительном применении гидроксида алюминия его всасывание в кровь может привести к алюминиевому поражению костей (остеомаляции), а также к алюминиевой энцефалопатии. Поэтому чаще для связывания фосфора вместо лекарств, содержащих алюминий, используют препараты, в состав которых входит кальций в виде карбоната (например, Turns) или ацетата (например, PhosLo), при этом образуются малорастворимые комплексные соединения с фосфатами пищи, которые выделяются с калом. Для коррекции гипокальциемии, которая сохраняется несмотря на снижение уровня фосфатов, назначают активную форму витамина D, кальцитриол, и дополнительный прием кальция с пищей. Превращение витамина D в его активную форму пораженными почками нарушено, поэтому кальций недостаточно всасывается из кишечника. Важно снизить уровень фосфатов до назначения витамина D и препаратов кальция, так как в случае повышения уровней кальция и фосфора происходит отложение этих солей в мягких тканях. Если костные изменения, обусловленные почечной недостаточностью, остаются выраженными, что подтверждается сканированием скелета, то выполняют субтотальную парати-реоидэктомию. Такая мера снизит секрецию паратгормона и вызванную им деминерализацию костей. Метаболический ацидоз обычно поддается коррекции диетой и диализом. Пациенты с ХПН привыкают к сниженному уровню бикарбоната сыворотки, и острой симптоматики не возникает до тех пор, пока уровень бикарбоната сыворотки не упадет до 15-16 мэкв/л. В это время необходим прием бикарбоната или проведение диализа. Ограничение поступления белка с пищей значительно уменьшает уровни азотистых метаболитов в крови. Исследования показали, что поступление белка до 50 г/сут может замедлить прогрессирование почечной недостаточности. Белки, включенные в диету при ХПН, должны иметь высокую биологическую ценность — это яйца, молоко, птица и мясо. При таком питании более эффективно используются незаменимые аминокислоты и образуется меньше азотистых метаболитов. Пониженное поступление белка также ограничивает накопление кислот, фосфора и калия в организме. Как было указано при рассмотрении диетотерапии пациентов с ОПН, большое количество углеводов и жиров в пище дает достаточно калорий, чтобы предотвратить или уменьшить катаболизм. По мере про-грессирования уремии возникают тошнота и рвота. Прием пиши может быть недостаточным для обеспечения потребностей организма, поэтому назначают кормление через зонд или парентеральное питание. При проведении диализа прием белка можно увеличить. Пациентам, которым проводится гемодиализ, прием белка увеличивают до 1 — 1,5 г/кг идеального веса. Нормы белка у пациентов, получающих перитонеальный диализ, можно увеличить даже до 1,5-2 г/кг идеального веса, так как с пери-тонеальным диализатом удаляется достаточно большое количество альбумина. В диете с низким содержанием белка обычно не хватает водорастворимых витаминов, поэтому их необходимо назначить дополнительно. К этой группе витаминов относят: фолиевую кислоту, пиридоксин, комплекс витаминов В и аскорбиновую кислоту. В случае коагулопатии показан прием витамина К. Анемия при ХПН обусловлена разнообразными причинами, в том числе угнетением эритропоэза, уменьшением продолжительности жизни эритроцитов, склонностью тромбоцитов к разрушению и предрасположенностью к желудочно-кишечным кровотечениям в результате уремии. При ХПН обычный уровень гематокрита составляет 16-22%. В медикаментозную терапию таких пациентов обязательно включают фолиевую кислоту или препараты железа. Перо-ральные препараты железа не следует принимать одновременно с антацидами, так как последние уменьшают всасывание железа из желудочно-кишечного тракта. У некоторых пациентов для стимуляции эритропоэза применяют андрогены (тестостерона про-пионат, нандролона деканоат и флюоксиместерон). Однако при длительном употреблении этих препаратов возникают побочные эффекты: у женщин — гирсутизм, изменения голоса, появление акне; у мужчин — увеличение мышечной массы, улучшение половой функции, вплоть до возникновения при-апизма. Благодаря современным генетическим технологиям появился человеческий рекомбинантный эритропоэтин или эпоэтин альфа (эпоген). Этот препарат при ХПН вводят подкожно три раза в неделю в случае, когда гематокрит не превышает 30%. Эпоген можно вводить внутривенно в конце гемодиализа. Клиническое улучшение обычно возникает через 2-6 нед лечения. Наиболее частый побочный эффект этого препарата — развитие или усугубление артериальной гипертензии. Это осложнение обусловлено отчасти гемодинамическими изменениями, связанными с увеличением гематокрита, а также увеличением количества тромбоцитов, обусловливающим состояние гиперкоагуляции. Так как быстрое повышение гематокрита может сопровождаться судорогами, в начале лечения пациентов просят воздерживаться от активной деятельности, например, вождения автомобиля, или работы на тяжелых машинах. Состояние гиперкоагуляции может потребовать гепа-ринотерапии во время диализа для предотвращения свертывания крови в трубках диализного аппарата. Если у пациента нет таких острых симптомов, как одышка, тахикардия, сердцебиение или выраженный упадок сил, то переливание крови не проводят. Если кровь переливают часто, то уменьшается собственная гипоксическая стимуляция образования эритроцитов, а вероятность трансфузионного гепатита возрастает. При трансфузионной терапии введение клеточных компонентов крови уменьшает количество поступающей в организм жидкости, а использование отмытых клеток может уменьшить частоту гепатита и накопление комплексов антиген-антитело. До последнего времени гемотрансфузий избегали, считая, что они могут привести к отторжению почки, если она будет в последующем трансплантирована, из-за сенсибилизации антигенами гистосовместимости. Применение гемотрансфузий перед трансплантацией почки вызывает много споров. Однако у некоторых пациентов при подготовке к трансплантации почки прибегают к гемотрансфузиям, чтобы снизить риск отторжения почки. Поражения кожи включают сухость кожи, зуд и пурпуру. С помощью местного применения мазей или лосьонов удается несколько уменьшить кожный зуд. Применяется облучение ультрафиолетом В. Во многих случаях зуд исчезает после проведения диализа, но иногда эта процедура приводит к обострению зуда. Многие лекарства частично или полностью выводятся почками, поэтому у пациентов с заболеваниями почек необходимо тщательно подбирать дозы, чтобы предотвратить токсическое действие лекарств. С большой осторожностью следует применять нефротокси-ческие препараты, такие как антибиотики и рентгеноконтрастные вещества. Диализ не влияет на уровень дигоксина, но уменьшает уровень калия в сыворотке. Возможность токсических эффектов сердечных глико-зидов, связанных с гипокалиемией, при проведении диализа возрастает, поэтому необходим тщательный мониторинг уровня калия в сыворотке крови. _ Диализ — процесс перемещения жидкости и частиц из одного отсека с жидкостью в другой через полупроницаемую мембрану. Клинически диализ представляет собой механический процесс удаления продуктов белкового обмена, поддержания водно-электролитного баланса и коррекции кислотно-основного равновесия у пациентов с нарушением функции почек. Таким образом, аппарат для диализа становится искусственной почкой (рис. 27-5). Выделяют три основных типа диализа — гемодиализ, перитонеальный диализ и непрерывная гемофиль-трация. Во всех типах диализа один из двух отсеков диализной системы заполняется кровью пациента. При перитонеальном диализе брюшная полость выполняет роль огсека с диализирующей жидкостью, а брюшина действует как полупроницаемая мембрана. В табл. 27-4 приведено сравнение различных типов диализа. Диализ можно использовать в острой фазе почечной недостаточности, а также для поддержания жизни пациента при ХПН до выполнения трансплантации почки. Диализ применяют также в лечении случайных или преднамеренных отравлений в качестве средства, очищающего организм от лекарств или токсинов. При выборе метода диализа учитывается клиническое состояние пациента и неотложность данной процедуры. Метод лечения должен быть составной частью общего холистического подхода к восстановлению здоровья. В настоящее время пациент может выбрать метод из всех имеющихся возможностей диализа, включающих госпитализацию, амбулаторный диализ или диализ на дому. Диализ основан на принципах диффузии, осмоса и фильтрации (рис. 27—6). Диффузия предполагает движение частиц (ионов) из области большей концентрации в область меньшей концентрации. Диффузия при диализе приводит к перемещению электролитов, мочевины, креатинина и мочевой кислоты из крови пациента в диализат. Эритроциты и белковые молекулы слишком велики и не проходят через поры полупроницаемой мембраны, поэтому не выходят из крови в диализат. Осмос предполагает движение воды через полупроницаемую мембрану из области меньшей концентрации растворенных веществ в область большей их концентрации. Рисунок 27-5. Полый волоконный диализатор. Кровь входит через отверстие в верхушке диализатора и протекает по тысячам тонких полых нитевидных волокон (целлофановых капилляров), которые функционируют как полупроницаемая мембрана. Кровь выходит наружу через отверстие в основании диализатора. Диализирующий раствор входит через отверстие в дне диализатора, течет вверх, омывая полые волокна, и выходит наружу через отверстие в верхушке диализатора. Кровь и диализирующий раствор текут одновременно. Стрелки показывают направление тока крови и диализата. Дализат содержит глюкозу, за счет которой концентрация растворенных в нем частиц более высокая, чем в крови пациента, поэтому избыток жидкости перемещается из крови в диализат (рис. 27-7). Чем выше концентрация глюкозы в диализате, тем выше осмотический градиент, усиливающий выход жидкости в диализат из крови. Например, диализирующий раствор, содержащий 4,25% глюкозы, будет «вытягивать» больше жидкости, чем раствор, содержащий 1,5% глюкозы. Фильтрация предполагает движение жидкости через полупроницаемую мембрану в результате искусственно созданного градиента давления. Во время гемодиализа диализатор создает градиент давления, способствующий более эффективному движению жидкости по сравнению с осмосом. При непрерывной артериовенозной гемофильтрации градиент давления для ультрафильтрации создается артериальным давлением самого пациента. Таблица 27-4. Сравнительная характеристика методов диализа. Характеристика Гемодиализ Перитонеальный диализ Скорость Большая (длительность одной процедуры 3-8 ч) Невелика — вначале процедуНевелика — непрерывное ру проводят ежечасно, затем удаление воды и режим меняют: процедура длится электролитов несколько часов или непрерывная Преимущества Быстрая коррекция водноэлектролитных нарушений Предпочтителен для пациентов, Предпочтителен для которые не переносят быстрых пациентов, которые не изменений уровня жидкости и переносят быстрых электролитов; не вызывает изменений уровня жидкровопотери; может применяться кости и электролитов; не немедленно вызывает кровопотери; может применяться немедленно Недостатки Может вызвать быстрые изменения Более медленная коррекция уровня жидкости и электролитов, водно-электролитных нарушений; нарушение электролитного баланса; необходима хирургическая необходим доступ к сосудом; установка перитонеапьного возможна кровопотеря; риск гепатита катетера; риск перитонита; В; необходимо формирование шунта риск перфорации кишки или для выполнения процедуры мочевого пузыря; риск инфицирования места пункции и пункционного канала Необходим Не нужен; поэтому предпочтителен у пациентов с изменениями сосудов; необходим доступ в брюшную полость Не возникают Белок теряется с диализатом (до Доступ к сосудам Потери белка Непрерывная гемофильтра ция Необходим доступ к сосудам; фильтр может разорваться или отсоединиться, вызывая кровопотерю Необходим доступ к артерии и вене Не возникают 1 г/л) Гепаринизация Необходима; системная или местная Незначительная или не нужна Гепаринизация трубок фильтра; минимальная системная гепаринизация Стоимость Высокая Высокая (дороговизна фильтров) Оборудование Сложное Ручная процедура достаточно дорогая; автоматическая — дорогая Для ручной процедуры — простое; для автоматической — сложное Простое Рисунок 27-6. Принципы диализа. А - осмос; Б - диффузия; В - ультрафильтрация: положительный градиент давления; Г - ультрафильтрация: отрицательный градиент давления. Рисунок 27-7. Диализ: результирующее движение жидкости и растворённых веществ при осмосе и диффузии. Диализ начинают в том случае, когда консервативными мероприятиями не удается уменьшить симптомы уремии у пациента с ХПН или при необходимости экстренного воздействия, например, в случае ОПН или передозировки лекарств. Одним из показаний к гемодиализу является снижение клу-бочковой фильтрации ниже 5-10 мл/мин; другим показанием — поддержание уровня остаточного азота мочевины ниже 80-100 мг/дл, а креатинина сыворотки — ниже 8-10 мг/дл. Экстренный диализ необходим для устранения отека легких, гиперкалиемии или других угрожающих жизни осложнений почечной недостаточности. Гемодиализ. Принципиальная схема гемодиализа включает удаление «нефильтрованной» крови пациента; фильтрацию электролитов, мочевины, креатинина и других компонентов с помощью диализа; и возвращение «отфильтрованной» крови обратно пациенту. Чтобы удалять и возвращать кровь, необходим доступ к сосудам. Можно использовать различные методы для доступа к сосудам: канюляцию крупного сосуда (бедренного или подключичного) и введение двух однопросветных катетеров или одного большого двухпросветного катетера, создание хирургическим путем внутреннего или наружного артерио-венозного шунта (рис. 27—8). Помимо доступа к сосудам, для гемодиализа необходимо блокировать свертывание крови, проходящей через диализный аппарат. Для гемодиализа может также потребоваться механический насос, создающий искусственные градиенты давления, с помощью которых происходит фильтрация. Гемодиализ — самый быстрый и поэтому наиболее эффективный вид диализа. Чрескожную катетеризацию бедренной или подключичной вены можно выполнить быстро, но эти катетеры обычно удается использовать для диализа лишь короткое время. Рисунок 27-8. Наружный артериовенозный шунт. Осложнения такой катетеризации включают инфекцию, эмболию, обструкцию сгустками крови и кровотечение. При использовании двух однопросветных катетеров один из них вводят в бедренную вену в дистальном направлении для забора крови, а второй — в проксимальном направлении для возврата крови. Если применяется двухпросветный катетер, то его нижнее отверстие соответствует артериальному концу и предназначено для забора крови, а верхнее — венозному — для возврата крови. Внутренний артериовенозный шунт создают хирургическим путем, анастомозируя артерию и вену. При соединении артерии и вены в результате высокого градиента давления возникает расширение и набухание венозного колена. Артериовенозный шунт недоступен для немедленного использования; однако через 2—6 нед, во время которых происходит «созревание» шунта, расширенное венозное колено можно пунктировать толстыми иглами. Одну из игл устанавливают в выступающий участок вены, и насос проталкивает обогащенную кислородом кровь из вены в диализатор. Возврат крови происходит через иглу, ранее установленную выше первой иглы в ту же вену, или через иглу в другой вене (рис. 27-9). Артериовенозный шунт — это синтетический или сосудистый протез, анастомозированный с артерией и веной, который можно канюлировать толстыми иглами для последующего диализа. Функционирование сосудистого шунта и свища сопровождается сходными осложнениями: тромбозом, кровотечением, инфицированием, образованием аневризм, отеком и ишемией кисти из-за синдрома обкрадывания (артериальная перфузия кисти уменьшается из-за того, что слишком много крови сбрасывается в вену). Так как шунт и свищ укрыты кожей, они менее подвержены инфицированию по сравнению с другими видами сосудистых доступов. Наружный артериовеноэный шунт включает установку отдельных силастиковых канюль в артерию и вену руки или ноги. Свободные концы этих канюль через подкожные туннели выводят на кожу на расстоянии 2-4 см от концов сосудов. В период между процедурами диализа обе канюли соединяют тефлоно-вым коннектором и оставляют его на поверхности. При проведении диализа коннектор удаляют и в просвет канюль вводят иглы. Забирают кровь из артериальной канюли, нагнетают ее в диализатор, а затем возвращают в венозную канюлю. По окончании диализа канюли соединяют трубкой. Возможные осложнения наружного шунта — инфицирование, кровотечение, образование тромба, ишемия и случайное или преднамеренное отсоединение трубки от канюль с последующим кровотечением. Наиболее частые осложнения шунтов — инфицирование и образование тромбов — ограничивают срок использования шунтов, который не превышает 8—10 мес. В настоящее время наружные шунты используются редко. При сформированных сосудистых доступах в виде свища или шунта для проведения гемодиализа необходимо соблюдать осторожность, чтобы не нарушить кровоток в конечности. Пациенту рекомендуют не носить тесную или сдавливающую одежду и во время сна не заводить руку за голову. Над кроватью пациента наклеивают табличку, запрещающую медперсоналу измерять артериальное давление и пунктировать вены на конечности, где расположен сосудистый доступ. Область доступа регулярно осматривают для своевременного выявления признаков инфекции, а при проведении процедуры строго соблюдают правила асептики. Медсестре следует пальпировать и выслушивать область сосудистого доступа и немедленно сообщать врачу при обнаружении дрожания или шума, а также в случае подозрения на тромбоз или закупорку шунта. Рисунок 27-9. Внутренний артериовенозный шунт: А - типы шунтов; Б - вид руки с шунтом; В установлены иглы для диализа. Гемодиализ — сложная процедура, которая требует специальных навыков и знаний от медсестер. Применяются следующие системы для гемодиализа: спиралевидная (редко используется), плоская (параллельная) пластина и полая волоконная система. В плоском пластинчатом и полом волоконном диализаторах на основании баланса двух систем гидростатического давления происходит регуляция скорости и количества удаленной жидкости: в отсеке с кровью — положительный градиент давления, а в отсеке с диализирующим раствором — отрицательный. Независимо от применяемой системы процесс диализа происходит одинаково. В диализаторе отсеки с кровью и диализирующим раствором отделены друг от друга полупроницаемой мембраной. Кровь забирают из артериального колена сосудистого шунта, под давлением пропускают через аппарат со скоростью 100-300 мл/мин и возвращают в сосудистое русло пациента через венозное колено сосудистого шунта. Ди-ализирующий раствор в специальном отсеке подогревают до температуры тела и под давлением пропускают через аппарат в направлении, противоположном движению крови через диализатор, со скоростью 300—900 мл/мин. В артериальном конце в кровь добавляют гепарин, чтобы предотвратить свертывание крови в диализаторе. Если у пациента высок риск кровотечений, то в венозном конце, где кровь возвращается в русло, добавляют протамина сульфат, антагонист гепарина (это средство иногда вводят по окончании диализа). Отсек с диализирующим раствором специально готовят в соответствии с потребностями пациента. Например, для увеличения осмотического градиента и дополнительного удаления воды в отсек добавляют глюкозу, а диализирующий раствор с высокой концентрацией калия используют у пациентов, получающих сердечные гликозиды, для предотвращения ги-покалиемии и дигиталисной интоксикации. При выраженном ацидозе в отсек добавляют бикарбонат или ацетат натрия, которые, попадая в кровоток, метабо-лизируются в ионы бикарбоната, уменьшающие степень ацидоза. Таким образом, изменяя концентрации компонентов диализирующего раствора и гидростатическое давление по обеим сторонам полупроницаемой мембраны, во время диализа можно регулировать количество удаляемой жидкости и метаболитов, а также вводить в организм необходимые вещества. При ОПН может потребоваться ежедневный гемодиализ; однако, как правило, проводится три сеанса в неделю длительностью каждого по 3—5 ч. Пациент с ХПН может выбрать лечение в гемодиализном центре или на дому (если члены семьи или близкий человек владеет техникой процедуры). Примерно 15% пациентов в настоящее время выбирают диализ на дому. Преимущества гемодиализа на дому — психологический комфорт благодаря самостоятельному уходу, а также свободному графику проведения гемодиализа. Продукт современных технологий — портативная переносная искусственная почка, по размерам сопоставимая с чемоданчиком. Диализируюший раствор готовят в домашних условиях, смешивая концентрированный раствор с водой, обработанной в деионизиру-ющей фильтрационной колонке, которую присоединяют к крану в ванной комнате или на кухне. В настоящее время этот метод доступен небольшому количеству пациентов, но дает дополнительные возможности при проведении длительного гемодиализа. Портативный диализатор позволяет пациенту быть мобильным во время гемодиализа, тогда как обычная процедура требует пребывания в постели или в откидном кресле. Большинство пациентов предпочитают во время гемодиализа смотреть телевизор или читать. Многие пациенты думают, что почувствуют себя лучше сразу же после гемодиализа, но в сущности это не так. В большинстве случаев после процедуры возникает небольшой дискомфорт, который исчезает через несколько часов. Наилучшее самочувствие обычно отмечается на следующий день после процедуры. Пациенты после гемодиализа чувствуют себя не лучшим образом по многим причинам. Одно из осложнений первых нескольких сеансов диализа — синдром дисбаланса электролитов, возникающий из-за быстрых изменений в составе внеклеточной жидкости. Такие электролиты, как мочевина и натрий удаляются из крови быстрее, чем из спинномозговой жидкости или головного мозга. В результате высокий осмотический градиент в клетках головного мозга приводит к притоку жидкости в них — возникает отек мозга с соответствующими симптомами: тошнотой, рвотой, головной болью, спутанностью сознания, а иногда и судорогами. Быстрые изменения осмоляль-ности могут также вызвать мышечные спазмы и гипо-тензию. В этом случае уменьшают скорость диализа, вводят маннитол или другой гипертонический раствор, чтобы вывести жидкость из отечных клеток головного мозга обратно в кровеносное русло. Тяжелые проявления синдрома электролитного дисбаланса обычно отмечаются у пациентов с выраженными биохимическими изменениями крови до диализа; однако такие проявления могут отмечаться в той или иной степени во время каждого сеанса гемодиализа — именно поэтому пациенты не чувствуют себя лучшим образом сразу же после гемодиализа. В результате внезапного удаления из циркуляции определенного объема крови возможно возникновение гипотензии и шока. Чтобы избежать этих осложнений, проводят тщательный мониторинг функциональных показателей и регулируют скорость фильтрации. Быстродействующие гипотензивные препараты не следует принимать до окончания сеанса диализа. Другие лекарства, например, нитраты и седативные средства могут спровоцировать гипотензию. Врач и медсестра должны тщательно проверить режим приема лекарств пациентом, чтобы предотвратить возможные осложнения. К другим осложнениям гемодиализа относят мышечные спазмы из-за резких изменений уровня электролитов, возможность кровопотери, сепсис, гепатит и диализную энцефалопатию. ПРАВОВЫЕ ВОПРОСЫ Отказ пациенту в диализе В описываемом случае медсестра была бесконтрактным работником (с ней не был заключен трудовой договор), работала в течение 11 лет, из которых последние 3 года — в отделении гемодиализа. В 1982 г. начальник периодически направлял эту медсестру для проведения диализа пациенту, перенесшему две ампутации конечностей и страдающему многочисленными сопутствующими заболеваниями. Медсестре приходилось дважды прекращать процедуры: один раз — из-за остановки сердца, а второй — из-за выраженного внутреннего кровотечения у пациента во время сеанса гемодиализа. После этих эпизодов медсестра снова была направлена для проведения гемодиализа этому пациенту. Она информировала старшую медсестру о том, что имеет серьезные возражения морального и медицинского плана против проведения этой процедуры пациенту, который находится в терминальном состоянии, а гемодиализ вызовет дополнительные осложнения. Старшая медсестра поручила это задание другой медсестре. В следующий раз, когда этому же пациенту был назначен гемодиализ, медсестра снова отказалась, но старшая медсестра отказалась поручать это задание другому исполнителю. Медсестра побеседовала с лечащим врачом — он сказал ей, что семья пациента настаивает на проведении гемодиализа, без которого пациент не выживет. Медсестра по-прежнему отказывалась проводить это лечение и, несмотря на просьбу администрации, не изменила своего решения. После чего последовал приказ об увольнении этой медсестры. Медсестра подала в суд иск против администрации больницы по поводу незаконного увольнения с работы, утверждая, что администрация больницы не имела права увольнять ее и такое действие является нарушением трудового законодательства. Перед судом был поставлен вопрос — действительно ли в трудовом законодательстве отражены этические принципы медсестры, на которые она ссылается, мотивируя свой отказ, т. е. позволяет ли законодательство медсестре отказаться от лечения пациента, если это заставляет ее идти против своей совести. Суд признал правоту больничной администрации и сделал следующее заявление: Этические принципы человека — это личная, моральная оценка — позволяют медсестре иметь личное, моральное представление, но их не следует возводить до уровня государственной политики, предусматривающей право пациентов получать лечение в больницах, при этом основной процесс лечения осуществляет врач, а назначения врача должны выполняться. Медсестра оспорила решение суда, так как ее отказ проводить диализ пациенту имел юридическое значение в связи с тем, что она следовала Кодексу медсестры. Суд обсудил роль профессиональных этических кодексов в качестве источников государственной политики в случае бесконтрактного приема на работу. Если суд признает, что работодатель нарушил трудовое законодательство, уволив работника (в сущности полагая, что положение о бесконтрактной работе является исключением в законодательстве), то это решение должно быть строго обосновано. Суд постановил, что все уставы и юридические заключения составляются или выносятся на основании законодательства, при этом профессиональный этический кодекс, хотя и ориентируется в целом на трудовое законодательство, может не во всем соответствовать ему. Суд заявил, что этический кодекс, созданный лишь для защиты профессиональных интересов, недостаточен; трудовое законодательство разработано для всего общества в целом и не может содержаться в документе, который определяет стандарт поведения, выгодный лишь отдельной медсестре. Важным для мнения суда стал тот факт, что медсестра никогда не ссылалась на свои обязанности по этическому кодексу, когда говорила старшей медсестре о том, что не будет проводить печение данному пациенту. В сущности, медсестра говорила старшей медсестре, что ею двигали лишь собственные моральные принципы. Кроме того, суд отметил, что и пациент, и его семья просили продолжать гемодиализ, а это — основное право пациента, и лечение не может быть прекращено против его воли. Суд отметил, что эти факты явно перевешивают доводы медсестры, которая считает, что лечение губительно для этого пациента. Позиция медсестры отражает лишь индивидуальные и профессиональные интересы, в то время как пациентам необходимо знать, когда они могут воспользоваться сестринской помощью и могут ли они воспользоваться ею вообще. Более того, кок указывает больничная администрация, будет совершенно невозможно управлять больницей, если каждая медсестра или администратор откажется выполнять свои обязанности, ссылаясь на личные убеждения, касающиеся права на жизнь. Суд заключил: «Отказ медсестры проводить процедуру, возможно, избавлял ее от угрызений совести, но не приносил облегчения ни обществу в целом, ни пациенту, ни его семье». Последняя может возникнуть в результате токсического действия алюминия, представляет собой прогрессирующее неврологическое нарушение и проявляется расстройствами речи, деменцией, миоклоническими судорогами и дискоординацией движений. Токсическое действие алюминия обусловлено наличием алюминия в воде, находящейся в отсеке для диализирующего раствора; приемом антацидов, содержащих алюминий, для снижения уровня фосфатов; уменьшением способности почек к экскреции алюминия. В настоящее время для решения этой проблемы предложены системы очистки воды и новые антацидные средства, связывающие фосфаты. Непрерывная гемофилырация. Непрерывная артериовенозная гемофильтрация — метод лечения острой или хронической почечной недостаточности, использующий для фильтрации собственный артериовенозный фадиент давления пациента. Процедура изображена на рис. 27—10. Как и при гемодиализе, необходим сосудистый доступ — канюляция крупной артерии и вены. Соединительные трубки и фильтр заправляют гепаринизированным физиологическим раствором. В отличие от гемодиализа, специальная аппаратура не используется. Рисунок 27-10. Непрерывная артериовенозная гемофильтрация. Кровь поступает в артериальное колено из системной циркуляции, затем по трубкам идет к фильтру и возвращается в кровоток через венозное колено — все это происходит под действием собственного градиента давления крови пациента. Основу этой процедуры составляет использование высокопроницаемого фильтра из полых волокон (размеры фильтра всего лишь 12,5 на 4,5 см, например, Amicon Diqfilter20). Специальный фильтр удаляет из плазмы воду и все несвязанные вещества с молекулярной массой 500-10 000 дальтон. При этом образуется «ультрафильтрат», который поступает затем в градуированный измерительный прибор, расположенный у края постели пациента, в качестве емкости для отделяемого. Среднего артериального давления 60 мм рт. ст. достаточно, чтобы создать градиент давления, необходимый для образования ультрафильтрата. Чтобы увеличить скорость фильтрации, можно использовать насос. Гемофильтрация микромолекул основана на принципе конвекции — некоторые составные части плазмы переносятся через полупроницаемую мембрану в результате градиента гидростатического давления в системе. Элементы крупнее 10 000 дальтон задерживаются фильтром, поэтому альбумин и другие белки, а также вещества, связанные с белками (например, некоторые препараты), не теряются, а возвращаются пациенту. Частицы промежуточных размеров, например, глюкоза и некоторые витамины, удаляются при конвекции в зависимости от времени, за которое кровь пациента проходит через фильтр. Следовательно, при низкой скорости фильтрации эти вещества могут быть удалены из крови. По эффективности удаления из крови креатинина гемодиализ превосходит гемофильтрацию. Эффективность лечения почечной недостаточности при гемодиализе также выше, чем при гемофильтрации. Так как гемофильтрация проводится непрерывно, она не сопровождается резкими изменениями водноэлектролитного баланса, происходящими при периодическом гемодиализе, и лучше переносится пациентами с нестабильной гемодинамикой (например, страдающими застойной сердечной недостаточностью, резистентной к терапии диуретиками) или пациентами, которым ограничен прием жидкости, но необходимы парентеральное питание или массивная инфузионная терапия. Применение непрерывной ар-териовенозной гемофильтрации возможно только в условиях специализированных отделений, так как необходим тщательный мониторинг функциональных показателей и водно-электролитного баланса. Растворенные вещества, проходящие через фильтр, удаляются в количестве, прямо пропорциональном объему воды в плазме; с небольшим объемом воды уходит небольшое количество растворенных веществ, которые пропускает фильтр. В результате такого процесса концентрация растворенных веществ в крови пациента не меняется. Чтобы уменьшить концентрацию определенных веществ в крови пациента, необходимо заменить удаляемую плазму на раствор, в котором нет этих веществ. Например, пациенту с повышенным уровнем натрия вводят раствор, не содержащий ионов натрия. Потребность во внутривенном введении замещающих растворов уточняется в соответствии со скоростью ультрафильтрации, регулируя которую можно контролировать массу тела и уменьшение объема жидкости. Пациентам, которым проводится непрерывная артериовенозная гемофильтрация, рекомендуют взвешиваться один раз за процедуру. Необходимость в замещающей терапии — еще одно неудобство гемофильтрации. За сутки гемофильтрации объем вводимой внутривенно замещающей жидкости может достигать 24-36 л. Процедура перитонеального диализа ДЕЙСТВИЕ Проверить назначение врача на выполнение диализа Уточнить состав диализирующего раствора, особенно концентрацию глюкозы Добавить лекарства (гепарин или натрия бикарбонат), которые назначены врачом Проверить время «циклов» (каждый час или другой режим) Согреть диализирующий раствор до температуры тела Заправить аппарат диализирующим раствором, наложить зажим на соединительные трубки и в асептических условиях подсоединить их к перитонеальному катетеру Подвесить емкость с диализирующим раствором на стойку, снять зажим с трубок, при этом раствор быстро поступает в брюшную полость; пережать трубки Диализирующий раствор должен распределиться в брюшной полости в течение 30-40 мин, как назначено врачом Следует наблюдать за пациентом, выявляя симптомы дискомфорта, изменения пульса, АД, дыхания Емкость с диализатом опускают, снимают зажим с трубок — диализат вытекает из брюшной полости Измерить количество выделившегося диализата; оценить обьем введенного и вытекшего раствора, определить разницу Повторить все этапы — введение, экспозиция и эвакуация — как назначено врачом ОБОСНОВАНИЕ Чем выше концентрация глюкозы, тем выше осмотическое давление, перемещающее жидкость в диализирующий раствор Врачом могут быть назначены дополнительные лекарства для коррекции электролитного или кислотно-основного баланса; «циклы» диализа могут быть назначены каждый час или в ином режиме Это способствует вазодипатации, выведению шлаков и комфортному состоянию; предотвращает потерю тепла; диализирующий раствор следует согревать, используя сухое тепло, например, сухожаровой шкаф, электрогрелку, микроволновую печь или термостат; согревание диализирующего раствора в теплой ванночке увеличивает риск перитонита; небольшое количество воды при переворачивании и протыкании емкости может пролиться в области отверстия и способствовать проникновению инфекции в систему трубок; соединительные трубки можно легко удалить Необходимо подготовить трубки, заполнить их жидкостью, чтобы предотвратить попадание воздуха в брюшную полость; процедуру проводят в строгих асептических условиях, чтобы не допустить перитонита или инфицирования в зоне стояния катетера Введение диализирующего раствора осуществляется под действием силы тяжести; оно занимает около 10 мин; медленное поступления диализирующего раствора свидетельствует о возможной закупорке катетера В этот промежуток времени происходит диализ Многие пациенты ощущают переполнение живота в то время, когда диализат находится в брюшной полости; нарушения дыхания могут быть обусловлены ограничением подвижности диафрагмы; при любых изменениях пульса, АД, дыхания назначают неотложную терапию Эвакуация диализата обычно занимает 20-30 мин; диализат должен быть без запаха, иметь цвет от прозрачного до желтого; возможно образование пены в нем, обусловленное наличием белков Цель диализа — удаление жидкости и метаболитов; при диализе должен достигаться отрицательный водный баланс Режим диализа поддерживается в соответствии с назначениями врача Непрерывная артериовенозная гемофильтрация может продолжаться до 30-40 дней, но гемофильтр необходимо менять каждые 12-48 часов из-за накапливающихся в нем сгустков крови или снижения фильтрующей способности. В норме полученный ультрафильтрат прозрачный, желтого цвета. Если он становится кровянистым или розовым, то скорее всего произошел разрыв фильтрационной мембраны и фильтр следует заменить. Существует несколько вариантов непрерывной артериовенозной гемофильтрации, например, медленная непрерывная ультрафильтрация и непрерывная вено-венозная ультрафильтрация. А Б В Рисунок 27-11. Три типа катетеров, используемых для перитонеального диализа: А - катетер Тенкхоффа (TenckhoH) с двумя дакроновыми манжетками для фиксации катетера и предотвращения подтекания диализата и его инфицирования. Подкожный туннель — дополнительная мера профилактики инфекции; Б - катетер Gore-tex с дакроновой манжеткой выше фланца; В катетер с манжеткой и широким дисковидным абдоминальным концом. Рисунок 27-12. Перитонеальный диализ в домашних условиях. Перитонеальный диализ. Перитонеальный диализ можно использовать при консервативном лечении как хронической, так и острой почечной недостаточности. При этой форме диализа брюшина пациента служит мембраной, через которую происходит диализ. Перитонеальный катетер хирургическим путем устанавливают между двумя листками брюшины —висцеральным, покрывающим органы брюшной полости, и париетальным, выстилающим стенки брюшной полости. Эт ические аспект ы • Можно ли разрешить умственно отсталому субъекту быть донором почки для своего брата (сестры)? • Каковы действия медсестры при подписании умирающим пациентом согласия на использование своих органов для трансплантации? Что делать, если семья пациента не дает согласие, чтобы его органы использовались для трансплантации? Этические аспекты Диализирующий раствор вводят в полость брюшины, некоторое время выжидают, чтобы раствор равномерно распределился («отстоялся») в ней, при этом происходит диффузия, фильтрация и осмос между кровью пациента и диализируюшимраствором; затем полученный раствор эвакуируют из брюшной полости. Перитонеальный катетер можно ввести в брюшную полость с помощью троакара, но обычно выполняют небольшую операцию, чтобы установить катетер под контролем зрения. Существует множество разновидностей катетеров, но наиболее распространенный из них имеет длину около 25 см и снабжен одной или двумя дакроновыми манжетками, которые располагают в подкожной клетчатке и брюшной полости (рис. 27—11). Манжетки способствуют фиксации катетера и препятствуют проникновению микроорганизмов в брюшную полость через входное отверстие на коже. Перитонеальный конец катетера снабжен многочисленными отверстиями, через которые вводят и эвакуируют диализиру-ющий раствор. Снаружи катетер соединен со стерильной диализной системой, состоящей из емкости для ди-ализируюшего раствора и соединительных трубок. Сразу после введения катетер промывают гепаринизиро-ванным диализирующим раствором, чтобы удалить кровь и фибрин из системы трубок. Некоторые врачи рекомендуют проведение перитонеального диализа сразу после введения катетера в брюшную полость, но другие предпочитают выждать 5-7 дней, чтобы до начала диализа зажила рана в месте установки катетера. Осложнения при установке катетера — инфекция, перфорация кишки или мочевого пузыря, кровотечение. Коричневатое отделяемое по катетеру может свидетельствовать о перфорации кишки, при этом возникает понос и сильная боль. При повреждении мочевого пузыря отделяемое по катетеру окрашено в желтый цвет. Существует три основных типа перитонеального диализа — перемежающийся перитонеальный диализ, непрерывный амбулаторный перитонеальный диализ и циклический непрерывный перитонеальный диализ. Процесс, лежащий в основе этих типов диализа, один и тот же. Удаление жидкости во время диализа зависит от осмотического градиента, создаваемого концентрацией глюкозы в диализирующем растворе. Выпускаются готовые диализирующие растворы в емкостях по 1-2 л, содержащие 1,5%, 2,5% и 4,25% раствор глюкозы. По электролитному составу диализиурющий раствор напоминает плазму. Как и при гемодиализе, в диализирующий раствор можно добавлять различные вещества в зависимости от особенностей состояния пациента. Всегда добавляют гепарин, чтобы предотвратить образование сгустков крови в системе трубок. При диабете в диализирующий раствор добавляют инсулин. Чтобы предотвратить гипотермию, увеличить перитонеальный клиренс и создать комфортное состояние, диализирующий раствор нагревают до температуры тела. Диализирующий раствор вводят в брюшную полость, дают равномерно распределиться, а затем эвакуируют. Время оставления диализата в брюшной полости зависит от типа перитонеального диализа. Максимальные изменения уровней электролитов возникают в первые несколько минут, а через 15-30 мин наступает равновесие. Следовательно, при ручном диализе время экспозиции составляет 20-30 мин, а при автоматической смене циклов диализа — 10—20 мин. При перемежающемся перитонеальном диализе процедуры проводят 3-5 раз в неделю. Длительность каждой процедуры 8-12 ч. Диализ обычно проводят в то время, когда пациент спит. Автоматическое оборудование контролирует время введения и эвакуации диализирующего раствора. Непрерывный амбулаторный перитонеальный диализ предполагает ручное введение и эвакуацию диализирующего раствора пациентом 4-5 раз в день, время экспозиции в течение каждого сеанса от 4 до 8 ч. Например, пациент может вводить 2 л диализирующего раствора в 7:00. Как только раствор введен (это занимает как правило около 10 мин), пациент пережимает трубки, скручивает в трубочку пустую емкость и прикрепляет ее к одежде. В полдень пациент может осуществить следующий цикл — опускает пустую емкость, снимает зажим с трубок, и раствор свободно вытекает из брюшной полости. Для опорожнения брюшной полости необходимо около 10—20 мин. Затем соединительные трубки снова пережимают, емкость отсоединяют и выбрасывают и снова начинают весь цикл перитонеального диализа (рис. 27-12). Активность пациента в период между процедурами не ограничивают. Обычно во время непрерывного амбулаторного перитонеального диализа пациент осуществляет 4 цикла в течение дня и один 8-часовой цикл ночью. Преимущество такого типа перитонеального диализа состоит в том, что не требуется специального оборудования, нет необходимости ограничивать обычную для пациента активность и, что самое важное, непрерывный процесс напоминает нормальное функционирование почек. Поэтому пациенту не назначают особой диеты, не ограничивают прием жидкости — гомеостаз поддерживается достаточно легко. Циклический непрерывный перитонеальный диализ представляет собой комбинацию перемежающегося перитонеального диализа, проводимого в ночное время, и непрерывного амбулаторного перитонеального диализа днем. Таким образом выполняют 3-4 цикла диализа ночью, используя аппарат для перитонеального диализа. При последнем цикле в брюшной полости остается 2 л диализирующего раствора на весь день — этот объем раствора эвакуируют после включения аппарата ночью. Такая система позволяет уменьшить риск инфицирования, так как становится открытой лишь дважды в сутки — один раз утром (отсоединение от аппарата) и один раз вечером (подсоединение к аппарату). При ОПН может потребоваться ручное проведение перитонеального диализа каждый час; однако в этом случае методом выбора является гемодиализ. Осложнения перитонеального диализа — перитонит, нарушение проходимости диализных трубок, боль в животе, кровотечение, электролитные нарушения, аритмии и респираторный дистресс. Перитонит — наиболее опасное осложнение. Боль в животе, лихорадка, перитонеальные симптомы и поступление по дренажам мутного диализата, содержащего большое количество лейкоцитов — признаки перитонита. Возможны также понос, рвота, вздутие живота. В диализирующий раствор добавляют антибиотики и вводят их непосредственно в брюшную полость. Требуется также и системная антибиотикотерапия. Если такое лечение оказывается неэффективным, то перитонеальныи катетер удаляют, а пациенту проводят гемодиализ. Инфекцию в зоне стояния перитонеального катетера обычно вызывают Staphylococcus aureus и Staphylococcus epidermidis. Показана антибактериальная терапия. Если инфекция рапространяется вглубь вдоль катетера, вызывая нагноение подкожного туннеля или формирование абсцесса, то катетер удаляют, абсцесс вскрывают и дренируют. При должном уходе перитонеальныи катетер можно не удалять в течение 18 мес или дольше. Ежедневный уход за катетером включает обработку окружающей кожи раствором антисептика, выявление признаков инфекции (покраснение или экссудация) и наложение сухой стерильной повязки. Трансплантация почки Трансплантация почки представляет собой хирургическую пересадку почки от одного человека другому. Благодаря прогрессу в иммуносупрессивной терапии и в типировании тканей трансплантация стала одним из вариантов лечения ХПН. Почечный трансплантат (аллотрансплантат) можно взять от живого донора или от трупа. От живых доноров в настоящее время берут почки примерно в 25-35% случаев аллотрансплантации, а во всех остальных случаях для трансплантации используют трупные почки. В настоящее время выживаемость в течение года составляет 80-90% после трансплантации почки, взятой от живого донора-родственника, а после пересадки трупной почки — 70—90%. После успешной трансплантации почка обычно нормально функционирует, и реципиент более не нуждается в диализе. Механизм, по которому человек разрешает использовать свои органы для трансплантации после смерти, обеспечивается специальным законодательным актом об использовании донорских органов. Сразу после удаления донорских почек их консервируют и транспортируют в соответствии с поступающими заявками от центров трансплантации. Один из методов консервации почки, позволяющий сохранить ее жизнеспособность в течение 36 ч, заключается в погружении ее в холодный раствор электролитов и помещении в холодильный контейнер для транспортировки. Другой метод — использование специального перфузионного насоса. Прокачивание холодного раствора альбумина и электролитов через почечную артерию уменьшает интенсивность обмена веществ в почке и позволяет сохранить ее жизнеспособность в течение 72 ч. Донорская почка, забираемая как от живого донора, так и от трупа, должна хорошо функционировать, не иметь признаков воспаления; кроме того, у донора не должно быть системных заболеваний, таких как диабет, артериальная гипертензия, злокачественной опухоли, локализующейся вне центральной нервной системы. Исследования у живых доноров-родственников показали, что после взятия почки почечный кровоток и клубочковая фильтрация в единственной оставшейся почке увеличиваются до 70—80% предоперационного уровня, когда функционировали обе почки. Кроме того, суточный клиренс креатинина у доноров в течение 6 лет после взятия почки достигает 87% дооперационного уровня. В настоящее время трансплантацию почки выполняют и пациентам группы высокого риска. Это больные, страдающие сахарным диабетом, перенесшие онкологические операции, юного или пожилого возраста. Противопоказания к пересадке почки — хронические заболевания дыхательной системы, активная фаза инфекции, поздние стадии злокачественных опухолей. Пациентов с системными поражениями сосудов, заболеваниями печени, психическими расстройствами тщательно обследуют. Носителям вируса гепатита В трансплантация не противопоказана, но риск неблагоприятного исхода операции высок. Главное условие успешной трансплантации почки — гистосовместимость между донорским органом и реципиентом. Важные факторы, определяющие гистосовместимость — антигены групп крови АВО и лейкоцитарные антигены человека системы HLA. Вопрос о необходимости переливания донорской крови реципиенту перед трансплантацией спорный, но последние исследования показали, что такие переливания уменьшают частоту реакции отторжения и увеличивают срок жизни трансплантата. Точный механизм этого явления не установлен, но считают, что предварительная сенсибилизация донорской тканью в течение нескольких месяцев перед трансплантацией не только способствует приживлению трансплантата, но и позволяет выявить тех реципиентов, у которых возникнет отторжение донорского органа. Реципиентам трупной почки перед трансплантацией также показаны переливания сходной по эритроцитарным антигенам крови от случайно подобранных доноров. Перед трансплантацией почки реципиент должен быть в наилучшем состоянии здоровья. Не более чем за 24 ч до трансплантации проводят диализ для коррекции водно-электролитных нарушений. Также назначают иммуносупрессивную терапию, чтобы подавить защитные механизмы и уменьшить риск отторжения. При трансплантации почку помешают внебрюшинно в подвздошную ямку. Это наиболее удобное место, так как почка защищена тазовыми костями и легко осуществлять манипуляции на подвздошных сосудах. Почечную артерию анастомозируют с внутренней подвздошной артерией реципиента. Формируют анастомоз между почечной веной и наружной подвздошной веной. Мочеточник донорской почки имплантируют в мочевой пузырь реципиента. Пересаженная почка обычно начинает выделять мочу сразу после восстановления кровотока в ней, но иногда появление мочи задерживается на несколько дней. В послеоперационном периоде может потребоваться диализ, пока функция пересаженной почки не достигнет должного уровня. Если возможно, собственные почки реципиента не удаляют. Считается, что они физиологически активны, поскольку выполняют определенные эндокринные и обменные функции и, следовательно, участвуют в поддержании жизнедеятельности пациента. Эти почки обеспечивают синтез эритропоэтина, регулируют артериальное давление, синтез простагландинов и обмен веществ. Нефрэктомию перед трансплантацией выполняют в тех случаях, когда собственные почки реципиента поражены воспалительным процессом или вызывают выраженную артериальную гипертензию. Главное осложнение после трансплантации почки — отторжение трансплантата. Иммуносупрессив-ная терапия состоит в назначении азатиоприна (имуран) и кортикостероидов. Азатиоприн, ингиби-руя синтез ДНК и РНК, подавляет образование антител. Кортикостероиды уменьшают продукцию антител и препятствуют образованию комплекса антиген-антитело, а также предотвращают миграцию лейкоцитов в трансплантат. Циклоспорин (сандим-мун) был одобрен для использования в трансплантологии в 1983 г. Управлением США по продуктам и лекарствам. Этот препарат специфически ингибиру-ет продукцию антител, способствующих отторжению трансплантата, но не подавляет клетки костного мозга и не нарушает воспалительные реакции в организме. Благодаря своей специфичности циклоспорин значительно увеличил срок жизни трансплантатов даже у пациентов с высоким риском отторжения. Препараты поликлональных антител, например, антилимфоцитарный глобулин и антитимо-цитарный глобулин, можно использовать в период острой реакции отторжения. В настоящее время в лечении острой реакции отторжения вызывают интерес также препараты моноклональных антител. СЕСТРИНСКАЯ ПОМОЩЬ Пациенту с почечной недостаточностью СЕСТРИНСКОЕ ОБСЛЕДОВАНИЕ Сестринское обследование пациента с почечной недостаточностью включает оценку состояния систем органов на основе субъективных и объективных данных. Важно собрать подробный анамнез, выяснить перенесенные заболевания, принимаемые препараты, семейный анамнез, а также тщательно оценить имеющиеся симптомы и синдромы. К почечной недостаточности могут привести некоторые хронические заболевания, такие как сахарный диабет и системная красная волчанка. Необходимо учитывать указания в семейном анамнезе на нефролитиаз или поликистоз почек. Главный фактор развития почечной недостаточности — недостаточная перфузия почечной ткани, поэтому медсестре следует выявить существующие и имевшиеся ранее заболевания почек, которые могут привести к снижению перфузии почечной ткани. Например, эпизод артериальной гипотензии может вызвать снижение перфузии почечной ткани. Гипотензия может быть обусловлена многими причинами, в том числе заболеваниями сердца (застойная сердечная недостаточность, инфаркт миокарда, аритмии). Гипотензию может вызвать также недостаточный объем циркулирующей плазмы в связи с дегидратацией или кровопотерей. Уменьшение объема циркулирующей крови может быть вызвано потерей жидкости в результате рвоты, назогастрального зондирования или диареи. Некоторые препараты, особенно диуретики и другие гипотензивные средства, могут вызвать эпизод артериальной гипотензии. Также необходимо учитывать анафилактические реакции на переливание крови, на лекарства, пищевые продукты или укусы насекомых.ealth nursing К группе риска почечных заболеваний можно отнести пациентов с анамнестическими указаниями на заболевания сердечно-сосудистой системы — поражение периферических сосудов или артериальную гипертензию. Медсестра должна подробно записать сведения о приеме лекарств, так как многие препараты могут быть нефротоксичными. Кроме того, следует оценить, может ли пациент менять свой режим в зависимости от распорядка лечения. Пропуски в приеме назначенных гипотензивных, антиаритмических или сердечных препаратов могут способствовать развитию почечной недостаточности. Также выясняют, принимает ли пациент лекарства, продаваемые без рецепта, так как в них может содержаться натрий, калий и вещества, влияющие на артериальное давление. Следует спросить, употребляет ли пациент заменители поваренной соли, поскольку многие из них содержат калий. Уточняют, нет ли в анамнезе травм живота или недавно выполненной хирургической операции. Как тупая, так и проникающая травма может вызвать почечную недостаточность из-за повреждения почки, кровотечения, инфекции. Женщин расспрашивают о токсикозе беременности или недавно перенесенных абортах. Любая инфекция может вызвать лихорадку с потерей жидкости и дегидратацией. Сепсис может привести к вазодилатации с последующей артериальной гипотензией. Обследуют все основные системы организма, поражение которых может нарушить функцию почек. Исследование сердечно-сосудистой системы включает измерение АД, поскольку как артериальная гипертензия, так и гипотензия способствуют развитию изменений в почках. Сердечные аритмии могут вызвать снижение сердечного выброса и, следовательно, нарушить перфузию почечной паренхимы. Лихорадочные состояния могут привести к дегидратации. Наличие галопирующего ритма S3 или S4 свидетельствует о застойной сердечной недостаточности или гипертонической болезни. Шум трения перикарда — признак уремического перикардита. Осмотрев слизистые оболочки, можно сделать вывод о состоянии водного баланса. При этом обращают внимание на влажность слизистых оболочек. Оценивают тургор кожи, смотрят, нет ли отеков. Прыгающий пульс указывает на перегрузку жидкостью. Напряжение яремных вен — признак повышенного давления наполнения правого предсердия, обусловленного перегрузкой жидкостью или нарушениями сердечной деятельности. Обращают внимание на цвет кожи. Бледность может свидетельствовать об анемии, вызванной снижением продукции эритропоэтина почками. Выделение пигмента урохрома через кожу придает ей желтоватый оттенок. Зуд, пурпура или уремический «иней» на коже — признаки почечной недостаточности. При уремии меняется окраска ногтевых лож. Медсестра может выявить ногти Терри — темная кайма позади свободного края ногтя, за которой следует белая полоска; а также линии Мюрке — красные полосы на ногтях. Пациент может также сообщить о ломкости волос и ногтей. Необходимо исследование дыхательной системы. Почечная недостаточность приводит к перегрузке жидкостью и развитию «мокрого легкого». Наличие хрипов при аускультации указывает на скопление жидкости в альвеолах. Хриплое дыхание — признак скопления секрета в крупных воздухоносных путях. Ослабленные пациенты не могут отхаркивать мокроту из воздухоносных путей. При метаболическом ацидозе, обусловленном почечной недостаточностью, усиливается вентиляция легких. Это способствует удалению избытка углекислоты из организма и нормализации рН крови. При острой перегрузке жидкостью может возникнуть отек легких. В легких влажные хрипы, выделяется пенистая мокрота. Обследование мочеполовой системы включает оценку мочеотделения. Следует выяснить, увеличивается или уменьшается количество выделяемой мочи, стала ли моча темнее, отмечается ли ее помутнение. Потемнение мочи указывает на повышение ее концентрации или на примесь в ней крови. Причиной помутнения мочи иногда бывает появление в ней почечных цилиндров (клеточный детрит, возникающий из-за изменений в почечной фильтрации). При наличии инфекции моча становится мутной из-за присутствия лейкоцитов. Пенистая моча может свидетельствовать о наличии в ней белка. Исследование ЖКТ дает медсестре важную информацию, касающуюся деятельности почек. Из-за уремии у пациента может возникнуть тошнота или рвота. Иногда отмечается анорексия. При уремии пациенты жалуются на металлический привкус во рту, уремический запах от кожи и слизистых оболочек, запах аммиака изо рта. Важно тщательно проанализировать пищевые привычки пациента, выяснить, не изменилась ли масса тела, понимает ли пациент ограничения диеты и может ли им следовать. При неврологическом обследовании можно обнаружить расстройство сознания: спутанность сознания, беспокойство или сонливость могут свидетельствовать об уремии. Важно выслушать членов семьи о психических изменениях у пациента. У многих пациентов отмечаются симптомы периферической нейро-патии (ощущение жжения, зуд или покалывание, особенно в нижних конечностях), которые являются ранними признаками уремии. При гипокальциемии появляются тремор и судорожная активность. Медсестра должна осмотреть также место расположения сосудистого доступа для диализа. Аускультативно в зоне расположения шунта можно выслушать шум, пальпаторно — определить дрожание. Осматривают конечность дистальнее шунта, обращая внимание на периферическое кровообращение — ошупывают пульс на периферических артериях, оценивают кожную температуру и чувствительность. При наличии перитонеального катетера проверяют, нет ли признаков инфекции вокруг него (покраснение, жар, болезненность). Необходимо выяснить график диализа и определить время последней процедуры. Если возможно лабораторное обследование, то следует выяснить, нет ли признаков почечной недостаточности (повышение уровня креатинина, азота мочевины, калия). Часто отмечается метаболический ацидоз. Можно обнаружить изменения на ЭКГ — заостренный зубец Т или расширение комплекса QRS, свидетельствующие о гиперкалиемии. СЕСТРИНСКИЙ ДИАГНОЗ Постановка сестринского диагноза для пациентов с почечной недостаточностью могут включать следующие аспекты: ~ нарушение мочеотделения, связанное с дегидратацией; ~ повышение объема жидкости, обусловленное снижением количества мочи, на фоне ограниченного приема пищи и жидкости; ~ тревога или страх, связанные с исходом заболевания, или стресс, вызванный госпитализацией; ~ невозможность поддерживать здоровье в связи с недостаточными знаниями о новых или сложных методах лечения; ~ невозможность проводить поддерживающую терапию дома в связи с хроническим истощающим заболеванием, недостаточной системой поддержки, недостаточной информацией или финансовой несостоятельностью; ~ риск травм в связи с повышенной кровоточивостью, повышенной утомляемостью, стрессом, склонностью к патологическим переломам; - риск нарушений дыхания из-за перегрузки жидкостью и повышенной утомляемости; ~ нарушения питания: недостаточное поступление питательных веществ, связанное с анорексией; - нарушение целостности кожи, связанное с расчесами из-за зуда; ~ риск инфекции, обусловленный почечной недостаточностью или нарушением иммунитета; ~ низкая толерантность к физической нагрузке вследствие почечной недостаточности, анемии, повышенной утомляемости или периферической нейропатии; ~ ощущение безнадежности или бессилия, вызванные хроническим заболеванием ~ Нарушение схемы тела в связи с хроническим заболеванием и утратой некоторых функций ~ Недостаток в информации о течении заболевания, плане лечения и принципах ухода в отдаленный сроки ~ Изменения чувствительности в связи с водно-электролитными нарушениями - Расстройство половой функции, обусловленные повышенной утомляемостью, снижением либидо ~ Нарушения сна, связанные с госпитализацией или уремией ~ Нарушения мышления, связанные с депрессией или тревогой - Нежелание сотрудничать с медперсоналом, обусловленное сложным, длительным лечением ПЛАНИРОВАНИЕ/ОЖИДАЕМЫЕ РЕЗУЛЬТАТЫ Ожидаемые результаты у пациента с почечной недостаточностью связаны со стадией и тяжестью заболевания почек. Конечная цель — восстановить до приемлемого уровня общее состояние и предотвратить дальнейшее углубление физического и психологического дискомфорта. Ожидаемые результаты включают следующее: ~ поддержание артериального давления, частоты сердечных сокращений и сердечного ритма в приемлемых пределах; - восстановление и поддержание веса; ~ ограничение приема жидкости и определенных продуктов; - прием достаточного количества калорий, чтобы уменьшить распад белка; ~ поддержание целостности кожных покровов ~ применение мер по защите сосудистого доступа (шунт, фистуле, сосудистый протез) или места расположения перитонеального катетера; - понимание своего заболевания и лечебного режима; ~ осознание мероприятий по профилактике возможных осложнений заболевания; ~ способность описать необходимость применения лекарств и методов лечения, и их побочные эффекты; ~ соблюдение рационального режима отдыха и сна, способствующего нормальной активности без стресса и утомления; ~ поддержание оптимального режима диализа, предписанного врачом; ~ выработка эффективных механизмов преодоления; ~ составление плана поддерживания здоровья; ~ отсутствие инфекционных осложнений; ~ сохранение своей роли в семье; ВЫПОЛНЕНИЕ ПЛАНА Прием жидкостей При уходе за пациентами с почечной недостаточностью необходим тщательный учет поступающей в организм и выделяемой им жидкости. Врач назначает лечебные процедуры на основании записей о суточном приеме жидкости и суточном диурезе, а также с учетом массы тела пациента, определяемой ежедневно. Когда пациент находится в критическом состоянии, например, при ОПН, медсестра ведет почасовой контроль за введенной и выделенной жидкостью. Парентеральное введение жидкости осуществляется с помощью насосадозатора, чтобы можно было регулировать ее объем. Если пациенту запрещают прием пищи и жидкости, то необходим тщательный уход за полостью рта. Проблему жажды можно решить, используя кубики льда или орошая ротовую полость пациента водой; в других случаях можно просто смачивать губы. Если прием жидкостей внутрь разрешен, то сведения об ограничении суточного объема жидкостей сообщаются всем сестринским сменам, чтобы пациенту разрешали пить. Медсестра оценивает водный баланс пациента не реже чем каждые 4 ч, основываясь на показателях АД, пульса, частоты дыхания, степени кровенаполнения яремных вен, наличии отеков, состоянии слизистых оболочек. Также необходимо выслушивать легкие и сердце, чтобы вовремя обнаружить S3 ритм сердца или хрипы в легких — признаки перегрузки жидкостью. Отеки обычно в первую очередь появляются в нижних отделах легких и в нижней половине тела — на ступнях и лодыжках, на крестце. У пациентов в критическом состоянии гемодинамические показатели и водный баланс оценивают с помощью датчиков, связанных с сосудистыми катетерами. Когда пациент выздоравливает после ОПН и диурез начинает увеличиваться, необходимо предотвратить дегидратацию, ориентируясь по клиническим признакам (уменьшение массы тела, снижение тургора кожи, тахикардия, артериальная гипотензия, сухость слизистых оболочек, жалобы на жажду). Диета Уремия обычно сопровождается тошнотой, анорексией и неприятным вкусом во рту. В связи с этим питание у пациентов с почечной недостаточностью встречает ряд трудностей. Во многих случаях тошнота и рвота усиливаются утром, поэтому целесообразно построить режим питания так, чтобы он включал легкий завтрак утром и более плотную еду позже. Кроме того, тошнота и рвота встречаются чаше, если пациент принимает пищу в течение одного часа перед процедурой диализа. Режим питания обычно включает ограничение белков, натрия и калия. Желательно, чтобы диета была высококалорийной, богатой незаменимыми аминокислотами и содержала не менее 100 г углеводов ежедневно. Как и во всех случаях, благоприятная обстановка и привлекательный вид пиши способствуют тому, что пациенты следуют необходимым ограничениям в еде и придерживаются оптимальной диеты. Замечено, что комбинация повышенного питания с ежедневным диализом обеспечивает быстрое выздоровление при ОПН. Однако у таких пациентов необходим мониторинг водно-электролитного баланса и тщательный уход, чтобы предотвратить развитие инфекции. Отдых/комфорт Пациенты с почечной недостаточностью обычно быстро устают. Состояние усталости связано не только с сопутствующей анемией, но и с нарушениями сна. Замечено, что пациенты с ХПН страдают нарушениями сна, особенно в ночь перед диализом. Отчасти это связано с тревогой, а отчасти — с высоким уровнем циркулирующих уремических токсинов. Сестринский уход должен быть направлен на помощь пациенту, на обеспечение непрерываемого отдыха и сна. Можно использовать таблички: «Не беспокоить, пациент спит». ^ Рекомендации но питанию Пищевые потребности при заболеваниях почек у взрослых ОСТРЫЕ ЗАБОЛЕВАНИЯ Энергетическая ценность: обычно 30-50 ккал на 1 кг массы тела Белок: 0,6 г/кг идеальной массы тела при отсутствии диализа; на фоне диализа — 1,0-1,5 г/кг Копий: 1000 мг/сут Жидкости: ограничивается выведением жидкости + 500 мл во время олигурической фазы Фосфор: 1-1,2 г/сут Капьций: индивидуально, в соответствии с лабораторными показателями ХРОНИЧЕСКИЕ ЗАБОЛЕВАНИЯ Энергетическая ценность: 30-35 ккап/кг идеальной массы тела Белок: 1-1,2 г/кг идеальной массы тела при нормальном уровне креатинина и нормальной функции почек Натрий: 2-3 r/сут (перитонеальный диализ); 6-8 г/сут Калий: 2-3 г/сут (перитонеальный диализ); 3-4 г/сут Фосфор: 1-1,2 г/сут (перитонеальный диализ); 1,5-2 г/сут Капьций: зависит от уровня кальция в сыворотке Профилактика инфекции и травм Пациенты с почечной недостаточностью особенно подвержены инфекциям из-за нарушений иммунной системы и слабовыраженной воспалительной реакции, поэтому необходимы меры по предотвращению инфекции. По возможности следует избегать установки уретрального катетера, который является «входными воротами» инфекции. Если введение катетера необходимо, то эту процедуру следует выполнять строго в асептических условиях. Так как кожа представляет собой первый барьер, препятствующий проникновению микроорганизмов, необходимо тщательно следить за ней, не допускать ее повреждения. Нанесение на кожу смягчающих веществ уменьшает ее расчесывание и последующее раздражение. Травматизация кожи чаще возникает в отечных участках и над костными выступами. Частая смена положения лежачих пациентов, использование специальных матрасов — важные меры профилактики кожных поражений. Медсестра должна обеспечивать уход за местом сосудистого доступа, строго придерживаясь правил асептики, и выявлять ранние признаки инфекции. При уремии у пациентов отмечается спутанность сознания, поэтому необходимо внимание медсестры, чтобы уберечь их от нанесения себе увечий. Кровать опускают достаточно низко, при необходимости поднимают боковые ограничители. При уходе за такими пациентами важно часто ориентировать их в окружающем пространстве. Психологическая помощь Пациентам с почечной недостаточностью требуется и психологическая, и физическая помощь. При острой почечной недостаточности пациента следует часто информировать о том, что делается все возможное, чтобы восстановить нормальную функцию почки. Пациента может пугать обстановка в отделении интенсивной терапии. Подробные разъяснения очень важны для психологического комфорта пациента и его семьи. При ХПН пациент поставлен перед лицом угрожающего жизни заболевания и неясности будущего, он вынужден постоянно менять образ жизни, и его роль в семье может измениться. Например, если муж долго не в состоянии работать, то функцию кормильца семьи приходится брать на себя жене. Хроническая почечная недостаточность приводит к нарушению половой функции, что угрожает прочности брака и семьи. Может потребоваться консультация сексопатолога. Повышенная утомляемость усугубляет психологический стресс, связанный с хронической почечной недостаточностью. У пациентов может возникнуть депрессия, а низкий уровень качества жизни иногда приводит к суицидальным мыслям. Медсестра играет важную роль, доброжелательно помогая пациенту и его семье выражать и обсуждать свои чувства и заботы. Она может принять на себя долю ответственности за выполнение лечебного плана. Самоконтроль и активное участие в выполнении лечебного плана позволяют пациенту строго придерживаться назначений и повышают его самооценку. Обучение пациента Важный аспект любого плана сестринской помощи — обучение пациента. Процесс обучения основан на теории запоминания звуков. Медсестра оценивает готовность пациента усваивать информацию и разрабатывает инструкции, которые далее приобретают индивидуальные черты. Необходимо выяснить, как пациент усваивал информацию в прошлом и сейчас. Пациент с хроническим заболеванием не только должен быть осведомлен о своей болезни и ее проявлениях, но также должен уметь указать, какое поведение и какие виды деятельности способствуют усугублению симптомов. Важно, чтобы пациенты, получающие массивную медикаментозную терапию, были хорошо информированы о назначенных им лекарствах. Пациента и его семью следует предупредить о необходимости обязательной консультации с врачом перед приемом препаратов, отпускаемых без рецепта. Многие из таких препаратов содержат большое количество натрия. Некоторые средства, например, аэрозоли для носа, содержат вазоактивные вещества, которые могут усугубить артериальную гипертензию. Как пациента, так и его семью необходимо научить определять проходимость сосудистого шунта и распознавать признаки осложнений. В результате уремии снижается уровень сознания, поэтому иногда пациент не может воспринимать инструкции. Необходимо активное вовлечение членов семьи во все аспекты обучения пациента. Предоперационный уход Цель предоперационного ухода — восстановить оптимальный уровень физиологического состояния и обмена веществ у пациента с терминальной почечной недостаточностью. В этих случаях может потребоваться диализ. Необходимо обращать особое внимание на выявление и лечение очагов инфекции до операции и при назначении иммуносупрессивной терапии в дальнейшем. Обязательно предоперационное обучение, как и во всех других случаях. У пациентов, хорошо информированных о хирургической операции и послеоперационном периоде, возникает меньшее количество осложнений и быстрее происходит выздоровление. ПРИНЦИПЫ УХОДА НА ДОМУ ПЕРИТОНЕАЛЬНЫЙ ДИАЛИЗ Существует два вида перитонеапьного диализа, проводимого на дому: непрерывный амбулаторный перитонеальный диализ и непрерывный циклический перитонеальный диализ. При непрерывном амбулаторном диализе процедура выполняется непрерывно в течение суток — Анализирующий раствор вводят в брюшную полость, пережимают трубки на 4-6 ч, а затем содержимое эвакуируют. При этой процедуре используют специальную пластиковую емкость и трубки, которые соединены с катетером, установленным хирургическим путем в брюшную полость. Непрерывный циклический перитонеальный диализ проводят во время сна пациента в течение 8-10 ч. Автоматический диализатор соединяют с перитонеальным катетером, и происходит непрерывное циклическое введение диализирую-щего раствора и его эвакуация из брюшной полости. Эти виды перитонеального диализа основаны на одном и том же принципе. Анализирующий раствор вводят в брюшную полость, оставляют на некоторое время, и через брюшину, которая выполняет роль полупроницаемой мембраны, метаболиты из крови попадают в диализат. Через определенное время содержимое эвакуируют из брюшной полости и вводят новую порцию диализирующего раствора. Это сложный и длительный процесс, поэтому для перитонеального диализа пациентов направляют в специализированные центры, где предоставляют обучение и специальные растворы для диализа, а также проводят динамическое наблюдение и обследование. БЛИЖАЙШИЕ ЦЕЛИ Следует добиться, чтобы к моменту выписки: - пациент понимал суть процедуры перитонеального диализа в домашних условиях и демонстрировал самостоятельное проведение процедуры; - пациент понимал физиологические процессы, лежащие в основе перитонеального диализа; - пациент понимал необходимость ограничений в питании и приеме жидкости; - у пациента было все необходимое для выполнения процедур. ОТДАЛЕННЫЕ ЦЕЛИ ~ Пациент должен уметь выполнять процедуры без осложнений. ~ Процедура включена в образ жизни пациента при наименьших ограничениях ежедневной активности. СЕСТРИНСКОЕ ОБСЛЕДОВАНИЕ Поддержание здоровья. Пациент или помощник должен понимать суть процедуры и необходимость тщательного соблюдения асептики, чтобы предотвратить перитонит; для проведения процедуры нужно иметь достаточное пространство. Питание и обмен веществ. Так как постоянный перитонеальный диализ позволяет регулировать водный баланс и обменные процессы в течение суток, пациенту разрешается обычная диета с умеренным ограничением жидкости. Выделение. Вода и метаболиты выводятся из организма с диализатом. Физическая активность. Хотя перитонеальный диализ не требует особых ограничений физической активности, тем не менее целесообразно обсудить с лечащим врачом допустимые виды деятельности. Половая и репродуктивная функции. Многие пациенты, которым проводится диализ, продолжают вести активную половую жизнь; в некоторых случаях перитонеальный диализ может вызвать повышение половой активности, так как у пациента снижается раздражительность и утомляемость; иногда отмечается снижение полового влечения в связи с основным заболеванием почек; диализ влияет на пациентов по-разному, поэтому все вопросы, связанные с половой жизнью, необходимо решать в индивидуальном порядке. ПЛАНИРОВАНИЕ Выписку пациента, получающего перитонеальный диализ на дому, следует планировать по договоренности с персоналом центра перитонеального диализа. Послеоперационный уход Уход за пациентом после трансплантации почки не отличается от послеоперационного ухода за любым хирургическим больным. Проводится частый мониторинг пульса, АД, частоты дыхания, оценивается количество отделяемого по страховым дренажам. После трансплантации почки пациенты получают иммуносупрессивную терапию, поэтому их изолируют. Все контактирующие с этими пациентами должны тщательно мыть руки. Необходимо наблюдать за изменением водно-электролитного баланса, так как после трансплантации иногда возникает необходимость в диализе, пока пересаженная почка не начнет адекватно функционировать. Кроме того, необходимо следить за появлением симптомов отторжения трансплантата — уменьшение диуреза, отеки, лихорадка, боль и напряжение мышц в зоне пересаженной почки, увеличение массы тела, повышение АД, лейкоцитоз или лимфоцитоз крови. ПРИНЦИПЫ УХОДА НА ДОМУ Продолжение ПЕРИТОНЕАЛЬНЫЙ ДИАЛИЗ .................. ПЛАНИРОВАНИЕ (Продолжение) Пациента следует проинструктировать по вопросам проведения процедуры непрерывного пертонеально-го диализа: - в условиях соблюдения чистоты, используя стерильные материалы, пластиковую емкость со стерильным диализирующим раствором присоединяют к перитонеальному катетеру; - емкость поднимают до уровня плеча или выше; - снимают зажим с трубок, соединяющих емкость и перитонеальный катетер, при этом диализирующий раствор поступает в брюшную полость под действием силы тяжести; - как только пластиковая емкость опустеет, на соединительные трубки вновь накладывают зажим, а емкость сворачивают в трубочку и помещают под одежду или в карман; эта часть процедуры занимает 7-10 мин; - далее пациент может вернуться к своей обычной деятельности, при этом диализат находится в брюшной полости; - когда пройдет установленное время нахождения диализата в брюшной полости (обычно 4-6 ч днем и 8 ч ночью), пациент разворачивает пластиковую емкость и опускает ее ниже уровня брюшной полости; затем снимает зажим с соединительных трубок, и под действием силы тяжести диализат вытекает из брюшной полости в пластиковую емкость; этот процесс занимает 20-35 мин. - емкость с использованным диализатом выбрасывают; - к перитонеальному катетеру присоединяют новый пакет с диализирующим раствором, и весь процесс повторяют; «смена раствора» (время эвакуации диализата из брюшной полости, присоединение в стерильных условиях новой емкости с диализирующим раствором и введение его в брюшную полость) занимает 30-45 мин. Необходимо проинструктировать пациента по поводу симптомов перитонита и нарушений водно-электролитного баланса. Следует проводить постоянный мониторинг водно-электролитного баланса; пациенту объясняют, как определять степень гидратации (измерение массы тела, АД и определение концентрации глюкозы в диализате); может потребоваться ограничение приема электролитов, таких как натрий, калий или фосфаты. Ограничения определенных пищевых продуктов и пищевые потребности должны согласовываться с лечащим врачом; может потребоваться дополнительный прием белка в связи с его потерями при диализе. Пациентов, которым проводится непрерывный циклический перитонеальный диализ, необходимо проинструктировать о работе автоматического диализатора, который используется в домашних условиях; диализатор обычно программируют на 8-10-часовую работу (на время сна пациента); аппарат заливают достаточным количеством диализирующего раствора, чтобы можно было провести необходимое количество циклов диализа; перитонеальный катетер присоединяют к трубкам, и в течение ночи непрерывно проводятся циклы диализа — поступление диализирующего раствора в брюшную полость, затем опорожнение — до тех пор, пока запрограммированный процесс не закончится. ВЫПОЛНЕНИЕ ПЛАНА Когда пациент готов к выписке, все инструкции по уходу, данные ранее, следует уточнить. Пациента необходимо информировать, где будет проводиться динамическое наблюдение, где можно получить расходные материалы для диализа, с кем связаться в экстренной ситуации; если и пациент, и его помощник пожилые люди, то необходимо связаться со службой оказания помощи на дому. ДОКУМЕНТИРОВАНИЕ Больничная медсестра должна записать все мероприятия, связанные с обучением пациента, документировать его знание и умение проделать процедуры самостоятельно, а также переносимость процедуры. Если обучение проводит диализная медсестра, то это также должно быть записано; если медсестру нанимает администрация больницы, то это должно быть отражено в истории болезни; если медсестра, проводившая обучение, приглашена из независимого диализного центра, то больничная медсестра отмечает это, а также указывает ее фамилию и номер телефона. Если пациенту необходимы другие виды медицинской помощи, то следует связаться со службой помощи на дому, чтобы после выписки обеспечить квалифицированное сестринское пособие; все это указывают в документах при выписке. ОЦЕНКА РЕЗУЛЬТАТОВ/ДОКУМЕНТИРОВАНИЕ Оценка эффективности лечебных мероприятий осуществляется непрерывно в процессе их проведения. Учитывают полученные результаты, корректируют план ухода. Действия медсестры эффективны, если удается восстановить и удержать стабильный «сухой» вес, АД в приемлемых границах. Пациенты, которым проводится гемодиализ, должны оберегать место расположения сосудистого доступа. Правильно составленный план сестринского ухода поможет пациенту придерживаться ограничений диеты и приема жидкости. Важно, чтобы пациент был информирован о заболевании и мог описать мероприятия, которые позволяют улучшить состояние здоровья и предотвратить инфекцию. Наконец, пациент должен уметь объяснить необходимость приема лекарств и непрерывного контроля. Разрабатываемый план ухода должен отражать индивидуальные потребности пациента. При уходе за пациентом с почечной недостаточностью чрезвычайно важен учет объема введенной и выделенной жидкости, ежедневный контроль массы тела, пульса, АД, частоты дыхания. Именно на этих данных основывается уход за пациентом и многие специальные лечебные мероприятия. Абсолютно необходимо, чтобы медсестра аккуратно записывала данные физикального обследования пациента и результаты лечения. Наконец, медсестре следует перенести значения функциональных показателей, данные о количестве введенной жидкости и выделенной мочи, лабораторные показатели и сведения о приеме лекарств в диализный или трансплантационный лист. ПРЕЕМСТВЕННОСТЬ УХОДА Реабилитация У пациента, выздоравливающего после ХПН, нормальная функция почек может восстанавливаться в течение года. В последнюю очередь возвращается к норме концентрационная способность почек. До этого времени необходимо, проводить постоянный мониторинг. Необходимы ограничения жидкости и определенных пищевых продуктов. Пока не произойдет полное выздоровление, пациент нуждается в физиологической и психологической поддержке. Такие пациенты должны быть осведомлены о факторах, вызвавших острую почечную недостаточность, чтобы предупредить их повторное воздействие. Кроме того, необходимы лечение других заболеваний, динамическое наблюдение и контрольные обследования, чтобы избежать повторного эпизода ХПН. Длительный уход Пациенты с ХПН сталкиваются с заболеванием, требующим пожизненного лечения, и неопределенностью прогноза. Таких пациентов следует наблюдать непрерывно в течение всей их жизни. По мере прогрессирования заболевания пациента все больше удручает качество жизни. Возникает множество проблем, связанных с эмоциональным стрессом и финансовыми неурядицами. Все это время пациент и его семья нуждаются в поддержке. Следует искать и максимально использовать эффективные стратегии решения проблем пациента. Оптимальный план ухода и лечения должен строиться вокруг индивидуальных потребностей и запросов пациента и его семьи. Уход на дому Диализ на дому — один из альтернативных видов помощи пациентам с ХПН. Он дает возможность оптимального контроля за здоровьем пациента, зависимость которого от медицинских специалистов существенно уменьшается. Пациентов, выбирающих этот вид лечения, следует поддерживать и помогать приспособить домашние условия и свой образ жизни к задачам лечения. Пациенты и их семьи должны всегда иметь возможность получить необходимую им информацию. Медсестры, занимающиеся уходом на дому, могут обеспечить полный объем обследований и вмешательств, необходимых пациенту. Если пациент решил отказаться от лечения, то ему следует обеспечить достойные условия умирания дома, в хосписе или в больнице. Пациент с терминальной стадией заболевания почек находится в критическом состоянии. Если пациент откажется от диализа или ему не удастся подобрать почку для трансплантации, то он умрет. Симптомы терминальной стадии заболевания почек рассмотрены в разделе о ХПН. Они ярко выражены и истощают пациента. Например, отмечается значительная анемия, тяжелый ацидоз, выраженная одышка. Неврологические расстройства проявляются сонливостью или комой. Отмечаются значительные водно-электролитные нарушения. Появляются признаки тяжелой уремии — изменения цвета кожи, кровоточивость, уремический «иней» на коже, тошнота и рвота. Для медсестры важно понять, что пациенты с хроническими истощающими заболеваниями иногда хотят отказаться от лечения, а не вести жизнь, качество которой их не устраивает. Не следует осуждать пациента и его семью за принятое решение, каким бы оно ни было. ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ 1. Каков оптимальный план помощи на дому пациенту, которому проводится непрерывный амбулаторный перитонеальный диализ? 2. Сравните гемодиализ и перитонеальный диализ, перечислите не менее пяти критериев, которые отличают их. 3. Рассмотрите хотя бы один симптом нарушения деятельности сердечно-сосудистой, дыхательной, мочеполовой, пищеварительной, нервной систем, кожу и кроветворения при хронической почечной недостаточности. 4. Разработайте диету с низким содержанием пури-новых оснований для пациентов, у которых образуются уратные камни в почках. 5. Разработайте план обучения пациента, направленный на предотвращение рецидивирующих инфекций мочевых путей. 6. Сравните олигурическую и диуретическую фазы ОПН, используя не менее пяти критериев. 7. Назовите пять симптомов пиелонефрита и опишите действия медсестры, направленные на облегчение или устранение каждого из них. 8. Опишите не менее пяти клинических проявлений уремического синдрома и разработайте по два сестринских вмешательства, осуществляемых по поводу каждого из них. 9. Как вы будете оценивать сестринские вмешательства у пациента с опухолью почки? ЗАБОЛЕВАНИЯ, СОПРОВОЖДАЮЩИЕСЯ ПОРАЖЕНИЕМ БАЗАЛЬНЫХ ЯДЕР При заболеваниях, сопровождающихся поражением базальных ядер головного мозга, возникают два типа неврологических расстройств: с уменьшением объема движений и с избыточной подвижностью. БОЛЕЗНЬ ПАРКИНСОНА ОПРЕДЕЛЕНИЕ Болезнь Паркинсона или паркинсонизм характеризуется двигательными нарушениями, включающими тремор покоя, брадикинезию, ригидность и утрату постуральных рефлексов. Эти расстройства возникают в результате гибели нейронов в базальных ганглиях и других отделах экстрапирамидной системы, а также вследствие дефицита нейромедиаторов. ЭТИОЛОГИЯ И ЭПИДЕМИОЛОГИЯ Заболеваемость болезнью Паркинсона составляет 20 на 100 000 населения в год, а распространенность 187 на 100 000 населения. Около 1% людей старше 50 лет страдают этим заболеванием. Симптомы болезни Паркинсона возникают в 40-70 лет, наиболее часто - в 60 лет. До 30 лет паркинсонизм встречается редко. Мужчины болеют несколько чаше, чем женщины. После появления препарата леводопа (L-ДОФА) смертность от этого заболевания сравнялась с обычной смертностью в этом возрасте. Роль генетических и вирусных факторов в этиологии болезни Паркинсона окончательно не установлена. Предполагают, что важную роль играют эндогенные факторы, поскольку с возрастом количество нейронов, содержащих дофамин, постепенно уменьшается и возрастает их чувствительность к токсинам. Изучение токсических веществ в окружающей среде, в том числе некоторых «кустарных» наркотиков, таких как 1-метил4-фенил-1, 2, 3, 6-тетрагидропиридин (МФТП), привело к разработке новых методов лечения паркинсонизма. Нейротоксический эффект МФТП купируется с помощью ингибиторов моноаминоксидазы (МАО). Изучение токсических свойств природных оксидантов, свободных радикалов и эндогенных дефектов ферментных систем, продолжающееся и в настоящее время, уже привело к успешным испытаниям ингибитора МАО селегилина (элдеприла), замедляющего течение паркинсонизма. ПАТОЛОГИЧЕСКАЯ ФИЗИОЛОГИЯ Механизм формирования нарушений, возникающих при паркинсонизме, прояснился в процессе изучения экстрапирамидной системы (см. рис. 31-2), выявления роли медиаторов, участвующих в связях между черной субстанцией и базальными ганглиями (полосатым телом). Экстрапирамидная система регулирует деятельность многих отделов ЦНС и контролирует произвольную и рефлекторную двигательную активность, поддержание позы, мышечный тонус, координацию движений. В полосатом теле обнаружены медиаторы дофамин, ацетилхолин и гамма-аминомасляная кислота (ГАМК). При паркинсонизме патологический процесс ведет к утрате пигментных клеток в черной субстанции и понижению уровня моноаминергического медиатора дофамина. Уменьшается поступление дофамина от черной субстанции к полосатому телу и в результате снижается тормозное влияние этого медиатора на полосатое тело и усиливается действие активирующего нейроны ацетилхолина (см. жирную линию на рис. 31—2). Нарушение равновесия между ацетилхолином и дофамином ведет к усилению тонической активности альфамотонейронов, которая вызывает сопротивление пассивным движениям, ригидность и брадикинезию. Подсчитано, что для появления симптомов паркинсонизма уровень дофамина в полосатом теле должен снизиться до 20% от нормального. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ Как отмечалось выше, для паркинсонизма характерны одно или несколько двигательных расстройств: ригидность, брадикинезия, тремор покоя, нарушение постуральных рефлексов. При пассивных и активных движениях во всех направлениях наблюдаются скованность и выраженное напряжение мышц. Ригидность и выраженная скованность мышц обнаруживается при пассивных движениях конечностей и ощущается как сгибание свинцовой трубы, а в сочетании с тремором ведет к появлению симптома зубчатого колеса. Брадикинезия или замедление движений может проявляться различным образом. Считается, что это расстройство наиболее устойчиво к лечению. При брадикинезии страдают многие рефлекторные или стереотипные движения: мигание, глотание, движения мимической мускулатуры, содружественные движения рук при ходьбе. Прогрессируя, это расстройство может привести к тотальной акинезии или полному отсутствию движений. Акинезия может наблюдаться при более сложных движениях, например, при одновременном выполнении двух действий (беседе во время ходьбы). Тремор возникает в дистальных отделах конечностей в покое и уменьшается при выполнении активных движений. Паркинсонизм ведет к утрате постуральных рефлексов, в том числе предупредительного постурального рефлекса. При смещении центра тяжести у больных легко возникает движение назад (ретропульсия) или вперед (пропульсия). Утрата рефлексов вместе с характерной для паркинсонизма сгибательной позой часто ведут к появлению шаркающей, семенящей походки, темп которой постоянно нарастает, и пациент как будто догоняет свой центр тяжести. Болезнь Паркинсона развивается медленно и может оставаться незамеченной вплоть до появления тремора. На рис. 31-3 показаны 5 этапов развития болезни. Паркинсонизм вначале поражает одну половину тела, но по мере прогрессирования распространяется на вторую. При этом может наблюдаться снижение когнитивных функций, сопровождающееся брадифренией (замедлением мышления), расстройствами памяти и зрительнопространственного гнозиса. Могут возникнуть слюнотечение, дисфагия, нарушения речи (ускоренная, невнятная, тихая речь), запоры и учащение мочеиспускания. Более чем у 40% больных развивается депрессия, а у 15% - деменция. Часто с возрастом у больных нарастает тревога. Паркинсонизм диагностируется на основании клинической картины. Для выявления излечимых причин этого синдрома используются анамнестические данные, ЭЭГ, КТ, МРТ, сывороточные тесты (соотношение медь/церулоплазмин в сыворотке, общий и биохимический анализ крови). Рисунок 31-2. Наиболее характерные патологические изменения при паркинсонизме Рис. 31-3. Стадии паркинсонизма: А - сгибание пораженной руки; пациент отклоняется в здоровую сторону; Б - медленная, шаркающая походка; В затруднения при ходьбе возрастают, пациент ищет за что удержаться, чтобы предотвратить падение; Г - слабость прогрессирует; при движении пациенту требуется помощь другого человека; Д глубокая инвалидность; из-за нарастающей слабости пациент передвигается в кресле-каталке. РАБОТА МЕДИЦИНСКОЙ КОМАНДЫ Для лечения паркинсонизма попрежнему наиболее эффективны антихолинергические и дофаминергические средства, а также агонисты дофамина. Трансплантация фетальных тканей в полосатое тело остается преимущественно экспериментальной методикой. Диета и физические упражнения ведут к улучшению состояния пациента. Важно также выявлять и лечить другие хронические заболевания, влияющие на качество жизни пациента. Протективная терапия Селегилин (элдеприл), применяющийся для защиты нейронов, пораженных при паркинсонизме, вызвал вторую революцию в лечении этой болезни. Первой революцией было использование леводопы. Лечение элдеприлом можно начать сразу же после постановки диагноза. В таком случае редко возникает необходимость в проведении симптоматической терапии. Использование элдеприла позволяет продлить время, в течение которого леводопу назначают в дозе, которая на 50% меньше обычной. Побочные эффекты элдеприла немногочисленны (см. табл. 31—2). Однако в тех случаях, когда симптомы паркинсонизма препятствуют повседневной активности и ведут к инва-лидизации, необходимо начать симптоматическую терапию. Симптоматическая лекарственная терапия При нерезко выраженной симптоматике заболевания больные могут получать холинолитики и амантадин (симметрел). Холинолитики вызывают задержку мочи, нарушения памяти, дезориентацию и галлюцинации. Эти побочные эффекты затрудняют использование таких средств у пожилых больных. Холинолитики уменьшают проявления заболевания приблизительно на 20%. Амантадин способствует высвобождению дофамина из депо, действуя как непрямой агонист дофамина, и обладает слабым холинолитическим действием. ■ Таблица 31-2. Фармакологический обзор: Симптоматическая и протективная терапия при болезни Паркинсона Препараты Побочные эффекты Действия медсестры Обычная доза* ПРОТЕКТИВНАЯ ТЕРАПИЯ Селегилин (Элдеприл) 5 мг 1-2 раза в сутки (принимать не более 10 мг/сутки) СИМПТОМАТИЧЕСКАЯ ТЕРАПИЯ Холинолитические средства Бензатропин 0,5-4 мг (Когентин) Бипериден (Акинетон) Тригексифенидил (Артан) Профенамин (Парзидол) 1 -2 раза в сутки 2-8 мг 3-4 раза в сутки 1 -4 мг 3-4 раза в сутки 30-40 мг 3-5 раз в сутки Ортостатическая гипотония, другие нарушения со стороны ЦНС, сердечно-сосудистой системы, ЖКТ, мочеполовой системы, дистония, головная боль, половая дисфункция, сыпь Рассказать пациенту и членам его семьи о действии препарата и возможных побочных эффектах. Указать на дозировку препарата и подчеркнуть, что пациент не должен превышать предписанную дозу. Подчеркнуть необходимость вставать медленно из положения лежа или сидя, чтобы избежать ортостатической гипотензии. Характерные для всех холинолитиков: сухость во рту, мидриаз, ухудшение зрения, запоры, задержка мочи, спутанность сознания, психические нарушения Поддерживать гигиену полости рта, увеличить потребление жидкости, использовать жевательную резинку без сахара. Следить и сообщать о появлении побочных эффектов: задержки мочи, снижении остроты зрения, спутанности сознания, тепловом изнурении. Помочь пациенту бороться с запорами (прием достаточного количества жидкое- 1 ти и клетчатки) и ортостатической гипо-тензией (подниматься медленно). Предупредить пациента, что ему нельзя внезапно прекращать прием лекарств, в противном случае возможен токсический эффект. Рекомендовать ежегодное обследование у офтальмолога для своевременного выявления глаукомы. Тошнота, гипотензия. Психические нарушения, гипокинезия, гиперкинезы. Большинство побочных эффектов зависят от дозы. Научить пациента выявлять побочные эффекты и признаки недостаточного или избыточного (передозировка) приема препарата. Предупредить о недопустимости внезапного прекращения приема препарата. Те же, что и у L-ДОФЫ (т.е. нарушения со стороны ЦНС, сердечно-сосудистой системы, ЖКТ Проинформировать о всех тревожных симптомах ДОФАМИНЕРГИЧЕСКИЕ СРЕДСТВА Леводопа (L-ДОФА) 500 мг - 5 г 3-5 раз в сутки Карбидопа/Леводопа 10/100,215/250, (Синемет) 25/100 Т 3-7 раз в сутки АГОНИСТЫ ДОФАМИНА Бромкрипти н (Парлодел) ПЕРГОЛИДА МЕЗИЛЕТ (Пермакс) ДРУГИЕ Амантадин (Симметрел) 2,5-7,5 мг 2-5 раз в сутки 3 мг в сутки (постепенно нарастающая доза) 50-100 мг 2 раза в сутки Те же, что и у L-ДОФЫ (тошнота, гипотензия) Те же, что и у L-ДОФЫ Отеки на ногах Профилактика гриппа При приеме на ночь — бессонница. Сообщать о всех симптомах. Научить пациента: • принимать препарат вместе с пищей; • медленно изменять положение тела. Сообщать о всех симптомах.. Научить пациента: • избегать резкого изменения положения тела; • не прекращать лечение; • принимать препарат вместе с пищей. *В несколько приемов Следующая широко используемая группа препаратов — это дофаминергические средства: леводопа и карбидопа/леводопа (синемет). Леводопа вызывает множество побочных эффектов, поэтому чаще используется сочетание карбидопа/леводопа. Леводофа — это предшественник дофамина, который в отличие от последнего может проходить через гематоэнцефалический барьер. В головном мозге этот препарат преобразуется в дофамин, который взаимодействует с рецепторами в полосатом теле. Карбидофа смягчает тяжелые побочные эффекты дофамина (гипотензию, желудочно-кишечные расстройства), блокируя его разрушение в периферических тканях. Существует пролонгированная, медленно высвобождающаяся форма карбидопы. Агонисты дофамина прямого действия, такие как бромкриптин (парлодел) и, более современный препарат перголид, взаимодействуют с рецепторами дофамина в полосатом теле. Эти средства вызывают такие же побочные эффекты, как и препараты лево-допы. Некоторые врачи рекомендуют назначать бромкриптин на ранних стадиях лечения паркинсонизма, перед использованием сочетания карбидо-па/леводопа. В табл. 31-2 приведены основные препараты, использующиеся при лечении паркинсонизма, их дозы и побочные эффекты. После длительного, более 5 лет, применения до-фаминэргических препаратов и по мере прогресси-рования паркинсонизма реакция пациента на лечение становится менее предсказуемой. Эффективные в прошлом дозы могут вызвать нарастание побочных реакций, таких как дискинезии или галлюцинации. Другую проблему представляет синдром истощения эффекта (феномен «изнашивания»). В таких случаях перед введением очередной дозы препарата снижается подвижность пациента. Это осложнение устраняют более частым введением лекарственных средств, применением селегилина и препаратов леводопы длительного действия. Такие колебания можно устранить внутривенным или интрадуоденальным введением препаратов, однако эти методы не применяются при длительном лечении. Другое непредсказуемое осложнение паркинсонизма — это акинетические пароксизмы (синдром «включения-выключения»), вызванные чрезмерной реакцией на дофаминергические препараты. У пациента наблюдается резкая смена периодов «включения» с нормальной подвижностью, периодами «выключения» с полной неподвижностью. Во время периодов «включения» могут возникнуть непроизвольные движения - дискинезии. В результате наблюдаются колебания выраженности симптомов в течение дня, непредсказуемость которых сильно огорчает пациента. Прием дофаминергических препаратов периодически прекращают («лекарственные каникулы») для того, чтобы восстановить чувствительность рецепторов и реакцию на эти средства. В такие периоды пациент около 10 дней не получает препараты, после чего прием возобновляют в меньших дозах. Поддерживающая терапия Для поддержания сил и активности пациент должен соблюдать диету и выполнять упражнения. Некоторые авторы рекомендуют диету с низким содержанием белка в дневное время и высокобелковую пищу на ночь. Такая диета улучшает поступление ле-водофы в головной мозг в течение дня. При прохождении гематоэнцефалического барьера леводопа конкурирует с другими аминокислотами. Это обусловлено тем, что за определенный период времени в ЦНС может поступить только определенное количество аминокислот. Снижение потребления белка устраняет конкуренцию леводопы с другими аминокислотами за попадание в ЦНС. При прогрессировании заболевания и отсутствии положительной реакции на лечение пациентам показаны помощь логопеда, физиотерапевта и психотерапевта. Такие консультации помогли многим больным стать сильнее и научиться творческому подходу к своим проблемам. В некоторых клиниках для уменьшения тремора производится стереотаксическая таламотомия. Предпринимаются попытки трансплантации клеток надпочечников и фетальной черной субстанции в мозг пациентов для повышения выработки катехо-ламинов в ЦНС, однако явных длительных положительных результатов достигнуто пока не было. СЕСТРИНСКАЯ ПОМОЩЬ Пациенту с болезнью Паркинсона СЕСТРИНСКОЕ ОБСЛЕДОВАНИЕ Сестринское обследование начинается с выяснения степени информированности пациента о его болезни, принимаемых препаратах, а также реакции на терапию. Необходимо выяснить, насколько пациент сохраняет подвижность и как колеблется его состояние на фоне лечения. Например, какую часть времени в состоянии бодрствования пациент сохраняет подвижность. Оценивая физическое состояние пациента, медсестра учитывает двигательную активность, способность выполнять простые действия и повседневные дела. Исследуя двигательную систему, необходимо уточнить, когда в последний раз пациент принял лекарства, поскольку двигательная активность может изменяться от приема к приему. Обследование проводится с учетом особенностей пациента и должно включать как оценку мышечной силы, тонуса, походки, координации движений, речи, проведение пробы на выполнение простых действий (например, встать с кресла, пройти определенное расстояние) с учетом времени их выполнения. Необходимо отметить наличие тремора и насильственных движений. В тяжелых случаях следует оценить питание пациента, его массу тела, акт глотания. Оценивается также половая функция, которая часто нарушается при паркинсонизме. Определить взаимоотношения между больным и членами его семьи можно, выяснив характер их деятельности, общения и способы принятия решений. Изучение домашнего окружения пациента часто помогает выявить проблемы безопасности жизни пациента и необходимость в каких-либо приспособлениях. Регулярно оцениваются когнитивные функции и эмоциональное состояние пациента. СЕСТРИНСКИЙ ДИАГНОЗ При паркинсонизме, как и при многих других дегенеративных заболеваниях, постановка сестринских диагнозов зависит от стадии болезни. Тяжесть состояния пациента может колебаться от минимальной выраженности симптомов до полной неподвижности. Специфическими для паркинсонизма сестринскими диагнозами являются: ~ понижение способности больных к самообслуживанию вследствие замедления движений и мышечной ригидности; ~ повышение травматизма из-за нарушения по-стуральных функций и мышечной ригидности ~ нарушение вербальной коммуникации из-за замедления движений; - нарушение питания: недостаточное поступление питательных веществ, связанное с нарушением координации мышц полости рта и глотки; ~ недостаток знаний, обусловленный сложностью проблемы и колебаниями в схеме лечения^ ~ недостаточная эффективность механизмов преодоления, обусловленная колебаниями выраженности симптомов и прогрессирующим характером заболевания. ПЛАНИРОВАНИЕ/ОЖИДАЕМЫЕ РЕЗУЛЬТАТЫ Основная цель при планировании сестринского ухода заключается в максимальном усилении возможностей пациента и уменьшении его изоляции, которая может сформироваться при хроническом обездвиживающем заболевании. Для пациентов с паркинсонизмом ожидаемые результаты включают: ~ осуществление ухода или руководство уходом за собой; ~ поддержание нормальной подвижности и предупреждение физических травм; ~ поддержание нормальной коммуникации и социальной активности; " поддержание массы тела на уровне, соответствующем возрастной норме (прием достаточного количества пищи для поддержания активности, обеспечивающей нормальную деятельность); ~ способность рассказать о действии принимаемых лекарственных средств и контролировать свою схему лечения; ~ демонстрация осведомленности о болезни, ее лечении и механизмах преодоления, способствующих оптимальному участию членов семьи. ВЫПОЛНЕНИЕ ПЛАНА Пациент с паркинсонизмом госпитализируется на время изменения и коррекции терапии, а также во время «лекарственных каникул». Другими показаниями к госпитализации могут быть только хирургическое лечение или сопутствующие заболевания. Уход за пациентом должен в первую очередь включать оценку эффективности лечения и заботу о нем в периоды беспомощности. Ухаживая за пациентом с паркинсонизмом, медсестра вначале устанавливает режим дня, который пациент соблюдает дома при обычном уходе за собой. В периоды обездвиженности пациенту требуется помощь во время еды, мытья, одевания и естественных отправлений. Особое внимание уделяется соблюдению гигиены. Пациентам со слюнотечением, плохой гигиеной полости рта, потной и жирной кожей требуется ежедневное принятие ванны, мытье головы и очищение рта после еды. Для обеспечения безопасности во время мытья используются поручни, скамейки, нескользкие покрытия, набирается небольшое количество воды, перед тем, как выйти из ванны, ее полностью опорожняют. Использование одежды с крупными застежками «молниями», кнопками или застежками-липучками, а также хорошо подогнанной обуви с резиновой подошвой и низкими каблуками облегчает одевание. По мере улучшения пациенту советуют составлять дневной план своих действий и выполнять эти действия в разумный срок. В рамках обычной повседневной деятельности следует дополнительно планировать прогулку пациента в сопровождении медсестры или кого-либо из членов семьи, чтобы скомпенсировать пониженную активность. Нахождение пациента в одном положении в течение длительного времени повышает ригидность и может усилить дискомфорт. Пациенты, находящиеся на постельном режиме, должны выполнять комплекс активных и пассивных движений не менее трех раз в день. Важный аспект ухода за пациентом - предотвращение падений, особенно, если в течение какого-то периода он был неподвижен или же у него длительное время сохранялись скованность и шаркающая походка. Медсестра должна научить пациента способам усиления сознательного контроля над движениями, например, маршировать большими шагами, мысленно считая при этом, тренироваться в ходьбе, шагая по воображаемой линии, покачиваться из стороны в сторону, чтобы начать движение. Обучение должно включать упражнения на улучшение позы (например, стоять, прижимаясь к стене плечами, ягодицами и пятками). Для того, чтобы уменьшить скованность и тревогу во время периодов «выключения», выполняются упражнения на расслабление, во время которых пациент максимально растягивает и сокращает мышечные группы, слушая специально подготовленную запись. Коммуникационные трудности требуют нескольких подходов. Посоветуйте пациенту делать глубокий вдох перед началом разговора, пользоваться жестами вместо слов и использовать диафрагмальное дыхание. Разговаривая с пациентами, медсестра должна быть терпеливой, поскольку многие больные отвечают медленно. Ригидность мимических мышц часто скрывает истинные чувства пациента, медсестра должна быть внимательной и не принимать гипомимию за отсутствие эмоциональных реакций. Если появляются расстройства памяти, то план по уходу за пациентом должен быть соответственно пересмотрен. При нарушении речи сестра должна учесть возможность столь же выраженных нарушений глотания, поскольку при этом поражаются одни и те же мышцы. Эти нарушения особенно заметны в периоды «выключения». Во время приема пищи следует избегать всего, что может отвлечь внимание пациента, и помочь ему сосредоточиться на процессе еды. Пища должна легко пережевываться, пациенту дают загущенные жидкости и полутвердую пищу, которые легче глотать, чем обычные жидкости. Пациент всегда должен есть в вертикальном положении. При паркинсонизме может отсутствовать кашлевой рефлекс, защищающий от аспирации пищи и жидкости. Может потребоваться отсасывание. Пациенты с избыточной секрецией, слюнотечением и нарушением глотания, которые способны самостоятельно отсосать выделения, могут использовать катетер Янкера. Пациентов регулярно взвешивают. Для лечения запоров, связанных с пониженной моторикой ЖКТ, рекомендуют как можно больше двигаться, выпивать минимум 6-8 (по 250 мл) стаканов воды и добавить к диете грубую пищу, такую как отруби или семя подорожника. Медсестра должна рассказать пациенту и членам его семьи о действии лекарственных препаратов, включая максимальную концентрацию и продолжительность действия, а также побочные эффекты (см. табл. 31-2). Дофаминергические препараты принимаются натощак за 30-60 мин до еды, чтобы улучшить их всасывание. Диета с преобладанием высокобелковой пиши в вечерние часы способствует всасыванию препаратов в течение дня. Суточная схема приема лекарств зависит от распределения активности пациента в течение дня. Если у пациента наблюдаются колебание симптоматики или побочные эффекты, то, основываясь на записи в дневнике, можно установить «виновный» препарат. ОЦЕНКА РЕЗУЛЬТАТОВ/ДОКУМЕНТИРОВАНИЕ При удачно составленном плане пациент контролирует схему приема лекарственных средств и другие аспекты ухода за ним. Пациент и члены его семьи должны показать, что они понимают характер заболевания и план его лечения. Пациент должен поддерживать нормальную массу тела и следить за собой. Он может участвовать в тренировочной программе, составленной с учетом его проблем. Медицинский дневник можно использовать дома или в больнице, чтобы зафиксировать реакцию пациента на препараты, особенно во время корректировки лечения или в периоды, когда его прерывают. Такая информация часто представляет собой эффективный способ активизировать обучение правилам лекарственной терапии. В карте должны быть указаны все препараты, принимаемые больным, обучение упражнениям и соблюдению диеты. Записываются также сведения о нарушениях сна, запорах, расстройствах памяти и депрессии. ПРЕЕМСТВЕННОСТЬ УХОДА Пациент с паркинсонизмом должен часто контактировать с медсестрой, чтобы регулировать прием лекарств и другие аспекты лечения. Для того, чтобы проследить за изменениями в статусе пациента и его реакцией на препараты, часто достаточно телефонного звонка от хорошо информированного пациента. Чем больше пациент и члены его семьи знают о паркинсонизме, тем более вероятно, что они смогут успешно бороться с этим прогрессирующим заболеванием. Важную роль играет долговременное планирование. Согласно статистическим данным, болезнь Паркинсона не влияет на продолжительность жизни, но снижает ее качество. Пациенту важно сохранять активность. Занятия хобби, регулярные прогулки, участие в общественных тренировочных программах и группах поддержки, постоянное общение — все это позволяет дольше сохранить то качество жизни, которое было у пациента до болезни. Постоянный уход требуется только больным с тяжелой деменцией, неподвижностью и ограниченными возможностями.