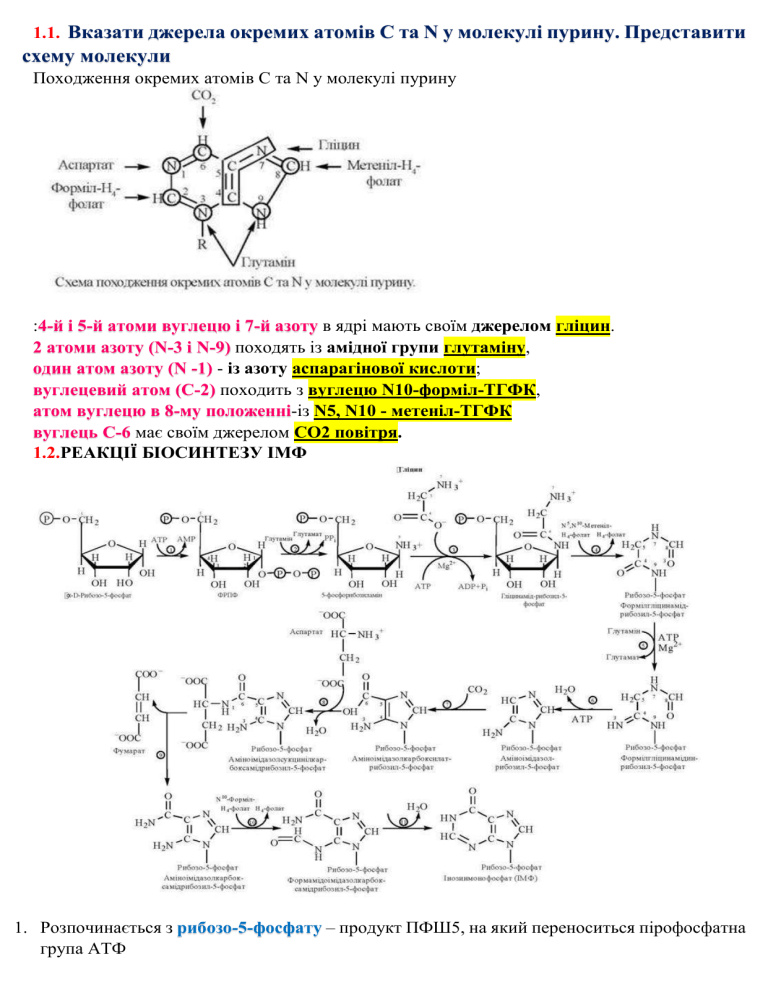
1.1. Вказати джерела окремих атомів С та N у молекулі пурину. Представити схему молекули Походження окремих атомів C та N у молекулі пурину :4-й і 5-й атоми вуглецю і 7-й азоту в ядрі мають своїм джерелом гліцин. 2 атоми азоту (N-3 і N-9) походять із амідної групи глутаміну, один атом азоту (N -1) - із азоту аспарагінової кислоти; вуглецевий атом (С-2) походить з вуглецю N10-форміл-ТГФК, атом вуглецю в 8-му положенні-із N5, N10 - метеніл-ТГФК вуглець С-6 має своїм джерелом СО2 повітря. 1.2.РЕАКЦІЇ БІОСИНТЕЗУ ІМФ 1. Розпочинається з рибозо-5-фосфату – продукт ПФШ5, на який переноситься пірофосфатна група АТФ Фермент: ФРПФ-синтетаза 2. 5-фосфорибозил-1-пірофосфат (ФРПФ) взаємодіє з глутаміном (донор NН2-групи) з утворенням β-5-фосфорибозиламін Фермент: ФРПФ-амідотрансферази в процесі реакції (разом із вивільненням пірофосфату і вільної глутамінової кислоти) відбувається зміна його конфігурації (з α- на β-) це ключова реакція в синтезі пуринів і інгібується за принципом зворотного зв’язку пуриновими нуклеотидами, які утворюються з фосфорибозиламіну 3.Приєднання молекула гліцину до вільної NН2-групи β-5-фосфорибозиламіну (реакція вимагає енергії АТФ) з утворенням гліцинамідрибонуклеотиду Фермент: фосфорибозилгліцинамідсинтетаза 4.Приєднання формільної групи з N5, N10-метеніл-ТГФК з утворенням N-формілгліцинамідрибонуклеотиду Фермент: гліцинамідрибонуклеотидтрансформілаза 5. На формільну групу N-формілгліцинамідрибонуклеотиду переноситься амідна група глутаміну і синтезується N-формілгліцинамідинрибонуклеотид (реакція йде із затратою енергії АТФ) Фермент: N-формілгліцинамідрибонуклеотидамідолігаза 6. Замикання п’ятичленного імідазольного кільце з утворенням 5-аміноімідазолрибонуклеотид Фермент: амідоімідазолрибонуклеотидсинтетаза 7. 5-аміноімідазолрибонуклеотид акцептує СО2 з утворенням рибонуклеотиду 5-аміноімідазол-4-карбоксинуклеотиду Фермент: аміноімідазолрибонуклеотидкарбоксилаза 8. Карбоксильна група рибонуклеотиду 5-аміноімідазол-4-карбоксинуклеотиду взаємодіє з NН2 - групою аспарагінової кислоти з утворенням 5-аміноімідазол-4-N-сукцинілкарбоксіамідрибонуклеотиду (реакція вимагає затрати енергії АТФ) Фермент: аміноімідазолсукцинокарбоксамідрибонуклеотидсинтетаза 9. Вуглецевий скелет аспарагінової кислоти відокремлюється у вигляді фумарової кислоти й утворюється 5-аміноімідазол-4-карбоксамідрибонуклеотид, тобто із аспарагінової кислоти в 1-е положення майбутнього пуринового ядра входить атом азоту. Фермент: аденілсукциназа 10. Останній вуглецевий атом пуринового кільця вмонтовується у вигляді формільного залишка (джерело N10-форміл-ТГФК), який приєднується до 5 - NН2-групи з утворенням 5-формілімідоімідазол-4-карбоксіамідрибонуклеотид Фермент: аміноімідазолкарбоксамідрибонуклеотидтрансформілаза 11. Замикання другого кільця + відщеплення води утворюється перший пуриновий нуклеотид – інозинова кислота (ІМФ) – попередник пуринових нуклеотидів( АМФ чи ГМФ) у складі нуклеїнових кислот. Фермент: інозиніказа 1.3. Представити послідовність реакцій синтезу АМФ, ГМФ, АТФ,ГТФ. УТВОРЕННЯ АМФ ТА ГМФ Інозинмонофосфат - попередником в утворенні інших пуринових рибонуклеотидів — аденозинмонофосфату (АМФ) та гуанозинмонофосфату (ГМФ). Синтез АМФ : 1) заміщення кисню при С-6 пурину на аміногрупу( донором є аспарагінова кислота); проміжний продукт реакції — аденілосукцинат, утворення якого потребує хімічної енергії у формі макроергічного зв’язку ГТФ; 2) розщеплення аденілосукцинату з вивільненням фумарату та утворенням аденозин-5'монофосфату. Синтез ГМФ : 1) окислення вуглецю (С-2) в кільці пурину з утворенням ксантилової кислоти (ксантозин-5'-монофосфату); реакція потребує НАД+ - акцептора водню; 2) заміщення кисню при C-2 на аміногрупу(донором є амідна група глутаміну); + розщеплення 2-ох макроергічних зв’язків АТФ — в результаті реакції утворюється гуанозин-5'монофосфат. Схема утворення аденілової (АМФ) та гуанілової (ГМФ) кислот з ІМФ. Утворення АТФ та ГТФ Перетворення нуклеозидмонофосфатів на нуклеозиддифосфати та нуклеозидтрифосфати реалізується за рахунок макроергічних зв’язків АТФ Фермент 1: нуклеозидмонофосфокіназа Фермент 2: нуклеозиддифосфокіназа Утворення ГТФ з ГМФ: Перетворення АМФ на АДФ Фермент : аденілаткіназа 1.4. Вказати назви метаболітів, ферментів; дати пояснення механізму синтезу пуринових нуклеотидів – de novo; вказати локалізацію цього процесу. Локалізація процесу: головний - печінка, а запасний шлях – у позапечінкових тканинах, де економно повторно використовуються вільні пуринові основи. Зокрема в еритроцитах, лейкоцитах, клітинах головного мозку відбувається утворення нуклеотидів із “готових” вільних пуринових основ — аденіну, гуаніну та 6-оксипурину (гіпоксантину). Механізм більш швидкого біосинтезу пуриннуклеотидів шляхом повторного включення в метаболізм вільних азотистих основ отримав назву “шляху реутилізації”. Реакції повторного використання пуринів для синтезу нуклеотидів: (1) Фермент: аденінфосфорибозилтрансфераза (2) Фермент: гіпоксантингуанінфосфорибозилтрансфераза 1.5. Пояснити і представити у вигляді схеми контроль синтезу пуринових нуклеотидів. Синтез пуринових нуклеотидів регулюється за принципом негативного зворотного зв’язку — кінцеві продукти біосинтетичного шляху (АМФ, ГМФ, АТФ, ГТФ) гальмують певні ферментативні реакції їх утворення. Синтез пуринових нуклеотидів Ф O H2C Ф O O H2C O АМФ АТФ Глн OH ФРДФ-синтетаза O Ф O HO OH 5-Фосфорибозил-1дифосфат (ФРДФ) HO OH Рибозо-5-фосфат Глу ФФн Ф H2C O NH2 O ФРДФамідотрансфераза Ф HO OH 5-Фосфорибозиламін Глі АТФ ФосфорибозилгліцинMg2+ амідсинтетаза АДФ + Фн АДФ + Фн Глу O NH C CH2 HN C АТФ + Н2О Глн NH C C H2 H ТГФК O АТФ + Н2О Гліцинамідрибонуклеотид Амідоімідазолрибонуклеотидсинтетаза Аспартат АТФ N СО2 COOH Н+ C CH H2N C C Гліцинамідрибонуклеоти NH Риб Ф O д-трансформілаза N-Формілгліцинамідрибонуклеотид АДФ + Фн HC NH2 CH2 H ФормілгліцинамідинC NH Риб Ф рибонуклеотидамідолігаз O NH Риб Ф а N-Формілгліцинамідинрибонуклеотид Н 2О N5, N10=CH-ТГФК N Риб ФАміноімідазолрибону- H N C 2 клеотидкарбоксилаза 5-Аміноімідазолрибонуклеотид Mg2+ N CH2-COOH АДФ CH-NH O C COOH C N CH Аміноімідазол-4-NC H N 2 сукцинокарбоксамідN Риб Ф N Риб Ф рибонуклеотидсинтетаза 5-Аміноімідазол-4-NCH 5-Аміноімідазол-4карбоксирибонуклеотид сукцинокарбоксамідрибонуклеотид Аденілосукцинатліаза O O HN HC C N C C Н2О N CH H2N Інозиніказа N Риб Ф Інозинова кислота (ІМФ) O C C C H C HN N CH N К+ 5-Аміноімідазол-4карбоксамідрибонуклеоти Риб Ф д-трансформілаза 5-Формамідоімідазол-4карбоксамідрибонуклеотид Фумарат O N10-CHO-ТГФК ТГФК H2N C H2N C C N CH N Риб Ф 5-Аміноімідазол-4карбоксамід-рибонуклеотид Шляхи синтезу нуклеотидів Схема синтезу АМФ і ГМФ з ІМФ 1. Контроль ранньої стадії синтезу пуриннуклеотидів реалізується двома механізмами: 1.1. Шляхом зменшення при дії АМФ та ГМФ активності ферменту, що перетворює α-Dрибозо-5-фосфат на 5-фосфорибозил-1-пірофосфат (ФРПФ) — 5-фосфорибозил-1-пірофосфатсинтетази. 1.2. Шляхом інгібірування при дії ІМФ, АМФ та ГМФ активності регуляторного алостеричного ферменту, що перетворює ФРПФ на 5-фосфорибозиламін — глутамін-ФРПФ-амідотрансферази; це — найважливіший пункт контролю швидкості всього біосинтетичного шляху. 2. Контроль пункту розгалуження в синтезі пуриннуклеотидів, тобто перетворення ІМФ на АМФ та ГМФ відбувається за такими механізмами: 2.1. АМФ гальмує власне утворення з ІМФ шляхом інгібірування активності ферменту аденілосукцинатсинтетази, який перетворює ІМФ на аденілосукцинат; 2.2. ГМФ гальмує власне утворення з ІМФ шляхом інгібірування ферменту ІМФ-дегідрогенази, який перетворює ІМФ на ксантозинмонофосфат. 2.3. АТФ та ГТФ є джерелами метаболічної енергії для синтезу один одного: АТФ необхідний для перетворення ІМФ на ГМФ (та ГТФ), тоді як ГТФ необхідний для перетворення ІМФ на АМФ (та АТФ); тому збільшення (зменшення) концентрації кожного з нуклеозидтрифосфатів призводить до відповідних змін у швидкості утворення іншого нуклеозидтрифосфату, що забезпечує їх координований синтез. 2.1. Вказати джерела окремих атомів С та N у піримідиновому кільці. Метаболічними попередниками атомів вуглецю та азоту в молекулах піримідинів є амінокислота L-аспартат та карбамоїлфосфат 2.2. Синтез піримідинових нуклеотидів Відбувається шляхом приєднання пентози у формі 5-фосфорибозил-1-пірофосфату вже після утворення піримідинового циклу з попередників із лінійним ланцюгом. Локалізація: цитозоль клітин із взаємодії СО2, NН3 і аспартату. СО2 Глн 2 АТФ Mg COOH CH2 NH2 2 АДФ + ФН Глу C O 2+ Карбамоїлфосфатсинтетаза O Ф + Карбамоїлфосфат CH-COOH H2N Аспартат Аспартаткарбамоїлтрансфера за O COOH NН2 ФН Н2О CH2 НАД+ CH2 HN CH-COOH CH-COOH Дигідрооротаза O N N H H N-карбамоїласпарагінова Дигідрооротова кислота кислота O C CH ФРДР ФФН CH-COOH ОротатфосфоN рибозилтрансфераза H Оротова кислота O Дигідрооротатдегідрогеназа O O HN НАДН + Н+ СО2 CH HN O O N CH-COOH ОМФ-декарбоксилазаO Рибозо- Ф Оротидин-5'-фосфат (ОМФ) CH HN N CH Рибозо- Ф Уридин-5'-фосфат (УМФ Схема синтезу УМФ І стадія синтезу УМФ - утворення карбамоїлфосфату з глутаміну Каталізатор: цитоплазматична карбамоїлфосфатсинтетаза II стадія: Утворення N-карбамоїласпарагінової кислоти з карбамоїлфосфату та аспартату ІІІ стадія: N-карбамоїласпарагінова кислота піддається циклізації з утворенням дигідрооротової кислоти Каталізатор: дигідрооротаза відщепленням молекули води ІV стадія: Дегідрування дигідрооротової кислоти з перетворенням на оротову кислоту НАД-вмісний фермент: дигідрооротатдегідрогеназа V стадія: Оротова кислота реагує з ФРПФ (5-Фосфорибозил-1-пірофосфат) (донор рибозо-фосфату) з утворенням оротидин-5’-фосфату (ОМФ) Каталізатор: УМФ-синтаза VІ стадія: Декарбоксилювання оротидин-5’-фосфату (ОМФ) з утворенням піримідинового нуклеотиду - УМФ. УМФ УДФ і УТФ здійснюється, як і в пуринових нуклеотидів, шляхом фосфотрансферазних реакцій: Утворення УДФ: Каталізатор: Нуклеозидмонофосфаткіназа (НМФ-кіназа) УМФ + АТФ → УДФ + АДФ Утворення УТФ: Каталізатор: нуклеозиддифосфаткіназа (НДФ-кіназа) УДФ + АТФ → УТФ + АДФ Амінування УТФ з утворенням ЦТФ беруть участь глутамін (донор аміногрупи) та АТФ: АТФ-залежне заміщення кетогрупи урацилу на амідну групу глутаміну з утворенням цитидин-5’-трифосфату (ЦТФ): Фермент: ЦТФ-синтетаза УТФ + Глн + АТФ → ЦТФ + Глу + АДФ + Фн У прокаріот у цій реакції використовується переважно вільний аміак, тоді як в тварин ЦТФсинтетаза каталізує включення амідної Глутамін (NH3) + CO2 + АТФ + аспартат групи глутаміну в 4-е положення піримідинового кільця УТФ. Оротова кислота Рибозо-5-фосфат 1 ОМФ 2 Глутамін СО2 Глутамат УТФ УМФ Урацил ЦТФ Цитозин ЦМФ NH3 !!!Утворений ЦТФ служить негативним ефектором регуляторного алостеричного ферменту аспартаткарбамоїлтрансферази, інгібуючи за типом зворотного зв’язку початкову стадію біосинтезу піримідинових нуклеотидів, АТФ гальмує це інгібування. Частина ЦМФ УМФ Фермент: цитидиндезамінази Дигідроурацил b - Aланін СО2 + NH3 Сечовина Рис. 7.10. Схема метаболізму піримідинових нуклеотидів: 1, 2 - дефекти ферментів при оротацидурії 2.3. Регуляція синтезу піримідинових нуклеотидів 2 регуляторні ферменти: 1. карбамоїлфосфатсинтетази, активність якої Глутамін (-NH ) + CO посилює ФРПФ, а алостеричними інгібіторами виступають УТФ – кінцевий продукт біосинтетич1 АТФ ного процесу та пуринові нуклеотиди; + ФРПФ 2. аспартаткарбамоїлтрансферази, активатоКарбамоїлфосфат Аспартат ром якої слугує АТФ, а алостеричним інгібітором 2 виступає ЦТФ. Уреїдосукцинат Значення: запобігання надлишковому синтезу не Оротат ФРД лише УМФ, а й усіх інших піримідинових нуклеоФ ОМФ тидів і забезпечення збалансованого утворення всіх УМФ 4-ьох основних пуринових і піримідинових нуклеоУТФ тидів, необхідних для синтезу РНК. 2 2 ЦТФ дТТФ Рис. 7.11. Схема регуляції синтезу піримідинових нуклеотидів РЕГУЛЯЦІЯ СИНТЕЗУ ПІРИМІДИНОВИХ НУКЛЕОТИДІВ РЕГУЛЯЦІЯ СИНТЕЗУ ПУРИНОВИХ НУКЛЕОТИДІВ 2.4. Оротацидурія Спадкове порушення синтезу оротової кислоти характеризується утворенням надлишку оротової кислоти Кількість виведеної оротової кислоти в складі сечі при цьому може зростати до 1,0 – 1,5 г , що в 1 000 разів перевищує норму. Оротатацидурія І типу порушення піримідинового обміну зумовлене дефіцитом 2-ох ферментів: оротатфосфорибозилтрансферази, яка каталізує перетворення оротату на оротидилат декарбоксилази, що каталізує перетворення оротидилату на уридинмонофосфат. Клінічний прояв: Діти народжуються нормальними, але впродовж першого року життя в них розвивається мегалобластична анемія, згодом вони відстають у рості і розумовому розвитку. У сечі виявляють кристали оротової кислоти помаранчевого кольору (помаранчева кристалоурія). Захворювання ставить дітей у залежність від зовнішніх джерел уридину. Вживання уридину чи цитидину зменшення утворення й екскреції оротової кислоти, відновлює нормальний ріст і розвиток. Таке лікування повинно продовжуватися впродовж усього життя. Оратацидурія ІІ типу розвивається при нестачі тільки 1-ого ферменту – оротидин-5-фосфатдекарбоксилази Клінічний прояв: У таких пацієнтів у сечі виявляють оротидин на відміну від І типу патології, при якій більшою мірою екскретується оротова кислота. Вторинна оротова ацидурія (синдром Рейє) виникає при пошкодженні мітохондрій печінкипорушується утилізація карбамоїлфосфату, він включається в цикл синтезу оротової кислоти. Лікування подагри алопуринолом симптоматична оротацидурія, так як його метаболіти інгібують О-5-ФДК. При порушенні орнітинового циклу нагромаджується карбамоїлфосфат, який використовується в синтезі УМФ 3.1. Синтез дезоксирибонуклеотидів *відбувається в клітинах, котрі вступають у S-фазу клітинного циклу та готуються до синтезу ДНК та поділу. Біосинтез РНК *вимагає наявності пуринових (АТФ, ГТФ) та піримідинових (ЦТФ, УТФ) рибонуклеотидів Для біосинтезу генетичних ДНК необхідні дезоксирибонуклеотиди пуринового — дАТФ, дГТФ — та піримідинового — дЦТФ, дТТФ (ТТФ) ряду. Попередники дезоксирибонуклеотидів - рибонуклеотиди у формі нуклеозиддифосфатів (НДФ) (переважно) та нуклеозидтрифосфатів (НТФ). Механізм перетворення рибонуклеотидів на дезоксирибонуклеотиди Відновлення гідроксильної групи при С-2' рибози з утворенням 2'-дезоксирибози Перетворення НДФ(нуклеозиддифосфатів) на відповідні дНДФ Донор відновлювальних еквівалентів : відновлений НАДФ (НАДФН + Н+): !!!Обов’язкова наявність рибонуклеотидредуктазного комплексу: власне рибонуклеотидредуктаза (РНР) білок тіоредоксин тіоредоксинредуктази Функція: відновлення рибози в 2-дезоксирибозу, що вимагає наявності 2 ат. Н2 (їх джерело - відновлений термостабільний білок тіоредоксин, що містить 2 вільні SН-групи на 108 амінокислотних залишків. Окиснення тіоредоксину з утворенням дисульфідного містка за участі РНР Фермент: тіоредоксинредуктаза ФАД-вмісний (вимагає наявності відновленого НАДФН) Утворення дезоксирибонуклеотидів *рибонуклеозиддифосфат(РДФ) Тіоредоксин-(SH2) + РДФ Рибонуклеотидредуктаза Тіоредоксин-(S2) + НАДФH + Н+ Тіоредоксинредуктаза Тіоредоксин-(S2) + дРДФ Тіоредоксин-(SH2) + НАДФ+ тіоредоксинредуктаза + рибонуклеотидредуктаза = електроно-транспортний ланцюг відновлення НДФ до дНДФ: (1) переносу водню від (НАДФН + Н+) на ФАД флавінового ферменту тіоредоксинредуктази; (2) переносу водню від відновленої тіоредоксинредуктази на SH-групи тіоредоксину; (3) переносу водню від відновленого тіоредоксину на SH-групи рибонуклеотидредуктази; (4) переносу водню від відновлених сульфгідрильних груп рибонуклеотидредуктази на НДФ з утворенням дНДФ. 3.2. Біосинтез тимідилових нуклеотидів Утворення тимідин-5’-монофосфату (дТМФ) з дУМФ (метилювання урацилу) Каталізатор: тимідилатсинтаза O HN Н O O P O OН O CH2 H H C C N НАДФ+ C CH N5, N10-СН2-ТГФК ДГФК Тимідилатсинтаза H H OH дУМФ HN НАДФН O H O ТГФК O НO P O OН O CH2 H C C N C CH3 CH O H H H OH дТМФ H Донор метильної групи : N5,N10-метилен-ТГФК - віддає протон(2 молекули Гідрогену)одним з кінцевих продуктів реакції є не тетрагідро-, а дигідрофолієва кислота (ДГФК). Відновлення дигідрофолієвої кислоти до ТГФК Фермент: НАДФН-залежна дигідрофолатредуктаза Фосфотрансферазна реакція: дТМФ (Тимідин-5’-монофосфат) дТДФ + ТТФ Дефосфорилування дУДФ/ гідролітичне дезамінування дЦМФ утворення дУМФ (субстрату тимідилатсинтазної реакції) Фермент: дЦМФ-дезаміназа «Запасний» шлях синтезу дезоксирибонуклеотидів Відбувається в тих клітинах, які здатні до швидкого поділу Функція: забезпечує повторне використання тиміну та дезоксицитидину Тимін + Дезоксирибозо-1-фосфат тимідин + Н3РО4 Фермент: тимідинфосфорилаза Утворення дТМФ: Тимідин + АТФ дТМФ + АДФ Фермент: тимідинкіназа Дезоксицитидин + АТФ дЦМФ + АДФ Фермент: Дезоксицитидинкіназа 3.3 Пояснити механізм дії протипухлинних засобів - структурних аналогів дТМФ, похідних птерину: Біосинтез нових 4-х дезоксирибонуклеозидтрифосфатів (дАТФ, дГТФ, дЦТФ та дТТФ), що необхідні для реплікації ДНК не відбувається у фазі G0. У зв’язку з цим, хімічні сполуки, які блокують синтез de novo зазначених дНТФ, унеможливлюють подвоєння ДНК та поділ клітин — концепція, що покладена в основу фармакологічної дії багатьох протипухлинних лікарських засобів. Саме за таким механізмом реалізується затримка поділу клітин злоякісних пухлин, яка відбувається під впливом препаратів, що блокують синтез тимідилату дТМФ: 1) структурних аналогів дУМФ, що здатні до взаємодії з тимідилатсинтазою (блокуючи її каталітичну дію за мех. конкурентного інгібірування); Прикладом є ефект протипухлинних засобів антиметаболітної дії 5-Фторурацилу (аналога урацилу) та Фторафуру (аналога уридину, що в організмі людини також утворює вільний 5-фторурацил): Після надходження в організм 5-фторурацил перетворюється на 5-фтордезоксиуридин-5'монофосфат (5-фтор-дУМФ), тобто безпосередній структурний аналог дУМФ — субстрату тимідилатсинтази; сполучення 5-фтордУМФ з ферментом протидіє зв’язуванню активного центру останнього із справжнім субстратом (дУМФ), що блокує утворення дТМФ; 2) похідних птерину Аміноптерину та Метотрексату, що, маючи подібність до частини молекули фолієвої кислоти, діють як її структурні аналоги → виступають як конкурентні інгібітори дигідрофолатредуктази; гальмування каталітичної дії цього ферменту протидіє регенерації Н4-фолату з Н2-фолату → порушує біосинтез дТМФ. Інгібітори синтезу дТМФ як протипухлинні препарати. Деякі структурні аналоги пуринів, піримідинів і фолієвої кислоти є інгібіторами синтезу дезоксирибонуклеотидів (блокують реплікацію ДНК і поділ клітин). 5-фторурацил та фторафур (аналог уриO F дину, що в організмі людини також утворює HN вільний 5-фторурацил) діє за механізмом N O H конкурентного інгібування. 5Фторурацил В організмі 5-фторурацил 5-Фтор-дУМФ 5-Фтор-дУМФ Фермент:оротатфосфорибозилтрансфедТМФ дУМФ раза E /через проміжне утворення нуклеозиду з подальшим фосфорилуванням. Перетворюючись на нуклеозиддифосфат, N ,N -метилен-H F HF 5-фторурацил може брати участь у реакції, Гліцин яку каталізує РНР, і відновлюватися до Н + НАДФН відповідного дезоксипохідного. Серин E 1 5 10 4 2 + H4F (ТГФК) 2 Під впливом фосфатази 5-Фтор-дУМФ втрачає фосфат і утворений при цьому 5Рис. 7.15. Механізм Фтор-дУМФ зв’язується з тимідилатсинпротипухлинної дії сполук, що тазою та N5,N10-метилен-Н4-фолатом блокують синтез дТМФ: Е1комплекс схожий на проміжну сполуку в тимідилатсинтаза; Е2реакції перетворення дУМФ на дТМФ. дигідрофолатредуктаза; Н4FТимідилатсинтаза заблоковується, а синтез дТМФ припиняється. тетрагідрофолатповністю (ТГФК); H2F- цитозинарабінозид дигідрофолат ФК(цитарабін) – у ньому залишок рибози заміщений на стереоізомер – арабінозу. Використання препарату: хіміотерапія раку( при гострій мієлоцитарній лейкемії). В організмі препарат може перетворюватися на дНТФ, інгібувати ДНК полімерази та знижувати швидкість реплікації. Структурні аналоги фолієвої кислоти - аміноптерин та метотрексат - конкурентні інгібітори дигідрофолатредуктази, порушують синтез пуринових нуклеотидів і перетворення дУМФ на дТМФ, знижуючи тим самим внутрішньоклітинну концентрацію субстратів синтезу ДНК і РНК. Їх широко застосовують у хіміотерапії пухлин. НАДФ Аміноптерин Метотрексат 4.1,2 Написати реакції розпаду пуринових нуклеотидів з утворенням сечової кислоти, зазначити ферменти, що каталізують ці реакції: Джерелом вільних пуринових та піримідинових нуклеотидів є розщеплення власних НК гідролітичними ферментами ДНК-азами та РНК-азами та біосинтез нуклеотидів в тканинах. Вільні нуклеотиди, які не використовуються для синтезу НК, підлягають розщепленню з утворенням кінцевих продуктів азотистого (нуклеїнового) обміну. Розщеплення пуринових нуклеотидів (АМФ та ГМФ) включає реакції: I. Відщеплення фосфатної групи з утворенням нуклеозидів аденозину та гуанозину ФЕРМЕНТ 5'-нуклеотидаза II. Дезамінування на рівні аденозину (ФЕРМЕНТ аденозиндезаміназа) або на рівні гуаніну (ФЕРМЕНТ гуаніндезаміназа); III. Відщеплення від нуклеозидів пентозного залишку D-рибози (ФЕРМЕНТ нуклеозидаза) або пентозофосфату в цілому (ФЕРМЕНТ фосфорилази); IV. Подальший катаболізм гіпоксантину (що утворився з АМФ) або ксантину (що утворився з ГМФ) з утворенням кінцевого продукту сечової кислоти (2,6,8-триоксипурину) ФЕРМЕНТ ксантиноксидазою. Ксантиндегідрогеназа — ФАД-залежний флавопротеїн, який окислює пурини до сечової кислоти; містить у своєму складі також іони заліза та молібдену. В ксантионоксидазних реакціях як окисник використовується молекулярний кисень О2, який відновлюється до перекису водню: гіпоксантин + О2 + Н2О → ксантин + Н2О2; ксантин + О2 + Н2О → сечова кислота + Н2О2. Описати відмінності катаболізму пуринів у різних видів тварин 4.3 Підтриманню розчинного стану уратів в організмі людини сприяє їх зв’язування з білками крові. гіперурикемія — щонайменше збільшення вмісту сечової кислоти в крові; супроводжується випадінням у тканинах кристалів уратів, що клінічно проявляється розвитком подагри. Подагра захворювання, основним проявом якого є розвиток важкого больового синдрому внаслідок відкладення кристалів уратів у порожнинах суглобів та розвитку процесу запалення. Алопуринол – препарат з метою зменшення гіперурикемії при подагрі o За механізмом дії його структруний аналог – алоксантин є незворотним інгібітором ксантиноксидази; o застосування значно зменшує вміст сечової кислоти в крові, що сприяє полегшенню клінічних проявів захворювання. Синдром Леша-Ніхана Хвороба є зчепленою з Х-хромосомою, розвивається тільки у хлопчиків: симптоми, властивих подагрі + тяжкі нервово-психічні порушення: у дітей спостерігають: розумову відсталість агресивність, часто спрямовану на себе (намагання нанести пошкодження своїм губам, язику, пальцям спастичні паралічі ниркова недостатність камені в нирках Механізм неврологічних порушень невідомий, хоч у цих хворих і виявлене зниження активності ферментів синтезу дофаміну в екстрапірамідній системі. важка форма гіперурікемії (9 - 12 мг/дл). Екскреція сечової кислоти перевищує 600 мг/добу що потребує для виведення не менше 2,7 л сечі. Біохімічною основою ензимопатії є генетичний дефект синтезу гіпоксантингуанінфосфорибозилтрансферази (забезпечує повторне використання вільних гіпоксантину та гуаніну - “шлях реутилізації”). →аномальне накопичення гіпоксантину та гуаніну, які, перетворюючись на сечову кислоту, спричиняють розвиток гіперурикемії. У ранньому віці: Тофуси - це подагричні вузлики, які представляють собою скупчення кристалів сечової кислоти, обмежені сполучною тканиною. Вони з'являються при тривалому перебігу подагри і виникають через 6 років після першого подагричного нападу. Уратне каміння у сечовидільних шляхах Значні неврологічні відхилення, що супроводжуються порушенням мови, церебральними паралічами, зниженням інтелекту, схильністю до самокаліцтва – укуси губ, язика, пальців. У перші місяці життя неврологічні розлади не виявляються, проте на білизні, памперсах, спостерігають рожеві , оранжеві плями, викликані присутністю у сечі кристалів сечової кислоти. При відсутності лікування хворі вмирають у віці до 10 років через порушення функції нирок. 5 Представити схему катаболізму піримідинових нуклеотидів; зазначити метаболізм продуктів їх розпаду: I. II. III. IV. Відщепленні рибозофосфату від піримідинових нуклеотидів Окислення піримідинів Катаболізм азотистих основ (урацилу, цитозину, тиміну) - розрив піримідинових циклів з утворенням в якості продуктів похідних амінокислот —β-аланіну та βаміноізобутирату. β-аланін розшеплюється до СО2 та аміаку β-аміноізобутират може метаболізуватися подібно до інших розгалужених амінокислот з утворенням сукциніл-КоА. Кінцеві продукти тиміну (сукциніл-КоА з бета-аміноізобутирату) і цитозину, урацилу O NH2 N N N рибоза N Гуанозин Н3РО4 N рибоза N Аденозин Н 2О H2N Аденозиндезаміназа Рибозо-1-ф NH3 OH NH H2N N Гуанін Н 2О Нуклеозидфосфорилаза OH H 2O O NH3 H2O2 N HN Ксантиноксидаза NH N Гіпоксантин Гуаніндезаміназа O 2 N N N HN N рибоза N Інозин Н3РО4 Рибозо-1-ф Нуклеозидфосфорилаза O N N N HN O NH NH Ксантин Н2О + О2 Ксантиноксидаза Н2О2 NH2 2C H O NH2 Сечовина + C 2 Н2О O Алантоїказа COOH Гліоксилова кислота O C O NH2 NH2 COOH C O HN CH NH Алантоїнова кислота Н2О Алантоїназа O O NH2 СО2 NH O NH О2 Уриказа NH Алантоїн HN O NН O N Н N Н Сечова кислота Схема (катаболізму) розпаду пуринових нуклеотидів Реакції розпаду АМФ і ГМФ: - відщеплення фосфатної групи з утворенням нуклеозидів аденозину та гуанозину Фермент: 5-нуклеозидаза - дезамінування нуклеозидів Фермент 1 : аденозиндезаміназа Фермент 2 : гуаніндезаміназа - відщеплення від нуклеозидів залишка D-рибози Фермент: нуклеозидаза /пентозофосфату Фермент: фосфорилаза - катаболізм гіпоксантину (з АМФ) або ксантину (з ГМФ) з утворенням сечової кислоти. Окиснення гіпоксантину до ксантину з подальшим його перетворенням на сечову кислоту Фермент: ксантиноксидаза (– аеробна оксидоредуктаза, простетична група – містить ФАД (буває НАД), іони заліза (Fe3+) та молібдену; окислює пурини молекулярним киснем з утворенням пероксиду водню. Локалізація ферменту: печінка, кишка. Інгібітор ксантиноксидази: структурний аналог – алопуринол. NH2 Н2О N O O NH3 O HN Цитидиндезаміназа O N рибоза Цитидин HN O N рибоза Уридин Н 2О Н3РО4 Н3РО4 УридиннуклеозидазаТимідинфосфорилаза Рибоза HN 2'-дезоксирибоза 2'-дезоксирибозо-1- Ф O O C C C O N дезоксирибоза Тимідин Н 2О УридинфосфорилазаУридиннуклеозидаза Рибозо-1- Ф CH3 CH HN CH O C C CH3 CH N H Тимін N H Урацил НАДФН НАДФН Дигідроурацилдегідрогеназа НАДФ+ HN НАДФ+ O O C C CH2 HN C O CH-CH3 O C CH2 N H Дигідроурацил CH2 N H Дигідротимін Н2О Н 2О Дигідропіримідиназа COOH NH2 CH-CH3 COOH NH2 CH2 O C CH2 N H N-Карбамоїлізомасляна кислота O C CH2 N H N-Карбамоїлпропіонова кислота Н2О СО2 Н2О NH3 NH3 COOH COOH CH2 CH2 -NH2 b-Аланін СО2 Сечовина HC CH3 CH2 -NH2 b-Аміноізомасляна кислота Рис. 7.12. Схема розпаду піримідинових нуклеозидів Відновлення тиміну: дигідротимін гідроліз до N-карбамоїлізобутирату (уреїдоізобутирату) розпад на b-аміноізобутират, СО2 і NH3. Розпад піримідинових нуклеотидів супроводжується розкриттям кільця. Процес розпочинається відщепленням рибозофосфату з подальшим окисненням піримідинових основ. Кінцеві продукти реакції : СО2, NН3, сечовина, β-аланін (може служити джерелом для синтезу ансерину і карнозину, для утворення КоА; у тваринних тканинах піддається подальшому розпаду) і β-аміноізомасляна кислота. У тканинах тварин відкрита специфічна амінотрансфераза, яка каталізує трансамінування між β-аланіном і піровиноградною кислотою з утворенням α-аланіну і формілацетату: CH2 -NH2 CH3 CH2 C O COOH b-Аланін + COOH ПВК CH3 CHO CH-NH2 + CH2 COOH COOH b-Аланін Формілацетат Формілацетат далі підлягає окиснювальному декарбоксилуванню з утворенням вуглекислоти та ацетил-КоА. Субстрат для ксантиноксидази – гіпоксантин. Як пентозофосфатний шлях (ПФШ) повязаний з синтезом пуринів? Синтез пуринових нуклеотидів починається з рибозо-5-фосфата, який утворюється з глюкози в результаті пентозофосфатного шляху. Саме на цьому метаболіті, як на фундаменті, потім, крок за кроком формується пуринове кільце. 1-а реакція: (енергозатратний процес) Ф O H 2C Ф O O H2C O АМФ АТФ Глн OH ФРДФ-синтетаза O Ф O HO OH 5-Фосфорибозил-1дифосфат (ФРДФ) HO OH Рибозо-5-фосфат Глу ФФн Ф O C Гл АТ ФосфорибозилгліцинMg2+ амідсинтетаза H2C O NH2 АД HO OH АДФ + Фн АТФ + Н2О 5-Фосфорибозиламін Глу O Глн NH Глі АТФ O C C H2 H H ФормілгліцинамідинN C C ФосфорибозилгліцинNH Риб Ф рибонуклеотидамідолігаз Mg2+ NH Риб Ф O амідсинтетаза а N-ФормілгліцинN-Формілгліцинамідмідинрибонуклеотид АДФ + Фн рибонуклеотид CH2 H2C O NH2 HO OH 5-Фосфорибозила ФРДФамідотрансфераза NH O ФРДФамідотрансфераза Ф 3-я реакція: Глу ФФн Ф Н 2О N , N =CH-ТГФК 5 ТГФК 10 NH2 CH2 C Гліцинамідрибонуклеоти NH Риб O д-трансформілаза Гліцинамідрибонукл Н 2О ТФ + Н2О N5, N10=CH-ТГФК NH2 АмідоімідазолрибоCH2 нуклеотидсинтетаза C инамідрибонуклеоти NH Риб Ф O -трансформілаза АДФ + Фн Гліцинамідрибонуклеотид HC N COOH + СО2 Н CH2-COOH Аспартат АТФ C N АДФ CH-NH Mg2+ COOH C O C N CH C Аміноімідазол-4-NCH N C Енергозатратні АміноімідазолрибонуC H N реакції (у синтезі пуринових основ): Риб Ф N 2 H2N C сукцинокарбоксамідN Р N Риб Фз рибозо-5-фосфату, який є продуклеотидкарбоксилаза 1. синтез інозинової кислоти розпочинається рибонуклеотидсинтетаза 5-Аміноімідазол-45-Аміноімідазол5-Аміноімідазол-4CH2пентозофосфатного -COOH ктом циклу і на який переноситься пірофосфатна група сукцинокарбоксам рибонуклеотид карбоксирибонуклеотид АДФ рибонуклеотид CH-NH O фермента ФРПФ-синтетази. АТФ за участі C COOHNН2-групи N 3.До вільної β-5-фосфорибозиламіну приєднується молекула гліцину C Аденілосукцинатліаза (реакція вимагає енергіїCH АТФ) з утворенням гліцинамідрибонуклеотиду, фермент оімідазол-4-NC H N 2 нокарбоксамідN Риб Ф Фу фосфорибозилгліцинамідсинтетаза. O O леотидсинтетаза O 5-Аміноімідазол-4-N10 N глутаміну -CHO-ТГФКі синте5. На формільну переноситься амідна ТГФК група Н2О групу останнього сукцинокарбоксамідC N C N C рибонуклеотид C H2N N (реакція йде Cзується N-формілгліцинамідинрибонуклеотид К+ із затратоюHенергії C N CH 2 CHфермент АТФ), N-формілгліцинамідрибонуклеотидамідолігаза. CH Інозиніказа O C H C 5-Аміноімідазол-4CАденілосукцинатліаза N C HN 8. N Карбоксильна група рибонуклеотиду 5-аміноімідазол-4-карбоксинуклеотиду N карбоксамідрибонуклеоти N H2N Риб Ф Риб Ф Фумарат д-трансформілаза Р взаємодіє з NН2 O - групою аспарагінової кислоти з утворенням 5-аміноімідазол-4N10-CHO-ТГФК 5-Формамідоімідазол-45-АміноімідазолN-сукцинілкарбоксіамідрибонуклеотиду. нова кислота (ІМФ) C карбоксамід-рибонукл + N карбоксамідрибонуклеотид К (реакція вимагає C H2N затрати енергії АТФ) CH ноімідазол-4Фермент: аміноімідазолсукцинокарбоксамідрибонуклеотидсинтетази C Mg2+ амідрибонуклеоти ансформілаза H2N N Риб Ф Синтетичні реакції (у синтезі пуринових основ) 5-Аміноімідазол-4карбоксамід-рибонуклеотид 2. 5-фосфорибозил-1-пірофосфат (ФРПФ) взаємодіє з глутаміном (донор NН2групи) під впливом ФРПФ-амідотрансферази утворюється β-5-фосфорибозиламін : в процесі реакції (разом із вивільненням пірофосфату і вільної глутамінової кислоти) відбувається зміна його конфігурації (з α- на β-) це ключова реакція в синтезі пуринів і інгібується за принципом зворотного зв’язку пуриновими нуклеотидами, які утворюються з фосфорибозиламіну. 3. До вільної NН2-групи β-5-фосфорибозиламіну приєднується молекула гліцину (реакція вимагає енергії АТФ) з утворенням гліцинамідрибонуклеотиду, фермент фосфорибозилгліцинамідсинтетаза. 4. Далі ланцюг подовжується за рахунок приєднання формільної групи з N5, N10метеніл-ТГФК з утворенням N-формілгліцинамідрибонуклеотиду, фермент гліцинамідрибонуклеотидтрансформілаза. 5. На формільну групу останнього переноситься амідна група глутаміну і синтезується N-формілгліцинамідинрибонуклеотид (реакція йде із затратою енергії АТФ), фермент N-формілгліцинамідрибонуклеотидамідолігаза. 7. 5-аміноімідазолрибонуклеотид здатний акцептувати СО2 з утворенням рибонуклеотиду 5-аміноімідазол-4-карбоксинуклеотиду, фермент аміноімідазолрибонуклеотидкарбоксилаза. 8. Карбоксильна група цього продукту взаємодіє з NН2 - групою аспарагінової кислоти з утворенням 5-аміноімідазол-4-N-сукцинілкарбоксіамідрибонуклеотиду. Ця реакція вимагає затрати енергії АТФ Фермент: аміноімідазолсукцинокарбоксамідрибонуклеотидсинтетази. 9. У наступній реакції вуглецевий скелет аспарагінової кислоти відокремлюється у вигляді фумарової кислоти й утворюється 5-аміноімідазол-4-карбоксамідрибонуклеотид, тобто із аспарагінової кислоти в 1-е положення майбутнього пуринового ядра за участі фермента аденілсукцинази входить атом азоту. 10. Останній вуглецевий атом пуринового кільця вмонтовується у вигляді формільного залишка (джерело N10-форміл-ТГФК), який приєднується до 5 - NН2групи з утворенням 5-формілімідоімідазол-4-карбоксіамідрибонуклеотид, фермент аміноімідазолкарбоксамідрибонуклеотидтрансформілаза. Донор азотів пуринового ядра Джерело азотів піримідинового ядра Коли ми розуміємо, що пентоза іде на утворення нуклеотидів? 1-а реакція синтезу пуринів, коли рибозо-5-фосфат (як «затравка») під дією ферменту фосфорибозилдифосфат-синтатаза перетворюється на 5-фосфорибозил-1дифосфат. Щоб з рибози утворити дезоксирибозу:







