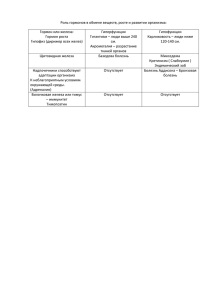
Болезнь де-Тони-Дебре-Фанкони Это врождённое заболевание, наследуется по аутосомно-рецессивному типу. Комплекс биохимических и клинических проявлений поражения проксимальных почечных канальцев с нарушением канальцевой реабсорбции фосфата, глюкозы, аминокислот и бикарбоната. Чаще всего синдром является компонентом других наследственных болезней: цистиноз, тирозинемия типа I, галактоземия, болезнь Вильсона, непереносимость фруктозы. Семейные варианты синдрома наследуются аутосомно-рецессивно, аутосомнодоминантно либо сцепленно с Xхромосомой. Считается, что в основе болезни лежат генетически обусловленные дефекты ферментативного фосфорилирования в почечных канальцах (комбинированная тубулопатия), дефицит ферментов 2-го и 3-го комплексов дыхательной цепи — сукцинатдегидрогеназного и цитохромоксидазного. Учёные относят заболевание к разряду митохондриальных болезней. Патогенез Патологические изменения представляют собой один из вариантов вторичного гиперпаратиреоза. Основное звено патогенеза — митохондриальный ферментный дефект в цикле Кребса, ферментная тубулопатия, характеризующаяся нарушением реабсорбции глюкозы, аминокислот, фосфатов и бикарбонатов в канальцах почек. Потеря аминокислот и бикарбоната способствует развитию метаболического ацидоза, на фоне которого усиливается резорбция костной ткани и снижается реабсорбция калия и кальция в канальцах почек, что приводит к развитию гипокалиемии и гиперкальциурии. Потеря фосфора ведёт к развитию рахита, а у детей старшего возраста и взрослых — к остеомаляции. Выделяют 2 формы заболевания — первичную и вторичную. Первичная форма, или тубулопатия, связанная с недостаточностью энзимов, обеспечивающих транспорт глюкозы, фосфатов, аминокислот, бикарбонатов. Вторичная развивается при обменных (гликогенозы, галактоземия, цистиноз, фруктоземия) и приобретенных (миелома) болезнях, отравлении солями тяжелых металлов. Манифестация заболевания происходит на втором полугодии или в начале 2-го года жизни. Характерны: отставание в росте и массе тела, задержка психомоторного развития, возможно немотивированное повышение температуры тела, вначале в виде субфебрилитета, в дальнейшем — приступов лихорадки, появляются полиурия и жажда, при недостаточном употреблении жидкости возникают признаки дегидратации, потери калия с мочой обусловливают мышечную гипотонию, гипорефлексию, нарушение реабсорбции бикарбонатов провоцирует ацидоз, появляются, а затем прогрессируют костные изменения: искривление ног, нередки спонтанные переломы, отмечаются частые респираторные инфекции. Диагноз подтверждается лабораторными данными при выявлении глюкозурии, фосфатурии, аминоацидурии, гипофосфатемии, ацидоза. В крови повышено содержание щелочной фосфатазы, в моче — калия и натрия. Постепенно развиваются гипоизостенурия (постоянный удельный вес мочи) и протеинурия. На рентгенограммах — остеопороз трубчатых костей нижних конечностей. Основные принципы лечения — коррекция электролитных нарушений, сдвигов в кислотно-щелочном равновесии, устранение дефицита калия и бикарбонатов. Увеличивают потребление фосфора с пищей, ограничивают потребление продуктов, включающих серосодержащие аминокислоты, назначают большие дозы витамина D. Для лечения цистиноза с целью подавления накопления цистина в тканях и проксимальных почечных канальцах применяют меркаптамин. Назначают препараты кальция и витамина D, при хронической почечной недостаточности проводится гемодиализ. Прогноз определяется тяжестью основного патологического процесса и осложнений (хроническая почечная недостаточность, пиелонефрит, и интерстициальный нефрит). Фосфат диабет Наследственный фосфат-диабет или витамин D-резистентный рахит — генетически обусловленное заболевание, наследуется по аутосомно-рецессивному типу. Возникающие мутации гена приводят к развитию витамин-D-резистентного гипофосфатемического рахита с гипокальциемией. Имеется другая форма гипофосфатемии — Х- сцепленная доминантная гипофосфатемия. Наследственный дефект ведет к: • нарушению первичного всасывания кальция и фосфора в кишечнике; • нарушению обратного всасывания (реабсорбции) фосфатов в почечных канальцах; • изменению синтеза витамина D в печени и почках, в частности к недостаточному образованию 25-оксихолекальциферола [25-(ОН)D3] в организме; • повышенной чувствительности эпителия канальцев почек к действию паратгормона. Ведущие клинические проявления витамин-Dрезистентного рахита: • искривления скелета, преимущественно нижних конечностей, по типу варусных деформаций; общий остеопороз. • отмечается задержка физического развития и нарушения походки («утиная»). • поражения скелета без лечения прогрессируют, способствуют задержке становления статико-моторных функций ребенка. • интеллект у детей, страдающих фосфат-диабетом, как правило, не нарушается. Первые признаки заболевания появляются обычно на 2-м году жизни и носят прогрессирующий характер. Возможны ранняя (в конце 1-го года жизни) и поздняя манифестация (4—10 лет) болезни. Диагностика 1. Анализ анамнеза и жалоб (опрос родителей), 2. Рентгенограмма костей (изменений в структуре костной ткани и нарушений в зонах роста костей (метафизах)). гиперфосфатурия. 3. Важнейшие биохимические признаки, которые позволяют поставить диагноз: • низкий уровень фосфора в сыворотке крови — 0,5—0,8 ммоль/л (норма —1,0—1,6 ммоль/л); • повышенная экскреция фосфатов с мочой — более 20 ммоль/сут; • высокий клиренс фосфатов мочи — 0,5—0,8 мл/с (норма 0,1—0,25 мл/сут) • повышение уровня щелочной фосфатазы в крови. 4. Генетический анализ на обнаружение изменений в Х-хромосоме у ребенка. Лечение -большие дозы витамина D (иногда пожизненно). препараты фосфора, кальция, витамины А и Е. при слабых деформациях скелета -ортопедическое лечение (корсет). Почечноканальцевый ацидоз Почечный канальцевый ацидоз (ПКА) — клиниколабораторный симптомокомплекс, характеризующийся метаболическим ацидозом и снижением способности почек подкислять мочу. Развивается как результат недостаточной реабсорбции бикарбонатов в проксимальных канальцах и/или нарушения ацидогенеза в дистальных канальцах почек. Выделяют 5 клинико-биохимических типов наследственного почечного ацидоза. 1-й тип — ПКА (дистальный, синдром БатлераОлбрайта), наследуемый по аутосомно- доминантному типу. Возникает вследствие нарушения продукции или транспорта водородных ионов (Н+). Снижение почками способности устанавливать градиент концентрации Н+ между кровью и первичной мочой обусловливает метаболический гиперхлоремический ацидоз. С мочой выводятся бикарбонаты и снижаются почечные потери кислот и аммиака. В результате усиленной экскреции натрия развивается полиурия. Моча резко щелочная. Потеря кальция формирует остеопороз, остеомаляцию. В условиях щелочной среды мочи, повышенной гиперкальциурии, гипоцитратурии происходит выпадение солей кальция в виде осадка. Соли откладываются в интерстиции, клетках почечного эпителия, просвете канальцев. К 3—5 годам развивается двусторонний нефрокальциноз. Этот тип ПКА чаще встречается у девочек. В раннем возрасте доминирует неспецифическая симптоматика: бледность кожных покровов, гипотрофия, мышечная гипотония, субфебрилитет, снижение аппетита, склонность к запорам. На фоне полиурии и полидипсии развивается картина обезвоживания. Со временем появляются рахитоподобные изменения костной ткани. Дети отстают в физическом и нервно-психическом развитии. При лабораторном исследовании выявляют: • • • • • • метаболический ацидоз (дефицит ВЕ = -10—20 ммоль/л); гипофосфатемию (0,9—1,0 ммоль/л); гипокальциемию (менее 2,2 ммоль/л); гиперкальциурию до 10—20 мг/кг/сут (при норме 1—5 мг/кг/сут); щелочную мочу (рН мочи 6,7—7,1); значительное снижение концентрационной функции почек (плотность мочи 1001—1008). 2-й тип ПКА (проксимальный) наследуется по рецессивному, сцепленному с Ххромосомой типу наследования. Снижение секреции водородных ионов (Н+) в проксимальных канальцах почек вызывает снижение обратного всасывания (реабсорбции) бикарбоната при сохранении кислотности мочи в дистальном отделе нефрона. Большое количество бикарбонатов поступает с мочой в дистальный отдел канальцев. Это приводит к стимуляции альдостерона, что в свою очередь вызывает повышенную реабсорбцию натрия и выделение калия. Возникает гипокалиемия. Чаще болеют мальчики. У детей в первые месяцы жизни отмечаются полиурия, полидипсия, субфебрилитет вплоть до лихорадки. Происходит задержка нарастания массы тела и роста. Появляются рахитоподобные изменения скелета. При тяжелом течении возможна ацидемическая рвота. В крови выявляют: метаболический ацидоз, снижение бикарбонатов, рН, калия, повышение хлора. Почечный порог реабсорбции бикарбонатов снижен до 19—20 ммоль/л и ниже (норма — 25 ммоль/л, у детей раннего возраста — 21 ммоль/л и выше). 3-й тип — смешанный. Встречается редко, наследуется по аутосомнорецессивному типу. Основой является частичное нарушение реабсорбции аниона гидрокарбоната в проксимальных канальцах почек и снижение секреции H+ дистальными канальцами. Характерны мышечная гипотония, рахитоподобные изменения скелета, остеопороз, нефролитиаз и нефрокальциноз, эпизоды гипокалиемии. В крови — значительный дефицит оснований (ВЕ = -6,0—10,0 ммоль/л), калия, гидрокарбонатов; в моче — снижение экскреции титруемых кислот, аммиака, увеличенная экскреция гидрокарбонатов, щелочная реакция мочи. 4-й тип — ПКА с гиперкалиемией. Наследуется по аутосомно-рецессивному типу, связан с резистентностью почечных канальцев к действию альдостерона или нарушением его синтеза, что приводит к потерям ионов натрия с мочой, гипонатриемии, гиперкалиемии и метаболическому ацидозу. Клиническая картина характеризуется задержкой роста. Могут наблюдаться непостоянные глюкозурия и гипераминоацидурия. Для диагностики данного типа ПКА решающее значение имеет высокий уровень альдостерона, ренина и калия в плазме (при нормальном содержании кортизола в крови и моче). 5-й тип — ПКА с глухотой. Тип наследования — аутосомно-рецессивный. Клинически наблюдаются выраженная задержка роста, психомоторного развития и потеря слуха. В крови — метаболический ацидоз различной степени выраженности при нормальном уровне калия. Реакция мочи — щелочная. Лечение состоит из коррекции рН и электролитного баланса. Алкилирующие вещества, такие как бикарбонат натрия, бикарбонат калия или цитрат натрия, помогают достигнуть относительно нормальной концентрации бикарбонатов в плазме (22–24 мЭкв/л [22–24 ммоль/л]). Цитрат калия применяется, когда имеет место персистирующая гипокалиемия, или при наличии кальциевых камней, потому что натрий увеличивает экскрецию кальция. Витамин D и пероральные добавки кальция. Гипо- и авитаминозы Роль витаминов в обмене веществ: 1. витамины – предшественники коферментов и простетических групп ферментов. Например, В1 – тиамин – входит в состав кофермента декарбоксилаз кетокислот в виде ТПФ (ТДФ), В2 – рибофлавин – входит в состав коферментов дегидрогеназ в форме ФМН и ФАД, РР – никотинамид – входит в состав НАД и НАДФ – коферментов дегидрогеназ; 2. витамины – предшественники гормонов (витамин D3 – предшественник кальцитриола); 3. витамины могут использоваться для синтеза медиаторов (витамин С – для синтеза норадреналина и серотонина); 4. витамины участвуют в образовании гормонов (витамин С – в образовании кортикостероидов); 5. витамины необходимы для синтеза незаменимых АМК (витамин В12 – метионин). Возраст 0-3 мес 4-6 мес 7-12 мес 1-3 года 4-8 лет м: 9-13 м: 14-18 ж: 9-13 ж: 14-18 Фолат мкг 65 65 80 150 200 300 400 300 400 РР мг 2 2 4 6 8 12 16 12 14 В1 мг 0,3 0,4 0,5 0,5 0,6 0,9 1,2 0,9 1,0 В2 мг 0,4 0,5 0,6 0,5 0,6 0,9 1,3 0,9 1,0 В6 мг 0,4 0,5 0,6 0,5 0,6 1,0 1,3 1,0 1,2 В12 мкг 0,3 0,4 0,5 0,9 1,2 1,8 2,4 1,8 2,4 Вит.D ЕД 400 400 400 600 600 600 600 600 600 Вит.А мкг 400 400 500 300 400 600 900 600 700 Вит.С мг 30 35 40 15 25 45 75 45 65 Вит.Е мг 4 4 5 6 7 11 15 11 15 Вит.К мкг 2,0 2,0 2,5 30 55 60 75 60 75 Принято выделять две основные группы факторов, обусловливающих развитие витаминной недостаточности: 1) экзогенные (внешние), приводящие к первичным (алиментарным) авитаминозам и гиповитаминозам; 2) эндогенные (внутренние). Алиментарные (экзогенные) гиповитаминозы развиваются вследствие недостаточного поступления витаминов с пищей при длительном вскармливании одним коровьим (дефицит витаминов С, группы В, РР, Д) или козьим молоком (дефицит фолатов), позднем введении овощных при­ кормов, соков, при неправильном их приготовлении, недостаточном количестве фруктов и овощей (гиповитаминоз С), избытке углеводов в рационе 228 Детские болезни. Том 1 при большом потреблении рафинированных высококалорийных продуктов — сахар, белый хлеб, кондитерские изделия (гиповитаминозы A, D, В„ С), длительном вскармливании бедными жирами смесями — разведения­ ми коровьего молока (дефицит жирорастворимых витаминов А, К, D, а так­ же С), недостаточном количестве животных белков в пище при строгом вегетарианстве (гиповитаминозы В1 2 , D, В2), неправильном приготовлении и хранении пищевых продуктов (повторное подогревание, кипячение, длительное неправильное хранение и др.). Особую группу составляют «медикаментозные» гиповитаминозы, возникающие при назначении сульфаниламидов и триметоприма (дефицит фолатов), дифенина и фенобарбитала (гиповитаминозы D, К, Вг), изониазида (гиповитаминоз В6), антибиотиков (гиповитаминоз К), антацидов (дефициты железа, фосфатов, кальция), дигиталиса (дефицит магния, кальция), минеральных масел (дефицит жирорастворимых витаминов A, D, Е, К), пеницилламина (дефицит витамина В6). Эндогенная витаминная недостаточность бывает: 1) резорбционной, то есть обусловленной частичным разрушением витаминов в пищеварительном тракте или нарушением их всасывания; 2) диссимиляционной, то есть возникающей вследствие нарушения усвоения витаминов тканями. Резорбционный гиповитаминоз может быть связан с заболеваниями: 1) желудка (при пониженной кислотообразующей функции, особенно ахилии, разрушаются витамины В,, С, РР, а при поражении дна желудка с нарушением синтеза гастромукопротеина нарушается всасывание витамина В1 2 и развивается мегалобластическая анемия; при гиперацидных состояниях наблюдаются гиповитаминозы А, С, РР); 2) желчного пузыря и поджелудочной железы (при недостаточном поступлении желчи вследствие атрезии желчных путей, синдрома сгущения желчи, желчнокаменной болезни, хронических гепатитов и циррозов, муковисцидозе, хроническом панкреатите развивается дефицит жирорастворимых витаминов А, К, Е, D); 3) кишечника (целиакия и другие синдромы мальабсорбции, энтероколиты приводят к гиповигаминозам А, К, Е, D, Н, С, группы В). Диссимиляционный гиповитаминоз развивается при любых тяжелых и дли­ тельных инфекционных заболеваниях, особенно протекающих с высокой температурой тела; при избытке в питании углеводов, недостатке белков, большой физической нагрузке у спортсменов, курении, наркомании и др. Клиника и диагностика: Неспецифические клинические проявления и последствия дефицита витаминов могут быть разнообразны: • • • • • • • • ухудшение самочувствия; снижение умственной и физической работоспособности населения (у детей - нарушения поведения и снижение активности, задержка или особенности психомоторного развития); нарушение процессов детоксикации в организме; нарушение функционирования иммунной системы (снижение сопротивляемости к инфекциям, то есть частые респираторные болезни); замедление темпов физического развития; снижение регенерационного потенциала органов и систем; предрасположенность к развитию различных патологических состояний; хронизация заболеваний. Постановка диагноза «специфический гиповитаминоз» иногда достаточно трудна, так как признаки отдельных гиповитаминозов не всегда достаточно специфичны. Например, глоссит может наблюдаться при гиповитаминозах РР, В6, В2, В12, а фолликулярный гиперкератоз — при недостатке витаминов А, С и др. В этих случаях целесообразно выделять ведущий синдром, анализировать анамнез, сопоставлять клиническую картину с результатами биохимических исследований. Например, ангулярный стоматит в сочетании с васкуляризацией роговицы, сухость слизистых оболочек рта, губ возникает при недостатке рибофлавина, а ангулярный стоматит в сочетании с гипертрофией сосочков языка указывает на недостаток никотиновой кислоты. Ангулярный стоматит, сочетающийся с гипохромной анемией и ложкообразными вдавливаниями ногтей пальцев рук, типичен для больных, получающих с пищей недостаточное количество железа. • Содержание витамина С в плазме - менее 0,006 г/л, в суточной моче менее 0,005 г. • Содержание витамина А в сыворотке крови - менее 0,7 мкмоль/л, содержание каротина - менее 1,0 мкмоль/л; • Содержание фолиевой кислоты в плазме крови менее 4,8 нмоль/л; • Содержание витамина В12 в плазме крови менее 10 пмоль/л; • Содержание метилникотинамида: в суточной моче - менее 4 мг, в часовой - менее 0,3 мг. Пиридиннуклеотидов(НДЦ и НАДФ) менее 0,3 мкг в 1 мл крови; • Содержание витамина В1 в плазме крови - менее 14,8 мкмоль/л, в су­ точной моче натощак - менее 10 мкг. Пировиноградной кислоты в суточной моче более 30 мг, в плазме - более 0,144 ммоль/л (0,01 г/л), • • • • особенно после физической нагрузки. Снижение активности транскетолаз эритроцитов; Содержание витамина В2 в суточной моче менее 30 мкг или менее 125 мкг на 1 г креатинина; В6 - ксантуренурия более 0,005 г в сутки, уровень 4-пиридоксиновой кислоты в часовой моче менее 0,0005 г. Зеленый цвет мочи при добавлении 10% хлорного железа. При В6-зависимых судорогах - снятие ЭЭГ после в/м введения 100 мг пиридоксина; Вит Е - уровень в плазме крови менее 0,5 мг/л, повышенный процент гемолиза в 0,12% растворе перекиси водорода; Вит К - увеличение протромбинового времени, низкие уровни витамин-Кзависимых факторов крови (II, VII, IX, X), а также С и S-протеинов, остеокальцина, появление в крови неактивных предшественников II, VII, IX, X факторов свертывания; Лечение Заключается в диетотерапии – формирование разнообразного рациона с достаточным количеством как растительной, так и животной пищи. Применение витаминных препаратов необходимо только при назначении их врачом, поскольку при избыточном и нерациональном применении их можно вызвать состояние, характеризующееся избытком определенного витамина – гипервитаминоз. При применении витаминных препаратов предпочтение стоит отдавать монопрепаратам (содержащим какой-либо один витамин), поскольку одни витамины могут отрицательно влиять на всасывание других в желудочно-кишечном тракте либо конкурировать за транспортные системы в организме. Профилактика Правильное, разнообразное питание ребенка с достаточным использованием овощей и фруктов, особенно весной, когда чаще развивается дефицит витаминов. При вскармливании ребенка первых месяцев жизни коровьим молоком и его разведениями необходимо дополнительно назначать витамины С, А, РР, Е в дозах, соответствующих суточным потребностям. Потребность ребенка в витаминах увеличивается при инфекционных заболеваниях с лихорадкой, хронических заболеваниях органов пищеварения, дыхания, печени, почек, при назначении антибиотиков и сульфаниламидов. В этих случаях в комплексе лечения даже при отсутствии клинических признаков гиповитаминозов должно быть предусмотрено и применение витаминов С, В1, В2, А, В6 в дозах, превышающих возрастные физиологические потребности в 3-4 раза. Рекомендации по кормлению и уходув целяхразвития здорового ребенка и время болезни. Игра, игровая терапия Рекомендации ВОЗ и ЮНИСЕФ по оптимальному кормлению детей грудного и раннего возраста заключаются в следующем: • раннее начало грудного вскармливания в течение часа после рождения ребенка; • исключительное грудное вскармливание в течение первых шести месяцев жизни; и • введение надлежащего питательного и безопасного прикорма в возрасте шести месяцев наряду с продолжением грудного вскармливания до достижения ребенком возраста двух лет и больше. Грудное вскармливание Исключительное грудное вскармливание в течение шести месяцев имеет много преимуществ для детей грудного возраста и их матерей. Основными из них являются защита от желудочно-кишечных инфекций. Благодаря раннему началу грудного вскармливания – в течение часа после рождения ребенка — обеспечивается защита новорожденного от инфекций и снижается смертность новорожденных. Риск смерти в результате диареи и других инфекций может быть более высоким среди детей, находившихся ранее на частичном грудном вскармливании или вообще не находившихся на грудном вскармливании. Грудное молоко является также важным источником энергии и питательных веществ для детей в возрасте 6-23 месяцев. Оно может обеспечивать половину или более всех энергетических потребностей ребенка в возрасте 6-12 месяцев и одну треть энергетических потребностей ребенка в возрасте 12-24 месяцев. Грудное молоко является также важным источником энергии и питательных веществ во время болезни и способствует снижению смертности среди детей, испытывающих недостаточность питания. Дети и подростки, находившиеся в грудном возрасте на грудном вскармливании, с меньшей вероятностью имеют избыточный вес или страдают от ожирения. Кроме того, они демонстрируют более высокие результаты тестов на интеллектуальное развитие и лучшую посещаемость школ. Грудное вскармливание связано с более высоким доходом во взрослой жизни. Более длительное грудное вскармливание способствует также укреплению здоровья и благополучия матерей; оно снижает риск развития рака яичников и молочной железы и позволяет делать перерывы между беременностями — исключительное грудное вскармливание детей в возрасте до шести месяцев оказывает гормональное воздействие, которое часто вызывает отсутствие менструаций. Это естественный (хотя и ненадежный) метод предупреждения беременности, известный как метод лактационной аменореи. Десять принципов для медицинских учреждений для обеспечения успешного грудного вскармливания: 1) Иметь в письменной форме политику грудного вскармливания, которая в установленном порядке доводится до сведения всего медицинского персонала. 2) Подготовить весь медицинский персонал в области приобретения навыков, необходимых для проведения этой политики. 3) Информировать всех беременных женщин о преимуществах и осуществлении грудного вскармливания. 4) Помогать матерям в проведении первого грудного вскармливания спустя полчаса после родов. 5) Показывать матерям, как проводить грудное вскармливание и как поддерживать лактацию даже в случае, если им придется разлучиться со своими детьми. 6) Не давать новорожденным детям никакой другой пищи и питья помимо грудного молока, если нет иных медицинских предписаний. 7) Практиковать совместное пребывание в одной палате, позволяющее матерям и грудным детям находиться вместе 24 часа в сутки. 8) Поощрять грудное вскармливание по требованию – всякий раз, когда ребенок голоден. 9) Не давать соски-пустышки детям, находящимся на грудном вскармливании. 10) Поощрять создание групп поддержки грудного вскармливания и направлять к ним матерей после выписки из больницы или клиники. Прикорм Примерно в возрасте шести месяцев потребности ребенка в энергии и питательных веществах начинают превышать тот уровень, на котором они могут быть удовлетворены грудным молоком, и введение прикорма становится необходимым. В этом возрасте ребенок готов к употреблению других пищевых продуктов и по своему развитию. Не введение прикорма по достижению ребенком возраста шести месяцев или ненадлежащее введение прикорма могут сказаться на росте ребенка. Руководящие принципы по надлежащему прикорму заключаются в следующем: • продолжайте частое, по требованию, грудное вскармливание до достижения ребенком двухлетнего возраста или больше; • проявляйте чуткость при кормлении ребенка (например, непосредственно кормите детей грудного возраста и помогайте детям более старшего возраста. Кормите медленно и терпеливо, поощряйте, но не принуждайте, разговаривайте с ребенком и сохраняйте с ним зрительный контакт); • практикуйте надлежащую гигиену и надлежащее обращение с пищевыми продуктами; • начинайте в возрасте шести месяцев с небольших количеств пищевых продуктов и постепенно увеличивайте их по мере того, как ребенок становится старше; • постепенно повышайте консистенцию пищи и делайте ее более разнообразной; • увеличивайте число кормлений ребенка – 2-3 раза в день для детей в возрасте 6-8 месяцев и 3-4 раза в день для детей в возрасте 9-23 месяцев с 1-2 дополнительными перекусываниями по желанию ребенка; • по мере необходимости используйте для прикорма обогащенные пищевые продукты или витаминно-минеральные добавки; • увеличивайте количество питья, в том числе с помощью грудного вскармливания, и предлагайте мягкую, любимую пищу. При уходе за больным ребенком могут быть специальные диеты, где имеются ограничения соответственно болезни ребенка (стол 7, 5, 10 и др.). Обычно, когда речь идет об инфекционных заболеваниях, для грудничков – учащение кормлений, для деток раннего возраста – соблюдение водного баланса, еда должна быть богатой витаминами, и должна в полной мере восполнять энергетические затраты организма в период болезни. Игротерапия Игра является не только одним из самых любимых занятий малышей, но и ведущей деятельностью детей, начиная с самых ранних лет и до школьного возраста. А способность играть сохраняется у индивида на протяжении жизни. С помощью игры происходит развитие моторных функций и когнитивных способностей у ребенка. Также она является главным методом обучения для ребенка. Для детей игра представляет собой основную возможность взаимодействия с окружением, вследствие чего она выполняет и функцию социализации. Кроме этого в игровом процессе ребенок естественно отыгрывает зарождающиеся в нем негативные эмоции. Игротерапия являет собой ответвление арттерапии, оказание помощи и достижение психологического комфорта индивидом посредством игровой деятельности. Она представляет собой довольно эффективный коррекционный метод для работы с малышами, имеющими абсолютно разные психические особенности. Данный метод не рекомендуется практиковать в работе с индивидами, страдающими полным аутизмом или неконтактной шизофренией. Игровую терапию применяют: • при травмах психологического характера, связанных с разводом родителей; • для улучшения успеваемости детей при трудностях в учебе; • для коррекции агрессивного и тревожного поведения; • для профилактики и лечения различных фобий, детских страхов; • при умственной отсталости и задержках в психическом развитии для ускорения развития; • при заикании и многих других проблемах. При выборе методов игротерапии нужно исходить из требований конкретных целей коррекционного воздействия и из того, насколько устойчивы показатели результативности воздействия на индивида именно игровой терапии. В качестве параметра эффективности игротерапии учитывается устремленность детей к поддержанию коммуникаций и взаимодействию с окружением в коллективе. Это проявляется в позитивных личностных трансформациях, сдвигах, проистекающих в самосознании, улучшении психоэмоционального самочувствия, положительной динамике интеллектуального развития вследствие снятия эмоциональной тревожности и напряжения. Так, например, игротерапия общения заключается в занятиях подвижного характера, которые помогают выстраивать положительные, эмоционально теплые взаимоотношения с детьми. Занятия игротерапией не требуют специфического оборудования, а ее техники носят больше интуитивный характер. М. Панфилова, разработчик методов игротерапии, доказала, что посредством игр малыша можно обучить правильному построению диалога, снизить его гиперактивность. Игротерапия Панфилова представляет собой комплекс современных психотерапевтических методик, состоящий из игровой терапии, сказкотерапии, метода беседы, арт-терапии, телесной терапии, элементов психодрамы, жетонной терапии и др. Питание при ЖДА. Классификация препаратов железа. Первая помощь при отравлении препаратами железа. При развитии анемии у детей, находящихся на естественном вскармливании, необходимо, прежде всего обеспечить полно­ценное питание матери, а также провести соответствующую коррекцию пищевого рациона ребенка. В питании матери должны широко использоваться продукты с высоким содержа­нием железа (субпродукты, мясо, яйца и др.), а также овощи и фрукты, в состав которых входят вещества, принимающие участие в гемопоэзе: медь, кобальт, железо и др. К ним отно­сятся: морковь, цветная капуста, свекла, томаты, яблоки, груши, инжир, хурма, курага, черная смородина, черника, алыча. В рацион кормящей матери рекомендуется также вводить но­вые специальные продукты на молочной основе, обогащенные белком, витаминами и минеральными веществами, - "Фемилак I" и "Фемилак II", предназначенные для беременных жен­щин и кормящих матерей. Если ребенок, больной железодефицитной анемией, вынужденно переводится на искусственное вскармливание, то в его рационе следует использовать современные адаптированные молочные смеси, обогащенные всем комплексом витаминов и микроэлементов. При этом для детей первых месяцев жизни рекомендуются такие адаптированные смеси, как "Алеся I", "Симилак с железом", "Энфамил с железом", содержание же­леза в которых составляет 1,2 мг на 100 мл готовой смеси. В молочных смесях европейского производства количество же­леза составляет 0,7—0,8 мг на 100 мл; это смеси "Сэмпер Бэби I", "НАН", "Нутрилон", "Хумана I". Детям второго полугодия жизни дают так называемые "последующие смеси" — молоч­ные смеси с более высоким содержанием белка. Для детей, страдающих анемией, можно рекомендовать обогащенные же­лезом смеси "Сэмпер Бэби 2", "Энфамил 2", "Галлия 2", "Хайнц для детей с 6 месяцев", "НАН 6-12". Есть отечественный аналог – «Гулазык». Разрабатывая рацион больных железодефицитной анемией детей более старшего возраста (после 1 года), необходимо обращать внимание на достаточное включение продуктов с вы­соким содержанием железа и аскорбиновой кислоты. По содержанию железа продукты подразделяются на богатые, содержащие более 5 мг железа/100 г, умеренно богатые - менее 5 мг и бедные железом - менее 1 мг. Важно также включать в рацион детей достаточное количество продуктов с высоким содержанием аскорбиновой кисло­ты, способствующей более полному усвоению железа. Аскорбиновая кислота содержится в свежем шиповнике (650 мг/100 г), черной смо­родине и облепихе (200 мг/100 г), немного меньше в землянике садовой (60 мг/100 г), апельсинах (60 мг/100 г), грейпфрутах (45 мг/100 г), шпинате (55 мг/100 г), лимонах (40 мг/100 г), мандаринах (38 мг/100 г), крыжовнике (30 мг/100 г). При использовании этих продуктов в питании больных детей можно повысить усвоение железа из пищи почти в 5 раз. В рационах детей с железодефицитной анемией квота мясных продуктов должна быть увеличена примерно на 15-20 %. Суточную норму мяса лучше давать дробно - в 2 приема, в первой половине дня с овощным блюдом или серыми кашами, причем предпочтение отдается овсяной и гречневой. Употребление каш из белых круп (рисовая, манная), а также макаронных изделий должно быть ограничено, а в острый период заболевания полностью исключено из диеты больного ребенка. В настоящее время выделяют две группы препаратов железа — ионные и неионные. Ионные препараты, железа. Подавляющее большинство препаратов являются солевыми (сульфатные и хлоридные соли) и полисахаридными (глюконатные, фумаратные комбинации) соединениями двухвалентного железа. Сульфат железа характеризуется высокой степенью всасывания (более 10%), наименьшей токсичностью и небольшим процентом побочных эффектов по сравнению с другими его солями. Хуже всего всасывается железо при приеме его хлоридных соединений (менее 4%); они же чаще вызывают побочные реакции. Солевые (ионные) препараты железа (пероральные лекарственные формы) Хлорид железа (II) - Гемофер Сульфат железа (II) - Актиферрин - Тардиферон - Ферроплекс - Феррокаль Глюконат железа (II) - Тотема Несолевые (неионные) препараты железа Железо (III) - гидроксид полимальтозный комплекс - Феррум Лек (пероральные формы) - МальтоферФол - Мальтофер Гидроксид полимальтозный комплекс (полиизомаль- тозат железа III) - Феррум Лек (раствор для в/м введения) Гидроксил сахарозный комплекс (сахарат железа III) - Венофер (раствор для в/в введения) Фумарат железа (II) - Ферронат - Хафетол Неионные препараты железа являются медикаментами, лишенными указанных побочных эффектов. Это соединения гидроксид-полимальтозного комплекса трехвалентного железа (Мальтофер и Мальтофер Фол, Феррум Лек). Неионная химическая структура и активный транспортный механизм в кишечнике (нет необходимости в окислении ферроксидазой-1 и др.) теоретически (да и практически) сводит на нет указанные выше побочные эффекты ионных ферропрепаратов, а при насыщении организма железом всасывание железа из препарата полностью прекращается. Лечение • Кишечный лаваж • Хелаторная терапия (в тяжелых случаях) Пострадавшие с ярко выраженными симптомами или с высокой концентрацией железа в крови нуждаются в госпитализации. Даже после рвоты в желудке может остаться большое количество железа. Пострадавшему могут назначить промывание желудка и кишечника (кишечный лаваж) специальным раствором полиэтиленгликоля, который дают перорально или через пропущенную в желудок трубку, хотя эффективность этого метода не доказана. При тяжелом отравлении пострадавшему назначают внутривенные вливания дефероксамина — препарата, который связывает железо в крови (так называемая хелаторная терапия) и выводит его из организма с мочой.