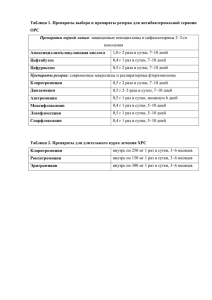
Бекетов А. И. Курс лекций по фармакологии (учебное пособие для отечественных и иностранных
студентов): В 2 ч. Часть 1. – 2-е изд., перераб. и доп. – Симферополь, 1998. – 100 с.
Книга содержит тексты лекций автора по всем разделам фармакологии, предусмотренным Учебной
Программой для студентов лечебного, педиатрического и стоматологического факультетов. В них
изложены современные представления о лекарственных средствах с освещением вопросов
классификации, механизмов действия, терапевтических и побочных эффектов, показаний и
противопоказаний для применения, которые служат клинической основой рациональной фармакологии.
Опыт преподавания клинической фармакологии позволил автору выделить сведения, имеющие
фундаментальное значение для подготовки врача. В начале каждой лекции даны вопросы, помогающие
студентам составить представление о ее содержании. Приложение к курсу лекций, содержащее
экзаменационные вопросы и список препаратов, которые студенты должны уметь выписать в рецептах
на экзамене по фармакологии и на выпускных государственных экзаменах, имеет целью помочь при
подготовке к ним. В списке препаратов приведены основные синонимы их названий, которые широко
используются в иностранной справочной литературе и фармацевтическими фирмами. Синонимы
прежде всего предназначены выпускникам вуза, которым предстоит работа в зарубежных странах.
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ:
ЛВ — лекарственное вещество
ЛС — лекарственное средство
ФТ — фармакотерапия
МД — механизм действия
ПЭ — побочные эффекты
В/в — внутривенно
П/к — подкожно
В/м — внутримышечно
Пор. — порошок
Таб. — таблетка
Др. — драже
Амп. — ампула
Р-р — раствор
АД — артериальное давление
ЦНС — центральная нервная система
ССС — сердечно-сосудистая система
ЖКТ — желудочно-кишечный тракт
КОС — кислотно-основное состояние
ХР — холинорецептор
АР — адренорецептор
АЦХ — ацетилхолин
НА — норадреналин
цАМФ — циклический аденозинмонофосфат
Фл. — флакон
Лекция 1.
ВВЕДЕНИЕ.
ОСНОВНЫЕ ПОНЯТИЯ ОБЩЕЙ ФАРМАКОЛОГИИ.
В .этом разделе будут рассмотрены наиболее общие фармакологические понятия, знание которых
способствует формированию фармакологического мышления. Без этого невозможно составить глубокое
представление о взаимодействии лекарств с организмом больного и объективно оценить достигнутый
эффект от применения лекарства.
В этой лекции мы рассмотрим следующие основные вопросы:
*-что изучает фармакология и ее значение для современной медицины;
* -основные разделы фармакологии;
*-понятие о лекарстве и яде;
* -из чего и как получают ЛВ;
*-как изучают ЛВ и внедряют их в клинику;
Основные понятия фармакокинетики:
*-пути введения ЛВ в организм;
*-биодоступность ЛВ и от чего она зависит;
* -всасывание ЛВ при разных путях введения;
*-проникновение ЛВ через биологические мембраны;
*-основные биологические барьеры организма и их значение;
*-транспорт и распределение ЛВ в крови и тканях;
* -концентрация ЛВ в крови, от чего она зависит, ее значение для действия лекарств, период
полувыведеиия (полураспада);
*-биотрансформация ЛВ, роль печени;
* -экскреция ЛВ, факторы, влияющие на нее;
* -понятие об элиминации веществ, основные органы элиминации.
Фармакология - наука, изучающая взаимодействие ЛВ с организмом на биомолекулярном,
субклеточном, клеточном, органном, системном и организменном уровнях. Она также изучает
последствия применения лекарств, связанные с изменением генетического материала и психики
человека.
Развитие фармакологии идет по двум главным направлениям; фундаментальные исследования для
выяснения принципов и механизмов действия ЛС и разработка эффективных препаратов как основы
лечения заболеваний. Фармакология является универсальным методом лечения. Прогресс ее оказал
благотворное влияние как на клиническую медицину, так и на медикобиологические науки.
Фармакология тесно связана с биологией, морфологией, нормальной и патологической физиологией,
с клиническими дисциплинами и оказывает огромное влияние на их развитие. С помощью ЛВ изучают
тончайшие и сложные процессы в организме и управляют ими.
Под лекарством понимают любое вещество, которое можно использовать с целью профилактики и
лечения заболеваний. Между лекарством и ядом нет принципиального различия, так как любое
лекарство в большой дозе может вызвать токсический эффект и, наоборот, ядовитые вещества в
определенных дозах оказывают лечебное действие.
ЛС получают из разных источников. Главный из них - химический синтез. За ним следует мир
растений, из которых получают более 30% препаратов. Многие средства получают из тканей животных,
грибов, микроорганизмов, минералов. Создание лекарств является сложным и дорогостоящим
процессом. Оно осуществляется в тесном содружестве химиков, фармакологов, клиницистов.
Основными путями создания препаратов являются: 1) направленный синтез, основанный на знании
свойств биологически активных веществ; 2) эмпирический поиск методом скрининга; 3) получение
препаратов из растений, животных, минералов; 4) выделение активных веществ из грибов и
микроорганизмов.
Направленный синтез осуществляется путем воспроизведения биогенных веществ, образующихся в
организме (напр., адреналин), создания антиметаболитов, являющихся структурными аналогами
естественных метаболитов (напр., сульфаниламиды), путем изменения структуры известных
биологически активных соединений с целью усиления их действия (напр., преднизолон), а также
создание препаратов на основе изучения их химических превращений в организме.
Под скринингом понимают эмпирический поиск ЛС путем "просеивания" через фармакологические
исследования веществ с неизвестными свойствами. Этот метод слишком трудоемкий, дорогой и
малоэффективный.
Традиционными методами создания новых ЛС являются модификация соединений с известной
биологической активностью с целью их совершенствования и выяснение зависимости между
структурой веществ и их фармакологическим действием, что служит основой синтеза новых ЛС.
Принципиально новым подходом к синтезу ЛВ является выяснение трехмерной структуры
макромолекул-мишеней (рецепторы, ферменты и др.), с которыми взаимодействуют биологически
активные вещества. Прогрессу в этой области способствуют рентгеноструктурный анализ и
спектроскопия на основе ядерно-магнитного резонанса, генная инженерия, а также компьютерное
моделирование структуры молекул и их взаимодействия с ЛВ. На этой основе создают ЛВ с высоким
сродством с рецепторами и, следовательно, с большой избирательностью действия и эффективностью.
Наиболее древним способом получения лекарств является выделение их из растений. Вначале
использовали растения, обработанные простейшими способами (порошки, настои, отвары, настойки,
экстракты). Впоследствии научились выделять из растений химически чистые вещества (алкалоиды,
гликозиды и др.). Многие препараты получают из животных тканей (гормоны и др.), из минералов
(соли, кислоты и др.), из грибов и микроорганизмов (антибиотики, вакцины, сыворотки).
Внедрение ЛС в практику проходит ряд этапов. Первым является фармакологическое изучение в
эксперименте на животных: выяснение механизма действия, эффектов, всасывания, превращения и
выделения, побочного действия сравнительная оценка с эталонным препаратом, изучение действия на
патологической модели. Вторым этапом является экспертная оценка результатов фармакологического
исследования, третьим - клинические испытания. После этого специалисты решают судьбу соединения,
либо предлагая его производство и внедрение в практику, либо отвергая.
В последние годы выделилась самостоятельная дисциплина - клиническая фармакология. Это
обусловлено сложностью переноса экспериментальных данных на больного человека, необходимостью
изучать действие ЛВ на больном, разрабатывать принципы и методы рационального применения
лекарств, исследовать и предупреждать осложнения лекарственной терапии и т.п.
Фармакология делится на общую и частную. Первая изучает наиболее общие закономерности
взаимодействия лекарств с организмом, вторая -взаимодействие отдельных групп препаратов с
организмом. Основными разделами фармакологии являются фармакокинетика и фармакодинамика.
Фармакокинетика изучает процессы движения и превращения ЛВ в организме, фармакодинамика - их
действие.
Фармакокинетика.
Пути введения ЛС. От них зависят скорость наступления и достижения максимального эффекта, его
продолжительность и интенсивность. Поэтому необходимо учитывать особенности и принципы выбора
путей введения лекарств. Их подразделяют на энтеральные (через пищеварительный тракт) и
парентеральные (минуя пищеварительный тракт).
Самый простой, удобный и распространенный путь введения - через рот. Однако при этом
необходимо учитывать наличие и характер патологического процесса в органах пищеварения, секрецию
пищеварительных желез, растворимость ЛВ в липидах, способность к диссоциации, возможность
многократного выделения веществ в просвет кишечника и повторного всасывания (циклические
процессы), состояние микробной флоры кишечника, взаимодействие с различными пищевыми и
лекарственными веществами и т.п. Это является серьезным недостатком энтерального пути введения,
так как все указанные факторы влияют на всасывание и биодоступность препарата. Под
биодоступностью понимают отношение количества ЛВ, растворенного в крови через определенное
время после его приема, к принятой дозе внутрь, выраженное в процентах. Напр., если биодоступность
препарата равна 50%, следовательно, 50% принятой дозы не поступило в кровь. Кроме указанных
факторов на биодоступность лекарств влияют их лекарственные формы, разрушение в пищевом канале
и при прохождении через печень.
К энтеральным путям относятся также введение через слизистую рта (напр., под язык), через
прямую кишку. При этих путях введения ЛВ сразу поступают в общий ток крови без первичного
прохождения через печень.
К парентеральным путям введения относятся инъекции, ингаляции и введение через кожу. С
помощью инъекций лекарства вводят под кожу, в мышцы, в вены, артерии, в полости. При этом эффект
наступает быстро, особенно при внутривенном введении, и обеспечивается точность дозировки.
Биодоступность в большинстве случаев составляет 100%. Под кожу и в мышцы не следует вводить
препараты, обладающие сильным раздражающим действием, а в сосуды - нерастворимые соединения и
маслянные растворы из-за опасности возникновения эмболии. Недостатком инъекций является
травмирование тканей, необходимость соблюдать стерильность и опасность непредсказуемых реакций
(шок, коллапс, судороги).
С помощью ингаляций вводят газообразные, парообразные вещества и аэрозоли. При этом ЛВ
поступают в кровь в неизмененном виде, эффект наступает быстро. Недостатком являются реакции
раздражения, сопровождающиеся спазмами гортани, бронхов, кашлем, рефлекторными влияниями на
сердце и т.п.
Через кожу вводят жирорастворимые вещества (в форме мазей и линиментов) и электролиты
(методом электрофореза).
Всасывание ЛВ. В пищеварительном тракте оно зависит от многих факторов. Ионизированные
формы ЛВ плохо растворяются в липидах и плохо всасываются. Поэтому всасывание электролитов
соответствует растворимости в липидах неионизированной формы вещества. Слабокислые соединения
(напр., салицилаты) в кислой среде желудка (рН 1,0-1,5) ионизируются плохо, поэтому всасываются
преимущественно в желудке. Слабые основания (напр., алкалоиды) лучше всасываются в кишечнике
(рН в 12-перстной кишке около 6,6), так как плохо ионизируются в щелочной среде. Особенно сложно
учитывать этот фактор у детей, так как рН желудочного сока у них непрерывна снижается от периода
новорожденнрсти (близок к нейтральному значению) до 3 лет (около 1,5 - как у взрослого). Необходимо
также учитывать, что наиболее кислой среда желудка бывает во время и сразу после еды, а наименее
кислой - за 1 час до еды и через 1,5-2 ч. после нее. Поэтому кислые соединения следует назначать во
время или сразу после еды, а основания за 1 ч. до еды или через 1,5-2 ч. после еды.
Большое влияние на всасывание лекарств оказывают объем и характер пищи, которая может
изменить рН среды. Существенное значение имеет также хелатообразоаание (хелаты внутрикомплексмые соединения, центральным звеном которых является атом металла). Хелатные
соединения плохо всасываются в кишечнике. Они образуются при взаимодействии ЛВ с молочными
продуктами, содержащими казеинат кальция, овощами, содержащими железо, и т.п. Жиры повышают
всасывание жирорастворимых лекарств (витамины А, Д, К, Е, противоглистные препараты и др.).
Поскольку всасывание большинства лекарств происходит в кишечнике, большое значение имеет
скорость опорожнения желудка, которая зависит от моторики желудка и характера пищи. Всасывание
может быть затруднено при воспалении слизистой желудка и кишечника, при нарушении
кровообращения, при одновременном приеме нескольких ЛС. Напр., основания способствуют
ионизации кислых соединений и затрудняют их всасывание, и наоборот. Вещества, замедляющие
перистальтику кишечника (спазмолитики, холиноблокаторы и др.), способствуют всасыванию, а
вещества, ускоряющие перистальтику (холиномиметики, слабительные), ухудшают всасывание.
При назначении ЛС внутрь имеет значение лекарственная форма. Общим правилом является то,
что жидкие формы всасываются лучше, чем порошки, всасываемость которых зависит от степени
дисперсности частиц, а порошки всасываются лучше, чем таблетки, драже и гранулы. При назначении
лекарств внутрь детям в возрасте до 5 лет предпочтение следует отдавать жидким лекарственным
формам, которые лучше всасываются и меньше раздражают слизистые оболочки.
Таким образом, биодоступность ЛС при назначении внутрь зависит от многих факторов, колеблется
в широких пределах и трудно предсказуема. Особенно это относится к детям.
При парентеральном введении ЛВ поступают либо непосредственно в кровь, либо всасываются из
подкожной клетчатки, мышц и полостей (в зависимости от видов инъекций), из альвеол (при
ингаляции), минуя печень. Врач может более точно предусмотреть концентрацию ЛВ в крови и
эффективную дозу. При введении ЛВ под кожу и в мышцы необходимо учитывать состояние
кровообращения, так как при замедлении кровотока скорость всасывания может существенно
замедлиться.
При выборе пути введения ЛС необходимо учитывать следующие основные факторы: а)
лекарственную форму, б) стойкость препарата в пищеварительных соках, в) способность всасываться
через слизистую пищевого канала и биодоступность, г) цель терапии (для оказания экстренной помощи
предпочтение отдают парентеральному пути введения, особенно внутривенному).
Во время движения ЛВ в организме они проникают через биологические мембраны, имеющие
липопротеиновую структуру, микропоры и ферменты. Различают следующие механизмы
проникновения через мембраны.
1. Пассивная диффузия по градиенту концентрации вещества. Таким способом переносятся
липофильные (обычно неполярные) соединения. Она осуществляется без затраты энергии. Движение
молекул облегчается за счет слабых электростатических взаимодействий (дипольные связи, Ван-дерВаальсовы и др.).
2. Фильтрация через микропоры мембран за счет гидростатического и осмотического давлений, без
затраты энергии. Таким способом переносятся мелкие гидрофильные молекулы и некоторые ионы.
3. Активный транспорт с помощью транспортных систем и затратой энергии, которая образуется
за счет расщепления АТФ. Он может осуществляться против градиента концентрации. Таким способом
переносятся определённые гидрофильные вещества, сахара, ионы, аминокислоты, пиримидины.
4. Пиноцитоз - инвагинация мембраны с образованием пузырька и захватом крупных молекул,
которые продвигаются к противоположной мембране и с помощью экзоцитоза отдают их в
окружающую среду.
ЛВ преодолевают также биологические барьеры, имеющие сложную структуру. Главными
барьерами являются гистогематический, гематоэнцефалический, плацентарный, гематофолликулярный,
гематотестикулярный и эпителий молочных желез. Гистогематическмй барьер представляет собой
капиллярную стенку, состоящую из клеток эндотелия, цементирующего вещества (гиалуроновая
кислота и др.), ферментов и мелких пор. Липоидорастворимые вещества проходят через мембраны
клеток, водорастворимые - через цементирующее вещество и поры. Через капиллярную стенку хорошо
проникают вещества с молекулярной массой до 5-6 тыс. Гематоэнцефалический барьер состоит из
мозговых капилляров и астроцитов (клетки нейроглии). Он обладает избирательной проницаемостью.
Для ионизированных молекул непроницаем. Однако при воспалительных процессах, нарушениях
кислотно-основного состояния, при некоторых нарушениях обмена веществ его проницаемость резко
возрастает, в результате чего мозг становится подвержен вредному действию различных веществ. У
детей до одного года ГЭБ недостаточно сформирован, поэтому слабо защищает ткань мозга не только
от ксенобиотиков (инородных веществ), но и от продуктов метаболизма (напр.,билиру6ин).
Плацентарный барьер очень порозный на ранних стадиях беременности, а также при многих
заболеваниях (воспалительные процессы, токсикозы беременности и др.). Он обеспечивает защиту
плода от ксенобиотиков, однако его защитная роль ограничена. ЛВ с молекулярной массой меньше 400
легко проникают через плаценту путем пассивной диффузии. Проницаемость плаценты зависит от
многих условий и постепенно возрастает до 32-35 недель беременности. Некоторые - вещества
накапливаются в организме плода и могут оказывать токсическое действие. Поэтому во время
беременности, особенно в первые 2-3 мес., назначение ЛС требует особой осторожности.
Гематофолликулярный и гематотестикулярный барьеры защищают половые клетки от
повреждения ксенобиотиками. Они содержат липопротеиновые мембраны и легко проницаемы для
липофильных неионизированных молекул (наркотические средства, алкоголь и Др.). Поэтому возможно
повреждение генного материала (мутагенный эффект). Последствия такого повреждения могут тяжело
отразиться на потомстве. Эпителий молочных желез также легко проницаем для липофильных
соединений. рН молока составляет 6,5-7,0, поэтому ЛВ с основными свойствами ионизируются слабо и
легко проникают в молоко, кислые ЛВ ионизируются а большей степени и проникают хуже. Если ЛС,
принимаемые кормящей матерью, токсичны или могут накапливаться в молоке а опасных
концентрациях, грудное вскармливание ребенка необходимо прекратить или заменить ЛС менее
опасным.
Распределение ЛВ в организме осуществляется системой кровообращения и лимфообращения.
Самые высокие концентрации ЛВ создаются в хорошо кровоснабжаемых органах (мозг, почки, печень,
легкие), самые низкие - в жировой клетчатке, в костях. Распределение зависит от скорости
проникновения ЛВ через биологические мембраны и барьеры. Большая роль принадлежит альбуминам,
которые выполняют связывающую и транспортную функции. Различают 3 фракции вещества: а)
свободная, б) связанная с белками, в) фиксированная в тканях. Фракции находятся в динамическом
равновесии и непрерывно переходят одна в другую. Действие оказывает только свободная фракция, она
же подвергается биотрансформации и экскреции. Поэтому чем выше концентрация в крови и тканях
свободной фракции ЛВ, тем быстрее и сильнее действие. Напр., лишь 3-5% строфантина в крови
связываются с альбуминами, поэтому он быстро проникает в сердечную мышцу и начинает действовать
через 10-15 мин, тогда как дигитоксин связывается с белками крови на 95-97%, поэтому его действие
развивается очень медленно.
Содержание свободной фракции ЛВ в плазме крови зависит от содержания альбуминов. При низком
содержании белков (болезни печени, почек, голодание) концентрация свободной фракции резко
возрастает, что может привести к усилению эффекта и развитию интоксикации, либо, наоборот, к
ослаблению в результате увеличения скорости выведения из организма.
Некоторые ЛВ могут депонироваться в тканях, образуя внеклеточные и клеточные депо.
Депонирование происходит за счет связывания с белками и фосфолипидами. Прочность связывания
различна. Одни ЛВ (напр., средства для наркоза) образуют непрочные комплексы с фосфолипидами и
быстро выводятся из жировых депо. Другие (сульфаниламиды длительного действия, соли тяжелых
металлов) прочно связываются с белками и долго задерживаются в тканях.
Наиболее интегративным показателем фармакокинетических процессов является кривая
концентрации вещества в плазме крови. Под концентрацией понимают сумму свободной и связанной
с белками фракций ЛВ. Она отражает различные фазы фармакокинетики: всасывание, распределение и
элиминацию (обезвреживание) вещества. Кривая отражает время от введения ЛВ до появления
начального эффекта (латентный период действия), время от появления эффекта до его максимума,
время от появления эффекта до его окончания (продолжительность действия). Наиболее важными для
клиники являются время развития максимального эффекта и продолжительность действия лекарства,
следовательно, концентрация зависит от дозы, биодоступности препарата, скорости распределения в
организме, биотрансформации и экскреции.
Биотрансформация (химическое превращение ЛВ) происходит преимущественно в печени, а также
в почках, легких, стенке кишечника и в других органах. Биотрансформации подвергается большинство
ЛВ. Исключение составляют наркозные средства и гидрофильные ионизированные соединения,
которые выделяются в неизмененном виде. Результатом биотрансформации является превращение
липоидорастворимых соединений в водорастворимые и выведение их из организма.
Различают два основных вида биотрансформации - метаболизм и конъюгация. Метаболизм
происходит при участии оксидазных систем, основными компонентами которых являются цитохром Р450
и
НАДФН
(никотинамидадениндинуклеотид-фосфат).
Метаболическое
превращение
осуществляется за счет окисления, восстановления и гидролиза. Большинство веществ
метаболизируется путем окисления, для которого необходим кислород. Поэтому нарушение
кровообращения, гипоксия резко снижают метаболизм ЛВ. Конъюгация представляет
биосинтетический процесс, результатом которого является образование парных соединений ЛВ с
биогенными веществами (глюкуроновая, серная, уксусная кислоты, глютатион, глицин и др.).
Основную роль в биотрансформации играют микросомальные ферменты печени, степень активности
которых обусловливает вариабильность реакции людей на ЛВ. Чем выше их активность, тем ниже
концентрация ЛВ и фармакологический эффект, и наоборот. Активность микросомальных ферментов
снижается при заболеваниях печени, интоксикации алкоголем, другими ядами, нарушениях
кровообращения и т.п.
Экскреция ЛВ происходит преимущественно в почках. Ряд ЛВ выводятся с желчью в просвет
кишечника, легкими, молочными, потовыми и сальными железами. ЛВ экскретируются в виде
метаболитов, конъюгатов или в неизмененном виде. Экскреция зависит от растворимости ЛВ в воде и
жирах. Водорастворимые соединения выводятся с мочой полностью, так как не подвергаются
обратному всасыванию, жирорастворимые легко подвергаются реабсорбции в почечных канальцах.
Имеют значение также реакция мочи (кислые соединения быстрее выводятся щелочной мочой,
основания кислой),кровоснабжение почек (при снижении АД ухудшается клубочковая фильтрация),
патологические процессы в почках. При назначении ЛС эти факторы надо учитывать.
При выведении ЛВ с желчью (тетрациклины, гликозиды и др.) надо учитывать возможность
повторного всасывания в кишечнике. Некоторые ЛВ выделяются через желудок и кишечник (морфин,
соли тяжелых металлов), через молочные железы (большинство липофильных соединений), через
потовые и сальные железы (препараты брома, йода).
Особое значение имеет экскреция ЛВ с молоком. Большинство ЛВ проникает в молоко матери. Если
препарат легко всасывается в кишечнике ребенка, он может попадать в его организм в значительном
количестве и вызывать нежелательные последствия. Поэтому если фармакотерапия матери неизбежна,
кормление ребенка грудным молоком необходимо прекратить в следующих случаях: а) когда ЛВ
выделяется с молоком в таком количестве, которое может вызвать побочные эффекты у ребенка; б)
когда ЛВ даже в небольшом количестве опасно для ребенка; в) когда мать страдает тяжелыми
заболеваниями печени, почек, сердца и у нее резко замедлена элиминация ЛВ.
Под элиминацией ЛВ понимают их инактивацию в результате биотрансформации и экскреции. Она
оценивается по периоду полувыведения препарата и константе элиминации. Период полувыведения это время, за которое концентрация ЛВ в крови уменьшается вдвое. Его обычно используют как
показатель убыли препарата из крови. Константа элиминации - это часть ЛВ в процентах, на которую
уменьшается его содержание в организме за единицу времени (обычно в течение суток). Она должна
учитываться при определении поддерживающей дозы.
Лекция 2.
ОСНОВНЫЕ ПОНЯТИЯ ОБЩЕЙ ФАРМАКОЛОГИИ (продолжение)
В этой лекции мы рассмотрим следующие основные вопросы:
• - что изучает фармакодинамика;
• - понятие о циторецепторах, их виды и локализация, взаимодействие ЛВ с циторецепторами,
агонисты и антагонисты;
* - взаимодействие ЛВ с ферментами, каналами мембран, высвобождение из депонированного
состояния;
• - виды действия ЛВ, факторы, влияющие на действие ЛВ;
* - изменения действия ЛВ при повторном введении (кумуляция, привыкание, лекарственная
зависимость);
* - взаимодействие ЛВ при комбинированном применении;
* - виды лекарственной терапии;
• - осложнения лекарственной терапии.
Фармакодинамика.
Это раздел фармакологии, изучающий механизмы действия, фармакологические, терапевтические и
побочные эффекты ЛВ.
Изменения функций организма под влиянием ЛВ обусловлены взаимодействием его молекул с
молекулами организма, которое обозначают как первичную фармакологическую реакцию, Она
определяет сущность механизма действия ЛВ. ЛВ могут взаимодействовать с циторецепторами,
ферментами, ионными каналами и т.д. Циторецепторами (фармакологическими рецепторами)
называют активные центры макромолекул, встроенных в мембраны или имеющих иную локализацию.
Известны холинорецепторы, адренорецепторы, гистаминорецепторы, серотонинорецепторы, ГАМКрецепторы, опиатные рецепторы и многие другие. Их название связано с эндогенными веществами,
которые взаимодействуют с циторецепторами. Механизм действия (МД) многих ЛВ обусловлен
взаимодействием с циторецепторами. Это взаимодействие может сопровождаться усилением функции
(миметический эффект) или ее ослаблением (литический эффект). Так действуют холиномиметики и
холинолитики, адреномиметики и адренолитики и др. Специфика циторецепторов определяет
специфичность действия ЛВ. Учет этого фактора необходим для правильного выбора ЛВ. Поэтому
необходимо иметь четкое представление о роли и локализации циторецепторов, о взаимодействии с
ними ЛВ и эффектах, которыми сопровождается это взаимодействие.
ЛВ, которые при взаимодействии с циторецепторами оказывают, стимулирующее влияние на
клетки, называют агонистами, а вещества, устраняющие или ослабляющие эффекты агонистов,
называют антагонистами. Антагонисты бывают конкурентными, т.е. конкурирующими с агонистами
за связь с циторецепторамм, и неконкурентными, если они действуют на другие участки молекул,
связанные с циторецепторами. Связь ЛВ с циторецепторами осуществляется за счет межмолекулярного
взаимодействия и может быть прочной (необратимой) и непрочной (обратимой). Она может быть
избирательной (селективной) и неизбирательной (напр., салбутамол и изадрин).
МД ЛВ может быть связан с ингибирующим действием на ферменты. Напр., прозерин, ингибируя
ацетилхолинэстеразу, предохраняет ацетилхолин от ферментативного расщепления, в результате чего
возрастает тонус холинергической системы. МД многих ЛВ связан с блокадой ионных каналов
мембран клеток, в результате чего замедляется движение ионов и уменьшается их содержание в
структурах клетки (напр., блокаторы кальциевых, калиевых, натриевых каналов). Некоторые ЛВ
способствуют выходу ионов и молекул из клеточных и тканевых депо. МД ряда ЛВ обусловлен
истощением запасов медиатора в окончаниях нервов в результате нарушения синтеза или обратного
нейронального захвата.
Таким образом, первичная фармакологическая реакция осуществляется на молекулярном уровне,
поэтому скрыта от непосредственного наблюдения. Она проявляется в виде фармакологических
эффектов, которые могут быть зарегистрированы обычными методами (напр., АД, работа сердца,
органов дыхания, пищеварения и т.п.).
Виды действия ЛВ.
Для понимания причинно-следственных связей большое значение имеет направленность и
локализация действия ЛВ. Различают местное, рефлекторное и резорбтивное действие. Под местным
действием понимают действие ЛВ на месте его приложения. В чистом виде такое действие встречается
крайне редко. Под рефлекторным понимают действие, возникающее в результате раздражения нервных
окончаний и передающееся через ЦНС или с помощью аксон-рефлексов. Оно может возникать как при
местном, так и резорбтивном действии (действие горчичников, цититона). резорбтивное действие - это
действие, возникающее после всасывания (резорбции) ЛВ в кровь. Видами резорбтивного действия
являются прямое и косвенное, основное и побочное, избирательное и общеклеточное, обратимое и
необратимое. Пряное - это действие, возникающее на месте контакта ЛВ с тканью. Косвенное действие, проявляющееся в результате изменения других функций (напр., увеличение диуреза под
влиянием сердечных гликозидов). Под основным понимают такое действие, на которое расчитывает
врач при назначении лекарства (напр., понижение АД под влиянием октадина при гипертонии).
Побочное - это, как правило, нежелательное действие. Оно проявляется изменением тех функций, на
которые лечение не направлено. Напр.,при назначении октадина наряду с понижением АД могут
возникнуть диспептические расстройства. Избирательным (селективным) называют такое действие,
которое проявляется в изменении функций определенного органа или системы. Обычно это связано с
влиянием ЛВ на функционально однозначные циторецепторы (салбутамол, пилокарпин).
Общеклеточное (неизбирательное) действие проявляется неспецифично в разных органах и системах.
Напр., действие наркозных средств, алкоголя. Обратимое - это действие, которое прекращается сразу
после элиминации ЛВ. Необратимое действие возникает в результате образования прочных связей ЛВ
с рецепторами {обычно ковалентных), что приводит к необратимому выключению их функции (напр.,
прозерин вызывает обратимое ингибирование ацетилхолинэстеразы, а фосфакол - необратимое).
Факторы, влияющие на действие Л В.
Их можно подразделить на 3 группы: 1) свойства ЛВ; 2) факторы, связанные с организмом; 3)
факторы внешней среды.
К 1 гр. относят структуру ЛВ, его физико-химические и физические свойства, лекарственную
форму и дозу. Химическое строение ЛВ определяет его МД и токсичность. Чем больше структура
молекул обеспечивает контакт с рецепторами, тем активнее ЛВ. Особенно важно пространственное
соответствие молекул ЛВ и рецепторов. Большое значение имеет степень диссоциации, растворимость в
липидах и воде, способность проникать через мембраны и барьеры. Лекарственная форма и способ ее
введения также играют важную роль. От дозы зависит сила и продолжительность действия, вероятность
возникновения токсических эффектов. Между дозой и концентрацией ЛВ в крови существует прямая
зависимость. Различают разовую, суточную и курсовую дозу. По эффекту различают минимально
действующие, или пороговые дозы, средние терапевтические, высшие разовые и суточные дозы,
токсические и смертельные дозы. Иногда используют ударные дозы, которые превышают средние
терапевтические.
Для оценки активности и безопасности препарата большое значение имеет терапевтический
индекс, под которым понимают отношение дозы, вызывающей гибель 50% животных, к дозе, дающей
фармакологический эффект в 50% случаев. Другим показателем безопасности ЛС является широта
терапевтического действий, которая характеризуется разницей между минимально действующей и
высшей терапевтической дозами. Чем больше эти показатели, тем менее опасно лекарство.
К факторам, связанным с организмом больного, относят возраст, пол, генетические особенности,
состояние больного, биологические ритмы. Возраст больного оказывает большое влияние на действие
ЛВ. Учет этого фактора необходим прежде всего у детей и стариков. Организм ребенка находится в
стадии формирования и созревания, поэтому многие защитные реакции у него развиты слабо.
Основными особенностями, которые необходимо учитывать при назначении ЛС детям, являются
нервно-психический статус, склонность к аллергическим, судорожным и другим неожиданным
реакциям, замедленная биотрансформация и экскреция веществ, недостаточное развитие биологических
барьеров, особенно ГЭБ, слабый иммунитет, особенности обмена веществ. У детей до 2-3 лет понижена
связь ЛВ с белками плазмы, поэтому повышено содержание свободной фракции, что ведет к усилению
эффектов ЛВ. Таким образом, назначение и дозироаание ЛС детям имеет свои особенности и
сложности. Этими проблемами занимается педиатрическая фармакология.
Пожилой (свыше 60 лет) и, особенно, старческий возраст (свыше 75 лет) оказывают значительное
влияние на действие ЛС. В процессе старения происходят существенные сдвиги в обмене веществ,
процессах адаптации, функциональной активности органов и систем. Повышается чувствительность
ЦНС к угнетающим ЛВ, снижается активность стимуляторов. Понижается тонус вегетативной нервной
системы, эндокринных желез и суживаются возможности компенсации. В связи с этим
сосудорасширяющие ЛВ могут легко вызвать коллапс, а сосудосуживающие - чрезмерный подъем АД,
инсульт, так как сосуды становятся ломкими. Повышается склонность к тромбообразованию, поэтому
опасно использовать коагулянты. Снижается содержание альбуминов крови и возрастает свободная
фракция ЛВ, ослабевает биотрансформация ЛВ в печени и экскреция в почках. Поэтому чем старше
возраст больного, тем осторожнее надо назначать лекарства и уменьшать их дозы.
Состояние больного также необходимо учитывать. Ослабленные, истощенные больные нуждаются в
снижении дозы в 1,5-2 раза. При шоке, кровопотере и других тяжелых состояниях резко возрастает
чувствительность к ЛВ угнетающего типа действия (наркотики, нейролептики и Др.). Такие больные
слабо реагируют на действие стимуляторов (аналептики, адреномиметики и др.), а введение их в
повышенных дозах может легко привести к истощению функций. Необходимо также учитывать
сопутствующее заболевания. Напр., при лечении гипертонической болезни бета-адреноблокаторами
необходимо убедиться, что у больного нет наклонности к бронхоспазму.
Пол имеет значение, главным образом, при назначении ЛС беременным, кормящим матерям, в
период меноррагии. Применение ЛС в период беременности и родов может сопровождаться
отрицательными последствиями для плода и ребенка. В период грудного вскармливания ЛВ может
накапливаться в молоке в опасных для младенца концентрациях.
Биологические ритмы представляют собой чередование активности процессов через определенные
интервалы времени. Зависимость действия ЛВ от биоритмических процессов и влияние их на эти
процессы изучает хронофармакология. Биоритмы могут иметь сезонный, месячный и суточный
характер (циркадный). Знание и учет ритмов необходимы для выбора оптимальных режимов
применения ЛС (хронофармакотерапия). Напр., установлено, что максимальная продукция гормонов
коры надпочечников происходит в утренние часы и в это время повышена чувствительность тканей к
ним. Поэтому применение препаратов этих гормонов в утренние часы не только повышает
эффективность терапии, но и уменьшает опасность осложнений.
Некоторые эффекты ЛВ обусловлены генетически. Изучением этой проблемы занимается
фармакогенетика, являющаяся разделом медицинской генетики. К генетически обусловленным
реакциям относится идиосинкразия. Внешне она проявляется покраснением, отеком кожи и слизистых,
нарушением дыхания, АД, лихорадкой и другими растройствами вплоть до шока. Типичным примером
идиосинкразии является сенная лихорадка - бурная реакция некоторых лиц на запах сена.
Наследственно обусловленных реакций на ЛВ известно много. Чаще всего они связаны с
наследственной недостаточностью ферментов (энзимопатии). Напр., при недостатке глюкозо-6фосфатдегидрогеназы
и
глютатион-редуктазы
эритроцитов
противомалярийные
средства,
сульфаниламиды, производные нитрофурана, пиразолона вызывают гемолиз эритроцитов и желтуху.
Фармакогенетика занимается также изучением мутагенных эффектов ЛС. Так как многие реакции
организма на действие ЛВ генетически обусловлены, фармакогенетика имеет большое значение для
индивидуализации лечения и прогнозирования эффективности и безопасности фармакотерапии.
Факторы внешней среды также оказывают определенное влияние на действие ЛВ. К ним относят
социальные условия, вызывающие психоэмоциональное напряжение, сверхсильные шумы, вибрацию,
повышенную радиацию, загрязнение окружающей среды, резкие колебания температуры, влажности и
т.п. Психоэмоциональный стресс может усилить действие ЛС на ЦНС. После длительной вибрации,
сильного шума, резкого охлаждения усиливается действие средств для наркоза, снотворных,
нейролептиков. Облучение приводит к изменению и извращению действия многих ЛС. Некоторые ЛВ
повышают чувствительность организма к солнечным лучам (напр., фотосенсибилизация при лечении
сульфаниламидами).
Изменение действия ЛС при повторных введениях.
Во многих случаях ЛС применяют длительно. При этом их действие может существенно изменяться
- усиливаться или ослабевать. Усиление эффекта может быть обусловлено кумуляцией - материальной
или функциональной. Под материальной кумуляцией понимают накопление ЛВ (дигитоксин, стрихнин
и др.), под функциональной - накопление эффекта ЛВ (алкоголь, кофеин и др.). Следствием кумуляции
является проявление токсических эффектов.
Снижение эффектов ЛС при повторном применении возникает в результате привыкания
(толерантности) организма. Причинами привыкания могут быть уменьшение всасывания, ускорение
биотрансформации и экскреции, снижение чувствительности рецепторов. Чтобы преодолеть
привыкание, надо увеличивать дозы, что нередко приводит к интоксикации. Часто привыкание к
одному препарату сопровождается привыканием к другим ЛС этой группы (перекрестное привыкание к
антибиотикам и др.). Если при повторном введении происходит быстрое ослабление эффекта, такое
привыкание называют тахифилаксией (напр., при введении эфедрина).
Использование нейротропных средств центрального действия может вызвать лекарственную
зависимость (пристрастие), которая сопровождается постоянным желанием принимать ЛС с целью
улучшения настроения, самочувствия (эйфория) или для предупреждения тяжелых ощущений
(абстиненция). Зависимость может быть психической (кокаин) и физической (морфин), при которой
отмена препарата сопровождается тяжелыми психическими и физическими расстройствами. Это
состояние называют наркоманией. Чаще всего она возникает при применении морфина, героина,
кокаина, марихуаны и других наркотиков.
Взаимодействие Л В.
При лечении многих заболеваний используют комбинированную терапию. Чтобы комбинации ЛВ
были эффективными и безопасными, необходимо знать, как они взаимодействуют. Различают 2 вида
взаимодействия - фармацевтическое и фармакологическое. Фармацевтическое взаимодействие может
проявиться в несовместимости ЛВ в процессе изготовления лекарств, их хранения или смешивания в
растворах. При этом происходит снижение или исчезновение активности компонентов смеси или
появление токсичности. Фармакологическое взаимодействие реализуется на уровне фармакокинетики
или фармакодинамики. Взаимодействие на уровне фармакокинетики осуществляется в процессе
всасывания (рассмотрено в 1-й лекции), транспорта, биотрансформации и экскреции. Во время
транспорта ЛВ кровью может возникнуть конкуренция за связь с белками, что сопровождается
повышением концентрации свободной фракции вытесняемого ЛВ. Напр., салицилаты вытесняют
бутамид, который может вызвать гипогликемическую кому. При взаимодействии на уровне
биотрансформации может проявиться индуцирующий или ингибирующий эффекты на микросомальные
ферменты печени. Повышение активности ферментов (индукция) фенобарбиталом, дифенином
сопровождается ускорением биотрансформации других ЛВ, а ингибирование (угнетение) -замедлением
инактивации (напр., при лечении тетурамом). Взаимодействие на уровне экскреции может приводить к
ускорению или задержке в организме ЛВ. Так, ЛВ с основными свойствами ускоряют выведение с
мочой веществ с кислыми свойствами, и наоборот (натрия гидрокарбонат и салицилаты), что можно
использовать при отравлении (напр., введение натрия гидрокарбоната при отравлении салицилатами и
барбитуратами).
Взаимодействие ЛВ на фармакодинамической основе проявляется в форме синергизма или
антагонизма. Синергизм - усиление действия взаимодействующих ЛВ. Он проявляется в 2 формах:
суммирование (аддитивный) и потенцирование. Под первым понимают простое сложение эффектов,
под вторым - умножение эффектов. Синергизм может быть прямым, если ЛВ действуют на один
субстрат, или косвенным, если ЛВ действуют на разные субстраты. Антагонизм - ослабление эффекта
взаимодействующих ЛВ. Он бывает физиологическим, химическим, физико-химическим и физическим.
Физиологический антагонизм проявляется на уровне биологического субстрата, напр., рецепторов. Он
может быть прямым и косвенным, односторонним и двухсторонним. Примером прямого антагонизма
является взаимодействие холиномиметиков и холиноблокаторов. Этот антагонизм является
односторонним, так как холиноблокаторы прекращают действие холиномиметиков, но не наоборот.
Косвенный антагонизм обусловлен взаимодействием ЛВ с разным МД. Напр., пилокарпин вызывает
сужение зрачка, стимулируя холинорецепторы круговой мышцы радужки, а адреналин расширяет
зрачок, стимулируя адренорецепторы радиальной мышцы радужки. Примером двухстороннего
антагонизма является взаимодействие между наркотиками и стимуляторами ЦНС. Химический
антагонизм - это вид химического взаимодействия, в результате которого образуется неактивное
соединение и утрачивается фармакологический эффект (напр., при взаимодействии унитиола и
сердечных гликозидов). Примером физико-химического антагонизма является нейтрализации
действия гепарина протамина сульфатом в результате электростатического взаимодействия.
Физический антагонизм обусловлен физическими свойствами ЛВ. Напр., активированный уголь
адсорбирует на своей поверхности молекулы многих веществ.
Антагонизм является основой антидотной терапии, т.е. лечения отравлений с помощью
антагонистов. Напр., при отравлении холиномиметиками широко используют холиноблокаторы, при
отравлении морфином применяют его антагонист налоксон, при отравлении мышьяком, солями
тяжелых металлов, сердечными гликозидами назначают унитиол, активированный уголь используют
для адсорбции ядов, попавших в кишечник.
Виды лекарственной терапии.
ЛС используют для профилактики и лечения заболеваний. Основными видами фармакотерапии
являются этиотропная, патогенетическая и симптоматическая. Этиотропная ФТ имеет целью
устранение причины заболевания. Примером такой ФТ является использование противомикробных ЛС
(антибиотики, сульфаниламиды, противопаразитарные и др.). Патогенетическая ФТ направлена на
патогенез заболевания. Напр., применение сердечных гликозидов при недостаточности сердца.
Разновидностью ее является заместительная терапия (назначение инсулина при сахарном диабете,
витаминов при гиповитаминозах и авитаминозах). Симптоматическая ФТ направлена на устранение
симптомов заболевания (аналгетики, стимуляторы дыхания и др.).
Осложнения лекарственной терапии.
Наряду с терапевтическим действием ЛС могут оказывать побочное действие. Существуют
различные классификации побочных эффектов. Их можно сгруппировать в следующие 4 группы.
1. Осложнения, связанные с абсолютной и относительной передозировкой препаратов (отравления
ЛС): а) абсолютная передозировка -превышение предельно допустимой дозы; б) относительная
передозировка -слишком быстрое введение препарата в кровь, тяжелые заболевания органов
элиминации (печень, почки, сердечно-сосудистая система).
2. Осложнения, связанные с токсическими свойствами ЛС при длительном применении:
нейротоксические, гепатотоксические, нефротоксические, гематотоксические, ульцерогенные (язва
желудка, 12-перстной кишки), обострение скрыто протекающих заболеваний, синдром отмены,
мутагенное, тератогенное, эмбриотоксическое действие, угнетение иммунозащитных свойств
организма.
3. Осложнения, обусловленные повышенной чувствительностью организма: аллергические
реакции, идиосинкразия.
4. Лекарственная зависимость (пристрастие, наркомания). Осложнения, связанные с абсолютной
передозировкой не нуждаются в коментариях. Относительная передозировка может возникнуть, если
врач не учитывает скорость распределения ЛВ в организме или состояние органов элиминации. Напр.,
при быстром введении строфантина в вену его концентрация в сердце нарастает слишком быстро, что
может вызвать нарушения сердечного ритма. При тяжелых болезнях печени замедляется
биотрансформация ЛВ, а при нарушении выделительной функции почек - их выведение, что
сопровождается повышением их концентрации и токсичности. Во всех случаях нарушения элиминации
ЛС возрастает риск их кумуляции и осложнений.
Токсические свойства ЛС являются специфическими, так как обусловлены их структурой. Напр.,
для актибиотиков-аминогликозидов характерно поражение черепномозговых нервов и почек, для
левомицетина - кроветворного аппарата, для бутадиона - ульцерогенное действие, для бетаадреноблокаторов - усиление скрыто протекающей сердечной недостаточности. Синдром отмены
возникает при внезапном прекращении лечения. Напр., внезапная отмена глюкокортикоидов может
вызвать синдром острой надпочечниковой недостаточности.
Большой проблемой является мутагенное, тератогенное и эмбриотоксическое действие ЛС.
Мутагенный эффект возникает в результате воздействия ЛВ на половые клетки (противоопухолевые
ЛС и др.), что может сопровождаться наследственно обусловленными заболеваниями. Тератогенное
действие возникает при назначении ЛС во время беременности. Оно проявляется, в виде аномалий
развития плода, или уродств. Особое внимание к этому эффекту возникло после "талидомидной
катастрофы" в начале 60-х гг. Применение талидомида во время беременности сопровождалось
массовыми уродствами плода. В связи с этим многие страны приняли законодательства для
предупреждения подобных случаев. Теперь ни один новый препарат без проверки на тератогенность не
допускают к применению.
При назначении ЛС беременным надо учитывать критические периоды в развитии эмбриона, во
время которых внешние воздействия легко изменяют морфогенез и вызывают аномалии развития или
гибель плода: период имплантации (1-2 недели), период плацентации (3-4 недели) и период
органогенеза (3-8 нед.). Следовательно, наиболее опасным является 1-й триместр беременности (2-3
мес), когда идет закладка и формирование органов и систем. Тератогенное действие может проявиться
морфологически и иеморфологически. К 1-му виду относят дефекты развития органов, ко 2-му дефекты развития психики. Особой осторожности требует назначение ЛС в первые 2-3 мес.
беременности. Отрицательное действие на плод может проявиться не только тератогенными
эффектами, но и задержкой развития или гибелью плода и эмбриона. Если эти эффекты возникают в
первые 12 недель беременности, их называют эмбритоксическими, если позже - фетотоксическими.
Угнетение иммунозащитных свойств организма (иммунодепрессивный эффект) сопровождается
обострением скрыто протекающих инфекций (напр., кортикостероиды, цитостатики).
Аллергические реакции являются наиболее распространенными осложнениями ФТ. Они
обусловлены образованием антител на ЛС, которые либо сами обладают антигенными свойствами, либо
приобретают их в процессе превращения в организме, либо индуцируют образование антигенов. Этот
процесс повышения чувствительности организма к ЛВ называют сенсибилизацией. Аллергические
реакции бывают немедленного и замедленного типов. Наиболее опасной из них является
анафилактический шок. Идиосинкразия и пристрастие были рассмотрены выше.
Усвоение основных принципов и понятий общей фармакологии является непременным условием для
изучения частной фармакологии.
Лекция 3.
ЛС, ДЕЙСТВУЮЩИЕ НА АФФЕРЕНТНУЮ ИННЕРВАЦИЮ.
К
ним
относятся:
1)
ЛС,
снижающие
чувствительность
афферентных
нервов
(местноанестезирующие); 2) ЛС, защищающие нервные окончания от раздражения (вяжущие,
обволакивающие, адсорбирующие, мягчительные); 3) ЛС, стимулирующие афферентную иннервацию
(раздражающие). Необходимо изучить:
* - понятие местной анестезии и ее отличие от общей анестезии;
* - МД местных анестетиков и их классификацию; - всасывание, распределение и элиминацию
анестетиков; - системные эффекты анестетиков, виды местной анестезии; - особенности
фармакокинетики, фармакодинамики и применения кокаина, дикаина, новокаина, лидокаина,
тримекаина, совкаина, сущность кокаиновой наркомании;
* - механизм защитного действия вяжущих, обволакивающих, адсорбирующих и мягчительных средств,
их применение;
* - механизмы местного и системного действия раздражающих средств, применение.
Местноанестезирующие средства.
Под местной анестезией понимают выключение чувствительности при прямом контакте ЛВ с
нервными проводниками и рецепторами без выключения сознания, рефлексов и мышечного тонуса (в
отличие от наркоза). Местные анестетики - это ЛВ, вызывающие обратимое угнетение проводимости и
возбудимости рецепторов и проводников при нанесении на них.
Первым анестетиком был кокаин, полученный Ниманом и Вилером в 1859 г. из листьев кока,
которые с древних времен использовались индейцами Южной Америки в качестве тонизирующего
средства. Впервые действие кокаина изучил русский ученый Анреп в 1879 г., который предложил
использовать его в качестве обезболивающего средства.
Большинство местных анестетиков являются аминами, у которых аминогруппа соединена с
ароматическим радикалом эфирной или амидной связью. Поэтому по химическому строению они
делятся на 2 группы: 1) сложные зфиры аминоспиртов и ароматических кислот, 2) замещенные амиды
кислот. К первым относятся кокаин (производное бензойиой кислоты), новокаин, дикаин, анестезин
(производные парааминобензойной кислоты), ко вторым -ксикаин (лидокаин) и тримекаин
(производные ксилидина), совкаин (производное холинкарбоновой кислоты). Препараты, имеющие
амидную связь, обладают более длительным действием, чем анестетики с эфирной связью, которая
разрушается эстеразами крови и тканей.
Для проявления анестезирующего эффекта анестетики должны пройти следующие этапы
превращении: 1) используемая соль анестетика хорошо растворима в воде, но плохо в липидах,
поэтому через мембраны поникает слабо и анестезирующим действием не обладает; 2) в тканевой
жидкости соль анестетика превращается в неионизированное липофильное основание, которое хорошо
проникает через мембраны; 3) основание анестетика приобретает катионную форму, которая
взаимодействует с рецепторами внутри натриевых каналов мембран, в результате чего нарушается
прохождение ионов натрия (и калия) через каналы мембран. Это препятствует возникновению
потенциала действия и вызывает блок проведения и генерации импульсов. Имеет значение также
конкурентное взаимодействие с ионами кальция, которые регулируют "открытие-закрытие" ионных
каналов. В этом проявляется аналогия а действии местных и общих анестетиков: те и другие блокируют
генерацию возбуждения в мембранах. Поэтому наркотические вещества (эфир и др.) могут вызвать
местную анестезию, а местные анестетики при в/в введении - общую анестезию. С этим, очевидно,
связан потенцирующий эффект при совместном применении местных анестетиков. наркотических,
снотворных и анальгезирующих ЛС.
Местные анестетики блокируют проведение возбуждения по всем видам нервных волокон:
чувствительным, двигательным, вегетативным, но с разной скоростью и в разных концентрациях.
Наиболее чувствительны к ним тонкие безмякотные волокна, по которым проводится болевая,
тактильная и температурная чувствительность, затем - симпатические волокна, что сопровождается
расширением сосудов, и в последнюю очередь блокируются двигательные волокна. Восстановление
проведения импульсов идет в обратном порядке.
Местная анестезия развивается только при непосредственном контакте с анестетиком. При
резорбтивном действии ЦНС парализуется раньше, чем устраняется местная чувствительность.
Обезвреживание анестетиков осуществляется путем биотрансформации. Вещества с эфирной
связью гидролизуются эстеразами: новокаин холинэстеразой плазмы, кокаин, дикаин, анестезин эстеразами печени. Биотрансформация анестетиков с амидной связью просходит в печени путем ее
разрушения (напр., лидокаин). Продукты распада выводятся печеночным кровотоком. Сниженный
печеночный кровоток способствует удлинению периода полураспада и увеличению концентрации в
крови, что может привести к интоксикации. Анестетики легко проникают в легкие, печень, почки, ЦНС,
через плаценту. Если в кровь поступает значительное количество вещества, возникает токсический
эффект: возбуждение, затем паралич центров продолговатого мозга. Это проявляется вначале
беспокойством, одышкой, повышением АД, бледностью кожи, повышением температуры, а затем угнетением дыхания и кровообращения. При интоксикации применяют кислород, искусственную
вентиляцию легких, в/в введение барбитуратов, сибазона, адреналина, норадреналина.
Аллергические реакции наиболее часто вызывают анестетитики с эфирной связью, особенно
новокаин. Наиболее опасной из них является анафиликтический шок.
Местные анестетитики используют для следующих видов анестезии:
Терминальная (концевая, поверхностная, аппликационная) - путем нанесения анестетика на
слизистые оболочки. Применяют анестетики, хорошо всасывающиеся через слизистые (кокаин, дикаин,
лидокаин, анестезин). Их используют в оториноларингологии, офтальмологии, урологии, стомалогии,
при лечении ожогов, ран, язв и т.п.
Проводниковая (регионарная) - блокада нервных волокон. При этом нарушается проведение
импульсов к ЦНС и утрачивается чувствительность в той области, которая иннервируется данным
нервом. Используют новокаин, лидокаин, тримекаин. Одним из вариантов этой анестезии является
спинномозговая, которая осуществляется введением анестетика в субдуральное пространство.
Инфильтрационная анестезия проводится путем послойного пропитывания тканей р-ром
анестетика. При этом выключаются рецепторы и проводники. Используют новокаин, лидокаин и
тримекаин. Этот вид анестезии широко применяют в хирургии.
Внутрикостная анестезия осуществляется введением анестетика в губчатое вещество кости, выше
места введения накладывают жгут. Распределение анестетика происходит в тканях конечности.
Длительность анестезии определяется допустимым сроком наложения жгута. Этот вид анестезии
используют в ортопедии и травматологии.
Выбор вида анестезии зависит от характера, объема и травматичности оперативного
вмешательства. Для каждого вида анестезии имеются препараты выбора и техника исполнения. Выбор
анестетика зависит от способности поникать в слизистые оболочки, от силы и длительности действия и
токсичности. При диагностических и малотравматичных вмешательствах на поверхностно
расположенных участках применяют терминальную анестезию. Для инфильтрационной,
проводниковой и внутрикостной анестезии применяют малотоксичные и относительно безопасные
средства. Для спинномозговой анестезии обычно используют совкаин, обладающий сильным и
длительным действием, а также лидокаин. Важно правильно выбрать концентрацию р-ра.
Слабоконцентрированные р-ры, введенные в большом количестве, распространяются в тканях широко,
но плохо диффундируют через мембраны, тогда как концентрированные р-ры в малом количестве
распространяются хуже, но диффундируют лучше. Эффект же зависит не от общего количества
анестетика, а от той его части, которая проникает в нервные образования. Поэтому увеличение
количества р-ра еще не означает усиления анестезирующего эффекта, часто это приводит лишь к
усилению токсического действия.
При анестезии хорошо васкуляризированных тканей (лицо, полость рта, глотка, гортань и др.)
анестетик всасывается быстро, что может привести к интоксикации. Чтобы уменьшить этот эффект и
удлинить действие препарата, добавляют сосудосуживающие ЛС (адреналин, норадреналин). При этом
концентрация адреналина не должна превышать 1:200000 (1 мл на 200 мл анестетика), так как сам
адреналин может вызвать тахикардию, гипертензию, головную боль, беспокойство.
Характеристика отдельных анестетиков.
Кокаин - алкалоид из листьев Эритроксилон Кока, произрастающего в Южной Америке.
Всасывается хорошо, анестезия наступает через 3-5 мин, продолжительность эффекта - 30-60 мин.
Оказывает выраженное симпатомиметическое действие, угнетая обратный нейрональный захват
норадреналина, дофамина и серотонина в синапсах. Это сопровождается стимуляцией ССС и ЦНС и
развитием пристрастия. Действие на ЦНС проявляется эйфорией, беспокойством, возбуждением,
которое может прогрессировать в психозы с галлюцинациями, спутанностью сознания, параноидным
мышлением, судорогами, рвотой, сердечными аритмиями. Это обусловлено дофаминергическими и
серотонинергическими эффектами кокаина. Спазмы сосудов, повышение АД, тахикардия, снижение
аппетита являются следствием адреномиметического эффекта. Симптомы возбуждения при
интоксикации быстро сменяются угнетением ЦНС, дыхания и кровообращения. К кокаину особенно
чувствительны дети. Смерть обычно наступает от паралича дыхательного центра. Для оказания
неотложной помощи в/в вводят тиолентал-натрий, диазепам, аминазин, проводят искусственную
вентиляцию легких. Кокаинизм возникает при длительном применении кокаина и приводит к
интеллектуальной и моральной деградации. Абстиненция (болезнь воздержания) проявляется
психическими и вегетативными расстройствами.
Новокаин по силе анестезирующего эффекта уступает кокаину в 2 раза, но в 4 раза менее токсичен.
Применяют для инфильтрационной (0,25-0,5%), проводниковой (1-2%) анестезии и для различных
видов блокад. Действует около 30 мин. При передозировке вызывает повышение рефлекторной
возбудимости, тошноту, рвоту, падение АД, слабость, нарушение дыхания. Нередко наблюдается
идиосинкразия (сыпь, зуд, отек подкожной клетчатки, головокружение). При интоксикации назначают
тиопентал-натрий, диазепам, эфедрин, строфантин, искусственное дыхание.
Дикаин по силе действия превосходит новокаин в 15 раз, но в 10 раз токсичнее его и 2 раза
токсичнее кокаина. Используют для поверхностной анестезии слизистых оболочек, детям до 10 лет
противопоказан.
Лидокаин (ксикаин) действует сильнее и продолжительнее новокаина в 2-3 раза. Применяется для
всех видов анестезии. Переносится хорошо, но при быстром всасывании может вызвать коллапс.
Тримекаин сильнее новокаина в 2,5-3 раза и менее токсичен. По своим свойствам близок к
лидокаину. Используют для инфильтрационной и проводниковой анестезии, иногда для терминальной
(2-5%).
Совками сильнее новокаина в 15-20 раз и в 6-8 раз превосходит его по продолжительности действия,
поэтому удобен для спинномозговой анестезии. Однако по токсичности превосходит новокаин в 15-20
раз, в связи с чем опасен для инфильтрационной и проводниковом анестезии.
Вяжущие средства.
Коагулируют белки на поверхности слизистых оболочек, образуя пленку, которая защищает их от
повреждающих факторов. При этом происходит "стягивание" поверхности слизистой, сужение сосудов
и уменьшение воспаления. Вяжущие средства делятся на органические и неорганические. К 1 гр.
относятся танин, танальбин, теальбин, настои и отвары из коры дуба, корневища лапчатки, цветов
ромашки, корневища змеевика, ягод черники и др. Ко 2 гр. относятся слабые р-ры солей цинка, меди,
алюминия, свинца. Они образуют плотные альбуминаты, которые составляют основу защитной пленки.
Вяжущие ЛС используют для лечения кожных заболеваний, воспалительных заболеваний полости
рта, носа, зева, гортани, кишечника. При заболеваниях кишечника применяют танальбин, теальбин,
настои, отвары. При отравлениях алкалоидами (морфин, атропин и др.) используют танин. Однако его
соединения с алкалоидами нестойки и их надо быстро удалить. Танин также осаждает соли .тяжелых
металлов и гликозиды, поэтому его применяют для промывания желудка при отравлении этими
веществами.
Обволакивающие средства.
Это вещества, которые набухают в воде, образуя коллоидные р-ры, обволакивающие слизистую
оболочку и защищающие ее. Используют различные крахмалы, семена льна, клубни салепа, магния
силикат, гидрат окиси алюминия и др. Их применяют для лечения воспалительных заболеваний
кишечника в виде слизей и в комбинации с раздражающими веществами.
Адсорбирующие средства.
К ним относятся мелко измельченные индифферентные порошки с большой адсорбционной
поверхностью: уголь активированный, тальк, белая глина и др. Они адсорбируют различные вещества и
защищают слизистые от раздражения, а также препятствуют их всасыванию. Применяют при
диспептических расстройствах, метеоризме, воспалительных заболеваниях ЖКТ, при отравлениях.
Мягчительные средства.
Включают жиры, жироподобные и жирорастворимые вещества. Их используют либо самостоятельно
при заболеваниях кожи и слизистых, либо в качестве основы для мазей, паст, линиментов, свечей
(вазелин, масло вазелиновое, ланолин, глицерин, воск, масло какао, очищенное свиное сало,
растительные масла, парафин и др.
Раздражающие средства.
Возбуждают чувствительные нервные окончания, что сопровождается местными и рефлекторными
эффектами (улучшение кровоснабжения, изменение трофики тканей и т.п.). Кроме того некоторые
способствуют освобождению из связанного состояния биологически активных веществ (гистамин,
брадикинин и др.), оказывающих местное сосудорасширяющее действие, которое сопровождается
гиперемией и улучшением питания тканей. Раздражающие ЛС применяют для ослабления боли в
области пораженнного органа ("отвлекающее" действие) и для улучшения трофики больных органов.
Это действие осуществляется рефлекторно. При этом используют взаимосвязь определенных участков
кожи через соответствующий сегмент спинного мозга с определенными внутренними органами (зоны
Захарьина-Геда). Возникновение потока импульсов с кожи приводит к погашению доминантного очага
возбуждения в ЦНС, возникшего под влиянием потока импульсов из пораженного органа. Имеют
значение также аксон-рефлексы, которые замыкаются между сегментами кожи и больным органом,
минуя ЦНС. Все эти эффекты приводят к улучшению кровоснабжения и трофики органа, ослаблению
боли и воспаления.
В качестве раздражающих средств применяют горчичники, скипидар, камфору, ментол, р-р аммиака
и др. МД горчицы состоит в том, что при смачивании горчичника теплой водой (до 40 град.) под
влиянием фермента мирозина происходит расщепление гликозида синигрина с образованием эфирного
горчичного масла, оказывающего раздражающее действие. Аналогичными свойствами обладают и
другие эфирные масла. Особенностью ментола является способность избирательно возбуждать
холодовые рецепторы, что вызывает ощущение холода. Это приводит к рефлекторному расширению
сосудов внутренних органов (сердца, мозга и др.). Ментол входит в состав валидола, который
применяют при стенокардии. Эфирные масла используют при миозитах, невралгиях, заболеваниях
органов дыхания, мигрени, стенокардии и др. Р-р аммиака {нашатырный спирт) применяют для
стимуляции дыхания при обмороках, опьянении. Раздражая рецепторы дыхательных путей, он
стимулирует дыхание и может вызвать рвоту (напр., при опьянении).
Лекция 4.
ЛС, ВЛИЯЮЩИЕ НА ЭФФЕРЕНТНУЮ ИННЕРВАЦИЮ.
К ним относятся вещества, влияющие на передачу нервных импульсов в холинергических и
адренергических синапсах. К эфферентным нервам относятся вегетативные (парасимпатические и
симпатические) и двигательные (соматические) нервы. Первые иннервируют преимущественно
внутренние органы, вторые - скелетные мышцы. По названию медиатора, осуществляющего передачу
импульсов в синапсах, все эфферентные нервы подразделяют на холинергические (ацетилхолин) и
адренергические (норадреналин). К холинергическим относятся двигательные нервы, все
преганглионарные, постганглионарные парасимпатические нервы, а также симпатические нервы,
иннервирующие потовые железы. К адренергическим относятся постганглионарные симпатические
нервы.
В этом лекции мы рассмотрим следующие основные вопросы:
* - структура синапса и понятие о медиаторах;
* - классификация синапсов и их распределение;
* - механизм передачи импульсов в холинергических синапсах;
* - виды холинергических синапсов и их локализация в организме;
* - классификация ЛС, влияющих на передачу импульсов в холинергических синапсах;
*- основные эффекты ацетилхолина (АЦХ);
* - МД антихолиэстеразных средств, их фармакологические эффекты, показания и противопоказания к
применению, побочные эффекты;
* - МД и эффекты м-холиномиметиков, их применение;
* - МД н-холиномиметиков, основные эффекты и применение.
Структура различных синапсов принципиально одинакова. Синапс - это место контакта окончания
нервного волокна с эффекторной клеткой или с другим нервным окончанием. В синапсе различают
пресинаптическую часть, постсинаптическую часть и разделяющую их синаптическую щель. На
окончании нервного волокна расположена пресинаптическая мембрана, на иинервируемой клетке постсинаптическая мембрана. Синаптическая щель заполнена гелем.
Термин "синапс" ввел английский ученый Шерингтон в 1897 г., а медиатор впервые обнаружил
австрийский ученый Леви в 1921 г. Учение о синаптической передаче окончательно сформировалось в
40-х годах. Соответственно медиатору синапсы называют холннергическими и адренергическими.
Холинергические синапсы находятся в поперечнополосатых мышцах, во всех вегетативных ганглиях, в
окончаниях парасимпатических постганглионарных волокон, в мозговом слое надпочечников, в
потовых железах, в каротидных клубочках, в сосудах скелетных мышц, в ЦНС (кора, латеральное
коленчатое тело, ядра ствола мозга, клетки Рэншоу). Адренергические синапсы расположены в
окончаниях постганглионарных симпатических волокон, за исключением потовых желез, в ЦНС
(гипоталамус, средний мозг, полосатое тело, базальные ганглии).
Медиатор холинергических синапсов ацетилхолин образуется в нервном окончании из холина и
ацетата под влиянием фермента холинацетилазы и накапливается в везикулах, из которых
выбрасывается через пресинаптическую мембрану а синаптическую щель под влиянием нервного
импульса, быстро достигая постсинаптической мембраны с расположенными на ней
холинорецепторами.
Холинорецепторы
(ХР)
представляют
собой
активные
центры
специализированных белковых молекул, встроенных в мембрану. После взаимодействия с ХР АЦХ
разрушается ацетилхолинэстеразой. При этом холин подвергается обратному захвату нервными
окончаниями, а ацетат включается в цикл Кребса.
Передача импульсов в синапсе осуществляется следующим образом. Импульс вызывает движение
ионов и повышает проницаемость пресинаптической мембраны, через которую из прилегающих
везикул АЦХ выделяется в синаптическую щель. До взаимодействия АЦХ с ХР постсинаптическая
мембрана находится в состоянии покоя (поляризации). Она имеет положительный заряд на внешней
поверхности (в основном за счет ионов натрия) и отрицательный на внутренней поверхности (за счет
отрицательно заряженных анионов кислот). Разность потенциала составляет 70 мв (потенциал покоя).
При взаимодействии АЦХ с ХР изменяется их конфигурация и открываются ионные каналы, по
которым ионы натрия устремляются внутрь клетки, а ионы калия - из клетки (по градиенту
концентрации). Возникает потенциал действия (около 110 мв) и фаза деполяризации мембраны.
Возбуждение передается на клетку. После расщепления АЦХ холинэстеразой ХР восстанавливают свою
конфигурацию, натрий вытесняется из клетки, а калий возвращается в клетку с помощью натриевокалиевого насоса мембраны. Происходит реполяризация мембраны, т.е. восстановление исходного
состояния.
Существуют два типа ХР. Одни избирательно реагируют не только на АЦХ, но и на яд гриба
мухомора мускарин. Их назвали мускариночувствительными (м-холинорецепторы). Другие
проявляют высокую чувствительность не только к АЦХ, но и к яду листьев табака никотину. Их
назвали никотиночувствительными (н-холинорецепторы). М-ХР локализованы в гладких мышцах
глаза, ЖКТ, бронхов, желчевыводящих и мочевыводящих путей, сосудов скелетных мышц, тазовых
органов, в секреторных клетках слюнных, желудочных, кишечных, бронхиальных, потовых желез, в
ЦНС. Н-ХР находятся в вегетативных ганглиях, в мозговом слое надпочечников, в каротидных
клубочках, в скелетных мышцах, в мышцах диафрагмы, голосовых связок, в ЦНС.
ХОЛИНЕРГИЧЕСКИЕ СРЕДСТВА.
Холинергическими называют вещества, усиливающие или угнетающие передачу - импульсов в
холинергических синапсах. Их подразделяют на холиномиметические к холиноблокирующие ЛС.
Каждая из этих групп делится на подгруппы в зависимости от влияния на те или иные ХР.
1. Холиномиметические ЛС: а) м-н-холиномиметики прямого действия (ацетилхолин, карбахолин);
б) м-н-холиномиметики непрямого действия, или антихолинэстеразные (физостигмин, прозерин,
галантамин, фосфакол); б) м-холииомиметики (пилокарпин, ацеклидин); в) н-холиномиметики
(лобелин, цититон).
2. Холиноблокирующие ЛС: а) м-холиноблокаторы (атропин, платифиллин, скололамин,
гиосциамин, гоматропин, метацин); б) н-холиноблокаторы-ганглиоблокаторы (бензогексоний,
пентамин, пахикарпин, арфонад, гигроний, пирилен); миорелаксанты (тубокурарин, дитилин,
анатруксоний).
Холиномиметические ЛС.
М-н-холиномиметики ПРЯМОГО действия. АЦХ быстро разрушается холинэстеразой, поэтому
действует непродолжительно (5-15 мин при п/к введении), карбахолин разрушается медленно и
действует до 4 ч. Эти вещества производят все эффекты, связанные с возбуждением холинергических
нервов, т.е. мускарино- и никотинолодобные.
Возбуждение м-ХР приводит к повышению тонуса гладких мышц, увеличению секреции
пищеварительных, бронхиальных, слезных и лотовых желез. Это проявляется следующими эффектами.
Происходит сужение зрачка (миоз) в результате сокращения круговой мышцы радужной оболочки
глаза; снижение внутриглазного давления, так как при сокращении мышцы радужки расширяются
шлемов канал и фонтановы пространства, по которым увеличивается отток жидкости из передней
камеры глаза; спазм аккомодации в результате сокращения ресничной мышцы и расслабления цинновой
связки, регулирующих кривизну хрусталика, который становится более выпуклым и устанавливается на
ближнюю точку -видения. Секреция слезных желез возрастает. Со стороны бронхов наблюдается
повышение тонуса гладкой мускулатуры и развитие бронхоспазма, увеличение секреции бронхиальных
желез. Повышается тонус и усиливается перистальтика ЖКТ, возрастает секреция пищеварительных
желез, повышается тонус желчного пузыря и желчевыводящих путей, усиливается секреция
поджелудочной железы. Возрастает тонус мочевого пузыря, мочеточников, уретры, усиливается
секреция потовых желез. Стимуляция м-ХР сердечно-сосудистой системы сопровождается урежением
ритма сердца, замедлением проводимости, автоматизма и сократимости миокарда, расширением
сосудов скелетных мышц и органов малого таза, снижением АД.
Возбуждение н-ХР проявляется учащением и углублением дыхания в результате стимуляции
рецепторов сонной пазухи (каротидных клубочков), откуда рефлекс передается в дыхательный центр.
Увеличивается выделение адреналина из мозгового слоя надпочечников в кровь, однако его
кардиотоническое и сосудосуживающее действие подавляется угнетением работы сердца и гипотензией
в результате стимуляции м-ХР. Эффекты, связанные с увеличением передачи импульсов через
симпатические ганглии (сужение сосудов, усиление работы сердца), также маскируются эффектами,
обусловленными возбуждением м-ХР. Если предварительно ввести атропин, блокирующий м-ХР, то
действие м-н-холииомиметиков на н-ХР проявляется отчетливо. АЦХ и карбахолин повышают тонус
скелетных мышц и могут вызвать их фибриляцию. Этот эффект связан с усилением передачи импульсов
с окончаний двигательных нервов на мышцы в результате стимуляции н-ХР. В больших дозах они
блокируют н-ХР, что сопровождается угнетением ганглионарной и нервно-мышечной проводимости и
снижением секреции адреналина из надпочечников. Через ГЭБ эти вещества не проникают, так как
имеют ионизированные молекулы, поэтому в обычных дозах на ЦНС не влияют. Карбахолин можно
использовать для снижения внутриглазного давления при глаукоме, при атонии мочевого пузыря.
М-н-холиномиметики
непрямого
действия
(антихолинэстеоазные).
Это
вещества,
стимулирующие м- и н-ХР за счет накопления АЦХ в синапсах. МД обусловлен угнетением
холинэстеразы, что приводит к замедлению гидролиза АЦХ и увеличению его концентрации в
синапсах. Накопление АЦХ под их влиянием воспроизводит все эффекты АЦХ (за исключением
стимуляции дыхания). Перечисленные выше эффекты, связанные со стимуляцией м- и н-ХР,
характерны для всех ингибиторов холинэстеразы. Действие их на ЦНС зависит от проникновения через
ГЭБ. Вещества, содержащие третичный азот (физостигмин, галантамин, фосфакол), хорошо проникают
в мозг и усиливают холинергические влияния, а вещества с четвертичным азотом (прозерин) проникают
плохо и действуют преимущественно на периферические синапсы.
По характеру действия на холинэстеразу они подразделяются на вещества обратимого и
необратимого действия. К первым относятся физостигмин, галантамин и прозерин. Они вызывают
обратимую инактивацию холинэстеразы, так как образуют с ней непрочную связь. Вторую группу
составляют фосфорорганмчвские соединения (ФОС), которые используют не только в виде ЛС
(фосфакол), но и для уничтожения насекомых (хлорофос, дихлофос, карбофос и др.), а также а качестве
боевых отравляющих веществ нервно-паралитического действия (зарин и др.). они образуют с
холинэстеразой прочную ковалентную связь, которая очень медленно гидролизуется водой (около 20
суток). Поэтому угнетение холинэстеразы приобретает необратимый характер.
Антихолинэстеразные ЛС применяют при следующих заболеваниях: 1) остаточные явления после
полиомиэлита, травм черепа, кровоизлияний в мозг (галантамин); 2) миастения - заболевание,
характеризующееся прогрессирующей мышечной слабостью (прозерин, галантамин); 3) глаукома
(фосфакол, физостигмин); 4) атония кишечника, мочевого пузыря (прозерин); 5) передозировка
мышечных релаксантов (прозерин). Эти вещества противопоказаны при бронхиальной астме и
заболеваниях сердца с нарушением проводимости.
Отравления чаще всего возникают при попадании в организм ФОС, обладающих необратимым
действием. Вначале развивается миоз, нарушение аккомодации глаза, саливация и затруднение
дыхания, повышение АД, позывы на мочеиспускание. Тонус мышц нарастает, усилвается бронхоспазм,
резко затрудняется дыхание, развивается брадикардия, снижается АД, рвота, понос, фибриллярные
подергивания мышц, возникают приступы клонических судорог. Смерть, как правило, связана с резким
нарушением дыхания. Первая помощь состоит во введении атропина, реактиваторов холинэстеазы
(дипероксим и др.), барбитуратов (для снятия судорог), гмпертензивных ЛС (мезатон, эфедрин),
искусственной вентиляции легких (лучше кислородом).
М-холиномиметики. Мускарин не применяется из-за высокой токсичности. Его используют в
научных исследованиях. В качестве ЛС применяют пилокарпин и ацеклидин. МД этих ЛВ связан с
прямой стимуляцией м-ХР, что сопровождается фармакологическими эффектами, обусловленными их
возбуждением. Они проявляются сужением зрачка, понижением внутриглазного давления, спазмом
аккомодации, повышением тонуса гладких мышц бронхов, ЖКТ, желче- и мочевыводящих путей,
увеличением секреции бронхиальных, пищеварительных желез, потовых желез, снижением
автоматизма, возбудимости, проводмости и сократимости миокарда, расширением сосудов скелетных
мышц, половых органов, снижением АД. Из этих эффектов практическое значение имеют снижение
внутриглазного давления и повышение тонуса кишечника. Остальные эффекты чаще всего вызывают
нежелательные последствия: спазм аккомодации нарушает адаптацию зрения, угнетение работы сердца
может вызвать нарушение кровообращения и даже внезапную остановку сердца (синкопэ). Поэтому
вводить эти препараты в/в не рекомендуется. Нежелательны также снижение АД. спазм бронхов,
гиперкинезы.
Действие м-холиномиметиков на глаз имеет большое значение при лечении глаукомы, которая
нередко дает обострения (кризы), являющиеся частой причиной слепоты и поэтому нуждаются в
экстренной терапии. Закапывание в глаз р-ров холиномиметиков вызывает снижение внутриглазного
давления. Их также применяют при атонии кишечника. При глаукоме применяют пилокарпин, при
атонии - ацеклидин, который дает меньше побочных эффектов. М-холиномиметики противопоказаны
при бронхиальной астме, нарушении проводимости в сердце, при тяжелых заболеваниях сердца, при
эпилепсии, гиперкинезах, беременности (из-за опасности выкидыша). При отравлении мхолиномиметиками (чаще всего мухомором) первая помощь состоит в промывании желудка и введении
атропина, являющегося антагонистом этих веществ за счет блокады м-ХР.
Н-холиноминетики. Никотин лечебного значения не имеет. При курении вместе с продуктами
горения табака он способствует развитию многих заболеваний. Никотин имеет высокую токсичность.
Вместе с дымом при курении вдыхаются и другие ядовитые продукты: смолы, фенол, окись углерода,
синильная кислота, радиоактивный полоний и Др. Влечение к Курению обусловлено
фармакологическими эффектами никотина, связанными с возбуждением н-ХР ЦНС (кора,
продолговатый и спинной мозг), что сопровождается субъективным ощущением повышения
работоспособности. Имеет значение также выделение адреналина из надпочечников, который усиливает
кровообращение. Большую роль в развитии влечения играет привычка и психологическое воздействие
окружающей обстановки. Курение способствует развитию сердечно-сосудистых заболеваний
(гипертоническая болезнь, стенокардия, атеросклероз и др.), бронхолегочных заболеваний (бронхиты,
эмфизема, рак легкого), заболеваний ЖКТ (язвенная болезнь, гастриты). Избавление от этой вредной
привычки зависит прежде всего от самого курильщика. Этому могут помочь некоторые ЛС (напр.,
табекс), содержащие цитизин или лобелин.
Лобелин и цититон избирательно стимулируют н-ХР. Практическое значение имеет возбуждение
н-ХР каротидных клубочков, которое сопровождается рефлекторным возбуждением дыхательного
центра. Поэтому их используют как стимуляторы дыхания. Эффект кратковременный (2-3 мин) и
проявляется только при в/в введении. Одновременно усиливается работа сердца и повышается АД в
результате выделения адреналина из надпочечников и ускорения проведения импульсов через
симпатические ганглии. Эти препараты показаны при угнетении дыхания, вызванном отравлением
окисью углерода, при утоплении, асфиксии новорожденных, травме мозга, для профилактики
ателектаза и пневмонии. Однако медицинское значение их ограничено. Чаще используют аналептики
прямого и смешанного действия.
Лекция 5.
ХОЛИНОБЛОКИРУЮЩИЕ ЛС.
Холиноблокаторами называют ЛВ, угнетающие холинергические влияния в результате блокады ХР.
В зависимости от способности проникать через ГЭБ этот эффект развивается преимущественно в
периферических синапсах или в синапсах ЦНС. Поэтому их подразделяют на периферические и
центральные холиноблокаторы. Периферические холиноблокаторы делятся на 2 группы: мхолиноблокаторы и н-холиноблокаторы. В этой лекции будут рассмотрены периферические
холиноблокаторы. Центральные холиноблокаторы используют, в основном, для лечения гиперкинезов и
в качестве транквилизаторов, поэтому они будут представлены в соответствующих разделах
фармакологии. Необходимо изучить следующие вопросы:
* - классификация холиноблокаторов;
* - МД и основные эффекты м-холиноблокаторов (атропина, платифиллина, скополамина, метацина и
др.); особенности их фармакокинетики и фармакодинамики; показания, противопоказания и
побочные эффекты;
* - МД и основные эффекты ганглиоблокаторов, их классификация, применение, побочные эффекты
(ПЭ);
* - классификация миорелаксантов по МД и продолжительности действия;
* - особенности фармакодинамики разных групп миорелаксантов, их применение, ПЭ и неотложная
помощь.
М-холиноблокаторы.
В эту группу входят алкалоиды (атропин, платифиллин, скополамин, гиосциамин) и синтетические
препараты (метацин, фубромеган). Главным представителем является атропин, поэтому мхолиноблокаторм называют группой атропина. Вещества этой группы блокируют м-ХР,
расположенные на мембранах эффекторных клеток возле окончаний постганглионарных
холинергических нервов. При проникновении в ЦНС они блокируют м-ХР мозга. Блокируя м-ХР, они
препятствуют взаимодействию с ними АЦХ. На синтез АЦХ не влияют. Таким образом, их действие
проявляется на уровне постсинаптической мембраны. Антагонизм с АЦХ имеет конкурентный
характер. Он является практически односторонним, так как сродство атропина с м-ХР в 1000 раз выше,
чем АЦХ. Это отнсится и к другим м-холиноблокаторам. Препараты этой группы проявляют
преимущественно периферическое действие. Влияние на ЦНС в терапевтических дозах выражено слабо
(за исключением скополамина) и имеет ограниченное практическое значение.
Функции различных органов находятся под контролем адренергической и холинергической
иннервации, поэтому меняя тонус той или другой иннервации, можно регулировать степень активности
органа. Следовательно, холиноблокаторы не только ослабляют холинергические эффекты, но и
приводят к преобладанию адренергических влияний. Фармакологические эффекты м-холиноблокаторов
можно рассмотреть на примере атропина.
Атропин - алкалоид, содержащийся в ягодах красавки (белладонны), листьях дурмана и белены.
Эти растения с древних времен широко использовались в медицине. Практически наиболее важное
действие атропин оказывает на глаз, бронхи. ЖКТ и ССС.
Действие на глаз прямо противоположно действию пилокарпина. Атропин расслабляет круговую
мышцу радужки, суживающую зрачок, и цилиарную мышцу, регулирующую кривизну хрусталика.
Результатом этого действия является расширение зрачка (мидриаз) и уменьшение кривизны хрусталика
(паралич аккомодации). При расслаблении мышцы радужки ее основание утолщается и сдавливает
шлемов канал и фонтановы пространства, что приводит к затруднению оттока - жидкости из передней
камеры глаза и повышению внутриглазного давления. При глаукоме это сопровождается резкими
болями в глазу, ухудшением зрения, возможной отслойкой сетчатки и слепотой. Мидриаз используют
при воспалении радужки (иридоциклит) с целью профилактики ее сращения с капсулой хрусталика и
для обеспечения покоя глазу. Паралич аккомодации используют с диагностической целью при подборе
очков и для осмотра глазного дна.
Действие на бронхи проявляется расслаблением гладких мышц и снятием бронхоспазма, что
используют при бронхиальной астме и при отравлениях холиномиметиками. Одновременно угнетается
секреция бронхиальных желез и затрудняется отхождение мокроты, что является нежелательным.
Действие на ЖКТ, желче- и мочевыводящие пути состоит а угнетении тонуса гладких мышц и
секреции. Устраняются спазмы, уменьшается перистальтика, замедляется продвижение содержимого
ЖКТ, снижается тонус желчного пузыря и желчевыводящего протока, его сфинктеров, что способствует
выходу желчи в кишечник. Устраняются спазмы сфинктеров мочевого пузыря, мочеточников и
улучшается мочеотдление. Секреция слюнных, желудочных, кишечных желез, поджелудочной железы
уменьшается. Эти эффекты используют при лечении гиперацидных гастритов, язвенной болезни
желудка и 12-перстной кишки, при спастических энтероколитах, панкреатитах, а также в стоматологии
при гиперсаливации.
Действие на ССС проявляется учащением ритма, повышением автоматизма, возбудимости и
проводимости в сердце. Эти эффекты наиболее выражены на фоне ослабления сердечной деятельности
в результате повышения тонуса вагуса. Если при этом АД снижено, то атропин нормализует его.
Тахикардия наиболее выражена у молодых; у детей до 2-3 лет вагус мало тонизирован, поэтому атропин
действует на них слабее. У стариков также нередко наблюдается естественный максимальный ритм
сердца, поэтому атропин у них выраженной тахикардии не вызывает.
Атропин угнетает секрецию потовых желез и уменьшает потоотделение. Действие на подкорковые
двигательные центры (стрио-палидарная система) проявляется относительно слабо, так как препараты
группы атропина в терапевтических дозах мало проникают в мозг. Однако при паркинсонизме они
могут оказывать лечебное действие, блокируя м-ХР. При этом заболевании более эффекивны
центральные холинолитики.
При отравлении атропином или содержащими его растениями возникают характерные
признаки: зрачки резко расширены, кожа сухая, гиперемированная, температура тела повышена,
сухость во рту, нарушение глотания, хриплый голос, психомоторное возбуждение, бред, галлюцинации,
тахикардия ("скачущий пульс"). Лечение: для купирования психомоторного возбуждения барбитураты, аминазин; для борьбы с тахикардией - прозерин; промывание желудка, охлаждение,
катетериризация мочевого пузыря при скоплении мочи.
Другие м-холиноблокаторы по действию сходны с атропином, но имеют некоторые особенности.
Скополамин лучше проникает в мозг, особенно в ядра вестибулярного аппарата, поэтому оказывает
успокаивающее действие и ослабляет синдром укачивания (морская, воздушная, космическая болезнь).
Он входит в состав препарата против укачивания "Аэрон". Платифиллин слабее атропина по
спазмолитическому действию, но меньше угнетает секрецию и слабее действует на сердце. Метацин на
ЦНС практически не действует, так как не проникает через ГЭБ, Платифиллин и метацин действуют на
глаз менее продолжительно (4-6 ч), чем атропин (до 12 сут) и скополамин (3-4 сут), поэтому их удобнее
использовать для диагностических целей. Все м-холиноблокаторы противопоказаны при глаукоме и
тяжелых заболеваниях миокарда.
Периферические н-холиноблокаторы
Установлено, что н-ХР ганглиев и скелетных мышц проявляют неодинаковую чувствительность к
некоторым веществам. Н-ХР ганглиев легко блокируются ЛВ типа бензогексония, а мышечные н-ХР тубокурарином. Н-холиноблокирующее действие этих веществ обусловлено наличием двух
четвертичных атомов азота (аммониевых групп), а преимущественное действие на ганглии или мышцы
зависит от расстояния между атомами азота. Ганглиоблокирующий эффект проявляется, если между
атомами азота находятся 5 или 6 атомов углерода, а миорелаксирующий - при расстоянии в 10 атомов
углерода.
Ганглиоблокирующие средства
Ганглиоблокаторы - Л В, блокирующие передачу импульсов в ганглиях симпатической и
парасимпатической систем. Точкой их приложения являются н-ХР ганглионарных клеток. Блокада
осуществляется по конкурентному типу, т.е. они конкурируют с АЦХ за связь с н-ХР. На синтез АЦХ
не влияют.
По структуре Ганглиоблокаторы делятся на бисчетвертичные аммониевые соединения
(бензогексоний, пентамин, гигроний, арфонад) и третичные амины (пахикарпин, пирилен). Для врача
важнее их деление по продолжительности действия: 1) короткого действия (гигроний, арфонад); 2)
средней продолжительности (бензогексоний, пентамин, пахикарпин); 3) длительного действия
(пирилен, камфоний).
Препараты короткого действия используют преимущественно для кратковременного применения.
Для длительного применения наиболее удобны препараты длительного и среднего действия.
Всасывание в кишечнике и проникновение через ГЭБ зависит от структуры молекул. Хорошо
всасываются и проникают через ГЭБ третичные амины (пирилен, пахикарпин), что обеспечивает
удобство их применения (через рот). Но проникая через ГЭБ, при длительном применении они могут
вызывать ПЭ со стороны ЦНС (тремор, преходящие психические нарушения). Четвертичные амины
(бензогексоний, пентамин) плохо всасываются и плохо проникают через ГЭБ. Поэтому их назначают
преимущественно парэнтерально.
Наиболее важное практическое значение имеет действие ганглиоблокаторов на ССС. В результате
блокады н-ХР симпатических ганглиев нарушается проведение сосудосуживающих импульсов и
происходит расширение периферических сосудов. Наиболее сильно расширяются резистивные сосуды
(метартериолы, артериолы, мелкие артерии). Одновременно расширяются емкостные сосуды (венулы,
мелкие вены). Происходит снижение АД и центрального венозного давления, давления спинномозговой жидкости, скорости кровотока, притока крови к сердцу и легким, падает легочное АД,
уменьшается нагрузка на сердце. Блокируются сердечно-сосудистые рефлексы как патологические
(напр., при шоке, инфаркте), так и компенсаторные. При кровопотере угнетение компенсаторных.
рефлексов может привести к опасному падению АД. При умеренном снижении АД (80-100 мм рт.ст.) в
результате замедления кроаотока в тканях возрастает утилизация кислорода и снабжение кислородом
тканей может даже увеличиваться. Если же АД падает ниже 80 мм рт.ст., возникает гипоксия тканей.
Эти эффекты частично обусловлены также блокадой н-ХР мозгового слоя надпочечников, в результате
чего снижается выделение адреналина в кровь.
Блокада парасимпатических ганглиев приводит к ослаблению секреторной и моторной функций
ЖКТ. Этот эффект можно использовать при лечении язвенной болезни. Однако при длительном
применении ганглиоблокаторов часто возникают упорные запоры, трудно поддающиеся лечению.
Некоторые (пахикарпин) стимулируют сокращения матки, поэтому их применяют для ускорения родов.
Основные показания для применения: 1) гипертоническая болезнь (преимущественно при
гипертонических кризах, злокачественном течении гипертонии) пентамин, бензогексоний; 2)
облитерирующий эндартериит, болезнь Рейно, акроцианоз; 3) управляемая гипотония (гигроний,
арфонад); 4) отек легких и мозга (гигроний, арфонад, пентамин, беизогексомий); 5) слабость родовой
деятельности (пахикарпин).
Наиболее серьезными ПЭ являются ортостатическая гипотензия (коллапс) и атония кишечника
(запор). Для профилактики коллапса рекомендуется вводить Ганглиоблокаторы парэнтерально в
лежачем положении, встатавать с постели постепенно не раньше чем через 2 ч после инъекции. При
возникновении коллапса вводят адреналин, мезатон или эфедрин, прозерин, аналептики.
Ганглиоблокаторы противопоказаны при гипотонии, кровопотере, коронарной недостаточности,
кардиосклерозе и атеросклерозе, глаукоме, угнетении выделительной функции почек.
Мышечные релаксанты.
Это ЛВ, расслабляющие скелетные мышцы. МД состоит в блокаде передачи импульсов с окончаний
двигательных нервов на мышечные клетки в результате. влияния на н-ХР. Родоначальником этой
группы является яд кураре, который индейцы Южной Америки использовали для смазывания
наконечников стрел. Сведения о нем привезли в Европу моряки экспедиции Колумба. Угнетение
нервно-мышечной передачи ядом кураре доказали Клод Бернар в 1851 г. и русский ученый Е.В.
Пеликан в 1857 г. В медицинскую практику эти ЛС внедрены после исследований Гриффитса и
Джонсона в 1942 г.
По МД миорелаксанты делятся на 3 рруппы: 1) антидеполяризующие (тубокурарина хлорид,
анатруксоний, панкурония бромид, мелликтин и др.); 2) деполярнэующе (дитилин); 3) смешанного
действия (диоксоний). В химическом отношении большинство их являются бисчетвертичными
аммониевыми соединениями, а мелликтин - третичным амином.
МД антидеполяризующих ЛС связан с блокадой н"ХР. Они являются конкурентными
антагонистами АЦХ и препятствуют его взаимодействию с н-ХР. При увеличении концентрации АЦХ в
синапсах происходит вытеснение релаксанта из связи с н-ХР и деполярзация постсинаптической
мембраны. Характерными чертами этого блока являются: а) отсутствие фазы фибриляции мышц перед
их расслаблением; б) отсутствие потери калия мышцами; в) усиление нервно-мышечного блока
средствами для наркоза, местными анестетиками; г) антагонизм с антихолииэстеразными веществами.
МД деполяризующих ЛС связан со структурным сходством их с АЦХ (молекула дитилина
представляет удвоенную молекулу АЦХ). благодаря этому они подобно АЦХ вызывают деполяризацию
постсинаптической мембраны. Однако гидролиз их холинэстеразой происходит медленно, благодаря
чему деполяризация длится несколько минут. В этот период н-ХР нечувствительны к АЦХ и импульсы
не передаются, что и приводит к релаксации мышц. Характерными чертами этого блока являются: а)
фибриляция мышц сразу после введения препарата; б) потеря калия мышцами; в) усиление блока
антихолинэстеразными веществами.
МД релаксантов со смешанным влиянием на постсииаптическую мембрану вначале заключается в
развитии деполяризации, а затем антидеполяризации. Таким свойством обладает диоксоний.
Основным эффектом миорелаксантов является расслабление скелетных мышц, которое происходит в
определенной последовательности: мимические мышцы лица, мышцы шеи, мышцы гортани,
конечностей, туловища, диафрагмы. Паралич межреберных мышц и диафрагмы приводит к остановке
дыхания и больного надо переводить на искусственное дыхание. Расслабление мышц и обездвиживание
больного устраняют двигательные реакции на операционную травму и облегчают работу хирурга, что
позволяет проводить операции под поверхностным наркозом и уменьшает опасность осложнений от
наркоза.
Избирательность действия миорелаксантов на н-ХР скелетных мышц относительна. При увеличении
доз они начинают действовать и на другие н-ХР. Антидеполяризующие ЛС могут вызвать блокаду
ганглиев, мозгового слоя надпочечников и снижение АД, при применении дитилииа АД, наоборот,
повышается в результате стимуляции симпатических ганглиев и мозгового слоя надпочечников.
По
силе
миорелаксирующего
эффекта
их
разделяют
в
следующем
порядке:
пипекуроний>панкуроний>анатруксоний>тубокурарин>дитилин>мелликтин. По продолжительности
действия делят на 3 группы: а) короткого действия (5-10 мин) - дитилин, б) средней
продолжительности (25-50 мин) - тубокурарин, пипекуроний, панкуроний, анатруксоний; в)
длительного действия (более 60 мин) - анатруксоний, пипекуроний, панкуроний в больших дозах.
Выбор препарата зависит от МД, силы и продолжительности эффекта и цели назначения.
Основные показания: а) оперативные вмешательства; 6) интубация трахеи; в) вправление отломков
костей, вывихов суставов; г) снятие судорог при столбняке, при электросудорожной терапии,
отравлении стрихнином. ПЭ проявляются в виде гипотонии (аитидеполяризующие), гипертензии
(деполяризующие), тахикардии (анатруксоний), аритмии (дитилин), бронхоспазма (тубокурарин),
мышечных болей (дитилин). При наследственной недостаточности холинэстеразы крови под влиянием
дитилина может- возникнуть длительное апноэ (до 6-8 ч). При передозировке антидеполяризующих ЛС
применяют антихолинэстеразные ЛС (прозерин). Антагонистов дитилина нет, поэтому при его
передозировке проводят переливание крови и симптоматическую терапию. При назначении
миорелаксантов необходимо иметь аппарат для искусственного дыхания.
Лекция 6.
АДРЕНЕРГИЧЕСКИЕ СРЕДСТВА.
К ним относятся ЛВ, влияющие на передачу импульсов в адренергических синапсах. Делятся на
средства, усиливающие передачу импульсов (адренопозитивные, адреномиметические), и ЛС,
ослабляющие
передачу
импульсов
в
адренергических
синапсах
(адренонегативные,
антиадренергические). Необходимо знать следующие вопросы:
• -синтез медиатора и его взаимодействие с адренорецепторамм;
• - виды адренорецепторов, их локализация и функция;
•- классификация адренергических ЛС;
• - характеристика стимуляторов а- и в-адренорецепторов;
• - МД и основные эффекты адреналина, норадреналмна и эфедрина, их применение и ПЭ;
• - МД и основные эффекты альфа-адреномиметиков, их применение и ПЭ;
• - МД, основные и ПЭ в-адреномиметиков, особенности их применения;
Медиатором адренергических синапсов является норадреналин, который синтезируется в
окончаниях симпатических нервных волокон. Источником является фенилаланин, из которого
последовательно образуются тирозин, диоксифенилаланин, дофамин, норадреналин и адреналин.
Норадреналин (НА) депонируется в везикулах в виде стабильной и лабильной фракций. Под влиянием
импульса НА выделяется в синаптическую щель через пресинаптическую мембрану и стимулирует
адренорецепторы (АР), которые. являются липолротендными молелулами, встроенными в
постсииалтнческую мембрану. При взаимодействии с НА или подобными ему веществами
(адреномиметиками) они изменяют свою конфигурацию и обеспечивают движение ионов через
мембрану, что приводит к ее деполяризации и изменению функции клетки. Инактивация НА
осуществляется путем ферментативного расщепления катехол-орто-метилтрансферазой (КОМТ) и
обратного нейронального захвата (80%). Следовательно, пополнение запасов НА идет
преимущественно за счет обратного захвата и лишь 20% за счет синтеза. В инактивации НА участвует
также моноаминоксидаза (МАО), которая находится в цитоплазме нервного окончания.
АР обладают различной чувствительностью к разным ЛВ и подразделяются на а- и в-АР, а-АР
делятся на а1 и а2-АР. а1-АР расположены на постсинаптической мембране, а2-АР - на
пресинаптической мембране и лостсинаптически. Пресинаптические а2-АР регулируют освобождение
НА из нервных окончаний по принципу обратной связи, а внесинаптические а2-АР стимулируются
циркулирующим НА и адреналином. а-АР локализованы преимущественно в сосудах. в-АР делятся на
в1-АР (в сердце) и в2-АР (в бронхах, матке, кишечнике, сосудах). в-АР находятся на постсинаптической
мембране. Предполагается, что в2-АР имеются также на пресинаптической мембране, осуществляя
положительную обратную связь, т.е. способствуют освобождению НА из нервных окончаний.
а1-АР преобладают в сосудах кожи, подкожной клетчатки, слизистых оболочек, почек, кишечника, в
сфинктерах ЖКТ, в селезенке, в радиальной мышце радужной оболочки глаза, а в2-АР - в сосудах
скелетных мышц, в сердце, гладких мышцах бронхов, матки, кишечника. При стимуляции а-АРнаблюдается сужение сосудов, повышение АД, расширение зрачка, угнетение тонуса и моторики
кишечника, сокращение сфинктеров ЖКТ, капсулы селезенки, матки. Стимуляция в-АР сопровождается
расширением сосудов скелетных мышц (в2-АР), усилением работы сердца (в1), снижением тонуса
мышц бронхов, ЖКТ, матки (в2), увеличением гликогенолиза (в2) и липолиза (В1).
ЛС могут воздействовать на передачу импульсов в адренергических синапсах влиянием на
следующие процессы: 1) синтез НА, 2) депонирование НА в везикулах, 3) ферментативное расщепление
НА, 4) выделение НА из окончаний нервов, 5) обратный нейрональный захват НА, 6) активность АР
пресинаптической и постсинаптической мембран.
Адренергические ЛС принято делить с учетом их влияния на АР. По влиянию на АР
постсиналтической мембраны они делятся на адреномиметики и адреноблокаторы, а по влиянию на
пресинаптическую мембрану (окончания симпатических нервов) - на симпатомиметики и
симпатолитики.
Классификация адренергических ЛС: 1) а- и в-адреномиметики (адреналин, НА); 2) аадреномиметики (мезатон, нафтизин, галазолин); 3) в-адреномиметики (изадрин, салбутамол,
тербуталин и др.); 4) симпатомиметики (эфедрин); 5) а-адреноблокаторы (дигидроэрготамин, тропафен,
фентоламин, празозин); 6) в-адреноблокаторы (анаприлин, метопролол и др.); 7) а-в-адреноблокаторы
(лабеталол); 8) симпатолитики (октадин, резерпин, орнид).
Адреномиметические ЛС.
а-, в-адреномиметики. Основным ЛС этой группы является адреналин, Относится к
фенилалкиламинам (катехоламинам). Содержится в хромафиновых клетках мозгового вещества
надпочечников. Вызывает все эффекты, связанные с возбуждением а1, а2, в1 и в2-АР. Основными
эффектами адреналина (А) являются усиление работы сердца, повышение АД, сахара крови,
расширение бронхов.
Действие на сердце обусловлено стимуляцией в1-АР, которые связаны с аденилатциклазой клеток.
Активация ее приводит к усилению синтеза циклического аденозинмонофосфата (цАМФ), который
стимулирует фосфорилазу и гликогенолиз. В результате усиливаются процессы окислительного
фосфорилирования, возрастает потребление кислорода и образование энергии, что приводит к
увеличению сократимости миокарда и минутного объема крови. Стимулируя АР синусного узла,
адреналин повышает автоматизм, возбудимость и частоту сердечных сокращений, ускоряет проведение
импульсов в миокарде. В связи с резким повышением потребления кислорода коэффициент полезного
действия сердца (отношение работы к потреблению кислорода) снижается. При коронарной
недостаточности это может привести к гипоксии миокарда, истощению его резервов и развитию острой
сердечной слабости. При заболеваниях миокарда и коронарных сосудов он противопоказан,
Действие адреналина на сосуды зависит от наличия в них а- или в-АР. Стимуляция а1-АР вызывает
сокращение прекапиллярных сфинктеров, метартериол, артериол, венул, мелких артерий и вен.
Капиллярный кровоток уменьшается и происходит шунтирование крови через артерио-венозные
анастомозы, что приводит к гипоксии тканей. Однако сосуды скелетных мышц, сердца и мозга, в
которых находятся в2-АР, расширяются. В целом под влиянием адреналина артериальное и
центральное венозное давление возрастают, увеличивается возврат крови к сердцу. Происходт
повышение систолического и снижение диастолического АД. Систолическое АД возрастает за счет
усиления работы сердца, а диастолическое снижается, главным образом, за счет расширения сосудов
скелетных мышц.
Адреналин вызывает резкое усиление гликогенолиза, особенно в депо гликогена (печень, мышцы) и
повышает сахар крови, являясь антагонистом инсулина, который снижает сахар крови за счет усиления
его утилизации. Возрастает содержание молочной кислоты, усиливается липолиз и повышается уровень
свободных жирных кислот в крови.
Через ГЭБ адреналин проникает плохо, в основном, в области гипоталамуса, и оказывает
незначительное стимулирующее действие на центр терморегуляции, секрецию некоторых гормонов
гипофиза. Он тормозит моторику ЖКТ и матки, но эти эффекты существеного значения не имеют.
Адреналин действует кратковременно (16-30 мин), так как быстро разрушается и частично
депонируется в тканях, связываясь с белками, которые предохраняют его от разрушения. При
повышении тонуса симпатической системы адреналин освобождается из связанного состояния и
оказывает неблагоприятное действие на сердце, что может привести к гипоксии и инфаркту миокарда.
Адреналин применяют парэнтерально и местно, так как при приеме внутрь он разрушается. Его
назначают при анафилактическом шоке и некоторых других аллергических реакциях немедленного
типа, при бронхиальной астме, острой гипотензии, гипогликемической коме, при угнетении
возбудимости и проводимости в миокарде, для удлинения действия местных анестетиков, при
остановке сердца. Местно назначают при открытоугольной глаукоме, для остановки капиллярных
кровотечений. Адреналин противопоказан при органических заболеваниях сердца и сосудов,
гипертонии, при тиреотоксикозе, сахарном диабете, при фторотановом и циклопропановом наркозе (изза опасности развития аритмии сердца).
Норадреналин стимулирует а1, а2 и в1-АР и практически не влияет на в2-АР. Поэтому НА действует
преимущественно на ССС, повышая АД. Повышается как систолическое, так и диастолическое АД.
Этот эффект обусловлен действием на а1-АР сосудов и повышением периферического сосудистого
сопротивления в результате спазма мелких сосудов. При этом снижается тканевой кровоток и
развивается гипоксия. В связи с этим НА противопоказан при гиповолемическом шоке из-за
возможности усиления интоксикации продуктами распада. В таких случаях более эффективны аадреноблокаторы. Быстрый подъем АД стимулирует рефлекс с механорецепторов сосудов, что
приводит к развитию синусовой брадикардии, поэтому минутный объем сердца не возрастает. На
гладкие мышцы, обмен веществ и ЦНС НА оказывает незначительное влияние. НА применяют при
остром снижении АД, вводят в/в, так как при п/к и в/м введении он вызывает сильный местный спазм
сосудов, что может сопровождаться некрозом.
Эфедрин является симпатомиметиком или адреномиметиком непрямого действия. Его действие
направлено преимущественно на пресинаптическую мембрану и проявляется увеличением
освобождения НА из симпатических окончаний. Кроме того, он оказывает прямое действие на АР
постсиналтической мембраны. Эфедрин стимулирует все АР, поэтому сходен с адреналином, но менее
активен (в 50-100 раз). Действие развивается постепенно и продолжается более длительно, чем у
адреналина (в 7-10 раз). Он не разрушается при приеме внутрь, поэтому может назначаться через рот и
парэнтерально. Через ГЭБ проникает хорошо и стимулирует ЦНС. Это может вызвать возбуждение,
бессоницу. При повторном введении эфедрина с небольшим интервалом (10-30 мин) развивается
ослабление эффекта (тахифилаксия, или быстрое привыкание), связанное с уменьшением содержания
НА в везикулах. Эфедрин применяют а тех же случаях, что и адреналин, а также при патологической
сонливости.
а-адреномиметики - ЛВ, оказывающие избирательное стимулирующее действие на а-АР. К ним
относятся мезатон, иафтизин и галазолин. Мезатон действует на а1-АР постсинаптической мембраны,
вызывая сужение сосудов и повышение АД. На сердце непосредственно не действует. Разрушается
медленнее, чем НА, и действует при в/в введении 20-30 мин. Эффективен при приеме внутрь.
Применяют преимущественно при коллапсе, рините, для продления действия анестетиков, при
открытоугольной глаукоме. Нафтизин и галазолин действуют преимущественно на
постсинаптические а2-АР. Их применяют местно при ринитах.
в-адреномиметики оказывают прямое стимулирующее действие на в-АР. К ним относятся изадрин,
салбутамол, фенотерол, тербуталин, орципреналин и др. Изадрин стимулирует в1 и в2-АР, действуя на
сердце, гладкие мышцы и обмен веществ. Стимуляция в1-АР сопровождается увеличением частоты и
силы сокращений сердца, возбудимости, автоматизма и проводимости, увеличением минутного объема.
При этом систолическое АД повышается, а диастолическое снижается за счет стимуляции в2-АР
сосудов и их расширения. Стимуляция в2-АР гладких мышц приводит к расширению бронхов,
снижению тонуса ЖКТ, матки. Изадрин стимулирует гликогенолиз и липолиз и увеличивает
содержание сахара и жирных кислот в крови. ПЭ проявляются в виде тахикардии, тремора, головной
боли. Он противопоказан при заболеваниях сердца, сахарном диабете, тиреотоксикозе.
Салбутамол, фенотерол и тербуталин оказывают преимущественое влияние на в2-АР. На сердце
они действуют слабо. Наиболее ценным эффектом является расслабление гладких мышц бронхов и
снятие бронхоспазма, что используют при лечении бронхиальной астмы. Они также снижают тонус
матки и ослабляют чрезмерную родовую деятельность. Не разрушаются КОМТ, поэтому действуют
длительно (6-8 ч). Применяют внутрь, парэнтерально, ингаляционно.
Лекция 7.
АНТИАДРЕНЕРГИЧЕСКИЕ ЛС.
К ним относятся адреноблокаторы и симпатолитики. Эти ЛС приобрели большое значение, особенно
в кардиологии. Их используют в лечении таких распространенных заболеваний ССС как ишемическая
болезнь сердца, сердечные аритмии и гипертоническая болезнь.
В лекции будут рассмотрены следующие вопросы:
* -МД, основные и ПЭ а-адреноблокаторов, особенности их применения;
* -МД и фармакологические эффекты в-адреноблокаторов, показания к применению, ПЭ и
противопоказания;
* -МД, эффекты и применение лабеталола;
* -Симпатолитики, их МД, основные и ПЭ, особенности фармакокинетики и фармакодииамики
октадина и резерпина, показания и противопоказания.
Адреноблокирующие ЛС.
Адреноблокаторы (адренолитики) угнетают адренорецепторы, экранируя активные центры
макромолекул, в результате чего они утрачивают чувствительность к НА и другим катехоламинам. Их
подразделяют на а-адреноблокаторы, в-адреноблокаторы и а-в-адреноблокаторы.
а-адреноблакаторы блокируют а-АР гладких мышц сосудов, не влияя на высвобождение НА из
симпатических окончаний. В терапевтических дозах они предупреждают ил устраняют сужение
сосудов, вызываемое возбуждением симпатических нервов или НА и адреналином. Это сопровождается
быстрым снижением АД. Если на фоне их действия ввести адреналин, то он не только не повышает АД,
но может даже снизить его ("извращенный эффект"). Связано это с тем, что на фоне блокады а-АР
проявляется действие адреналина только на в-АР, в том числе и на в2-АР сосудов скелетных мышц,
возбуждение которых дает сосудорасширяющий и гипотензивный эффект. В то же время аадреноблокаторы не угнетают стимулирующего действия симпатических нервов и адреналина на
сердце, так как не блокируют в-АР сердца. Они предупреждают сокращение капсулы селезенки, матки,
радиальной мышцы радужки, вызываемые адреналином и НА, не влияют на тонус гладких мышц
бронхов.
Практическое значение имеет расширение периферических сосудов, которое используют при
нарушениях кровообращения (эндартериит, болезнь Рейно, акроцианоз), а также при геморрагическом и
кардиогенном шоке для снятия спазма мелких сосудов и восстановления микроциркуляции. Их
применяют также при гипертоническом кризе, отеке легких, феохромоцитоме (опухоль мозгового слоя
надпочечников, при которой выделяется в кровь много адреналина и резко повышается АД).
К этой группе относятся фентодамин, тропафен, пирроксан, дигидрированные алкалоиды
спорыньи (дигидроэргогоксин, дигидроэрготамин). Эти препараты блокируют как постсинаптические
а1-АР, так и пресинаптические а2-АР. Блокада а2-АР по принципу обратной отрицательной связи
приводит к увеличению высвобождения НА из симпатических окончаний. В этом главная причина ПЭ тахикардии, быстрой утраты эффекта (привыкание). Поэтому неселективные альфа-адреноблокаторы
недостаточно эффективны при длительном применении. Созданы препараты с избирательным
(селективным) действием на постсинаптические а1-АР. К ним относится празозин. Он оказывает
выраженное гипотензивное действие а течение 6-8 ч, привыкание развивается медленно, тахикардию не
вызывает. Применяют при лечении гипертонической болезни.
в-адреноблокаторы подразделяют на неселективные и селективные. К первым относится анаприлин
(пропранолол, индерал, обзидан), окспренолол (тразикор), пиндолол (вискен), надолол, алпренолол, ко
второй группе -метопролол (бетолок, селокен), талинолол (корданум). Неселективные в-блокаторы
угнетают в1 и в2-АР, поэтому имеют более широкий спектр действия. Селекгивные блокируют
преимущественно в1-АР сердца, поэтому их называют кардиоселективными. Некоторые препараты
(окспренолол, пиндолол, алпренолол) обладают симпатомиметической активностью, что позволяет
использовать их при брадикардии, сердечной недостаточности. По длительности эффекта различают
препараты короткого действия (анаприлин, метопролол, окспренолол, алпренолол), препараты средней
продолжительности действия (пиндолол) и препараты длительного действия (соталол, надолол,
атенолол). Наличие препаратов разной продолжительности действия позволяет применять их
дифференцированно.
Действие в-адреноблокаторов на ССС слагается из следующих эффектов: уменьшение ЧСС,
сократимости миокарда, снижение автоматизма, возбудимости и проводимости в сердце, ударного и
минутного объема, АД, потребления кислорода миокардом. Периферическое сосудистое сопротивление
и диастолическое АД повышаются из-за блокады в2-АР сосудов. Блокада в2-АР почек приводит к
уменьшению образования ренина, а в последующем -ангиотензина. Уменьшаются адренергические
влияния со стороны ЦНС. Следовательно, антигипертензивный эффект в-блокаторов связан с
уменьшением работы сердца, образования ренина и тонуса вазомоторных центров. Лечебное действие
при стенокардии обусловлено снижением потребности миокарда в кислороде, а антиаритмическое уменьшением автоматизма, возбудимости и проводимости в сердце. Эти эффекты и определяют
применение бета-адреноблокаторов при лечении гипертонической болезни, ишемической болезни
сердца, нарушений сердечного ритма. К ПЭ бета-адреноблокаторов относятся брадикардия, гипотензия,
сердечная недостаточность, атрио-вентрикулярная блокада, обострение бронхиальной астмы,
заболеваний ЖКТ. Они противопоказаны при брадикардии, гипотонии, бронхиальной астме, сердечной
недостаточности, нарушении проводмости в сердце, язвенной болезни желудка и 12-перстной кишки.
а-в-адреноблокаторы угнетают оба типа АР. К ним относится лабеталол. Наиболее выраженные
эффекты связаны с блокадой в-АР. Он уменьшает обмен веществ и потребление кислорода в миокарде,
снижает автоматизм и проводимость, сердечный выброс и работу сердца. Блокируя а-АР сосудов,
лабеталол снижает сосудистое сопротивление. Основным эффектом лабеталола является снижение АД,
поэтому его применяют для лечения гипертонической болезни.
Симпатолитические средства.
Это ЛВ, действующие на симпатические нервные окончания. Эффект их противоположен
симпатомиметикам. На АР не влияют, поэтому не ослабляют, а даже усиливают действие прямых
адреномиметиков. В эту группу входят октадин, резерпин и орнид. Они отличаются как по МД, так и по
фармакологическим эффектам. Октадин является периферический симлатолитиком, так как через ГЭБ
не проникает. Он угнетает передачу импульсов с окончаний симпатических нервов на гладкие мышцы
сосудов, что приводит к их расширению. МД октадина объясняют влиянием на пресинаптическую
мембрану, которое приводит к уменьшению обратного захвата НА. Считают, что октадин также
вытесняет НА из везикул, что способствует его разрушению МАО. Это приводит к постепенному
истощению запасов медиатора в нервных окончаниях и угнетению передачи импульсов. Гипотензтаное
действие октадина развивается в течение нескольких дней и продолжается до 2 недель. При этом
снижаются минутный объем сердца и вазопрессорные рефлексы, развивается брадикардия. ПЭ октадина
связаны с относительным преобладанием тонуса холинергической системы в результате ослабления
влияний адренергической системы. Они проявляются повышением тонуса бронхиальной мускулатуры,
усилением перистальтики и секреции ЖКТ, диспептическими расстройствами, обострением язвенной
болезни, выраженной брадикардией, сужением зрачков. Эти ПЭ можно ослабить или предупредить
введением м-холиноблокаторов. Октадин применяют при гипертонической болезни. Он противопоказан
при бронхиальной астме, гиперацидных гастритах, язвенной болезни, тяжелых заболеваниях сердца.
Резерпин действует на уровне мембран везикул, затрудняя захват дофамина, в результате чего
снижается синтез НА. Уменьшается также обратный захват НА везикулами, в результате чего он
разрушается МАО в цитоплазме нервного окончания. Это приводит к истощению запасов НА в
симпатических нервах. В отличие от октадина резерпин хорошо проникает через ГЭБ и снижает
содержание НА, дофамина и серотонина в мозге. Поэтому он оказывает седативное (успокаивающее) и
антипсихотическое действие. Гипотензивный эффект развивается медленно и достигает максимума
через несколько суток. Он связан с уменьшением сердечного выброса, сосудистого сопротвления и
прессорных рефлексов. Резерпин применяют для лечения гипертонической болезни и психических
заболеваний. Периферические ПЭ резерпина сходны с октадином и связаны с преобладанием
холннергической системы. Он также может вызывать центральные ПЭ в виде депрессии,
паркинсонизма, снижения половой потенции.
Орнид уменьшает проницаемость пресинаптической мембраны для НА, угнетает МАО и снижает
обратный нейрональный захват НА. Действует продолжительно (5-8 ч) и применяется
преимущественно при сердечных аритмиях.
Лекция 8.
СРЕДСТВА, РЕГУЛИРУЮЩИЕ ФУНКЦИИ ЦНС.
В настоящее время медицина располагает большим арсеналом ЛС, с помощью которых можно
воздействовать на различные функции ЦНС: восприятие боли, психо-эмоциональное состояние, сон и
бодрствование и т.д. ЛВ, действующие на ЦНС, можно разделить на 2 группы: 1) ЛВ угнетающего типа
действия; 2) ЛВ стимулирующего типа действия. К 1-й группе относятся: а) средства для наркоза, б)
алкоголи, в) снотоворные средства, г) противосудорожные (противоэпилептические и
противопаркинсонические), д) анальгетики, е) нейролептики, ж) транквилизаторы, з) седативные
средства. К ЛС 2-й группы относятся: а) антидепреесанты, б) психостимуляторы, в) аналептики, г)
общетонизирующие средства (адаптогены), д) галлюциногеиы, е) ноотропные средства.
Средства для наркоза
Это вещества, вызывающие обратимое угнетение ЦНС, проявляющееся выключением сознания, всех
видов чувствительности, рефлексов и расслаблением скелетной мускулатуры.
Попытки устранить боль при оперативных вмешательствах делались еще в глубокой древности.
Однако подлинная история наркоза начинается с 40 гг. прошлого столетия. Первым применил эфирный
наркоз Лонг в 1842 г., но опубликовал свое сообщение лишь в 1852 г. Поэтому лавры первооткрывателя
достались американцу Мортону, который в 1846 г. впервые публично продемонстрировал действие
наркоза. В России первым применил эфирный наркоз хирург Иноземцев. Широкое внедрение эфира в
практику осуществил Н.И.Пирогов в период Кавказской войны. Он же ввел в широкую практику
хлороформный наркоз. Поэтому Н.И.Пирогов по праву считается одним из основоположников
хирургического обезболивания.
В этой лекции будут рассмотрены следующие вопросы:
* - современные представления о МД наркотических средств;
* - классификация средств для наркоза;
* - последовательность развития ингаляционного наркоза (эфирного);
* - фармакологические эффекты и отрицательные последствия эфирного наркоза;
* - фторотан, особенности его фармакодинамики и возможные ПЭ;
* - особенности действия и применения энфлурана и метоксифлурана;
* - характеистика газового наркоза, фармакодинамика и применение азота закиси и циклопропана, их
ПЭ;
* - характеристика средств для неингаляционного наркоза (тиопентала-натрия, гексенала, пропанидида,
кетамина, предиона, натрия оксибутирата;
* - сущность и виды комбинированного наркоза.
Наркоз - сложное биологическое явление, зависящее от многих причин. Действие наркотических
средств проявляется на разных уровнях организации биологических систем - от молекулярного до
организма в целом. Наркоз вызывают вещества, имеющие существенные различия в химическом
строении. У них отсутствует избирательность действия. Поэтому не существует единого МД. Общим
для них является лишь то, что у высших животных они угнетают межнейронную передачу возбуждения
в ЦНС. При этом нарушаются взаимоотношения между различными отделами ЦНС. Предполагают, что
нарушение межнейронной передачи связано с изменением функции мембран нейронов, в частности,
проницаемости ионных каналов натрия и калия, что тормозит процесс деполяризации. Взаимодействие
с мембранами, по-видимому, зависит от структуры и физико-химических свойств наркотических ЛС.
Для одних ЛС это может быть высокая растворимость в липидах и накопление в нервной ткани, для
других адсорбция на границе раздела фаз, для третьих – взаимодействие с молекулами воды,
образование кристалл-гидратов за счет вандерваальсовых связей и увеличение электрического
сопротивления среды в области синапса. Не ислючено, что нарушение передачи импульсов может быть
за счет угнетения высвобождения медиаторов (напр., АЦХ) или влияния на специфические рецепторы.
Таким образом, МД средств для наркоза на молекулярном уровне недостаточно ясен. Разные отделы
ЦНС имеют различную чувствительность к наркотическим ЛВ. Наиболее высокую чувствительность
проявляют синапсы ретикулярной формации, а наименьшую продолговатого мозга. Имеются различия
и в других отделах ЦНС. Этим объясняют стадийность развития наркоза.
Средства для наркоза делятся на две группы:
1. Средства для ингаляционного наркоза: а) летучие жидкости (эфир, фторотан, хлороформ,
энфлуран, метоксифлуран); б) газообразные вещества (азота закись, циклопропан).
2. Средства для неингаляционного наркоза: тиопентал-натрий, гексенал, пропанидид, кетамин,
предион, натрия оксибутират.
Наиболее важными требованиями, которым должны отвечать средства для наркоза, являются: 1)
быстрота развития наркоза и отсутствие стадии возбуждения; 2) достаточная глубина и управляемость
наркоза; 3) достаточная широта наркотического действия; 4) минимальные ПЭ; 5) техническая простота
применения и безопасность в пожарном отношении. Ни одно из современных средств для наркоза не
отвечает всем этим требованиям.
Средства для ингаляционного наркоза.
Применяют в виде паров или газов обычно с помощью наркозных аппаратов, регулирующих подачу
наркотического средства в дыхательные пути. Из легких они поступают в кровь. Скорость и глубина
наркоза зависят от концентрации ЛВ в крови. В организме они распределяются относительно
равномерно, но больше накапливаются в хорошо васкуляризированных органах (мозг, печень, почки,
сердце). Из организма выделяются, в основном, через легкие в неизмененном виде.
Действие на ЦНС проявляется в определенной последовательности: головной мозг, спинной мозг,
продолговатый мозг. Это позволяет достигать глубокого наркоза без угнетения жизненно важных
центров - дыхательного и сосудодвигательного. Течение наркоза можно разделить на ряд стадий или
периодов, которые наиболее четко различаются при эфирном наркозе: 1) стадия аналгезии (оглушения);
2) стадия возбуждения; 3) стадия хирургического наркоза, которая подразделяется на 3 уровня -
поверхностный, выраженный и глубокий наркоз; 4) стадия пробуждения. Быстрота перехода одной
стадии в Другую зависит от концентрации эфира во вдыхаемом воздухе и в крови.
Стадия аналгезии характеризуется утратой болевой чувствительности при частичном сохранении
других видов чувствительности и спутанностью сознания. Она продолжается 1-3 мин, но ее можно
продлить, если поддерживать соотвествующую концентрацию эфира в крови. В этой стадии ярко
проявляется раздражающее действие эфира на слизистые дыхательных путей (чувство удушья,
нерегулярное дыхание, беспокойство больного). При углублении наркоза эти явления проходят.
Мышечный тонус и рефлексы сохранены. В стадии аналгезии можно проводить лишь кратковременные
простые операции (вскрытие абсцесса, фурункула, удаление зуба и т.п.).
Стадия возбуждения характеризуется двигательным и речевым возбуждением, нарушением ритма
дыхания, сердечной деятельности, повышением рефлекторной возбудимости и мышечного тонуса,
утратой сознания. В результате повышения тонуса симпатической иннервации и выброса адреналина из
надпочечников развивается тахикардия, повышается АД, расширяются зрачки, повышается сахар крови.
Раздражение дыхательных путей парами эфира может вызвать рвоту, рефлекторную остановку дыхания
и сердца. Хирургические вмешательства в этой стадии опасны. В развитии стадии возбуждения
участвуют три главных фактора: 1) ослабление процессов внутреннего торможения и дезинтеграция
работы коры мозга (речевое и двигательное возбуждение); 2) растормаживание вегетативных центров
гипоталамуса; 3) поток импульсов из дыхательных путей и сосудов, рецепторы которых раздражаются
эфиром.
Стадия хирургического наркоза характеризуется регулярным глубоким дыханием, урежением
пульса и нормализацией АД, снижением тонуса мышц, угнетением всех видов чувствительности и
рефлексов. По мере углубления наркоза наблюдаются 3 уровня. 1-й уровень утрата сознания и боли, но
при сильном раздражении возникает ответная двигательная реакция. Дыхание спокойное, глубокое,
мышечный тонус частично сохранен, зрачки умеренно сужены и реагируют на свет. 2-й уровень дальнейшее ослабление рефлексов и мышечного тонуса, дыхание глубокое, работа сердца и АД близки
к норме. 3-й уровень - полное расслабление мышц, рефлексы отсутствуют, зрачки умеренно расширены,
не реагируют на свет, дыхание более частое и поверхностное, диафрагмальное, АД слегка снижено,
пульс учащается. Этот уровень обеспечивает возможность проведения любых хирургических
вмешательств, но в то же время требует особого внимания, так как граничит с передозировкой. При
передозировке эфира дыхание становится редким и поверхностным, движения грудной клетки и
диафрагмы рассогласовываются, возникает кислородное голодание, кровь темного цвета, мышечный
тонус отсутствует, зрачки предельно расширены, не реагируют на свет, АД прогрессивно падает.
Наступает паралич дыхательного центра.
Стадия пробуждения начинается сразу после прекращения подачи эфира. Около 90% эфира
выводится легкими, но этот процесс растягивается на несколько дней. Восстановление функций идет в
обратном порядке: в первую очередь восстанавливаются рефлексы и мышечный тонус, в последнюю сознание.
Эфир - летучая жидкость с температурой кипения 34-38°. Достоинствами его являются большая
широта наркотического действия, слабое угнетающее действие на ССС, на паренхиматозные органы, на
дыхание, достаточная глубина наркоза и четкое управлением им. К недостаткам эфира относятся
раздражение слизистых оболочек, вызывающее обильное слюноотделение, увеличение секреции
бронхиальных желез, отрицательные рефлексы на сердце, спазмы гортани. С этим связана также
выраженная стадия возбуждения. Эфир слабее, чем другие наркотики, угнетает сердце, печень, почки.
Он вызывает увеличение сахара, молочной и пировиноградной кислот в крови, сдвиг реакции крови в
кислую сторону, увеличение секреции адреналина и гидрокортизона. Эти эффекты связаны с
повышением тонуса симпато-адреналовой системы.
Фторотан - летучая невоспламеняющаяся и невзрывоопасная жидкость с температурой кипения 50
градусов. Относится к наиболее сильным наркотикам, в 3 раза сильнее эфира, но аналгезирующее
действие у него слабее. При вдыхании паров фторотана наркоз наступает быстро (через 3-5 мин).
Стадия возбуждения выражена слабо или отсутствует. Не раздражает дыхательные пути. Стадия
хирургического наркоза протекает подобно эфирному наркозу. Пробуждение быстрое, рвоты,
посленаркозной депрессии не вызывает. Около 80% фторотана выделяется легкими в неизмененном
виде. Широта действия близка к эфиру, наркоз легко управляем. Однако токсичность по отношению к
ССС более высокая, чем у эфира. Фторотан ослабляет сократимость миокарда, снижает АД. Этот
эффект связан с угнетением сосудодвигательного центра, блокадой симпатических ганглиев и прямым
действием на сосуды. Он может вызвать аритмию сердца в результате угнетения миокарда и
сенсибилизации его к адреналину. Поэтому на фоне фторотанового наркоза введение адреналина, НА и
эфедрина противопоказано. Можно вводить мезатон. На печень фторотан оказывает более сильное
действие, чем эфир, и при заболеваниях печени может вызвать дегенеративные изменения.
Таким образом, положительные свойства эфира и фторотана дополняют друг друга, что позволяет
использовать их азеотропную смесь, содержащую 31,7% эфира и 68,3% фторотана.
Энфлуран и метоксифлуран также обладают высокой наркотической активностью. Свойства
энфлурана близки фторотану, метоксифлуран действует медленнее фторотана и нередко поражает
почки, поэтому его применяют редко.
Газообразные наркотические средства. К ним относятся азота закись и цихлопропан. Газовый
наркоз требует специальной аппаратуры, с помощью которой наркотик подается в смеси с кислородом
под определенным давлением в дыхательные пути.
Азота закись применяют в смеси с кислородом 4:1. Наркоз при этом поверхностный и не
сопровождается расслаблением мышц, т.е. не бывает глубже 1-го уровня. Поэтому азота закись обычно
применяют с другими наркотиками и миорелаксантами. Это единственный недостаток азота закиси. Во
всем остальном это идеальное средство. Она обладает сильным аналгезирующм действием, не
раздражает слизистые, не дает стадии возбуждения, пробуждение наступает сразу после прекращения
наркотизации, никаких осложнений не вызывает. Ее применяют при обезболивании родов, инфаркте
миокарда, травмах.
Циклопропан по наркотической активности превосходит азота закись в 6 раз, не раздражает
слизистые, имеет большую широту наркотического действия. В смеси с кислородом 1:4 вызывает
быстрый наркоз с расслаблением мускулатуры. Пробуждение наступает быстро. Основным
недостатком циклопропана является токсичность для сердца. Он может вызвать нарушения ритма,
повышает чувствительность миокарда к в-адреномиметикам, поэтому на фоне циклопропанового
наркоза их применять опасно. Его действие на сердце устраняется в-адреноблокаторами.
Средства для неингаляционного наркоза.
Их назначают преимущественно в/в. Впервые неингаляционный наркоз применил Н.И.Пирогов в
1847 г. Но широкое применение ом получил после исследований Н.П.Кравкова и С.П.Федорова в 19031910 гг. В настоящее время для в/в наркоза используют тиопентал-натрий, гексенал, пропанидид,
предион, кетамин, натрия оксибутират.
Тиопентал-натрий при медленном в/в введении вызывает наркоз сразу, без стадии возбуждения.
Продолжительность наркоза - 20-30 мин. Наиболее высокие концентрации препарата создаются а мозге,
сердце, печени и почках. Прекращение наркоза связано с перераспределением вещества и накоплением
его в жировой ткани (до 80%), в результате чего концентрация в мозге резко снижается. Инактивация
просходит медленно, поэтому поступая в кровь из жирового депо, тиопентал-натрий вызывает
длительную посленаркозную депрессию. Его действие распространяется на все отделы ЦНС, но
наиболее сильно - на ретикулярную формацию. При быстром введении может наступить резкое
угнетение дыхания и кровообращения. Поэтому вводить препарат надо медленно, наблюдая за
состоянием больного. У некоторых во время введения наркотика возникают мышечные подергивания и
ларингоспазм. Он угнетает дыхательный центр сильнее эфира при равной глубине наркоза. В отличие
от эфира оказывает слабый аналгезирующий эффект. Сердце и печень угнетает слабее ингаляционных
наркотиков. Применяют тиопентал-натрий при непродолжительных операциях и для вводного наркоза.
Гексянал обладает сходными свойствами.
Предион (виадрил) является стероидным производным. Он обладает невысокой наркотической
активностью, поэтому используется, в основном, для вводного наркоза. Наркоз развивается постепенно
в течение 5-15 мин. без стадии возбуждения. Предион малотоксичен, на дыхание, ССС, печень и почки
оказывает слабое влияние. Наиболее частым осложнением являются тромбофлебиты из-за его
раздражающих свойств. Продолжительность наркоза -20-30 мин.
Кетамин по продолжительности эффекта относится к препаратам среднего действия. Его вводят в/в
и в/м. При в/в введении наркоз наступает через 30-60. сек., продолжительность - 5-10 мин., а при в/м через 2-6 мин., продолжительность 15-30 мин. Наркотическая активность низкая: вызывает аналгезию и
утрату сознания, но рефлексы и мышечный тонус сохраняются. Кетамин применяют при
кратковременных операциях и для вводного наркоза.
Натрия оксибутират - производное гамма-аминомаслянной кислоты (ГАМК), которая является
тормозным медиатором ЦНС. В отличие от ГАМК он хорошо проникает через ГЭБ, оказывает
успокаивающее, снотворное, наркотическое и антигипоксическое действие. Наркотическая и
аналгезирующая активность у него недостаточна, но мышцы расслабляет хорошо. Действие развивается
медленно (через 30-40 мин после в/в введения), но действует продолжительно (до 3 ч). Стадию
возбуждения не вызывает. При приеме внутрь наркоз наступает через 40-60 мин. Препарат
малотоксичен, дыхание и кровообращение не угнетает. Применяют для вводного и базисного наркоза,
при гипоксии мозга, при судорогах, шоке. Усиливает действие других наркотических средств, не влияя
на их токсичность.
Пропанидид (сомбревин) - наркотик ультракороткого действия (3-5 мин). Наркоз наступает быстро,
без стадии возбуждения и быстро прекращается из-за гидролиза пропанидида холинэстеразой крови.
Малотоксичен, не вызывает серьезных осложнений, но может вызывать тромбофлебиты, иногда
мышечные подергивания. Пробуждение быстрое, без депрессии. Применяют при кратковременных
операциях и для вводного наркоза.
Комбинированный наркоз.
Осуществляется сочетанием различных наркотических ЛС, а также наркотических с
ненаркотическими. Это связано с тем,что каждому наркотику свойственны положительные и
отрицательные эффекты. Комбинирование позволяет устранить или уменьшить отрицательное действие
и усилить положительное. Наиболее часто комбинируют ЛС для ингаляционного наркоза с ЛС для
неингаляционмого наркоза. При этом введение а наркоз осуществляют с помощью неингаляциомного
наркотика, а последующий наркоз - с помощью ингаляционного. Широко применяют также
комбинации с ненаркотическими ЛС (нейролептиками, транквилизаторами, мышечными релаксантами,
аналгетиками, холиноблокаторами). Для подготовки больного к наркозу (премедикация) используют
транквилизаторы, аналгетики, холиноблокаторы. Непосредственно перед операцией в/в вводят
неингаляционный наркотик. Если планируется интубация, вводят миорелаксант (обычно дитилин).
Лекция 9.
СПИРТ ЭТИЛОВЫЙ. СНОТВОРНЫЕ СРЕДСТВА.
Необходимо изучить следующие вопросы:
* -местное действие спирта этилового;
* -фармакокинетика и фармакодинамика, медицинское применение спирта;
*-острое и хроническое отравление спиртом, лечение отравлений;
* -современные представления о природе сна;
* -МД снотворных средств, их классификация;
* -особенности действия барбитуратов, алифатических соединений и бензодиазепинов;
* -применение снотворных средств, ПЭ и лечение отравлений снотворными.
Спирт этиловый.
Спирты (алкоголи) представляют собой углеводороды алифатического ряда, к которым присоединен
гидроксильный радикал (-ОН). С увеличением числа углеродных атомов (молекулярной массы)
токсичность спиртов возрастает. Так, пропиловый спирт токсичнее этилового, бутиловый токсичнее
пропилового, амиловый токсичнее бутилового. Исключением из этого правила является метиловый
спирт (древесный), который значительно токсичнее этилового, хотя имеет в своей молекуле один атом
углерода. Его токсичность обусловлена превращением в организме с образованием ядовитых продуктов
формальдегида и муравьиной кислоты, которые резко угнетают ЦНС, сердце, вызывают атрофию
зрительного нерва. Примесь высокомолекулярных спиртов к этиловому спирту в плохо очищенных
алкогольных напитках (самогон и др.) резко усиливает его токсичность.
В медицинской практике используют чистый этиловый спирт. Различают местное и резорбтивное
действие спирта. На кожу и слизистые он оказывает раздражающее действие, растворяет жиры,
отнимает воду и свертывает белок. Раздражающее действие проявляется гиперемией, ощущением тепла
и используется в виде компрессов (40% р-р спирта). Спирт оказывает антисептическое действие в
результате коагуляции белка в микробных клетках. Эффект возрастает с увеличением концентрации
спирта. Для дезинфекции кожи используют 70% спирт, который лучше проникает в протоки сальных и
потовых желез, так как меньше денатурирует белок и дегидратирует кожу. Для стерилизации
инструментов применяют 95% спирт. В концентрации 18-20% спирт прекращает бродильные и
гнилостные процессы.
При приеме внутрь спирт раздражает слизистые полости рта и желудка, усиливая секрецию желез.
Малые концентрации (до 10-12%) не снижают активность пепсина, а более высокие концентрации
угнетают переваривающую способность желудочного сока. При этом выделяется слизь, которая
защищает слизистую желудка, может наступить спазм привратника и угнетение моторики желудка.
Длительное применение спирта в высоких концентрациях сопровождается развитием катаррального
состояния слизистой.
20% спирта всасывается в желудке, 80% - в тонком кишечнике. Скорость всасывания зависит от
характера и количества пищи. Наиболее сильно всасывание спирта задерживают мясо, картофель,
жиры. Максимальная концентрация спирта в крови наступает через 1-1,5 ч. после приема.
Распределение спирта в организме происходит быстро, так как он хорошо растворяется в липидах и
легко преодолевает биологические барьеры. Концентрация в различных органах зависит от их
кровоснабжения (наиболее высокая в печени и мозге). 90% спирта окисляется до воды и СО2, остальное
количество выделяется через легкие и почки в неизмененном виде. При окислении 1 г спирта
образуется 7,1 ккал тепла. Окисление происходит в печени со скоростью 10 мл/ч.
Спирт является типичным наркотиком, поэтому оказывает угнетающее действие на ЦНС. При
приеме больших доз спирта можно выделить 3 стадии: 1) стадия возбуждения (эйфории); 2) стадия
наркотического торможения: 3) агональная стадия. Стадия возбуждения, в отличие от средств для
наркоза, продолжительна. В лаборатории И.П.Павлова установлено, что она является мнимой, так как
связана с угнетением тормозных процессов. Поэтому даже небольшие дозы алкоголя снижают
умственную работоспособность. Алкогольная эйфория характеризуется повышением настроения,
ослаблением самоконтроля, критического анализа своего поведения и т.п. С увеличением концентрации
спирта в крови развивается угнетение ЦНС: вялость, сонливость, аналгезия, растройство речи,
нарушение координации движений, снижение тонуса мышц, АД, учащение пульса, угнетение
спинальных рефлексов. Широта наркотического действия незначительна и стадия наркоза легко
переходит в агональную стадию, которая характеризуется угнетением дыхания и кровообращения.
Поэтому спирт для наркоза не применяют.
В небольших дозах спирт увеличивает теплопродукцию и теплоотдачу, связанную с расширением
кожных сосудов. При этом возникает ощущение тепла. На морозе спирт может ускорить потерю тепла и
переохлаждение, поэтому для согревания его следует использовать только после попадания человека с
мороза в теплое помещение. В состоянии опьянения опасность замерзнуть резко возрастает.
Спирт применяют, в основном, как антисептик. Его можно использовать также для снятия психоэмоционального напряжения, для профилактики шока при травмах, как энергетическое средство
истощенным больным.
Острое отравление спиртом характеризуется развитием алкогольной комы. Опьянение наступает
при концентрации спирта в крови 1-2 г/л; 3-4 г/л вызывают тяжелую интоксикацию, а 5-8 г/л являются
смертельными. Лечение отравления направлено на восстановление дыхания (кислород, кофеин,
кордиамин) и кровообращения (строфантин, мезатон, эфедрин). Необходимо промыть желудок, ввести
в/в натрия гидрокарбонат для ликвидации ацидоза. В тяжелых случаях проводят гемодиализ.
Отравленного спиртом надо согревать.
Хроническое отравление (алкоголизм) возникает при частом и длительном употреблении алкоголя
и характеризуется развитием психической и физической зависимости (алкогольной наркомании).
Кардинальным признаком алкоголизма является болезненная потребность в опохмелении. При
алкоголизме наиболее сильно страдает психика: ослабление интеллекта, памяти, внимания, чувства
долга, ответственности, умственной работоспособности и т.п. Постепенно развивается деградация
личности, психические расстройства, цирроз печени, гастрит, дистрофия миокарда, почек,
полиневриты. Алкоголь хорошо проникает через плаценту и эпителий молочных желез и оказывает
отрицательное действие на плод и грудного младенца. Лечение алкоголизма проводят различными
методами. Главной целью является выработка у алкоголика отрицательного отношения к алкоголю.
Применяют методы психотерапии, гипноза, противоалкогольные ЛС (тетурам, эспераль и др.). Тетурам
и эспераль задерживают окисление спирта на уровне ацетальдегида в результате угнетения
ацетальдегидоксидазы, в результате чего возникают симптомы интоксикации (боли в сердце, головная
боль, гипотония, тошнота, рвота, чувство страха и т.п.). Эти явления постепенно формируют
отвращение к алкоголю. Эспераль является тетурамом пролонгированного действия и имплантируется
под кожу. При назначении этих ЛС алкоголь принимают в строго ограниченном количестве, так как
превышение его дозы может вызвать тяжелое отравление ацетальдегидом и смерть. Для лечения
алкоголизма используют психотропные ЛС, а также апоморфин, который назначают для выработки
отрицательного рефлекса на алкоголь.
Снотворные средства.
Сон - активный процесс, необходимый для восстановления энергетических ресурсов и функций
ЦНС. Он является защитным механизмом и обеспечивает переход организма от активной деятельности
к состоянию покоя. Механизм сна очень сложный и до конца не выяснен. Установлено, что сон не
является однородным состоянием и состоит из двух фаз, которые чередуются между собой.
1. "Медленный" или "синхронизированный" сон, при котором наблюдаются синхронная работа
нейронов коры, медленная высоковольтная активность на ЭЭГ, снижение обменных процессов,
секреции желез, температуры тела и АД, преобладание тонуса холинергической системы. Фазы
медленного сна составляют около 75% времени сна.
2. "Быстрый" или "десинхронизированный" сон, характеризующийся быстрой низковольтной
активностью на ЭЭГ, свойственной состоянию бодрствования, быстрыми движениями глаз, наличием
сновидений, повышенным тонусом адренергической системы, увеличением секреции катехоламинов,
кортикостероидов, усилением обмена веществ и потребления кислорода мозгом, повышением тонуса
сосудов и работы сердца. Поскольку эти процессы имеют парадоксальный характер, фазу быстрого сна
называют также "парадоксальным" сном. В общей сложности она занимает около 25% времени сна.
Правильное чередование и соотношение фаз является признаком нормального сна. Любое нарушение
баланса фаз приводит к нарушениям ЦНС.
Различают пробуждающую систему (активирующая часть ретикулярной формации) и систему
засыпания (гипногенная система), которая включает нижние отделы ствола, базальные ядра переднего
мозга, латеральные преталамические и медиальные таламические области, хвостатое ядро. Обе системы
связаны с лимбической системой и корой больших полушарий мозга. Во время сна активность
гипногенной системы возрастает, а пробуждающей снижается. Химическая основа сна неизвестна.
Выделен пептид д-сна, обладающий гипногенным действием, во время сна накапливаются ГАМК,
серотонин, АЦХ, а во время пробуждения преобладают катехоламины.
Снотворные ЛС изменяют соотношение этих систем в пользу гипногенной. Одни снотворные
(барбитураты) угнетают активирующую ретикулярную формацию, другие (бензодиазепины) лимбическую систему и ее связи с другими системами, обеспечивающими смену сна и бодрствования.
Большинство снотворных изменяют структуру сна прежде всего за счет укорочения фазы "быстрого"
сна. После их отмены возникает феномен "отдачи", который характеризуется укорочением
"медленного" и удлинением фазы "быстрого" сна, наличием кошмарных сновидений, частыми
пробуждениями. В этом принципиальное отличие медикаментозного сна от физиологического.
Высокий ритм жизни и большие психоэмоциональные перегрузки создают условия для нарушения
сна. От бессоницы страдают от 20 до 30% населения многих стран. Различают 3 основных формы
нарушения сна: 1) нарушение процесса засыпания ("юношеская" форма), связанное с ослаблением
функций восходящей тормозной системы ствола мозга, преобладанием активирующей системы
ретикулярной формации и гиперфункцией лимбической системы (эмоции); 2) поверхностный сон с
частыми пробуждениями и трудным засыпанием а результате преобладания фазы "быстрого" сна; 3)
быстрое засыпание, но укороченный сон в результате снижения активности гипногенной системы
("старческая" бессоница). 1-я форма обычно встречается у молодых, а 2-я и 3-я - у пожилых лиц со
склерозом сосудов мозга.
Снотворные ЛС подразделяют на 2 группы: 1) снотворные с наркотическим типом действия - а)
гетероциклические соединения (барбитураты): фенобарбитал, барбитал, барбитал-натрий, барбамил,
этаминал-натрий; б) алифатческие соединения (хлоралгидрат, бромизовал); 2) снотворные с
транквилизируюшим эффектом: производные бензодиазепина (нитразепам, феназепам и др.).
Для 1-й группы ЛС характерно отсутствие избирательности действия на ЦНС, последовательность
развития успокаивающего, снотворного и наркотического эффектов в зависимости от доз. Однако для
наркоза их не применяют из-за малой широты наркотического действия. Барбитураты действуют
преимущественно на активирующую часть ретикулярной формации, укорачивая "быстрый" сон и
удлиняя "медленный". Отмена барбитуратов может сопровождаться феноменом "отдачи". В кишечнике
они почти полностью всасываются, так как хорошо растворимы в липидах. От 5 до 75% связываются с
белками крови. У барбамила и этаминала-натрия действие наступает через 10-30 мин, у барбитала и
фенобарбитала - через 40-60 мин. Продолжительность действия примерно одинакова. Метаболизм
происходит в печени и зависит как от структуры препарата, так и от функции печени. Барбамил и
этаминал-натрий обезвреживаются быстро и выводятся почками преимущественно в виде метаболитов,
не вызывая последействия (сонливость, вялость). Барбитал и фенобарбитал элиминируют медленно
(50% за 3,5 суток), поэтому вызывают последействие. При повторном введении они способны
кумулировать, особенно при заболеваниях печени. Феномен "отдачи" может наблюдаться несколько
недель после отмены препарататов. При длительном применении барбитуратов развиваются
привыкание и лекарственная зависимость (психическая и физическая), которая при отмене препарата
проявляется абстиненцией (беспокойство, раздражительность, рвота, нарушение зрения, судороги,
ортостатическая гипотония и т.п.). В дозах от 1/3 до 1/20 снотворной они оказывают успокаивающее
действие.
При остром отравлении барбитуратами развивается кома (отсутствие сознания, угнетение
рефлексов, мышечного тонуса, дыхания, падение АД, угнетение функции почек). Лечение: промывание
желудка, внутрь активированный уголь, солевое слабительное, форсированный диурез, введение натрия
гидрокарбоната. При тяжелом отравлении проводят гемосорбцию и гемодиализ. Для восстановления
дыхания используют искусственное дыхание с кислородом. При нетяжелом отравлении можно ввести
стимуляторы дыхания (бемегрид, коразол и др.). Для нормализации кровообращения применяют
адреномиметики, переливание крови, кровезаменителей.
Алифатические соединения (хлоралгидрат, бромизовал) почти не нарушают структуру сна. В
больших дозах вызывают наркоз. Хлоралгидрат используют, в основном, при непереносимости
барбитуратов и как противосудорожное. Он оказывает раздражающее действие на слизистые. поэтому
противопоказан при гастритах и язвенной болезни желудка. Его назначают вместе с обволакивающими
средствами. После всасывания превращается в трихлорэтанол, который и вызывает сон.
Обезвреживание происходит в печени. При заболеваниях печени и почек противопоказан.
Кумулятивными свойствами не обладает. При длительном применении может вызвать привыкание и
лекарственную зависимость. Бромизовал оказывает более слабый снотворный эффект. У него хорошо
выражены седативные свойства, поэтому его используют преимущественно как успокаивающее
средство.
Производные бензодиазепина наряду с транквилизирующим действием способствуют наступлению
сна. Снотворное действие наиболее выражено у нитразепама, который обладает также
миорелаксирующими и противосудорожными свойствами. Нитразепам действует преимущественно на
лимбическую систему и в меньшей степени - на кору и ретикулярную формацию. Миорелаксация
связана с угнетением передачи двигательных импульсов в синапсах спинного мозга. Он почти не
нарушает структуру сна, поэтому сон близок к естественному. Последействие и феномен "отдачи" не
возникают. При приеме внутрь сон наступает через 30-60 мин и продолжается до 8 ч. Инактивация
препарата происходит в печени без влияния на ее функции. Нитразепам мало токсичен, имеет
достаточную широту терапевтического действия. Он особенно эффективен при нарушениях сна,
связанных с психоэмоциональным напряжением.
Натрия оксибутират обладает хорошим снотворным действием, малой токсичностью, не нарушает
структуру сна, не вызывает последействия и феномена "отдачи", так как является производным
тормозного медиатора ЦНС -ГАМК.
Лекция 10.
НАРКОТИЧЕСКИЕ АНАЛЬГЕТИКИ.
В эту группу входят ЛВ, избирательно подавляющие чувство боли за счет влияния на ЦНС и
способные вызывать пристрастие (наркоманию).
Необходимо знать следующие вопросы:
•-механизм формирования боли. роль опиатных рецепторов, алкалоиды опия;
•-классификация наркотических анальгетиков:
* -МД и основные фармакологические эффекты морфина;
* -острое и хроническое отравление морфином, борьба с наркоманией;
* -особенности фармакокинетики и фармакодинамики омнопона, промедола, фентанила, пиритрамида,
пентазоцина;
* -показания и противопоказания для применения наркотических анальгетиков;
* -антагонисты морфина (налорфин, налоксон), их МД и применение.
Боль - субъективная реакция, возникающая при раздражении болевых рецепоров. Она служит
сигналом опасности, предохраняющим организм от повреждающих факторов. В то же время длительная
интенсивная боль вызывает не только тягостные ощущения, но и приводит к тяжелым нарушениям
функций, вплоть до развития шока. Устранение или предупреждение такой боли имеет большое
значение. Механизм боли очень сложен. Болевые ощущения зависят от соотношения и взаимодействия
болевой (ноцицептивной) и противоболевой (антиноцицептивной) систем. Болевая система включает
рецепторы боли, нервные проводники, вставочные нейроны и проводящие пути спинного мозга,
структуры головного мозга (ретикулярная формация, лимбическая система, таламус, гипоталамус,
кора), по которым болевые раздражения поступают в ЦНС, анализируются и вознкают ответные
реакции к скелетным мышцам (двигательные реакции) и к вегетативным нервам (вегетативные
реакции). Противоболевая система включает опиатные рецепторы ЦНС, нисходящие пути, вставочные
нейроны и нейроны задних рогов спинного мозга. Ее роль состоит в торможении болевых реакций. В
регуляции этой системы участвуют серотонин, НА, АЦХ и пептиды с анальгетической активностью
(энкефалины и эндорфины), так называемые эндогенные опиоиды. Открытие этих механизмов
возникновения и подавления боли имеет большое значение как для понимания действия анальгетиков,
так и для создания новых эффективных болеутоляющих средств.
Действие наркотических аиальгетиков обусловлено взаимодействием с опиатными рецепторами,
локализованными в ЦНС и периферических органах. Различают агонисты и антагонисты опиатных
рецепторов.
Родоначальником этой группы является морфин, который получают из опия. Опий - высохший
млечный сок из недозрелых головок снотворного мака. Болеутоляющее и одурманивающее действие
опия было известно еще древним шумерам за 4000 лет до н.э. Позднее эти сведения распространились в
Египет, Китай, Индию, Грецию и другие страны. В чистом виде морфин был выделен из опия
Сертюрнером в 1806 г. и получил название морфина в честь древнегреческого бога сна и сновидений
Морфея. Из опия выделено свыше 20 алкалоидов. Около 10% опия составляет морфин. По структуре
алкалоиды делятся на производные фенантрена (морфин, кодеин, тебаин и др.) и производные
изохинолина (папаверин, наркотин). Первые действуют преимущественно на ЦНС, вторые - на гладкие
мышцы кишечника, бронхов, сосудов и других органов (спазмолитическое).
К наркотическим анальгетикам относятся: 1) производные фенантрена (препараты опия,
омнопон, морфин, кодеин и др.); 2) производные пиперидина (промедол, фентанил, пиритрамид); 3)
прозводные гептанона (фенадон, пальфиум и др.).
Морфин является основным алкалоидом опия. В фармакодинамике морфина главное значение имеет
болеутоляющее действие. МД морфина сложный. Считают, что главную роль играет стимуляция
опиатных рецепторов, которая сопровождается активацией нисходящей противоболевой системы. В
результате этого угнетается передача импульсов в синапсах ЦНС, ослабляется психоэмоциональное
восприятие боли, ее оценка и реакция на нее. Возникает седативный эффект в результате снижения
функций активирующей части ретикулярной формации, лимбической системы, таламуса и
гипоталамуса. Усиление тормозных влияний противоболевой системы приводит к снижению
активности нейронов спинного мозга, что сопровождается уменьшением двигательных и вегетативных
реакций. Кроме того, морфин угнетает межнейронную передачу импульсов, идущих от рецепторов
боли, на разных уровнях ЦНС.
Таким образом, болеутоляющий эффект морфина слагается из стимуляции противоболевой системы
и ослабления влияний болевой системы на уровне ЦНС.
Успокаивающее действие морфина часто сопровождается улучшением настроения, положительным
восприятием обстановки, жизни, чувством душевного комфорта. Это безотчетно приятное состояние
называют эйфорией. Вслед за эйфорией развиваются сонливость и неглубокий сон с яркими
сновидениями (морфийный сон). После прекращения действия морфина может наблюдаться ощущение
депрессии, снижения работоспособности и т.п. Психические и физические расстройства после
прекращения действия морфина наиболее ярко выражены при возникновении пристрастия
(наркомании).
Морфин оказывает различное влияние на центры продолговатого мозга. Он угнетает дыхательный
и кашлевой центры. При действии терапевтических доз урежение дыхания компенсируется его
углублением, но при увеличении доз происходит уменьшение минутного объема дыхания. В
токсических дозах морфин вызывает резкое угнетение дыхания (типа Чейна-Стокса) вплоть до паралича
дыхательного центра. У большинства людей морфин угнетает центр рвоты, но у некоторых вызывает
тошноту и рвоту. Он стимулирует центр глазодвигательного нерва и вызывает сужение зрачков,
возбуждает центр вагуса и урежает сердечные сокращения. На сосудодвигательный центр существенно
не влияет и не нарушает кровообращение. Морфин угнетает центр теплорегуляции и снижает
температуру, ослабляет окислительные процессы и выработку тепла. понижает аппетит и диурез.
Стимулируя опиатные рецепторы гладких мышц, морфин повышает тонус сфинктеров ЖКТ, мочевого
пузыря, тонус кишечника, желчевыводящих и мочевыводящих путей, бронхиальных мышц и вызывает
запоры. Из ЖКТ морфин всасывается недостаточно, поэтому его назначают парэнтерально. Действует
4-6 ч. 90% морфина метаболизируется в печени, 10% выделяется через почки и ЖКТ в неизмененном
виде.
Омнопон - новогаленовый препарат опия. представляющий сумму алкалоидов и очищенный от
балластных веществ. Около 50% омнопона составляет морфин. Благодаря наличию папаверина
омнопон оказывает, наряду с болеутоляющим, слабое спазмолитическое действие. В остальном сходен
с морфином.
Кодеин значительно уступает морфину по анальгетическому эффекту, но имеет выраженное
противокашлевое действие. Его назначают при затяжном сухом кашле.
Производные пиперидина (промедол, фентанил, пиритрамид, пентазоцин) являются синтетическими
заменителями морфина. Промедол по силе анальгетического эффекта уступает морфину в 2-3 раза, но
меньше угнетает дыхание, реже вызывает тошноту и рвоту, не угнетает перистальтику ЖКТ, снижает
тонус гладких мышц бронхов, желче- и мочевыводящих путей, шейки матки, расширяет зрачки. Эти
эффекты обусловлены м-холинолитическими свойствами. Фентанил по болеутоляющему действию
превосходит морфин в 100-400 раз, действует быстро (через 1-3 мин) и полностью подавляет боль, не
выключая сознания. Сильнее морфина угнетает дыхание. В комбинации с нейролептиком
дроперидолом его используют для иейролептанальгезии. Смесь называют таламонал. Пиритрамид
действует сильнее и продолжительнее морфина. Пентазоцин по силе анальгетического эффекта
уступает морфину, но не вызывает эйфорию и редко вызывает пристрастие, меньше угнетает дыхание,
перистальтику кишечника, вызывает тахикардию и повышает АД. Он является частичным антагонистом
опиатных рецепторов, поэтому ослабляет некоторые эффекты морфина.
Показания для применения наркотических анальгетиков: 1) травмы, угрожающие развитием
шока; 2) при подготовке к операции и после нее; 3) приступы почечно- и желчнокаменной болезни
(колики) - промедол или омнопон с атропином; 4) инфаркт миокарда; 5) злокачественные
иноперабильные опухоли. Противопоказания: 1) недостаточность функции дыхания; 2) острые
заболевания органов брюшной полости (до установления диагноза); 3) травмы черепа (из-за опасности
повышения внутричерепного давления и отека мозга); 4) детям до 3 лет и в старческом возрасте (из-за
опасности угнетения дыхания).
Антагонсты наркотических аналгетиков. Налорфин - агонист-антагонист опиатных рецепторов,
поэтому имеет частичное сходство с морфином (анальгезия, брадикардия, сужение зрачков), но слабее
его. В отличие от морфина не вызывает пристрастие, у морфинистов вызывает абстиненцию. При
отравлении морфином устраняет угнетение дыхания, брадикардию, спазмы гладкой мускулатуры.
Налоксон - полный антагонист морфина, так как блокирует все опиатные рецепторы, поэтому
устраняет основные эффекты наркотических анальгетиков.
Острое отравление морфином проявляется комой: отсутствие сознания, резкое угнетение дыхания,
развитие периодического дыхания Чейна-Стокса, зрачки резко сужены, спинальные рефлексы
повышены, температура тела снижена. Лечение: искусственное дыхание, кислород, введение этимизола,
налорфина или налоксона для восстановления дыхания, согревание больного.
Хроническое отравление (морфинизм) возникает в результате пристрастия и привыкания. В связи с
привыканием морфинист вынужден постоянно увеличивать дозу для получения эффекта, что усиливает
интоксикацию и зависимость. Постепенно развиваются расстройства психики, утрата чувства долга,
достоинства, ограничивается круг интересов, ослабевает воля, истощаются силы, возникают
вегетативные расстройства (потеря аппетита, запоры, усиленное потоотделение, нарушение работы
сердца, быстрое исхудание). Происходит постепенное разрушение личности. После прекращения
действия наркотика возникает тяжелая абстиненция (болезнь воздержания). сопровождающаяся
серьезными психическими и физическими нарушениями, которые устраняются морфином. Связано это
с тем, что при развитии наркомании снижается выработка естественных стимуляторов опиатных
рецепторов (энкефалинов и эндорфинов), заменителем которых становится наркотик. Лечение
морфинизма проводится в специальных наркологических отделениях. Оно должно быть длительным, но
даже после излечения эффект обычно нестойкий и часто возникают рецидивы наркомании.
Лекция 11.
НЕНАРКОТИЧЕСКИЕ АНАЛЬГЕТИКИ,ЖАРОПОНИЖАЮЩИЕ, ПРОТИВОВОСПАЛИТЕЛЬНЫЕ
СРЕДСТВА.
К этой группе относятся ЛВ, обладающие болеутоляющим, жаропонижающим и
противоспалительным действием. Необходимо знать:
•-отличия ненаркотических анальгетиков от наркотических;
• -МД и основные фармакологические эффекты ненаркотических анальгетиков;
• -классификация анальгезирующих и противоспалительных средств;
• -основные и ПЭ салицилатов, показания и противопоказания к применению;
•-основные и ПЭ производных пиразолона и анилина, их применение;
• -характеристика нестероидных противовоспалительных ЛС. применение, сравнительная
эффективность и токсичность.
Ненаркотические аналыетики существенно отличаются от наркотических: отсутствие привыкания
и лекарственной зависимости, более слабый анальгетический эффект, болеутоляющее действие
проявляется преимущественно при болях, связанных с воспалением (у наркотических - при болях,
связанных с повреждением тканей), действуют преимущественно на периферические органы
(наркотические - на ЦНС), оказывают выраженный противоспалительный и жаропонижающий
эффекты, не угнетают дыхание и т.д.
МД ненаркотических анальгетиков и противоспалительных ЛС связан с угнетением синтеза
простагландинов (ПГ) в результате инактивации фермента цнклооксигеназы. ПГ образуются в
процессе превращения арахидоновой кислоты: фосфолипиды -(+фосфолипаза)- арахидоновая кислота
(+ циклооксигеназа) - циклические эндопероксиды - простагландины -(воспаление, боль, лихорадка).
ПГ повышают чувствительность болевых рецепторов к "медиаторам воспаления" (брадикииин,
гистамин, серотонин и др.) и другим химическим и механическим раздражителям. Одновременно они
усиливают воспаление, отек, что приводит к механическому сдавливанию нервных волокон и
рецепторов и усиливает боль. Этим можно объяснить тот факт, что болеутоляющий эффект
анальгетиков наиболее выражен при воспалении тканей, заключенных в трудно растяжимые оболочки
(ткань зуба, суставы, нервные стволы, мозговые оболочки, мышечные волокна).
Таким образом, угнетение синтеза ПГ приводит к уменьшению воспаления и боли. Одновременно
анальгетики угнетают проведение импульсов в ЦНС. Жаропонижающий эффект также объясняется
угнетением синтеза ПГ, в частности, ПГИ1, который возбуждает центр терморегуляции. Этот эффект
проявляется только на фоне лихорадки и обусловлен увеличением теплоотдачи за счет расширения
кожных сосудов и потоотделения.
К изучаемой группе ЛС относятся: 1) производные салициловой кислоты (салицилаты) ацетилсалициловая кислота (аспирин), салициламид, метилсалицилат, натрия салицилат; 2)
производные пиразолона - анальгин, бутадион; 3) производные анилина - фенацетин, парацетамол; 4)
производные антраниловой кислоты - мефенамовая кислота и ее натриевая соль; 5) производные
индолуксусной кислоты - индометацин; 6) производные фенилуксусной кислоты - диклофенак-натрий
(вольтарен); 7) производные фенилпропионовой кислоты - напроксен.
Салицилаты являются наиболее старыми и изученными средствами. Они проявляют выраженное
болеутоляющее, противоспалительное и жаропонижающее действие, стимулируют дыхание (особенно в
больших дозах), что может привести к развитию алкалоза, существенно не влияют на ССС. Салицилаты
угнетают агрегацию тромбоцитов и снижают свертывание крови. Этот эффект связан с угнетением
синтеза тромбоксана. Увеличивают желчевыделение и экскрецию мочевой кислоты через почки,
поэтому могут использоваться при подагре. В больших дозах угнетают синтез белка, увеличивают
распад аминокислот и жиров, снижают сахар крови при сахарном диабете. Применяют при различных
формах ревматизма, неревматическом артрите, подагре, арталгии, невралгии, миозитах, невритах,
головной, зубной боли, при лихорадке. При лихорадке необходимо учитывать, что умеренное
повышение температуры оказывает защитное действие, так как стимулирует фагоцитарную реакцию,
образование антител, ферментативную активность, барьерную функцию печени и повышает
устойчивость к микробным токсинам. Поэтому для снижения температуры их следует назначать при
высокой лихорадке, которая становится опасной для организма. Это относится и к другим
жаропонижающим ЛС. ПЭ салицилатов связаны с раздражающим действием на ЖКТ, угнетением
синтеза ПГ, возбуждением рецепторов пусковой зоны рвотного центра. Они проявляются
диспептическими расстройствами (тошнота, рвота), изъязвлениями, кровоточивостью слизистой. При
приеме больших доз возникают звон в ушах, ослабление слуха, аллергия. При отравлении
салицилатами наблюдаются нарушения ЦНС, ЖКТ, КОС, гипокалиемия, дегидратация, гипертермия.
Лечение, промывание желудка, адсорбенты, солевые слабительные, нормализация КОС (введение
натрия гидрокарбоната) и водно-электролитного баланса, диуретики быстрого действия (фуросемид). В
тяжелых случах проводят переливание крови и гемодиализ.
Наиболее широко применяют ацетилсалициловую кислоту (аспирин). Метилсалицилат хорошо
всасывается через кожу, поэтому его применяют для втираний в болезненную область. Салициламид и
натрия салицилат применяют реже. Салициловая кислота обладает кератопластическим и
кератолитическим действием в зависимости от концентраций, а также противомикробным, поэтому ее
используют местно в виде мазей, паст, спиртовых р-ров.
Производные пиразолона (анальгин, бутадион) обладают аналогичными эффектами. Болеутоляющий
и жаропонижающий эффекты более выражены у анальгина, а противовоспалительный - у бутадиона.
Они хорошо всасываются в ЖКТ. Анальгин хорошо растворяется в воде, поэтому его можно назначать
в инъекциях. Эти препараты показаны при тех же заболеваниях, что и салицилаты. Наиболее опасным
ПЭ является угнетение кроветворения. Бутадион часто вызывает диспептические расстройства,
обострение язвы желудка и 12-перстной кишки, нарушения функции печени, отеки, аллергические
реакции.
Производные анилина (фенацетин, парацетамол) оказывают преимущественно болеутоляющее и
жаропонижающее действие и слабое противовоспалительное. Фенацетин в организме превращается в
парацетамол, который и оказывает действие. Поэтому применяют преимущественно парацетамол. ПЭ
возникают редко. Фенацетин в больших дозах может вызвать образование метгемоглобина и
сульфгемоглобина в крови, а также поражение почек ("фенацетиновый нефрит").
Производные антраниловой кислоты (мефенамовая и флуфенамовая кислоты и их соли) по силе
анальгетического и противоспалительного эффектов примерно равны ацетилсалициловой кислоте. Они
хорошо всасываются, связываются с белками плазмы и выводятся почками, а основном, в виде
метаболитов. Применяют при хроническом ревматизме. ПЭ связаны с раздражением слизистых и
угнетением синтеза ПГ (диспептические расстройства).
Индометацин (метиндол, индоцид, интебан) - производное индолуксусной кислоты, обладает
преимущественно противоспалительным действием (превосходит салицилаты и бутадион). В
кишечнике всасывается хорошо и действует длительно. Его назначают при ревматизме, подагре. ПЭ
возникают у 30-50% больных: диспептические расстройства, нарушения ЦНС (головная боль,
головокружение, иногда депрессия, галлюцинации), угнетение кроветворения. Противопоказан при
психических заболеваниях, эпилепсии, паркинсонизме, заболеваниях ЖКТ, при беременности и
грудном вскармливании ребенка.
Диклофенак-натрий (ортофен, вольтарен) - производное фенилуксусной кислоты, обладает высокой
активностью, большой широтой терапевтического действия, малой токсичностью и продолжительным
эффектом. ПЭ:
диспептические расстройства, аллергические реакции.
Ибупрофен (бруфен) - производное фенилпропионовой кислоты, по противоспалительному эффекту
равен бутадиону и превосходит салицилаты, реже вызывает ПЭ (в основном, диспептические).
Напроксен (напросин) - производное нафтилпропионовой кислоты, уступает ортофену по
противоспалительному эффекту, но превосходит по болеутоляющему и по продолжительности
действия. Мало токсичен, может вызывать диспептические расстройства.
По силе противоспалительного эффекта перечисленные ЛС можно расположить в следующем
порядке:
иидометацин>ортофен>напроксен>ибупрофен>бутадион>мефенамовая
кислота>ацетилсалициловая кислота>анальгин. Эти ЛС составляют группу нестероидных
противовоспалительных средств (НПВС). Все они обладают противоспалительным, болеутоляющим и
жаропонижающим действием. Эти эффекты обусловлены угнетениием синтеза ПГ на стадии
превращения арахидоновой кислоты в эндопероксиды, так как НПВС ингибируют циклооксигеназу.
НПВС действуют преимущественно на экссудативную фазу воспалительной реакции. Другую группу
противоспалительных ЛС составляют глюкокортикоиды (кортизон, гидрокортизон, преднизолон,
дексаметазон, триамцинолон и др.), имеющие стероидную структуру - стероидные
Противовоспалительные средства (СПВС). МД стероидных ЛВС сложен. Предполагают, что основное
значение имеет угнетение фосфолипазы А2, которая обеспечивает образование арахидоновой кислоты
из фосфолипидов. Это приводит к уменьшению синтеза ПГ, лейкотриенов и оксикислот. Снижение
уровня ПГ сопровождается уменьшением боли, гиперемии и экссудации, а снижение оксикислот и
лейкотриенов - угнетением миграции лейкоцитов в очаг воспаления. СПВС действуют на все фазы
воспаления.
Противоспалительпые ЛС имеют большое значение в лечении многих заболеваний и патологических
состояний.
Лекция 12.
ПРОТИВОЭПИЛЕПТИЧЕСКИЕ ЛС. ПРОТИВОПАРКИНСОНИЧЕСКИЕ ЛС.
В эту группу входят ЛВ, используемые для лечения эпилепсии и паркинсонизма. В лекции будут
рассмотрены следующие вопросы:
*- возможные МД противоэпилептических ЛС;
* - классификация противоэпилептических ЛС по применению;
* - ЛС для лечения больших судорожных припадков и эпилептического статуса;
* - ЛС для лечения психомоторных припадков эпилепсии;
* - ЛС для лечения малых припадков эпилепсии и миоклонус-эпилепсии;
* - механизмы развития паркинсонизма и классификация противопаркинсонических ЛС,
* - МД. применение и ПЭ противопаркинсонических ЛС.
Противоэпилептические средства.
Эпилепсия - хроническое заболевание, протекающее в следующих формах: 1) большие судорожные
припадки; 2) психомоторные припадки; 3) малые припадки; 4) миоклонус-эпилепсия. Соответственно
этим формам подразделяют Противоэпилептические ЛС. МД этих ЛС недостаточно выяснен. Повидимому, он слагается из подавления активности нейронов эпилептогенного очага и угнетения
передачи импульсов из него. Считают, что это действие связано со стабилизацией клеточных мембран,
угнетением процесса деполяризации. возможно, в результате действия на натриевые каналы. Очевидно,
имеет значение увеличение содержания тормозного медиатора - ГАМК.
При больших судорожных припадках используют фенобарбитал, дифенин, гексамидин, натрия
вальпроат, карбамазепин, клоназепам. Препаратами выбора являются фенобарбитал и дифенин.
Действие фенобарбитала было рассмотрено в теме "Снотворные средства". Противоэпилептическое
действие фенобарбитала связывают с угнетением нейронов эпилептогенного очага и распространения
возбуждения на двигательные нейроны коры. Его назначают в субгипнотических дозах. Он оказывает
также седативное и снотворное действие, может кумулировать и вызывать лекарственную зависимость.
Дифенин способствует выведению ионов натрия из нейронов и препятствует их возбуждению при
передаче импульсов из эпилептогенного очага и с пирамидного тракта на мотонейроны спинного мозга.
Он отличается от фенобарбитала более избирательным действием, отсутствием снотворного эффекта,
менее выраженными кумулятивными свойствами. ПЭ проявляются нарушениями ЦНС
(головокружение, атаксия, тремор, нистагм, диплопия и Др.), гиперпластическим гингивитом,
диспептическими расстройствами, кожными высыпаниями. Остальные ЛС имеют менее выраженное
действие, поэтому рассматриваются как вспомогательные. Их используют, главным образом, при
непереносимости фенобарбитала и дифенина. Гексамидин и хлоракон оказывают менее выраженное
противосудорожное действие, но переносятся больными, как правило, легче. При длительном
применении могут вызывать диспептические расстройства, угнетать функции печени, почек,
кроветворных органов, поэтому необходим постоянный контроль.
Иногда большие припадки приобретают затяжной характер и следуют один за другим. Возникает
эпилептический статус. Для его купирования используют в/в введения сибазона (диазепама),
клоназепама, фенобарбитала-натрия. дифенина-натрия и средств для наркоза. Лучшими являются
сибазон и клоназепам.
Психомоторные припадки характеризуются неосознанными и немотивированными поступками,
сумеречным сознанием и автоматизмом поведения. При этом утрачивается память на события,
происшедшие в период припадка. Для лечения используют те же препараты, что и при больших
припадках. Препаратом выбора является карбамазепин (финлепсин), который наряду с
противоэпилептическим действием оказывает успокаивающий .эффект и улучшает настроение. Его
можно использовать при всех остальных формам эпилепсии. ПЭ: нарушения ЦНС (головная боль.
головокружение. нарушение аккомодации зрения), дислептические расстройства. Карбамазепин нельзя
комбинировать с ингибиторами МАО (ниаламид и др.) и с алкоголем.
При малых припадках используют триметин и этосуксимид. МД триметина связан с угнетением
полисинаптических рефлексов спинного мозга и нейронов. Препарат токсичен и может вызывать
тяжелые поражения кроветворного аппарата (аплаксическая анемия, агранулоцитоз). поэтому
необходим систематический контроль за кровью. Вызывает поражения почек, печени, аллергические
реакции. Этосуксимид менее токсичен, при малых припадках используют преимущественно его.
Однако контроль за кровью также обязателен.
Миоклонус-эпилепсия проявляется судорожными подергиваниями мышц без потери сознания. Она
наиболее устойчива к лечению. Препаратами выбора являются транквилизаторы из группы
бензодиазепинов (сибазон, нитразепам, клоназепам). Считают, что их действие связано с активацией
ГАМК через бензодиазепиновые рецепторы.
Натрия вальпроат активен при больших, малых припадках и миоклонус-эпилепсии. Считают, что
МД его связан с накоплением ГАМК.
Противопаркинсонические средства.
Паркинсонизм - заболевание, при котором резко повышен тонус мышц, наблюдается тремор
(постоянное непроизвольное дрожание), скованность движений. Считают, что эта болезнь связана со
снижением содержания дофамина в базальных ядрах и в черной субстанции. При этом снижается
тормозное влияние неостриатум на мотонейроны спинного мозга. В связи с этим для лечения
используют ЛВ, которые увеличивают содержание дофамина или стимулируют дофаминовые
рецепторы. При дефиците дофамина начинают преобладать холйнергические влияния, участвующие в
регуляции функций экстрапирамидной системы. Поэтому лечебного эффекта можно добиться также за
счет блокады холинорецепторов. В связи с этим Противопаркинсонические ЛС можно разделить на 2
группы: 1) ЛВ, активирующие дофаминергические влияния (леводопа, мидантан); 2) ЛВ, угнетающие
холинергические влияния (циклодол, тропацин, амизил).
Леводопа - левовращающий изомер предшественника дофамина -диоксифенилаланина. Дофамин
плохо проникает через ГЭБ, леводола - хорошо, благодаря чему накапливается в стриопалидарной
системе и восстанавливает запасы дофамина. Лечебный эффект леводопы проявляется при болезни
Паркинсона, но при лекарственном паркинсонизме она неэффективна. Действие развивается медленно
(через неделю) и достигает максимума через месяц. Лечение длительными курсами. ПЭ:
диспептические расстройства, ортостатическая гипотензия, сердечные аритмии и др. связаны с
накоплением дофамина в периферических органах и могут быть ослаблены при комбинировании
леводопы с ЛВ, угнетающими ее превращение в дофамин на периферии (напр., карбидопа). Ее можно
комбинировать с центральными холинолитиками, но нельзя с ингибиторами МАО (возникновение
гипертензии) и витамином В6 (ослабление лечебного эффекта).
Мидантан способствует освобождению дофамина и угнетает его обратный нейрональный захват.
Он эффективен как при болезни Паркинсона, так и при симптоматическом паркинсонизме. Действие
развивается через 1-2 дня. ПЭ возникают редко (диспепсия, бессоница, ортостатическая гипотензия,
головокружение и т.п.).
Для блокады м-холинорецепторов используют циклодол, тропацин, амизил и др. Они хорошо
проникают в мозг и блокируют м-ХР базальных ядер, благодаря чему устраняют двигательные
нарушения, связанные с поражением экстрапирамидной системы. Наряду с центральными эффектами
они оказывают периферическое холинолитическое действие, что является причиной ПЭ (сухость во рту,
тахикардия, повышение внутриглазного давления, нарушение аккомодации, угнетение перистальтики и
секреции ЖКТ). Со стороны ЦНС могут наблюдаться возбуждение, галлюцинации. Эти препараты
применяют как при болезни Паркинсона, так и при симптоматическом паркинсонизме.
Лекция 13.
ПСИХОТРОПНЫЕ СРЕДСТВА.
Это большая группа ЛС, оказывающих преимущественное влияние на психические процессы. Их
используют при лечении психических и невротических заболеваний. По характеру влияния на ЦНС их
делят на ЛВ с преимущественно угнетающим (депремирующим) действием и ЛВ с
преимущественно стимулирующим действием. В 1 группу входят нейролептики, транквилизаторы,
седативные средства, соли лития, во 2-ю -психостимуляторы, ноотропные средства, аналептики,
общетонизирующие (адаптогены) и дислептики (галлюциногены). Промежуточное положение
занимают антидепрессанты. В этой лекции будут рассмотрены нейролептики, транквилизаторы,
седативные, соли лития и антидепрессанты.
Необходимо изучить следующие вопросы:
* - сущность нейролептического эффекта, МД и основные эффекты нейролептиков;
* - классификация нейролептиков по химической структуре;
* - основные и ПЭ препаратов фенотиазинового ряда, их особенности и применение;
* - производные бутирофенона (галоперидол, дроперидол), особенности их действия и применения;
* - характеристика нейролептического эффекта клозапина и резерпина;
* - соли лития, особенности их действия и применения;
* - сущность транквилизирующего эффекта, классификация транквилизаторов;
* - МД и основные эффекты различных групп транквилизаторов;
*- характеристика седативных средств и их применение;
* - сущность антидепрессивного действия, классификация антиделрессантов;
* - МД, основные и ПЭ различных антидепрессантов, особенности их применения.
Нейролептические средства.
Это ЛВ, для которых основным является антипсихотическое и седативное (успокаивающее)
действие. Антипсихотическое действие проявляется устранением бреда и галлюцинаций, замедлением
развития психических заболеваний, а седативное - ослаблением возбуждения, тревоги, страха, агрессии,
двигательной активности.
МД нейролептиков связывают с угнетением дофаминовых рецепторов лимбической системы.
Установлено, что нейролептики блокируют дофаминовые Д2-рецепторы, поэтому являются
антагонистами как самого дофамина, так и средств, возбуждающих дофаминовые рецепторы. Считают,
что антидофаминовый эффект лежит в основе антипсихотического действия. Седативное действие
связано с блокадой адренорецепторов активирующей части ретикулярной формации, в результате чего
затрудняется передача импульсов в кору мозга. Имеются данные, что нейролептики угнетают также
выход норадреналина и дофамина через пресинаптические мембраны и их обратный нейрональный
захват.
Угнетая дофаминовые рецепторы лимбической системы, где локализованы центры эмоций,
связанные с вегетативными и эндокринными центрами, нейролептики снижают вегетативный
компонент и эмоциональную окраску психических реакций. В результате исчезает психическое
напряжение, страх, снижается инициатива и интерес к окружающему до полного безразличия,
устраняеттся психомоторное возбуждение и агрессивность, облегчается контакт с больными. Высшая
нервная деятельность при этом существенно не страдает, но способность к запоминанию ослабевает.
В МД нейролептиков участвует также их влияние на обмен веществ в ЦНС: угнетение аэробного
гликолиза в нейронах, обмена фосфолипидов и белков, трансмембранного переноса метаболитов и т.д.
Нейролептики по химической структуре делят на следующие группы: 1) производные фенотиазина
(аминазин, этаперазин, трифтазин, фторфеназин); 2) производные тиоксантена (хлорпротиксен); 3)
производные бутирофенона (галоперидол, дроперидол); 4) производные дибензодиазепина (клозапин);
5) бензамиды (сульпирид); 6) алкалоиды (резерпин).
Наиболее типичным представителем фенотназиновых производных является аминазин,
проявляющий центральное и периферическое действие. Действие локализуется преимущественно в
лимбико-ретикулярном комплексе, результатом которого является антипсихотический и седативный
эффекты. В больших дозах аминазин оказывает гипнотическое действие в виде поверхностного сна. К
центральным эффектам относят также расслабление мышц, сзязанное с угнетением облегчающего
влияния ретикулярной формации на спинальные рефлексы. Угнетая центр терморегуляции, аминазин
вызывает гипотермию, которая значительно усиливается при одновременном искусственном
охлаждении тела. Этот эффект используют при искусственной гипотермии в хирургии. Аминазин
обладает противорвотным действием, которое проявляется при интоксикациях (азотемия, лучевая
болезнь, токсикозы беременных, при интоксикации противоопухолевыми ЛС и т.д.). Механизм
противорвотного действия связан с угнетением дофаминовых рецепторов пусковой зоны (триггер-зоиы)
рвотного центра. При рвоте, связанной с раздражением вестибулярного аппарата (морская, воздушная
болезнь), а также с раздражением слизистой оболочки пищевого канала, аминазин мало эффективен.
Аминазин потенцирует действие средств для наркоза, снотворных, наркотических,
анальгетиков, усиливая также их угнетающее влияние на дыхательный Центр. Он угнетает
вазомоторный центр. Этот эффект суммируется с периферическим а-адреноблокирующим действием на
уровне сосудистой стенки, что приводит к понижению АД и угнетению вазомоторных рефлексов, в
результате чего возрастает чувствительность организма к кровопотере. Аминазин блокирует Н,гистаминорецепторы и оказывает антигистаминное действие. Этот эффект наиболее выражен у
дипразина. Местно аминазин оказывает раздражающее действие.
Из кишечника аминазин всасывается плохо, метаболизируется в печени, угнетая ее ферменты,
выводится почками и кишечником медленно. При длительном применении седативный и
гипотензивный эффекты постепенно ослабевают, антипсихотический сохраняется. ПЭ:
"нейролептический синдром" (психическая депрессия, паркинсонизм, спазмы мышц), желтуха,
аллергия, раздражение слизистых, ортостатическая гипотензия, угнетение кроветворения.
Этаперазин отличается от аминазина более мощным противорвотным действием (в 5-10 раз).
Трифтазин сильнее аминазина по антипсихотическому и противорвотному действию, но слабее по
седатианому, меньше снижает АД и расслабляет мышцы. Фторфеназин по своим свойствам близок к
трифтазину.
Хлорпротиксен - производное тиоксантена, уступает аминазину по аотипсихотическому эффекту, но
обладает выраженным седативным действием, а также антидепрессивными свойствами.
Галоперидол является основным препаратом группы бутирофенона. Главным его преимуществом
перед аминазмиом является более быстрое и сильное антипсихотическое действие. При парэнтеральном
введении он купирует психическое возбуждение любой природы, включая галлюцинации, МЛ сходен с
аминазином. В больших дозах вызывает полный покой и безразличие к окружающему, подавляет
инициативу и двигательную активность. При этом тонус мышц возрастает в результате блокады
тормозных влияний экстрапирамидной системы на спинальные рефлексы. Препарат оказывает сильное
противорвотное, противосудорожное действие, слабо угнетает вазомоторный центр и периферические
а-АР, поэтому не вызывает снижения АД и ортостатического коллапса. Однако он подавляет
избыточные сосудистые реакции на травму, с которыми связаны необратимые изменения при шоке.
Противошоковое действие, а также способность потенцировать действие средств для наркоза и
наркотических анальгетиков в сочетании с нейролептическим эффектом позволяют использовать эту
группу в нейролептанальгезии. С этой целью обычно применяют смесь дроперидола, обладающего
быстрым, но непродолжительным действием, с анальгетиком фентанилом (таламонал).
Клозапин оказывает значительный антипсихотический эффект и меньше вызывает явления
паркинсонизма при длительном применении. По МД и основным эффектам он сходен с аминазином, но
сильнее действует на м-ХР головного мозга.
Сульпирид (эглонил, догматид) - производное бензамидов, избирательно блокирует дофаминовые
Д2-рецепторы. Обладает выраженным антипсихотическим и противорвотным действием, но слабым
седативным.
Резерпин - алкалоид раувольфии, обладает слабым антипсихотическим действием и применяется при
непереносимости других нейролептиков, а также при сочетании психозов с гипертонической болезнью.
Более подробно рассмотрен в разделе симпатолитиков (лекция 7).
Основной сферой применения неиролептиков является психиатрия. Их также широко используют
при внутренних заболеваниях, в хирургии, при рвоте, икоте, при лечении наркомании и алкоголизма.
Их не следует назначать при болезнях печени, при сердечной недостаточности, нарушениях
кроветворения, органических поражениях ЦНС.
Средства для лечения маниакальных состояний.
При маниакальных состояниях используют 2 группы ЛС: 1) нейролептики; 2) соли лития. Более
специфическим действием обладают соли лития, которые устраняют мании, не вызывая общей
заторможенности и депрессии. Их лечебный эффект проявляется только при маниях. МД изучен
недостаточно. Возможно, он связан с уменьшением содержания НА в адренергических синапсах ЦНС.
Лития карбонат хорошо всасывается в кишечнике, в тканях распределяется равномерно, но через ГЭБ
проникает медленно, поэтому антиманиакальное действие развивается постепенно (в течение 2-3
недель). Выделяется почками, но 80% подвергается обратному всасыванию и концентрация в крови
снижается медленно, поэтому может кумулировать. Кумуляция усиливается при снижении натрия в
организме (напр., при лечении диуретиками, ограничении соли в пищевом рационе). Часть лития
карбоната выделяется с молоком и может вызвать отравление грудного младенца. Препараты лития
токсичны, имеют малую широту терапевтического действия. ПЭ: диспепсия, слабость, тремор,
полиурия, жажда. Противопоказаны при заболеваниях почек, печени, щитовидной железы, желудка.
При интоксикации для ускорения выведения из организма назначают осмотические диуретики
(маннитол, мочевина), натрия гидрокарбонат, гемодиализ, гемосорбцию.
Транквилизаторы.
К ним относятся ЛВ, оказывающие успокаивающее действие на психику, устраняющие чувство
страха, тревоги, напряжения, беспокойства. Их используют преимущественно при неврозах и
неврозоподобных состояниях. В отличие от неиролептиков они мало эффективны при психозах, не
вызывают паркинсонизма, не влияют на вегетативную иннервацию (за исключением центральных
холинолитиков), не нарушают работоспособность и даже могут ее повысить за счет снятия чувства
тревоги и беспокойства. Поэтому их широко используют не только больные, но и практически здоровые
люди. Они обладают миорелаксирующим действием и повышают порог судорог.
По химической структуре транквилизаторы подразделяют на 4 группы: 1) производные
бензодиазепина (хлозепид, сибазон, феназепам, нозепам, мезапам и др.); 2) производные пропандиола
(мепротан); 3) производные дифенилметана (амизил); 4) разного химического строения (триоксазин,
оксилидин).
Наибольшее применение имеют производные бензодиазепина. МД обусловлен стимуляцией
бензодиазепиновых рецепторов, сопровождающейся возбуждением ГАМК-рецепторов. Так как ГАМК
является тормозным медиатором ЦНС, усиление ее влияний приводит к седативному эффекту.
Действие локализуется в лимбической системе, ответственной за формирование эмоций. Препараты
этой группы назначают в тех случаях, когда необходимо снять эмоциональное напряжение, страх,
беспокойство, напряжение мышц при подготовке к оперативным вмешательствам, при нарушениях
функций внутренних органов, при климактерических расстройствах, для профилактики
психоэмоционального стресса и т.п. Миорелаксирующий эффект связывают с угнетением спинальных
рефлексов и облегачающих влияний по нисходящим нервным путям. Поэтому транквилизаторы относят
к миорелаксантам центрального действия в отличие от курареподобных ЛС, относящихся к
периферическим миорелаксантам. Этот эффект используют для усиления миорелаксации во время
наркоза и при лечении судорог. Они потенцируют действие наркотических, снотворных средств,
алкоголя, анальгетиков и других веществ, угнетающих ЦНС. На вегетативную систему не действуют и
не влияют на дыхание и кровообращение.
Производные бензодиазепина отличаются друг от друга по силе и продолжительности действия.
Наиболее сильным и длительным действием обладает феназепам. Для мезапама и сибазона характерно
минимальное гипнотическое действие (способствовать наступлению сна). Этот эффект наиболее
выражен у нитразепама.
Биотрансформация препаратов происходит в печени, экскреция - почками. ПЭ возникают редко, в
основном, при длительном бесконтрольном применении (сонливость, вялость, головная боль, снижение
половой активности, нарушение менструального цикла, аллергия). Возможно развитие привыкания и
лекарственной зависимости (физической и психической).
Мепротан по своим свойствам близок к бензодиазепинам. Наряду с антиневротическим действием
вызывает расслабление мышц и противосудорожное действие. Потенцирует действие средств для
наркоза, снотворных, алкоголя, наркотических анальгетиков. Быстро всасывается в кишечнике и
действует через 20-30 мин, легко проникает через плаценту, поэтому во время беременности его
следует назначать осторожно. Область применения и ПЭ мепротана аналогичны бензодиазепиновым
препаратам.
Амизил - м-холиноблокатор центрального действия, по своему действию и применению сходен с
другими транквилизаторами, но обладает выраженным влиянием на парасимпатическую систему:
расслабляет гладкие мышцы, угнетает секрецию желез, расширяет зрачок, вызывает тахикардию. Эти
эффекты значительно слабее, чем у атропина. Амизил обладает также антигистаминным,
антисеротониновым и местноанестезирующим действием. ПЭ связаны с его м-холиноблокирующими
свойствами.
Буспирон - препарат нового поколения, обладающий более избирательным транквилизирующим
эффектом. В отличие от производных бензодиазепина он не оказывает седативно-гипнотического,
миорелаксирующего и противосудорожного действия. По силе действия примерно равен сибазону, но
его эффект развивается медленно (1-2 нед.). ПЭ вызывает редко (головокружение, головная боль,
парестезии, диспептические расстройства).
Седативные средства.
Обладают менее выраженным успокаивающим действием по сравнению с транквилизаторами, не
устраняют чувство страха, не оказывают потенцирующего и миорелаксирующего действия. К ним
относятся препараты брома, валерианы, пустырника.
Препараты брома применяют в виде натрия бромида и калия бромида. Они хорошо всасываются в
кишечнике и равномерно накапливаются в разных отделах ЦНС. Действие брома на ЦНС изучено в
лаборатории И. П. Павлова. Установлено, что бром усиливает процессы внутреннего торможения и
способствует их концентрации, нормализуя соотношение между процессами возбуждения и
торможения. Успокаивающий эффект зависит от типа нервной системы и ее функционального
состояния: при слабом типе действие брома усиливается, поэтому дозы надо снижать, а при сильном
типе - наоборот. Поэтому препараты брома надо дозировать строго индивидуально. Бром выделяется из
организма медленно (50-60 сут.), поэтому может кумулировать и вызывать явления бромизма (вялость,
заторможенность, сонливость, ослабление памяти, половой потенции, высыпания на коже в виде угрей,
насморк, кашель и т.п.). Для ускорения выведения брома из организма назначают натрия хлорид.
Аналогичным действием обладают препараты валерианы, травы пустырника, содержащие
эфирные масла, алкалоиды, дубильные вещества. Их применяют в виде настоек, экстрактов, настоев.
Антидепрессанты.
Это ЛВ, устраняющие симптомы эмоционального торможения и психической депрессии. По
действию на ЦНС они занимают промежуточное положение между депремирующими и
стимулирующими ЛС. Их используют, главный образом, при психических заболеваниях,
сопровождающихся депрессией (тоска, подавленное настроение, чувство безнадежности и
безысходности, наклонность к суицидальным поступкам, отсутствие инициативы, желания трудиться и
т.п.). По типу действия их делят на тимолептики и тимоэректики, а по МД - на ЛВ, потенцирующие
действие моноаминов, и ЛВ, ингибирующие моноаминоксидазу (МАО).
Тимолептики - это ЛС, устраняющие депрессию у психически больных. По структуре делятся на
трициклические и четырехциклические соединения. К первым относятся имизин, амитриптилин,
азафен, ко вторым - пиразидол. Считает, что МД этих ЛВ состоит в усилении адренергических и
серотонинергических влияний, связанных с накоплением в синапсах НА и серотонина в результате
угнетения обратного нейронального захвата. Усиление адренергических влияний приводит к
повышению тонуса активирующей части ретикулярной формации на кору мозга, а накопление
серотонина - к снижению возбудимости центров отрицательных эмоций в лимбической системе. Они
оказывают также м-холиноблокирующее, антигистаминное и спазмолитическое действие. Имизин
наряду с антидепрессивным действием оказывает психостимулирующий эффект, сопровождающийся
бессоницей, эйфорией, возбуждением. Седативный эффект выражен слабо. Амитриптилин
психостимулирующим действием не обладает, но психоседативный эффект у него сильнее, чем у
имизина, и более выражено м-холинолитическое и антигистаминное действие. Лечебный эффект этих
ЛС проявляется через 10-14 дней. ПЭ: сухость во рту, нарушение аккомодации зрения, повышение
внутриглазного давления, тахикардия, запор, снижение диуреза. АД, ортостатическая гипотензия и др.
Азафен слабее по антидепрессивному эффекту, но оказывает выраженное седативное действие, не
обладает м-холинолитическими свойствами, дает меньше ПЭ и хорошо переносится. Его назначают, в
основном, лицам пожилого возраста. Указанные препараты нельзя комбинировать с ингибиторами
МАО, так как при этом возникает интоксикация. Они противопоказаны при заболеваниях печени,
почек, кроветворных органов, при глаукоме, тиреотоксикозе, сахарном диабете, гипертрофии
предстательной железы, в первые 3 мес. беременности.
Пиразидол по МД сходен с имизином. Обладает антидепрессивным и седативным действием, мхолиноблокирующих свойств не имеет,переносится хорошо, ПЭ возникают редко.
Тимоэректики - ЛВ, устраняющие психическую депрессию и улучшающие настроение не только у
больных, но и у здоровых лиц. МД связан с угнетением МАО, фермента, разрушающего биогенные
амины (НА, адреналин, дофамин, серотонин). Это приводит к накоплению в ЦНС моноаминов и
усилению
синаптической
передачи
импульсов.
Они
обладают
антидепрессивным
и
психостимулирующим действием, являются антагонистами резерпина, усиливают прессорное действие
симпатомиметиков (эфедрин, фенамин) и тирамина, который содержится в некоторых пищевых
продуктах (сыр, пиво, икра и др.). Поэтому их нельзя назначать вместе с указанными веществами.
Из этой группы используют преимущественно ниаламид, обладающий относительно слабым
антидепрессивным эффектом, но наименее токсичный. ПЭ: возбуждение ЦНС (бессоница, тремор,
судороги), гепатиты, ортостатическая гипотензия. Из группы ингибиторов МАО наиболее сильным
антидепрессивным эффектом обладает трансамин, который по структуре и действию сходен с
фенамином. Он вызывает много ПЭ, в том числе - гипертонию. Все ингибиторы МАО противопоказаны
при болезнях печени, почек, при нарушениях мозгового кровообращения, психическом возбуждении.
Лекция 14.
СТИМУЛЯТОРЫ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ.
К этой группе ЛС относятся психостимуляторы, ноотропные, общетонизирующие, аналептики,
психодислептики.
В лекции будут проанализированы следующие вопросы:
* - сущность психостимулирующего действия, классификация психостимуляторов;
* - МД, основные и ПЭ фенамина, пиридрола, меридила и сиднокарба;
* - МД, фармакокинетика, фармакодинамика и применение кофеина;
* - МД и фармакологические эффекты ноотропных ЛС, их применение;
* - характеристика общетоннзирующих средств и их применение;
* - психодислептики, их фармакологическое и токсикологическое значение.
Психостимуляторы.
К ним относятся ЛВ, устраняющие или ослабляющие утомление, сонливость, повышающие
умственную и физическую работоспособность. Однако увеличение работоспособности при их
применении достигается за счет более быстрого и полного использования энергетических резервов
организма, что может привести к их истощению. Это сопровождается развитием бессоницы,
раздражительности и упадком сил. Поэтому при назначении психостимуляторов необходимо
предусмотреть полноценный отдых.
По химическому строению психостимуляторы подразделяют на следующие группы: 1)
фенилалкиламины (фенамин); 2) производные пиперидина (пиридрол, меридил); 3) производные
сиднонимина (сиднокарб, сиднофен); 4) метилксантины (кофеин).
Фенамин по структуре близок адреналину, но лишен гидроксильных групп, благодаря чему более
стоек и хорошо проникает через ГЭБ. Поэтому обладает сильным центральным и более слабым
периферическим действием, МД фенамина связан с увеличением высвобождения НА и дофамина из
симпатических окончаний и из депо в тканях, а также с затруднением их обратного захвата. Благодаря
этому усиливается передача импульсов преимущественно в активирующей части ретикулярной
формации, а также в лимбической системе и коре. Следовательно, фенамин действует противоположно
нейролептикам. Стимулируя центр насыщения, он подавляет чувство голода и снижает аппетит.
Фенамин повышает обмен веществ, возбуждает центры продолговатого мозга и усиливает дыхание и
кровообращение. Сосудосуживающий эффект и повышение АД обусловлены стимуляцией
вазомоторного центра и симпатомиметическим эффектом в стенках сосудов. Однако по прессорному
эффекту он уступает адреналину в 100 раз, превосходя его по продолжительности действия.
Недостатками фенамина являются кумулятивные свойства, развитие пристрастия, извращенные
реакции на него у некоторых людей (угнетение вместо стимуляции) и развитие гипертензии. Из-за
способности вызывать пристрастие он отнесен к группе наркотиков и его применение строго
ограничено.
Пиридрол и перидил по действию близки фенамину, но не вызывают периферических
симпатомиметических эффектов, поэтому существенно не влияют на ССС. Опасность развития
лекарственной зависимости при их применении выражена слабее.
Сиднокарб и сиднофен - активные психостимуляторы с постепенным и длительным действием. На
ССС не влияют, так как не обладают периферическим симпатомиметическим эффектом. ПЭ возникают
редко.
Кофеин - алкалоид, содержащийся в листьях чая, зернах кофе, плодах какао, орехах кола, которые с
древнейших времен используются для приготовления возбуждающих напитков. По структуре близок к
некоторым продуктам пуринового обмена - мочевой кислоте, ксантину и др. Этим объясняют
незначительную токсичность по сравнению с другими алкалоидами и большую широту
терапевтического действия кофеина. К метилксантинам относятся также теобромин и теофиллин,
обладающие слабым возбуждающим действием на ЦНС. Кофеин хорошо всасывается в кишечнике и
равномерно распределяется в организме. Действие развивается через 15-30 мин. Большая часть кофеина
быстро разрушается и выводится через почки в виде метаболитов, около 10% - в неизмененном виде.
Существуют две гипотезы о МД кофеина. Согласно первой гипотезе, действие кофеина обусловлено
угнетением фосфодиэстеразы - фермента, катализирующего превращение циклического
аденозинмонофосфата (цАМФ) в АМФ. Это приводит к увеличению содержания цАМФ в клетках, в
результате чего возрастает активность фосфорилазы - фермента, усиливающего процессы
гликогенолиза, потребление кислорода и образование энергии. Однако против этой гипотезы есть
существенное возражение. Дело в том, что угнетающее действие кофеина на фосфодиэстеразу
проявляется в концентрациях, которые при применении терапевтических доз кофеина в организме не
создаются. Согласно второй гипотезе, МД кофеина связан с блокадой рецепторов, медиатором которых
является аденозин. Установлено, что кофеин вызывает эффекты, противоположные эффектам аденозина
по отношению к ЦНС, ССС, диурезу, гликогенолизу, липолизу, высвобождению гистамина,
катехоламинов. Таким образом, кофеин и аденозин действуют как конкурентные антагонисты, причем
антагонизм проявляется при применении терапевтических доз кофеина.
Стимулирующее действие кофеина на ЦНС проявляется в определенной последовательности: кора,
продолговатый мозг, спинной мозг. Существенного влияния на ретикулярную формацию не оказывает.
Его действие направлено непосредственно на нейроны коры, тогда как другие психостимуляторы
действуют на кору опосредованно через стволовую часть мозга. Исследованиями школы И. П. Павлова
доказано, что кофеин усиливает процессы возбуждения в коре мозга, ослабляя процессы торможения
и, следовательно, действует противоположно брому. Действие кофеина зависит от дозы и типа нервной
системы. Поэтому одна и та же доза у разных людей может вызвать разную реакцию. При слабом типе
нервной системы дозу кофеина надо уменьшать, а при сильном - увеличивать. В основе действия
кофеина на ЦНС лежит его способность облегчать передачу возбуждения в межнейронных синапсах и
повышать суммацию подпороговых импульсов, в результате чего возрастает возбудимость нейронов и
ускоряется рефлекторный ответ. Кофеин, как и напитки, его содержащие (чай, кофе), стимулируют
психическую Деятельность, устраняют сонливость, вызывают ощущение бодрости, повышают
умственную работоспособность. Кофеин является антагонистом средств для наркоза, снотворных,
алкоголя, наркотических анальгетиков и используется при их передозировке.
Кофеин возбуждает центры продолговатого мозга, особенно при парэнтеральном введении
относительно больших доз. Следовательно, наряду с психостимулирующим действием он обладает
свойствами аналептика, стимулируя дыхание и кровообращение на фоне их угнетения. Возбуждая
центр вагуса, кофеин вызывает брадикардию, но у некоторых людей учащает сокращения сердца за счет
прямого кардиотонического эффекта. Кофеин также стимулирует нейроны спинного мозга, усиливая
двигательные рефлексы и мышечный тонус. Этот эффект проявляется при применении относительно
высоких доз.
Под влиянием кофеина улучшается кровообращение в результате повышения тонуса вазомоторного
центра и прямого действия на сердце и сосуды. Работа сердца и просвет сосудов при применении
кофеина зависят от соотношения центральных и периферических эффектов. Сосуды различных
областей реагируют на кофеин по разному: сосуды сердца, почек и скелетных мышц расширяются,
сосуды органов брюшной полости, подкожной клетчатки, селезенки суживаются. Повышается тонус
сосудов мозга, что способствует венозному оттоку крови, снижению внутричерепного давления и
набухания - мозговых оболочек. Этот эффект используют при лечении головной боли, мигрени. На
фоне сниженного АД кофеин его повышает, а на нормальное АД не действует. За счет указанных
эффектов кофеин улучшает кровоснабжение жизненно важных органов, что имеет большое значение
при оказании неотложной помощи.
На почки кофеин оказывает непостоянное действие. В большинстве случаев увеличивает диурез за
счет усиления клубочковой фильтрации и угнетения реабсорбции в канальцах. Под влиянием кофеина
повышается тонус мышц и физическая работоспособность. Этот эффект обусловлен как стимуляцией
ЦНС, так и усилением окислительных процессов, о чем свидетельствует увеличение основного обмена.
Кофеин увеличивает секрецию желудочного и кишечного сока.
Кофеин назначают для улучшения умственной и физической работоспособности, как аналептик при
отравлении ядами, угнетающими ЦНС, при гипотонии, головной боли. Он противопоказан при
повышенной возбудимости, бессоннице, гипертонической болезни, атеросклерозе, органических
заболеваниях сердца, при глаукоме.
Острое отравление кофеином характеризуется сильным двигательным возбуждением,
спутанностью сознания, головокружением, сердцебиением, болями в сердце, аритмией. Лечение:
снотворные, наркозные средства. Хроническое отравление обычно связано со злоупотреблением чаем
или кофе. Оно проявляется повышенной возбудимостью, бессонницей, тахикардией, болями в сердце,
нарушениями сердечного ритма, тремором рук. Лечение состоит в отмене этих напитков и назначении
валерианы, брома, снотворных.
Ноотропные средства.
Это ЛВ, улучшающие умственную деятельность и память. Эффект проявляется только при
органических заболеваниях головного мозга. Он связан с улучшением энергетических процессов в
мозговой ткани, поэтому проявляется при длительном курсовом лечении. При этом уменьшаются
явления гипоксии мозга и снижается наклонность к судорогам.
Ноотропные ЛС являются препаратами ГАМК или ее производными. Они воспроизводят
метаболические эффекты ГАМК, которая служит тормозным медиатором ЦНС и регулирует обмен
веществ, стимулируя тканевое дыхание. Аминалон - препарат ГАМК, полученный синтетическим путем.
Он плохо проникает через ГЭБ, но при заболеваниях мозга проникновение улучшается. Аминалон
увеличивает кровоснабжение мозга, уменьшает гипоксию, оказывает противосудорожное действие,
умеренно снижает повышенное АД, нормализует содержание сахара в крови. Пирацетам (ноотропил) -
циклическое производное ГАМК. Он вызывает те же эффекты, что и аминалон. Преимуществом
пирацетама является хорошее проникновение через ГЭ6. Пикамилон -отечественный препарат,
являющийся производным ГАМК и никотиновой кислоты. Сочетание ноотропного действия ГАМК с
влиянием никотиновой кислоты на обмен веществ и сосуды обеспечивает благоприятное действие при
различных органических и функциональных нарушениях мозга и системы его кровоснабжения. Он
улучшает тканевое дыхание, уменьшает гипоксию, увеличивает мозговой кровоток, повышает
устойчивость мозговой ткани к различным неблагоприятным воздействиям.
Ноотропные ЛС применяют при умственной недостаточности, связанной с нарушением мозгового
кровообращения, при алкогольном слабоумии, при отставании умственного развития детей, в
старческом возрасте, при травмах черепа. ПЭ возникают редко.
Общетонизирующие средства.
К этой группе относятся ЛС преимущественно растительного происхождения, издавна применяемые
в народной медицине. Лечебный эффект проявляется только при длительном применении. Препараты
характеризуются низкой токсичностью, большой широтой терапевтического действия, легким
стимулирующим действием без выраженного возбуждения. При их применении улучшаются
самочувствие, аппетит, работоспособность, возрастает мышечная сила, масса тела, усиливается
энергетический обмен, нормализуется секреция гормонов коры надпочечников, половых гормонов,
повышается устойчивость организма к действию неблагоприятных факторов. Поэтому эти ЛС называют
адаптогенами. К ним относятся препараты корня женьшеня, плодов лимонника, элеутерококка,
левзеи и др. Общетонизирующим действием обладают стрихнин и секуренин в малых дозах. Но у них
малая широта действия, высокая токсичность, способность кумулировать. При увеличении доз эти ЛС
оказывают выраженное возбуждающее и аналептическое действие и могут вызвать судороги. Их
рассматривают в группе аналептиков.
Психодислептики (галлюциногены).
Занимают особое положение среди психотропных средств. У нормальных людей они вызывают
значительные расстройства психики, сопровождающиеся бредом, галлюцинациями, утратой контроля
над собой. К психодислептикам относятся диэтиламид лизергиновой кислоты (ДЛК-25, ЛСД-25),
псилоцибин, мескалин, марихуана (гашиш, анаша) и др. При приеме ДЛК-25 явления острого психоза
возникают от ничтожных доз (0,04-0,06 мг) и продолжаются 6-8 ч. Иногда психоз приобретает
необратимый характер. Он во многом сходен со спонтанными психозами, поэтому ДЛК-25 используют
для получения экспериментальной модели шизофрении. Мескалин - алкалоид одного из видов кактуса,
псилоцибин - алкалоид некоторых видов грибов, произрастающих в Мексике, марихуану получают из
индийской конопли.
Все указанные средства относятся к группе наркотиков, поэтому на них распространяются
международные законы по борьбе с наркоманией.
Аналептики будут рассмотрены в лекции по средствам, регулирующим функции органов дыхания,
так как их используют преимущественно в качестве стимуляторов дыхания при неотложных
состояниях.
Лекция 15.
СРЕДСТВА, РЕГУЛИРУЮЩИЕ ФУНКЦИИ ОРГАНОВ ДЫХАНИЯ.
В эту группу входят ЛС, используемые для лечения бронхообструктивных заболеваний, для борьбы с
кашлем и облегчения выделения мокроты, для стимуляции дыхания и для лечения отека легких.
Большую группу заболеваний органов дыхания составляют инфекции, но ЛС для их лечения будут
рассмотрены в группе антимикробных средств.
Средства для лечения бронхообструктивных заболеваний.
По этой теме необходимо знать следующие вопросы:
* - механизмы патогенеза бронхиальной обструкции, на которые воздействуют ЛС;
* - классификация ЛС, используемых для леченя бронхообструктивных заболеваний;
* - МД, основные и ПЭ селективных в2-адреномиметиков, изадрина, адреналина и эфедрина:
* - МД, основные и ПЭ м-холиноблокаторов;
* - МД, основные и ПЭ эуфиллина, применение при бронхиальной астме;
*- противоаллергические, десенсибилизирующие и противоспалительные ЛС при лечении
бронхиальной астмы, их МД, основные и ПЭ, показания и противопоказания для назначения;
* - применение отхаркивающих ЛС при бронхиальной астме.
Бронхообструктивные заболевание являются наиболее частой причиной нарушений легочного
газообмена. Независимо от причины этих заболеваний патофизиологической основой обструкции
бронхов служат воспаление и отек слизистой бронхов, спазм бронхиальных мышц и закупорка просвета
бронхов вязким секретом. Лечебные мероприятия должны быть направлены на устранение этих
факторов, которые взаимосвязаны и усиливают друг друга.
Основное значение имеет воспалительный процесс в бронхах, который способствует развитию
бронхоспазма и накоплению вязкого секрета. Бронхоспазм возникает в результате нарушения
нейрогенной и гуморальной регуляции тонуса бронхиальных мышц. К нейрогенным факторам
относятся угнетение в2-АР и активация м-ХР. Гуморальными факторами, провоцирующими
бронхоспазм, являются медиаторы аллергических реакций (гистамин, серотонин, медленно
действующая субстанция анафилаксии и др.), выделяемые тучными клетками, базофилами и
тромбоцитами.
Возбуждение в2-АР сопровождается активацией аденилатциклазы, накоплением цАМФ, который
блокирует кальциевые каналы, уменьшает активность актомиозина и расслабляет гладкие мышцы
бронхов. Поэтому в2-адреномиметики расслабляют мышцы бронхов, а в-адрвноблокаторы
способствуют их спазму. Возбуждение м-ХР приводит к активации гуанилатциклазы и увеличению
синтеза циклического гуанозинмонофосфата (цГМФ), под влиянием которого возрастает поступление
ионов кальция в клетки, что сопровождается активацией актомиозина и повышением тонуса гладких
мышц. Поэтому м-холиноблокаторы препятствуют развитию бронхоспазма, а холиномиметики
способствуют. При увеличении цАМФ снижается выделение гистамина из тучных клеток и базофилов,
угнетается синтез антител, а при увеличении концентрации цГМФ возникают противоположные
эффекты. Таким образом, для устранения бронхоспазма можно использовать в2-адреномиметики и мхолиноблокаторы. Содержание цАМФ можно увеличить также за счет угнетения фосфодиэстеразы,
которая обеспечивает его гидролиз. Таким действием обладают эуфиллин и теофиллин. Спазм
бронхов можно устранить антагонистами кальция, которые уменьшают вход кальция в клетки,
простагландинами группы Е, повышающими содержание цАМФ и снижающими высвобождение
факторов анафилаксии. Большое значение имеют противоспалительные, противоаллергические и
десенсибилизирующие ЛС. Их лечебное действие обусловлено угнетением синтеза и выделения
факторов аллергии и восстановлением функции в2-АР (глюкокортикоиды, кромолин-натрий и
кетотифен). Для удаления вязкого воспалительного секрета из бронхов используют отхаркивающие ЛС.
Классификация ЛС для лечения бронхообструктивных заболевании включает следующие
препараты: 1) бронхорасщиряющие (бронхолитические) ЛС - а) в2-адреномиметики (салбутамол,
фенотерол, тербуталин, орцилреналин, изадрин, адреналин, эфедрин); 6) м-холиноблокаторы
(ипратропия бромид, атропин, платифиллин); в) миотропные средства (эуфиллин, теофиллин); 2)
противоспалительные, антиаллергические и десенсибилизирующие средства (глюкокортикоиды,
кромолин-натрий, кетотифен); 3} отхаркивающие (мокротолитические) средства. Если астма имеет
инфекционно-аллергическое происхождение, используют также противомикробные ЛС.
Бронхолитики.
Основными ЛС для купирования приступа бронхиальной астмы являются селективные в2адреномиметики (салбутамол, тербуталин, фенотерол, спиропент, орципреналин), Они избирательно
стимулируют в2-АР гладких мышц и тучных клеток, что сопровождается активацией аденилатциклазы
и накоплением цАМФ, который препятствует открытию кальциевых каналов в мембранах и связывает
ионы кальция в клетках. Это сопровождается снижением активности актомиозина и расслаблением
бронхиальных мышц, а также торможением выхода медиаторов аллергии из тучных клеток. Они не
оказывают выраженного действия на сердце и сосуды, поэтому ПЭ (тахикардия, повышение АД)
возникают редко. Эти ЛВ не разрушаются КОМТ, поэтому действуют длительно (4-6 ч) и могут
назначаться ингаляционно, внутрь и в инъекциях. Основной путь введения ингаляционный с. помощью
дозирующих ингаляторов. Препарат поступает непосредственно в бронхи, что позволяет создавать
достаточные концентрации в бронхах небольшими дозами и снижать ПЭ. Действие развивается быстро.
Если контакт аэрозоля со слизистой бронхов затруднен из-за скопления слизи или резкого затруднения
дыхания, предпочтение отдают энтеральному и инъекционному путям введения. ПЭ чаще всего
возникают при бесконтрольном использовании и передозировке препаратов. Наиболее серьезным
осложнением является развитие рефрактерности в2-АР, в результате чего бронхолитический эффект
исчезает, а расширение сосудов бронхов приводит к увеличению экссудации и отека слизистой. В таких
случаях возрастает опасность формирования астматического статуса. Признаком рефрактерности в2-АР
является отсутствие эффекта адреномиметиков в течение 4 ч. и более.
Изадрин стимулирует как в2-АР, так и в1-АР, поэтому обладает выраженным кардиотропным
действием. В настоящее время его используют редко из-за частых ПЭ (тахикардия, аритмия, ишемия
миокарда и боли в сердце).
Адреналин стимулирует все а- и в-АР, поэтому обладает широким спектром действия. Наряду с
бронхолитическим эффектом он суживает сосуды (за исключением сосудов скелетных мышц и сердца),
повышает АД, усиливает работу сердца, повышает сахар крови. Эти эффекты при лечении
бронхиальной астмы нежелательны. Однако бронхолитический эффект возникает от дозы, которая мало
влияет на сердце и сосуды, поэтому при правильном применении адреналина ПЭ можно свести до
минимума. Назначают в/м, так как из подкожной клетчатки всасывание адреналина замедленно из-за
спазма сосудов в результате возбуждения а-АР. Эффект возникает через 3-5 мин и сохраняется 30-40
мин. Адреналин противопоказан при заболеваниях сердца и сосудов, аритмиях, гипертонии, сахарном
диабете, тиреотоксикозе, а также при рефрактерности в2-АР.
Эфедрина гидрохлорид - непрямой а-в-адреномиметик (симпатомиметик). По силе действия
значительно уступает адреналину, но превосходит его по продолжительности эффекта. Не разрушается
в пищевом канале, легко всасывается, поэтому назначается внутрь и парэнтерально. При приеме внутрь
эффект развивается через 30-40 мин, при в/м введении - через 15 мин, продолжительность действия - 46 ч. Назначают при нетяжелых приступах. Противопоказан в тех же случаях, что и адреналин. При его
применении возможны возбуждение ЦНС и бессоница. В последние годы его используют мало.
М-холиноблокаторы. Механизм бронхолитического действия связан с блокадой м-ХР гладких мышц
и тучных клеток, благодаря чему устраняется действие на них АЦХ. Это приводит к расслаблению
мышц бронхов, угнетению дегрануляции тучных клеток и повышению устойчивости к факторам
ананафилаксии. Угнетается также секреция бронхиальных желез.
Основной препарат этой группы - ипратропия бромид (атровент). Помимо блокады м-ХР он
тормозит выделение тромбоксана А2 из тромбоцицитов, который считают мощным спазмогеном.
Препарат плохо проникает через мембраны, поэтому оказывает незначительное резорбтивное действие.
Его применяют ингаляционно в виде аэрозоля. Эффект возникает через 20-30 мин, достигает максимума
через 1,5-2 ч. и сохраняется 4-8 ч. По активности уступает в2-адреномиметикам, но привыкание к нему
развивается значительно медленнее. ПЭ: иногда чувство першения в горле и умеренная сухость во рту.
Атропин обладает слабым бронхолитическим эффектом и действует преимущественно а тех случаях,
когда бронхоспазм связан с повышенной чувствительностью гладких мышц к холинергическим
влияниям (напр., после гриппа, при хронических бронхитах и т.п.). В детской практике атропин и
синтетитические м-холиноблокаторы не применяют. Они обладают широким спектром действия,
поэтому вызывают много ПЭ (сухость во рту, нарушение выделения мокроты, тахикардия и др.).
Платифиллин вызывает меньше ПЭ, но бронхолитическое действие у него выражено недостаточно.
Миотропные бронхолитики (эуфиллин, теофиллин). МД эуфиллина сложный. Он угнетает
фосфодиэстеразу, что приводит к накоплению цАМФ, ослабляет бронхоспастическое действие ПГ F2а,
стимулирует освобождение адреналина из надпочечников и НА из симпатических окончаний.
Увеличение содержания НА и адреналина связывают с блокадой аденозиновых рецепторов, стимуляция
которых тормозит выделение катехоламинов. Эуфиллин оказывает также стабилизирующее действие на
мембраны тучных клеток и уменьшает выделение факторов анафилаксии. Помимо бронхолитического
эффекта эуфиллин улучшает вентиляцию легких за счет усиления сокращений диафрагмы и
межреберных мышц, расширяет сосуды легких, почек, сердца, скелетных мышц и уменьшает
гемодинамическую нагрузку на сердце. Непосредственно на сердце оказывает кардиотоническое
действие и увеличивает потребление кислорода.
Эуфиллин при приеме внутрь всасывается хорошо (90%). Для быстрого эффекта вводят в/в. При в/м
введении всасывается медленно и оказывает раздражающее действие. В крови 50-60% связывается с
белками, в тканях распределяется равномерно. Терапевтическая концентрация в крови достигается при
приеме внутрь через 1-2 ч.и сохраняется до 6 ч. Метаболизм осуществляется в печени, замедляется при
гипоксии, лихорадке, сердечной и печеночной недостаточности, а также в ночное время. 3 этих случаях
дозу эуфиллина необходимо уменьшать. Выводится почками в виде метаболитов (90%) и в
неизмененном виде (10%). ПЭ: раздражение ЖКТ и диспептические расстройства, возбуждение ЦНС
(беспокойство, бессоница, тремор, при тяжелой интоксикации - судороги, галлюцинации), тахикардия,
аритмия, иногда сердечная недостаточность. Эуфиллин противопоказан при гиперацидных гастритах,
язвенной болезни, органических заболеваниях сердца и коронарных сосудов, атеросклерозе и т.д.
Противоаллергические, десенси6илизирующие и противовоспалительные средства включают: 1)
ЛС, тормозящие высвобождение тучными клетками медиаторов анафилаксии (кромолин-натрий,
кетотифен); 2) глюкокортикоиды (бекламетазон, преднизолон, дексаметазон, триамцинолон).
Кромолин-натрий (интал) угнетает фосфодиэстеразу, что сопровождается накоплением цАМФ и
снижением проницаемости мембран тучных клеток. Лечебный эффект максимально проявляется при
аллергической (атопической) бронхиальной астме, менее выражен при рефлекторной астме и почти не
проявляется при инфекционно-аллергической. Препарат действует только профилактически и не
купирует возникший приступ. Поэтому его назначают для профилактики приступов в межприступном
периоде. Он более эффективен у детей и может действовать при гормонозависимой астме. В кишечнике
не всасывается, поэтому назначается только ингаляционно. Продолжительность действия - 4-6 ч. Не
токсичен, не вызывает привыкания и зависимости. ПЭ (кашель, першение в горле) связаны с
раздражающим действием и их легко устранить, запивая ингаляции теплой водой. Отмену препарата
надо производить постепенно, уменьшая число ингаляций в течение 10-14 дней.
Кетотифен (задитен) тормозит высвобождение из тучных клеток гистамина и других факторов
анафилаксии, угнетая фосфодиэстеразу и блокируя кальциевые каналы. Он предупреждает
бронхоспазм, вызванный аллергенами и неспецифическими провоцирующими факторами. Кетотифен
хорошо всасывается в кишечнике и действует 12 ч. Биотрансформация происходит в печени путем
деметилирования и образования конъюгатов с глюкуроновой кислотой. Выделяется с мочой в виде
активных метаболитов. Нетоксичен, но в первые дни приема может вызывать сонливость, связанную с
антигистаминным действием. Назначают длительно.
Глюкокортикоиды оказывают влияние на все звенья патогенеза бронхиальной обструкции. Они
незаменимы при тяжелой бронхиальной астме, которая приобрела гормонозависимый характер, и при
астматическом состоянии. МД связывают со стабилизацией мембран тучных клеток и их гранул,
торможением синтеза и высвобождения медиаторов воспаления (простагландины, лейкотриены,
кинины, протеазы и др.), медиаторов анафилаксии, антител, с увеличением синтеза цАМФ и угнетением
цГМФ, с повышением чувствительности в2-АР, а также с прямым действием на гладкие мышцы
бронхов.
В крови глюкокортикоиды находятся в свободном и связанном состоянии, инактивируются в печени
путем конъюгации с глюкуроновой и серной кислотами, конъюгаты выделяются почками. Препараты
назначают ингаляционно, внутрь, в/м и в/в. Для ингаляций используют беклометазона дипропионат
(Бекломет, Бекотид), триамцинолона ацетонид, которые через слизистые бронхов всасываются плохо и
оказывают местное действие. Эффект развивается постепенно, поэтому для купирования приступа их не
применяют. При длительном применении могут вызвать кандидоз полости рта. Внутрь и парэнтерально
назначают првднизолон, дексаметазон, триамцинолон и гидрокортизон. Их используют а тех
случаях, когда ингаляционные препараты недостаточно эффективны, а также при развитии
астматического состояния. ПЭ при коротких курсах лечения обычно не возникают, а при длительном
применении могут возникать разнообразные нарушения обмена веществ, функций ЦНС, эндокринных
желез, ЖКТ, ССС, опорно-двигательиого аппарата и т.д.
Комбинированные препараты (теофедрин, солутан, антасман, беродуал, дитэк и др.) испольауют для
купирования и профилактики приступов. Принцип комбинирования основан на синергидном
взаимодействии ЛС с разным МД. Помимо патентованных ЛС можно использовать следующие
комбинации: 1) эуфиллин с адреналином, 2) эуфиллин с в2-адреномиметиками, 3) адреномиметики с
ипратропия бромидом, 4) в2-адреномиметики с беклометазоном, 5) эуфиллин с преднизолоном (при
астматическом статусе).
Отхаркивающие ЛС имеют важное значение в лечении бронхиальной астмы. Во время приступа
происходит накопление вязкого секрета в бронхах, связанное с гиперсекрецией бронхиальных желез и
угнетением моторной функции бронхиол и мерцательного эпителия. Для улучшения выделения
мокроты преимущественно используют отхаркивающие средства прямого действия (муколитики): калия
йодид, натрия йодид, натрия гидрокарбонат, ацетилцистеин (мукалтин), бромгексин и др. Более
подробно об этих ЛС будет сказано в следующей лекции.
Лекция 16.
СРЕДСТВА, РЕГУЛИРУЮЩИЕ ФУНКЦИИ ОРГАНОВ ДЫХАНИЯ (продолжение).
В этой лекции будут изложены основные сведения о ЛС, используемых при кашле, отеке легких и
угнетении дыхания. Необходимо знать следующие вопросы:
* - применение противокашлевых и отхаркивающих ЛС;
*- МД, основные и ПЭ противокашлевых ЛС;
* - классификация отхаркивающих ЛС, их МД и применение;
* - классификация стимуляторов дыхания, их МД, основные и ПЭ;
* - принципы терапии отека легких, особенности применения ЛС при разных видах отека легких.
Противокашлевые и отхаркивающие средства.
Самоочищение слизистой оболочки дыхательных путей от инородных частиц происходит за счет
усиления секреции бронхиальных желез, повышения активности мерцательного эпителия и
перистальтики бронхиол. Раздражение кашлевых рефлексогенных зон, особенно в области бифуркации
трахеи, сопровождается кашлем. Кашель - рефлекторный акт, координируемый кашлевым центром,
расположенным в продолговатом мозге. Кашель служит защитной реакцией, способствующей
устранению раздражающего агента из дыхательных путей. Однако при воспалении слизистой секрет
становится вязким за счет накопления белков, мукополисахаридов, лейкоцитов и выделяется с трудом.
Кашель приобретает затяжной характер, истощая силы больного. Приступы кашля сопровождаются
повышением тонуса бронхиальной мускулатуры, растяжением паренхимы легких, снижением легочной
вентиляции, нарушением работы сердца и кровообращения в малом и большом кругах. Для ослабления
кашля применяют ЛС, угнетающие кашель (противокашлевые), и ЛС, улучшающие выделение мокроты
(отхаркивающие).
Противокашлевые ЛС делятся на 2 группы: 1) центрального действия, угнетающие кашлевой
центр (кодеин, этилморфин, глауцин); 2) периферического действия, блокирующие чувствительные
нервные окончания кашлевых рефлексогенных зон (либексии). Применяют их при длительном сухом
кашле, который сопровождает хронические воспалительные процессы дыхательных путей. Кодеин,
кодеина фосфат и этилморфина гидрохлорид относятся к алкалоидам опия (производным
фенантрена), поэтому могут вызвать сходные с морфином ПЭ: угнетение дыхательного центра и
уменьшение легочной вентиляции, а при длительном применении - пристрастие и запоры. Детям до 2
лет противопоказаны. Глауцина гидрохлорид угнетает кашлевой центр более избирательно, не угнетает
дыхание и выделение мокроты, не вызывает лекарственной зависимости, запоров и не противопоказан
детям. Он обладает адренолитическим эффектом, может снижать АД, поэтому при гипотонии не
рекомендуется. Либексин обладает местноанестезирующим и спазмолитическим действием. Его
применяют при катаррах верхних дыхательных путей, бронхитах, бронхиальной астме и других
бронхолегочных заболеваниях. ЛС, угнетающие кашель, обычно комбинируют с отхаркивающими.
Отхаркивающие ЛС по МД делятся на 2 группы: 1) рефлекторного действия; 2) прямого действия. К
ЛС рефлекторного действия, относятся трава термопсиса, корень ипекакуаны, корень алтея,
корень истода, корневище и корень синюхи, трава фиалки трехцветной, ликорин и др.
Отхаркивающий эффект этих ЛС связан с раздражением слизистой желудка, откуда импульсы
поступают в центр вагуса, а из него - к железам и мышцам бронхов, что приводит к усилению секреции,
функции мерцательного эпителия и перистальтики бронхиол. Это сопровождается разжижением
мокроты и ускорением ее выделения, уменьшением раздражения, воспаления и кашля. В больших дозах
они могут вызывать рвоту, которой предшествует длительный период тошноты и раздражение
слизистой желудка, поэтому как рвотные средства их не используют. ЛС рефлектороного действия
назначают преимущественно в виде настоев, отваров, настоек, экстрактов, микстур, некоторые (напр.,
термопсис) в табпетках.
К ЛС прямого действия относятся препараты йода, аммония хлорид, натрия бензоат, натрия
гидрокарбонат, терпингидрат, эфирные масла, содержащиеся в плодах аниса, траве чабреца,
траве душицы, багульника и др., пертуссин, нашатырно-анисовые капли, ацетилцистеин,
бромгексин,
протеолитические
ферменты
(трипсин,
химопсин,
химотрипсин,
дезоксирибонуклеаэа). После всасывания эти ЛВ выделяются бронхиальными железами, стимулируя
секрецию и моторную функцию мерцательного эпителия и бронхиол.
Калия йодид и натрия йодид вызывают разжижение мокроты и оказывают хороший отхаркивающий
эффект. При длительном применении могут вызвать явления йодизма: насморк, слюнотечение,
слезотечение, угревидную сыпь на коже. ПЭ связаны с раздражающим действием йода в местах
выделения. При их появлении препараты йода надо отменить и увеличить количество поваренной соли
в пище. Их назначают при трудноотделяемой вязкой мокроте. Противопоказаны при острых
воспалительных процессах в органах дыхания и при туберкулезе легких. Эфирные масла и щелочи
действуют наиболее благоприятно в виде ингаляций, усиливая секрецию бронхиальных желез, оказывая
бронхолитическое и протнвомикробное действие. Муколитики действуют непосредственно на вязкий
секрет бронхиальных желез, изменяя его физико-химические свойства. Это сопровождается
разжижением мокроты. Ацетилцистеин (мукалтин) расщепляет дисульфидные связи кислых
мукопротеиновых и мукополисахаридных молекул, протеолитические ферменты разрывают пептидные
связи белковых молекул. Их назначают в виде ингаляций, бромгексин - внутрь. Муколитики применяют
при наличии густой, вязкой гнойной мокроты, образующейся при хронических бронхитах, абсцессах,
бронхоэктазах, в основе которых лежит воспаление микробной природы. Поэтому их обычно
комбинируют с противомикробными ЛС, а для лучшего поступления в патологические очаги - с
бронхолитиками. Для улучшения разжижения мокроты вместе с отхаркивающими ЛС рекомендуется
обильное теплое питье.
Стимуляторы дыхания (аналептики).
При угнетении дыхания используют стимуляторы дыхания, возбуждающие дыхательный и
сосудодвигательный центры продолговатого мозга. Так как они восстанавливают жизненно важные
функции (дыхание и кровообращение), их называют аналептиками, что означает оживляющие средства.
Стимуляция центра дыхания приводит к увеличению легочной вентиляции и газообмена,
повышению содержания кислорода и уменьшению углекислоты в крови, к увеличению доставки
кислорода тканям и выведению продуктов метаболизма, к стимуляции окислительновосстановительных процессов и нормализации кислотно-основного состояния. Стимуляция
сосудодвигательного центра вызывает повышение тонуса сосудов, сосудистого сопротивления и АД,
улучшает гемодинамику. Некоторые аналептики (кофеин, камфора, кордиамин) обладают прямым
действием на сердце. Эффекты проявляются, главным образом, на фоне угнетения дыхания и
кровообращения.
Большинство аналептиков в больших дозах могут вызывать судороги. Разница между дозами,
стимулирующими дыхание, и судорожными дозами относительно небольшая. Судороги охватывают
также дыхательную мускулатуру, что сопровождается расстройством дыхания и газообмена,
увеличением нагрузки на сердце и опасностью возникновения аритмий. Резкое увеличение потребности
нейронов в кислороде при недостаточной его доставке приводит к гипоксии и развитию
дегенеративных процессов в ЦНС. Аналептики являются антагонистами средств для наркоза,
снотворных, алкоголя, наркотических анальгетиков и оказывают "пробуждающий" эффект,
который проявляется уменьшением глубины и продолжительности наркоза и сна, восстановлением
рефлексов, мышечного тонуса и сознания. Однако этот эффект выражен лишь при применении больших
доз. Поэтому их следует назначать в дозах, достаточных для восстановления дыхания, кровообращения
и некоторых рефлексов при легкой и средней тяжести угнетения этих функций. Антагонизм между
аналептиками и средствами, угнетающими ЦНС, двухсторонний, поэтому при передозировке
аналептиков и возникновении судорог используют средства для наркоза и снотворные.
МД аналептиков связывают с повышением возбудимости нейронов, улучшением функции
рефлекторного аппарата, сокращением латентного периода и усилением рефлекторных ответов.
Возбуждающий эффект наиболее ярко проявляется на фоне угрожающего жизни угнетения ЦНС.
По направленности действия аналептики делятся на 3 группы: 1) прямого действия на дыхательный
центр (бемегрид, этимизол, кофеин, стрихнин); 2) смешаниого действия (кордиамин, камфора,
углекислота); 3) рефлекторного действия (лобелин, цититон); Обладая общими свойствами, отдельные
препараты отличаются по основному и побочному действию. Выбор ЛС зависит от причины,
вызвавшей угнетение дыхания, и характера нарушений.
Бемегрид применяют, главным образом, при отравлении барбитуратами и средствами для наркоза,
для быстрого выведения из наркоза, а также при угнетении дыхания и кровообращения, вызванном
другими причинами. ЕГО ВВОДЯТ в/в медленно по 5-10 мл 0,5% р-ра каждые 3-5 мин. до восстановления
дыхания, кровообращения и рефлексов. При появлении судорожных подергиваний мышц введение надо
прекратить.
Этимизол занимает особое положение, так как наряду с возбуждением центров продолговатого
мозга оказывает угнетающее действие на кору мозга. Поэтому он не дает "пробуждающего" эффекта
при отравлении наркозными и снотворными средствами. Он сочетает в себе свойства аналептика и
транквилизатора, так как может даже усиливать снотворный эффект. Его применяют преимущественно
при отравлении наркотическими анальгетиками, а также в психиатрии как успокаивающее ЛС.
Этимизол стимулирует гипоталамус и выработку адренокортикотропного гормона гипофиза, что
сопровождается стимуляцией коры надпочечников и увеличением содержания кортикостероидов в
крови, в результате чего возникают противоспалительный и противоаллергический эффекты. Поэтому
этимизол можно использовать при лечении бронхиальной астмы и воспалительных процессов.
Кофеин подробно описан в лекции по "психостимуляторам". Аналептический эффект проявляется
при парэитеральном применении достаточных доз, стимулирующих центры продолговатого мозга. Как
аналептик кофеин слабее бемегрида, но в отличие от него оказывает выраженное кардиотоническое
действие, поэтому проявляет более значительное влияние на кровообращение. Его назначают
преимущественно при отравлении алкоголем и сочетании острой дыхательной недостаточности с
сердечной.
Стрихнин - алкалоид из семян чилибухи, или "рвотного ореха", произрастающего в тропических
районах Азии и Африки. Он возбуждает все отделы ЦНС: усиливает функциональную активность коры,
органов чувств, центров продолговатого мозга, спинного мозга. Это проявляется улучшением зрения,
вкуса, слуха, тактильной чувствительности, тонуса мышц, работы сердца и обмена веществ. Таким
образом, стрихнин оказывает общетонизирующее действие. МД стрихнина связывают с ослаблением
постсинаптического торможения, медиатором которого является глицин. Прямое действие на центры
продолговатого мозга слабее, чем у бемегрида, но стрихнин повышает их чувствительность к
физиологическим стимулам, в результате чего возрастает объем легочной вентиляции, повышается АД
и усиливаются сосудосуживающие рефлексы. Возбуждение центра вагуса приводит к замедлению
ритма сердечных сокращений. Наибольшей чувствительностью к стрихнину обладает спинной мозг.
Уже в малых дозах стрихнин повышает рефлекторную возбудимость спинного мозга, что проявляется
усилением рефлекторных реакций, повышением тонуса скелетных и гладких мышц. Ослабление
постсинаптического торможения приводит к облегчению межнейронной передачи импульсов,
ускорению центральных рефлекторных реакций и увеличению иррадиации возбуждения в ЦНС. При
этом ослабевает сопряженное (реципроктное) торможение и возрастает тонус мышц-антагонистов.
Стрихнин имеет небольшую широту терапевтического действия и способен кумулировать, поэтому
можно легко вызвать передозировку. При отравлении стрихнином резко возрастает рефлекторная
возбудимость и развиваются тетанические судороги, возникающие в ответ на любое раздражение.
После нескольких приступов судорог может наступить паралич ЦНС. Лечение: введение ЛС,
угнетающих ЦНС (фторотан, тиопентал-натрий, хлоралгидрат, сибазон, натрия оксибутират),
мышечных релаксантов, промывание желудка р-ром калия перманганата, активированный уголь и
солевое слабительное внутрь, полный покой.
Стрихнин применяют как общетонизирующее ЛС при функциональном понижении зрения и слуха,
при атонии кишечника и миастении, при половой импотенции функционального характера, как
аналептик для стимуляции дыхания и кровообращения. Он противопоказан при гипертонии,
атеросклерозе, стенокардии, бронхиальной астме, болезнях печени и почек, эпилепсии и детям до 2 лет.
Аналептики смешанного действия стимулируют дыхательный центр непосредственно и
рефлекторно через хеморецепторы синокаротидной зоны. Кордиамин стимулирует дыхание и
кровообращение. Повышение АД и улучшение кровообращения связано с прямым действием на
сосудодаигательнь.и центр и сердце, особенно при сердечной недостаточности. Его назначают внутрь и
парэнтерально при ослаблении дыхания и кровообращения, вызванном интоксикацией, инфекционными
заболеваниями, шоком и др.
Камфора - бициклический кетон терпенового ряда, входит в состав эфирных масел камфорного
лавра, камфорного базилика и др. Используют также синтетическую камфору. Камфора хорошо
всасывается и частично окисляется. Продукты окисления соединяются с глюкуроновой кислотой и
выделяются почками. Часть камфоры выделяется через дыхательные пути. Местно оказывает
раздражающее и антисептическое действие. Стимулирует центры продолговатого мозга
непосредственно и рефлекторно. Действует медленно, но более продолжительно, чем другие
аналептики. Камфора повышает АД за счет сужения сосудов брюшных органов, расширяя при этом
сосуды мозга, легких и сердца. Тонус венозных сосудов возрастает, что приводит к увеличению
венозного возврата к сердцу. Различное влияние камфоры на сосуды связано с возбуждающим
действием на сосудодвигательный центр и прямым расширяющим действием на стенки сосудов. При
угнетении сердца различными ядами камфора оказывает прямое стимулирующее и детоксицирующее
действие на миокард. Кардиотонический эффект обусловлен симпатомиметическим влиянием и
активацией окислительного фосфорилирования. В больших дозах камфора возбуждает кору мозга,
особенно двигательные зоны, повышает рефлекторную возбудимость спинного мозга и может вызвать
клоно-тонические судороги. Камфора усиливает секрецию бронхиальных желез, разжижает мокроту и
улучшает ее выделение, стимулирует секрецию желчи и потовых желез. В воде растворяется плохо, в
масле и спирте - хорошо. Поэтому ее применяют в виде р-ров в масле п/к для улучшения дыхания и
кровообращения при отравлениях, инфекционных заболеваниях. Местно назначают в виде мазей,
втираний при воспалительных процессах, при зуде, для профилактики пролежней и т.п.
Противопоказана больным, склонным к судорожным припадкам.
Углекислота является физиологическим регулятором дыхания и кровообращения. На дыхательный
центр действует прямо и рефлекторно. Вдыхание 3% СО2 повышает вентиляцию легких в 2 раза, а
вдыхание 7,5% - в 5-10 раз. Максимальный эффект развивается через 5-6 мин. Вдыхание больших
концентраций СО2 (свыше 10%) вызывает сильный ацидоз, бурную одышку, судороги и паралич
дыхания. Возбуждение сосудодвигательного центра приводит к повышению тонуса периферических
сосудов и повышению АД. При этом сосуды легких, сердца, мышц и мозга расширяются. Расширение
связано с прямым действием на гладкие мышцы сосудов.
Углекислоту применяют для стимуляции дыхания при отравлении наркозными средствами, окисью
углерода, сероводородом, при асфиксии новорожденных, при заболеваниях, сопровождающихся
ослаблением дыхания, для профилактики ателектаза легких после наркоза и т.п. Ее можно применять
только при отсутствии выраженной гиперкапнии, так как дальнейшее повышение концентрации СО2 в
крови может вызвать паралич центра дыхания. Если через 5-8 мин. после начала ингаляции СО2
дыхание не улучшается, ее надо прекратить. Используют смесь СО2 (5-7%) с кислородом (93-95%) карбоген.
Цититон и лобелин стимулируют дыхательный центр рефлекторно за счет возбуждения
хеморецепторов каротидных клубочков. При в/в введении развивается сильный и быстрый эффект, но
кратковременный (2-3 мин). В ряде случаев, особенно при рефлекторной остановке дыхания, они могут
способствовать стойкому восстановлению дыхания и кровообращения. При отравлении наркозными и
снотоворными средствами эти препараты мало эффективны.
Средства, применяемые при отеке легких.
Отек легких сопровождается острой дыхательной недостаточностью. поэтому требует неотложной
терапии. Причины отека легких разнообразны. Различают 4 основных вида отека: 1) кардиогенный (при
левожелудочковой недостаточности); 2) токсический (при отравлении раздражающими и
удушающими газами и парами, при уремии, анафилактическом шоке, инфекциях); 3) неирогенный (при
черепно-мозговых травмах, коме, менингите, энцефалите); 4) отек, вызванный длительным
сопротивлением на вдохе (ларингоспазм, отек гортани, инородное тело в дыхательных путях,
искусственное дыхание с отрицательным давлением на вдохе).
Наиболее характерными признаками отека легких являются беспокойство. удушье, одышка, цианоз,
клокочущее дыхание с выделением розовой пенистой мокроты, обильный пот, слабость. Главную
опасность представляет вспениваиие отечной жидкости в дыхательных путях, которая закупоривает их
и вызывает гипоксию. Поэтому необходима ингаляция пеногасителей и кислорода, а также отсасывание
пены.
К средствам специфической терапии относятся ганглиоблокаторы, сосудорасширяющие ЛС
миотропного действия, а-адреноблокагоры, сердечные гликозиды, дегидратирующие и диуретические
ЛС, глюкокортикоиды, наркотические анальгетики. Выбор ЛС зависит от вида отека легких.
При кардиогенном отеке показано применение сердечных гликозидов быстрого действия
(строфантин, коргликон), которые вводят в/в. Лечебный эффект обусловлен усилением работы сердца
и улучшением венозного оттока из легких. Противопоказанием является митральный стеноз и
экстрасистолия. Применяют в/в капельное вливание р-ра дофамина с определенной скоростью.
диуретика фуросемида, глюкокортикоидов (преднизолон), наркотических анальгетиков (морфин).
Отек легких с артериальной гипертензией лечится с помощью ЛС, уменьшающих венозный
возврат к сердцу, понижающих легочное АД и кровенаполнение легких. Это сопровождается
уменьшением транссудации жидкости в альвеолы и увеличением ее всасывания в кровь. Используют
ганглиоблокаторы короткого действия (гигроний, арфонад), средней продолжительности действия
(бензогексоний, пентамин), а-адреноблокаторы (фентоламин, аминазин, дроперидол), миотропные
вазодилататоры (натрия нитропруссид, нитроглицерин), осмотические диуретики (маннит,
мочевина), вызывающие дегидратацию легочной ткани, диуретики быстрого и сильного действия
(фуросемид, кислота этакриновая).
При отеке легких на фоне нормотензии снижение АД опасно, поэтому гипотензивные ЛС надо
применять осторожно и под контролем АД. Используют преимущественно мероприятия общего
характера, дегидратирующие и мочегонные ЛС, противоотечные средства (глюкокортнкоиды),
аиальгетики.
При отекв легких на фоне гипотензии для нормализации АД применяют адремомиметики
(мезатон, эфедрин), дофамин, под контролем АД назначают дегидратирующие (маннит, мочевина) и
сильные диуретики. Глюкокортикоиды (преднизолон, гидрокортизон) оказывают противоотечное,
противовоспалительное и иммунодепрессианое действие, особенно эффективны при анафилактическом
отеке легких, но могут с успехом применяться и при других формах отека. Наркотические анальгетики
(морфин, промедол) уменьшают венозный возврат крови к сердцу и кровенаполнение легких, угнетают
одышку и кашель, снижают потребность в кислороде, оказывают успокаивающее действие, поэтому
используются при разных видах отека легких, за исключением отека при травмах черепа. Пеногасители
показаны при всех видах отека легких. К ним относятся спирт этиловый и антифомсилан. Лечебное
действие основано на уменьшении поверхностного натяжения пены и превращении ее в жидкость,
объем которой во много раз меньше, чем пены. Их назначают ингаляционно вместе с кислородом.
Антифомсилан не раздражает дыхательные пути, не угнетает ЦНС и действует быстрее спирта.
Лекция 17.
СРЕДСТВА, РЕГУЛИРУЮЩИЕ ФУНКЦИИ ОРГАНОВ ПИЩЕВАРЕНИЯ.
В этой лекции будут рассмотрены следующие вопросы:
* - МД и эффекты ЛС, стимулирующих и угнетающих аппетит;
* - МД, основные и ПЭ ЛС, регулирующих секреторно-моторную функцию желудка, показания и
противопоказания к их применению;
* - рвотные и противорвотные ЛС, их МД, эффекты и применение;
• - ЛС, влияющие на внешнесекреторную функцию печени, их применение;
• - ЛС, влияющие на внешнесекреторную функцию поджелудочной железы;
* - ЛС, регулирующие секреторно-моторную функцию кишечника;
• - классификация и МД слабительных ЛС, принципы их применения;
• - противопоносные ЛС, принципы их рационального применения.
Современная медицина располагает большим арсеналом ЛС для лечения заболеваний органов
пищеварения. В этот раздел фармакологии большой вклад внесли исследования И. П. Павлова,
заложившие научные основы терапии нарушений секреторно-моторной функции органов пищеварения.
Средства, регулирующие аппетит.
Делятся на средства, повышающие и понижающие аппетит. Действие связано с влиянием на центры
голода и насыщения, расположенные в гипоталамусе, а также с лимбической системой и корой мозга.
К ЛС, повышающим аппетит, относят горечи. Это вещества, обладающие горьким вкусом и не
оказывающие выраженного резорбтивного действия: настойка горькая, настойка полыни и др.
Свойствами горечей обладают также вкусовые вещества (пряности): семена тмина, мята, корица,
гвоздика, ваниль, перец, горчица, чеснок, хрен, редька и др. Стимулируют аппетит виноградное вино и
пиво. МД горечей состоит в том, что они раздражают вкусовые рецепторы рта и рефлекторно
возбуждают центр голода, что приводит к усилению секреции желез желудка при приеме пищи.
Одновременно возрастает секреция слюнных желез и поджелудочной железы. Горечи следует
принимать за 15-30 мин. до еды.
К ЛС, понижающим аппетит (анорексигенным), относятся производные фенамина (фепранон,
дезопимон, фенфлурамин) и изоиндола (мазиндол). Фенамнн является эффективным анорексигенным
средством, но из-за ПЭ для понижения аппетита не применяется. Фепранон и дезопимон слабее его. но
меньше возбуждают ЦНС и ССС, редко вызывают пристрастие. МД связан со стимуляцией центра
насыщения в результате активации адренергических влияний. При длительном применении могут
вызывать ПЭ: бессоница, беспокойство, тахикардия, повышение АД, привыкание и пристрастие.
Противопоказаны при гипертонии, нарушении мозгового кровообрашения, тиреотоксикозе, сахарном
диабете, эпилепсии. Фенфлурамин оказывает седативное действие и не повышает АД. МД связан с
усилением высвобождения и затруднением обратного захвата серотонина и угнетением дофаминовых
рецепторов, что сопровождается уменьшением содержания серотонина, дофаминергических влияний и
угнетением центра голода. Препарат также тормозит всасывание и синтез триглицеридов и ускоряет
обмен жиров. ПЭ: сонливость, депрессия, раздражение слизистой желудка, иногда эйфория и
лекарственная зависимость. Мазиндол - сильный анорексиген, МД которого связан с усилением
высвобождения НА и дофамина и угнетением их обратного захвата. Он угнетает всасывание и синтез
триглицеридов и холестерина. ПЭ: бессонница, беспокойство, сухость во рту, тошнота, аллергические
реакции. иногда лекарственная зависимость.
Основным показанием для назначения анорексигенных ЛС является алиментарное ожирение.
Однако эти ЛС являются лишь компонентом комплексной терапии ожирения, включающей
ограничение диеты, занятия лечебной физкультурой и т.п. Они наиболее сильно угнетают аппетит в
первые недели приема, а затем их эффект снижается. Поэтому их следует применять не более 6-10
недель.
Средства, регулирующие секреторно-моторную функцию желудка.
Эта группа включает ЛС. используемые с диагностической целью. ЛС заместительной терапии и ЛС,
понижающие секрецию и моторику желудка.
К ЛС, используемым с диагностической целью, относятся гистамин и пентагастрин. Их
назначают перед взятием желудочного сока на исследование. При функциональной недостаточности
желез желудка они повышают их секрецию, при органических нарушениях слизистой секреторная
реакция отсутствует. МД гистамина на железы желудка связан с возбуждением Н2гистаминорецепторов. Для устранения эффектов гистамина на Н1-рецепторы (снижение АД, спазм
бронхов, кишечника и др.) перед его введением назначают блокаторы этих рецепторов (димедрол,
дипразин, супрастин и др.). Пентагастрин является синтетическим заменителем гастрина, который
образуется в антральной части желудка. Он стимулирует железы желудка сильнее гистамина, не
вызывая ПЭ, обеспечивает образование внутреннего фактора Кастла и усиливает секрецию
поджелудочной железы и желчеобразование.
ЛС заместительной терапии (натуральный и искусственный желудочный сок, пепсин, кислота
хлористоводородная и препараты, их содержащие -ацидин-пепсии и др.) используют при недостаточной
функции желез желудка.
ЛС, влияющие на секреторно-моторную функцию желудка включают м-холиноблокаторы,
ганглиоблокаторы, блокаторы Н2-гистаминорецепторов и антацидные средства. Для ослабления
влияний вагуса на секрецию и моторику желудка назначают м-холиноблокаторы и
ганглиоблокаторы. Однако они обладают широким спектром действия, поэтому дают много ПЭ.
Созданы ЛС селективного действия на м-ХР ЖКТ, к которым относится пирензепин (гастрозепин). Из
кишечника всасывается плохо, не проникает через ГЭБ и плаценту. Угнетает как базальную, так и
вызванную секрецию соляной кислоты, пепсина и гастрина, повышает устойчивость слизистой желудка
к действию раздражителей (гастропротективное действие). К блокаторам Н2-гистаминорецепторов
относятся ранитидин и циметидин. Они снижают секрецию хлористоводородной кислоты и, в меньшей
степени, пепсина под влиянием гистамина, пентагастрина, пищи, растяжения желудка, а также ее
базальную секрецию. Через ГЭБ проникают плохо, выделяются через почки преимущетвенно в
неизмененном виде. Ранитидин обладает более высокой избирательностью действия и меньшей
токсичностью. Циметидин слабее ранитидина в 5-10 раз, чаще вызывает ПЭ (гинекомастия, угнетение
функций печени, лейкопения). Омепразол - противоязвенный препарат принципиально нового типа
действия. Он снижает кислотность желудочного сока за счет угнетения функции протонового насоса
(Н+,К+-АТФ-азы) париетальных клеток желудка, являясь необратимым ингибитором мембранной
Н+,К+-АТФ-азы. Этим эффектом обладает сульфенамид, который быстро образуется в кислой среде
канальцев париетальных клеток из омепразола. Он активно подавляет секрецию хлористоводородной
кислоты и пепсина и защищает слизистую желудка, не влияя на моторику желудка. Высоко эффективен
при язвенной болезни желудка и 12-перстной кишки, при язвенном эзофагите и гиперацидных
гастритах. Хорошо переносится и редко вызывает ПЭ (диспептические расстройства, головная боль и
др.).
Антацидные средства - это ЛВ, имеющие щелочную реакцию и нейтрализующие
хлористоводородную кислоту желудочного сока, что приводит к снижению активности пепсина. Их
назначают для нейтрализации повышенной кислотности среды желудка. Одновременно они
стимулируют секрецию панкреатического сока. К ним относятся натрия гидрокарбонат, магния окись,
кальция карбонат, алюминия гидроокись, магния трисиликат. Выбор препарата зависит от его свойств и
характера патологии. Наиболее быстрым, но коротким действием обладает натрия гидрокарбонат.
При взаимодействии с кислотой образуется углекислота, которая растягивает желудок и приводит к
вторичной волне секреции. Всасываясь в кровь, натрия гидрокарбонат может вызвать системный
алкалоз. Магния окись и магния трисиликат значительно активнее натрия гидрокарбоната, действуют
медленее, но продолжительнее. Из кишечника всасываются незначительно и системным действием не
обладают. Могут давать послабляющий эффект. Алюминия гидроокись оказывает продолжительное
антацидное и адсорбирующее действие. Алкалоза не вызывает, может вызвать запор. Она входит в
состав альмагеля, оказывающего антацидное, адсорбирующее и обволакивающее действие. Кальция
карбонат осажденный действует быстро и в желудке образует углекислоту. В больших дозах может
вызвать гиперкальциемию и алкалоз. Антацидные ЛС показаны при язвенной болезни желудка и 12перстной кишки, гиперацидных гастритах, пептической язве и т.п. Их целесообразно принимать перед
возникновением симптомов, связанных с повышенной агрессивностью желудочного сока.
В лечении гастритов и язвенной болезни большое значение приобрели гастропротекторы - ЛВ,
действующие на слизистую желудка и защищающие ее от повреждающих факторов. Их подразделяют
на 2 группы: 1) механически защищающие слизистую оболочку (сукралфат, висмута цитрат
основной); 2) повышающие защитную функцию слизи и устойчивость слизистой ободочки
(карбеноксолон, мизопростол). Сукралфат (антепсин) - гель, который в кислой среде образует вязкое и
клейкое вещество, покрывающее язвенную поверхность на 6 ч. и защищающее ее от повреждающих
факторов. Принимают перед едой и сном. Нельзя комбинировать с антацидными и антигистаминными
ЛС. Не всасывается и не оказывает резорбтивмого действия. ПЭ (запоры, сухость во рту) возникают
редко. Висмута цитрат основной (де-нол, висмута субцитрат) - коллоидная суспензия, образующая
в кислой среде осадок, покрывающий язвенную поверхность. ПЭ не дает. Карбеноксолон натрий
(биогастрон) усиливает барьерную функцию слизи. Его получают из солодки. Он усиливает секрецию
слизи, делая ее более вязкой, благодаря чему она создает прочный защитный барьер. Так как по
структуре он сходен с кортикостероидами, то может вызывать аналогичные ПЭ (задержка натрия и
воды в организме, отеки, гипокалиемия, повышение АД), которые устраняются спиронолактоном, но
при этом исчезает терапевтический эффект. Тиазидные диуретики устраняют отеки, но не снижают
терапевтического действия. Мизопростол - синтетический простагландин Е1. ПГ Е1 и Е2 повышают
устойчивость слизистой желудка, снижают секрецию хлористоводородной кислоты и увеличивают
секрецию слизи. Этим объясняется МД мизопростола, эффективного при приеме внутрь.
В настоящее время широко используют комбинированные ЛС, которые не только регулируют
секреторно-моторную функцию, но и защищают слизистую оболочку желудка и кишечника,
способствуют ее регенерации. К ним относятся гастрофарм, солкосерил, фосфолюгель, эглонилфорте и др. Процессы регенерации слизистой стимулируют также анаболические стероиды
(ретаболил, феноболил и др.), метилурацил, витамин U, оксиферрискорбон натрия.
Для регуляции моторики желудка используют холинергические ЛС. Холиномиметики (ацеклидин,
прозерин и др.) усиливают моторику, м-холиноблокаторы и ганглиоблокаторы угнетают. Действие этих
ЛС рассмотрено ранее. Применяют также ЛС, сочетающие оба типа действия (бускопан, пробантин).
Рвотные и противорвотные средства.
Рвота регулируется рвотным центром, расположенным а продолговатом мозге. Там же находится
пусковая зона рвотного центра (тригер-зона), регулируемая дофаминовыми рецепторами. Рвота
возникает при раздражении пусковой зоны различными стимулами (рефлексы с вестибулярного
аппарата, с рецепторов слизистой желудка и кишечника, с вкусового, обонятельного и зрительного
анализаторов, прямое действие токсинов на дофаминовые рецепторы). Рвоте предшествует тошнота.
Рвоту вызывают для удаления раздражающих и токсических веществ, попавших в желудок. С этой
целью используют апоморфина гидрохлорид, стимулирующий дофаминовые рецепторы пусковой зоны.
После п/к введения эффект возникает быстро, поэтому период тошноты короткий. Показан для
быстрого удаления токсических веществ из желудка, если промывание его невозможно.
Противопоказан при тяжелых заболеваниях ССС, ожогах пищеводами желудка кислотами и щелочами,
при язве желудка и 12-перстной кишки, при легочных кровотечениях и беременности. Иногда
используют при лечении алкоголизма для выработки отрицательного условного рефлекса на алкоголь.
Тошнота и рвота являются симптомами различных нарушений: вестибулярных, мозжечковых,
желудочно-кишечных, обменных, токсических, рефлекторных и др. Поэтому выбор подтиворвотных
средств определяется причинами, вызвавшими рвоту. Действие препарата должно быть направлено на
механизмы, способствующие возникновению рвоты. Напр., при воздушной и морской болезни
используют ЛС, угнетающие рефлекторные влияния с вестибулярного аппарата на рвотный центр. К
ним относятся скополамин, который входит в таблетки "Аэрон", антигистаминные средства (дипразин,
супрастин), симпатомиметики (эфедрин), витамины (пиридоксин) и др.
Наиболее частой причиной тошноты и рвоты служат заболевания ЖКТ. В этих случаях эффекта
можно достигнуть холинолитиками, антигистаминными, транквилизаторами, седативными,
анестезирующими ЛС. При рвоте, вызванной действием токсинов на рецепторы пусковой зоны
рвотного центра (противоопухолевые ЛС, сердечные гликозиды, токсикозы беременных, азотемия и
др.). эффективны нейролвптики (аминазин, этаперазин, трифтазин, галоперидол и др.). МД которых
объясняют блокадой дофамииовых рецепторов. Препаратом широкого спектра применения является
метоклопрамид (реглан, церукал). МД также обусловлен блокадой дофаминовых рецепторов, но
метоклопрамид действует более избирательно на рвотный центр, чем нейролептики, поэтому не
вызывает депрессии. Его назначают для устранения тошноты и рвоты, вызванных раздражением ЖКТ,
при лучевой болезни, уремии и различных интоксикациях.
Желчегонные средства.
Применяют при нарушениях внешнесекреторной функции печени. Недостаток желчи приводит к
нарушению эмульгирования и всасывания жиров, жирорастворимых витаминов, к развитию гнилостной
микрофлоры в кишечнике и угнетению его моторики. Основными компонентами желчи являются
желчные кислоты. Секрецию и выделение желчи регулирует холецистокинин - гормон слизистой
дуоденум. Он вызывает сокращение желчного пузыря и расслабление сфинктера Одди, обеспечивая
поступление желчи в кишечник. Недостаточное поступление желчи может быть обусловлено: 1)
нарушением желчеобразовательной функции печени; 2) нарушением желчевыделения. Для лечения
используют многие ЛС, которые условно делят на 2 группы: 1) ЛС, стимулирующие образование
желчи (холесекретики, холеретики); 2) ЛС, способствующие выделению желчи (холецистокинетики,
холагога).
1. Холесекретики - препараты желчных кислот и желчи (хологон, дехолин, аллохол, холензим),
растительные средства, содержащие флавоны, витамины, эфирные масла (холосас, кукурузные рыльца,
цветы бессмертника, пижма и др.), синтетические ЛС (оксафенамид, никодин, циквалон,
дегидрохолевая кислота и др.). Показаны при угнетении секреции желчи. Противопоказаны при острых
и значительных поражениях печени, закупорке желчных протоков камнем и т.п., так как создают
дополнительную нагрузку на печень и могут усилить желтуху.
2. Холецистокинетики подразделяются на ЛВ, вызывающие сокращение желчного пузыря и
расслабление сфинктера Одди (холецистокинин, питуитрин, магния сульфат, сорбит и др.), и ЛВ,
устраняющие спазмы желчных путей (атропин, платифиллин, папаверин, но-шпа и др.). Те и другие
способствуют выходу желчи в кишечник.
Эта классификация довольно относительна, так как ЛС, стимулирующие образование желчи,
одновременно увеличивают ее выделение, а ЛС, увеличивающие желчевыделение, способствуют
желчеобразованию. Наиболее важным фактором при лечении заболеваний печени и желчевыводящих
путей является улучшение оттока желчи, что устраняет ее застой и всасывание в кровь, уменьшает
опасность развития инфекции в желчных путях и образования желчных камней.
При лечении заболеваний печени широко используют гепатопротекторы-ЛС, защищающие
печень. Такими свойствами обладают легален, эссенциалефорте, содержащий эссенциальные
(необходимые) фосфолипиды, витамины (пиридоксин, цианокобаламин, никотинамид и др.).
ЛС, влияющие на внешнесекреторную функцию поджелудочной железы.
Ферменты поджелудочной железы участвуют в расщеплении белков, жиров и углеводов. Их
активность тормозится ингибиторами, которые вырабатываются клетками панкреас, печени,
околоушных желез и других органов. При панкреатитах защитное действие ингибиторов становится
недостаточным, что приводит к активизации протеолитических ферментов и "самоперевариванию"
поджелудочной железы. Это требует введения ингибиторов ферментов. Секрецию панкреатического
сока стимулируют гормоны кишечника секретин и холецистокинин, применяемые с диагностической
целью. В качестве средства заместительной терапии используют панкреатин, получаемый из
поджелудочной железы убойного скота. Он содержит ферменты трипсин и амилазу, которые
расщепляют белки и углеводы. Панкреатин назначают при недостаточности функций панкреас, печени,
желез желудка. Его целесообразно сочетать с хлористоводородной кислотой, пепсином, желчегонными
средствами.
В норме в поджелудочной железе образуется трипсиноген, который превращается в активный
трипсин только в кишечнике под влиянием энтерокиназы. При остром воспалении панкреас активация
трипсиногена происходит в ткани железы под влиянием цитокиназы, что сопровождается
"самоперевариваиием" железы. При этом в кровь выделяется брадикинин, вызывающий расширение
сосудов и падение АД. Лечение острого панкреатита направлено на уменьшение секреции панкреас с
помощью м-холиноблокаторов (атропин и др.) и угнетение протеолитических ферментов (трипсина и
калликреина) с помощью ингибиторов (контрикал, трасилол, инипрол).
Средства, влияющие на моторику кишечника.
Делятся на: 1) ЛС, угнетающие моторику; 2) ЛС, усиливающие моторику. К 1 гр. относятся м-
холиноблокаторы, ганглиоблокаторы и спазмолитики миотропного действия (папаверин, но-шпа,
дибазол и др.). ко 2-й -м-холиномиметики (ацеклидин), антихолинэстеразные (прозерин, галантамин и
др.), вазопрессин, слабительные средства. Все ЛС, за исключением слабительных, были рассмотрены
ранее.
Слабительные средства - это вещества, ускоряющие продвижение содержимого, кишечника и
наступление дефекации. В зависимости от локализации и МД их делят на следующие группы: 1) ЛС;
действующие преимущественно на тонкий кишечник; 2) ЛС, действующие преимущественно на
толстый кишечник; 3) ЛС, действующие на все отделы кишечника. По происхождению слабительные
подразделяют на: 1) солевые (магния сульфат, натрия сульфат); 2) растительные масла (касторовое
масло); 3) содержащие антрагликозиды (листья сенны, кора крушины, корень ревеня); 4) синтетические
(фенолфталеин, изафенин).
К средствам, действующим преимущественно на тонкий кищечник, относится касторовое масло.
Его действие начинается в 12-перстной кишке, где под влиянием липазы образуется рициноловая
кислота, которая раздражает рецепторы кишечника и усиливает перистальтику, вызывая дефекацию
через 2-6 ч. Назначают при острых запорах. При отравлении жирорастворимыми веществами его
применять не следует.
К ЛС, действующим на толстый кишечник, относятся корень ревеня, кора крушины, лист сенны,
фенолфталеин, изафенин. В растительных ЛС содержатся антрагликозиды, которые в печени
превращаются в эмодин, хризофановую кислоту и др., раздражающие слизистую толстых кишок, в
результате чего через 8-12 ч. наступает послабляющий эффект. Поэтому их назначают обычно на ночь.
Фенолфталеин всасывается в тонком кишечнике, а выделяется в толстом, усиливая его перистальтику.
Эффект наступает через 6-8 ч. Он может кумулировать и оказывать вредное действие на почки.
Изафенин по действию и применению сходен с фенолфталеином.
К ЛС, действующим на все отделы кишечника, относятся солевые слабительные - магния
сульфат и натрия сульфат. Они быстро диссоциируют в кишечнике на ионы, которые плохо
всасываются и создают высокое осмотическое давление в просвете кишок. Это затрудняет всасывание
воды и способствует ее выходу в просвет кишечника, в результате чего возрастает объем содержимого
кишечника, раздражаются рецепторы и усиливается перистальтика на всем протяжении кишечника.
Солевые слабительные надо назначать с достаточным количеством теплой воды (1-2 стакана). Эффект
наступает через 2-4 ч. Их назначают обычно однократно, так как частое применение раздражает
слизистую.
Слабительные ЛС показаны: 1) при отравлениях (солевые); 2) при лечении глистных инвазий
(солевые); 3) для дегидратации при отеке мозга (солевые); 4) при подготовке к рентгеновскому
исследованию кишечника и позвоночника (касторовое масло, препараты, действующие на толстый
кишечник); 5) при хронических запорах (препараты, действующие на толстый кишечник). ПЭ могут
быть связаны с передозировкой (коликообразные боли в животе, рвота, понос), с длительным
бесконтрольным применением (воспалительные процессы в кишечнике, привыкание). Они
противопоказаны при остром аппендиците и холецистите, перитоните, механической непроходимости
кишечника, ущемленной грыже, кровотечениях в ЖКТ, маточных кровотечениях. Их надо осторожно
применять при беременности из-за опасности выкидыша.
Противопоносные средства.
Понос является симптомом многих заболеваний (отравления, инфекции. болезни желудка и
поджелудочной железы и т.п.). Для устранения поноса необходимо прежде всего выяснить причину. В
качестве ЛС симптоматической терапии используют вяжущие, обволакивающие и адсорбирующие
средства, которые обладают неспецифическим противоспалительным и закрепляющим действием,
защищая слизистую оболочку кишечника от раздражающих агентов.
ПРИЛОЖЕНИЯ.
ВОПРОСЫ ДЛЯ ПОДГОТОВКИ К ЭКЗАМЕНУ.
1.Содержание фармакологии и ее место среди других медицинских и биологических наук.
2.Дсстижения и основные направления развития современной фармакологии.
3.Роль отечественных и зарубежных ученых в становлении и развитии экспериментальной и
клинической фармакологии (В.И.Дыбковский, Р.Бухгейм, Ю.О.Петровский, Н.П.Кравков,
С.В.Аничков, В.В.Закусов, З.В.Ермольева).
4. Фармакологические работы отечественных физиологов и клиницистов (И.М.Сеченов, И.П.Павлов,
С.П.Боткин, Н.И.Пирогов).
5.Основные научные направления украинских ученых-фармакологов (А.И.Черкес, П.В.Родионов,
Г.Е.Батрак, Н.С.Шварсалон).
6.Пути поиска и разработки новых лекарственных средств: эмпирический путь, получение препаратов
из лекарственного сырья растительного, животного и минерального происхождения, направленный
химический синтез.
7.Основные разделы фармакологии: общая фармакология, частная фармакология, фармакогенетика,
хронофармакология, клиническая фармакология, педиатрическая и гериатрическая фармакология.
8.Пути введения ЛВ в организм.
9.Всасывание ЛВ. Основные механизмы всасывания, факторы, влияющие на всасывание.
Биодоступность.
10.Распределение Л8 в организме. Биологические барьеры (гематоэнцефалический и плацентарный).
Депонирование лекарств.
11.Химические превращения ЛВ в организме.
12.Пути выведения ЛВ из организма.
13.Локализация и основные принципы (механизмы) действия лекарств. Понятие о рецепторах,
агонистах и антагонистах.
14.Виды действия ЛС.
15.Основные виды лекарственной терапии.
16.Зависимость фармакологического эффекта от свойств ЛС (химическое строение, физические и
химические свойства и др.).
17.Дозы и концентрации ЛС. Широта терапевтического действия лекарств. Биологическая
стандартизация.
18.Значение возраста, пола, состояния организма и биологических ритмов для действия лекарств.
19.Зависимость фармакологического эффекта от патологического состояния организма, биологических
ритмов, генетических и антропогенных факторов.
20.3начение факторов внешней среды для действия лекарств.
21.Действие лекарств при повторном их применении (кумуляция, привыкание, тахифилаксия).
22.Лекарственная зависимость. Медицинские и социальные аспекты.
23. Несовместимость ЛС (фармацевтическая и фармакологическая).
24.Комбинированное действие ЛС (синергизм, антагонизм, антидотизм).
25.Основное и побочное действие лекарств. Аллергические реакции. Идиосинкразия. Токсические
эффекты.
26.Тератогенность, эмбриотоксичность, мутагенный и канцерогенный эффекты.
27.Характеристика понятий "фармакодинамика", "фармакокинетика", "фармакотерапия".
28.Государственный контроль качества лекарств в Украине. Функции Фармакологического и
Фармакопейного комитетов и Государственной комиссии по контролю за качеством ЛС.
29.Структура рецепта. Официнальные и магистральные прописи лекарств. Особенности выписывания
ядовитых, сильнодействующих и наркотических средств.
30.Лекарственные формы. Правила их выписывания.
31.Анестезирующие средства. Механизм действия. Виды местной анестезии.
32.Вяжущие, обволакивающие, адсорбирующие и раздражающие средства. Принципы их действия и
показания к применению.
33.Классификация средств, влияющих на передачу возбуждения в холинергических синапсах.
34.М- и н-холиномиметические средства. Основные эффекты. Применение.
35.М-холиномиметические средства. Основные эффекты. Показания к применению. Токсические
эффекты. Лечение отравлений.
36.Н-холиномиметические средства. Основные эффекты. Показания к применению. Токсическое
действие никотина. Лечение острого отравления никотином. Отрицательные последствия курения.
37.Антихолинэстеразные средства. Классификация. Основные эффекты. Показания к применению.
38.Побочное и токсическое действие антихолинэстеразных средств. Лечение отравлений. Применение
реактиваторов холинэстеразы.
39.М-холиноблокирующие средства, МД, основные эффекты. Показания к применению. Токсическое
действие атропина. Лечение отравлений.
40.Классификация периферических н-холиноблокаторов. Ганглиоблокаторы. Локализация и МД.
Основные эффекты. Применение. Побочное действие.
41.Курареподобные средства. Классификация по МД. Применение. Возможные осложнения.
Антагонисты курареподобных средств.
42.Классификация средств, влияющих на передачу возбуждения в адренергических синапсах.
43.Альфа- и бета-адреномиметики прямого и непрямого действия. МД, основные эффекты, применение.
44.Вещества, стимулирующие преимущественно а-АР. Основные эффекты. Показания к назначению.
45.Вещества, стимулирующие преимущественно в-АР. Основные эффекты. Показания к назначению.
46.Вещества, блокирующие а-АР. Основные эффекты. Показания к назначению.
47.Вещества, блокирующие в-АР. Основные эффекты. Показания к назначению.
48.Симпатолитические ЛС. Локализация, МД, основные эффекты. Показания к назначению. Побочное
действие.
49.Понятие о наркозе. Основные МД, стадии наркоза. Классификация средств для наркоза. Понятие о
широте наркотического действия.
50.Средства для ингаляционного наркоза. Основные эффекты. Осложнения ингаляционного наркоза.
Меры помощи.
51.Средства для неингаляционного наркоза. Основные эффекты. Показания к применению. Токсические
эффекты.
52.Резорбтивное и местное действие этилового спирта. Применение в медицинской практике.
53.Острое и хроническое отравление спиртом и его лечение. Алкоголизм и его социальные аспекты.
Принципы фармакотерапии алкоголизма. Тетурам.
54.Современные представления о природе сна. Основные виды бессоницы. Классификация снотворных
ЛС. Возможные МД.
55.Сравнительная характеристика снотворных ЛС. Влияние на структуру сна. Возможность развития
лекарственной зависимости. Острое отравление снотворными ЛС и принципы его лечения.
56.Наркотические анальгетики. Центральные и периферические эффекты. Опиатные рецепторы и их
эндогенные лиганды. МД морфина. Применение.
57.Острое отравление морфином. Лечение. Антагонисты наркотических анальгетиков. Привыкание,
лекарственная зависимость (морфинизм), медицинские и социальные последствия, профилактика и
лечение.
58.Классификация
ненаркотических
анальгетиков.
Механизмы
противовоспалительного,
болеутоляющего и жаропонижающего действия. Показания. ПЭ.
59.Противоэпилептические ЛС. Применение при разных формах эпилепсии, МД. Средства для
купирования эпилептического статуса. ПЭ противоэпилептических ЛС.
60.Противопаркинсонические ЛС: МД, сравнительная оценка эффективности препаратов, основные и
ПЭ.
61.Классификация психотропных ЛС. Нейролептики: МД, основные и ПЭ, применение. Понятие о
нейролептанальгезии. Соли лития.
62.Транквилизаторы: МД, основные и ПЭ, применение. Возможность развития лекарственной
зависимости.
63.Антидепрессанты: МД, основные и ПЭ, показания к назначению.
64.Седативные ЛС: влияние на ЦНС, показания к применению, ПЭ.
65.Психостимулирующие ЛС: МД, основные и ПЭ, применение, возможность развития лекарственной
зависимости.
66.Ноотропные ЛС: влияние на метаболизм в ЦНС, показания к применению.
67.Аналептики: МД на ЦНС, основные и ПЭ, показания к назначению.
68.Общетонизирующие ЛС, применение. МД и фармакологические эффекты стрихнина, отравление,
принципы оказания помощи при отравлении.
69.Классификация стимуляторов дыхания по МД. Сравнительная характеристика групп препаратов.
Показания к применению.
70.Противокашлевые ЛС. Деление их по МД, применение. Возможность развития привыкания и
лекарственной зависимости к ЛС центрального действия.
71.Классификация отхаркивающих ЛС по локализации и МД. Пути введения. применение.
72.Бронхолитические ЛС: классификация по МД, основные и ПЭ, применение.
73.ЛС, применяемые при отеке легких. Принципы действия, комбинированное применение препаратов.
74.ЛС, стимулирующие и понижающие аппетит, МД, показания к применению.
75.ЛС, усиливающие секрецию желез желудка, используемые с диагностической целью. Средства
заместительной терапии.
76.МД средств, понижающих секрецию желез желудка, применение.
77.Сравнительная характеристика антацидных ЛС, показания к назначению.
78.Локализация и МД средств, усиливающих и угнетающих моторику желудка и кишечника, показания
к назначению.
79.МД рвотных и противорвотных ЛС, показания к применению.
80.Классификация ЛС, стимулирующих образование и выделение желчи, их сравнительная
характеристика, показания к назначению.
81.ЛС, применяемые при нарушении экскреторной функции поджелудочной железы. Показания к
назначению.
82.Классификация слабительных средств. Локализация и МД солевых слабительных, показания к
назначению.
83.Локализация и МД касторового масла, слабительных средств, содержащих антрагликозиды,
фенолфталеина и изафенина. Показания к назначению.
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, КОТОРЫЕ НЕОБХОДИМО УМЕТЬ ВЫПИСАТЬ В РЕЦЕПТАХ
НА ЭКЗАМЕНЕ ПО ФАРМАКОЛОГИИ
Формы выпуска
Название препарата и ею основные Средние терапевтические
синонимы
дозы для взрослых и пути
введения
Средства, влияющие на афферентную иннервацию
1-3% р-р для анестезии глаза, Порошок
Дикаин (Dicaium). Tеtгacаini
2-5% р-р для анестезии
hydrochloridum, Amethocaine,
слизистых рта. носа, гортани.
Intercaine, Pantocain и др.
Пор., амп. no 1,2,5,10
0,25-0,5% p-p для
Новокаин (Novocainum). Procaini
hydrochloridum, Аminocainе, Pancain, инфильтрационной анестезии, мл, 0,25, 0,5, 1 и 2%р1-2% для проводниковой, 5% ра.
Protocaine и др.
спинномозговой
0,25-0,5% р-р для инфильтр.; Амп. по 10 и 20 мл 1%
Лидокаина гидрохлорид (Lidocaini
hydrochloridum), Xycain, Xylocain и 0,5-2% р-р для проводниковой р-ра, по 2 и 10 мл 2%
и 1-5% р-р для терминальной р-ра, по 2 мл 10% рдр.
анестезии.
ра.
Порошок.
Танин (Tanninum, Acidum tannicum). 1-2% р-р для полосканий, 3Измельченная кора по
Кора дуба (Cortex Quercus)
10% мазь. Отвар 1:10 для
полосканий полости рта, зева, 50 и100 г
гортани
Крахмал (Amylum)
Слизь по 15-30 мл внутрь и в Порошок
клизмах, пор. в присыпках,
наружно
Пор., таб. по 0,.25 и
Уголь активированный (Carbo
Внутрь по 1-2 г при
0,5 г.
activatus)
метеоризме, по 20-30 г при
отравлении
Средства, влияющие на эфферентную иннервацию.
Пилокарпина гидрохлорид
1-2% р-р в глазных каплях.
Пор., фл., по 5 и 10 мл
(Pilocarpini hydrосhloridum). Pilocar
1-2% р-ра
Ацеклидин (Асесlidinum). Glaudin,
2-5% р-р в глазных каплях, 3- Пор., амп. по 1 и 2 мл
Glaucostat, Glaunorm
5% глазная мазь, 0,002 г п/к. 0.2% р-ра, 3-5% мазь
Прозерин (Proserinum). Neostigmini Внутрь по 0,015 г, п/к по
Пор., таб. по 0,015 г,
methylsulfas, Prostigmin и др.
0,0005 г, в глаз - 0,5% р-р
амп. - 1 мл 0,05% р-ра
Лобелина гидрохлорид (Lobelini
0,003-0,005 г в/в.
Амп. и шприцтюбики
hydrochloridum). Lobatox, Lobeton
по 1 мл 1% р-ра
Атропина сульфат (Atrорini sulfas).
Внутрь, п/к и в/м по 0,0005 г, Пор., таб. по 0,0005 г,
0,5-1% р-р в глазных каплях
амп., шприц-тюбики 1 мл 0,1% р-ра
Платифиллина гидротартрат
Внутрь и п/к по 0,005 г, 1-2% Пор., таб. по 0,005 г,
(Platyphyllini hydrotartras)
Бензогексоний (Benzohexonium).
Hexamethonii benzosuIfonas
Тубокурарина хлорид (Tubocurarini
chloridum) Curarin, Tubarine и др.
Дитилин (Dithylinum) Suxamethonii
iodidum, Cysthenon и др.
Адреналина гидрохлорид (Adrenalini
hydrochloridum). Epinephrinum,
Paranephirine и др.
Норадреналина гидротартрат
(Noradrenalini hydrotartras)
Levarterinoli bitartras. Norepinephrine
Мезатон (Mesatonum). Phenyleprini
hydrochloridum, Neophryn и др.
р-р в глазных каплях
Внутрь по 0,1 и 0,25 г, п/к, в/м
и в/в по 0,025 г
В/в гю 0,0005 г/кг
амп. 1 мл 0,2% р-ра
Таб. по 0,1 и 0,25 г,
амп. - 1 мл 2,5% р-ра
Амп. по 1,5 мл 1% р
ра
В/в по 0,002 г/кг
Амп. по 5 и 10 мл 2%
р-ра
П/к, в/м по 0,0003-0,001 г, в/в Амп. по 1 мл 0,1% ркапельно (0,3-1 мл 0,1% р-ра. ра. фл. по 10 мл 0,1%
р-ра
В/в капельно по 4-8 мг (2-4 мл Амп. по 1 мл 0,2% р0,2% р-pa)
ра.
Внутрь по 0,01-0,025 г, п/к и
в/м - 0,003-0,005 г, в/в - 0,0010,003 г.
Внутрь, п/к, в/м и в/в по 0,025
г.
Ингаляционно по 0,2 мг в
форме аэрозоля.
Ингаляционно по 0,1 мг,
внутрь по 2-4 мг
Внутрь по 0,5-1 мг.
Порошок, амп. по 1
мл 1% р-ра
Эфедрина гидрохлорид (Epnedrini
Пор., таб. по 0,025 г
hydrochloridum), Ерhаlonе и др.
амп. - 1 мл 5% р-ра
Фенотерол (Fenoterolum), Berotec,
Аэрозол. баллоны
Partusisten.
(300 доз)
Сальбутамол (Satbutamolum).
Аэрозол. балл (200
Ventolinum и др.
доз), таб. по 2 и 4 мг
Празозин (Prasosinum). Adversuten,
Таб. по 1 и 5 мг
Deprasolin, Minipress, Pratsiol.
Анаприлин (AnapriIinum). Inderal,
Внутрь по 0,01-0,04 г
Таб. по 0,01 и 0,04 г
Obsidan, Propranolol и др.
Талинолол (ТаIinoIоIum). Cordanum. Внутрь по 0,05 г.
Драже по 0,05 г
Резерпин (Reserpinum). Rausedyl,
Внутрь по 0,1-0,25 мг.
Пор., таб. по 0,1 и 0,25
Serpasil и др.
мг.
Октадин (Octadinum). Guanethidini
Внутрь по 0,025-0,05 г
Пор., таб. по 0,025 г
sulfas, Isinelin, Isobarin и др.
Средства, влияющие на центральную нервную систему.
Эфир для наркоза (Aether pro
Ингаляционно
Флаконы по 100 мл
narcosi). Anesthetic Ether.
Фторотан (Phthorotanum).
Ингаляционно.
Флаконы по 50 мл.
Halothanum, Fluothane.
Тиопентал-натрий (ThiopentalurnВ/в по 0,4-0,6 г.
Флаконы по 0,5 и 1 г
natrium). Pentothal sodium и др.
В/в по 2-3 мг/кг, в/м по 4-8
Амп. по 2 и 10 мл 5%
Кетамина гидрохлорид (Ketamini
мг/кг.
p-ра
hydrochloridum). Kalipsol, Ketalar и
др.
Пор., амп. по 10 мл
Натрия оксибутират (Natrii
В/в по 70-120 мг/кг, в/м по
oxybutyras). Oxybat sodium.
120-150 мг/кг, внутрь -100-200 20% р-ра, флаконы
мг/кг.
Фенобарбитал (Phenobarbitalum).
Внутрь по 0,1 г.
Пор., таб. по 0,05 и 0,1
Luminal и др.
г.
Внутрь по 0,1-0,2 г.
Порошок.
Эгаминал-натрий (Aetnaminalumnatrium). Nembutal natrium,
Pentobarbitalum natricum и др.
Внутрь по 0,01 г.
Таб. по 0,005 и 0,01 г
Нитразепам (Nitrazepamum).
Mogadon, Neozepam, Radedorm,
Eunoctin и др.
Хлоралгидрат (Chlorali hydras).
Внутрь и ректально по 0,5-1 г. Порошок.
Морфина гидрохлорид (Morphini
П/к по 0,01 г.
Амп. и шприц-тюбики
hydrochloridum).
по 1 мл 1% р-ра.
Промедол (Promedolum).
Внутрь по 0,025 г, п/к - 0,02 г.
Trimepiridini hydrochloridum.
Кислотa ацетилсалициловая (Acidum Внутрь no 0,25-0,5 г.
aceitylsalicylicum). Aspirin, Aspro,
Acesal
Анальгин (Analginum). Dipyrone,
Внутрь, в/м и в/в по 0,25-0,5 г.
Hunalgin и др.
Таб. по 0,025 г, амп.
по 1 мл 1-2% р-ра
Пор., таб. по 0,25 и 0,5
г
Пор., таб. по 0,5 г,
амп. по 1 и 2 мл 50%
р-ра
Внутрь по 0,025-0,05 г, в/м по Таб. по 0,025 и 0,015 г
Ортофен (Ortophenum). Diclofenacnatrium, Voltaren, Rewodina, Feloran и 0,075 г.
др.
Дифенин (Dipheninum) Phenytoinum, Внутрь по 1/2-1 таблетке
Таблетки
Dihydantoin
Карбамазепин (Carbamazepinum).
Внутрь по 0,2-0,4 г.
Таб. по 0,2 г
Finlepsin, Tegretol
Циклодол (Cyclodolum)
Внутрь по 0,001-0,005 г
Таб. по 0,001, 0,002 и
Trihexyphenidini hydrochloridum
0,005
Леводопа (Levodopum). Avodopa,
Внутрь по 0,25-1 г
Капс. и таб. по 0,25 и
Dopaflex и др.
0,5 г
Наком (Nakom). "Sinemet".
Внутрь по 1/2-1 таб.
Таблетки.
Внутрь по 0,025-0,1 г, в/м и
Др. по 0,025, 0,05 и
Аминазин (Aminazinum).
в/в по 0,1 и 0,025 г
0,1 г, амп. - 1, 2, 5 и 10
Chlorpromazini hydrochloridum,
Largactil, Hibernal и др.
мл 2,5% р-ра
Трифтазин (Тriftazinum). Stelazine,
Внутрь по 0,005 г, в/м по
Таб. по 1,5 и 10 мг,
Influoperazini hydrochloridum и др.
0,001-0,002 г
амп. по 1 мл 0,2% р-ра
Галоперидол (Наloperidolum).
Внутрь по 0,5-1 мг, в/м по 2-5 Таб. по 1, 5 и 5 мг,
Galophen, Haloperidin и др.
мг.
амп - 1 мл 0,5% р-ра.
Сибазон (Sibazonum). Diazepam,
Внутрь по 0,005-0,015 г, в/м и Таб. по 0,005 г, амп.
Seduxen, Relanium.
в/в по 0,01 г
0,5%-2 мл
Имипрамин (lmipraminum). Imizinum, Внутрь по 0,025-0,05 г, в/м - Таб. по 0,025 г, амп.
Melipramin
0,025 г
1,25% - 2 мл
Амитриптилин (Amitriptylinum).
Внутрь по 0,025-0,05 г, в/м и Taб.no 0,025 r, амп. - 2
Tepemin, Triptizol и др.
в/в по 0,025-0,04 г
мл 1%.
Пирацетам (Pyracetamum) Nootropil, Внутрь по 0,4 г, в/м и в/в по 1- Капс. по 0,4 г, таб. Piramem и др.
2 г.
0,2 г, амп. 20%-5 мл.
Кофеин-бензоат натрия (Coffeinum- Внутрь по 0,1-0,2 г, п/к по 0,1- Пор., таб. 0,1 и 0,2 г,
natrii benzoas)
0,2 г.
амп. 10 и 20% - 1-2 мл
Кордиамин (Cordiaminum).
П/к, в/м и в/в по 1 мл, внутрь Амп. по 1 и 2 мл, фл.
Nicethamidum
по 30 капель.
по15 мл
Бемeгрид (Bemegridum).
В/в по 0,01-0,025 г.
Амп. 0,5% - 10 мл
Камфора (Sol. Camphorae оIeosae
П/к по 0,2-1 г.
Амп. по 1 и 2 мл
20% pro injectionibus)
этимизол (Aethimizolum).
В/м и в/в по 0,03-0,06 г,
Амп. 1% и 5% - 3 и 5
внутрь по 0,1 г.
мл, таб. 0,1
Настойка валерианы (Tinct.
Внутрь по 20-30 капель
Фл. по 30 мл
Valerianae)
Настойка женьшеня (Tinct. Ginseng) Внутрь по 20-30 капель
Фл. по 50 мл
Средства, влияющие на функции органов дыхания
Кодеина фосфат (Codeini phosphas) Внутрь по 0,01-0,02 г.
Порошок.
Либексин (Libexin). Prenoxdiazin
Внутрь по 0,1 г.
Таб по 0,1 г.
Мукалтин (Mucaltinum)
Внутрь по 1-2 таб.
Таблетки.
Тpaвa термопсиса (Herba
Внутрь в виде настоя 1:200,
Трава, пор., таб.,
Thermopsidis)
пор. по 0,05 г и по 1-2 таб.
экстр.
Дезоксирибонуклеаза
Ингаляционно по 3 мл 0,2% р- Фл. по 5, 10, 25 и 50
(Desoxyribonucleasum)
pa
мг
Калия иодид (Kalii iodidum)
Эуфиллин (Euphyllinum).
Aminophyllinum, Diaphyllin
Внутрь по 0,3-1 г (1-3% р-р)
Внутрь по 0,1-0,2 г., в/м по
0,24-0,36 г, в/в - 0,12-0,24 г
Порошок
Пор., таб. 0,15, амп.
24% - 1 мл, 2,4% - 10
мл
Kanc. no 0,02 г
Кромолин-натрий (Cromolyn sodium). Ингаляционно по 0,02 г.
Intal, Sodium cromoglicate
Средства, влияющие на функции органов пищеварения
Настойка полыни (Тinct. Absinthii)
Внутрь по 15-20 капель
Фл. по 25 мл
Фепранон (Phepranonum).
Внутрь по 0,025 г.
Др. по 0,025 г
Amfepramonum и др.
Кислота хлористоводородная развед. Внутрь по 10-15 капель
Флаконы
(Асidum hydrochloricum dilutum)
Пепсин (Pepsinum).
Внутрь по 0,2-0, 5 г.
Порошок
Магния окись (Magnesii oxydum)
Внутрь по 0,25-1 г
Пор., таб. 0,5 г
Де-нол (De-Nol). Вiscolcitrat
Внутрь по 1-2 таб.
Таб. по 0,12 г
Ранитидин (Ranitidine). Aciloc,
Внутрь по 0,15 г
Таб. по 0,15 г
Anistal, Raniplex и др.
Таб. "Холензим" (Tаb.
Внутрь по 1 таб.
Таблетки
"Cholenzymum")
Оксафенамид (Oxaphenamidum)
Внутрь по 0,25-0,5 г
Таб. по 0,25 г
Панкреaтин (Pancreatinum)
Внутрь по 0,5-1 г
Пор., таб. 0,5 г.
Контрикал (Contrycal)
В/в по 10000-20000 ЕД
|Фл. no 10000, 30000,
50000 ЕД
Магния сульфат (Magnesii sulfas)
Внутрь по 10-30г, в/м и в/в по Пор., амп. 20 и 25% 5-20 мл 20-25% р-ра
5,10, 20мл.
Масло касторовое (Oleum Riсini)
Внутрь по 15-30 г (15-30
Фл. по 30, 50 мл, капс.
капсул)
по 1 г
Фенопфталеин (PhenoIphtalеinum).
Внутрь по 0,1-0,2 г
Таб. по 0,1 г
Laxin, Purgophen
aпоморфина гидрохлорид
П/к no 0,002-0,005 г
Пор., амп. 1% - 1 мл
(Apomorphini hydrochloridum)
Этаперзин (Aethaperazinum).
Внутрь по 0,004-0,01 г
Таб. по 0,004, 0,006 и
Perphenazini hydrochloridum
0,01г.
Примечание: при выписывании ЛС в рецептах студент должен знать их групповую
принадлежность, основной МД, особенности фармакокинетики и фармакодинамики, показания и
противопоказания, ПЭ; уметь рассчитать дозы для больных пожилого и старческого возраста, и
детей разного возраста.
СОДЕРЖАНИЕ
Лекция 1. Введение. Основные понятия общей фармакологии
1
Лекция 2. Основные понятия общей фармакологии (продолж.)
8
Лекция 3. ЛС, действующие на афферентную иннервацию: местноанестезирующие средства, вяжущие
средства, обволакивающие средства, адсорбирующие средства, мягчительные средства,
раздражающие средства
17
Лекция 4. ЛС, влияющие на эфферентную иннервацию: холиномиметические средства
22
Лекция 5. Холиноблокирующие ЛС
27
Лекция 6. Адренергические средства: адреномиметические ЛС
33
Лекция 7. Антиадренергическне средства: адреноблокирующие ЛС, симпатолитические ЛС
37
Лекция 8. Средства, регулирующие функции ЦНС: средства для наркоза
40
Лекция 9. Спирт этиловый. Снотворные срвдства
46
Лекция 10. Наркотические анальгетики
51
Лекция 11. Ненаркотические анальгетики, жаропонижающие, противовоспалительные средства 55
Лекция 12. Противоэпилептические ЛС. Противопаркиисонические
58
Лекция 13. Психотропные средства: нейролептические средства, средства для лечения маниакальных
состояний, транквилизаторы, седативные средства, антидепрессанты
61
Лекция 14. Стимуляторы центральной нервной системы: психостимуляторы, ноотропные средства,
общетонизирующие средства, психодислептики
67
Лекция 15. Средства, регулирующие функции органов дыхания: средства для лечения
бронхообструктивных зааболеваний
72
Лекция 16. Средства, регулирующие функции органов дыхания: противокашлевые и отхаркивающие
средства, стимуляторы дыхания, средства для лечения отека легких
77
Лекция 17. Средства, регулирующие функции органов пищеварения
84
Приложения. Вопросы для подготовки к экзамену по фармакологии
91
Лекарственные препараты, которые необходимо уметь выписать в рецептах на экзамене по
фармакологии
95
Содержание
100
Профессор А.И. Бекетов. Курс лекций по фармакологии (учебно-методическое пособие для
отечественных и иностранных студентов). Часть II. 2-е издание (переработанное и дополненное), г.
Симферополь, 1997 г. 127 стр.
Во 2-й части лекционного курса представлены разделы частной фармакологии в соответствии с
Учебной Программой для студентов медицинского и стоматологического факультетов. Лекции в
кратком изложении содержат современные представления о механизмах действия лекарственных
средств, особенностях их фармакокинетики и фармакодинамики, показаниях и противопоказаниях для
применения в медицинской практике и возможных осложнениях лекарственной терапии. Даны также
некоторые сведения о патогенетических механизмах патологических состояний, необходимые для
понимания возможных направлений фармакологического воздействия на заболевание и рационального
выбора препаратов. При подготовке лекций автор использовал опыт преподавания клинической
фармакологии и фармакотерапии, позволившей выделить вопросы, имеющие фундаментальное
значение для формирования врача. В начале каждой лекции выделены основные вопросы, помогающие
студентам сразу получить представление о ее содержании. В приложении к лекциям даны
экзаменационные вопросы и список препаратов, которые студенты должны уметь выписать на экзамене
по фармакологии и на выпускных государственных экзаменах. Кроме основного названия препарата
указаны синонимы, наиболее часто используемые в иностранных справочниках и фармацевтическими
фирмами.
Условные обозначения:
ЛС
- лекарственное средство
ЛВ
- лекарственное вещество
МД - механизм действия
ПЭ
- побочные эффекты
В/в
- внутривенно
В/м - внутримышечно
П/к - подкожно
Пор. - порошок
Таб. - таблетка
Др.
- драже
Амп. - ампула
Фл. - флакон
Р-р
- раствор
ФК - фармакокинетика
ССС - сердечно-сосудистая система
ЧСС - частота сердечных сокращении
АД
- артериальное давление
ЭКГ - электрокардиограмма
ЦНС - центральная нервная система
ГЭБ - гемато-энцефалическии барьер
ЖКТ - желудочно-кишечный тракт
ХР
- холинорецептор
АР
- адреиорецептор
КОС - кислотно-основное состояние
ВЭБ - водно-электролитный баланс
Ф-ция - функция
Д-вие - действие
ФД - фармакодинамика
Лекция 18
СЕРДЕЧНЫЕ ГЛИКОЗИДЫ
Сердечные гликозиды — вещества растительного происхождения, обладающие кардиотоническим
действием. Они являются основными ЛС, используемыми при лечении острой и хронической сердечной
недостаточности, поэтому значение этих препаратов очень велико.
Вам необходимо овладеть следующими знаниями:
* история открытия и внедрения в практику сердечных гликозидов;
* — источники получения сердечных гликозидов и их химическое строение:
* — фармакокинетические особенности различных гликозидов н их значение;
* — классификация препаратов сердечных гликозидов;
* — фармакодннамика сердечных гликозндов: МЛ и основные эффекты;
* — критерии оценки терапевтического действия сердечных гликозидов;
* — основные принципы назначения и дозирования сердечных гликозидов;
* — взаимодействие сердечных гликозидов с другими средствами;
* интокснкация сердечными гликозидами, профилактика и лечение.
Сердечные гликозиды содержатся во многий растениях: наперстянка (пурпурная, шерстистая,
ржавая, реснитчатая, крупноцветная), строфант, ландыш, горицвет, желтушник и др. В народной
медицине используются давно. В России наперстянку начали выращивать с 1730 г. Лечебные свойства
наперстянки впервые описал и внедрил ее а практику английский врач и ботаник Уитеринг в 1785 г.
Большой вклад в изучение сердечных гликозидов внесли русские ученые. В 1865 г. Е. П. Пеликан
изучил действие строфанта на сердце. Действие горицвета исследовав Н. А. Бубнов, а действие
ландыша — Н. П. Богоявленский в лаборатории И. П. Павлова при клинике С. П. Боткина (1880–1881
гг). Н. Д. Стражеско в 1910 г. внедрил в клиническую практику строфантин. В СССР изучением
сердечных гликозидов широко занимались А. И. Черкес и его школа фармакологов (И. С. Чекман и др.).
Молекула сердечных гликозидов состоит из двух частей: сахаристой (гликон) и несахаристой
(агликон, генин). Агликон имеет стероидную структуру и обеспечивает специфическое действие на
миокард, Глюкон представляет различные сахара и определяет фармакокинетические особенности
гликозидов (растворимость, всасывание, проникновение через мембраны, связывание с белками,
распределение, выведение) и, следовательно, влияет на активность и токсичность. Основными
гликозидами являются дигитоксин (из наперстянки пурпурной), дигоксин (из наперстянки шерстистой),
строфантин (из строфанта), комваллатоксин (из ландыша).
фармакокинетика. Всасывание в ЖКТ прямо зависит от растворимости в липидах: чем выше
растворимость, тем полнее всасывание (дигитоксин — 95–100%, дигоксин — 50–80%, целанид — 20–
40%, строфантин и коргликон — 2–5%). Поэтому дигитоксин целесообразно вводить через рот,
дигоксин и целанид можно назначать как внутрь, так и парэнтерально, строфантин и коргликон —
только парэнтерально. Внутрь назначают также препараты горицвета — настой травы, адонизид.
Всасывание гликозидов зависит от ряда факторов и может отличаться у разных больных в 2–3 раза.
Всасывание ухудшается при приеме во время еды или сразу после нее, при гиповитаминозах,
нарушениях кровообращения, заболеваниях ЖКТ, печени, под влиянием некоторых ЛС (антациды,
содержащие алюминий, тетрациклины, аминогликозиды, слабительные, ганглиоблокаторы, мхолиноблокаторы). Галеновые препараты (порошки, настои, настойки), а также неогаленовые
всасываются хуже, чем чистые гликозиды.
При парэнтеральном введении препараты гликозидов необходимо разводить изотоническим
раствором натрия хлорида или 5–10% раствором глюкозы. Гипертонические растворы глюкозы (20–
40%), натрия гидрокарбонат, аскорбиновая кислота инактивируют глюкозиды, поэтому несовместимы с
ними. Сердечные гликозиды обладают сильным раздражающим действием и при введении под кожу
или в мышцу вызывают резкую боль, а при повторных введениях — дегенерацию ткани. Поэтому эти
пути введения используют редко, предварительно вводя в место инъекции 1–2% раствор новокаина.
В крови сердечные гликозиды связываются с белками в зависимости от полярности молекул: чем
меньше полярность, тем больше связь (у дигитоксина — 97%, у дигоксина и целанида — 15–30%,
строфантин и коргликон практически не связываются). Поэтому строфантин и коргликон быстро
покидают сосудистое русло и проникают в миокард, действуя быстро. Действие гликозидов
наперстянки развивается постепенно по мере отщепления от молекул белка и проникновения в миокард.
Наиболее медленно этот процесс развивается при применении дигитоксина. Этим объясняется разная
продолжительность латентного периода действия гликозидов.
При гипопротеинемии (болезни печени, почек, дистрофия) связь с белками снижается и возрастает
свободная фракция гликозида, в результате чего повышается его токсичность, В таких случаях лучше
использовать строфантин или коргликон, действие которых не зависит от содержания белков крови.
Некоторые вещества (бутадион, сульфаниламиды, фенобарбитал, бутамид, неодикумарин, холестерин,
свободные жирные кислоты) могут вытеснять гликозиды из связи с белками, что также увеличивает
опасность интоксикации.
Терапевтические и токсические эффекты гликозидов определяются их концентрацией в миокарде,
которая зависит от растворимости в липидах и связывания с белками тканей. Дигитоксин поглощается
миокардом в 6 раз больше, чем строфантин. Поскольку он образует более прочные связи с белками,
выведение его из миокарда происходит значительно медленнее, чем других гликозидов. С этим связаны
продолжительность эффекта и способность к кумуляции.
Элиминация (обезвреживание) гликозидов происходит в печени и почках. Строфантин и коргликон
практически не подвергаются биотрансформации и выделяются с желчью до 90% в неизмененном виде.
Так как они всасываются в ЖКТ плохо, то почти полностыо выводятся с каловыми массами. Патология
почек мало влияет на их кинетику, но при нарушении желчевыделительмой функции может возникнуть
кумуляция. Дигоксин преимущественно выводится с мочой в неизмененном виде, поэтому при
нарушений выделительной функции почек его действие усиливается и возрастает опасность кумуляции.
Дигитоксин инактивируется в печени и выводится в виде метаболиитов и конъюгатов, поэтому для его
обезвреживания основное значение имеет состояние печени.
Классификация сердечных гликозидов основана на особенностях их фармакокинетики. Их
подразделяют на 3 группы: 1) гликозиды быстрого, но непродолжительного действия (строфантин,
коргликон); 2) гликозиды средней продолжительности действия (дигоксин, целанид); 3) гликозиды
длительного действия (дигитоксин). Сравнительная характеристика гликозидов приведена в таблице.
Назван Всасы Латентный
период
вание
ие
гликоз в ЖКТ
ида
(%) Внутрь в/в
Развитие
максимума
эффекта
Внут
в/в
рь
30–90
5–10 не
Строфа 2–5
не
нтин
примен мин прим мин
еняю
.
Коргли 2–5
т
кон
Дигокс 50–80 0,5–2 ч 15–30 6–8 1–6 час
ин
мин час
Дигито 90–100 2–4 ч
ксин
30–60 8–12 4–12
мин час
час
Выведение гликозида
за 24 ч ПП полное
(КЭ)
85–90% 8 час 1–2
дня
20–30% 34–
46
час
7–10% 8–9
дней
2–7
дней
До 21
дня
КЭ — коэффициент элиминации (количество обезвреженного гликозида за 24 часа, выраженное в %
от введенной дозы); ПП — период полувыведения (время, в течение которого концентрация ЛВ в крови
снижается на 50%).
Данные, представленные в таблице, показывают, что наиболее длительно задерживается в организме
дигитоксин, поэтому он обладает высокими кумулятивными способностями, что необходимо учитывать
при его назначении. Способность накапливаться в организме менее выражена у дигоксина и слабо
проявляется у строфантина и коргликона. По длительности действия и способности к кумуляции
глинозиды можно расположить в следующем порядке: дигитоксин > дигоксин > целанид > строфантин
> коргликон > адонизид.
Фармакодинамика. Основным свойством гликозидов является их избирательное действие на
сердце, которое характеризуется 5 основными эффектами: 1) положительное инотропное действие
(усиление и укорочение систолы); 2) отрицательное хронотропное действие (удлинение диастолы и
урежение сердечных сокращений); 3) отрицательное дромотропное действие (замедление проведения
импульсов по проводящим путям сердца); 4) положительное тонотропное действие (повышение тонуса
миокарда и уменьшение размеров дилатированного сердца);
5) положительное батмотропное действие (повышение возбудимости миокарда).
Наиболее ценным свойством гликозидов является первичное кардиотоническое (инотропное)
действие, в результате чего возрастает коэффициент полезного действия миокарда и уменьшается или
ликвидируется сердечная недостаточность. Систола становится более быстрой и мощной. Это
сопровождается увеличением ударного и минутного объема сердца. Систолический эффект гликозидов
на ЭКГ проявляется увеличением амплитуды зубца К, укорочением комплекса QRS и интервала Q–Т,
снижением S–Т ниже изоэлектрической линии, уменьшением или инверсией зубца Т.
Кардиотонический эффект гликозидов обусловлен влиянием на обменные процессы в сердечной
мышце. Считают что МД гликозидов связан первично с угнетением транспортной Nа+-К+-АТФ-азы
мембран кардиомиоцитоа, что приводит к увеличению концентрации ионов натрия внутри клетки и
снижению содержания ионов калия. Это сопровождается, увеличением входа ионов кальция в клетки и
высвободения их из депо в саркоплаэматическом ретикулюме внутри клеток. Повышение концентрации
Са++ ослабляет тормозное влияние тропонинового комплекса на сократительный белок (актомиозин)
миокарда, что проявляется усилением сокращения мышечных волокон. Происходит сдвиг соотношения
концентраций натрия и калия, кальция и калия в пользу первых. Если этот сдвиг не выходит за пределы
нормальных границ, работа сердца улучшается. Увеличение концентрации Са++ выше нормы и
снижение калия (гипокалигистия) в миокарде сопровождается развитием интоксикации.
Под влиянием Са++ увеличивается высвобождение катехоламинов из симпатических окончаний и
депо, усиливается гликогенолиз, процессы окислительного фосфорилирования, образование макроэргов
(АТФ, креатиифосфат) и их утилизация, улучшается утилизация молочной кислоты. При интоксикации
содержание АТФ, креатинфосфата, гликогена, наоборот, падает. Гликозиды вызывают сдвиг
окислительных процессов в сторону аэробного гликолиза, в результате чего улучшается утилизация
кислорода и повышается коэффициент полезного действия сердца (отношение полезной работы к
потребленному кислороду). Происходит разрыв порочного круга.
Отрицательное хронотропное действие проявляется в удлинении диастолы и урежении сердечных
сокращений. Это имеет важное значение, так как увеличивается время отдыха сердечной мышцы и
наполнение кровью сердца. МД связан с усилением влияний вагуса в результате раздражения
барорецепторов дуги аорты возросшей систолической волной и окончаний чувствительных нервов в
сердце самим гликозндом, что приводит к рефлекторному возбуждению центра вагуса. Определенное
значение имеет ослабление рефлекторных влияний с устьев полых вен (рефлекс Бейнбриджа) в
результате снижения венозного давления.
Отрицательный дромотропный эффект (замедление проводимости) связан с прямым действием
гликозидов на атрио-вентрикулярный узел и пучок Гиса, а также с возбуждением вагуса. Он имеет
значение при наличии мерцательной аритмии, так как усиливает фильтрацию импульсов, угнетая
проведение беспорядочных импульсов из эктопических очагов возбуждения в предсердиях.
Положительный тонотропный эффект связан непосредственно с инотропным и проявляется в
укорочении нитей миофибрилл и уменьшении размеров дилатированного сердца, что имеет
положительное значение для его кровоснабжения и метаболизма.
Сердечные гликозиды повышают возбудимость миокарда (положительный батмотропный эффект).
Однако в больших дозах они снижают возбудимость и повышают автоматизм сердца, что приводит к
образованию эктопических очагов возбуждения, посылающих импульсы независимо от синусного узла,
и возникновению аритмии (экстрасистолия).
Критерием лечебного действия гликозидов является уменьшение или исчезновение признаков
сердечной недостаточности, увеличение ударного и минутного объема, нормализация пульса,
повышение пульсового АД, урежение сердечного ритма до 55–60 в 1 мин, нормализация АД и
снижение центрального венозного давления, исчезновение отеков, одышки, цианоза, увеличение
суточного диуреза, снижение массы тела, нормализация ЭКГ.
Применение сердечных гликозидов. Показанием для назначения является наличие или угроза
возникновения острой, и хронической сердечной недостаточности. Однако применение их должно быть
строго обоснованным, нешаблонным и под тщательным врачебным контролем. Гликозидная терапия
включает 2 фазы: насыщения и поддержания.
1. Фаза насыщения преследует цель обеспечить быстрое. создание оптимальной концентрации
гликозида в сердце, т.е. полной терапевтической дозы (ПТД). ПТД для строфантина составляет 0,6 мг,
для дигитоксина — 2 мг, для дигоксина — 3 мг внутрь и 2 мг в/в. Для достижения фазы насыщения
используют 3 темпа: а) быстрый — 1–1,5 сутки; б) средний — 3–5 суток; в) медленный — 5–7 суток.
Для быстрого темпа насыщения используют преимущественно строфантин или коргликон, реже —
дигоксин. Ои применяется при возникновении острой сердечной недостаточности. ПТД вводят в/в в
течение 24–36 ч в 3 приема. При среднем темпе используют дигоксин. реже строфантин или коргликон,
ПТД которых вводят по схеме за 3–5 суток. Медленный темп насыщения обычно осуществляют
дигитоксином или дигоксином, которые назначают внутрь по схеме в течение 5–7 суток.
2. Фаза поддержания имеет целью стабилизацию достигнутого лечебного эффекта с помощью
поддерживающих доз (ПД). ПД определяют на основании коэффициента элиминации (см. таблицу) по
формуле:
ПД= ИТД х КЭ / 100
Например. ПТД дигоксина равна 3 мг, КЭ =20%; ПД, следовательно, будет равна 0,6 мг. Эту дозу
после достижения насыщения назначают ежедневно в 1–2 приема. Так как поддерживающая терапия
проводится длительно, предпочтение отдают дигитоксину и дигоксину, которые хорошо всасываются а
кишечнике.
Основой рациональной терапии является насыщение глнкозидами до уровня индивидуальной
оптимальной потребности. Фазу насыщения необходимо проводить в стационаре под тщательным
контролем, помня, что у разных больных индивидуальная ПТД может отличаться от ПТД препарата.
Поэтому нужно руководствоваться прежде всего клиническими данными.
При назначении сердечных гликозидов детям необходимо учитывать некоторые особенности,
которые проявляются преимущественно до 3 лет.
1. У детей раннего возраста отсутствует или слабо выражено ваготропное действие гликозидов, так
как тоническое возбуждение вагуса проявляется только к 2,5–3 годам. Поэтому бесплодно и опасно
добиваться у них брадикардии как у взрослых. Урежение ритма не должно быть ниже 90–100 в 1 мин.
2. У новорожденных (до 1 мес), особенно у недоношенных, чувствительность к гликозидам
повышена и легко возникают тяжелые нарушения ритма сердца.
3. У детей раннего возраста концентрация гликозидов в миокарде нарастает значительно быстрее,
чем у взрослых благодаря функции тебезиевых вен и рыхлости миокарда. В то же время толераитность
миокарда к гликозидам выше, чем у взрослых. Поэтому для достижения терапевтического эффекта
необходимо создавать более высокие концентрации в плазме крови, что приводит к уменьшению
широты терапевтического действия и повышает риск интоксикации. Так, оптимальная концентрация
дигоксина в крови у детей до 2 лет равна 30 нг/мл, а у взрослых — 24 нг/мл; поддерживающая доза
равна соответственно 0,004 мг/кг и 0,0014 мг/кг.
Взаимодействие сердечных гликозидов с другими ЛС. Они являются частью комплексной
терапии сердечной недостаточности. Если она развивается на фоне пневмонии или других тяжелых
инфекций,
гликозиды сочетают
с
противомикробными
средствами,
витаминотерапией,
противогистаминными и др. При наличии миокардита их применяют совместно со стероидными и
нестероидными противоспалительными средствами. При тяжелых отеках используют диуретики.
Кортикостероиды, диуретики (за исключением калийсберегающих) способствуют выведению калия,
что усиливает токсические эффекты гликозидов. Для устранения дефицита калия назначают препараты
калия (калия хлорид, аспаркам, панангин, калия оротат), пищевые продукты, богатые калием (печеный
картофель, сушеные фрукты и др.). Эффективность гликозидов повышают анаболические ЛС,
усиливающие синтез белка, витамины группы В (тиамин, пиридоксин, цианокобаламин, фолиевая
кислота), витамины А, С, Е, кокарбоксилаза. стимулирующие белковый, углеводный, липидный обмен,
окислительно-восстановительные процессы и энергообразование, ингаляция кислорода, уменьшающая
гипоксию миокарда.
Интоксикация сердечными гликозидами обычно развивается при неправильном дозировании,
повышенной чувствительности, при комбинировании с препаратами, вызывающими гипокалиемию, с
препаратами кальция. Механизм развития токсического эффекта связан с резким угнетением
транспортной АТФ-азы, результатом чего является избыточная потеря К+ клетками миокарда и
чрезмерное повышение концентрации Са++. Это приводит к нарушению мембранных процессов
(поляризации и деполяризации), угнетению обмена веществ. Функция миокарда ослабевает и
усиливается сердечная недостаточность. Резко угнетается проводимость, может развиться блокада
сердца. Повышение автоматизма вызывает появление множественных эктопических очагов
возбуждения и нарушений сердечного ритма. Эти эффекты усиливаются нейротропными влияниями:
перевозбуждение вагуса, выделение избыточного количества катехоламинов.
Симптомы интоксикации подразделяют на следующие группы: 1) кардиальные — нарушения ритма
(экстрасистолия). резкая брадикардия, затем тахикардия, признаки атрио-вентрикулярной блокады на
ЭКГ, нарастание сердечной недостаточности; 2) диспептические расстройства — потеря аппетита,
тошнота, рвота, боли а животе; 3) нарушение зрения — ксантопсия (окраска предметов в желтый цвет),
нарушение восприятия размеров тел, появление колец или шаров перед глазами (связаны с невритом
зрительного нерва); 4) нервно-психические — слабость, бессоница, головная боль, головокружение,
спутанность сознания, нарушение речи,
Неотложная помощь при интоксикации. Необходимо отменить препарат, промыть желудок,
назначить внутрь активированный уголь, солевое слабительное. Для химической нейтрализации
гликозида назначают унитиол в/м. Для восполнения потери калия применяют калия хлорид, аспаркам,
панангин, калия оротат, раствор глюкозы с инсулином для лучшего проникновения калия в клетки.
Избыток кальция можно нейтрализовать введением натрия цитрата, этиленаминтетрауксусной кислоты
(ЭДТА), тетацина-кальция. Для нормализации ритма сердца применяют лидокаин, верапамил, этмозин,
дифенин.
Неудачи при лечении сердечными гликозидами чаще всего бывают при неправильном подборе доз и
нарушении принципов гликозидной терапии. Отсутствие успеха может быть связано с тем, что резервы
миокарда исчерпаны, а тяжелые нарушения электролитного баланса приводят к интоксикации уже
после первых приемов гликозида. Повышенная чувствительность к гликозидам бывает при активном
ревматизме, при синих врожденных пороках сердца у детей (стеноз устья легочной артерии, тетрада
Фалло). При инфекционно-аллергическом миокардите, наоборот, нередко наблюдается резистентность
к гликозидам.
Сердечные гликозиды противопоказаны при нарушении сердечной проводимости, блокаде атриовентрикулярного узла, аритмии желудочков, дефиците калия.
Лекция 19
ПРОТИВОАРИТМИЧЕСКИЕ СРЕДСТВА
Нарушения ритма сердца — одно из наиболее частых и тяжелых осложнений заболеваний сердечнососудистой системы. Напр.. при инфаркте миокарда они возникают в 90% случаев. Аритмии нередко
появляются и при других видах патологии: тяжелые травмы, операции на крупных сосудах и легких,
интоксикации, наркоз фторотаном и циклопропаном, психоэмоциональное перенапряжение и т.п.
Особенно опасны желудочковые аритмии, которые требуют немедленной интенсивной терапии.
Причины нарушений сердечного ритма разнообразны: нарушения электролитного баланса в миокарде,
ишемия миокарда, ацидоз, тиреотоксикоз, повышенный тонус симпатической системы, микробные
токсины и др.
В лекции будут рассмотрены следующие вопросы:
* основные механизмы нарушении сердечного ритма;
* классификация противоаритмнческих средств по механизму действия;
* — характеристика ЛС, оказывающих прямое противоаритмическое действие на сердце;
* — МД, ФД, ФК, применение и ПЭ мембраностабилизируюших (мембраноденрессивиых) ЛС,
антагонистов кальция, амиодарона, препаратов калия и сердечных гликозидов;
* — МД, фармакологические эффекты и применение адренергических средств при нарушениях
сердечного ритма;
* — механизмы протнвоаритмического действия и применение холииергических ЛС при аритмиях
сердца.
Различают следующие виды аритмий: а) аритмии, связанные с нарушением автоматизма синусного
узла (синусовые тахикардия, брадикардия и аритмия); 6) аритмии, вызванные повышением
возбудимости миокарда и появлением эктопических очагов, посылающих беспорядочные импульсы
(экстрасистолия, пароксизмальная тахикардия); в) аритмии, возникающие при нарушениях
проводимости и блокаде импульсов (синоаурикулярные, атриовентрикулярные и внутрижелудочковые
нарушения проводимости); г) смешанные формы аритмий, когда причиной является одновременное
нарушение нескольких функций сердца — автоматизма, возбудимости и проводимости (мерцательная
аритмия и др.).
Развитию аритмий способствуют следующие факторы: а) нарушения функции естественного
водителя ритма (синусного узла) или появление эктопических водителей ритма в миокарде; б)
увеличение скорости деполяризации мембран; в) снижение потенциала покоя мембран и г) снижение
порога потенциала действия. Эти изменения характеризуют нарушения автоматизма и возбудимости.
Для нарушений проводимости характерно медленное нарастание потенциала действия и развитие блока
импульсов. Замедление проводимости предсердно-желудочковом узле на ЭКГ характеризуется
увеличением интервала Р–R, а внутри желудочков — длительности QRSТ.
Для возникновения экстрасистолии важное значение имеет укорочение эффективного рефрактерного
периода, под которым понимают минимальное время между двумя стимулами, вызывающими
потенциалы действия (распространяющееся возбуждение). Это сопровождается, укорочением фазы
реполяризации и потенциала действия. На ЭКГ наблюдается укорочение интервала Q–Т.
Помимо метаболических и электролитных нарушений в миокарде аритмии могут возникать при
изменениях тонуса адренергической и холинергической иннервации. Так, при стимуляции бетаадренорецепторов ускоряется деполяризация, укорачиваются реполяризация и потенциал действия,
увеличивается проводимость импульсов. При стимуляции м-холинорецепторов наблюдаются
противоположные явления: снижение автоматизма и проводимости вплоть до развития предсердножелудочкового блока.
Таким образом, существуют два основных пути противоаритмического действия: 1)
непосредственное воздействие ЛС на миокард; 2) опосредованное воздействие ЛС через вегетативную
иннервацию. Классификация включает:
1.Средства прямого действия на миокард: а) мембраностабилизирующие (мембранодепрессивные)
ЛС (хинидина сульфат, новокаинамид, аймалин, этмозин, дизопирамид, лидокаин, дифенин; б)
блокаторм кальциевых каналов (верапамил); в) средства, удлиняющие потенциал действия (амиодарон);
г) разные средства — препараты калия (калия хлорид, аспаркам, панангин), сердечные гликозиды
(дигитоксин, дигоксин, целанид), комбинированные препараты (пульс-норма и др.).
2.Средства,
действующие
через
вегетативную
иннервацию
(опосредованно):
а)
антиадренергические — в-адреноблокатора (анаприлин, метопролол, талинолол, окспренолол и др.);
симпатолитики (орнид); б) адреномиметики и симпатомиметики (изадрин, орципреналин, адреналина
гидрохлорид, эфедрина гидрохлорид); в) м-холиноблокаторы (атропина сульфат); г) холиномиметики
(прозерин, эдрофоний).
Как видно из классификации, большинство препаратов имеют широкий спектр применения. Лишь
хинидин, новокаинамид, аймалин, дизопирамид и этмозин используются только при аритмиях.
Препараты прямого действия на миокард
Оказывают влияние на основные функции сердца, нарушение которых приводит к развитию
аритмии. Они угнетают автоматизм клеток в результате удлинения фазы деполяризации. Некоторые из
них угнетают проводимость за счет замедления процесса деполяризации в проводящих путях. Под
влиянием этих препаратов увеличивается эффективный рефракторный период и снижается
возбудимость. Все эти .эффекты имеют большое значение для устранения аритмий разного генеза.
Угнетение автоматизма препятствует активации синусно-предсердного узла и появлению эктопических
водителей ритма, что имеет важное значение для устранения синусной 1ахикардии, экстрасистолии и
пароксизмальной тахикардии, Угнетение проводимости препятствует распространению чрезмерно
высоких ритмов импульсов при тахиаритмиях. Снижение возбудимости способствует нормализации
процессов деполяризации-реполяризации и распространения возбуждения. Ряд препаратов (хинидин,
верапамил) снижают сократимость миокарда, что является нежелательным, так как ведет к ухудшению
кровообращения, особенно в тех случаях, когда имеется сердечная недостаточность.
Средства, стабилизирующие мембраны клеток (мембранодепрессанты)
МД этих препаратов недостаточно ясен. Стабилизация мембран приводит к уменьшению входа Nа+
через натриевые каналы, вследствие чего удлиняется потенциал действия и эффективный рефракторный
период.
Хинидин — алкалоид из коры хинного дерева, является правовращающим изомером хинина, но в
отличие от него не обладает противомалярийным действием. Хинидин влияет на все функции сердца:
угнетает автоматизм, проводимость и сократимость миокарда. В больших дозах хинидин может вызвать
резкое угнетение проводимости, вплоть до блокады, и ослабление работы сердца с развитием сердечной
недостаточности. Он обладает также м-холиноблокирующим и антиадренергическим действием,
затрудняя передачу импульсов с окончаний вагуса и ослабляя адренергические влияния на сердце.
Препарат используют в виде хинидина сульфата внутрь. Он всасывается хорошо, максимальная
концентрация в крови создается через 1–3 ч, продолжительность действия 6–8 ч. Биотрансформация
препарата происходит в печени, поэтому при его назначении надо учитывать функцию печени. Из
организма выводится через почки в виде метаболитов (80%) и в неизмененном виде (20%).
Эффективной концентрацией в крови считают 4–6 мг/л. Для быстрого купирования аритмии хинидин
вначале назначают (после проверки на переносимость) в повышенных дозах и с короткими
интервалами, а после достижения эффекта переходят на поддерживающие дозы. Этот принцип
соблюдают и при назначении других противоаритмических средств. Хинидин применяют при
тахиаритмиях (пароксизмальная тахикардия, частая экстрасистолия, постоянная мерцательная аритмия,
пароксизмы мерцательной аритмии). Он является наиболее эффективным препаратом при лечении
постоянной мерцательной аритмии. При передозиоовке и индивидуально повышенной
чувствительности к хинидину могут наблюдаться угнетение сердечной деятельности, тошнота, рвота,
понос, аллергические кожные реакции. Хинидин противопоказан при идиосинкразии к нему,
декомпенсации сердечной деятельности, коронарной недостаточности, при блокадах сердца,
эндомиокардитах.
Новокаинамид подобно хинидину оказывает мембраностабилизирующее действие, угнетая
трансмембранный перенос ионов Nа+ и К+. Он обладает также местноанестезирующими,
ганглиоблокирующими и гипотензивными свойствами. Хорошо всасывается а кишечнике и плохо
проникает в мозг. Максимальная концентрация в крови создается через 1–2 ч и снижается со скоростью
10–15% в час. Эффективная концентрация — 3–9 мг/л. Выводится почками, а основном, а
неизмененном виде, поэтому выделительная функция почек играет важную роль в его действии.
Назначают при пароксизмальной тахикардии, экстрасистолии, пароксизмальной форме мерцательной
аритмии и для профилактики аритмий. При постоянной мерцательной аритмии неэффективен.
Новокаинамид вводят внутрь, в/м и в/в, поэтому удобен для оказания экстренной помощи (в/в струйно
или капельно в 5% растворе глюкозы). При этом надо следить за уровнем АД и при развитии коллапса
вводить мезатон или норадреналии. По активности Новокаинамид уступает хинидину, но лучше
переносится, поэтому назначается а более высоких дозах. ПЭ: гипотензия, слабость, головная боль,
диспептические расстройства, аллергия. Противопоказания: блокада сердца, декомпенсация сердца,
выраженный атеросклероз, идиосинкразия.
Аймалин — алкалоид раувольфии с хинидиноподобным действием, но менее токсичен и мало влияет
на сократимость миокарда, рм увеличивает коронарный кровоток, слабо снижает АД. При приеме
внутрь всасывается плохо, поэтому лучше вводить парэнтерально. Период полувыведения — 15 ч.
Назначают преимущественно при предсердных аритмиях (экстрасистолия, пароксизмальная
тахикардия, пароксизмальная мерцательная аритмия предсердий), но неэффективен при постоянной
мерцательной аритмии, синусовой тахикардии и трепетании предсердий. Применяют также при
интоксикации гликозидами. инфаркте миокарда, после электроимпульсного лечения. ПЭ: гипотония,
слабость, тошнота, рвота.
Этмозин — производное фенотиазина с хинидиноподобнмм действием, но меньше угнетает
проводимость и сократимость. Оказывает м-холиноблокирующее и коронарорасширяющее действие, на
АД практически не влияет. Из кишечника всасывается хорошо, действие развирается быстрее, чем при
видении хинидина. Период полувыведения — 48 ч. Применяют при превдсердных и желудочковых
аритмиях, в том числе при интоксикации сердечными гликозидами. при пароксизмальной мерцательной
аритмии, пароксизмальной тахикардии, инфаркте миокарда. Малотоксичен, иногда вызывает тошноту,
головокружение, умеренную гипотензию.
Хинидиноподобными свойствами обладает также дизопирамид (ритмодан). Применяют при
экстрасистолиях, пароксизмальной тахикардии, для профилактики мерцания и трепетания предсердий.
Назначают внутрь и в/в (при инфаркте миокарда). Противопоказан кардиогенном шоке, тяжелой
сердечной недостаточности, атриовентрикулярной блокаде, выраженной гипотонии, почечной
недостаточности, аденоме простаты.
Лидокаин относится к местным анестетикам и рассмотрен в лекции, посвященной этим ЛС. По
своим эффектам он сходен с новокаинамидом, но практически не влияет на сократимость миокарда и не
изменяет АД. Преимущественно подавляет автоматизм в мышце и проводящей системе желудочков.
Поэтому его назначают при желудочковых аритмиях (экстрасистолия, тахикардия, возникающие при
инфаркте, после операций и т.п.). Вводят в/в (струйно или капельно) и в/м. При в/в введении действует
кратковременно (10–20 мин), так как быстро инактивируется в печени (при заболеваниях печени
действие усиливается). ПЭ: слабость, сонливость, гипотония и др. Обычно переносится хорошо.
Дифенин относится к группе противоэпилептических средств и рассмотрен в соответствующей
лекции. Противоаритмическое действие связано с мембранодепрессивным эффектом и влиянием на
ЦНС. Подобно хинидину он подавляет автоматизм клеток, но не влияет на проводимость и
сократимость. В большей степени его действие сходно с лидокаином (преимущественно на волокна
Пуркинье, желудочки сердца). Действие на ЦНС проявляется угнетением адренергических влияний на
сердце. Применяют при аритмиях желудочкового происхождения, особенно связанных с интоксикацией
сердечными гликозидами. Из кишечника всасывается медленно, но биодоступность высокая (около
98%). Период полувыведения — больше суток, поэтому препарат может кумулировать.
К блокаторам кальциевых каналов относятся фенигидин, дилтиазем, верапамил и др.
Противоаритмический эффект наиболее выражен у верапамила. МД связан с блокадой транспорта Са++
через медленные кальциевые каналы мембран, что приводит к снижению концентрации Са++ в клетках
миокарда и проводящей системы. Верапамил угнетает проводимость и увеличивает эффективный
рефракторный период в предсердмо-желудочковом узле, снижает автоматизм синусного узла,
уменьшает сократимость миокарда и расширяет коронарные сосуды. При приеме внутрь всасывается
хорошо, максимальный эффект развивается через 1,5–2 ч, период полувыведения — 3 ч.
Инактивируется в печени и выводится почками в виде конъюгатов. Применяют при пароксизмальной
тахикардии, мерцательной аритмии, связанных с повышенным тонусом симпатической системы, с
интоксикацией гликозидами, ишемией миокарда. Вводят Внутрь и в/м. ПЭ: брадикардия, гипотония,
углубление сердечной недостаточности, аллергические реакции.
Амиодарон (кордарон) занимает особое положение. Его МД связан с прямым действием на
мембраны и угнетением адренергических влияний на сердце, в результате чего происходит удлинение
потенциала действия и эффективного рефрактериого периода. Этот эффект проявляется в предсердиях,
атриовентрикулярном узле и желудочках, где снижаются автоматизм, возбудимость и проводимость.
Кроме того, он снижает потребность миокарда в кислороде, блокируя в-АР и глюкагоновые рецепторы.
Этот эффект используют при стенокардии. Из ЖКТ препарат всасывается на 50% и выводится через
кишечник. Применяют при предсердных и желудочковых аритмиях, особенно при пароксизмальной
тахикардии и трепетании предсердий. ПЭ: резкая брадикардия, атриовентрикулярный блок, окраска
кожи в серо-голубой цвет, отложение микрокристаллов в роговице глаза (обратимое), нарушение
функции щитовидной железы.
Препараты калия. Их используют при аритмиях, вызванных дефицитом калия (при применении
диуретинов, глюкокортикоидов, сердечных гликозидов). Ионы калия действуют подобно вагусу:
снижают автоматизм, возбудимость, проводимость и сократимость, уменьшают ЧСС. В кишечнике
калий всасывается полиостью и быстро выделяется через почки. Применяют калия хлорид (внутрь, в/в),
аспаркам и панангин, содержащие, помимо калия, аспарагииат магния, который способствует
проникновению и фиксации калия в сердце и усиливает его действие. Калия хлорид входит в состав
поляризующей смеси вместе с глюкозой и инсулином для улучшения проникновения в клетки сердца,
которую применяют при инфаркте миокарда, при интоксикации гликозидами и эктопических аритмиях.
Сердечные гликозиды (см. лекцию 18) нормализуют обмен в миокарде и оказывают
противоаритмическое действие при мерцательной аритмии, трепетании и мерцании предсердий,
пароксизмальной тахикардии. Эффект складывается из следующих факторов: 1) угнетение
проводимости, 2) повышение тонуса вагуса, в результате чего увеличивается эффективный
рефракторный период предсердий и замедляется синусовый ритм; 3) нормализация кровообращения и
водно-электролитного баланса, что ослабляет ускоряющие рефлекторные влияния на сердце,
реализуемые через адренергические нервы.
Средства, действующие через вегетативную иннервацню сердца
Стимуляция в-АР сердца сопровождается повышением возбудимости, проводимости, частоты и силы
сердечных сокращений. Поэтому при значительном повышении тонуса адренергической иннервации,
выделении больших количеств адреналина из надпочечников или повышении чувствительности сердца
к катехоламинам может возникнуть аритмия. В таких случаях эффективны в-адреноблокаторы. Из них
наибольшее значение имеет анаприлин (пропранолол, индерал, обзидан). Он снижает активность
синусного узла и эктопических очагов. Прямое мембраностабилизирующее действие у него проявляется
только в больших дозах. Анаприлин угнетает асе функции сердца: автоматизм, возбудимость,
проводимость и сократимость. Применяют при маджелудочковых и желудочковых тахиаритмиях (см.
лекцию7).
Из симпатолитиков используют орнид, который снижает активность синусного узла и угнетает
проведение импульсов в предсердно-желудочковом узле, существенно не влияя на сократимость
миокарда.
Так как стимуляция в-АР приводит к увеличению проводимости, при аритмиях, связанных с
нарушением атриовентрикулярного проведения импульсов, используют изадрин, орципреналин,
адреналин и эфедрин. Основным показанием для их назначения является предсердно-желудочковая
блокада. Их также используют при синусовой брадикардии (см. лекцию 6).
Наряду с адренергической иннервацией работа сердца регулируется холинергическим нервом
(вагусом), возбуждение которого сопровождается замедлением проведения импульсов в синусопредсердном и предсердно-желудочковом узлах, уменьшением сократимости сердца. Поэтому при
возникновении блокады этих узлов используют м-холииоблокаторы (атропин). При выраженном
снижении тонуса вагуса (напр., при наджелудочкоеых тахиаритмиях) используют хилиномиметики из
группы аитихолинэстеразных средств (прозерии, эдрофоний). С этой же целью можно применять
мезатон, который повышает АД и рефлекторно тонизирует вагус (см. лекции 4 и 5).
Таким образом, арсенал противоаритмических средств большой и важно уметь делать правильный,
выбор наиболее эффективного в данной ситуации препарата.
Лекция 20
АНТИАНГИНАЛЬНЫЕ СРЕДСТВА
К ним относятся препараты с различным МД, используемые для профилактики и лечения
стенокардии посредством уменьшения потребности миокарда в кислороде или улучшения его
кровоснабжения.
Стенокардия является наиболее распространенной формой ишемической болезни сердца. Различают
2 формы стенокардии: стенокардию напряжения и стенокардию покоя. По характеру течения
стенокардия может быть стабильной и нестабильной. Стабильная стенокардия характеризуется
стереотипностью болевых приступов в течение 1–3-х и более месяцев, нестабильная — резким
качественным изменением приступов и повышенной опасностью возникновения инфаркта миокарда.
Вам необходимо знать следующие основные вопросы:
* — класификация антиангинальных ЛС по механизму их лечебного действия и основные принципы
применения;
* — МД, ФК, ФД, применение и ПЭ препаратов группы нитроглицерина;
* — МД, основные эффекты и применение антагонистов кальция;
* — МД, основные и ПЭ в-адреноблокаторов, нх применение при стенокардии;
* — МД, основные эффекты и применение в-адреномиметиков при стенокардии;
* — характеристика коронарорасширяющих средств, МД и применение дипиридамола,
карбокромена, лидофлазина, молсидомина;
* — антиангинальные средства разного МД: анаболические, антигипоксические,
антибрадикининовые;
* — общие принципы выбора и комбинирования антиангинальных ЛС;
* — общие прннципы фармакотерапии инфаркта миокарда.
Первое описание синдрома стенокардии относится к глубокой древности (папирусы Эберса, около
1550 г. до н.э.). В последние десятилетия заболеваемость ишемической болезнью сердца иепрерывно
растет. Это связано с психоэмоциональным напряжением, гиподинамией, несбалансированным
питанием, что приводит к развитию атеросклероза, включая склероз коронарных сосудов.
Основной причиной стенокардии является несоответствие между потребностью сердца в кислороде и
его доставкой коронарным кровотоком, что сопровождается развитием гипоксии миокарда и
накоплением недоокисленных продуктов метаболизма, которые раздражают рецепторы и вызывают
боль. При стабильной стенокардии это связано с атеросклеротическим стенозированием коронарных
сосудов, в результате чего коронарный кровоток не может существенно возрастать при увеличении
работы сердца. При нестабильной стенокардии гипоксия возникает, в основном, из-за спазма
коронарных сосудов. Эффективность медикаментозной терапии зависит от того, насколько удается
ликвидировать дисбаланс между потребностью сердца в кислороде и его доставкой. Это достигается
либо увеличением коронарного кровотока в зоне ишемии, либо уменьшением потребности миокарда в
кислороде.
Современные антиангинальные ЛС относятся к разным химическим и фармакологическим группам и
обладают разнообразным механизмом и спектром действия. Наибольшее значение получили 3 группы
препаратов: 1) препараты нитроглицерина; 2) в-адреноблокаторы; 3) антагонисты кальция. Другие ЛС
(коронароактивные, анаболические, антибрадикининовые и др.) имеют вспомогательное значение.
Учитывая разный характер течения стенокардии, очень важно иметь средства для быстрого
купирования приступов (нитроглицерин, валидол) и средства для предупреждения приступов (все
остальные).
Главным принципом лечения ишемической болезни сердца является дифференцированное
применение ЛС. Необходимо учитывать их различный МД, тяжесть и особенности течения
стенокардии. Медикаментозное лечение стенокардии должно сочетаться с мероприятиями общего
характера: снижение массы тела, устранение гиподинамии, курения, злоупотребления алкоголем,
физических и психоэмоциональных перегрузок.
Антиангинальные средства можно разделить на следующие группы:
1. Средства, понижающие потребность миокарда в кислороде и увеличивающие его доставку к
миокарду: а) органические нитраты (нитроглицерин, сустак, нитронг, тринитролонг, эринит,
нитросорбид и др.); б) блокаторы кальциевых каналов (фенигидин, дилтиазем, верапамил).
2. Средства, понижающие потребность миокарда в кислороде: в-адреноблокаторы (анаприлин,
метопролол, окспренолол, талинолол, пиндолол и др.).
3. Средства, увеличивающие доставку кислорода к миокарду (коронароактионые): а) средства
миотропного действия (дипиридамол, карбокромен, лидофлазин, молсидомин, но-шпа и др.); б)
стимуляторы в-АР (нонахлазин, оксифедрин); в) средства рефлекторного действия (валидол).
4. Разные средства: а) анаболические (инозин, калия оротат, ретаболил и др.); 6)
антибрадикининовые (пармидин).
Средства, понижающие потребиость миокарда в кислороде и увеличивающие его доставку
Нитроглицерин для купирования приступа стенокардии впервые применил американский врач и
исследователь Брунтон в 1860 г. До настоящего времени он является наиболее надежным средством для
быстрого купирования приступа стенокардии. Поэтому его называют “королем антиангинальных
средств”. По выражению французского кардиолога, стенокардия — это болезнь, которой можно болеть
30 лет и 30 сек. Действительно, при полном стенозе магистральной коронарной артерии смерть может
наступить почти мгновенно в результате остановки сердца. Поэтому нитроглицерин играет важнейшую
роль при купировании приступа стенокардии.
МД нитроглицерина до конца не выяснен. По-видимому, расширение коронарных сосудов не имеет
решающего значения для купирования приступа, так как даже при их резко выраженном склерозе
антиангинальный эффект сохраняется. Способность нитроглицерина купировать приступы стенокардии
определяется комплексом факторов. Прежде всего, это снижение венозного и артериального давления а
результате расширения периферических вен и артерий. Расширение вен приводит к уменьшению
венозного возврата к правому сердцу и снижению преднагрузки на сердце, а расширение артерий — к
уменьшению сосудистого сопротивления и постнагрузки на сердце. В результате снижения
гемодинамической нагрузки работа сердца и потребность в кислороде уменьшаются. 2-ым фактором
является улучшение кровоснабжения зоны ишемии в миокарде. Это связано с ослаблением
внутрикардиального сжатия и перераспределением кровотока в пользу внутренних (эндокардиальных)
слоев миокарда, испытывающих наибольшее сжатие во время систолы. Кроме того, нитроглицерин
ослабляет сосудосуживающие рефлексы на сердце и оказывает прямое коронарорасширяющее действие
в месте сужения сосуда. По-видимому, нитроглицерин угнетает передачу болевых импульсов из зоны
гипоксии, что способствует устранению боли при приступе. Все эти факторы в совокупности и
определяют МД нитроглицерина.
Нитроглицерин принимают обычно под язык в виде таблеток, по 1–2 капли 1% спиртового раствора
или в капсулах. Всасывание происходит быстро, действие развивается через 2–3 мин и продолжается до
30 мин. Из организма выводится полиостью за 40–50 мин. Имеются также раствор для в/в введения,
пластыри и мазь для нанесения на кожу. Препараты нитроглицерина следует хранить в защищенном от
света месте не более 2 мес. Привыкание к нему обычно не возникает. Противопоказания: инсульт,
повышенное внутричерепное давление, глаукома. ПЭ: головная боль, головокружение, тахикардия,
иногда коллапс. При длительном применении головная боль постепенно исчезает, а способность
купировать приступы сохраняется.
Препараты нитроглицерина пролонгированного действия: сустак, тринитролонг, нитронг. Это
особые лекарственные формы нитроглицерина, в которых наружная часть гранул (таблеток) при приеме
внутрь всасывается быстро (эффект через 10–15 мин), а внутренняя медленно, действуя несколько
часов. Благодаря этому в организме создается депо нитроглицерина. Сустак применяют в виде
таблеток, действие начинается через 10–15 мин и продолжается 4 ч. Тринитролонг — отечественный
препарат, применяемый в виде полимерной пластинки на десны, действует около 3–4 ч. Нитронг
(США) действует наиболее продолжительно (до 7–8 ч). Мазь, содержащая 2% маслянный раствор
нитроглицерина, наносится на кожу, действие начинается через 15–30 мин и продолжается до 5 ч.
Нитросорбид по действию сходен с нитроглицерин, но отличается более продолжительным
эффектом (4–6 ч). При приеме в виде аэрозоля эффект возникает через 5 мин, при приеме внутрь —
через 50–60 мин.
Блокаторы кальциевых каналов (антагонисты кальция) оказывают антиангинальный эффект за
счет уменьшения потребности миокарда в кислороде и улучшения коронарного кровообращения. МД
обусловлен блокированием входа Са++ в клетки миокарда и сосудов, в результате чего падает
активность актомиозина, что и служит причиной уменьшениея тонуса миофибрилл миокарда и гладких
мышц сосудов. Это сопровождается снижением напряжения миокарда, расширением коронарных
сосудов и увеличением коронарного кровотока, а также расширением периферических сосудов
(преимущественно — артерий), снижением сосудистого сопротивления и постнагрузки на сердце.
Помимо антиангинального эффекта они обладают противоаритмическим и гипотензивным действием.
В связи с этим их используют при нарушениях ритма сердца (верапамил) и гипертонической болезни
(фенигидин, дилтиазем). Кроме того, антагонисты кальция препятствуют агрегации тромбоцитов и
снижают тромбообразование, улучшая реологические свойства крови, что важно при сосудистых
нарушениях.
Применяют для профилактики приступов стенокардии напряжения вазоспастической стенокардии
покоя. При закладывании таблетки фенигидина (нифедипина) за щеку эффект развивается через 5–10
мин, максимальное действие — через 15–45 мин; при приеме внутрь действие начинается через 1 ч,
максимальное — через 2 ч, продолжительность — 4–6 ч. Из кишечника всасывается до 80% дозы.
Привыкание не наступает даже при длительном применении. ПЭ: головная боль, тахикардия,
гипотония, гиперемия кожи, запоры, аллергические реакции, возникают редко. Противопоказания:
кардиогенный шок, декомпенсация сердечном деятелоности, нарушения проводимости, брадикардия,
беременность, период грудного вскармливания.
Амиодарон относится к препаратам, уменьшающим потребность миокарда в кислороде и
увеличивающим его доставку. МД обусловлен блокадой в1-АР и глюкагоновых рецепторов миокарда и
расширением коронарных сосудов. Он обладает также противоаритмическим действием и более
подробно рассмотрен в предыдущей лекции.
Средства, понижающие потребность миокарда в кислороде
К ним относятся в-адреноблокатеры, которые подробно освещены в соответствующей лекции. МД
обусловлен блокадой в1-АР, в результате чего уменьшаются процессы гликолиза, липолиза и
потребление кислорода. Это сопровождается ослаблением работы сердца, ЧСС и минутного объема
сердца. в-Адреноблокаторы оказывают также противоаритмическое и антигипертензивное Действие,
поэтому широко используются при этих видах патологии.
По влиянию на в-АР их подразделяют на препараты иеиз6нрательного действия (анаприлии,
окспренолол, пиндолол и др.), блокирующие в1- и в2-АР, и кардиоселективные (метопролол,
талинолол, атенолол и др.), блокирующие преимущественно в-АР сердца. Некоторые, наряду с
блокадой в-АР, оказывают симпатомиметический эффект, т.е. усиливают высвобождение
норадреналина из симпатических окончаний, что препятствует развитию брадикардии и гипотензии
(окспренолол, пиндолол, талинолол). Их подразделяют также на препараты длительного действия
(соталол, атенолол, надолол) с периодом полувыведеиия 12–24 ч; препараты средней
продолжительности действия (пиндолол) с периодом полувыведения 4–6 ч и препараты короткого
действия (анаприлин, окспренолол, метопролол и др.) — период полураспада 2–3 ч. Наличие
препаратов с разными характеристиками позволяет применять их дифференцированно с учетом разных
форм стенокардии и сопутствующих заболеваний. Напр., кардиоселективные в-адреноблокаторы
предпочтительны при наличии бронхообструктивных заболеваний, эндартериита, сахарного диабета.
При брадикардии, скрытой сердечной недостаточности, атриовентрикулярной блокаде можно
использовать в-адреноблокаторы с симпатомиметической активностью (см. также лекцию 7).
Средства, увеличивающие доставку кислорода к миокарду
Основным эффектом этих препаратов является расширение коронарных сосудов и увеличение
кровоснабжения миокарда. Это обусловлено либо прямым миотропным действие на сосуды, либо
опосредованно через изменение метаболизма миокарда и увеличение содержания сосудорасширяющих
метаболитов, а также в результате стимуляции в-АР. К препаратам миотропного действия относятся
дипиридамол, карбокромен, лидофлазии, молсидомин, но-шпа и др. Дипиридамол (курантил)
расширяет коронарные сосуды и увеличивает кровоток преимущественно в мелких сосудах миокарда, в
результате чего улучшается микроциркуляция, увеличивается колатеральный кровоток в зоне ишемии.
Кроме того, ом улучшает реологические свойства крови за счет угнетения агрегации тромбоцитов. МД
связывают с накоплением аденозина в миокарде в результате уменьшения его обратного захвата и
угнетения аденозиндезаминазы, расщепляющей аденозин. Дипиридамол применяют при
вазоспастической стенокардии без явления склероза коронарных сосудов. Назначают внутрь в
таблетках. Карбокромен (интенсаин) расширяет коронарные сосуды и увеличивает кровоснабжение
миокарда за счет иигибирования фосфодиэстеразы и накопления цАМФ. Он также способствует
развитию коллатеральных сосудов в зоне ишемии. Применяют преимущественно при стенокардии
напряжения без выраженных явлений коронаросклероза. Назначают внутрь. В первые 10–12 дней могут
наблюдаться неприятные ощущения в области сердца. Противопоказания: множественные стенозы
коронарных артерий, язвенная болезнь желудка, гастриты, болезни печени, почек. Лидофлазин
увеличивает коронарный кровоток за счет аденозинового механизма (подобно дипиридамолу). На
работу сердца и АД не влияет. Молсидомин (корватон) снижает тонус коронарных артерий и вен,
увеличивает коронарный кровоток, уменьшает потребление кислорода миокардом, обладает свойствами
антиагреганта. Работу сердца может стимулировать. Назначают внутрь и под язык в таблетках. Но-шпа,
папаверин и эуфиллин являются спазмолитиками миотропиого действия, расширяют коронарные
сосуды и увеличивают кровоснабжение миокарда. МД связывают с угнетением фосфодизстеразы и
накоплением ц-АМФ, а также аденозина. Эти препараты увеличивают потребность миокарда в
кислороде, поэтому при атеросклерозе коронарных артерий их назначать не следует. В основном
применяют при вазоспастической стенокардии.
Общим недостатком вазодилататоров является зависимость их действия от исходного просвета
сосудов. В зоне ишемии сосуды обычно максимально расширены, поэтому на них вазодилататоры
миотропного действия не влияют, а расширяют сосуды в соседних неишемизированиых областях, а
которые оттекает кровь. Возникает “синдром обкрадывания”. Поэтому при наличии склеротического
стеноза они не только не улучшают кровоснабжение зоны ишемии, а даже могут ухудшить его. Кроме
того, расширяя периферические сосуды, они могут понизить АД. что усиливает гипоксию миокарада.
Средства, стимулирующие в-АР. К ним относятся нонахлазин и оксифедрин. Их лечебный
эффект связывают с улучшением коронарного кровообращения. Они расширяют коронарные сосуды за
счет стимуляции в-АР. увеличивают частоту и силу сердечных сокращений в результате стимуляции в1АР. Их основное значение состоит в лечебном эффекте при стенокардии напряжения, сочетающейся с
брадикардией и ослаблением сердечной деятельности. Эффект о6ычно развивается через 2–5 дней
после начала лечения. Оба препарата обладают умеренной противоаритмической активностью.
Переносятся хороша, иногда вызывают зуд, высыпания на коже, аллергические реакции.
Разные антиаигинальные средства. Валидол устраняет коронароспазм рефлекторно за счет
раздражения холодовых рецепторов. Представляет 25–30% раствор ментола в ментиловом эфире
изовалериановой кислоты. Эффект у него слабый, поэтому применяют при легких приступах
стенокардии, вызванных спазмом коронарных сосудов. Назначают под язык в таблетках. Если эффект
через 2–3 мин не наступает, следует принять нитроглицерин.
Анаболические средства используют в комплексной терапии стенокардии. Они стимулируют синтез
белка, нуклеиновых кислот, увеличивают запасы энергоносителей в миокарде (гликоген, АТФ,
креатинфосфат), увеличивают сократимость и коллатеральный кровоток. Различают нестероидные
аиаболики (калия оротат, фолиевая кислота, инозин) и стероидные (ретаболил и др.). Их применяют
обычно при стенокардии покоя в комбинации с другими антиангинальными ЛС.
Антибрадикининовые средства (пармидин) тормозят эффекты брадикинина, который нарушат
проницаемость капилляров, способствует развитию воспалительной реакции и т.п. Пармидин улучшает
микроциркуляцию, угнетает агрегацию тромбоцитов, активирует антисклеротические ферменты. Его
применяют преимущественно при стенокардии напряжения в сочетании с атеросклерозом
периферических сосудов (эндартериит).
Пиридоксинил-глиоксилат (глио-сиз) активирует анаэробный гликолиз и тормозит аэробный
гликолиз, в результате чего потребление кислорода в миокарде снижается. Благодаря этому возрастает
переносимость гипоксии (антигипоксаитный эффект). Его назначают преимущественно при
стенокардии покоя с распространенным стенозом коронарных сосудов.
Выбор антиангинальиых средств определяется степенью нарушения коронарного кровообращения
и характером течения стенокардии. Если нет существенных изменений в коронарных сосудах, то во
многих случаях назначения аитиангинальиых средств не требуется. Используют меры общего характера
(устранение факторов риска, седативиые средства, транквилизаторы), валидол, иногда антагонисты
кальция, вазодилататоры. При наличии локального коронаросклероза должен быть строгий выбор ЛС с
учетом их МД, формы стенокардии и характера ее течения. Наиболее сложную задачу представляет
лечение стенокардии с распространенным коронаросклерозом. Проблемы дифференцированного
лечения и тактика фармакотерапии разных форм стенокардии рассматриваются клинической
фармакологией.
Средства, применяемые при инфаркте миокарда
Инфаркт миокарда является наиболее тяжелым осложнением стенокардии. Он требует применения
комплекса лечебных мероприятий, важное место среди которых занимают ЛС. Так как инфаркт
сопровождается тяжелым болевым синдромом, необходимо применение наркотических анальгетиков
(фентанил, морфин, омнопон, промедол) или метода нейролептанальгезии (одновременное введение
нейролептика дроперидола и анальгетика фентанила). Инфаркту миокарда в 90% случаев сопутствуют
нарушения ритма сердца, поэтому введение противоаритмических ЛС для профилактики и устранения
аритмии обязательно (лидокаин, этмозин, аймалин). При выраженном угнетении сердечной
деятельности назначают сердечные гликозиды (строфантин, дигоксин), а при развитии резкой
гипотензии (кардиогенный шок) — гипертензнвные ЛС (дофамин в/в капельно, мезатон, норадреналин).
При шоке для устранения гипоксии тканей в результате компенсаторного спазма артериол, метартериол
и прекапилляров и связанной с ним интоксикации недоокисленными продуктами обмена веществ
назначают а-адреноблокаторы (фентоламин, тропафен, аминазин). Поскольку нарушение коронарного
кровообращения способствует развитию тромбоза сосудов, необходимо назначать антикоагулянты
прямого действия (гепарин) и фибринолитические средства (стрептокиназа, стрептодеказа,
фибринолизин). Для нормализации водно-электролитного баланса и кислотно-основного состояния
назначают растворы электролитов, натрия гидрокарбонат.
Фармакотерапия инфаркта миокарда должна проводиться под постоянным контролем за работой
сердца и уровня системного АД.
Лекция 21
АНТИГИПЕРТЕНЗИВНЫЕ (ГИПОТЕНЗИВНЫЕ) СРЕДСТВА. ГИПЕРТЕНЗИВНЫЕ СРЕДСТВА
К ним относятся представители различных фармакологических групп, снижающие системное АД и
применяемые для лечения гипертонической болезни. Гипертензивные средства используют при острых
и хронических гипотензиях.
В этой теме будут рассмотрены следующие основные вопросы:
*- современные представления об основных механизмах развития гипертонической болезни и
принципах фармакологической коррекции АД;
*-классификация аитигипертензивных средств;
* — МЛ и основные эффекты нейротропных ЛС пренмушетвеино центрального действия (резерпин,
клофелин, метилдофа, кавинтои);
* — МЛ и характеристика нейротропиых ЛС преимущественно периферического действия
(ганглиоблокаторы, симпатолитики, адреноблокаторы);
* — миотропные вазодилататоры, их примеиение и ПЭ;
* — антагонисты кальция, их МД и применение в кардиологии;
*- средства, угнетающие ренин-ангиотензиновую систему;
*-ЛС, нормализующие водно-солевой обмен, МД и применение салуретиков.
Согласно статистике Всемирной организации здравоохранения (ВОЗ), около 20% летальности
промышленно развитых стран связано с гипертонической болезнью и ее осложнениями. Проблема
лечения гипертонической болезни сложная, так как патогенез ее окончательно не установлен. В
соответствиис нейрогенной теорией Ланга-Мясникова важнейшим провоцирующим фактором развития
гипертонической
болезни
является
длительное
психоэмоциональное
перенапряжение,
сопровождающееся нарушением обменных процессов в мозге, стойким возбуждением лимбикоретикулярного комплекса и гиперреактивностыо гипоталамуса. Это приводит к повышению тонуса
центров симпатической иннервации, стимуляции нейрогуморальных систем (гиперсекреция
катехоламинов, адренокортикотропного гормона, вазопрессина, альдостерона, ренина, ангиотензина и
др.), к нарушениям водно-солевого обмена (увеличение содержания натрия и кальция в стенках сосудов
и в тканях). Все эти факторы способствуют увеличению работы сердца, сердечного выброса, тонуса
сосудов и общего сосудистого сопротивления, что в конечном итоге и приводит к развитию
артериальной гипертензии и формированию гипертонической болезни.
Фармакотерапия гипертонической болезни строится с учетом патогенетических механизмов, стадии
болезни и ФД препаратов. Важнейшим принципом является комбинированное воздействие на основные
звенья патогенеза болезни. Поэтому она должна быть направлена на: 1) уменьшение
психоэмоционального напряжения и нарушений метаболизма в ЦНС; 2) понижение активности
симпато-адреналовой системы; 3) устранение нарушений водно-электролитного баланса; 4) понижение
тонуса сосудов к работы сердца, составляющих гемодинамическую основу болезни.
Антигипертензивные ЛС делятся на 5 основных групп: 1. Нейротропные ЛС, подавляющие
стимулирующее влияние симпато-адреналовой системы на сердечно-сосудистую деятельность: а)
средства преимущественно центрального действия (резерпин, клофелин, метилдофа. кавинтон); 6)
средства преимущественно периферического действия (гаиглиоблокаторы, симпатолитики,
адреноблокаторы). 2. Миотропные вазодилататоры (апрессин, диазокснд, миноксидил, натрия
нитропруссид, дибазол, магния сульфат). 3. Антагонисты кальция (нифедипин и др.). 4. ЛС,
угнетающие ренин-ангиотензиновую систему (каптоприл, саралазин). 5. ЛС, регулирующие водносолевой обмен — диуретики (салуретики).
Нейротропные гипотензивные средства
Для снижения психоэмоционального напряжения, провоцирующего резкие подъемы АД, используют
профилактически седативные ЛС (препараты брома, валерианы, пустырника), снотоворные в малых
дозах (фенобарбитал, нитразепам и др.) и транквилизаторы (сибазон, феназепам, хлозепид, триоксазин,
мепротан и др.). Их применяют преимущественно при транзиторной (преходящей) гипертонии (1-я
стадия болезни), а также как вспомогательные средства при постоянной гипертензии.
Нейротропные средства преимущественно центрального действия снижают тонус центров
симпатической иннервации. Клофелин (катапрессан, клонидин, гемитон) понижает тонус вазомоторных
центров за счет стимуляции а2-АР, которая сопровождается уменьшением выделения норадреналина и
снижением активности нейронов продолговатого мозга и гипоталамуса. Это приводит к уменьшению
потока сосудосуживающих импульсов на периферию, снижению работы сердца и тонуса сосудов.
Одновременно клофелин оказывает успокаивающее действие. Из ЖКТ всасывается хорошо и
назначается преимущественно внутрь. Парэнтерально его вводят при гипертонических кризах. К ПЭ
относятся сонливость, угнетение секреции слюнных желез и желудка, запор, задержка натрия и воды,
поэтому его рекомендуется назначать с диуретиками. Клофелин потенцирует действие алкоголя,
снотворных, нейролептиков на ЦНС, поэтому назначать его с этими .препаратами не рекомендуется.
Метилдофа (допегит, альдомет) по МД сходна с клофелином. Она нарушает синтез норадреналина, в
результате чего образуется “ложный медиатор” — альфа-метилдофамин и альфа-метилнорадреналин,
которые стимулируют а2-АР. Это сопровождается угнетением вазомоторных центров и развитием
симпатодепрессорного эффекта. Метилдофа также угнетает образование ренина и ангиотензина.
Происходит постепенное снижение периферического сосудистого сопротивления и АД. Препарат
оказывает также успокаивающее действие, что способствует развитию сна. В кишечнике всасывается
около 50% дозы. Эффект развивается через 4–5 ч и продолжается до суток. Метилдофа не кумулирует и
не вызывает привыкания. Обычно ее комбинируют с диуретиками, что позволяет уменьшить дозу и ПЭ,
которые связаны с истощением запасов катехоламинов в ЦНС (вялость, сонливость, депрессия, иногда
паркинсонизм).
Резерпин по МД является симпатолитиком. Он тормозит обратный нейрональный захват
катехоламинов и серотонина, в основном, на уровне мембран везикул, что приводит к истощению их
запасов, ослаблению влияний центров симпатической иннервации на ССС и понижению АД.
Одновременно резерпин оказывает седативное и нейролептическое влияние на ЦНС. Центральные
эффекты связаны с проникновением резерпина через ГЭБ преимущественно в области лимбикоретикулярного комплекса. Но он обладает и периферическим симпатолитическим действием на
окончания симпатических нервов в стенке сосудов. При приеме внутрь эффект развивается медленно
(на 3–6 день), а после отмены продолжается еще до 2–3 недель. Наилучший эффект развивается при
лабильной и неосложненной гипертонии. ПЭ: адинамия, депрессия, паркинсонизм, брадикардия,
диспептические расстройства, обостренние язвенной болезни, бронхиальной астмы. Раунатии и
раувазаи действуют подобно резерпину, но уступают ему по эффективности. Они лучше переносятся и
меньше дают ПЭ.
Кавиитон, девинкан — алкалоиды барвинка малого, по химической структуре близки к резерпину и
сходны с ним по МД. Они уменьшают содержание катехоламинов в ЦНС и на периферии. По
гипотензивному действию слабее резерпина. Наилучший эффект дают при мозговых формах
гипертонической болезни, преимущественно в начальных стадиях. Они улучшают мозговое
кровообращения, уменьшают гипоксию мозга, оказывают успокаивающее действие. Выраженных ПЭ
не вызывают. Назначают внутрь и парэнтерально.
Нейротропные средства периферического действия включают ганглиоблокаторы, симпатолитики
и адреноблокаторы.
Ганглиоблокаторы блокируют проведение сосудосуживающих импульсов на уровне симпатических
ганглиев. МД обусловлен угнетением н-ХР, в результате чего затрудняется проведение возбуждения с
преганглионарных на постганглионарные волокна. Это сопровождается снижением тонуса артериол и
общего периферического сосудистого сопротивления, уменьшением тонуса вен и венозного возврата
крови к сердцу. При этом понижается АД, сердечный выброс, депонируется кровь а венах органов
брюшной полости, в нижних конечностях и уменьшается масса циркулирующей крови, снижается
давление в правом желудочке и легочной артерии, угнетаются рефлекторные сосудосуживающие
реакции. В настоящее время ганглиоблокаторы для лечения гипертонической болезни используют мало,
так как дают много ПЭ: ортостатическая гипотензия, угнетение перистальтики кишечника, запоры,
атония мочевого пузыря и др. К ним быстро развивается привыкание. Применяют при тяжелых
(осложненных) гипертонических кризах, прогрессирующей гипертонии, не поддающейся действию
других ЛС. Очень осторожно надо назначать больным старше 60 лет. При кризах обычно назначают
парэнтерально препараты средней продолжительности действия (бензогексоний, пентамин), а для
длительного применения — пирилен внутрь (действует 10–12 ч). Для управляемой гипотонии
применяют препараты короткого действия (гигроний, арфонад). Ганглиоблокаторы используют также
при лечении местных сосудистых спазмов (эндартериит, болезнь Рейно, акроцианоз) (см. также лекцию
5).
Симпатолитики. Основным препаратом является октадин. МД связан с истощением запасов
норадреналина в симпатических окончаниях, а результате чего угнетается передача сосудосуживающих
импульсов в периферических адренергических синапсах. Гипотензивный эффект развивается постпенно
(через 1–3 дня) и продолжается 1–3 недели после отмены препарата. ПЭ: ортостатическая гипотония,
брадикардия, диспептические расстройства, обострение язвенной болезни и бронхиальной астмы. Они
связаны с преобладанием тонуса холинергической системы в результате ослабления адренергических
влияний. Привыкание к октадину не развивается (см. также лекцию 7).
в-Адреноблокаторы являются одними из наиболее эффективных средств лечения гипертонический
болезни. МД обусловлен блокадой в-АР в сердце, почках и мозге, в результате чего уменьшается
сердечный выброс, образование ренина в почках и ангиотензина в крови, угнетаются центральные
симпатические влияния на сердце и сосуды. в-Адреноблокаторы являются препаратами выбора при
высоком тонусе симпатической системы, особенно в ранних стадиях болезни преимущественно у лиц
молодого и среднего возраста. Они предупреждают резкие подъемы АД, сглаживают пики АД, что
играет защитную роль для сердца и сосудов. Большим примуществом перед симпатолитиками является
равномерное снижение АД в вертикальном и горизонтальном положении и отсутствие ортостатической
гипотензии, так как они почти не снижают тонус вен. К этой группе относятся аналрилин
(пропранолол), окспренолол, метопролол, пиндолол и др. (см. также лекций 7, 19 и 20).
а-Адреноблокаторы делятся на 2 группы: 1) блокаторы а1-АР и а2-АР (фентоламин, тропафен,
дигидроэрготоксин, дигидроэрготамин, пирроксан) и селективные блокаторы а1-АР (празозин). Для
лечения гипертонической болезни используют празозин, оказывающий избирательное действие на
постсинаптические а1-АР. Он не нарушает механизм обратной отрицательной связи и, следовательно,
не вызывает избыточного высвобождения норадреналина из симпатических окончаний. Поэтому при
его применении не возникает тахикардия и Гипотензивный эффект более стойкий. Фентоламин,
тропафен и др. неселективные а-адреноблокаторы за счет блокада пресинаптических а2-АР усиливают
высвобождение норадреналина из симпатических окончаний, что приводит к тахикардии и ослаблению
гипотензивного действия. К ним быстро развивается привыкание. Их используют для устранения
местных сосудистых спазмов и при гипертоническом кризе.
Лабеталол является блокатором а-АР и в-АР, поэтому уменьшает работу сердца, ударный и
минутный объем крови, снижает образование ренина в почках, понижает тонус сосудов и сосудистое
сопротивление. Эти эффекты приводят к понижению АД. Лабеталол эффективен в разных стадиях
гипертонической болезни. К ПЭ относятся слабость, головокружение, ортостатическая гипотония (см.
лекцию 7).
Миотропные сосудорасширяющие ЛС (периферические вазодилататоры)
Действуют преимущественно на гладкие мышцы сосудов. МД связывают с угнетением обменных
процессов в гладкомышечных клетках (снижение активности ферментов, углеводного обмена,
содержания АТФ, креатинфосфата, актомиозина и т.п.). К ним относятся апрессин. диазоксид,
миноксидил, натрия нитропруссид, дибазол, магния сульфат.
Апрессин (гидралазии) расширяет артериолы и снижает сосудистое сопротивление, на венулы
оказывает слабое действие. Снижение АД сопровождается увеличением ЧСС и сердечного выброса, что
является нежелательным. ПЭ: боли в сердце, головная боль, диспептические расстройства, острый
ревматоидный синдром, иногда анемия, лейкопения, полиневрит. Применяют в комбинациях с
резерпином, в-адреноблокаторами, диуретиками. Это уменьшает ПЭ и усиливает гипотензивное
действие. Диазоксид действует преимущественно на артериолы и снижает сосудистое сопротивление.
Продолжительность эффекта — 12–18 ч. При в/в введении эффект наступает быстро, поэтому его
используют при гипертонических кризах. Он задерживает выведение натрия и воды, повышает сахар и
мочевую кислоту в крови. Поэтому его сочетают с диуретиками (фуросемид). Диазоксид используют
также для интенсивной терапии при злокачественной гипертонии с энцефалопатией. Миноксидил
обладает наиболее сильным действием из периферических вазодилататоров. Уменьшает сосудистое
сопротивление и АД. В ЖКТ хорошо всасывается и действует до 24 ч. Может задерживать в организме
натрий и воду и вызывать оволосение (гирсутизм) лица. Натрия нитропруссид снижает тонус
резистивных (артериальных) и емкостных (венозных) сосудов, поэтому уменьшает сосудистое
сопротивление и венозный возврат к сердцу. Его вводят в/в капельно при гипертонических кризах, для
управляемой гипотонии и при сердечной недостаточности. Дибазол оказывает спазмолитическое
действие на все гладкомышечные органы и сосуды. Гипотензивное действие умеренное и
непродолжительное, поэтому имеет вспомогательное значение. Вводят преимущественно при
гипертонических кризах в/в. Оказывает лечебное действие при остаточных явлениях после
полиомиэлита и при параличе лицевого нерва. Магния сульфат оказывает как периферическое, так и
центральное действие. Он угнетает высвобождение норадреналина из симпатических окончаний в
сосудах, снижает возбудимость вазомоторного центра, оказывает успокаивающее, противосудорожное,
а в больших дозах — наркотическое действие. Применяют при гипертонических кризах,
энцефалопатии, обострении гипертонической болезни. Из кишечника практически не всасывается,
оказывая слабительный эффект, поэтому для резорбтивного действия вводят в/в и в/м.
Продолжительность действия — 5–6 ч. При возникновении угнетения дыхания и резкой гипотеизии
вводят в/в кальция хлорид.
Антагонисты кальция. К ним относятся нифедипин (фенигидин, коринфар), фендилин, дилтиазем,
верапамил. При гипертонической болезни применяют, в основном, нифедипин. МД связан с блокадой
кальциевых каналов мембран гладкомышечных клеток, что приводит к уменьшению входа Са++ и
снижению активности актомиозина. Это сопровождается расширением сосудов (преимущественно
артерий), уменьшением сосудистого сопротивления и АД. Кроме того, они угнетают агрегацию
тромбоцитов, снижают свертываемость крови и улучшают ее реологические свойства.
Противопоказаны при беременности, брадикардии, нарушении проводимости а сердце, при сердечной
недостаточности (см. лекции 19 и 20).
Средства, угнетающие ренин-ангиотензиновую систему. К ним огносятся препараты, угнетающие
превращение ангиотензина-1 в ангиотензин-2 (каптоприл) и блокаторы ангиотензиновых рецепторов
(саралазин). Каптоприл являегся ингибитором ангиотензин-превращающего фермента (конвертазы),
что приводит к снижению продукции активного ангиотензина-2, понижению тонуса сосудов и АД.
Снижается также продукция альдостерона в коре надпочечников, что приводит к уменьшению
содержания натрия и воды а гканях. В развитии гипотензивного эффекта участвуют также брадихинин,
простацкклин и простагландин Е2, содержание которых под влиянием каптоприла возрастает.
Каптоприл хорошо всасывается из кишечника, гипотензивный эффект развивается через 30–60 мин и
продолжается 4–8 ч. Через ГЭБ и плаценту не проникает. Наиболее выраженный эффект проявляет при
повышенном содержании ренина в крови. Переносится хорошо. ПЭ: аллергические реакции,
тахикардия, нарушение вкуса, иногда — лейкопения.
Саралазин — блокатор ангиотензиновых рецепторов в сосудах и коре надпочечников, поэтому
препятствует взаимодействию ангиотензина-2 с рецепторами, снижает тонус сосудов и образование
альдостерона. Однако эффект кратковременный (6–8 мин) и проявляется только при в/в введении.
Поэтому для лечения гипертонической болезни он мало пригоден.
Средства, регулирующие водно-солевой обмен (диуретики). Являются одними из наиболее
эффективных средств для лечения гипертонической болезни. Обладают постоянным гипотензивным
эффектом и усиливают действие других гипотензивных ЛС. Используют преимущественно
дихлотиазид, клопамид, оксодолин. Гипотензивный эффект обусловлен выведением из организма
избытка натрия и воды, уменьшением объема экстрацелюлярной жидкости, в результате чего снижается
чувствительность гладких мышц сосудов к действию катехоламинов и других прессорных веществ, а
также уменьшается сдавливание сосудов и отек сосудистой стенки. Диуретики применяют
самостоятельно и в комбинации с другими гипотензивными ЛС, что позволяет значительно снижать
дозы. Основные ПЭ связаны с развитием гипокалиемии. Фуросемид и этакрииовая кислота для
длительной терапии мало пригодны. Их Можно использовать короткими курсами (3–5 дней) для
потенцирования действия гипотензивных ЛС при отеках и сердечной недостаточности.
Слироиолактон применяют при гипертонии, связанной с гиперальдостеронизмом, так как он является
антагонистом альдостероиа. Относится к калийсберегающим диуретикам, поэтому можно сочетать с
препаратами, вызывающими гипокалиемию.
Основным принципом фармакотерапии гипертонической болезни является последовательное
ступенеобразное и поэтапное применение антигипертензивных ЛС. Препаратами 1-й ступени являются
диуретики, 2-й — антиадренергические, 3-й — вазодилататоры, включая антагонисты кальция и
каптоприл. На 1-ом этапе используют диуретики или в-адреноблокаторы, на 2-ом — диуретики с
вазодилататорами или в-адреноблокаторы с диуретиками, на 3-м — диуретики с каптоприлом,
диуретики с клофелином или метилдофой, в-адреноблокаторы с диуретиками и вазодилататорами.
Диуретики являются основой фармакотерапии, когда задержка натрия и воды служит ведущим
механизмом гипертензии. Они остаются в комплексной терапии при назначении других гипотензивных
ЛС, чтобы предупредить задержку натрия и воды в организме, вызываемую антиадренергическими
средствами и вазодилататорами. Диуретики можно комбинировать со всеми основными
антигипертензивными ЛС.
Средства, применяемые для лечения гипертонического криза
Гипертонический криз характеризуется резким повышением АД и сопровождается нервнососудистыми и гуморальными нарушениями. В ранних стадиях гипертонической болезни при кризе
преобладают нарушения сердечной деятельности, выражающиеся в увеличении сердечного выброса
при мало измененном периферическом сосудистом сопротивлении. В более поздних стадиях болезни в
возникновении криза возрастает роль сопротивления сосудов и снижается роль сердечного выброса. В
соответствии с этим различают 2 основных типа криза: 1) гиперкинетический и 2)
гипокинетический. Для первого характерны резкая активация симпатоадреналовой системы, в
результате чего возникает тахикардия, значительно возрастает минутный объем крови и повышается
преимущественно систолическое АД при относительно небольшом повышении диастолического АД.
При 2 типе криза преобладает повышение диастолического АД а результате значительного увеличения
сопротивления сосудов, тогда как сердечный выброс изменяется мало или даже снижается.
Гипертонический криз может осложниться нарушениями мозгового и коронарного кровообращения,
отеком мозга и легких и т.п.
При гиперкинетическом кризе применяют антиадренергические ЛС центрального (клофелин в/м или
в/в) и периферического действия (бета-адреноблокаторй), а также вазодилататоры (дибазол в/в,
нифедипин и др.). Назначают также диуретики быстрого действия (фуросемид). При гипокинетическом
кризе наиболее эффективны ЛС, снижающие периферическое сопротивление сосудов (натрия
нитропруссид в/в, апрессин в/в или в/м, диазоксид в/в, ганглиоблокаторы — пентамин, бензогексоний,
особенно при появлении признаков отека мозга или легких). При резком возбуждении назначают
аминазин, дроперидол, магния сульфат в/м или в/в. Для снижения объема циркулирующей крови и
усиления диуреза применяют фуросемид, при стенокардических болях — нитроглицерин, морфии,
промедол.
Гипертензивные средства
Это ЛС, повышающие системное АД. Их применяют при острой артериальной гипотензии (обморок,
коллапс, шок). Подразделяют на: 1) ЛС, повышающие сердечный выброс и тонус периферических
сосудов (адреналин, эфедрин); 2) ЛС, преимущественно повышающие тонус сосудов (норадреналин,
мезатон, ангиотензинамид); 3) ЛС, повышающие сердечный выброс и снижающие периферическое
сосудистое сопротивление (дофамин).
Адрено- и симпатомиметнки были подробно рассмотрены в лекции 6.
Ангиотензинамид по сосудосуживающему действию превосходит норадреналин в 40 раз. МД связан
со стимуляцией ангиотензиновых рецепторов артериол, особенно внутренних органов, кожи и почек.
Кроме того, он усиливает секрецию альдостерона, что приводит к задержке натрия и воды,
способствующих повышению АД. Вводят в/в капельно под контролем АД. В результате спазма
артериол может нарушить микроциркуляцию, а при попадании под кожу — некроз.
При введении сосудосуживающих ЛС на фоне острой гипотензии в результате резкого спазма
артериол и прекалилляров может возникнуть артерио-венозное шунтирование и ухудшиться
микроциркуляция, что сопровождается гипоксией тканей и накоплением продуктов метаболизма,
усиливающих интоксикацию организма. В таких случаях необходимо вначале восстановить объем
циркулирующей крови введением плазмозамещающих растворов (полиглюкин, реополиглюкин и др.) и
только после этого вводить вазопрессорные средства. Для предупреждения спазма мелких артерий
используют в-адреноблокаторы.
При шоке, особенно кардиогенном, хорошим эффектом обладает дофамин. Он стимулирует работу
сердца за счет возбуждения бета-адренорецепторов, одновременно расширяя сосуды органов брюшной
полости, почек, сердца, легких в результате стимуляции дофаминовых рецепторов. Вводят в/в капельно
с таким расчетом, чтобы поддерживать АД на уровне 100–110 мм рт. ст.
При лечении хронических гипотензий используют стимуляторы ЦНС (кофеин, кордиамин,
препараты женьшеня, лимонника и др.)
Лекция 22
ЛС, ПРИМЕНЯЕМЫЕ ПРИ НЕДОСТАТОЧНОСТИ МОЗГОВОГО КРОВООБРАЩЕНИЯ.
ПРОТИВОАТЕРОСКЛЕРОТИЧЕСКИЕ СРЕДСТВА
Атеросклероз и мозговые сосудистые заболевания относятся к наиболее распространенной
патологии ССС. Они занимают одно из ведущих мест среди причин смертности населения
промышленно развитых стран, поэтому являются актуальной проблемой медицины. В этой лекции
будут освещены следующие основные вопросы:
* общие представления о патологии и видах нарушении мозгового кровообращения (МК);
* основные группы ЛС, используемых при недостаточностн МК;
* особенности действия и применения миотропных вазодилататоров при недостаточности МК;
* МД и применение антагонистов кальция при лечении ишемии мозга;
* ангиопротекгоры и их роль в лечении недостаточности МК;
* антигипоксанты и другие ЛС метаболического типа действия, используемые при нарушениях МК;
* основные препараты и принципы комплексной терапии мигрени;
* общие представления о патогенезе атеросклероза и классификация гиполипидемических средств;
* МД клофибрата и его производных, основные и ПЭ, применение;
* МД, основные и ПЭ ловастатина, никотиновой кислоты и ее производных;
* ЛС, усиливающие распад и выделение холестерина из организма;
* ЛС, препятствующие всасыванию холестерина;
* современные направления создания противоатеросклеротических ЛС.
Наиболее частыми причинами недостаточности МК являются атеросклероз и артериальная
гипертензия, которые сопровождаются органическими изменениями сосудов, снижнием их
эластичности, повышением сосудистого сопротивления и уменьшением МК. При этом нарушается
ауторегуляция МК, которая поддерживает его на адекватном уровне при изменениях системного АД.
Особую осторожность надо соблюдать при. назначении гипотензивных и гипертензивных ЛС больным
пожилого и старческого возраста, у которых атеросклеротические изменения сосудов суживают
диапазон приспособительных реакций и увеличивают риск возникновения ишемии мозга. Мозговые
сосудистые расстройства подразделяются на начальные проявления недостаточности МК,
дисциркуляторную энцефалопатию, преходящие нарушения МК, ишемический инсульт
(тромботический и нетромботический инфаркт мозга).
Достаточное кровоснабжение мозга зависит от тонуса сосудов, их эластичности, притока крови по
магистральным артериям и вязкости крови, обусловленной ее форменными элементами.
Профилактическое и лечебное применение ЛС при сосудистой патологии мозга направлено на
восстановление кровоснабжения мозга, нормализацию реологических свойств крови, устранение
гипоксии и метаболических нарушений. К ЛС, используемым при недостаточности МК, относятся
представители различных фармакологических групп: 1) миотропные вазодилататоры; 2) антагонисты
кальция; 3) ангиопротекторы; 4) антигипоксанты; 5) ЛС, нормализующие энергетический метаболизм
мозга; 6) ЛС, улучшающие реологические свойства крови.
Миотропные вазодилататоры. Для нормализации МК используют сосудорасширяющие ЛС,
действующие на разные механизмы регуляции сосудистого тонуса. Лечебный эффект вазодилататоров
связывают с улучшением кровоснабжения ишемизированной зоны и насыщения мозговой ткани
килородом. Применение вазодилататоров (эуфиллин, дибазол, диазоксид, миноксидил, папаверин, ношпа и др.) наиболее оправдано при хронической недостаточности МК. При острой ишемии мозга
назначение их менее целесообразно, а в ряде случаев даже противопоказано. Это обусловлено
следующими причинами: 1) расширением не только мозговых, но и периферических сосудов, что
приводит к снижению АД и ухудшению кровоснабжения мозга; 2) развитием синдрома “обкрадывания”
в зоне ишемии; 3) ухудшением оттока крови и повышением внутричерепного давления в результате
расширения венозных сосудов; 4) при стенозе магистральных артерий мозга происходит
компенсаторное расширение сосудов, расположенных дистальнее стенозированного участка и они
слабо реагируют на вазодилататоры, а в зоне стеноза создаются благоприятные условия для агрегации
форменных элементов крови, что способствует тромбообразованию в зоне ишемии.
Антагонисты кальция. Регуляция сосудистого тонуса и активности тромбоцитов зависит от
сбалансированного поступления ионов кальция в клетки. Избыточное поступление ионов Са++ через
каналы клеточных мембран лежит в основе спастического сокращения гладких мышц сосудов и
агрегации тромбоцитов. Поэтому в лечении ишемических заболеваний большое значение отводится
антагонистам кальция. Блокируя вход ионов Са++ через кальциевые каналы мембран гладко-мышечных
клеток и тромбоцитов, они устраняют спазм сосудов и ослабляют агрегацию тромбоцитов, что
сопровождается увеличением кровотока в зоне ишемии, улучшением реологических свойств крови и
ослаблением гиперкоагуляции. Это приводит к устранению гипоксии, уменьшению постишемических
расстройств в тканях мозга и ускорению восстановления нарушенных функций ЦНС. Благодаря
сочетанию способности к нормализации сосудистого тонуса с антиагрегантным действием,
проявляющимся у некоторых антагонистов кальция избирательно в системе МК, эти препараты имеют
преимущества перед другими сосудорасширяющими ЛС и перспективны при лечении нарушений МК.
Нимодипин — производное дигидропиридина, обладает избирательным действием на сосуды мозга.
На периферические сосуды практически не действует и не оказывает существенного влияния на АД .
Предотвращает действие на мозговые сосуды различных спазмогенов (серотонин, ангиотензин,
норадреналин, простагландины, симпатическая импульсация, артериальная гипертензия, сгустки крови
и т.п.). Нимодипин препятствует агрегации тромбоцитов, уменьшает вязкость крови, снижает уровень
фибриногена и липидов плазмы. Он блокирует также кальциевые каналы мембран нейронов,
предохраняя их от избыточного накопления ионов кальция. Этот эффект выражен сильнее, чем у других
антагонистов кальция. В кишечнике всасывается плохо, применяют парэнтерально. Переносится
хорошо, иногда возникают слабость, головокружение, головная боль, аллергические реакции.
Противопоказан в острой стадии инфаркта миокарда, при беременности.
Циннаризин (стугерон) — производное пиперидина. По МД и основным эффектам аналогичен
нимодипину. Он также обладает антигистаминными свойствами и снижает возбудимость
вестибулярного аппарата. Действует преимущественно на сосуды мозга, поэтому не вызывает
существенного снижения АД. В кишечнике всасывается хорошо и выводится почками в виде
метаболитов. Назначают внутрь курсами от нескольких недель до нескольких месяцев. Применяют при
нарушениях МК, связанных с атеросклерозом мозговых сосудов и гипертонической болезнью, с
травмами мозга, мигренью, а также при болезни Меньера, при укачивании на транспорте, при
нарушении периферического кровообращения и аллергических заболеваниях. Обычно переносится
хорошо, иногда вызывает сонливость, сухость во рту, диспептические расстройства.
Флуиаризин по МД и эффектам сходен с циннаризином. Особенно эффективен при головоружении,
связанном с нарушением МК. Применяют также при вестибулярных расстройствах и для профилактики
мигрени. Назначают внутрь. Переносится хорошо, может вызывать сонливость, экстрапирамидные
расстройства (у пожилых).
Фендилина гидрохлорид (сензит) — производное фенилалкиламинов. МД связан с блокадой
кальциевых каналов и угнетением фосфодиэстеразы, поэтому на сосуды действует как антагонист
кальция и миотропный вазодилататор. Он также блокирует вход кальция в нейроны, препятствует
активации фосфолипазы и образованию свободных жирных кислот, простагландинов, перекисных и
свободных радикалов, играющих важную роль в возникновении постишемических повреждений мозга.
Он увеличивает кровоток преимущественно в области гипоталамуса и ретикулярной формации и
повышает устойчивость к гипоксии. Применяют при острой и хронической ишемии мозга
спастического типа, а также при сочетании нарушений коронарного и мозгового кровообращения. ПЭ:
раздражение слизистых ЖКТ, тошнота, головная боль, аллергические реакции. Противопоказан при
беременности и в острой стадии инфаркта миокарда. Его не следует назначать одновременно с бетаадреноблокаторами.
Ангиопротекторы (аитиоксиданты, антиагреганты и др.). Под ангиопротекторами понимают ЛС,
нормализующие метаболические процессы в стенках сосудов и их проницаемость, предупреждающие
отложение липопротеинов, сложных углеводов, фибрина, кальция, деструкцию эластических волокон,
отечность сосудистой стенки и улучшающие микроциркуляцию. Ангиопротекторными свойствами
обладают различные ЛС: 1) угнетающие образование перекисей лилидов (аитиоксиданты); 2)
снижающие содержание холестерина и других липопротеинов в крови (гиполипидемические ЛС); 3)
подавляющие агрегацию тромбоцитов, эритроцитов и улучшающие микроциркуляцию; 4)
нормализующие функцию эндотелия сосудов.
При ишемии мозга понижается активность антиоксидантной системы и повышается образование
перекисей липидов в клетках крови, особенно в тромбоцитах. Это приводит к повреждению клеточных
мембран, увеличению проницаемости капилляров и ускорению агрегации тромбоцитов.
Антиоксидантным эффектом обладают многие ЛС (токоферола ацетат, аскорбиновая кислота. рутин,
экстракт элеутерококка, кислота липоевая, кислота глутаминовая, ксантинола никотинат,
пентоксифиллин и др.).
Ксантинола никотинат (компламин) является производным теофиллииа и никотиновой кислоты,
поэтому сочетает их свойства. Наряду с антиоксидантным действием уменьшает тонус сосудов мозга и
агрегацию тромбоцитов. МД связывают с ингибированием фосфодиэстеразы и накоплением цАМФ.
Назначают внутрь, в/м и в/в. Парэнтерально вводят при острой ишемии мозга. В/в вливание делают
очень медленно или капельно. предварительно растворив препарат в 5% растворе глюкозы. ПЭ:
покраснение кожи лица и шеи, слабость, головокружение, ощущение давления в голове.
Противопоказан при остром инфаркте миокарда, тяжелой сердечной недостаточности, кровотечениях, в
первые 3 мес. беременности, в сочетании с гипотензивиыми средствами.
Пентоксифиллин (трентал) — производное метилксантина и по химической структуре близок к
теобромину. По МД и основным эффектам близок компламину, но действует более эффективно.
Применяют при нарушениях мозгового и периферического кровообращения спастического и
атеросклеротического типов, при сосудистой патологии глазного дна и диабетических ангиопатиях.
При хронических нарушениях МК назначают внутрь курсами 2–3 нед. и более, а при острых
(нетромботический инсульт) — в/в или в сонную артерию. При приеме внутрь могут возникать
диспептические расстройства, покраснение лица, а при парэнтералоном — слабость, головокружение,
падение АД. Противопоказания такие же, как для компламина.
Кавинтон — производное индола, близкое по структуре девинкану — алкалоиду растения барвинка
малого. МД сходен с пентоксифиллином. Увеличивает кровоснабжение мозга, улучшает
микроциркуляцию и устраняет гипоксию мозговой ткани. Ценным свойством кавинтона является
способность увеличивать содержание катехоламинов в мозге, синтез которых нарушен при
атеросклерозе и церебросклерозе. Применяют преимущественно при неврологических и психических
нарушениях, вызванных недостаточностью МК на фоне атеросклероза, после инсульта, при
гипертонической энцефалолатии, при атеросклеротическом поражении сосудов глаза и т.п.
Выраженным аитиагрегантным действием обладают кислота ацетилсалициловая, антуран, гепарин,
реополиглюкин. МД кислоты ацетилсалициловой обусловлен угнетением циклооксигеназы, в
результате чего подавляется синтез тромбоксаиа А2, а также угнетением синтеза холестерина а печени.
Ее эффективность возрастает при взаимодействии с гепарином, обладающим многосторонним
аитикоагулянтным действием, включая антиагрегантный эффект.
Для улучшения реологических свойств крови при нарушениях МК используют метод гемодилюции.
С этой целью применяют реополиглюкин, который оказывает антиагрегантиое, антикоагулянтное и
гемодииамическое действие, в результате чего улучшается микроциркуляция м снабжение тканей
кислородом.
К ангиопротекторам, действующим преимущественно на эндотелий сосудов, относятся пармидин,
этамзилат, добезилат и др. Они обладают также антиагрегантными свойствами. Пармидин является
антагонистом брадикинина и благодаря этому ослабляет сокращение клеток эндотелия, уменьшает
промежутки между ними и препятствует проникновению атерогенных липопротеинов во внутреннюю
оболочку сосудов. Оказывает противовоспалительное действие, уменьшая отек эндотелия и липидную
инфильтрацию стенки сосудов, что способствует обратному развитию атеросклероза. Он также
уменьшает агрегацию тромбоцитов, стимулирует фибринолиз и снижает содержание холестерина в
крови. Применяют внутрь курсами по 2–3 мес. Обычно хорошо переносится. ПЭ: тошнота, головная
боль. кожные аллергические реакции.
Антигипоксанты и другие ЛС, улучшающие метаболизм в мозге. При недостаточности МК,
особенно острой ишемии мозга, ведущую роль играет кислородное голодание ткани и нарушение
энергетического метаболизма, прежде всего процессов окислительного фосфорилирования,
являющихся основным поставщиком энергий в клетках. Поэтому борьба с гипоксией и нормализация
Окислительных процессов являются одним из наиболее перспективных направлений защиты мозга от
ишемических повреждений. С этой целью используют антигипоксанты — вещества, облегчающие
реакцию организма на гипоксию. Эталонным представителем считают натрия оксибутират. В
седативной и снотворной дозах он увеличивает кровоснабжение мозга, утилизацию кислорода,
уменьшает образование молочной кислоты в ишемизировакной зоне и повышает устойчивость
нейронов к гипоксии.
Для борьбы с гипоксией и постишемическими повреждениями мозга используют ноотропные
средства, являющиеся производными гамма-аминомасляиной кислоты (аминалои, пирацетам,
пикамилон). ГАМК — естественный метаболит нервной ткани и выполняет функцию тормозного
медиатора. Поэтому производные ГАМК, наряду с высокой биологической активностью имеют низкую
токсичность и могут применяться длительными курсами лечения. Они увеличивают мозговой кровоток
и сказывают антигипоксическое действие, снижая функциональную активность нейронов и их
потребность в кислороде. Устойчивость нервных клеток в условиях ишемии я гипоксии повышается и
ускоряется восстановление нарушенных функций мозга. Защитное действие производных ГАМК
возрастает при комбинированном применении с энергоотдающими веществами (АТФ, креатинфосфат,
натрия сукцинат и др.).
Пикамилои — производное ГАМК и никотиновой кислоты. поэтому сочетает свойства
транквилизатора с избирательным действием на сосуды мозга и обмен веществ. Ноотропное действие
сочетается со стимулирующим влиянием на функции мозга. МД обусловлен взаимодействием с ГАМКрецепторами. Он ослабляет нейрогенные спазмы сосудов и восстанавливает МК, нарушенное
различными спазмогенами, оказывает благоприятное влияние на метаболизм, восстанавливает
физическую и умственную работоспособность а постишемическом периоде, при переутомлении и после
психоэмоционального стресса. В ЖКТ всасывается быстро, биодоступность — 50% (при в/м введении
— 90%). Легко проникает через ГЭБ. Многократно циркулирует между печенью и кишечником,
разрушаясь преимущественно микрофлорой кишечника. Метаболиты выводятся почками. Примеияют
при острых и хронических нарушениях МК легкой и средней тяжести, вегетососудистой дистонии, при
неврозах, астении, депрессии, для восстановления работоспособности. Хорошо переносится, иногда
возникают ПЭ (чувство тревоги, раздражительность, головокружение, головная боль, аллергия) при
длительном применении.
При возникновении нарушений МК на фоне гипертонического криза используют гипотеизивиые,
дегидратирующие, мочегонные, нейролептики, транквилизаторы с целью снижения АД,
предотвращения отека мозга и кровоизлияния в мозг. Проводят коррекцию водно-электролитного
баланса и кислотно-основного состояния.
Средства для лечения мигрени
Широко распространенной формой нарушений МК, особенно у женщин, является мигрень.
Основным патогенетическим фактором считают нарушение регуляции тонуса сосудов в бассейнах
наружной и внутренней сонных артерий, обусловленное дисфункцией вегетативной нервной системы.
У больных мигренью имеется гиперреактивность симпатоадреналовой системы и повышенная
чувствительность адренорецепторов мозговых сосудов к вазоактивным веществам. Важная роль
отводится также нарушению обмена нейротрансмиттеров и гормонов (пролактина, тиреотропного
гормона, половых гормонов). Ведущим фактором, провоцирующим приступ мигрени, является
психоэмоциональный стресс. В связи с этим профилактика и лечение приступов мигрени должны быть
комплексными. С этой целью используют адреноблокаторы (дигидроэрготамин, дигидроэрготоксин,
анаприлин), транквилизаторы (мезапам, сибазон, хлозепид) ноотропиые средства (аминалон,
пирацетам, пикамилон), аиальгетики (анальгин, парацетамол), антигистаминные препараты
(димедрол, супрастин и др.), сосудорасширяющие средства (кавинтон, компламии, циннаризин,
пентоксифиллин и др.).
Притивоатеросклеротичсские средства
Атеросклероз является основном причиной ишемической болезни сердца и мозга. Его развитие
связано с увеличением содержания в крови атерогенных липопротеинов. По величине и плотности
частиц они делятся иа 5 классов, из которых атерогеиными свойствами обладают липопротеины очень
низкой, низкой и промежуточной плотности. Увеличение концентрации липопротеинов очень высокой
плотности, наоборот, уменьшает опасность развития атеросклероза. В связи с этим лечение должно
быть направлено на уменьшение содержания атерогенных и увеличение антиатерогенных
липопротеинов. Это достигается с помощью гиполипидемических средств. Их подразделяют на
следующие группы:
1) ЛС, уменьшающие синтез атерогенных липопротеинов (клофибрат, безафибрат, фенофибрат,
гемфиброзин, ловастин, пробукол, кислота никотиновая, роникол); 2) ЛС, усиливающие распад и
выведение из организма атерогенных липопротеинов и липидов (холестирамин, колестипол,
декстротироксин, линетол, арахиден); 3) разные ЛС (антиоксиданты, гепариноиды и др.).
Основным принципом профилактики и лечения атеросклероза является сочетание специальной
диетотерапии и гилолипедемического препарата,
выбор которого зависит от типа
гиперлипопротеинемии.
Клофибрат (мисклерон, липомид) и его производные (безафибрат, фенофибрат, гемфиброзин)
применяют при всех типах гиперлипопротеинемий, за исключением 1-го, характеризующегося
увеличением в крови самых крупных частиц низкой плотности (хиломер). В организме они
превращаются в парахлорфеноксимаслянную кислоту, которая обладает гиполипидемической
активностью (снижает содержание липопротеинов низкой и очень низкой плотности, а при длительном
применении повышает содержание липопротеинов высокой плотности, препятствующих развитию
атеросклероза). Они также уменьшают агрегацию тромбоцитов, содержание фибрина и усиливают
фибринолитическую активность крови. Клофибрат всасывается в кишечнике хорошо, эффект
проявляется через 2–5 дней и достигав) максимума через несколько недель. Особенно эффективно
снижает содержание холестерина и триглицеридов. Малотоксичен. ПЭ: диспептические расстройства,
сонливость, сыпи, иногда лейкопения, образование желчных камней.
Ловастин — препарат микробного происхождения, избирательно угнетает синтез холестерина в
печени, что сопровождается снижением содержания в крови атерогенных липопротеинов, а также
небольшим увеличением антиатерогенных липопротеинов. Эффект развивается быстро и усиливается
при сочетании с холестирамином. Назначают внутрь. Максимальный эффект развивается через 2–4 ч.
Выводится преимущественно через ЖКТ. ПЭ возникают редко: диспептические расстройства, головная
боль, сыпи, миопатия. Противопоказания: беременность, заболевания печени, холестаз, миопатия.
Кислота никотиновая снижает преимущественно биосинтез триглицеридов и липопротеинов очень
низкой плотности, а при длительном применении повышает уровень липолротеинов высокой
плотности. Эффективна при всех типах гиперлипопротеинемии, за исключением 1-го. Для получения
эффекта назначают а высоких дозах, что способствует увеличению ПЭ (гиперемия кожи, зуд,
дислептические расстройства, язва желудка, нарушения функции печени, гипергликемия и др.). Легче
переносятся и дают меньше ПЭ ее производные: пиридилкарбинол (роникод), холексамнн,
ксантинола никотинат и др.
Декстротироксин (Д-тироксин) — правовращающий изомер тироксина. Усиливает распад
холестерина в печени и снижает содержание в крови липопротеинов низкой плотности (2-й и 3-й типы
гиперлипопротеинемии). Он повышает чувствительность миокарда к катехоламинам и способствует
развитию стенокардии. Этот эффект можно предупредить бета-адреноблокаторами. Назначают обычно
молодым лицам с пониженной функцией щитовидной железы.
Холестирамин, колестииол — ионообменные смолы, связывают в ЖКТ желчные кислоты. выводят
их с калом, уменьшают всасывание экзогенного холестерина и снижают содержание в крови
атерогенных липопротеинов. ПЭ: диспептические расстройства.
Линетол и арахиден — препараты ненасыщенных жирных кислот, увеличивают выделение
холестерина с желчью. Применяют в комплексной терапии гиперлипопротеинемии 2–5-го типов.
Противоатеросклеротическим действием обладают ангиопротекторы (пармидин и др.),
антиоксидаиты (токоферол, кислота аскорбиновая и др.), которые используют в комплексной терапии
атеросклероза.
В настоящее время в развитии атеросклероза большое значение придают снижению содержания
простациклина в крови и стенке сосуда, в результате чего возрастают адгезия и агрегация
тромбоцитов, которые выделяют вещества, повреждающие эндотелий сосудов. Это способствует
отложению липопротеинов и образованию атеросклеротической бляшки. В связи с этим идет поиск
синтетических аналогов простациклина, обладающих достаточным эффектом при приеме внутрь.
Таким образом, терапия атеросклероза должна быть комбинированной с применением ЛС,
обладающих разными механизмами действия.
Лекция 23
ЛС, ВЛИЯЮЩИЕ НА СИСТЕМУ КРОВИ
В эту группу входят ЛС, влияющие на кроветворение, и ЛС, влияющие на свертывание крови.
Для понимания их действия и применения необходимо знать следующие вопросы:
* классификация ЛС, влияющих на процессы кроветворения;
* основные препараты, стимулирующие и угнетающне эритропоэз, их МД и применение;
* характернстика средств, стимулирующих и угнетающих лейкопоэз;
* общие представления о свертывающей и антисвертывающей системах крови и пути воздействия на
них лекарствами;
* ЛС, повышающие свертывание крови (коагулянты), их МД и применеие;
* ЛС, угнетающие агрегацию тромбоцитов (антиагреганты), ИХ ПрИМеНеНИе;
* ЛС, понижающие свертывание крови (антикоагулянты): классификация, МД, принципы
применения, возможные ПЭ;
* ЛС, влияющие на снстему фибринолиза: ингибиторы и активаторы фибрннолиза, МД, показания к
назначению и ПЭ.
Средства, влияющие на кроветворение
Делятся на 2 группы: 1) ЛС, регулирующие эритропоэз {стимуляторы и ингибиторы) и 2) ЛС,
регулирующие лейкопоэз (стимуляторы и ингибиторы). Первые применяют при нарушениях
эритропоэза, вторые — лейкопоэза.
Стимуляторы эритропоэза усиливают синтез гемоглобина и продукцию эритроцитов, повышая их
содержание в крови. Их используют для лечения анемий. Анемии можно разделить на 4 группы: 1)
нормобластическая железодефицитная (гипохромная); 2) мегалобластическая гиперхромная; 3)
гипопластическая; 4) гемолитическая. В зависимости от вида анемий используют различные ЛС.
Средства для лечения железодефицитных анемий. Эти анемии характеризуются продукцией
нормальных эритроцитов, в уменьшенном количестве и с малым содержанием гемоглобина
(гипохромные). Основной причиной является дефицит железа при недостаточном поступлении с пищей,
нарушенном всасывании (низкая кислотность желудочного сока, воспалительные процессы а
кишечнике), при повышенной потребности (беременность), усиленном выведении из организма
(кровопотеря). Эти анемии встречаются наиболее часто. Для лечения используют препараты железа.
В кишечнике всасывается только двухвалентное (закисное) железо. Если в желудок поступает
трехвалентное (окисное) железо, оно в условиях кислой среды превращается в двухвалентное. Поэтому
при пониженной кислотности желудочного сока всасывание железа нарушается. В связи с этим лучше
использовать препараты двухвалетного железа, назначая их с хлористоводородной и аскорбиновой
кислотами для лучшего усвоения. Всасывание железа происходит преимущественно в 12-перстной
кишке. В клетках эпителия кишечника железо связывается с белком апоферритином, образуя комплекс
— ферритии, который в плазме крови отщепляет железо и оно присоединяется к в-глобулину
(трансферрину). В виде этого комплекса железо транспортируется в костный мозг и другие ткани, где
отщепляется и идет на построение гемоглобина, миоглобина, дыхательных ферментов или
депонируется в составе комплекса с апоферритином. Из организма железо выводится с калом, мочой,
потом, десквамированным эпителием кишечника. У женщин железо теряется также во время
менструаций.
Препараты железа (железа закисного сульфат, железа лактат и др.) назначают внутрь в капсулах
или драже со специальным покрытием, чтобы избежать образования сульфида железа, который
окрашивает зубы в черный цвет. Для лучшего усвоения их принимают до еды, сочетая с аскорбиновой и
хлористоводородной (соляной) кислотами. Всасыванию железа также способствуют фруктоза и
янтарная кислота, которые содержатся во фруктах. Указанные препараты всасываются лучше других
(до 15%). При приеме внутрь могут возникать раздражение слизистых, запор, так как железо связывает
сероводород, который является естественным стимулятором перистальтики кишечника.
Лечение считается эффективным, если суточный прирост гемоглобина составляет 1% от исходного.
Поэтому с учетом всасывания начальная доза железа сульфата составляет 0,8–1 г. Если при приеме
внутрь препараты железа малоэффективны, назначают препараты для парэнтерального введения
(ферковен, фербитол, феррум-лек и др.). Ферковен вводят в/в. При плохой переносимости ферковена
вводят в/м фербитол.
Стимулируют эритропоэз и способствуют усвоению железа препараты кобальта (коамид). Коамид
назначают п/к.
Средства для лечения мегалобластической анемии. Она характеризуется нарушением
эритропоэза, при котором наряду с уменьшением количества эритроцитов появляются их незрелые
формы (мегалобласты, мегалоциты, эритробласты) с повышенным содержанием гемоглобина
(гиперхромная анемия), характерные для эмбрионального типа кроветворения. Эта анемия (болезнь
Аддисона-Бирмера) была неизлечимой (злокачественной, пернициознрй), пока не установили ее
причину — дефицит витамина В12 (цианокобаламина) и фолиевой кислоты.
Для всасывания цианокобаламина (внешнего фактора Касла) необходим гликопротеин,
вырабатываемый слизистой пилорического отдела желудка (внутренний фактор Касла), с которым
цианокобаламин образует комплекс и в таком виде всасывается в тонком кишечнике. При недостатке
или утрате гликопротеина (резекция желудка, атрофия слизистой, заражение лентецом широким)
всасывание цианокобаламина нарушаетсяи возникает пернициозная анемия.
Витамин В12 поступает в организм с мясной и молочной пищей, с яйцами. В организме он входит в
состав ферментов всех клеток, но больше всего депонируется в печени. Его запасов хватает на 2–3 года,
поэтому алиментарный авитаминоз — крайне редкое явление. Цианокобаламин участвует во многих
биохимических процессах. Его можно рассматривать как стимулятор регенеративных процессов
вообще, в том числе и кроветворения. МД связан с участием цианобаламина в синтезе нуклеиновых
кислот и белка, в активации биологически активных веществ и окислительно-восстановительных
процессов. Применяют при мегалобластической, железодефицитной и гипопластической анемиях
разной этиологии, при лучевой болезни, заболеваниях печени, ЦНС, периферических нервов, после
тяжелых операций, инфекций, при дистрофии у детей. Вводят парэнтерально по 50–100 мкг, при
тяжелой анемии — 200–500 мкг. Можно комбинировать с фолиевой кислотой, препарами железа. ПЭ:
возбуждение, тахикардия, боли в сердце, аллергия.
Фолиевая кислота (витамин Вс) участвует во многих процессах (синтез метионина, серина, бетаина,
аминокислот, пуриновых и пиримидиновых оснований, нуклеиновых кислот). Применяют при
макроцитарной анемии, болезни спру, послеоперационной, лекарственной анемии, анемии беременных,
новорожденных, при лучевой болезни. При мегалобластической анемии она эффективна только в
сочетании с цианокобаламином.
Ингибиторы эритропоэза. Применяют при полицитемии, которая характеризуется повышенным
содержанием эритроцитов, в результате чего происходит сгущение крови, возрастает опасность
тромбообразования и затрудняется кпровоо6ращение. Для угнетения эритропоэза используют раствор
натрия фосфата, меченный фосфором-32 (радиактивный натрия фосфат). Его вводят внутрь или в/в и
дозируют в милликюри (мКи).
Стимуляторы лейколоэза. Значительное снижение числа лейкоцитов (лейкопения) возникает при
токсическом воздействии на костный мозг ядовитых и лекарственных веществ (бензол, мышьяк,
противопухолевые средства, бутадион, левомицетин и др.), ионизирующей радиации, микробных
токсинов и т.п., а также при усиленном разрушении лейкоцитоа антилейкоцитными антителами
(аллергический аграиулоцитоз). Лейкопения снижает устойчивость организма к инфекциям, поэтому
первыми проявлениями ее нередко бывают язвенно-некротические поражения полости рта и миндалин
инфекционной природы. Снижение числа лейкоцитов ниже 2000 а 1 мм представляет опасность для
жизни.
Развитие агранулоцитоза связано с угнетением синтеза нуклеиновых кислот и белков, необходимых
для построения клеточных структур. Поэтому а качестве стимуляторов лейкопоэза используют
производные нуклеиновых кислот: натрия иуклеинат (натриевая соль дрожжевой нуклеиновой
кислоты), пеитоксил (производное пиримидина), метилурацил (производное урацила), лейкоген и др.
Они стимулируют синтез нуклеиновых кислот и белка, усиливая лейкопоэз, процессы регенерации
(заживление ран, язв, ожогов, повреждений слизистых оболочек, печени и др.), а также повышают
синтез антител и активность макрофагов. Их назначают внутрь, парэнтерально и в мазях (метилурацил).
Противопоказаны при лимфогранулематозе и злокачественных новообразованиях костного мозга.
Ингибиторы лейкопоээа применяют при лейкозах и лимфогранулематозе. Они будут рассмотрены в
лекции по противоопухолевым средствам.
ЛС, влияющие на свертывание крови
К ним относятся: 1) ЛС, влияющие на агрегацию тромбоцитов; 2) ЛС, повышающие свертывание
крови (коагулянты); 3) ЛС, понижающие свертывание крови (антикоагулянты); 4) ингибиторы
фибринолиза; 5) стимуляторы фибринолиза.
Классическая теория Шмидта-Моравитца (1895–1905 гг) предполагала участие в процессе
свертывания крови 4-х основных факторов: а) протромбина — белка, синтезируемого в печени с
участием витамина К; б) тромбопластина — фермента, освобождающегося из тромбоцитов и некоторых
тканей при повреждении клеток; в) ионов кальция, постоянно присутствующих в крови; г) фибриногена
— белка крови, синтезируемого в печени.
В настоящее время известно, что этот процесс значительно сложнее и в нем участвуют несколько
десятков факторов. Одни обеспечивают адгезию и агрегацию тромбоцитов, другие — постоянную
готовность свертывающей системы вступить в реакцию коагуляции (прокоагулянты), третьи —
торможение свертывающей системы (антикоагулянты), четвертые — формирование тромба. Все эти
факторы находятся во взаимосвязи и динамическом равновесии, благодаря чему в нормальных
условиях кровь не свертывается.
Процесс тромбообразования проходит следующие стадии: 1) адгезия и агрегация тромбоцитов; 2)
активация тромбопластина; 3) превращение протромбина в тромбин; 4) превращение фибриногена в
фибрин и его полимеризация. Процесс этот сложный и включает активацию внутренней свертывающей
системы (фактор Хагемана, плазменный тромбопластин, аутопротромбин, антигемофильный глобулин
и др.) и внешней свертывающей системы (тканевой тромбопластин). Фибринолитическая система
включает превращение плазминогена в плазмин в результате высвобождения тканевого активатора. Она
тормозит избыточное образование тромба на конечной стадии. Система антикоагулянтов (тормозная
система) замедляет процесс свертывания крови (гепарин, антитромбин-3 и др.).
Средства, повышающие свертывание крови
Используют для остановки кровотечении, поэтому их называют гемостатиками. К коагулянтам
относятся: 1) нормальные компоненты свертывающей системы (витамин К, тромбин, фибриноген, ионы
Са++); 2) вещества, повышающие вязкость крови (желатин медицинский); 3) ЛС, уменьшающие
проницаемость сосудистой стенки и применяемые при капиллярных кровотечениях (адроксон,
растительные
препараты,
этамзилат);
4)
ингибиторы
фибринолиза
(аминокапроновая,
парааминометилбензойная кислоты, контрикал).
Препараты витамина К. Витамин К относится к жирорастворимым, поступает в организм с пищей
.и частично синтезируется микробами кишечника. Всасывание нарушается при недостаточном
поступлении желчи в кишечник (болезни печени и желчевыводящих путей), пои угнетении
микрофлоры антибактериальными ЛС, при хронических заболеваниях кишечника. Витамин К и его
заменитель викасол обеспечивают синтез протромбина и проконвертина в печени. Лечебный эффект
возникает через 12–18 ч. Суточная потребность в витамине К — 2 мг. Обмен происходит быстро,
поэтому при непоступление его в кровь через несколько дней развивается кровоточивость. Применяют
при дефиците витамина К и при передозировке антикоагулянтов непрямого действия. Витамин К и
викасол противопоказаны при повышенной свертываемости крови.
Тромбин и гемостатическая губка (препараты из крови человека) применяют местно для остановки
кровотечений из мелких сосудов. Раствором тромбина пропитывают марлевые салфетки, тампоны и
прикладывают к кровоточащей поверхности, а порошок губки наносят тонким слоем.
Фибриноген — белок плазмы человека, эффективен при пониженном содержании фибриногена в
крови (болезни печени, лучевая болезнь, кровопотери и т.п.). Выпускается во флаконах в виде порошка,
растворы готовят перед употреблением и вводят в/в капельно.
Препараты кальция. Ионы Са++ стимулируют образование тромбопластина, переход протромбина
в тромбин и полимеризацию фибрина. Назначают при гипокальциемии (напр., при переливании
цитратной крови), при повышенной проницаемости капилляров (лучевая болезнь, геморрагический
васкулит, кровотечения из легких, матки, пищевого канала), перед операциями. Используют кальция
хлорид (внутрь и в/в) и кальция глюконат (внутрь, в/м и в/в).
Желатин медицинский повышает вязкость крови. Назначают внутрь в виде 5–10% раствора или в/в
по 1 мл 10% раствора на 1 кг массы тела.
Средства растительного происхождения (лист крапивы, водяной перец, калина, арника, лагохилус
опьяняющий и др.) содержат дубильные вещества, витамины К, С, Р и др. Оказывают стабилизирующее
действие на сосудистую стенку и повышают прочность капилляров. Применяют в виде настоев,
отваров, настоек, экстрактов при хронических кровотечениях (маточных, кишечных и др.). С этой
целью используют также адроксон и этамзилат (синтетические средства), оказывающие
стабилизирующее действие на капилляры, улучшающие микроциркуляцию и оказывающие
гемостатический эффект.
Протамина сульфат — белковый препарат, антагонист гепарина. Назначают для нейтрализации
гепарина при передозировке. Вводят 1% раствор в/в. ПЭ: снижение АД, брадикардия, аллергия.
Противопоказан при гипотонии, тромбоцитопении, недостаточности надпочечников.
Ингибиторы фибринолиза. При активации фибринолиза нити фибрина быстро растворяются и
кровь не свертывается. Это связано с накоплением активаторов плазминогена (профибринолизина),
которые способствуют его превращению в активный плазмин (фибринолизин). Прямыми активаторами
плазминогена являются тканевые протеолитические ферменты (цитокиназы), которые освобождаются
лизосомами клеток при их повреждении, а также трипсин. Непрямыми активаторами являются
ферменты микробного происхождения (лизокииазы) стрептокиназа и др., которые влияют на
проактиватор плазминогена, превращая его в активную форму. Применяют кислоту
аминокапроновую, амбеи (препарат парааминометилбензойной кислоты) и контрикал. АКК и амбен
имеют структурное сходство с аминокислотой лизином, входящей в состав активатора плазминогена,
поэтому вступают с ним в реакцию и нарушают взаимодействие с плазминогеном, препятствуя его
превращению в плазмин. Контрикал угнетает непосредственно плазмин и другие протеолитические
ферменты (трипсин, калликреин). Ингибиторы фибринолиза проявляют высокую активность лишь при
кровотечениях на почве фибринолиза, которые часто носят угрожающий характер и требуют
неотложной терапии. АКК и амбен назначают внутрь и в/в. Они малотоксичны и хорошо переносятся.
Средства, понижающие свертывание крови (антитромботические)
К ним относятся антиагреганты, антикоагулянты и фибринолитики.
Процесс свертывания крови начинается с адгезии (прилипания к стенке сосуда в месте повреждения)
и агрегации (образования монетных столбиков) тромбоцитов. Эти процессы регулируются системой
тромбоксан-простациклин, которые образуются в процессе превращения арахидоновой кислоты.
Тромбоксаи А2 синтезируется в тромбоцитах. Он угнетает аденнлатциклазу и уменьшает содержание
цАМФ, что сопровождается повышением агрегации тромбоцитов и сужением сосудов. Аналогичным
действием обладают коллаген сосудистой стенки, тромбин, АДФ, серотонин, простагландии Е2,
катехоламины. Простациклин синтезируется а эндотелии сосуда. Он активирует аденилатциклазу и
увеличивает содержание цАМФ, что приводит к снижению агрегации тромбоцитов и расширению
сосудов. Аналогичным действием обладают гепарин, аденозин, АМФ, метилксантины, простагландин
Е1, антагонисты серотонина и др.
Антиагртанты — вещества, препятствующие агрегации тромбоцитов. По МД они делятся на
следующие группы: 1) средства, угнетающие циклооксигеназу (кислота ацетилсалициловая); 2)
средства, активирующие аденилатциклазу (простациклин); 3) средства, угнетающие фосфодиэстеразу
(дипиридамол); 4) антагонисты кальция (верапамил, нифедипин); 5) средства разного типа действия
(антуран и др.).
Кислота ацтилсалициловая (аспирин) угнетает циклооксигеназу, что приводит к уменьшению
синтеза эндопероксидов и их метаболитов — тромбоксана и простациклииа. Так как синтез
тромбоксаиа угнетается в большей степени, чем простациклина, это приводит к снижению агрегации
тромбоцитов. Циклооксигеназа тромбоцитов угнетается необратимо, поэтому антиагрегантиый эффект
продолжается несколько дней. Циклооксигеиаза сосудистой стенки восстанавливается через несколько
часов. Молодым людям препарат назначают в малых дозах, пожилым — в обычных.
Препараты простациклина неустойчивы в биологических средах, поэтому действуют кратковременно
(несколько минут). Это ограничивает их применение. Дипиридамол используют при коронарной
недостаточности. Антиагрегантный эффект связан с угнетением фосфодиэстеразы, накоплением цАМФ
и потенцированием действия аденозина. Механизм антиагрегантного действия антагонистов кальция
связан с блокадой входа кальция в тромбоциты, что приводит к снижению их агрегации. Антуран —
противоподагрическое ЛС, обладает антиагрегантным эффектом, но МД не совсем ясен. Предполагают,
что он связан с угнетением циклооксигеназы, уменьшением АДФ и серотонина.
Антиагрегаиты используют для профилактики тромбообразования. особенно при заболеваниях,
сопровождающихся наклонностью к гиперкоагуляции (инфаркт миокарда, нарушения мозгового
кровообращения, тромбофлебиты и др.), а также у лиц пожилого возраста.
Антикоагулянты делятся на: 1) антикоагулянты прямого действия, влияющие непосредственно на
факторы свертывания в самой крови (гепарин, натрия цитрат); 2) антикоагулянты непрямого действия,
влияющие на синтез факторов свертывания крови в печени (неодикумарнм, фенилин. синкумар).
Гепарии — ественный фактор, постоянно присутствующий в крови. Это полисахарид с
молекулярной массой 15–20 тыс., вырабатываемый тучными клетками. Благодаря наличию остатков
серной кислоты имеет сильный отрицательный заряд, способствующий его взаимодействию с белками.
МД гепарина включает 5 факторов: 1) уменьшает образование тромбопластина и превращение
протромбина в тромбин; 2) образует комплекс гепарин-антитромбин-3, который инактивирует
протромбин и превращение фибриногена в фибрин; 3) тормозит спонтанную полимеризацию
мономеров фибрина; 4) ослабляет ускоряющее действие катехоламинов и серотонина на свертывание
крови; 5) угнетает агрегацию тромбоцитов.
Гепарин активен не только в целом организме, но и при добавлении в кровь. При приеме внутрь он
разрушается, при п/к и в/м введении эффект непостоянен и могут возникать гематомы. Лучший эффект
— при в/в введении, он возникает сразу и продолжается 3–5 ч. Разрушается в печени ферментом
гепариназой. Метаболиты выводятся почками. Перед введением гепарина, затем каждые 4 ч в первые
сутки и 2 раза в сутки в дальнейшем необходимо определять время свертывания крови. Терапия
считается успешной, если время свертывания удлиняется в 2–3 раза. Инъекции делают каждые 4–6 ч.
Применяют для предупреждения и ограничения тромбообразования при инфаркте миокарда, тромбозе и
эмболии сосудов, при искусственном кровообращении во время операций на крупных сосудах, при
подключении аппарата искусственной почки, при переливании крови. Для лечения тромбофлебитов,
трофических язв его назначают местно а мази. ПЭ: аллергия, кровотечения, вызванные передозировкой.
При передозировке вводят протамина сульфат (1 мг нейтрализует 1 мг гепарина).
Натрия цитрат связывает ионы Са++ а крови, в результате чего снижается способность
тромбопластина вызывать превращение протромбина в тромбин и замедляется свертывание крови.
Используют для стабилизации крови при консервации, добавляя по 10 мл 4% раствора на каждые 100
мл крови. При переливании больших количеств такой крови возникает дефицит Са++ в организме,
который приводит к ухудшению работы сердца. Поэтому при переливании свыше 500 мл “цитратной”
крови на каждые 250 мл крови вводят в/в 5 мл 10% раствора кальция хлорида.
К антикоагулянтам прямого действия относится гирудин, вырабатываемый слюнными железами
медицинской пиявки. Он препятствует превращению фибриногена в фибрин.
Антикоагулянты непрямого действия делятся на а) производные оксикумарина (неодикумарин,
синкумар) и б) производные индандиона (фенилин). МД связан с конкурентным взаимодействием с
витамином К. В результате этого нарушается синтез протромбина и проконвертина в печени. Эти ЛС
эффективны только в целом организме. Они имеют длительный латентный период действия (18–48 ч).
Назначают внутрь, всасываются хорошо, действуют 2–4 дня и способны кумулировать. Выделяются
преимущественно почками в виде метаболитов, при этом. производные кумарина окрашивают мочу в
розовый цвет. Часть препаратов в неизмененном виде выделяется молоком, что необходимо учитывать
при грудном вскармливании ребенка. Показания: 1) тромбофлебиты, профилактика тромбообразования
после операций; 2) тяжелая стенокардия, инфаркт миокарда; 3) облитерирующий эндартериит.
Противопоказаны при геморрагическом диатезе, нефрите, язвенной болезни, эндокардите,
беременности, менструациях. Перед началом лечения и в процессе его надо определять время
свертывания крови и протромбиновый индекс, под которым понимают отношение нормального
протромбинового времени к протромбиновому времени в процессе лечения, выраженное в %%. Индекс
не должен быть менее 40%.
Наиболее частыми осложнениямн антикоагулянтной терапии являются кровоизлияния в подкожную
клетчатку, в слизистые оболочки, кровотечения, которые связаны с передозировкой. В этих случаях
назначают антагонисты — витамин К и викасоп, переливают кровь.
Фибринолитические средства способны растворять тромб (тромболитический эффект), что имеет
большое практическое значение. Фибринолизин – протеолитический фермент, постоянно
присутствующий в крови в неактивной форме (профибринолизин, или плазминоген). Ом лидирует нити
фибрина и предотвращает образование тромба. Вводят в/в капельио в изотоническом растворе натрия
хлорида обычно вместе с гепарииом. Стрептокиназа (стрептолиаза) — продукт гемолитического
стрептококка, стимулирует превращение плазминогена в плазмин. Вводят в/в капельио. Стрептодеказа
— препарат стрептокиназы пролонгированного действия (до 48 ч). Урокиназа — препарат из мочи,
действует подобно стрептокиназе, но меньше дает ПЭ. Применяется мало из-за сложности получения.
Фибринолитические ЛС эффективны только при свежих тромбах (не позднее 3 дней после
возникновения). Их применяют при тромбофлебитах, тромбоэмболии, инфаркте миокарда. Обязателен
контроль за фибринолитической активностью крови, содержанием фибриногена и плазмииогена. Они
противопоказаны при фибриногенопении, язвенной болезни. ПЭ: лихорадка, аллергические реакции.
Лекция 24
МОЧЕГОННЫЕ СРЕДСТВА. ПРОТИВОПОДАГРИЧЕСКИЕ СРЕДСТВА
Мочегонные ЛС (диуретики) — вещества, усиливающие выделение воды. солей и регулирующие
водно-солевой обмен. Их называют также салуретиками. Противоподагрические (урикозурические) ЛС
способствуют выведению солей мочевой кислоты (уратов) при нарушении пуринового обмеиа.
Необходимо знать следующие вопросы:
* основные причины возникновения отеков, требующие назначения диуретиков;
* механизмы мочеообразования и пути воздействия на них;
* классификация диуретиков, общая характеристика групп ЛС;
* МД, основные и ПЭ препаратов, угнетающих функцию эпителия почечных канальцев, их
применение;
* МД спиронолактона, применение калийсберегающих диуретиков;
* МД и фармакологические эффекты осмотических диуретиков, применение;
* кислотообразующие и диуретики растительного происхождения;
* сравнительная характеристика диуретиков и принципы их применения;
* МД, основные и ПЭ урикозурических ЛС, их применение.
Мочегонные средства
Основное значение в распределении и обмене воды принадлежит электролитам, особенно натрию.
Баланс электролитов находится под контролем гормонов коры надпочечников (прежде всего —
альдостерона) и антидиуретического гормона задней доли гипофиза (вазопрессина). Задержка воды с
образованием отеков происходит при нарушениях кровообращения, заболеваниях почек, печени, при
эндокринных заболеваниях (гиперальдостеронизм, гипотиреоз). Ведущую роль в развитии отеков
играет первичная задержка натрия, которая приводит к повышению осмотического давления и
вторичной задержке воды в тканях. Поэтому назначение диуретиков прежде всего преследует цель
удалить избыток натрия. Для понимания МД диуретиков необходимо знать механизмы
мочеобразования. Оно складывается из трех процессов: фильтрация, реабсорбция и секреция.
Фильтрация происходит а клубочках. Фильтрации подвергается почти вся плазма крови, за
исключением веществ, которые не проходят через калиллярную стенку (белки, липиды). Она зависит от
гидростатического давления крови (при снижении АД ниже 40 мм рт. ст. она прекращается),
онкотического давления и количества функционирующих клубочков. За сутки фильтруется около 150 л
воды и 1200 г натрия.
Секреция представляет активный процесс выделения в просвет каиальцев некоторых метаболитов
(мочевая кислота, калий и др.), многих ЛВ (пенициллииы, сульфаниламиды и др.) и имеет обменный
характер. Она осуществляется транспортными системами и требует затраты энергии.
Реабсорбция (обратное всасывание) происходит в канальцах. В норме реабсорбируется 99%
первичной мочи, следовательно, из 150 л в виде мочи выделяется лишь около 1,5 л воды и 5 г натрия.
Реабсорбция осуществляется против концентрационною градиента и идет с затратой энергии. Даже
небольшое угнетение реабсорбции приводит к значительному усилению диуреза. Реабсорбция является
ГЛАВНОЙ точкой приложения действия диуретиков.
Клетки почечного эпителия имеют 2 мембраны: одна (базальная) обращена в сторону паренхимы,
другая (апикальная) — в сторону просвета канальца. Натрий реабсорбируется в проксимальных
канальцах (активно и пассивно), в восходящей части петли Генле и в дистальных каиальцах.
Реабсорбция натрия через апикальную мембрану идет по концентрационному градиенту и не требует
затрате энергии, через базальную — против градиента концентрации, следовательно, с затратой
энергии. Ее источником является окисление и анаэробный гликолиз. Энергия аккумулируется в виде
АТФ. Главную роль а переносе натрия через базальную мембрану играет Na+, К+ —
аденозинтрифосфатаза, обеспечивающая расщепление АТФ.
Хлориды реабсорбируются пассивно в проксимальных канальцах, активно — в восходящем колене
петли Генле. Вода реабсорбируется только пассивно вслед за натрием, в основном, в нисходящем
колене петли Генле и в дистальных канальцах. Ее реабсорбцию регулирует вазопрессин, который
влияет на проницаемость мембран. Калий почти полностью реабсорбирует в проксимальных каиальцах,
а выделяется путем секреции в дисталъных каиальцах с помощью активного транспорта через
базальную мембрану и пассивно через апикальную мембрану. Реабсорбция натрия и калия регулируется
альдостероном.
Диуретического эффекта можно достигнуть следующими путями: 1) угнетением механизмов
активного транспорта через базальную мембрану; 2) уменьшением проницаемости апикальной
мембраны; 3) увеличением проницаемости апикальной мембраны для пассивного тока натрия; 4)
повышением осмотического давления в просвете почечных канальцев; 5) воздействием на
гормональную регуляцию реабсорбции натрия, калия и веды.
Существуют разные классификации диуретиков. По направленности действия их можно разделить
на следующие группы: 1) ЛС, угнетающие функцию эпителия канальцев — а) тиазидные (дихлотиазид,
циклометиазид) и нетиазидные (фуросемид, клопамид, оксодолин, диакарб, кислота этакриновая)
диуретики; б) органические соединения ртути (меркузал, промеран, новурит); в) ксантины (тамисал,
эуфиллин); г) производные птеридииа (триамтерен); 2) антагонисты альдостерона (спиронолактон); 3)
осмотические диуретики (маннит, мочевина); 4) кислотообразующие диуретики (аммония хлорид); 5)
средства растительного происхождения (листья толокнянки, хвощ полевой, березовые почки, ягоды
можжевельника и др.).
Эффективность диуретиков — зависит от того, на какой отдел нефрона они действуют. По
локализации действия различают: 1) диуретики, действующие преимущественна на клубочки и
увеличивающие скорость и объем фильтрации (сердечные гликозиды, эуфиллин, темисал); 2) на
проксимальные канальцы (диакарб); 3) на петлю Генле (дихлотиазид, циклометиазид, клопамид,
оксодолии — иа кортикальный сегмент; фуросемид, этакриновая кислота, ртутные диуретики — на
всем протяжении петли); 4) на дистальные канальцы (слиронолактон, триамтерен, амилорид).
Самыми сильными диуретинами являются препараты, действующие на всем протяжении петли Генле
(фуросемид, этакриновая кислота, ртутные диуретики), где происходит основная реабсорбция натрия и
хлора. Диуретинами средней силы считают препараты, действующие в кортикальном отделе петли
Генле (тиазидные и нетиазидные диуретики). К относительно слабым диуретинам относятся препараты,
действующие преимущественно на клубочки, проксимальные и дистальные канальцы. Осмотические
диуретики действуют на протяжении всего канальца, но их эффект зависит от степени дегидратации
тканей и может быть сильным, средним и даже слабым.
Средства, угнетающие функцию эпителия почечных канальцев
Это основная группа диуретиков, МД которых связан с угнетением реабсорбции натрия, хлора и
воды. Дихлотиазид и циклометиазид являются производными бензотиазина и относятся к числу
наиболее эффективных диуретинов. Они угнетают реабсорбцию натрия и хлора в корковом сегменте
петли Генле и в начальных отделах дистальных канальцев и увеличивают секрецию калия и кальция. В
то же время они задерживают выведение мочевой кислоты, что может усилить подагру. Эффект
проявляется при ацидозе и алкалозе. Хорошо всасываются в кишечнике, действие начинается через 30–
60 мин, достигает максимума через 2 ч и продолжается 8–12 ч. Привыкания не вызывают. При
гипертонии оказывают гипотензивное действие. ПЭ: гипокалиемия, для профилактики которой
применяют препараты калия, гипохлоремический алкалоз, диспепсия, слабость.
Оксодолии (хлорталидон, гигротон) и клопамид (бринальдикс) — нетиазидные диуретики,
обладающие более выраженным и продолжительным действием, чем дихлотиазид. Оксодолии
действует до 3 суток, клопамид — до 24 ч. По МД сходны с дихлотиазидом. Назначают внутрь,
привыкания не вызывают. ПЭ аналогичны дихлотиазиду.
Фуросемид и этакриновая кислота являются наиболее сильными диуретиками. Действуют на
протяжении петли Генле (“петлевые диуретики”). Угнетают активную реабсорбцию хлора и натрия,
увеличивая выведение калия. В диуретическом эффекте имеет значение также угнетение реабсорбции
натрия в проксимальных канальцах и увеличение клубочковой фильтрации за счет усиления почечного
кровотока. Выведение кальция увеличивают, а мочевой кислоты — задерживают. Активность не
зависит от ацидоза и алкалоза. Назначают внутрь и парэнтерально. При приеме внутрь фуросемид
действует через 20–30 мин в течение 3–4 ч, этакриновая кислота — через 60–90 мин в течение 8 ч. При
её введении эффект фуросемида развивается через 3–4 мин и продолжается 1,5–2 ч, а действие
этакриновой кислоты наступает через 15 мин и длится 3–4 ч. ПЭ: гипокалиемия, гипохлоремический
алкалоз. Применяют преимущественно для оказания неотложной помощи (отеки мозга, легких, тяжелые
отеки при сердечной недостаточности, острые отравления и др.).
Диакарб (фонурит) действует преимущественно на проксимальные канальцы. МД связан с
угнетением карбоангидразы в эпителии канальцев, у результате чего уменьшается образование
углекислоты с последующей диссоциацией на ионы водорода, обмен которых иа ионы натрия
снижается и натрия гидрокарбонат выводится с мочой. Моча приобретает щелочную реакцию, а
задержка водорода в крови приводит к развитию ацидоза. Диакарб значительно увеличивает выведение
калия и вызывает развитие гипокалиемии. Он понижает внутриглазное давление и секрецию
спинномозговой жидкости, что также связано с угнетением карбоангидразы. Всасывается в кишечнике
хорошо и действует 6–8 ч. При повторном введении эффект быстро ослабевает из-за развития ацидоза,
поэтому применяют по 3–4 дня с такими же перерывами. ПЭ: гипокалиемия.
Ртутные диуретики: меркузал, новурит, промеран. МД обусловлен способностью катиона ртути
связываться с сульфгидрильными группами ферментов, участвующих в транспорте электролитов через
канальцевые мембраны (сукцинатдегидрогеназа, транспортная АТФ-аза), а результате чего активность
их подавляется. Действуют преимущественно на проксимальные канальцы и восходящую часть петли
Генле, поэтому обладают сильным мочегонным эффектом. В связи с усиленным выведением хлора
моча становится кислой, а в крови развивается гипохлоремический алкалоз, который быстро снижает их
активность. В этом отношении они действуют противоположно диакарбу, поэтому при совместном
применении мочегонный эффект возрастает. Ртутные диуретмки усиливают выделение калия, но не
влияют на экскрецию аммиака, мочевой кислоты и натрия гидрокарбоната. Эффект развивается через
2–3 ч после введения и продолжается до суток. Введение аммония хлорида и калия хлорида вызывает
сдвиг рН крови в кислую сторону и восстанавливает активность ртутных диуретиков. Препараты ртути
токсичны и используются лишь в тех случаях, когда другие диуретики неэффективны. Они нарушают
функции почек, ЖКТ, нервной системы и противопоказаны при их заболеваниях.
Эуфиллин и темисал оказывают мочегонный эффект за счет улучшения почечного кровотока и
угнетения реабсорбции в проксимальных и дистальных канальцах. Действуют слабо и применяются при
нерезко выраженных отеках.
Триамтерен и амилорид действуют преимущественно на дистальные канальцы, угнетая
реабсорбцию натрия. Выведение калия не усиливают, поэтому относятся к калийсберегающим
диуретикам. При приеме внутрь максимальное действие развивается через 2 ч и продолжается 6–8 ч.
Обычно применяют в сочетании с диуретинами, вызывающими гипокалиемию. При передозировке
могут вызывать гиперкалиемию, азотемию, диспептические расстройства.
Антагинисты альдостерона
К ним относится спиронолактои (альдактон, верошпирон), МД которого связан со структурным
сходством с альдостероном — гормоном коры надпочечников, регулирующим минеральный обмен. Он
вступает с ним в конкурентные отношения, препятствуя синтезу ферментов пермеаз, регулирующих
обратное всасывание натрия и секрецию калия. При этом секреция калия и реабсорбция натрия
угнетаются, что приводит к диуретическому и калийсберегающему эффектам. Спиронолактон не влияет
на выведение мочевой кислоты и КОС, эффективен при ацидозе и алкалозе. Относится к диуретикам
слабого действия, но при гиперальдостеронизме эффект возрастает. Действие развивается через 2–5
дней. Применяют преимущественно при гиперальдостеронизме и в сочетании с диуретинами,
вызывающими гипокалиемию при длительном применении.
Осмотические диуретики
Маннитол и мочевина действуют на протяжении всего нефрона, но преимущественно в
проксимальных канальцах. При поступлении в кровь повышают осмотическое давление плазмы, в
результате чего жидкость из тканей переходит в кровь и возникает дегидратация, что имеет большое
значение при отеке мозга и легких, отравлениях. Фильтруясь в клубочках, они создают повышенное
осмотическое давление в канальцевой моче, затрудняющее реа6сорбцию воды и отчасти натрия, что и
приводит к мочегонному эффекту. На КОС крови не влияют. При в/в введении действие развивается
быстро. Маннитол (маннит) назначают только в/в, мочевину — в/в и внутрь. При нарушении
выделительной функции почек и острой сердечной недостаточности противопоказаны.
Кислотообразующие диуретики
Аммония хлорид в печени расщепляется с образованием мочевины и хлористоводородной кислоты,
которая вытесняет натрий из гидрокарбомата. Образовавшаяся углекислота выделяется легкими, а
содержание натрия гидрокарбомата падает, что приводит к развитию ацидоза. Этот эффект используют,
в основном, при возникновении гипохлоремического алкалоза (напр., при назначении ртутных
диуретиков). Мочегонное действие аммония хлорида слабое и зависит от образования мочевины и
натрия хлорида.
Диуретики растительного происхождения
В качестве мочегонных используют различные лекарственные растения, МД которых исследован
слабо. Они обладают умеренным эффектом, практически безвредны и применяются длительными
курсами при хронических заболеваниях. Применяют хвощ полевой, горицвет весенний, листья
толокнянки, березовые почки, ягоды можжевельника, ягоды земляники и др. в виде настоев,
отваров, настоек, экстрактов.
Диуретики показаны при отеках различного происхождения (заболевания ССС, почек, печени), при
острых отеках мозга,, легких, при гипертонической болезни, при отравлениях с целью ускорения
выведения яда из организма и т.д. Чтобы усилить положительный и ослабить отрицательные свойства
отдельных препаратов, используют комбинации диуретиков. Чаще всего комбинируют диуретики с
различным МД, учитывая при этом цель диуретической терапии: 1) маннитол с фуросемидом или
этакриновой кислотой — при форсированном диурезе (отравления, отек мозга, легких); 2) тиазидные и
нетиазидные диуретики с триамтереном, спиронолактоном, амилоридом — при длительном лечении
(сердечная недостаточность, гипертоническая болезнь) для профилактики гипокалиемии; 3) ртутные
диуретики с аммония хлоридом — для усиления мочегонного действия.
Противоподагрические средства
Уровень мочевой кислоты в крови здорового человека составляет 3–4 мг/%. При нарушении
пуринового обмена (подагра) содержание уратов возрастает до 6–14 мг/% и они начинают
откладываться в тканях (суставы, почки и др.), вызывая воспаление и образование почечных камней.
Для лечения подагры применяют: 1) ЛС, уменьшающие содержание мочевой кислоты в крови; 2)
противовоспалительные ЛС. К 1-й гр. относятся: 1) ЛС, увеличивающие выведение мочевой кислоты с
мочой (урикозурические) — этамид, пробеницид, сульфпиразон и 2) ЛС, уменьшающие образование
мочевой кислоты (аллопуринол).
Этамид и пробеницид оказывают урикозурический эффект за счет угнетения реабсорбции мочевой
кислоты и ее солей в почечных канальцах. Назначают при хронической подагре, мочекаменной болезни
с кристаллизацией уратов. ПЭ: диспептические расстройства. Сульфпиразон (антуран) в больших
дозах угнетает реабсорбцию мочевой кислоты в почечных канальцах. При его применении необходимо
обильное питье и прием натрия гидрокарбонта для подщелачивания мочи, чтобы предупредить
выпадение конкрементов в почках. ПЭ: диспептнческие расстройства, аллергия, образование камней в
почках. Уродаи — комбинированный препарат, повышающий растворимость уратов и их выделение.
Аллопуринол угнетает ксантиноксидазу и образование мочевой кислоты, содержание которой
нормализуется в крови через 7–10 дней, а полное рассасывание в тканях — через несколько месяцев.
ПЭ: диспепсия, аллергия, обострение подагры, иногда — угнетение кроветворения.
Для лечения острых приступов подагры применяют нестероидные и стероидные
противовоспалительные ЛС (см. лекцию 11). Специфическим противовоспалительным действием
обладает колхицин, МД которого связан с угнетением деления гранулоцитов и их миграции в очаг
воспаления, с уменьшением содержания гликопротеина, молочной кислоты и ферментов,
способствующих воспалительной реакции, с задержкой отложения кристаллов мочевой кислоты.
Действие развивается быстро и приступ купируется в течение нескольких часов. Хорошо всасывается в
кишечнике. Токсичен: тошнота, рвота, понос, боли в животе, угнетение кроветворения.
Противоподагрические ЛС рекомендуют использовать комбинированно, чтобы повысить
эффективность и уменьшить ЛЭ (напр., аллолуринол с антураном, колхицин с пробеницидом и т.п.).
Лекция 25
ЛС, ВЛИЯЮЩИЕ НА СОКРАТИТЕЛЬНУЮ АКТИВНОСТЬ МИОМЕТРИЯ
Подразделяются на: 1) ЛС, усиливающие ритмические сокращения матки; 2) ЛС, ослабляющие
сокращения матки; 3) ЛС, понижающие тонус шейки матки; 4) ЛС, повышающие тонус матки. Их
используют для регуляции родовой деятельности и остановки маточных кровотечений.
В лекции будут освещены следующие вопросы:
* общие представления о механизмах регуляции сокращений матки;
* МД окситоцина и препаратов, его содержащих, основные и ПЭ, применение;
* простагландины и их роль в регуляции сокращений матки, эффекты динопроста и динопростона,
показания к назначению;
* другие ЛС для стимуляции родовой деятельности, основные и ПЭ;
* ЛС, ослабляющие родовую деятельность, МД и показания к назначению;
* ЛС, применяемые для остановки маточных кровотечений, основные и ПЭ.
ЛС могут воздействовать на матку путем прямого влияния на гладкие мышцы или через нейрогенные
механизмы (адрено-, холино-, серотонино-, гистамино- и другие рецепторы). Ритмическая деятельность
матки ослабляется при блокаде а-АР и м-ХР и стимуляции в2-АР, усиливается при стимуляции а-АР, мХР и блокаде в2-АР. Чувствительность матки к нервно-гуморальным факторам уменьшается под
влиянием гестагенов, токоферола (витамин Е), магния, наркотических веществ, транквилизаторов и
возрастает под влиянием эстрогенов, ионов кальция и др.
Средства, усиливающие ритмические сокращения матки
К ним относятся окситоцин, дезаминокситоцин, питуитрин, гифотоцин, мамофизин, динопрост,
динопростон, пахикарпин, изоверин, прозерин. Они показаны при слабости родовой деятельности, для
нормализации инволюции матки в послеродовом и послеабортном периодах, при гипотонических
маточных кровотечения в раннем послеродовом периоде (окситоцин).
В гладких мышцах матки постоянно возникают потенциалы действия, которые иррадиируют по
миометрию и вызывают ритмические сокращения. Сила их зависит прежде всего от поляризации
клеточных мембран, на которую влияют эстрогены (при физиологическом уровне эстрогенов она
оптимальная, а при недостатке снижается) и гестагены (при увеличении содержания прогестерона
поляризация снижается). Вещества, увеличивающие проницаемость клеточных мембран для ионов,
повышают потенциал действия и усиливают сокращения матки (окситоцин, простагландины,
катехоламины, ацетилхолин и др.).
Окситоцин — гормон задней доли гипофиза. МД связывают со стимуляцией а-АР гладких мышц
матки, в результате чего возрастает ионный ток через мембраны и потенциал действия. В клетках
происходит накопление ионов кальция, которые активируют сократительный белок актомиозин.
Беременная матка более чувствительна к окситоцину, чем небеременная и с увеличением срока
беременности чувствительность возрастает, достигая максимума во время родов и в течение нескольких
дней после родов, в больших дозах окситоцин вызывает спастическое сокращение матки. Содержание
окситоцина увеличивается во время родов, сразу после них. при раздражении шейки матки, влагалища и
молочных желез. Он увеличивает секрецию молока за счет стимуляции выделения лактотропного
гормона гипофиза и прямого действия на эпителий желез. Наиболее эффективен при преждевременном
отхождемии околоплодных вод, при слабости родовой деятельности, связанной с атонией матки, при
гипотонических маточных кровотечениях. Дозируют в ЕД. Для стимуляции родов обычно вводят в/м в
индивидуально подобранных дозах (0,5–5 ЕД). Противопоказан при несоответствии размеров таза и
плода, при поперечном и косом положении плода, угрожающем разрыве матки, при наличии рубцов на
матке после кесарева сечения.
Дезамииоокситоцин — синтетический препарат, хорошо всасывающийся через слизистую полости
рта; Его применяют в таблетках по 50 ЕД за щеку до полного рассасывания (до 10 таб.). Для
стимуляции лактации назначают за 5 мин до кормленя.
Питуитрин — вытяжка из задней доли гипофиза, содержащая окситоцин и вазопрессин.
Присутствие вазопрессина вызывает сужение сосудов, повышение АД, уменьшение диуреза.
Применяют в тех же случаях, что и окситоцин, однако его не следует назначать при атеросклерозе,
гипертонии, заболеваниях сердца, тромбофлебитах, нефропатии беременных. Вводят п/к и в/м по 1–1,5
ЕД каждые 15–30 мин до наступления эффекта. Гифотоцин (питуитрин М) содержит меньше
вазопрессина, поэтому меньше влияет на ССС. Показания и противопоказания такие же, как: для
питуитрина. Маммофизин — экстракт из молочных желез и гипофиза (1:1). В 1 мл — 3 ЕД.
Применяют преимущественно для остановки маточных кровотечений, ускорения инволюции матки а
послеродовом периоде и стимуляции лактаций.
Простагландины образуются в различных органах и тканях из ненасыщенных жирных кислот
(арахидоновая и др.), стимулируют специфические функциональные структуры мембран и регулируют
метаболизм. Участвуют в регуляции гладких мышц, микроциркуляцни, секреции, работы сердца и т.п.
Наиболее выраженное влияние на матку оказывают простагландины F2-альфа (динопрост) и Е2
(динопростон), которые и применяют а акушерстве. Динопрост используют для стимуляции родовой
деятельности и вызывания аборта. Этот эффект в отличие от окситоцина проявляется в любые сроки
беременности и независимо от степени раскрытия шейки матки. Назначают в/в, в полость матки и
влагалища. Дозы подбирают индивидуально. Для стимуляции родов обычно вводят в/в капельно. ПЭ:
диспептические расстройства, тахикардия, бронхоспазм, повышение температуры, флебиты,
Противопоказания такие же, как для окситоцина, а также заболевания ССС, почек, печени,
бронхиальная астма, глаукома. Динопростон по действию и применению сходен с динопростом. Его
назначают внутрь и в/в капельно. Меры предосторожности и противопоказания такие же, как при
применении динопроста.
Пахикарпина гидройдид — ганглиоблокатор, повышающий тонус и усиливающий сокращения
матки. Он снижает АД, поэтому может назначаться роженицам, страдающим гипертонией. Вводят в/м и
п/к по 2–4 мл 3% раствора. Эффект возникает через 5–30 мин. Для усиления эффекта можно
одновременно назначать внутрь хинин по 0,2 г каждые 30 мин. В послеродовом периоде для ускорения
инволюции матки пахикарпин назначают внутрь по 0,1 г 2–3 раза в день. Противопоказан при
заболеваниях почек, печени, при стенокардии, нарушениях сердечной деятельности. Изоверин —
ганглиоблокатор, повышающий чувствительность матки к окситоцину. Применяют для стимуляции
родов и инволюции матки обычно в сочетании с окситоцином, питуитрином и др.
Стимулирующим действием на матку обладают также антихолинэстеразные средства (прозерин) и
бета-адреноблокаторы (анаприлин и др.).
Для расслабления шейки матки и облегчения течения родов используют атропина сульфат и
простагландины (динопрост, динопростон). Промедол также обладает способностью расслаблять
шейку матки наряду с болеутоляющим действием.
ЛС, ослабляющие сократительную активность миометрия
Применяют, главным образом, для задержки преждевременного наступления родов и ослабления
родовой деятельности при стремительных родах, чтобы предотвратить травмы родовых путей.
Используют бета2-адреномиметики (фенотерол), магния сульфат, наркотические ЛС. Фенотерол
(партусистен) оказывает токолитическое (ослабляющее) действие на матку за счет стимуляции бета2АР. Является эффективным средством для предупреждения преждевременных родов и не оказывает
отрицательного действия на плод. Вводят в/в капельно или внутрь. Может вызывать тахикардию,
мышечную слабость, противопоказан при пороках сердца, аритмиях, тиреотоксикозе, глаукоме. Магния
сульфат при парэнтеральном введении ослабляет сокращения матки, препятствуя входу кальция в
клетки. Средства для наркоза (азота закись, натрия оксибутират, фторотан) также ослабляют
сократительную активность миометрия и могут быть использованы для ослабления родовой
деятельности.
Средства, повышающие тонус миометрия
Применяют преимущественно при маточных атонических кровотечениях и для ускорения
инволюции матки в послеродовом и послеабортном периодах. МД связан со стойким повышением
тонуса матки и сжатием вследствие этого мелких сосудов миометрия.
Препараты спорыньи. Спорынья — грибок, паразитирующий на колосьях ржи. Он содержит сумму
биологически активных веществ, включая алкалоиды — производные лизергиновой кислоты.
Основными являются эрготамин и эргометрин. МД связан с прямым влиянием на гладкие мышцы
матки и, возможно, со стимуляцией альфа-АР. Вызывают длительное тоническое сокращение матки.
Эргометрин можно назначать внутрь. Эффект через 10–15 мин, продолжается несколько часов. При в/в
введение действие развивается сразу. Чувствительность матки к препаратам спорыньи зависит от ее
функционального состояния: на девственную матку они действуют слабее, чем на рожавшую, а на
беременную сильнее, чем на небеременную. Их можно назначать только после родов и отхождения
плаценты. Во время родов противопоказаны, так как спастическое сокращение матки может вызвать
отслойку плаценты, асфиксию и гибель плода. Противопоказаны также при стенокардии, спазмах
периферических сосудов, заболеваниях печени, почек, во время беременности. Выделяются с молоком,
поэтому их не следует назначать во время грудного вскармливания ребенка. ПЭ: тошнота, рвота, понос,
головные боли. При длительном применении могут возникнуть явления эрготизма в гангренозной и
судорожной формах, что связано со спазмом сосудов и повреждением эндотелия. Используют галеновы
(экстракт спорыньи густой), новогаленовы препараты (эрготал) м чистые алкалоиды (эргометрина
малеат, метил эргометрин, эргометрина гидротартрат). Эрготамин применяют также для лечения
мигрени, что связывают с ослаблением пульсации сосудов мозга и уменьшением раздражения
рецепторов мозговых оболочек.
Котарнина хлорид (стиптицин) также повышает тонус матки. Назначают внутрь и парэнтерально
при маточных кровотечениях. Выраженным кровоостанавливающим действием при атонических
маточных кровотечениях обладают окситоцин, питуитрин и просгагландииы. Окситоцин для остановки
кровотечений вводят в шейку матки сразу после отделения последа (плаценты), а затем в/м по 3–5 ЕД
2–3 раза в день. Применяют также растительные препараты в виде жидких экстрактов, настоек и
настоев: насгойка барбариса, экстракты пастушьей сумки, водяного перца, чистеца и др.
Лекция 26
ВИТАМИННЫЕ ПРЕПАРАТЫ
Главная роль витаминов состоит в активации процессов обмена веществ. Значение витаминов в
жизнедеятельности организма огромно, поэтому они интенсивно изучаются и широко используются в
различных областях медицины.
В этой лекции будут рассмотрены вопросы, касающиеся применения витаминов в качестве
ЛС:
* — история применения витаминов в медицине;
* — роль витаминов в процессах обмена веществ в организме;
* — виды нарушений витаминного обмена, основные виды витаминотерапии и
витаминопрофилактики;
* — классификация витаминных препаратов;
* — фармакологическая характеристика водорастворимых витаминов (В1, В2, В5, В6, В12, Вс, РР, С,
Р), их применение и ПЭ:
* — фармакинетческая характеристика жирорастворимых витаминов (А, Д, К, Е), применение и ПЭ;
* — комбинированное применение витаминных препаратов.
Первое дошедшее до нас описание авитаминоза относится к XV веку до н.э. В папирусе Эберса
содержится описание “куринной слепоты” и способа ее лечения (печенью черного петуха). Эта болезнь
связана с дефицитом витамина А, который в большом количестве содержится в печени. Плиний
Младший (I–II в.в. н. э.) описал цингу, возникшую среди римских легионеров во время войны с
германскими племенами. В средние века цинга стала бичом осажденных в крепостях (“лагерная
болезнь”) и моряков в дальних плаваниях. От цинги моряков погибло больше, чем во всех морских
сражениях средневековья. Но уже в XVI в. русские поморы знали, что от цинги можно избавиться с
помощью отвара хвои. С конца XVIII в. английским морякам стали выдавать лимонный сок и цинга на
кораблях почти исчезла. Однако лишь в 1930 г. Сент-Дьерди доказал, что причиной цинги является
недостаток в организме аскорбиновой кислоты, которую он назвал витамином С (от названия цинги —
скорбут). В 1933 г. был получен синтетический препарат витамина С. На кораблях японского флота
свирепствовала болезнь “бери-бери” (по японски — овца). Было установлено, что она возникает у
моряков, питающихся высококачественным полированным рисом. При использовании обычного риса с
добавками ячменя, овощей и мяса эта болезнь прекращалась. Впоследствии было установлено, что
причиной болезни является дефицит витамина В1.
Еще в 1880 г. Н.И.Лунин доказал, что помимо белков, жиров, углеводов и минеральных веществ
организму необходимы особые вещества, без которых наступает гибель. Эти вещества польский ученый
Функ (1911 г.) назвал витаминами (амины жизни). В настоящее время известно более 30 веществ,
обладающих свойствами витаминов. Раскрыта их структура, разработаны методы синтеза и создания
витаминных препаратов, способы обогащения продуктов витаминами, изучены их роль в организме,
клиника витаминной недостаточности, методы профилактики и лечения.
Витамины являются компонентами и катализаторами биохимических реакций. Они участвуют в
процессах ассимиляции и диссимиляции веществ, обеспечивая биохимический, физиологический и
морфологический гомеостаз организма. Витамины входят в состав ферментов в виде коферментов и
оказывают многообразное влияние на биохимические процессы, регулируя обмен белков, жиров,
углеводов, водно-солевой обмен. Потребность в витаминах меняется в зависимости от возраста, работы,
климата, характера питания и т.д. Чем тяжелее работа и нервно-психическое напряжение, тем выше
потребность в витаминах. У детей потребность выше, чем у взрослых, недостаток витаминов нередко
возникает при искусственном вскармливании. Потребность возрастает в условиях полярного и
тропического климата, при работе в горячих цехах, в период беременности и лактации и т.д.
При недостатке витаминов возникают гиповитаминозы и авитаминозы. Наиболее часто
встречаются гиповитаминозы, которые характеризуются неопределенной симптоматикой (быстрая
утомляемость, головная боль, слабость, понижение работоспособности, сопротивляемости к инфекциям
и другим заболеваниям, общее недомогание и т.п.). Авитаминозы являются наиболее ярким
проявлением витаминной недостаточности. Они характеризуются выраженной специфической
симптоматикой и обусловлены полным отсутствием или длительным значительным недостатком
витаминов. Без восполнения дефицита витаминов может довольно быстро наступить летальный исход.
Длительное
избыточное
применение
витаминов
нередко
сопровождается
развитием
гипервитаминозов, которые характеризуются специфическими для каждого витамина признаками.
Основными причинами дефицита витаминов являются: 1) пониженное содержание витаминов в
пище, обусловленное неправильной обработкой продуктов, их неполноценностью и т.п.; 2)
значительное возрастание суточной потребности в витаминах при беременности, лактации, инфекциях,
интоксикациях, тяжелой работе, экстремальных условиях и т.д. 3) нарушение всасывания витаминов
при заболеваниях ЖКТ, печени, желчевыводящих путей.
Витаминные препараты применяют с целью заместительной, адаптационной и фармакодинамической
терапии. Заместительная витаминотерапия применяется при лечении гиповитаминозов и
авитаминозов. Авитаминозы встречаются редко. Обычно врач имеет дело с гиповитаминозами, которые
возникают чаще как осложнение основного заболевания, поэтому их называют “вторичными” или
“эндогенными” гиповитаминозами, так как причина кроется в неспособности усваивать витамины из
пищи и утилизировать их в тканях. К факторам, способствующим развитию “вторичных”
гиповитаминозов, относятся: 1) заболевания органов пищеварения (около 75–80% больных страдают
.гиповитаминозами); 2) хроническая сердечная недостаточность, в результате которой развиваются
застойные явления в системе воротной вены, нарушаются, всасывание, депонирование и
биотрансформация витаминов; 3) хронические и острые инфекционные заболевания; 4) обширные
травмы, ожоги, опухоли. Адаптационная витаминотерапия используется для повышения адаптации
организма к экстремальным факторам внешней среды (полярный и тропический климат, подъем на
большую высоту, работа в горячих цехах, под водой, в космосе, длительное плавание и т.п.), а также
при некоторых состояниях, характеризующихся особенностями обмена веществ (беременность,
лактация, детский и старческий возраст). Во всех этих случаях необходимо дополнительное назначение
витаминных препаратов. Фармакодинамическая витаминотерапия применяется при лечении
заболеваний, не связанных с витаминной недостаточностью. Главное ее отличие от заместительной
терапии состоит в использовании витаминных препаратов в дозах, которые в десятки и сотни раз
превышают суточную потребность (напр., применение эргокальциферола по 100000 МЕ в сутки для
лечения туберкулезной волчанки кожи и слизистых оболочек).
Поскольку эндогенный гиповитаминоз почти всегда является комплексным. профилактика и лечение
его должны быть поливитаминными. Для этого используют различные поливитаминные препараты в
естественных соотношениях, часто с добавлением микроэлементов (декамевит, ундевит, гендевит и
др.). Дозы препаратов должны превышать суточную потребность в витаминах в 2–3 раза, а применение
должно быть курсовым. Необходимо соблюдать полноценное белковое питание, так как белки
способствуют усвоению витаминов.
Витамины принято делить на 2 группы: 1) водорастворимые и 2) жирорастворимые. К
водорастворимым относятся витамины В1 (тиамин), В2 (рибофлавин), РР (кислота никотиновая), В5
(кислота пантотеновая), В6 (пиридоксии), В12 (цианокобаламин), Вс (кислота фолиевая), С (кислота
аскорбиновая), Р (группа биофлавоноидов). К жирорастворимым относятся витамины А (ретинол), Д2
(эргокальциферол), Д3 (холекальциферол), Е (токоферол), К1 (филлохинон).
Препараты водорастворимых витаминов
Тиамии (витамин В1) содержится преимущественно в отрубях хлебных злаков, гороха, дрожжах и
др. После всасывания превращается в активную форму — тиамин-пирофосфат (кокарбоксилаза),
являющийся
коферментом
декарбоксилаз,
которые
обеспечивают
декарбоксилирование
пировиноградной и альфа-кетоглютаровой кислот и окисление глюкозы. При недостатке тиамина
нарушается углеводный обмен и происходит накопление кетокислот, что сопровождается невритами,
нарушениями функций ЦНС, ССС, мышечной слабостью, а в тяжелых случаях — парезами и
параличами, отеками, атрофией мышц, диспепсией (болезнь бери-бери). При дефиците тиамина при
беременности и лактации нарушается работа сердца у грудного ребенка, происходит задержка роста.
Применяют в виде тиамина бромида и тиамина хлорида, которые лучше усваиваются при в/м введении.
Показаны при гиповитаминозе В1, заболеваниях ЦНС и периферических нервов, при кожных
заболеваниях, интоксикациях, при повышенной потребности в витамине для профилактики
гиповитаминоза. Гипервитаминоз может возникнуть при передозировке и повышенной
чувствительности (тошнота, шум в ушах, головокружение, аллергия, иногда — шок).
Рибофлавин (витамин В2) содержится в печени, почках, яйцах, молоке, зерне, дрожжах. В
организме превращается в коферменты дегидрогеназ и оксидаз, участвующих в окислительновосстановительных процессах, обеспечивая окисление конечных продуктов обмена углеводов, жиров и
аминокислот. Гиповитаминоз характеризуется появлением трещин в углах рта и на губах (хейлоз),
поражением языка (глоссит), кожи возле носа и ушей, развитием кератита и конъюнктивита,
светобоязни, слезотечения, нарушением сумеречного зрения. У детей наблюдаются задержка роста,
судороги, иногда — анемия. Гипервитаминоз не возникает. Назначают внутрь, местно и парэнтерально
при гиповитаминозе, кератите, конъюнктивите, ирите, заболеваниях кожи, при инфекциях, лучевой
болезни и др.
Пиридоксин (витамин В6) содержится в зернах, мясе. рыбе и др. продуктах. После всасывания
превращается в пиридоксальфосфат, который участвует в обмене аминокислот, необходимых для
синтеза белков, ферментов, гемоглобина, в образовании глутаминовой, гамма-аминомасляной кислот,
серотонина и др. веществ, регулирующих функции ЦНС, усиливает синтез катехоламинов, усвоение
ненасыщенных жирных кислот, снижает уровень холестерина и липидов крови. Дефицит пиридоксина
развивается редко, напр., при лечении противотуберкулезными препаратами группы изониазида, при
беременности, переохлаждении, интенсивной физической работе. Он характеризуется развитием
дерматита, иногда судорог^ параличей, депрессии, анемии, хейлоза, глоссита. Назначают внутрь и
парэнтерально при нарушениях белкового обмена, кроветворения, при атеросклерозе, заболеваниях
ЦНС и периферических нервов, при токсикозах беременности, дистрофии, болезнях печени,
коллагенозах, детям при недоношенности, искусственном вскармливании, в период полового
созревания, при лечении изониазидом и антибиотиками.
Никотиновая кислота (витамин РР) в организме превращается в ннкотинамид, который участвует в
образовании
двух
коферментов
—
никотииамидадениндинуклеотид
(НАД)
и
никотинамидадениндинуклеотидфосфат (НАДФ), входящих в состав дегидрогеназ. Дегидрогенаэы
участвуют в окислительном фосфориллировании, выработке энергии и обезвреживании веществ в
печени. При дефиците витамина РР возникает пеллагра, характеризующаяся развитием диареи
(профузный понос), дерматита и деменции (слабоумия). Никотиновая кислота оказывает
сосудорасширяющее Действие, что используют при мигрени, эндартериитах, снижает содержание
холестерина и свободных жирных кислот, препятствует развитию атеросклероза. Назначают при
заболеваниях сердца, стенокардии, болезнях печени, при лучевой болезни, заболеваниях ЖКТ,
интоксикациях.
Кислота паитотеновая (витамин В5) содержится в большинстве растительных и животных
продуктов, а также синтезируется микрофлорой кишечника. Участвует в синтезе кофермента А,
регулирующего обмен жирных кислот, кетокислот, кортикостероидов, ацетилхолина и др.
Гиповитаминоз практически не возникает. Назначают в виде кальция пантотената внутрь, местно и
парэнтерально при невритах, невралгиях, аллергии, заболеваниях органов дыхания, язвах, ожогах и т.п.
Циаиокобаламии (витамин В12) синтезируется микробами и в большом количестве содержится в
печени и почках. Необходим для кроветворения, образования клеток эпителия, миэлина, процессов
регенерации. Гиповитаминоз характеризуется развитием мегалобластической анемии, глоссита,
атрофии слизистой, ахилии, нарушений нервной системы. В желудке образует комплекс с
гликопротеином (внутренний фактор Касла) и в таком виде всасывается, накапливаясь в печени.
Применяют в инъекциях при мегалобластической анемии, заболеваниях нервной системы, инфекциях,
лучевой болезни, для стимуляции репаративных процессов в период заживления. (См. лекцию 25).
Кислота фолиевая (витамин Вс) содержится в свежих овощах, яйцах, печени, сыре и т.д. В
организме превращается в тетрагидрофолиевую кислоту, которая участвует во многих обменных
процессах (синтез пуринов, пиримидинов, аминокислот, гистидина, метионина). При дефиците ее
возникает макроцитариая анемия, лейкопения, агранулоцитоз, тромбоцитопения, глоссит, стоматит,
гастрит, энтерит. Назначают внутрь при этих состояниях, а также при болезни спру и
мегалобластической анемии у беременных и детей.
Кислота пангамовая (витамин В15) относится к витаминоподобным веществам. Она служит
донатором метильных групп и обладает антигипоксантным действием. Применяют в виде кальция
пангамата при дистрофии миокарда, стенокардии, атеросклерозе, заболеваниях печени, при лечении
алкоголизма.
Кислота аскорбиновая (витамин С) содержится в шиповнике, хвое, цитрусовых, овощах, ягодах и
т.д. Легко разрушается при термической обработке, под влиянием кислорода, металлов (особенно
меди). Участвует в окислительно-восстановительных процессах, в образовании соединительной ткани и
коллагена, кортикостероидов, тирозина, в превращении фолиевой кислоты в тетрагидрофолиевую,
препятствует образованию перекисей липидов (антиоксидантный эффект). При гиповитаминозе
наблюдаются порозность и ломкость сосудов, замедление регенерации, снижение устойчивости к
инфекциям, уменьшение работоспособности, процессов адаптации. Авитаминоз (цинга)
характеризуется разрыхлением соединительной ткани (гингивит, кровоточивость десен, выпадение
зубов, кровоизлияния в кожу, мышцы, слизистые оболочки), поражением сердца, печени, обострением
инфекций. Назначают внутрь и парэнтерально при дефиците витамина С, инфекциях, интоксикациях,
лучевой болезни, болезнях сердца, печени, почек и др. При длительном применении в больших дозах
может вызвать повреждение островкового аппарата поджелудочной железы и способствовать развитию
сахарного диабета, нарушать функцию почек и провоцировать развитие гипертонии.
Рутин (витамин Р) объединяет группу биофлавоноидов, содержащихся в зеленом чае, цитрусах,
шиповнике, черноплодной рябине и др. Вместе с витамином С участвует в окислительновосстановительных процессах и препятствует образованию перекисей липидов. Он уменьшает ломкость
и проницаемость капилляров, поэтому применяют при повышенной проницаемсоти сосудов
(капилляротоксикоз, геморрагический диатез), при лучевой болезни, аллергии, полиартритах.
Витамин U содержится в капусте, спарже, сельдерее, свежих томатах. Является донатором
метильных групп и участвует в окислительно-восстанавительных процессах. Применяют внутрь при
язвенной болезни желудка и 12-перстной кишки, гастритах, колитах для стимуляции процессов
регенерации.
Препараты жирорастворимых витамином
Ретинол (витамин А) содержится в животных продуктах (рыбий жир, печень, масло, молоко и Др.).
Он включает группу близких по структуре и действию веществ. Участвует в окислительновосстановительных процессах, синтезе мукополисахаридов, белков, липидов, родопсина. В пище
содержатся неактивные провитамины (каротины), которые в слизистой кишечника превращаются в
активный витамин А. Для его всасывания необходимы желчные кислоты, поэтому при недостатке
желчи (заболевания печени, желчных путей) развивается дефицит витамина А. Запасов витамина,
содержащихся в печени, обычно хватает на 2 года. У новорожденных его хватает на 2–3 мес, а у
недоношенных запасов почти нет. При дефиците витамина развивается гиперкератоз (избыточное
ороговение эпителия), сухость слизистых и кожи, дерматит, конъюнктивит, ксерофтальмия,
кератомаляция, бронхит и др.), нарушается синтез родопсина в сетчатке глаза и расстраивается
сумеречное зрение (гемералопия, или “куринная слепота”). В тяжелых случаях кератомаляция
(размягчение и некроз роговицы) может привести к слепоте. Поражения кожи и слизистых
сопровождаются инфицированием, воспалительными процессами, замедлением заживления ран и язв.
Может развиться гипохромиая анемия.
Применяют в виде ретинола ацетата, ретинола пальмитата, концентрата витамина А внутрь, в/м и
местно. Показания: витаминная недостаточность, нарушения ороговения кожи, слизистых, заболевания
роговицы и сетчатки, ожоги, обморожения, заболевания печени, желудка, беременность, лактация. При
передозировке препаратов возникает гипервитаминоз, который проявляется сонливостью, вялостью,
головными болями, пигментацией кожи, сыпями, патологическим разрастанием костей, болями в них,
увеличением печени, селезенки и диспептическими расстройствами.
Витамин Д представляет группу витаминов, из которых наиболее активными являются
эргокальциферол (витамин Д2) и холекальциферол (витамин Д3). Они содержатся в животных
продуктах, особенно а жире печени трески, тунца, палтуса, кита. Витамин Д, может синтезироваться в
коже под влиянием солнечного света. Основная роль витамина Д состоит в регуляции обмена кальция и
фосфора. Он влияет на всасывание кальция и фосфора а кишечнике, на минерализацию костей и
мобилизацию кальция из них. на реабсорбцию кальция и фосфора в почках. При недостатке витамина Д
развивается рахит, остеомаляция и остеопороз. При рахите до 90–100% кальция и 60–70% фосфора не
всасываются, поэтому для восстановления уровня кальция а крови он начинает усиленно выделяться из
костей, что приводит к их размягчению. Новорожденные получают витамин Д с молоком матери,
поэтому его препараты рекомендуют включать в ее рацион. Через 2–3 мес. после рождения
доношенным и через 2–3 нед. недоношенным младенцам начинают давать витамин Д для профилактики
рахита. Необходимо помнить, что коровье молоко и яйца содержат мало витамина Д.
Эргокальциферол применяют в виде драже, растворов в масле и спирте, дозируют в междуранодиых
единицах действия (МЕ). Взрослым назначают в условиях севера, подводникам, космонавтам, при
переломах для ускорения сращения отломков костей. При передозировке возникает гипервитаминоз,
который характеризуется отложением кальция в почках, сосудах, сердце, легких, кишечнике, ЦНС
(гиперкальциноз), что приводит к нарушению их функций. Для лечения назначают кортикостероиды,
витамины Е, С, А, В1, препараты магния и калия.
Токоферол (витамин Е) представляет группу веществ, из которых наиболее активным является
альфа-токоферол. Он содержится во всех продуктах, особенно в растительных маслах. Токоферол —
естественный аитиоксидаит, препятствующий образованию перекисей лилидов, которые повреждают
клеточные мембраны и способствуют развитию атеросклероза. Для его всасывания необходимы
желчные кислоты. Накапливается а гипофизе, семенниках, надпочечниках. У животных авитамноз Е
приводит к утрате репродуктивной функции, дистрофии скелетных мышц и миокарда. У человека
авитаминоз не возникает. Применяют раствор токоферола ацетата а масле при самопроизвольных
абортах, мышечной дистрофии, стенокардии, климаксе, ревматоидных артритах, для профилактики
атеросклероза, для адаптации к стрессовым ситуациям.
Витамин К состоит из группы витаминов, из которых наиболее активен витамин К1 (филлохинон).
Содержится в шпинате, капусте, тыкве, печени и др., а также синтезируется микрофлорой кишечника.
Основная роль — синтез в печени факторов свертывания крови (протромбина, проконвертина и др.).
Поэтому дефицит витамина К приводит к снижению свертывания крови и кровоточивости. Чаще всего
он возникает при заболеваниях печени и желчных путей. Витамин К и его синтетический заменитель
викасол применяют в качестве коагулянта при нарушениях свертывания крови (см. лекцию 23).
Поливитмииные препараты
При взаимодействии многих витаминов их лечебно-профилактическое действие усиливается, а ПЭ
уменьшаются. Поэтому широко используют различные комбинации витаминных препаратов, учитывая,
что гиповитаминозы чаще всего связаны с поливитаминной недостаточностью. Создано много готовых
лекарственных форм поливитаминных препаратов, нередко с добавлением микроэлементов,
аминокислот и др. веществ (“Пентовит”, “Пангексавит”, “Декавит”, “Аэровит”, “Ундевит”,
“Декамевит”, “Глутамевит” и др.).
Лекция 27
ГОРМОНАЛЬНЫЕ СРЕДСТВА
Гормоны — это биологически активные вещества, вырабатываемые эндокринными железами. Они
регулируют процессы размножения, роста, развития организма и моделируют его защитные реакции.
Для них характерны высокая активность и специфичность действия.
Вам необходимо овладеть следующими знаниями:
* — общие принципы эндокринной регуляции организма;
* — механизмы взаимодействия между ГОрмонами и гормонов с органами-мишенями:
* — роль гормоноподобных веществ эпифиза и гипоталамуса в регуляции функций гипофиза;
* — классификация гормонов по химической структуре, виды препаратов;
* — основные виды гормональной терапии и принципы применения гормонов;
* — гормоны аденогипофиза, их роль, взаимодействие с эндокриннымн железами, виды препаратов,
применеие, возможные побочные эффекты;
* — гормоны нейрогипофиза, роль окситоцина и вазопрессина, их применеие, возможные ПЭ;
* — гормоны щитовидной железы, их синтез, влияние на обмен веществ, виды патологии,
применение при гипофункции щитовидной железы;
* — антитиреодные средства, классификация, основные и побочные эффекты;:
* — роль кальцитонина и гормона паращитовидной железы, применение, ПЭ.
Вместе с нервной системой железы внутренней секреции образуют сложный иейроэидокринный
комплекс, состоящий из 5 взаимодействующих уровней: 1) большие полушария, лимбикоретикуляриый комплекс и другие нервные центры; 2) гипоталамус и эпифиз; 3) гипофиз; 4)
периферические эндокринные железы; 5) органы-мишени. Посредниками между гипоталамусом и
гипофизом служат рилизинг-гормоны (либерины) и ингибирующие факторы (статины), а между
гипофизом и остальными железами — тропные гормоны гипофиза. Взаимодействие тропных гормонов
с другими эндокринными железами осуществляется через аденилатциклазную систему, сттимуляция
которой приводит к увеличению образования цАМФ, который, в свою очередь, через протеинкиназы
стимулирует синтез гормонов. Гормоны с кровотоком поступают к органам-мишеням и
взаимодействуют со специфическими рецепторами, расположенными на мембранах клеток или
внутриклеточно. Посредниками между рецепторами и внутриклеточными процессами обычно служат
аденилатциклаза, цАМФ и ионы кальция.
Основное влияние гормоны оказывают на транспорт через мембраны ионов и метаболитов и обмен
веществ. Воздействуя на генетический аппарат клеток, они изменяют функции и структуру органов.
Циторецепторы обладают избирательной чувстаительностыо к определенным гормонам. Напр.,
рецепторы матки чувствительны к окситоцину, рецепторы щитовидной железы — к тиреотропному
гормону и т.д.
Между гормонами существуют сииергидные и антагонистические взаимодействия. Известен
синергизм между тироксином и адреналином, эстрогенами и окситоцином. Антагонизм проявляется
между инсулином и адреналином, эстрогеиами и андрогенами. Эти взаимодействия необходимо
учитывать при комплексной гормонотерапии. Взаимодействие между гормонами может осуществляться
также путем усиления или торможения их синтеза. Напр., гормоны гипофиза стимулируют образование
гормонов других желез, а те, в свою очередь, тормозят выработку тройных гормонов гипофиза по
принципу обратной связи (“плюс-минус-взаимодействие”).
На функцию эндокринных желез мощное влияние оказывает ЦНС. Хорошо известно влияние стресса
на возникновение сахарного диабета, которое описал С.П.Боткин, на развитие тиреотоксикоза. на
половую потенцию и т.п. В свою очередь, эндокринная система оказывает, сильное влияние на ЦНС.
И.П.Павлов в экспериментах показал, что невроз легко возникает после кастрации, удаления
щитовидной железы.
Посредниками между нервными центрами и гипофизом являются гормоноподобные вещества,
вырабатываемые шишковидным телом (эпифизом). Одни из них стимулируют синтез гормонов
гипофиза (рилизинг-гормоиы, или либерины), другие тормозят (ингибирующие факторы, или статины).
Выработка их контролируется катехоламинами и серотонином. Поступая в гипофиз, они действуют на
специфические рецепторы его гормнообразующих клеток. Известны 7 либеринов и 3 статина.
Некоторые из них (напр., тиреотропин-рилизинг-гормон) используют для диагностики подбугорных и
гилофизарных форм тиреотоксикоза, при психических депрессиях.
Возникновение эндокринной патологии может быть связано: 1) с повышением или понижением
синтеза гормонов; 2) с нарушением нормального соотношения отдельных фракций гормонов (аномалии
обмена); 3) с нарушением транспорта гормонов: 4) с нарушением биотрансформации гормонов (напр.,
при заболеваниях печени).
По химическом структуре гормональные препараты делятся на: 1) вещества белкового и
пептидиого строения (препараты гормонов гипоталамуса, гипофиза, паращитовидной и поджелудочной
желез, кальцитонин); 2) производные аминокислот (тироксин, адреналин); 3) стероидиой структуры
(препараты гормонов коры надпочечников и половых гормонов).
Гормональные препараты бывают 4-х видов: 1) естественные, полученные в чистом виде (напр.,
инсулин); 2) синтетические (окситоцин, вазопрессии); 3) синтетические заменители, отличающиеся от
естественных гормонов по химической структуре (синестрол, преднизолон и др.); 4) органопрепараты
(экстракты желез, напр., питуитрин). Применяют для лечения эндокринных заболеваний
(реабилитационная, заместительная, стимулирующая терапия) и неэндокринных заболеваний
(адаптационная терапия, для повышения резистеитности организма, при инфекционно-аллергических
заболеваниях, при злокачественных опухолях, воспалительных процессах, коллагенозах, при сердечнососудистых заболеваниях, при инволюционных и психических болезнях и т.д.).
Для успешной терапии важен правильным подбор доз и курсов лечения. Необходимо помнить, что
при длительном применении больших доз гормональных препаратов возможна атрофия эндокринных
желез, в результате чего может возникнуть “синдром отмены” при внезапном прекращении лечения,
характеризующийся симптомами острой эндокринной недостаточности. Возможен также синдром
“обратного толчка” — резкое повышение активности эндокринной железы. Могут возникать
осложнения, связанные с чрезмерной гормональной стимуляцией (напр., гипогликемический шок при
передозировке инсулина).
Гормоны гипофиза
Гипофиз состоит из 3 долей: передней, задней и средней. В передней доле вырабатываются 6
тропиых
гормонов:
адренокортикотропный,
соматотропный,
тиреотропный,
фолликулостимулирующий, лютеинизирующий и лактотропный. Из образование регулируется
либеринами и статинами гипоталамуса. В средней доле содержится меланостимулирующий гормон, в
задней — окситоцин и вазопрессин. Передняя и средняя доли образуют аденогипофиз, задняя —
нейрогипофиз.
Синтез и выделение гормонов гипоталамуса и аденогипофиза регулируются по принципу обратной
связи: снижение содержания в крови гормонов стимулирует гипоталамо-гипофизарную систему, а
повышение — угнетает. Благодаря этому функции эндокринных желез и содержание гормонов
поддерживаются на оптимальном уровне.
Адренокортикотропный гормон (АКТТ) взаимодействует с рецепторами клеточных мембран в
коре надпочечников, в результате чего повышается активность аденилатциклазы, возрастает
содержание цАМФ в клетках и стимулируется синтез кортикостероидов из холестерина. АКТГ
усиливает преимущественно синтез глюкокортикоидов, поэтому его эффекты аналогичны этим
гормонам и будут подробно рассмотрены ниже. Таким образом, эффекты АКТГ опосредуются через
кортикостероиды и реализуются в регуляции углеводного, белкового, жирового и минерального
обмена. Применяют кортикотропин, получаемый из гипофизов убойного скота. Дозируют в ЕД, вводят
парэнтерально. Действует около 6 ч. Назначают обычно после длительного применения
глюкокортикоидов для восстановления функции коры надпочечников. Однако сам он также может
угнетать синтез рилизинг-гормона, что приводит к снижению синтеза АКТГ. ПЭ: отеки, повышение
АД, похудение, задержка регенерации, бессоница, обострение инфекций и др. Противопоказан при
тяжелой гипертонии, сахарном диабете, язвенной болезни, остром эндокардите, сердечной
недостаточности.
Соматотропный гормон (гормон роста) облдает видовой специфичностью. МД связан со
стимуляцией транспорта аминокислот, синтеза белка и распада жиров. Стимулирует рост скелета и
всего организма. Гиперсекреция гормона в период роста приводит к гигантизму, а после прекращения
роста — к акромегалии. Гипосекреция сопровождается нанизмом (карликовостью). Применяют в виде
соматотропииа при карликовости. Из-за сложности получения назначают редко. Является антагонистом
инсулина и может вызвать сахарный диабет. Соматостатин гипоталамуса из-за кратковременности
действия мало пригоден для лечения гигантизма и акромегалии. Для подавления гиперсекреции
гормона используют бромкриптин (дофаминомиметик).
Тиреотропный гормон (ТТГ) стимулирует секрецию гормонов щитовидной железы. Он влияет на
все стадии синтеза тироксина, рост и развитие железы. Применяют тиротропин (очищенный экстракт
передней доли гипофиза скота), который дозируют в ЕД и вводят п/к или в/м при гипофункции
щитовидной железы и для дифференциальной диагностики микседемы. Рилизинг-гормонам ТТГ
является протирелин, который используют для дифференциальной диагностики гипофункции
гипоталамуса или гипофиза при гипотиреозе.
К гонадотропиым гормонам гипофиза относятся фолликулостимулирующий и лютеинизирующий.
Фолликулостимулирующий у женщин стимулирует развитие фолликулов и синтез эстрогенов в
яичниках, а у мужчин — развитие семенных канальцев и сперматогенез. Применяют при половом
недоразвитии в виде гонадотропина менопаузного, получаемого из мочи женщин. Вводят в/м по 500–
1000 ЕД. Лютеинизирующий гормон стимулирует овуляцию и образование желтого тела в яичниках,
синтез и освобождение прогестерона и эстрогенов. У мужчин стимулирует развитие интерстициальных
клеток и синтез тестостерона. Применяют в виде гонадотропина хорионического, получаемого из
плаценты, назначают в/м В ЕД при бесплодии у женщин, при половом недоразвитии и крипторхизме
(задержка яичка в брюшной полости) у мужчин.
Лактотропиый гормон стимулирует развитие молочных желез и лактацию. Применяют в виде
лактина для усиления лактации в послеродовом периоде. Секреция гормона возрастает под влиянием
окситоцина.
Гормоном средней доли гипофиза является меланостнмулирующий, который повышает остроту
зрения и адаптацию к темноте за счет действия на сетчатку глаза. Препарат интермедин назначают при
дегенеративном ретините и куринной слепоте в глазных каплях в ЕД.
Гормонами задней доли гипофиза являются окситоцин и вазопрессин, представляющие пептиды.
Препараты окситоцина см. в лекции 25. Вазопрессин — антидиуретический гормон, регулирующий
реабсорбцию воды в почках и повышающий тонус гладких мышц, включая сосудистые. Увеличивает
проницаемость эпителия дистальных канальцев для воды и уменьшает диурез. Вазопрессорный эффект
проявляется под влиянием больших доз, в сотни раз превышающих антидиуретические. Применяют при
иесахарном диабете. С этой же целью назначают питуитрин и аднурекрин — экстракты из задней доли
гипофиза, содержащие вазопрессин.
Гормоны щитовидной железы. Антитиреоидные средства
Щитоводная железа продуцирует трийодтиронин, тироксин и кальцитонин. Синтез гормонов
проходит следующие этапы: 1) поглощение йодидов из крови и окисление их до йода; 2) присоединение
йода к аминокислоте тирозину и образование моно- и дийодтирозина; 3) образование трийодтиронина и
тироксина; 4) депонирование гормонов в составе белка тиреоглобулина. В кровь они поступают под
влиянием протеолитических ферментов, отщепляющих их от тиреоглобулина. Указанные процессы
регулируются тиреотропным гормоном гипофиза.
Трийодтиронин и тироксин стимулируют основной обмен, потребление кислорода, распад белков,
жиров, углеводов, холестерина, повышают температуру тела, усиливают действие адреналина.
Регулируют рост и развитие организма. При недостатке гормонов у детей возникает кретинизм, у
взрослых — микседема. Кретинизм характеризуется физическим и умственным недоразвитием, а
микседема — снижением обмена веществ, работоспособности, вялостью, апатией, отеками,
брадикардией. Для лечения этих состояний используют тироксин, трийодтиронина гидрохлорид и
тиреоидин. Действие тироксина развивается через 8–10 дней, трийодтиронина — через 1–2 дня. Он в
3–5 раз сильнее тироксина. Тиреоидин — препарат щитовидной железы, содержащий смесь гормонов.
Его сложно стандартизировать и дозировать, поэтому предпочтение отдают чистым гормонам. При
передозировке препаратов возникают повышенная возбудимость, потливость, тахикардия, тремор,
повышение температуры, снижение массы тела.
Антитиреоидные ЛС используют для лечения тиреотоксикоза (базедовой болезни), связанного с
гиперфункцией щитовидной железы. Они делятся на: 1) ЛС, угнетающие выработку тиреотропного
гормона гипофиза (препараты йода); 2) ЛС, угнетающие синтез гормонов щитовидной железы
(мерказолил); 3) препараты, нарушающие поглощение йода щитовидной железой (калия перхлорат); 4)
препараты, угнетающие митоз и разрушающие клеток фолликулов щитовидной железы (радиоактивный
йод). Йод и дийодтирозин снижает образование ТТГ, уменьшают массу щитовидной железы и ее
васкуляризацию. Это используют, главным образом, при подготовке к операции струмэктомии. Эффект
наблюдается 2–3 недели. Мерказолил назначают внутрь Под контролем состава крови, так как может
вызвать лейкопению и агранулоцитоз. Он вызывает также увеличение железы в связи с повышением
синтеза ТТГ по принципу обратной связи. Для предупреждения “зобогенного эффекта” применяют
препараты йода. Калия перхлорат применяют при нетяжелых формах тиреотоксикоза. Он также
угнетает кроветворение и хуже переносится. Радиоактивный йод используют для разрушения клеток
железы и угнетения их митоза. Эффект развивается медленно (через 1–2 мес). При избыточном
действии может возникнуть микседема.
Кальцитонии — полипептид, участвующий в регуляции обмена кальция. Он способствует фиксации
кальция в костях, снижая содержание кальция в крови. Применяют при остепорозе и иефрокальцинозе.
Гормон паращитовидной железы. Паратгормон регулирует обмен кальция и фосфора, повышая в
крови содержание кальция и снижая содержание фосфора. Уровень кальция возрастает в результате
декальцификации костей, улучшения всасывания кальция в кишечнике и реабсорбции в почках.
Снижение фосфора связано с уменьшением реабсорбции в почках. Применяют паратиреоидин,
получаемый из паращитовидных желез скота. Дозируют в ЕД и вводят п/к и в/м. Действие начинается
через 4 ч и продолжается до 24 ч, поэтому при возникновении тетании для быстрого эффекта вводят в/в
кальция хлорид в сочетании с паратиреоидином.
Лекция 28
ГОРМОНАЛЬНЫЕ СРЕДСТВА (ПРОДОЛЖЕНИЕ)
В этой лекции будет продолжено изложение темы: “Гормональные средства”.
По этому разделу необходимо знать следующие вопросы:
* — история создания препаратов инсулина (Л.В. Соболев, Бантинг и Бест);
* — МД инсулина, основные эффекты, препараты и их применение;
* — синтетические заменители инсулина, классификация, МД, применение, ПЭ;
* — основные осложнения при применении противодиабетических средств;
* — роль глюкагона в регуляции обмена веществ и ССС, применение, ПЭ;
* — гормоны коры надпочечников, классификация, регуляция их синтеза;
* — препараты глюкокортикоидов, МД, основные эффекты, применение, ПЭ;
* — препараты минералокортикоидов, МД, эффекты и применение;
* — женские половые гормоны, МД эстрогенов и гестагенов, их эффекты и применение;
* — препараты мужских половых гормонов, МД, основные и побочные эффекты, применение;
* — контрацептивные средства, классификация, МД, эффекты и применение;
* — МД, основные и побочные эффекты анаболических стероидов.
Гормоны поджелудочной железы. Синтетические противодиабетические ЛС
Бета-клетки островков Лангерганса продуцируют инсулин, а альфа-клетки — глюкагон. Инсулин
снижает содержание сахара в крови, а глюкагон повышает. Наибольшее практическое значение имеет
инсулин.
Инсулин впервые обнаружил Л.В. Соболев (1901 г) и предложил принцип его получения. В 1921 г.
Бантинг и Бест на основании исследований Соболева разработали технологию получения чистого
инсулина. В 1963 г. был осуществлен его синтез. МД инсулина связывают с его способностью
обеспечивать перенос глюкозы через клеточные мембраны, превращение ее в глюкозо-6-фосфат и
увеличивать образование гликогена. Он также увеличивает синтез белков и жиров. Считают, что эти
эффекты обусловлены взаимодействием инсулина со специфическими рецепторами мембран
ннсулиночувствительных клеток. При недостатке инсулина или снижении чувствительности к нему
утилизация глюкозы уменьшается и развивается сахарный диабет, который характеризуется
повышением сахара в крови (гипергликемия) и появлением его в моче (глюкозурия). Возникают жажда,
полиурия, снижается содержание гликогена в печени и мышцах, нарушается обмен белков, происходит
неполное окисление жиров, увеличивается их содержание, в крови (липемия) и возникает
метаболический ацидоз (кетонемия). В тяжелых случаях может развиться диабетическая кома.
Введение инсулина при сахарном диабете сопровождается снижением сахара крови, накоплением
гликогена в тканях, исчезновением глюкозурии, полиурии и жажды. Нормализуются белковый и
жировой обмен, показателем чего служит уменьшение общего азота мочи и исчезновение кетоновых
тел из крови (ацетон, ацетоуксусная и бетаоксимаслянная кислоты). Прекращается исхудание больного.
Инсулин вводят п/к, реже в/м, а при диабетической коме — в/в. Дозируют в ЕД. 1 ЕД способствует
утилизации от 2 до 5 г глюкозы. Действует 4–6 ч, инактивируется инсулиназой печени. Инъекции
болезненны и на месте инъекции нередко возникает воспаление. Чувствительность к инсулину различна
и колеблется в широких пределах. Нередко вызывает образование антител, что приводит к утрате
активности и возникновению аллергических реакций. Существует множество препаратов инсулина
разной
продолжительности
действия,
имеющих
особенности
применения.
Препараты
пролонгированного действия (протамин-цинк-инсулин. и др.) Образуют дело в месте инъекции и
действуют около 24–40 ч. Однако эффект развивается медленно (через 3–6 ч), поэтому для неотложной
помощи (напр., при коме), они непригодны и чаще вызывают аллергию.
Пероральные гипогликемические средства являются синтетическими заменителями инсулина.
Они делятся на: 1) производные сульфонил-мочевины (бутамид, хлорпропамид, букарбаи, цикламид,
глибенкламид) и 2) производные гуанидииа (глибутид, фенформин). МД препаратов 1-й группы
обусловлен стимуляцией бета-клеток поджелудочной железы и увеличением образования инсулина, МД
препаратов 2-й группы — угнетением всасывания глюкозы в кишечнике и увеличением ее поглощения
мышцами (без увеличения образования гликогена). Препараты 1-й гр. обладают сходными эффектами и
отличаются по продолжительности действия и переносимости больными. Бутамид действует 12 ч,
хлорпропамид — до 2–3 сут. ПЭ: диспептические расстройства, аллергия, угнетение кроветворения и
функции печени. При их применении усиливается непереносимость алкоголя, поэтому употреблять его
запрещается. Назначают при сахарном диабете легкой и средней тяжести у больных старше 40 лет.
Детям, в юношеском и молодом возрасте, а также при тяжелых формах диабета неэффективны из-за
органического поражения островкового аппарата, поэтому противопоказаны. Глибутид и фенформин
тормозят всасывание глюкозы в кишечнике и усиливают поглощение ее мышцами, не влияя на синтез
инсулина. Нормализуют обмен белка, способствуют снижению массы при ожирении за счет подавления
аппетита и синтеза жиров. Назначают при сахарном диабете умеренной степени, при резистентности к
инсулину и производным сульфонилмочевины. ПЭ: тошнота, рвота, понос. Дозируют в зависимости от
содержания сахара в крови и моче. Дозы всех гипогликемических средств должны быть такими, чтобы
обеспечить стойкое снижение сахара крови до нормального уровня. Обязательным условием терапии
является диета с ограничением углеводов.
Типичным ПЭ для всех портиводиабетических ЛС является гипогликемия, развивающаяся при
передозировке препаратов или нарушении пищевого режима. Наиболее тяжелым осложнением является
гипогликемический шок. Для устранения гипогликемии назначают сахар или белый хлеб внутрь (при
легкой степени), глюкозу в/в, адреналин, глюкагон.
Глюкагон — гормон альфа-клеток островков Лангерганса полипептидной структуры. Секрецию его
стимулируют гормон роста и белки пищи, а угнетают углеводы. Является антагонистом инсулина и
повышает сахар крови, снижая чувствительность тканей к инсулину, усиливая распад гликогена и
угнетая его отложение в печени. МД связан с активацией аденилатциклазы и накоплением цАМФ, что
сопровождается повышением активности фосфорилазы и угнетением гликогенсинтетазы. Глюкагон
стимулирует работу сердца, увеличивая ЧСС, сердечный выброс и проводимость. Он также,
увеличивает секрецию адреналина из надпочечников, гормона роста из гипофиза и тиреокальцитонина
(возникают гипокальциемия и гиперкальциурия). Действует кратковременно (период полураспада — 7
мин), так как быстро разрушается глюкагоназой. Применяют в/м и в/в при гипогликемической коме,
острой сердечной недостаточности и кардиогенном шоке.
Гормоны коры надпочечников
Имеют стероидную структуру и общее название — кортикостероиды. Подразделяются на
следующие группы: 1) глюкокортикоиды (гидрокортизон, кортизон, 11-дегидрокортистерон,
кортикостерон); 2) минералокортикоиды (альдостерон, 11-дезооксикортикостерон, 11-дезокси-17оксикортистерон); 3) половые гормоны (андростерон, андростендион, эстрон, прогестерон). Образуются
из холестерина или ацетилкоэнзима А. Этот процесс контролирует АКТГ гипофиза. Наиболее сильно
АКТГ влияет на синтез глюкокортикоидов. Синтез минералокортикоидов, в основном, зависит от
объема тканевой жидкости и содержания в крови натрия и калия, а также от системы ренин-
ангиотензин.
Глюкокортикоиды относятся к жизненно необходимым гормонам. Они легко прониакают через
мембраны и в клетках взаимодействуют со специфическими рецепторами, изменяя активность многих
ферментов. Результатом является изменение синтеза и обмена нуклеиновых кислот и белков. Основное
действие направлено на углеводный и белковый обмен и в меньшей степени на водно-солевой.
Действие на углеводный обмен проявляется уменьшением утилизации глюкозы из крови и увеличением
ее образования в печени, в результате чего возрастает содержание сахара в крови (гипергликемия), а
затем и в моче (глюкозурия). Таким образом, глюкокортикоиды являются антагонистами инсулина и
могут вызвать развитие сахарного диабета. Они также усиливают синтез глюкозы из аминокислот, что
приводит к снижению синтеза белка и ускорению выведения азота с мочой (отрицательный азотистый
баланс). Угнетение синтеза белка сопровождается замедлением регенеративных процессов,
заживления ран и язв, угнетением образования антител (иммунодепрессивный эффект). Влияние на
жировой обмен проявляется мобилизацией лилидов тканей, увеличением содержания недоокисленных
жирных кислот (кетоацидоз) и перераспределением жира (накопление на шее, плечах, лице —
“луноподобное лицо”). Влияние на водно-солевой обмен характеризуется задержкой натрия и воды за
счет усиления реабсорбции в почках, увеличением выведения калия с мочой, угнетением всасывания
кальция в кишечнике и увеличением его выведения почками. Следствием этих эффектов является
развитие гипертензии, гипокалиемии, гипокальциемии и остеопороза. Они также тормозят
пролиферацию миелоидной и лимфоидной ткани, снижая содержание лимфоцитов и эозинофилов,
оказывают выраженное противоспалительиое действие, связанное с угнетением синтеза
простагландинов, оксикислот и лейкотриенов, контролирующих миграцию лейкоцитов в очаг
воспаления. При этом происходит стабилизация мембран лизосом, уменьшается выход в цитоплазму
протеаз, играющих важную роль в воспалении, снижается проницаемость капилляров и экссудация
плазмы.
Иммунодепрессивное действие глюкокортикоидов объясняют угнетением Т-лимфоцитов,
макрофагов и цитотоксичности определенных популяций Т-лимфоцитов (так называемых “киллеров”).
Они угнетают также взаимодействие антигенов с антителами. Иммунодепрессивные и
антиаллергические свойства используют при лечении бронхиальной астмы, системной красной
волчанки, гемолитической анемии, узелкового периартериита и др. Однако это способствует
распространению инфекций в организме, для профилактики которых необходимо назначать
противомикробные средства.
Глюкокортикоиды оказывают выраженное влияние на ССС: усиливают работу сердца, повышают
тонус сосудов и АД за счет повышения чувствительности к катехолаоминам, активации ренинангиотензиновой системы, задержки натрия и воды. Поэтому они провоцируют развитие
гипертонической
болезни.
При
шоке способствуют
преодолению
сердечно-сосудистой
недостаточности. Используют гидрокортизон и его эфиры (ацетат, сукцинат), кортизона ацетат и
синтетические заменители: преднизолон, дексамметазои, триамцинолон, синафлан, флуметазона
пивалат, бекламетазона дипропиоиат и др. Их применяют внутрь, парентерально и местно. В/в и в/м
вводят водорастворимые препараты по экстренным показаниям. Синтетитческие аналоги и
производные естественных гормонов сходны по свойствам с гидрокортизоном, но отличаются
соотношением противовоспалительного действия и влияния на водно-солевой обмен. Преднизолон по
противовоспалительной активности превосходит гидрокортизон в 3–4 раза, но меньше задерживает
натрий, поэтому реже вызывает отеки и повышение АД. Дексаметазон и триамцииояон —
фторсодержащие
производные
преднизолона.
Первый
превосходит
гидрокортизон
по
противоспалительной активности в 30 раз, второй — в 5 раз. На водно-солевой обмен почти не
действуют. Они хорошо всасываются через кожу, поэтому при местном применении в мазях могут
оказывать резорбтивное действие. Синафлан и флуметазона павалат через кожу почти не всасываются.
Обладают высокой противовоспалительной, противоаллергической и противозудной активностью. Их
широко применяют местно. Так как они снижают сопротивляемость к инфекции, их сочетают с
противомикробмыми ЛС (с неомицином и др.): “Синалар-Н”, “Локакортен-Н” и др. К препаратам,
плохо всасывающимся через слизистые оболочки, относится беклометазона дипропионат, который
используют в виде ингаляций при бронхиальной астме и вазомоторных ринитах (полинозах).
Глюкокортикоиды применяют при многих заболеваниях. Прямым показанием является
недостаточность надпочечников (аддисонова болезнь). Но наиболее часто их назначают как
противовоспалительные, противоаллергические, десенсибилизирующие и иммунодепрессивные ЛС:
при ревматизме, коллагенозах, дерматитах, экземе, бронхиальной астме, сенной лихорадке и др.
инфекционно-аллергическмх заболеваниях, при анафилактическом шоке, при пересадке органов и
тканей и т.д ПЭ: отеки, гипертензия, гипокалиемия, стероидный сахарный диабет, обострение и
возникновение язвенной болезни желудка и 12-перстной кишки, остеопороз, обострение инфекционных
процессов, психические нарушения, угнетение кроветворения, ожирение и др. При внезапном
прекращении приема препаратов может развиться синдром отмены, характеризующийся симптомами
острой недостаточности надпочечников (гипокортикоидная кома).
Минералокортикоиды. Основным гормоном является альдостерон, регулирующий водно-солевой
обмен. МД связан с увеличением реабсорбции натрия и воды и усилением секреции калия в дистальных
канальцах
почек
в
результате
стимуляции
специфических
рецепторов.
Применяют
дезоксикортикостерона ацетат (ДОКСА) и дезоксикортикостерона триметилацетат. Их назначают
при хронической недостаточности надпочечников, при миастении и адинамии. ПЭ; отеки, повышение
АД.
Подовые гормоны и их синтетические заменители
Вырабатываются половыми железами и в небольших количествах — корой надпочечников.
Являются соединениями стероидной структуры. Основной функцией является формирование
вторичных половых признаков и продолжение вида. Они также участвуют в регуляции белкового
обмена. Функция половых желез и выработка ими гормонов контролируются гонадотропными
гормонами гипофиза.
Препараты женских половых гормонов. Эстрогены вырабатываются фолликулами, гестагены —
желтым телом. Основным гормоном фолликулов является эстрадиол. В период полового созревания
эстрогены обеспечивают развитие половых органов и вторичных половых признаков. Они избирательно
накапливаются в матке, влагалище и гипофизе, где взаимодействуют со специфическими рецепторами и
проявляют основное действие. Стимулируют синтез белка, увеличивают размеры клеток и
пролиферацию эпителия. Если эстрогены вырабатываются в недостаточном количестве, пролиферация
слизистой оболочки матки не происходит, менструации прекращаются и беременность становится
невозможной. Эстрогены обеспечивают 1-ю фазу менструального цикла — пролиферативную, поэтому
максимальная секреция их происходит в первые недели цикла, затем снижается и снова возрастает в
конце цикла. Вместе с гестагенами они обеспечивают отторжение слизистой оболочки (менструацию).
Во время беременности эстрогены образуются в плаценте; пик концентрации — в конце беременности.
Повышают чувствительность матки к окситоцииу, влияют на функции ЦНС, особенно вегетативных
центров. Поэтому во Время климакса нередко наблюдаются изменения психики и вегетативных
функций. В больших дозах подавляют рост гормонозависимых опухолей (рак простаты, вторичные
метастазы рака молочной железы). У мужчин этот эффект обусловлен прямым угнетением функций
половых желез и секреции гонадотропных гормонов гипофиза. Применяют преимущественно
эстрадиола дипропионат, который вводят в/м в маслянном растворе 1 раз в 2–4 дня. Эстрон
(фолликулин) получают из мочи беременных женщин. Он слабее эстрадиола. Самым активным
является этииилэстрадиол (в 50 раз активнее эстрона), назначают внутрь. Синтетическим заменителем
эстрадиола является синестрол, имеющий нестероидную структуру. Его назначают внутрь в табл. и в/м
в виде раствора в масле. Показания: аменорея (отсутствие менструаций), климактрические нарушения,
рак простаты, рак молочной железы у женщин старше 60 лет, подавление лактации. ПЭ: маточные
кровотечения, отеки, диспептические расстройства, у мужчин — феминизация, снижение полового
влечения, импотенция. Противопоказания: опухоли половых органов и молочных желез у женщин до
60 лет, маточные кровотечения, эндометрит.
Антиэстрогенные средства являются антагонистами эстрогенов, так как блокируют изс рецепторы,
увеличивают образование рилизинг-факторов гонадотропных гормонов, которые стимулируют
функцию яичников. Поэтому кломифена цитрат применяют при лечении бесплодия у женщин и рака
молочной железы.
Гестагены вырабатываются желтым телом, которое формируется на месте лопнувшего фолликула.
Основным гормоном является прогестерон. Он выделяется во 2-й половине менструального цикла, а
после оплодотворения яйцеклетки — весь период беременности. Основная роль — обеспечение
условий для имплантации оплодотворенной яйцеклетки и нормального течения беременности. Это
достигается следующими эффектами: 1) переход слизистой оболочки матки из фазы пролиферации а
фазу секреции и ее поддержание для дальнейшего развития эмбриона; 2) подавление созревания других
яйцеклеток; 3) снижение чувствительности матки к окситоцину. Прогестерон назначают в/м,
заменителем является прегнин, который вводят сублингвально. Применяют при аменорее, для
профилактики выкидыша, при нарушениях менструаций.
Препараты мужских подовых гормонов (андрогены). Тестостерон обеспечивает формирование
половых признаков, а после полового созревания регулирует сперматогенез и половую потенцию. Он
стимулирует синтез белка (анаболическое действие), тормозит рост гормонозависимых опухолей у
женщин (рак молочной железы, яичников). Назначают тестостерона пропионат и тестостерона
энантат (тестэнат) в/м: первый — 1 раз в 2 дня, второй — 1 раз в 3–4 недели. Синтетический
заменитель — метилтестостерон, который назначают сублингвально в таблетках. Применяют при
половом недоразвитии, импотенции, мужском климаксе, при раке молочной железы и яичников (у
женщин до 60 лет). При назначении женщинам могут вызвать мускулинизацию (вирилизм).
Контрацептивные (противозачаточные) средства
Предупреждают возникновение беременности и используются для регуляции рождаемости.
Подразделяют на 2 группы: 1) комбинированные эстрогенгестагенные препараты (бисекурин, овидон и
др.); 2) препараты, содержащие микродозы гестагенов (континуин). МД бисекурина и овидона состоит
в угнетении овуляции в результате подавления секреции гонадотропных гормонов гипофиза, что
приводит к изменению яичников и матки, препятствующему имплантации яйцеклетки. При правильном
применении они обеспечивают 100% предупреждение беременности. После прекращения приема
препаратов репродуктивная функция восстанавливается полностью. На последующее развитие плода не
влияют. ПЭ: головная боль, головокружение, уплотнение молочных желез, тошнота, рвота, кровянистые
выделения из матки, увеличение массы тела и снижение полового влечения. Обычно возникают в
первые 1–2 мес и в дальнейшем исчезают или ослабевают. Противопоказаны при тромбофлебитах,
опухолях половых органов и молочных желез, болезнях печени, психозах, сахарном диабете,
нарушениях мозгового кровообращения. Их назначают также при ряде гинекологических заболеваний.
Континуин (этиндиола ацетат) содержит только гестагены. МД, по-видимому, связан с изменением
цервикальной слизи и угнетением проникновения сперматозоидов в матку. Тормозит также
продвижение яйцеклетка по маточным трубам и нарушает ее имплантацию в слизистой матки.
Препараты этой группы менее надежны, чем препараты 1-й гр., но меньше дают ПЭ. Возможны
нарушения менструального цикла, иногда — тошнота, головная боль, депрессия. После прекращения
приема репродуктивная функция восстанавливается через 3 месяца.
Анаболические стероиды
По влиянию на обмен веществ сходны с андрогенами. Они стимулируют синтез белка, задерживают
выведение азота, фосфора, кальция. Это сопровождается увеличением массы скелетных мышц, костной
ткани, паренхиматозных органов, ускорением регенерации, повышением аппетита. К ним относятся
феноболин (дураболин, иероболил), ретаболил и метандростенолон (нерабол, дианобол). Феноболин
действует 7–15 дней, ретаболил — 3 недели. Действие развивается простепенно (через 1–3 дня).
Метандростенолон действует в течение 1 сут. и назначается 1–2 раза в день. Применяют при кахексии,
астении, после лучевой болезни, при остеопорозе, для ускорения регенерации тканей (напр., при
переломах), при длительном лечении глюкокортикоидами, при ишемической болезни сердца. ПЭ:
тошнота, отеки, маскулинизация у женщин.
Лекция 29
ЛС ДЛЯ РЕГУЛЯЦИИ ВОДНО-ЭЛЕКТРОЛИТНОГО БАЛАНСА. КИСЛОТНО-ОСНОВНОГО
СОСТОЯНИЯ И ПАРЭНТЕРАЛЬНОГО ПИТАНИЯ
Указанные ЛС широко применяют в медицинской практике, главным образом, для оказания
неотложной помощи при обезвоживании организма, нарушении осмотического равновесия, рН среды,
интоксикациях, тяжелых расстройствах кровообращения и дыхания и т.п.
Необходимо знать следующие вопросы:
• — роль воды. ионов щелочных, щелочно-земельных металлов, кислот и щелочен в поддержании
гомеостааа организма;
• — участие ионов натрия в регуляции осмотического давления и мембранных процессов, нарушения
натриевого обмена, препараты и их применение;
• — роль ионов калия в регуляции мембранных процессов, нарушения обмена калия, их коррекция,
препараты калия и их применение:
• — значение кальция для организма, обмен кальция к коррекция его нарушении, препараты кальция,
применение;
• — роль магния в организме, препараты магния, их применение, ПЭ;
* — основные виды нарушений водно-солевого баланса и принципы коррекции;
• — механизмы регуляции кислотно-основного состояния, ЛС для коррекции нарушений КОС;
• — препараты для парэнтерального питания, показания к применению.
Средства для регуляции водно-электролитного баланса
Нарушения водно-солевого баланса бывают трех типов: 1) обезвоживание в результате потери воды
из плазмы и межклеточной жидкости (обильное потоотделение, лихорадка и др.); в этом случае
повышается осмотическое давление плазмы и вода уходит из тканей; 2) потеря солей (длительные
рвота, понос и др.); при этом понижается осмотическое давление плазмы и вода переходит в ткани; 3)
равномерная потеря воды и солей (смешанные нарушения). Для коррекции водно-электролитного
баланса (ВЭБ) используют солевые растворы, содержащие в строго определенных соотношениях ионы
щелочных и щелочно-земельных металлов (натрий, калий, кальций, хлор, натрия гидрокарбонат). При
этом надо учитывать степень обезвоживания, функцию почек, потребности организма. Неблагоприятны
как обезвоживание (гипогидратация), так и перегрузка жидкостью (гипергидратация). В первом случае
развивается сгущение крови, гипотония, замедление кровотока, нарушения функций клеток, задержка
шлаков; во втором — отеки, повышение АД, расстройства сердечной деятельности. Вода составляет 60–
70% массы тела. Она несет 3 функции: 1) пластическую и транспортную; 2) универсального
растворителя; 3) химического реактива, участвующего во всех биохимических процессах. Вода
находится в 3 фракциях: в свободном состояний, в связанном с коллоидами и в составе молекул белков,
жиров и углеводов. Внутри клеток содержится около 50% воды, в межклеточном пространстве — 15%,
в сосудах — 5%. Суточная потребность здорового человека — 2500–2700 мл (40 мл/кг). Из них через
почки выделяется 1500 мл, с потом и через легкие — 1000 мл, с калом — 100 мл. При лихорадке с
потом может выделиться до 3–8 л воды. Главными электролитами являются натрий, калий, кальций,
хлор, натрия гидрокарбонат, магний, фосфатный анион. На основании электролитного состава плазмы
готовят солевые растворы. Наиболее физиологичными являются такие растворы, которые по составу
аналогичны солевому составу плазмы. Они должны отвечать 3 требованиям: 1) изотонии (равенство
осмотического давления с плазмой); 2) изоионии (равенство ионного состава с плазмой); 3) изогидрии
(равенство рН).
Примером такого раствора служит раствор Рингера, содержащий натрия хлорид, калия хлорид,
кальция хлорид и натрия гидрокарбонат. Для лучшей утилизации ионов обычно добавляют глюкозу.
Такие растворы называют глюкозосолевыми.
Натрий регулируется гормоном коры надпочечников альдостероном (см. лекцию 28). Nа+ —
главный внеклеточный ион, регулирующий осмотическое давление плазмы и внеклеточной жидкости, а
также возбудимость клеточных мембран и внутриклеточные процессы. Суточная потребность — 5–6 г
натрия хлорида. Натрий легко теряется с мочой, с потом при тяжелой работе и гипертермии. При этом
происходит обезвоживание организма. Задержка натрия в организме сопровождается отеками. Для
восстановления баланса натрия используют изотонический раствор натрия хлорида (0,9%), однако
вливание больших количеств его может изменить соотношение электролитов. Так как при
обезвоживании происходит потеря и других электролитов, лучше применять сбалансированный
(физиологический) раствор. У детей до 3 лет предпочтение отдают изотоническому раствору с
добавлением необходимых количеств других ионов, так как в этом возрасте они плохо выводятся
почками. Изотонический раствор у детей обычно используют вместе с 5% (изотоническим) раствором
глюкозы в соотношениях 1:3 (при вододефицитной форме) и 1:1 или 1:2 (при соледефицитной и
смешанной формах) обезвоживания. Его применяют также для промывания ран, для разведения
лекарств и т.д. Гипертонический раствор натрия хлорида (3–10%) применяют место для промывания
гнойных ран и в/в в небольших количествах пи дефиците натрия.
Калий находится преимущественно внутри клеток. Его содержание регулируется альдостероном. К+
регулирует функции мембран, участвуя в процессах поляризации и деполяризации. Суточная
потребность — 4–6 г. Содержание калия в желудочном и кишечном соках в 2 раза выше, чем в крови,
поэтому он легко теряется при рвоте и поносе. Потеря происходит также при применении диуретиков,
глюкокортикоидов, в послеоперационном периоде, при обширных ожогах, обморожениях и т.п.
Гипокалиемия характеризуется нарушением функций ЦНС (сонливость, спутанность сознания,
отсутствие глубоких рефлексов), мышечной и сердечной слабостью (брадикардия, дилатация сердца,
систолический шум), затруднением перистальтики кишечника, метеоризмом, признаками
непроходимости. Типичны изменения ЭКГ: удлинение P–Q и S–T, увеличение Р, уплощение,
удлинение, инверсия Т, аритмия и др. Назначают калия хлорид в/в (самостоятельно или в составе
“сбалансированного” раствора), а также внутрь в виде 10% раствора, так как в порошках и таблетках он
раздражает слизистые. Противопоказан при нарушении выделительной функции почек. Применяют
панаигии и аспаркам, содержащие асларагинат калия и магния, которые способствуют
проникновению и фиксации калия в тканях. Назначают диету, богатую калием (печеный картофель,
сушенные фрукты). При передозировке калия возникает гиперкалиемия, которая сопровождается
цианозом, брадикардией, ослаблением сократимости миокарда, изменениями ЭКГ (расширение
комплекса QRS, снижение зубцов, признаки атровентрикулярной блокады). Лечение: в/в 5% раствор
глюкозы, кальция хлорид, инсулин. Инсулин и глюкоза способствуют переходу калия в клетки.
Кальций участвует в формировании костной ткани, в свертывании крови, проницаемости
капилляров, нервной и сердечной деятельности, регулирует проницаемость мембран для натрия и
калия, сократимость гладкомышечных клеток. Обмен кальция регулируется витамином D (всасывание в
кишечнике и реабсорбция в почках), паратиреоидином и тиреокальцитонином (содержание а крови и
костях). Антагонист калия. При гипокальциемии возникают тетания (ларингоспазм, судороги),
сердечная слабость, гипотензия. Недостаток кальция у детей приводит к развитию рахита, у взрослых
— к остеомаляции. При гиперкальциемии развивается кальциноз (обызвестление) сосудов и почечных
канальцев. По действию на сердце кальций сходен с сердечными гликозидами, поэтому при совместном
применении повышает их активность и токсичность. Применяют кальция хлорид и кальция глюконат.
Последний медленно диссоциирует, поэтому оказывает менее выраженное раздражающее действие. Его
можно назначать в/м. Применяют при переломах костей, остеомаляции, рахите, при нарушении
свертывания крови, аллергии, отеке легких, при передозировке прапаратов калия и магния.
Содержание и обмен магния регулирует альдостерон. МД магния связан со способностью угнетать
освобождение катехоламинов из. симпатических окончаний. Поэтому магний является антагонистом
кальция, который стимулирует выделение норадреналина. Магний способствует поступлению калия
через мембраны и удержанию его в клетках, а также выделению кальция через почки. При недостатке
магния кальций выпадает в осадок и может закупоривать почечные канальцы. Магний уменьшает
возбудимость ЦНС, снижает тонус мышц (скелетных и гладких), оказывает противосудорожное,
наркотическое и гипотензивное действие. При приеме внутрь оказывает слабительное действие за счет
повышения осмотического давления в просвете кишечника в результате диссоциации на ионы, которые
плохо всасываются. Для резорбтивного действия вводят магния сульфат в/в и в/м при
гипертоническом кризе, эклампсии беременных, судорогах, при гипомагниемии. Гипомагниемия может
возникнуть при введении больших количеств растворов и форсированном диурезе, при
гиперальдостеронизме, при длительном применении диуретиков. При передозировке магния
развивается резкое угнетение ЦНС, дыхания, падение АД. В качестве антагониста применяют
препараты кальция.
Плазмозамещающие растворы используют при кровопотерях. Солевые растворы имеют мелкие
молекулы, поэтому быстро покидают сосудистое русло и действуют кратковременно (0,5–2 ч). В связи с
этим применяют синтетические полимеры глюкозы, имеющие крупные молекулы. Они длительно
удерживаются в сосудах и восстанавливают объем циркулирующей крови, чему способствует также
повышение осмотического давления плазмы. Используют полимеры глюкозы (декстраны) с
молекулярной массой от 10000 до 60000. К ним относятся полиглюкин, реополиглюкнн и др. Медленно
расщепляются с образованием глюкозы, подвергающейся утилизации. Около 40–60% выводится
почками в неизмененном виде. Не обладают антигенными свойствами, поэтому не вызывают
анафилактических реакций. Их можно вводить в большом количестве (до 2 л). Полиглюкин имеет
молекулярную массу около 60000, не проникает через капилляры и почечные клубочки. Через 3 суток в
крови остается до 30% введенного объема. Поэтому длительно возрастает объем крови, АД,
кровообращение, устраняется гипоксия. Противопоказан при травмах черепа, сотрясении мозга
(повышает внутричерепное давление). Реополиглюкин имеет массу 30–40 тыс., поэтому выводится из
организма быстрее. Он хорошо адсорбирует токсины, снижает вязкость крови, агрегацию тромбоцитов,
улучшает реологические свойства крови и микроциркуляцию. Применяют как плазмозаменитель, при
отравлениях, для улучшения кровообращения, при гипоксии, для профолактики тромбозов и т.п.
Гемодез — поливинилпирролидон, обладает дегидратирующим действием, так как повышает
осмотическое давление крови, улучшает микроциркуляцию, адсорбирует и выводит токсины. 80%
препарата выводится почками за 4 ч в неизмененном виде, удаляя токсины, поэтому его широко
применяют при интоксикациях. Противопоказан при кровоизлияниях в мозг, заболеваниях почек с
нарушением выделительной функции, при бронхиальной астме.
Средства для коррекции кислотно-основного состояния
Организм может нормально функционировать только при постоянстве рН внутренней среды (7,35–
7,40). Отклонения рН в кислую сторону называют ацидозом, в щелочную — алкалозом. Они бывают
компенсированными и некомпенсированными. Постоянство рН поддерживают буферные системы.
Важнейшими являются гидрокарбонатный, фосфатный, белковый и гемоглобиновый буферы. При
накоплении кислых или основных продуктов обмена емкость буферных систем падает и резервы
компенсации истощаются. Поэтому компенсированный (скрытый) ацидоз или алкалоз может перейти в
декомпенсированный. На практике чаще встречается ацидоз а виде респираторной, метаболической и
смешанной форм. Респираторный ацидоз возникает при нарушении легочного газообмена (угнетение
дыхания, бронхослазм, ателектаз легких, обширная пневмония, отек легких и т.п.). Он характеризуется
развитием гипоксемии и гиперкапнии. Назначения специальных средств не требуется. Необходимо
устранить причину, вызвавшую нарушение газообмена в легких. Метаболический ацидоз возникает при
нарушении обмена веществ (сахарный диабет и др.), при кровопотере, шоке, уремии и т.п. Смешанный
ацидоз (респираторно-метаболический) развивается при нарушениях легочного газообмена и обмена
веществ. Часто причиной служат циркуляторные расстройства (серденая недостаточность, гипертония,
тяжелые нарушения сердечного ритма и др.). Ацидоз сопровождается расстройствами функций ЦНС,
ССС, обмена веществ, ослаблением действия катехоламинов и т.п., которые, в свою очередь,
усугубляют метаболические и респираторные нарушения и усиливают явления ацидоза. Возникает
порочный круг. Для устранения ацидоза применяют растворы натрия гидрокарбоната, натрия лактата,
трисамина и др. Они нейтрализуют избыток кислых соединений и нормализуют рН среды. Первые 2
препарата являются экстрацеллюлярнмми буферами, так как плохо проникают в клетки, трисамин
проникает через мембраны легко и действует как вне-, так и внутри клеток. Натрия гидрокарбонат
восстанавливает резерв гидрокарбонатного буфера. Он образует натриевые соли органических кислот и
СО2 которая быстро выделяется через легкие. Поэтому для проявления терапевтического эффекта
необходима достаточная легочная вентиляция. При ее нарушении СО2 накапливается в крови и ацидоз
усиливается. Поскольку препарат плохо проникает в клетки, назначают средства, улучшающие
окислительные процессы в клетках (кокарбоксилаза, витамины С, В2, Р) или препараты, снижающие
процессы окисления и потребление кислорода (в-адреноблокаторы), а также соли калия для вытеснения
водорода. Для точного дозирования натрия гидрокарбоната надо знать щелочные резервы, рН крови и
напряжение СО2. Назначают внутрь, ректально и в/в при отравлениях барбитуратами, салицилатами и
др. кислыми соединениями, при метаболическом и смешанном ацидозе. При передозировке может
развиться алкалоз. Натрия лактат действует медленнее, но меньше зависит от легочной вентиляции.
МД обусловлен связыванием молочной кислоты и Н+-ионов, включением ее в цикл Кребса и
разрушением или превращением в глюкозу, в результате чего рН крови и тканей повышается.
Противопоказан при тяжелом метаболическом ацидозе и нарушении функции печени. Трисамин
способен быстро проникать в клетки и восстанавливать рН внутри и вне клеток. Он связывает Н+-ионы
и СО; при гипоксии, предотвращая раннее действие кислородного голодания на ферменты. При этом
нормализуется обмен веществ, уменьшается потеря калия, восстанавливается АД и сердечная
деятельность. Кроме того, он действует как осмотический диуретик и усиливает выделительную
функцию почек. При выраженной почечной недостаточности противопоказан. Эффективен при всех
видах ацидоза и гиперкалнии.
Растворы для парэнтерального питания
Энергетическая потребность человека при постельном режиме равна 1800–2000 ккал в сутки. Она
удовлетворяется за счет углеводов и в меньшей степени за счет жиров и белков. Суточная потребность
в белке — 0,8–1 г/кг, для детей значительно выше. С пищей человек получает свыше 20 аминокислот,
из которых 10 незаменимы. В период выздоровления потребность в белке возрастает в 2–3 раза. При
нарушении энтерального питания (непроходимость кишечника, рвота, понос, нарушения переваривания
и всасывания) приходится поддерживать обмен веществ парэнтеральным питанием. Оно должно
отвечать следующим требованиям: 1) обеспечение организма энергией; 2) снабжение пластическими
материалами; 3) поддержание водно-солевого обмена. Первые 2 требования можно удовлетворить
введением глюкозы, гидролизатов белков, аминокислот и ультраэмульсий жиров.
Глюкоза является наиболее ценным энергетическим веществом и основным источником энергии для
мозга, сердца, мышц и печени. Она может легко образовываться из аминокислот и жиров. При
транспорте через мембраны глюкоза присоединяет остаток фосфорной кислоты (фосфорилирование) и
вступает в обмен. Фосфорилирование стимулирует инсулин, который обеспечивает транспорт глюкозы
через мембраны и присоединение остатка фосфорной кислоты. Поэтому для лучшего усвоения глюкозы
целесообразно вводить инсулин. Глюкоза окисляется до углекислоты и воды. При хорошей работе
почек и сердца можно вводить до 3 л 5% раствора глюкозы в сутки. Однако это обеспечивает не более
1/3 потребности организма в калориях (1 л 5% раствора глюкозы дает лишь 200 ккал). Гипертонические
растворы глюкозы (20–40%) можно вводить только в/в в относительно небольших количествах при
заболеваниях сердца, отеке легких, мозга, травмах, черепа (как дегидратирующее). Глюкоза играет
важную роль в процессах дезинтоксикации в печени. Печень, богатая гликогеном, лучше противостоит
интоксикации.
Гидролизаты белков (аминопептид, аминокровин, гидролизин и др.) применяют для покрытия
дефицита белков. Они являются продуктами ферментативного или кислотного гидролиза белков крови,
казеина. Содержат пептиды и аминокислоты. Не обладают антигенными свойствами и
специфичностью, поэтому обычно не вызывают аллергических реакций. Содержат все незаменимые
аминокислоты. При утилизации 1 л раствора образуется 350–450 ккал. В сутки вводят 1–2 л раствора.
Их обычно комбинируют с вит. В12 и анаболическими средствами для лучшего усвоения.
Противопоказаны при заболеваниях почек, печени, нарушении кровообращения.
Так как глюкоза и гидролизаты белков не могут полиостью покрыть энергетические потребности
организма из-за большого объема вливаний, наряду с ними используют жировые ультраэмульсии
(напр., липофундин). Их готовят из растительных масел. Имеют очень мелкие частицы, проходящие
через капилляры, поэтому эмболию не вызывают. Эти препараты обладают большей калорийностью,
чем глюкоза и гидролизаты белков.
Лекция 30
АНТИГИСТАМИННЫЕ И ДРУГИЕ ПРОТИВОАЛЛЕРГИЧЕСКИЕ СРЕДСТВА.
ИММУНОМОДУЛИРУЮЩИЕ СРЕДСТВА
В лекции будут освещены следующие вопросы:
• — общие представления о развитии аллергических реакций;
• -основные принципы фармакотерапии аллергических реакций, классификация антиаллергических
средств;
• — МД гистамина, основные эффекты и его роль в развитии аллергии;
• — виды и локализация гистаминовых рецепторов, эффекты при их раздражении; классификация
антигистаминных ЛС;
• — блокаторы Н1-гисгаминорецепторов, их эффекты, применение, ПЭ;
• — блокаторы Н2-гистаминорецепторов, основные эффекты и применение;
• — ЛС, препятствующие высвобождению гистамина и др. факторов аллергии;
• — иммунодепрессивные ЛС (глюкокортикоиды, цитосгатики), МД, применение при аллергических
заболеваниях;
• — иммуностимулирующие (иммуномодулирующие) ЛС, эффекты и применение.
По данным ВОЗ, около 40% населения земного шара старадают аллергическими заболеваниями.
Аллергия — это состояние повышенной чувствительности организма к веществам, обладающим
антигенными свойствами. Различают аллергические реакции немедленного типа (анафилактический
шок, сывороточная болезнь, бронхиальная астма, крапивница, полиноз), возникающие в первые минуты
и часы после введения антигена, и реакции замедленного типа (аутоиммунные заболевания,
бактериальная аллергия, экзема и др.), развивающиеся постепенно. Аллергены могут быть экзогенного
и эндогенного происхождения. Процесс аллергизацми напоминает развитие иммунных реакций. В 1-й
стадии происходит фиксация антигена в лимфоцитах, во 2-й — образуются антитела
(иммуноглобулины), что сопровождается сенсибилизацией организма. Различают 2 типа антител:
фиксированные (клеточные), участвующие в реакциях замедленного типа, и свободные
(циркулирующие), участвующие в реакциях немедленного типа. При вторичном попадании антигенов в
сенсибилизированный организм возникает реакция с антителами и образование макромолекулярных
комплексов, которые активируют процессы протеолиза, липолиза и вызывают повреждение клеток.
Происходит высвобождение гистамина, серотонина, брадикинина, простагландинов, ацетилхолина,
медленно действующей субстанции анафилаксии, нарушающих функции различных органов и систем.
Реакция антиген-антитело приводит к образованию активных продуктов протеолиза из а-глобулинов
крови, нарушающих свертывание крови и микроциркуляцию. При развитии реакции замедленного типа
увеличивается содержание фактора, угнетающего миграцию макрофагов и лимфоцитов, лимфотоксинов
и митогенного (бластогенного) фактора. Таким образом, реакции немедленного типа обусловлены
гуморальным иммунитетом — антителами, продуцируемыми В-лимфоцитами, реакции замедленного
типа — клеточным иммунитетом и антителами, продуцируемыми Т-лимфоцигами.
Фармакотерапия аллергических заболеваний осуществляется по следующим направлениям: 1)
устранение контакта с аллергизирующими факторами; 2) специфическая гипосенсибилизация малыми
дозами аллергена; 3) неспецифическая гипосенсибилизация иммунодепрессантами; 4) подавление
освобождения медиаторов аллергии и их взаимодействия с рецепторами (собственно
противоаллергические ЛС); 5) симптоматическая ФТ (устранение общих проявлений аллергии:
анафилактический шок, сыпи, лихорадка и др.).
Противоаллергические ЛС можно разделить на 2 группы: 1) ЛС для лечения аллергических
реакций немедленного типа; 2) ЛС для лечения аллергических реакций замедленного типа. К 1-й группе
относятся: а) ЛС, угнетающие освобождение гистамина и др. биологически активных веществ из депо
(кромолин-натрий, кетотифен, глюкокортикоиды); б) блокаторы Н1-гистаминовых рецепторов
(димедрол, дипразин, супрастин, диазолин, фенкарол, тавегил); в) ЛС, угнетающие проявления
аллергических реакций (адреналин, эфедрин, в-адреномиметики, м-холиноблокаторы, эуфиллин); г) ЛС,
уменьшающие повреждения тканей (стероидные и нестероидные противовоспалительные средства). 2-я
группа включает: а) ЛС, угнетающие иммуногенез (иммунодепрессанты) -глюкокортикоиды,
циклоспорин и цитостатики; б) ЛС, уменьшающие повреждение тканей (стероидные и нестероидные
ПВС).
Гистамин — один из ведущих факторов патогенеза аллергии. Биогенный амин, продукт
декарбоксилирования аминокислоты гистидина. Главным депо гистамина являются тучные клетки
Эрлиха, которых особенно много по ходу мелких сосудов, в легочной ткани, коже, кишечнике.
Депонированный гистамин физиологически неактивен и не разрушается гистаминазой,
моноаминоксидазой и др. Небольшое количество циркулирует в свободной форме в крови. Общее
количество депонированного гистамина превышает сметельную дозу, поэтому при массивном
поступлении в кровь может вызвать летальный исход. Основными эффектами являются: 1) расширение
мелких сосудов, повышение их проницаемости, увеличение экссудации жидкости и развитие отека,
сгущение крови и понижение АД; 2) повышение тонуса гладких мышц ЖКТ, бронхов, желче- и
мочевыводящих путей; 3) усиление секреции желез. Гистамин регулирует местный кровоток,
транскапиллярный обмен, секрецию желез желудка и участвует в развитии 1-й фазы воспаления. Он
также стимулирует выделение адреналина и глюкокортикоидов надпочечниками. Количество
свободного гистамина возрастает под влиянием различных факторов: лекарств, пищевых продуктов,
экзо- и эндотоксинов, ионизирующей радиации, ультрафиолетового облучения и т.п. Основным
фактором, стимулирующим высвобождение гистамина, является комплекс антиген-антитело. Эффекты
гистамина реализуются через специфические рецепторы. Различают 2 типа гистаминовых рецепторов
— Н1- и Н2-рецепторы. Первые находятся преимущественно в гладких мышцах кишечника, бронхов,
желче- и мочевыводящих путей, в сердце, сосудах, ЦНС; вторые — в железах желудка, в матке, сердце,
жировой ткани, в тучных клетках, лимфоцитах, базофилах, нейтрофилах. Возбуждение Н1-рецепторов
сопровождается: 1) повышением тонуса гладких мышц ЖКТ, бронхов и др.; 2) снижением тонуса
артерий и повышением тонуса вен; 3) увеличением проницаемости капилляров; 4) угнетением
атриовентрикулярной проводимости в сердце. Стимуляция Н2-рецепторов вызывает: 1) снижение
тонуса артерий; 2) повышение секреции желудочного сока; 3) увеличение ЧСС; 4) угнетение
сократимости миометрия; 5) увеличение дегрануляции тучных клеток и базофилов, ускорение
выделения из них гистамина; 6) угнетение хемотаксиса нейтрофилов, лизосомных ферментов и
снижение активности Т-лимфоцитов; 7) увеличение липолиза и содержания жирных кислот в крови.
Гистамин применяют для функциональной диагностики заболеваний желудка, дифференциальной
диагностики феохромоцитомы, при спазмах периферических сосудов, при аллергических заболеваниях
(специфическая гипосенсибилизация). При передозировке может развиться гистаминовый шок по типу
анафилактического, лечение которого осуществляют по тем же правилам.
Антигистаминные средства. Являются блокаторами гистаминорецепторов. На синтез и
освобождение гистамина из тучных клеток не влияют. Делятся на 2 группы: 1) блокаторы Н1гистаминорецепторов и 2) блокаторы Н2-гистаминорецепторов. Блокаторы Н1-рецепторов обладают
антиаллергическими свойствами. К ним относятся димедрол, дипразин, супрастин, тавегил, диазолин,
фенкарол. Являются конкурентными антагонистами гистамина и устраняют следующие его эффекты:
спазм гладких мышц, гипотензию, увеличение проницаемости капилляров, развитие отека, гиперемию и
зуд кожи. На секрецию желудочных желез не влияют. Обладая общими свойствами, они имеют
некоторые различия. По влиянию на ЦНС можно выделить препараты с угнетающим действием
(димедрол, дипразин, супрастин) и препараты, не влияющие на ЦНС (диазолин). Слабый седативный
эффект оказывают фенкарол и тавегил. Димедрол, дипразии и супрастин оказывают успокаивающее и
снотворное действие. Их называют “ночными” ЛС; они также оказывают спазмолитическое и аадреноблокирующее действие, а димедрол — ганглиоблокирующее, поэтому могут понижать АД.
Диазолин называют “дневным” противогистаминным препаратом. Для всех указанных препаратов
характерно местноанестезирующее действие. По длительности действия делятся на препараты: 1)
короткого действия (4–6 ч) — димедрол, дипразин, супрастин; 2) средней продолжительности (8–12 ч)
— тавегил; 3) длительного действия (до 2 сут) — диазолин. Эти препараты применяют при
аллергических реакциях немедленного типа. При анафилактическом шоке они мало эффективны.
Средства, угнетающие ЦНС, можно назначать при бессонице, для потенцирования наркоза,
анальгетиков, местных анестетиков, при рвоте беременных, паркинсонизме, хорее, вестибулярных
расстройствах. ПЭ: сухость во рту, сонливость. Препараты с седативными свойствами не
рекомендуются лицам, связанным с оперативной работой, с работой на транспорте и т.п.
К блокаторам Н2-гистаминорецепторов относятся ранитидин и циметидин. Их используют при
заболеваниях желудка и 12-перстной кишки. При аллергических заболеваниях они малоэффективны
(см. лекцию 17).
ЛС, препятствующие освобождению гистамина и других факторов аллергии.. К ним относятся
кромолин-натрий (интал), кетотифен (задитен) и глюкокортикоиды (гидрокортизон, преднизолон,
дексаметазон и др.). Кромолин-натрий и кетотифен стабилизируют мембраны тучных клеток,
препятствуют входу кальция и дегрануляции тучных клеток,.следствием чего является уменьшение
выброса гистамина, медленно действующей субстанции анафилаксии и др. факторов. Их применяют
при бронхиальной астме, аллергических бронхитах, ринитах, сенной лихорадке и др. (см. лекцию 15).
Глюкокортикокды обладают разнообразным влиянием на обмен веществ. Десенсибилизирующее
противоаллергическое действие связано с угнетением иммуногенеза, дегрануляции тучных клеток,
базофилов, нейтрофилов и уменьшением выброса факторов анафилаксии (см. лекцию 28).
Для устранения тяжелых общих проявлений анафилаксии (особенно анафилактического шока,
коллапса, отека гортани, тяжелого бронхоспазма) используют адреналин и эуфиллин, при
необходимости — строфантин, корглюкон, дигоксин, преднизолон, гидрокортизон, плазмозамещающие
растворы (гемодез, реополиглюкин), фуросемид и др.
Для лечения аллергии замедленного типа (аутоиммунные заболевания) используют препараты,
угнетающие иммуногенез, и ЛС, уменьшающие повреждение тканей. К 1-й группе относятся
глюкокортикоиды, циклоспорин и цитостатики, являющиеся иммунодепрессантами. МД
глюкокортикоидов связан с угнетением пролиферации Т-лимфоцитов, процесса “узнавания” антигена,
снижением токсичности Т-лимфоцитов-киллеров (“убийц”) и с ускорением миграции макрофагов.
Цитостатики (азатиоприн и др.) преимущественно подавляют пролиферативную фазу иммунной
реакции. Циклоспорин относится к антибиотикам. МД связывают с угнетением образования
интерлейкина и пролиферации Т-лимфоцитов. В отличие от цитостатиков мало влияет на
кроветворение, но обладает нефротоксичностыо и гепатоксичностыо. Иммунодепрессанты применяют
для преодоления тканевой несовместимости при пересадке органов и тканей, при аутоиммунных
заболеваниях (красная волчанка, неспецифический ревматоидный полиартрит и др.).
К ЛС, уменьшающим повреждение тканей при возникновении очагов асептического
аллергического воспаления, относятся стероидные (глюкокортикоиды) и нестероидные
противоспалительные средства (салицилаты, ортофен, ибупрофен, напроксен, индометацин и др.) (см.
лекцию 11).
Иммуностимулирующие средства
К ним относятся ЛС, нормализующие иммунные реакции при иммунодефицитных состояниях
(иммуномодуляторы): препараты тимуса (тималин, тимозин, тактивин), интерферон, БЦЖ, левамизол и
др. Применяют при возникновении иммунного Дефицита, связанного с лучевой и лекарственной
терапией опухолей, с хроническими инфекциями и т.д. МД связывают с активацией макрофагов и Тлимфоцитов, включая Т-киллеры, т.е. клеточного иммунитета, а также с увеличением продукции
интерферонов. Левамизол синтетический препарат обладающий противоглистным действием. В то же
время оказывает выраженный иммуностимулирующий эффект, МД которого, по-видимому, связан со
стимуляцией Т-лимфоцитов и макрофагов. ПЭ иммуностимуляторов могут проявляться в виде
аллергии, диспептических расстройств, неврологических нарушений, угнетения кроветворения. Чаще
возникают при назначении синтетических препаратов (левамизол).
Лекция 31
ДЕЗИНФИЦИРУЮЩИЕ И АНТИСЕПТИЧЕСКИЕ СРЕДСТВА. ОСНОВНЫЕ ПРИНЦИПЫ
ХИМИОТЕРАПИИ
Большой арсенал этих ЛС можно разделить на следующие группы: 1) дезинфицирующие средства,
предназначенные для уничтожения возбудителей инфекционных заболеваний во внешней среде; 2)
антисептические ЛС, используемые для уничтожения возбудителей на коже, слизистых, раневой
поверхности; 3) химиотерапевтические ЛС, предназначенные для подавления возбудителей в
организме.
Вам необходимо знать следующие вопросы:
• — история создания противомикробных средств;
* — общая характеристика дезинфицирующих и антисептических средств;
* — классификация дезинфицирующих и антисептических ЛС;
* — МД и применение галоидосодержащих препаратов, окислителей, соединений металлов, кислот и
щелочей, возможные ПЭ и лечение отравлений;
* — характеристика противомикробных средств алифатического и ароматического ряда,
применение, ПЭ;
* — МД и применение антисептиков из групп красителей, детергентов, производных нитрофурана и
др.
* — история создания химиотерапевтических противомикробных средств;
* — основные принципы химиотерапии, классификация химиотерапевтических средств.
Дезинфицирующие и антисептические средства
Первую попытку использовать химические соединения для обеззараживания помещений и
предметов ухода за больными сделал русский фармаколог А.П. Нелюбин, который предложил для этой
цели белильную (хлорную) известь. В 1861 г. ее применил для обработки рук венгерский акушер И.
Земельвейс. В 1867 г. английский хирург Дж. Листер ввел в практику в качестве обеззараживающего
средства карболовую кислоту (фенол). Последующее развитие антисептики базируется на
фундаментальных открытиях Л.Пастера, И.И. Мечникова, Р.Коха и др. роли патогенных микробов в
развитии инфекционных заболеваний. Основное назначение дезинфицирующих и антисептических ЛС
— профилактика инфекционных заболеваний. Принципиальных различий между ними нет. В
зависимости от концентрации их можно использовать для дезинфекции как предметов окружающей
среды, так и покровных тканей организма. Важно, чтобы при дезинфекции они не повреждали
предметов и не представляли опасности для людей и животных, а при обработке кожи и слизистых
оболочек не оказывали раздражающего и прижигающего действия. Антисептики обладают
бактерицидным эффектом, который связан с коагуляцией белков микробных клеток, повреждением их
мембран, подавлением активности ферментов. У них нет избирательности действия, имеют широкий
спектр противомикробного действия, привыкание микробов к ним практически не возникает.
Противомикробная активность относительно низкая (1:100–1:1000), а токсичность достаточно высокая,
поэтому их применяют местно.
Делятся на 2 группы. 1. Неорганические вещества: а) галоидосодержащие (известь хлорная,
хлорамин, пантоцид, спиртовый раствор йода, раствор Люголя, йодоформ, йодинол и др.); б)
окислители (раствор перекиси водорода, калия перманганат); в) соединения металлов (препараты ртути,
серебра, цинка, меди, свинца, алюминия и др.); г) кислоты и щелочи (кислота салициловая, кислота
борная, раствор аммиака). 2. Органические соединения: а) соединения алифатического ряда
(препараты формальдегида, спирт этиловый); б) соединения ароматического ряда (препараты фенола,
ихтиол); а) детергенты (церигель, роккал, этоний и др.); г) красители (бриллиантовый зеленый,
метиленовый синий, этакридина лактат); д) бигуаниды (хлоргексидин); е) производные нитрофурана
(фурацилин).
Неорганические антисептики
Галлоидосодержащие вещества делятся на хлорсодержащие (хлорная известь, хлорамин, пантоцид)
и йодсодержащие (спиртовый раствор йода, раствор Люголя, йодинол, йодоформ). МД обусловлен
способностью отщеплять хлор и йод в воде с образованием хлорноватистой и йодноватистой кислот,
которые отщепляют кислород и галогены, оказывающие денатурирующее действие на белки
микробных клеток и вызывающие их гибель (бактерицидный эффект).
Хлорную известь используют для дезинфекции внешней среды, хлорамин и пантоцид — для
дезинфекции одежды, неметаллических инструментов, кожных покровов. Спиртовые растворы йода
применяют для дезинфекции кожи. Они могут вызывать раздражение. Более мягко действует раствор
Люголя, его обычно используют для смазывания слизистых оболочек. Йодотдающие вещества
(йодинол, йодонат) хорошо растворимы в воде, действуют более продолжительно и меньше
раздражают ткани. Препараты йода применяют для обработки кожи, при легких травмах, фурункулах,
грибковых заболеваниях. К ним возможна идиосинкразия.
Окислители — это вещества, легко отщепляющие свободный кислород. Перекись водорода при
контакте с поврежденной тканью расщепляется каталозой с выделением атомарного и молекулярного
кислорода. Первый действует как окислитель, второй вызывает образование пены, которая механически
очищает рану. Перманганат калия действует преимущественно атомарным кислородом как
окислитель. Окислители применяют для промывания ран, слизистых полости рта, спринцеваний, при
ожогах и язвах.
Соединения металлов обладают противомикробным и местным действием. Местное действие в
зависимости от катиона металла может быть вяжущее, раздражающее и прижигающее. При
взаимодействии с белком они образуют альбуминаты. Соединения, образующие плотные альбуминаты
(алюминий, свинец), оказывают вяжущее и раздражающее действие; образующие менее плотные
альбуминаты (железо, медь, цинк), в зависимости от концентрации оказывают вяжущий, раздражающий
и прижигающий эффекты; при образовании рыхлых альбуминатов — преимущественно прижигающий
эффект (препараты ртути, серебра). Антисептическое действие содей металлов проявляется в
концентрациях, которые не вызывают коагуляции белка. МД связан с блокадой сульфгидрильных групп
ферментов, в результате чего прекращаются окислительные процессы. Некоторые металлы обладают
олигодинамическим действием, которое проявляется в очень малых концентрациях и сопровождается
гибелью микробов (медь, серебро, таллий, кадмий). При хранении воды в медных, серебряных сосудах
или нахождении в воде предметов из меди и серебра в ней длительно не развиваются микроорганизмы и
она сохраняет свежесть (так называемая “святая вода”).
При отравлении солями металлов происходит резкое угнетение тиоловых ферментов в результате
присоединения катиона металла к сульфгидрильным группам. Наиболее ярко картина отравления
выражена при отравлении солями ртути, особенно сулемой. При попадани через рот возникают боли в
ротовой полости, по ходу пищевода, в животе, рвота, понос с кровавой слизью, головная боль,
разбитость, расстройства речи, походки, гемолиз эритроцитов, печеночная и почечная недостаточность,
нарушение работы сердца. При хроническом отравлении наблюдаются сухость во рту, синяя кайма и
язвы на деснах, анемия, брадикардия, гипотония, слабость, тремор рук, невриты, раздражительность,
бессоница. Лечение проводится по общим принципам: промывание желудка, активированный уголь,
молоко, яйца, солевое слабительное. Противоядием служит унитиол, который вводят в/м. Для борьбы с
нарушениями функций проводят симптоматическую терапию. Применяют препараты алюминия
(квасцы), свинца (свинцовая вода) для примочек, полосканий, спринцеваний; меди сульфат и цинка
сульфат при конъюнктивитах, уретритах, отравлении фосфором; серебра нитрат, протаргол,
колларгол — при заболеваниях глаз, язвах, эрозиях и т.п.; ртути дихлорид (сулема) — для
дезинфекции неметаллических предметов; ртути окись желтая — в глазной практике.
Кислоты и щелочи. В качестве антисептиков применяют слабые кислоты: борную, салициловую,
бензойную. Кислота салициловая используется в виде мазей, спиртовых растворов, в пастах,
присыпках. Кислоту борную применяют для промывания глаз, горла, при кожных заболеваниях.
Кислота бензойная используется преимущественно при грибковых заболеваниях кожи. Из щелочей
применяют водный раствор аммиака (нашатырный спирт) для обработки рук хирурга. Он оказывает
антисептическое и моющее действие.
Органические антисептики
Соединения алифатического ряда: растворы формальдегида (формалин), гексаметилентетрамин
(уротропин), спирт этиловый. Формальдегид легко проникает в микробную клетку и денатурирует
белок, связываясь с аминогруппами. На кожу и слизистые оказывает раздражающее и дегидратирующее
действие, уменьшая потоотделение. Применяют преимущественно в виде формалина,
представляющего 40% водный раствор формальдегида, из которого готовят растворы нужной
концентрации. При вдыхании больших количеств паров формальдегида может развиться отравление,
характеризующееся кашлем, слезотечением, угнетением ЦНС, печени и почек. Лечение: внутрь слизь
крахмальную, молоко, яичный белок, промывание желудка слабым раствором аммиака (перевод в
гексаметилентетрамин). Гексаметилентетрамин — соединение формальдегида с аммиаком. В кислой
среде быстро расщепляется на составные части, оказывающие бактерицидное действие. Спирт
этиловый подробно рассмотрен в лекции 9. Антисептический эффект связан с денатурацией белка и
дегидратацией. Для дезинфекции кожи применяют 70% спирт, который лучше проникает в протоки
потовых и сальных желез, так как не образует плотных белковых сгустков. Для стерилизации
инструментов и шовных материалов используют 90–96% спирт.
Соединения ароматического ряда (группа фенола): фенол (карболовая кислота), крезол, лизол,
тимол, резорцин, ихтиол. МД связан со способностью легко проникать через липопротеиновые
мембраны к денатурировать белок. Так как связь с белком непрочная, то одна молекула фенола может
прореагировать с несколькими молекулами белка. Эти вещества легко всасываются через слизистые и
кожу и могут вызывать отравление, которое проявляется вначале возбуждением, а затем параличом
ЦНС. 2% раствор фенола вызывает ожоги слизистой. Применяют для дезинфекции предметов внешней
среды. Деготь содержит фенол, крезолы, смолы и др. и обладает антисептическим, кератопластическим
и кератолитическим (в зависимости от концентрации) действием. Применяют в мазях при кожных
заболеваниях. Ихтиол получают из сланцевого известняка. Содержит ароматические соединения и
серу. Применяют в мазях и свечах ректальных и вагинальных.
Детергенты (поверхностно активные вещества — ПАВ): церигель, дегмицид, этоний,
хлоргексидил,
роккал.
Обладают
высокой
поверхностной
активностью,
моющими и
противомикробными свойствами. МД обусловлен снижением поверхностного натяжения на границе
раздела фаз (жидкой и твердой), в результате чего нарушается проницаемость мембран микробных
клеток и осмотическое равновесие, что приводит к их гибели.
Красители: этакридин, флавакридин, бриллиантовый зеленый, метиленовый синий. Действуют
преимущественно на грамположительные микробы. Эффект относительно невысокий, но они мало
раздражают ткани. Применяют для промывания ран, полостей в виде водных растворов, в мазях и
пастах при кожных заболеваниях. Бриллиантовый зеленый применяют обычно в спиртовом растворе
при гнойничковых заболеваниях кожи, для смазывания царапин, порезов, трещин. Метиленовый синий
используют как антисептик, а также как метгемоглобинообразователь при отравлениях цианидами
(препарат “Хромосмон”).
Производные нитрофурана. В качестве антисептика используют фурацилин. Он ингибирует
дыхательные ферменты, тормозит клеточное дыхание, в результате чего наступает бактерицидный
эффект. Спектр действия широкий. Применяют в виде 0,01–0,02% раствора для промывания ран,
полостей и т.д.
Основные принципы химиотерапии инфекционных заболеваний
Химиотерапия
инфекционных
заболеваний
осуществляется
различными
группами
химиотерапевтических средств (ХТС). К ним относятся ЛС, способные подавлять болезнетворные
микроорганизмы во внутренней среде организма без существенного вреда для него. ХТС —
этиотропные ЛС, устраняющие причину заболевания. От антисептиков они имеют ряд существенных
отличий. По типу действия они являются бактериостатическими или бактерицидными. МД ХТС
обусловлен либо нарушением функции клеточных мембран, либо угнетением определенных ферментов,
синтеза РНК, ДНК и белков микроорганизмов. ХТС обладают более избирательным действием, чем
антисептики, поэтому спектр их противомикробного действия ограничен. Антимикробная активность
очень высокая (действуют в разведении 1:1000000 и более), а токсичность, как правило, низкая,
поэтому они пригодны для резорбтивного действия. К большинству ХТС легко возникает
резистентность микроорганизмов, что является самым серьезным недостатком.
История ХТС начинается с применения хинина для лечения малярии. Однако до фундаментальных
исследований П. Эрлиха применение ХТС имело эмпирический характер. Эрлих сформулировал
основные принципы лечения инфекционных заболеваний и создал эффективное для своего времени
средство против сифилиса. Поэтому его по праву считают родоначальником современной
химиотерапии. 30-е годы нашего столетия ознаменовались созданием сульфаниламидных препаратов, а
с 1940 г. началась эра антибиотиков. В настоящее время арсенал ХТС обширный и содержит ЛС для
борьбы не только с бактериями, но и с простейшими, патогенными грибками, вирусами, паразитами.
ХТС можно классифицировать по структуре и применению: 1) антибиотики; 2)
сульфаниламидные средства; 3) производные нитрофурана; 4) синтетические ЛС разного строения; 5)
противотуберкулезные ЛС; 6) противосифилитические ЛС; 7) средства для лечения протозойных
инфекций; 8) лротивогрибковые ЛС; 9) противовирусные ЛС; 10) противопаразитарные
(антигельминтные) ЛС.
Для оценки ХТС решающее значение имеет химиотерапевтический индекс (ХИ), представляющий
отношение минимальной терапевтической дозы (МТД) к максимальной переносимой дозе (МПД),
выраженное в %% или дробью. Чем ниже ХИ, тем выше лечебный эффект и меньше риск осложнений
от препарата. Эффективная и безопасная химиотерапия базируется на следующих основных
принципах: 1. Рациональный выбор препарата на основе клинического и бактериологического
диагноза с учетом состояния и особенностей больного, его аллергологического анамнеза и
чувствительности возбудителей к ХТС. Отсутствие клинического улучшения в течение 2–3 суток
ставит вопрос об адекватности проводимой химиотерапии и ее пересмотре. 2. Выбор оптимальных
доз, путей введения и интервалов между приемами препарата с учетом возраста, массы тела, состояния
больного, локализации и тяжести инфекционного процесса, фармакокинетики препарата с целью
создания эффективной концентрации в организме. 3. Возможно раннее начало лечения, так как в
процессе заболевания возникают деструктивные изменения в органах, затрудняющие доступ препарата
в очаги инфекции. 4. Определение оптимального курса лечения. При острых инфекциях действие
ХТС проявляется быстрее, поэтому требуется более короткая интенсивная терапия, которая должна
продолжаться еще 2–3 дня после исчезновения клинических симптомов заболевания. При подострых и
хронических инфекциях ХТС действуют, как правило, медленнее, поэтому курс терапии должен быть
более продолжительным и при необходимости повторяться. Преждевременная отмена препарата
способствует возникновению резистентных форм микробов или рецидива заболевания. 5.
Комбинированное применение ХТС с целью усиления лечебного эффекта, ослабления побочного
действия и уменьшения вероятности развития устойчивых форм микроорганизмов. Использовать
можно только рациональные проверенные комбинации ХТС (как правило, не более 2–3 препаратов).
Показаниями для комбинированного применения ХТС служат: а) тяжелые инфекции, требующие
немедленного интенсивного лечения до постановки бактериологического диагноза и выявления
устойчивости микробов; б) смешанные инфекции или множественные процессы, вызываемые
различными возбудителями; в) необходимость предупредить развитие устойчивых форм
микроорганизмов. 6. Применение ХТС в комплексе с другими ЛС, способствующими активизации
защитных
сил
организма
(противовоспалительные,
жаропонижающие,
антигистаминные,
иммуностимулирующие, витаминные, сердечно-сосудистые и др. ЛС).
Лекция 32
АНТИБИОТИКИ
Это вещества, продуцируемые живыми организмами в процессе антибиоза. Основными источниками
получения антибиотиков (АБ) являются лучистые и плесневые грибки, некоторые бактерии, а также
синтетические аналоги и производные естественных АБ.
Вам необходимо знать следующие основные вопросы:
• — история создания антибиотиков;
• — основные приблемы антибиотикотерапии и пути их решения;
* — классификация АБ по структуре, спектру, типу и механизму действия;
* — взаимодействие А Б при комбинированном применении;
* — основные осложнения антибиотикотерапии;
* — фармакологическая характеристика биосинтетических пенициллинов;
* — полусинтетические пенициллины, классификация, особенности лротивомикробного действия и
применения;
* — фармакологическая характеристика цефалоспоринов, основные и ПЭ;
* — АБ-макролиды, МД, основные эффекты и применение, ПЭ;
* — МД, применение и ПЭ линкомицина и ристомицина;
* — фармакологическая характеристика тетрациклинов, их применение и ПЭ;
* — аминогликозиды, МЛ, тип и спектр антимикробиого действия, применение, противопоказания и
ПЭ;
* — фармакологическая характеристика полимиксинов, применение, ПЭ.
Понятие антибиоза ввели Л. Пастер и И. И. Мечников, которые “первые обнаружили, что в
присутствии некоторых микробов колонии других микробов не развиваются. В 1929 г. А. ФЛЕМИНГ
выделил из плесени пенициллин и установил его противомикробное действие. В 1940 г. Чейн и Флори
создали химически чистый препарат пенициллина, а в 1942 г. академик З. В. Ермольева разработала
отечественный способ промышленного производства пенициллина. После этих исследований началось
триумфальное шествие антибиотиков в медицине. Вскоре были созданы стрептомицин, левомицетин,
тетрациклины, цефалоспорины и др. АБ. В настоящее время их насчитывается несколько тысяч, однако
в медицинской практике используют лишь несколько десятков наиболее эффективных и наименее
токсичных препаратов.
АБ по своей противомикробиой активности превосходят все другие ХТС. Применение АБ не только
резко снизило тяжесть и летальность от многих инфекционных заболеваний, но и оказало
положительное влияние на их течение, изменило клиническую картину и уменьшило опасность
тяжелых осложнений. В то же время возникли проблемы, которые снижают эффективность и
безопасность АБ-терапии: 1) возникновение резистентных и полирезистентных (иногда АБ-зависимых)
штаммов микробов; 2) рост числа ПЭ АБ-терапии. Развитие резистентности микроорганизмов связано с
бессистемным и необоснованным применением АБ и несоблюдением принципов химиотерапии.
Назначение АБ без достаточных оснований, без учета состояния больного, наличия сопутствующей
патологии, аллергологического анамнеза не только снижает эффективность АБ-терапии, но и служит
причиной многих осложнений.
В основе приобретенной резистентности микроорганизмов лежит их способность вырабатывать
определенные ферменты, разрушающие АБ (напр., бета-лактамазы). Это свойство генетически
закрепляется и появляется штамм микробов, устойчивых к данному АБ. Так появились стафилококки и
стрептококки, устойчивые к биосинтетическим пенициллинам. Многие патогенные микробы приобрели
полирезистентность (устойчивость ко многим АБ и другим ХТС), что создает большие трудности для
терапии. Для преодоления резистентности используют следующие приемы: 1) строгое соблюдение
принципов химиотерапии; 2) комбинирование АБ между собой и с другими ХТС; 3) создание новых АБ
с заданными свойствами; 4) временное прекращение применения АБ, к которому возникло привыкание
микробов.
По химической структуре АБ делятся на следующие группы: 1) АБ, имеющие бета-лактамное
кольцо (пенициллины, цефалоспорины); 2) АБ, имеющие макроциклическое лактоновое кольцо
(макролиды); 3) АБ, имеющие 4 шестичленных кольца (тетрациклины); 4) производные
диоксиаминофенилпропана (левомицетин, синтомицин); 5) АБ, содержащие аминосахара
(аминогликозиды); б) циклические полипептиды (полимиксины); 7) АБ с макроциклической структурой
(рифамицины); 8) полиеновые АБ (противогрибковые); 9) АБ разного химического строения
(линкомицин, ристомицин, фузидин, грамицидин и др.); 10) противоопухолевые АБ (дактиномиции,
оливомицин, рубомицин, блеомицин, карминомицин и др.).
По спектру антимикробного действия АБ имеют существенные различия и подразделяются на: 1)
АБ, действующие преимущественно на грамположительные микробы (пенициллины, макролиды); 2)
АБ с преимущественным действием на грамотрицательные микробы (полимиксины); 3) АБ широкого
спектра действия (тетрациклины, левомицетин, цефалоспорины, аминогликозиды, ампициллин); 4) АБ,
действующие на грибки (нистатин, леворин, гризеофульвин, амфотеррицин, микогептин).
По типу антимикробного действия АБ подразделяются на бактерицидные (пенициллины,
цефалоспорины, аминогликозиды, полимиксины, ристомицин) и бактериостатические (макролиды,
тетрациклины, левомицетин).
По МД АБ делят на следующие группы: 1) АБ, нарушающие синтез клеточных мембран
(пенициллины, цефалоспорины); 2) АБ, нарушающие проницаемость цитоплазматических мембран
(полимиксины); 3) АБ, нарушающие синтез РНК (рифамицины); 4) АБ, нарушающие синтез белка
(тетрациклины, левомицетин, стрептомицин). Различают основные АБ (пенициллины, эритромицин,
тетрациклины, левомицетин, неомицин, гентамицин и др.), которые преимущественно используются на
практике, и резервные АБ, которые применяют, главным образом, при возникновении резистентности
микробов к основным АБ. Эффективность АБ зависит от достаточной концентрации в крови и тканях,
диапазон которой определяется разницей между оптимальной и минимально действующей
концентрацией, и достаточной продолжительностью действия. В зависимости от типа действия АБ
имеют особенности применения. Бактерицидные АБ (пенициллины, цефалоспорины, аминогликозиды,
полимиксины, рифамицины) используют преимущественно при тяжелых инфекциях. При этом можно
делать интервалы в лечении. Бактериостатические АБ (тетрациклины, макролиды, левомицетин,
полиеновые) применяют преимущественно при нетяжелых (малых) инфекциях и только непрерывно.
Усиления эффекта (синергизма) можно добиться путем правильного сочетания АБ или АБ с
другими ХТС. Наиболее эффективными комбинациями являются: 1) бензилпенициллины с
аминогликозидами; 2) ампициллин с гентамицином, тобрамицином, полимиксинами; 3)
диклоксациллин с бисептолом; 4) олеандомицин с сульфаниламидами короткого действия (этазол,
сульфадимезин, норсульфазол и др.); 5) тетрациклины с макролидами; 6) левомицетин с мистатином.
Между АБ могут возникать и антагонистические взаимоотношения, сопровождающиеся ослаблением
эффекта: 1) пенициллины с тетрациклинами, левомицетином, с сульфаниламидами длительного
действия (сульфадиметоксин, сульфапиридазин, сульфален); 2) тетрациклины со стрептомицином; 3)
макролиды с левомицетином. В большинстве случаев синергидное взаимодействие возникает при
сочетании АБ одного типа действия: бактерицидных с бактерицидными (напр., пенициллины с
аминогликозидами), бактериостатиков с бактериостатиками (напр., тетрациклин + олеандомицин =
олететрин). Особенно следует учитывать опасные сочетания АБ и других ХТС, которые использовать
категорически запрещено. К ним относятся препараты с Однонаправленным токсическим действием: 1)
аминогликозиды между собой, со стрептомицином, цефалоридином, полимиксинами, левомицетином,
амфотерицином, бисептолом; 2) левомицетин с амфотерицином, полимиксинами, ристомицином,
цефалоспоринами, сульфаниламидами, бисептолом; 3) ристомицин с микогептином, фузидином,
сульфаниламидами; 4) нистатин с микогептином.
Несмотря на то, что АБ обладают высокой избирательностью действия, они могут вызывать ряд
осложнений, которые можно подразделить на следующие группы. 1. Аллергические реакции
немедленного и замедленного типов. Наиболее опасными из них являются анафилактический шок,
ангионевротический отёк гортани, эксфолиативный дерматит, булезная эритема. Чаще других
вызывают пенициллины, особенно бициллины, но аллергия может возникать на любой антибиотик. 2.
Токсические реакции, специфичные для АБ и зависящие от дозы и продолжительности лечения. К
опасным реакциям относятся агранулоцитоз, апластическая анемия, тяжелые поражения печени и
почек. Они подразделяются на: а) нейротоксические реакции (невриты слухового, вестибулярного,
зрительного нервов, полиневриты, нарушения функций ЦНС); б) гепатотоксические реакции (гепатиты,
холестаз и др.); в) нефротоксические реакции (поражения почек); г) гематотоксические реакции
(угнетение кроветворного аппарата); д) раздражение ЖКТ; е) тератогенное действие (нарушение
развития плода). Поражения нервной системы и почек характерны для аминогликозидов,
стрептомицина, полимиксинов, поражения печени и желчевыводящих путей — для тетрациклинов,
угнетение кроветворения — для левомицетина, тератогенные эффекты — для тетрациклинов,
левомицетина, аминогликозидов. 3. Дисбактериозы (суперинфекции) развиваются в связи с
подавлением нормальной микрофлоры кишечника, в результате чего начинают бурно размножаться
условнопатогенные бактерии и грибки. Чаще всего они возникают при использовании АБ широкого
спектра действия (тетрациклины, левомицетин, ампициллин и др.). К дисбактериозам относятся
кандидамикозы, стафилококковый энтерит и др.
Группа пенициллинов
Пенициллины являются одними из наиболее активных и наименее токсичных АБ. Они
подразделяются на биосинтетические и полусинтетические. Биосинтетические пенициллины делятся
на: 1) препараты для парэнтерального введения (разрушаются в кислой среде желудка и в-лактамазами
микробов кишечника) — а) непродолжительного действия (бензилпенициллина натриевая соль и
бензипенициллина калиевая соль); б) продолжительного действия (бензилпенициллина новокаииовая
соль, бициллин-1, бициллин-5); 2) препараты для энтерального введения (не разрушаются в ЖКТ) —
феноксиметилпенициллин. Полусинтетические пенициллины: 1) для парэнтерального введения
(разрушаются в ЖКТ) — карбенициллии, 2) для энтерального и парэнтерального введения (не
разрушаются а ЖКТ) — оксациллин, ампициллин, ампиокс. Устойчивостью к пенициллиназе (влактамазе) обладает оксациллин. У него узкий спектр противомикробного действия. Ампициллин и
карбенициллин разрушаются пенициллиназой, вырабатываемой некоторыми микробами, спектр
действия широкий. Ампиокс — комбинированный препарат, состоящий из оксациллина и ампициллина.
В последние годы за рубежом появилась новая группа полусинтетических пенициллинов —
уреидопенициллины (пиперациллин и др.), обладающих широким спектром действия,
пенициллиназоустойчивостью и кислотоустойчивостью.
Все пенициллины обладают бактерицидным действием, связанным с нарушением синтеза мембран
микробных клеток. Поскольку они действуют на компоненты мембраны, которые в клетках человека не
образуются, их эффект является избирательным и не отражается на клетках макроорганизма.
Бензилпенициллин имеет высокую активность, действует преимущественно на грамположительные
микробы (стафилококки и стрептококки, не вырабатывающие пенициллиназу, пневмококки,
менингококки, гонококки, палочки дифтерии, сибирской язвы, газовой гангрены, столбняка,
спирохеты). Натриевая и калиевая соли бензилпенициллина хорошо растворимы в воде и назначаются
парэнтерально. В тканях распределяются равномерно, но плохо проникают в мозг и очаги воспаления.
Выделяются почками до 50% в неизмененном виде. Эффективные концентрации в крови
поддерживаются 3–5 ч, поэтому инъекции надо делать через 4–6 ч. Вводят в/м, иногда в/в (при сепсисе)
и в полости. Обладают раздражающим действием, поэтому инъекции болезненны. Для преодоления
устойчивости микробов в последние годы бензилпенициллин применяют в очень высоких дозах (до 1–2
млн ЕД на 1 кг массы тела в сутки). Для в/в и эндолюмбального введения используют только
кристаллическую натриевую соль. Бензилпенициллина новокаиновая соль и бициллины обладают
длительным действием, так как в месте инъекции образуют депо, из которого медленно всасываются в
кровь. Вводят в/м. Бензилпенициллина новокаиновую соль вводят 1–2 раза в сутки, бициллин-1 — 1 раз
в 5–7 дней, бициллин-5 — 1 раз в месяц. Феноксиметилпенициллин не разрушается в кислой среде,
поэтому его назначают внутрь каждые 4–6 ч, однако его эффект значительно слабее
бензилпенициллина.
Полусинтетические пенициллины расширяют возможности успешного лечения многих
инфекционных заболеваний, так как метод позволяет создавать препараты с заданными свойствами:
пенициллиназоустойчивость, кислотоустойчивость, расширение спектра противомикробного действия.
Оксациллин не разрушается пенициллиназой микробов, приобретших устойчивость к
биосинтетическим пенициллинам, и в кислой среде желудка, что позволяет использовать его для
подавления пенициллиноустойчивых возбудителей, назначая как внутрь, так и парэнтерально. По
спектру и продолжительности действия сходен с бензилпенициллином. Ампициллин, карбенициллин и
карфециллин имеют широкий спектр действия и применяются для подавления грамположительных и
грамотрицательных микробов. Они пенициллиназонеустойчивы, поэтому неэффективны против
микробов, вырабатывающих пенициллиназу. Ампициллин кислотоустойчив, поэтому его назначают
внутрь и парэнтерально, карбенициллин и карфециллин — только парэнтерально. Карбенициллин
особенно эффективен при заболеваниях, вызываемых синегнойной и кишечной палочками, а также
протеем.
Бензилпенициллины применяют при пневмониях, гнойных инфекциях, ангине, дифтерии, сифилисе,
гонорее, эпидемическом менингите, септическом эндокардите и т.д. Оксациллин является препаратом
выбора при заболеваниях, вызванных пенициллиноустойчивыми микробами. Ампициллин широко
используют при инфекциях ЖКТ, желче- и мочевыводящих путей, органов дыхания, гнойных
инфекциях. ПЭ пенициллинов чаще всего проявляются в виде аллергических реакций замедленного и
немедленного типов (кожные сыпи, отеки слизистых оболочек, лихорадка и др.). Наиболее тяжелой
формой является анафилактический шок. Для предупреждения аллергии необходимо учитывать
анамнез больного, проводить кожные пробы на чувствительность к пенициллину. Лечение включает
глюкокортикоиды, антигистаминмые средства, кальция хлорид и др. При анафилактическом шоке
вводят в/в адреналин или эфедрин, гидрокортизон или преднизолон, сердечные гликозиды, эуфиллин и
другие ЛС для восстановления функций ССС и дыхания. При приеме внутрь иногда возникают глоссит,
стоматит, тошнота, рвота; при в/м введении — боли, асептический некроз; при в/в — флебиты,
тромбофлебиты. При лечении ампициллином возможен дисбактериоз.
Цефалоспорины
По структуре и МД сходны с пенициллинами. Обладают бактерицидным действием, низкой
токсичностью и широким спектром действия, сходным с ампициллином. Устойчивы к пенициллиназе,
но разрушаются цефалоспориназой, поэтому эффективны при инфекциях, устойчивых к
беизилпенициллинам. По применению подразделяют на 2 группы: 1) для парэнтерального введения
(цефалоридин, цефалотин, цефотаксим); 2) для приема внутрь (цефалексин, цефаклор). Цефалотин и
цефалоридин больше действуют на грамположительные микробы, чем на грамотрицательные. Они
кислотоустойчивы, но в ЖКТ всасываются плохо, поэтому их вводят в/м и в/в. Через ГЭБ проникают
плохо, через плаценту — хорошо, но отрицательного действия на плод не оказывают. Применяют
преимущественно при инфекциях мочевыводящих путей, при неэффективности и непереносимости
пенициллинов. Являются препаратами выбора при пневмонии, вызванной палочкой Фридлендера.
Назначают каждые 4–6 ч. Цефотаксим устойчив к цефалоспориназе, поэтому применяется более
широко. Ценным свойством является активность в отношении синегнойной палочки. Цефалексин и
цефаклор хорошо всасываются в ЖКТ, поэтому их назначают внутрь. По спектру действия и
активности сходны с цефалотином. Устойчивы к пенициллиназе, но неустойчивы к цефалоспориназе.
Назначают в капсулах 4 раза в сутки. ПЭ: аллергические реакции (значительно реже, чем при
применении пенициллинов), иногда поражение почек (цефалоридин), раздражение тканей,
дисбактериозы.
Макролиды
К ним относятся эритромицин и олеандомицин. МД обусловлен угнетением синтеза белков. По типу
действия — бактериостатики. По спектру действия занимают промежуточное положение между АБ
узкого и широкого спектров действия. Наиболее чувствительны к ним грамположительные микробы.
Они действуют также на некоторые грамотрицательные микроорганизмы (кокки, палочки дифтерии,
анаэробы, риккетсии, возбудители трахомы, амебной дизентерии). Хорошо всасываются в кишечнике.
Эритромицин частично разрушается в кислой среде желудка, поэтому его применяют в капсулах и в
таблетках со специальным покрытием, обеспечивающим освобождение АБ в кишечнике. Макролиды
легко проникают в ткани, но в мозг почти не поступают. Через плаценту проходят легко, но на плод
отрицательного действия практически не оказывают. К ним быстро развивается устойчивость
микробов, поэтому их применяют как АБ резерва в тех случаях, когда имеются
пенициллиноустойчивые возбудители или аллергия к препаратам пенициллина. Они малотоксичны,
иногда вызывают аллергические реакции, диспептические расстройства, суперинфекции. При
сочетании с тетрациклинами эффект взаимно усиливается (олететрин, сигмамицин, тетраолеан).
Линкомицин. Ристомицин. Действуют преимущественно на грамположительные кокки,
возбудителей дифтерии, сибирской язвы, столбняка и др. Оказывают бактерицидное действие.
Линкомицин назначают в/м ив/в 2–3 раза в сутки. Он хорошо проникает в ткани, накапливается в
костях, поэтому эффективен при остеомиелите. Выводится преимущественно с желчью, создавая в ней
высокие концентрации. ПЭ: диспептические расстройства, иногда аллергия, лейкопения. Ристомицин
обычно назначают при неэффективности других АБ. Основным показанием является сепсис. Вводят в/в
капельно. Действует 12 ч, хорошо проникает в ткани, выводится почками в неизмененном виде,
создавая высокие концентрации в моче. При нарушении выделительной функции почек накапливается в
организме и может вызывать необратимое нарушение слуха, тромбоцитопению, кровотечение. После
в/в введения нередко возникает реакция обострения в виде лихорадки и ухудшения самочувствия, что
связано с массовой гибелью микробов в крови и выделением токсинов. Поэтому 1-ю инъекцию
рекомендуют делать в половинной дозе. Ристомицин нельзя сочетать с аминогликозидами, назначать
детям до 1 года и при заболеваниях почек.
Тетрациклины
Различают биосинтетические препараты (тетрациклин, окситетрациклин) и полусинтетические
(метациклин, доксициклин, морфоциклин). МД связывают с угнетением синтеза белка рибосомами
микроорганизмов, а также с ингибированием ферментов. Обладают бактериостатическим действием,
угнетая делящиеся клетки. Спектр действия широкий: подавляют рост и размножение
грамположительных и грамотрицательных кокков, возбудителей кишечных инфекций, чумы,
туляремии, холеры, бруцеллеза, пситтакоза, сифилиса, вирусов трахомы, риккетсии, простейших
(амебы) и т.д. В кишечнике всасываются удовлетворительно. Молоко, содержащее казеинат кальция,
задерживает всасывание, так как образует хелатные соединения с тетрациклинами. Наиболее
продолжительным действием обладает доксициклин, затем метациклин, окситетрациклин и
тетрациклин. Они хорошо проникают в ткани, включая плаценту, накапливаются в печени и костях.
Достаточные концентрации в ликворе создаются только при парэнтеральном введении. Выводятся с
мочой и желчью, причем часть препарата, выделившаяся с желчью в кишечнике подвергается
обратному всасыванию. Назначают преимущественно внутрь, морфоциклин — в/в. Интервалы между
введениями для тетрациклина и окситетрациклина — 4–8 ч, для метациклина — 10–12 ч, для
морфоциклина и доксициклина — 12–24 ч. ПЭ: раздражающее действие на слизистые (глоссит,
стоматит, диспепсия, боли при в/м инъекциях, тромбофлебиты при в/в введении), гепатотоксичность,
тератогенность (связывание кальция и нарушение формирования скелета и зубов). В связи с этим
тетрациклины противопоказаны во 2-й половине беременности и детям до 7 лет. Могут вызывать
фотосенсибилизацию, аллергию, дисбактериозы (кандидамикоз, стафилококковый энтерит,
суперинфекции протея, синегнойной палочки). Для профилактики кандидамикоза назначают нистатин,
других суперинфекций — соответствующие АБ.
Левомицетин. Относится к бактериостатикам широко спектра действия, аналогичного
тетрациклинам. МД обусловлен угнетением синтеза белка. Устойчивость бактерий к нему развивается
медленно. Хорошо всасывается из кишечника, легко проникает в Ткани, включая мозг.
Биотрансформация происходит в печени, около 10% выделяется через почки в неизмененном виде.
Применяют внутрь и местно (линимент). Для парэнтерального введения используют левомицетина
сукцинат натрия (хлороцид С). Назначают преимущественно для лечения брюшного тифа,
сальмонелезов, риккетсиозов, бруцелеза, инфекций, вызванных палочкой инфлюэнцы, а также при
неэффективности других АБ. Применяют короткими курсами под контролем крови. Повторные курсы
не рекомендуют. Противопоказан во время беременности и детям, так как может вызвать тяжелое
поражение ССС у новорожденного и грудного младенца (“синдром серого младенца”). Он может
вызвать угнетение кроветворения вплоть до развития аграиулоцитоза, а также дисбактериоз.
Аминогликозиды
К ним относятся стрептомицин, неомицин, мономицин, канамицин, гентамицин, сизомицин,
амикацин. Оказывают бактерицидный эффект, подавляя синтез белка в рибосомах. Спектр действия
широкий, особенно активны против грамотрицательных микробов. В ЖКТ всасываются плохо (около
97% дозы выводится с фекалиями в неизмененном виде), поэтому при приеме внутрь эффективны
против кишечных инфекций. Хорошо действуют местно при лечении ран, ожогов, дерматозов. При в/м
введении сохраняют активную концентрацию 8–12 ч, выводятся почками в неизмененном виде,
создавая в моче высокие концентрации, поэтому эффективны при инфекциях мочевыводящих путей
(пиэлиты, циститы, уретриты). Даже при нормальной выделительной функции почек могут
куммулировать и вызывать ПЭ. Заболевания почек резко усиливают опасность куммуляции. Наиболее
опасными ПЭ являются ототоксический и нефротоксический эффекты (возникновение глухоты и
поражения почек). Назначение беременной может вызвать глухоту ребенка, поражение почек и нервномышечной проводимости вплоть до остановки дыхания. Неомицина сульфат назначают только местно
и внутрь для лечения кишечных инфекций, особенно резистентных к другим АБ, а также при
подготовке больного к операции. Особенно активен против кишечной палочки, протея, синегнойной
палочки. При приеме внутрь может вызвать диспепсию, кандидамикоз. При местном применении
всасывается незначительно: мази, содержащие один неомицин или в комбинации с глюкокортикоидами
(“Локакортен-Н”, “Синалар-Н” и др.). Гентамицина сульфат применяют преимущественно при
инфекциях, вызванных синегнойной, кишечной палочками, протеем, устойчивыми стафилококками,
особенно при инфекциях мочевыводящих путей, сепсисе, раневой инфекции. Вводят в/м через 8–12 ч.
Он менее токсичен, чем неомицин. Сизомицин сходен с гентамицином, но более активен в отношении
синегнойной палочки, протея, клебсиелл, энтеробактера, относящихся к наиболее распространенным
хирургическим инфекциям. Вводят в/м, иногда в/в. Близкими свойствами обладает амикацин. Все
аминогликозиды нельзя комбинировать между собой из-за усиления ототоксичсского и
нефротоксического действия. Они противопоказаны при заболеваниях слухового нерва, нарушении
выделительной функции почек, беременным. Детям раннего возраста назначают только по жизненным
показаниям.
Полимиксины
Применяют преимущественно полимиксина М сульфат. Действует на грамотрицательные микробы
(кишечная и синегнойная палочки, возбудители дизентерии, паратифов, бруцеллеза, сальмонеллы). МД
обусловлен нарушением проницаемости цитоплазматической мембраны, в результате чего наступает
лизис микробов и бактерицидный эффект. Устойчивость микробов развивается очень медленно.
Применяют только внутрь и местно. При парэнтеральном введении вызывает тяжелые
нейротоксический и нефротоксический эффекты. Внутрь назначают при энтеритах, при подготовке к
операции на органах брюшной полости, местно — при лечении гнойных процессов. Противопоказан
при болезнях почек. Аллергических реакций практически не вызывает.
Лекция 33
СУЛЬФАНИЛАМИДНЫЕ ПРЕПАРАТЫ. ПРОИЗВОДНЫЕ НИТРОФУРАНА. СИНТЕТИЧЕСКИЕ
ПРОТИВОМИКРОБНЫЕ ЛС РАЗНОГО СТРОЕНИЯ. ПРОТИВОСИФИЛИТИЧЕСКИЕ СРЕДСТВА.
ПРОТИВОВИРУСНЫЕ ЛС. ПРОТИВОГРИБКОВЫЕ ЛС
В лекции будут рассмотрены следующие основные вопросы:
* — МД сульфаниламидов, спектр и тип протавомикробного действия;
* — классификация сульфаниламидиых препаратов по применению и продолжительности действия;
* — фармакологическая характеристика сульфаниламидов, применение, ПЭ;
* — МД, тип и спектр противомикробного действия производных нитрофурана, применение н ПЭ;
• — фармакологическая характеристика производных 8-оксихинолина, иафтиридина, хиноксалина,
показания к применению, ПЭ препаратов;
* — классификация противосифилитических ЛС, МД, применение, ПЭ;
• — характеристика противовирусных ЛС, классификация, МД и применение;
* — виды грибковых заболеваний, характеристика основных противогркбковых ЛС, показания, ПЭ.
В 1935 г. Г. Домагк обнаружил противомикробные свойства пронтозила (красного стрептоцида) и
ввел его в медицинскую практику. С этого момента началось широкое изучение и применение
сульфаниламидов (СА). Было установлено, что в организме пронтозил расщепляется с образованием
простейшего сульфаниламида — белого стрептоцида, который и обладает противомикробным
действием. Все препараты СА получены путем замещения атома водорода в амидной группе
стрептоцида различными радикалами, т.е. являются производными стрептоцида, имеют общий МД и
мало отличаются по спектру действия. Различия относятся лишь к силе, продолжительности действия и
ПЭ. МД СА обусловлен структурным сходством с парааминобензойной кислотой (ПАБК), в результате
чего между ними существуют конкурентные взаимоотношения. При достаточной концентрации СА
вытесняет ПАБК из процесса синтеза дигидрофолиевой и тетрагидрофолиевой кислот, необходимых
для синтеза пуриновых и пиримидиновых оснований, идущих на построение нуклеиновых кислот и
белков. Поскольку конкурентный антагонизм сдвинут в сторону ПАБК, концентрация СА должна
значительно превосходить концентрацию ПАБК. Только при этом условии СА вытесняют ПАБК. В
клетках человеческого организма этого не происходит, так как они получают готовую
дигидрофолиевую кислоту. Этим объясняют избирательность действия СА на микроорганизмы.
Угнетение синтеза белка сопровождается бактериостатическим эффектом, который проявляется
только в отношении тех микробов, которые самостоятельно не могут синтезировать ПАБК.
Присутствие в окружающей среде соединений, имеющих в своем составе ПАБК (гной, новокаин,
дикаин, анестезин) препятствует действию СА. Спектр противомикробного действия СА широкий. Они
подавляют развитие грамположительных и грамотрицательных микробов, крупных вирусов (напр.,
трахомы), простейших (возбудители малярии, токсоплазмоза), возбудителей глубоких микозов. При
несоблюдении принципов химиотерапии к ним развивается перекрестная устойчивость, особенно
характерная для кокков.
Большинство СА хорошо всасывается в ЖКТ и проникает в различные органы и ткани, включая
спинномозговую жидкость, что важно для лечения менингитов. Высокие концентрации СА создаются в
почках, печени, легких, коже. В костях не обнаруживаются. Биотрансформация СА происходит 2-мя
путями — метаболизмом и конъюгацией (присоединение остатка уксусной кислоты, или
ацетилирование). Из организма выводятся почками (частично в неизмененном виде). Часть препарата
подвергается реабсорбции, степень которой влияет на длительность циркуляции СА в организме и
продолжительность действия на микробы. Имеет значение также степень связывания с белками крови,
наиболее выраженная у СА длительного действия.
По применению СА подразделяются на 3 группы: 1) СА, хорошо всасывающиеся из ЖКТ и
применяемые для резорбтивного действия; 2) препараты, плохо всасывающиеся в ЖКТ и применяемые
для лечения кишечных инфекций} 3) препараты для местного применения. СА для резорбтивного
действия обеспечивают в крови высокие и устойчивые концентрации, поэтому их применяют при
инфекционных заболеваниях внутренних органов (пневмонии, менингиты, сепсис, гонорея и др.).
Некоторые СА хорошо всасываются и выводятся почками преимущественно в неизмененном виде,
создавая высокие концентрации в моче, поэтому их применяют для лечения инфекций мочевыводящих
путей (уросульфан, этазол).
СА для резорбтивного действия по продолжительности эффекта подразделяются на следующие
группы: а) непродолжительного действия (сульфадимезин, сульфазин, норсульфазол, этазол,
уросульфан); б) продолжительного действия (сульфапиридазин, сульфадиметоксин); в)
сверхдлительного действия (сульфален). Выделяют также группу комбинированных препаратов
(бактрим, сульфатен, потесептил).
При назначении СА необходимо строго соблюдать основные принципы химиотерапии. Препараты
непродолжительного действия назначают по 1 г 4–6 раз в сутки (интервалы между приемами — 4–6 ч),
курсовая доза — 36–40 г. Препараты длительного действия применяют по 1–2 г а сутки (в 1–2 приема),
курсовая доза — 5–6 г. Препараты сверхдлительного действия назначают по 0,5–1 г 1 раз в 7–10 дней.
СА, действующие преимущественно в просвете кишечника, применяют для лечения кишечных
инфекций (дизентерия, энтероколиты и др.). К ним относятся фталазол и сульгин.
Для местного применения используют стрептоцид, сульфацил-натрий, сульфадиазин серебра.
Стрептоцид назначают в виде присыпок, мазей, линиментов на кожу и раневые поверхности,
предварительно очистив их от гноя и некротических масс, сульфацил-натрий — в виде глазных капель,
сульфадиазин серебра — для лечения ожогов. Сульфацил-натрий хорошо растворим в воде, не
раздражает слизистые, поэтому может назначаться в виде 10–30% растворов при конъюнктивитах,
блефаритах, язвах роговицы, для профилактики гонорейного поражения глаз у новорожденных.
Комбинированные препараты содержат сульфаниламид и триметоприм, который угнетает
превращение дигидрофолиевой кислоты в тетрагидрофолиевую. Благодаря такому сочетанию эффект
значительно усиливается и становится бактерицидным. Бактрим (бисептол) представляет комбинацию
сульфаметоксазола и триметрприма. Он хорошо всасывается в кишечнике и действует 5–8 ч.
Выделяется почками. ПЭ: диспептические расстройства, аллергические реакции, иногда угнетение
кроветворения, печени, почек. Противопоказан детям до б лет, при нарушениях печени, кроветворения,
почек. Аналогичными свойствами обладают сульфатон и потесептил.
Общими ПЭ СА являются диспептические расстройства, нарушение функций ЦНС, кроветворения,
метгемоглобинообразование, гемолиз эритроцитов, кристаллурия и образование камней в почках. При
наличии в анамнезе этих нарушений СА противопоказаны. При назначении СА детям необходимо
учитывать следующее: 1) СА, образующие прочные связи с белками крови (этазол, сульфадиметоксин),
могут вытеснять билирубин, который у детей раннего возраста проникает через ГЭБ и при увеличении
его свободной фракции в плазме может вызвать опасную энцефалопатию; 2) СА хорошо проникают
через плаценту и при назначении беременным могут вызвать у новорожденных метгемоглобинемию и
билирубинемию, что опасно для них; 3) СА у детей раннего возраста, особенно у новорожденных,
могут задерживаться в организме из-за недостаточной функции почек; 4) новорожденным и в первые
месяцы жизни СА длительного действия назначать не рекомендуется, следует использовать препараты
короткого действия; 5) комбинированные препараты (бактрим и др.) детям до 6 лет не назначают.
Производные нитрофурана
Обладают широким спектром действия: подавляют грамположительные и грамотрицательные
микробы, крупные вирусы, простейших, некоторые виды патогенных грибков. МД связывают с
восстановлением нитрогруппы в аминогруппу и угнетением клеточного дыхания микроорганизмов. В
обычных концентрациях оказывают бактериостатическое действие, в более высоких — бактерицидное.
Устойчивость микробов развивается медленно. Перекрестной устойчивости к препаратам этой группы,
а также к АБ и СА не возникает. Эффективны против АБ-устойчивых и СА-устойчивых возбудителей.
Можно комбинировать с пенициллинами, стрептомицином, аминогликозидами, тетрациклннами. К этой
группе относятся фурациллин, фуразолидон, фурадонин, фурагин, солофур. Применяют для
лечения: а) гнойных и анаэробных инфекций, ангин, конъюнктивитов (местно — фурациллин,
фуразолидон, фурагин); б) инфекций мочевыводящих путей (фурадонин, фурагин, солофур); в)
пищевых токсикоинфекций, дизентерии, энтероколитов (фуразолидон, фурагин); г) гнойных
хирургических заболеваний (остеомиэлиты, септикопиемия, абсцесс легкого, перитониты, анаэробные
инфекции) — солофур; д) протозойных инфекций (лямблиоз, трихомонадоз) — фуразолидон.
Нитрофураны хорошо всасываются в кишечнике, легко проникают в ткани, распределяются
равномерно, выделяются преимущественно почками, не угнетают иммунитет. ПЭ: диспептические
расстройства, метгемоглобинемия, кровоточивость в результате угнетения агрегации тромбоцитов,
эмбриотоксичность (гемолиз эритроцитов у плода и новорожденного), аллергические реакции. ПЭ
ослабевают при одновременном назначении витаминов группы В. Для уменьшения ПЭ препараты не
рекомендуют назначать более 2-х недель. Во время лечения нитрофуранами нельзя употреблять
алкоголь из-за возникновения антабусного эффекта. Противопоказаны беременным, кормящим
матерям, детям раннего возраста.
Производные 8-оксихинолина
К ним относятся энтеросептол и нитроксолин (5-НОК). Энтеросептол подавляет развитие
грамположительных и грамотрицательных микробов и амеб. Из ЖКТ всасывается плохо, поэтому
создает высокие концентрации на всем протяжении кишечника. Применяют при бациллярной и
амебной дизентерии, энтероколитах разной этиологии, пищевых токсикоинфекциях. Переносится
хорошо, иногда вызывает диспептические расстройства, явления йодизма (содержит йод в молекуле),
при длительном применении может вызвать неврит зрительного нерва. Для уменьшения ПЭ не
рекомендуют назначать более 2-х недель, а между курсами делать перерывы в 4 недели.
Противопоказания: заболевания зрительного нерва, гипертиреоз, идиосинкразия к йоду. Нитроксолин
имеет широкий спектр действия, включая грибки. Быстро всасывается в кишечнике и, выделяясь через
почки, создает в моче высокие концентрации, поэтому эффективен при инфекциях мочевыводящих
путей. Моча приобретает яркожелтый цвет.
Производные нафтиридина
Основным препаратом является налидиксовая кислота (неграм). Действует преимущественно на
грамотрицательные микробы, но неэффективна против синегнойной палочки. Устойчивость микробов
развивается быстро. Хорошо всасывается в кишечнике и выводится, в основном, в неизмененном виде,
создавая в моче высокие концентрации. Применяют при инфекциях мочевыводящих путей, особенно
вызванных возбудителями, устойчивыми к АБ и СА. ПЭ: диспептические расстройства, сыпи, снижение
остроты зрения, головные боли. Противопоказания: выраженные нарушения зрения, печени, почек,
первые 3 мес. беременности, дети до 2 лет.
Производные хиноксалина
К ним относятся хиноксилин и диоксидин. Имеют широкий спектр действия, включая синегнойную
палочку, протей, анаэробы. Препараты токсичны, поэтому применяют при тяжелых гнойновоспалительных процессах, вызванных микробами, устойчивыми к другим ХТС. Назначают только
взрослым в условиях стационара под контролем врача. ПЭ: диспептические расстройства, головная
боль, головокружение, судороги.
Противосифилитические средства
Возбудителем сифилиса является бледная спирохета. В течении сифилиса различают 4 периода:
первичный, вторичный, третичный и четвертичный. При первичном сифилисе на месте внедрения
спирохет образуется язва (твердый шанкр). Во вторичном периоде развиваются поражения кожи и
слизистых оболочек, в третичном (гуммозном) поражаются внутренние органы и кости (висцеральный
сифилис), для четвертичного периода характерно поражение ЦНС (спинная сухотка и прогрессивный
паралич). Для лечения сифилиса используют антибиотики, органические соединения висмута и
мышьяка. Из АБ наиболее эффективны соли бензилпенициллина, подавляющие спирохеты во всех
периодах болезни. Их назначают с учетом основных принципов химиотерапии. Можно использовать
также бициллины. Устойчивость спирохеты к пенициллинам не возникает. При непереносимости
пенициллинов (тяжелые аллергические реакции) используют тетрациклины, макролиды,
цефалоспорины. Однако они уступают пенициллинам по эффективности.
Препараты висмута (бийохинол, бисмоверол, пентабисмол) оказывают бактериостатическое
действие, связанное с блокадой сульфгидрильных групп тиоловых ферментов спирохет, в результате
чего угнетается тканевое дыхание. По активности они значительно уступают АБ и препаратам
мышьяка. На другие микроорганизмы не действуют. Эффект развивается медленно. Вводят в/м при всех
формах сифилиса. ПЭ: темная кайма на деснах, гингивит, стоматит, диспептические нарушения,
дерматит, иногда нарушения печени и почек.
Препараты мышьяка (новарсенол и миарсенол). МД обусловлен блокадой сульфгидрильных групп
тиоловых ферментов и угнетением окислительных процессов, в результате чего возникает
бактериостатический эффект. Препараты токсичны: поражения ЦНС, полиневриты, угнетение
сердечной деятельности, снижение АД, агранулоцитоз, поражения печени и почек, дерматиты. Поэтому
их применяют редко, в основном, при неэффективности других противосифилитических ЛС.
Новарсенол вводится только в/в, миарсенол — в/м.
В третичном и четвертичном сифилисе назначают препараты йода для ускорения рассасывания
гумм.
Противовирусные средства
Лечение вирусных инфекций является одной из наиболее сложных задач химиотерапии. Вирусы
локализуются внутриклеточно, поэтому воздействовать на них, не повреждая клетки макроорганизма,
очень трудно. Имеется ряд препаратов, обладающих относителоно избирательным действием на клетки,
пораженные вирусами.
Известны следующие пути воздействия на вирусы: 1) угнетение адсорбции вируса на клетке и
проникновения его в клетку, а также процесса высвобождения генома вируса из белка (мидантан); 2)
угнетение синтеза вирусных ферментов (гуанидин); 3) угнетение синтеза нуклеиновых кислот — ДНК
(идоксуридин) и РНК (актиномицин Д); 4) угнетение “сборки” вирионов (метисазон); 5) повышение
устойчивости клетки к вирусу (интерфероны). По химической структуре и происхождению
противовирусные ЛС делятся на: 1) синтетические — производные адамантана (мидантан, ремантадин),
аналоги нуклеозидов (идоксуридин, видарабин); 2) вещества, продуцируемые клетками макроорганизма
(интерфероны).
Мидантан применяют для профилактики гриппа типа А. Для лечения он непригоден. Назначают
внутрь. ПЭ: нарушения функций ЦНС, диспептические расстройства, поражения кожи. Ремантадин
действует аналогично мидантану. Идоксуридин угнетает ДНК-полимеразу и репликацию вирусов.
Применяют местно при герпетическом поражении глаз (кератиты). Видарабин по МД сходен с
идоксуридином. Назначают в/в при герпетическом энцефалите, местно при герпетическом
кератоконъюнктивите и осложненном опоясывающем лишае. Меньше идоксуридина раздражает ткани
и лучше переносится. ПЭ: диспепсии, сыпи, психозы, тремор, тромбофлебиты. Метисазон нарушает
процесс “сборки” вирионов, угнетая синтез структурного белка. Эффективен против вируса оспы.
Применяют для профилактики оспы и уменьшения осложнений при противооспенной вакцинации.
Может вызывать диспептические расстройства. Оксолин применяют в виде мази при аденовирусных и
герпетических поражениях глаз, ринитах, пузырьковом и опоясывающем лишае, для профилактики
гриппа.
Интерфероны вырабатываются клетками организма при воздействии на них вирусов, обычно в самом
начале вирусной инфекции. Повышают устойчивость организма к вирусам. Специфической
активностью не обладают и имеют широкий спектр действия. Устойчивость вирусов к ним не
возникает. Для организма безвредны. МД связан с угнетением синтеза вирусных частиц, РНК и
репликации вирусов. Этот эффект опосредуется через стимуляцию выработки антивирусного белка
клетки. Основными недостатками являются кратковременность действия (период полураспада — 10
мин) и плохое проникновение через тканевые барьеры. Применяют для профилактики гриппа, при
герпетических поражениях глаз, кожи, половых органов, при острых вирусных респираторных
заболеваниях, вирусном гепатите, опоясывающем лишае. Они обладают также противоопухолевой
активностью. Назначают место и парэнтерально. Используют лейкоцитарный (альфа-) и фибробластный
(бета-) человеческий интерферон.
Противогрибковые средства
Заболевания, вызываемые патогенными и условно патогенными грибками (микозы), подразделяются
на 3 группы. 1. Кандидамикозы вызываются грибками типа Кандида. Для них характерны поражения
слизистых оболочек полости рта, глотки, пищевода, кишечника, трахеи, бронхов, наружных половых
органов. В тяжелых случаях может возникнуть септицемия (кандидасепсис). Чаще всего кандидозы
возникают у младенцев, стариков, ослабленных больных, при лечении антибиотиками широкого
спектра действия. 2. Дерматомикозы вызывают дерматофиты, поражающие эпидермис, ногти, волосы.
3. Системные микозы (гистоплазмоз, кокцидиомикоз, бластомикоз, криптококкоз и др.)
характеризуются поражением внутренних органов.
Основным препаратом для лечения кандидамикозов является антибиотик нистатин. Он обладает
фунгистатическим и фунгицидным действием, МД которого состоит в нарушении проницаемости
цитоллазматическеи мембраны. Резистентность грибков развивается редко. Из кишечника всасывается
плохо. Для лечения кандидозов слизистых назначают внутрь и местно. При кандидасепсисе назначают в
больших дозах, чтобы обеспечить эффективную концентрацию в крови. ПЭ, как правило, не вызывает.
Леворин применяют по тем же показаниям, но он более токсичен, поэтому назначают при
неэффективности нистатина. При устойчивости грибков к нистатину и леворину можно применять
клотримазол. Он токсичен, поэтому назначают только местно. Местно применяют также декамин
(аммониевое соединение), который переносится хорошо.
Основным препаратом для лечения дерматомикозов служит антибиотик гризеофульвин. Он угнетает
синтез РНК в дерматофитах и оказывает фунгистатическое действие. Резистентность грибков
практически не возникает. Хорошо всасывается в ЖКТ и накапливается в эпидермисе, волосах и ногтях.
Для резорбтивного действия назначают внутрь, для местного — в мазях с диметнлсульфоксидом
(ДМСО). При его применении рекомендуется удалять пораженные роговой слой кожи и ногти, сбривать
волосы. Лечение курсовое по 1–9 недель. ПЭ: головная боль, тошнота, крапивница, головокружение,
дезориентация в пространстве. При дерматомикозах применяют также миконазол, асмиказол,
ундецин, иитрофунгин, цинкудан, препараты йода.
Для лечения системных (глубоких) микозов применяют антибиотик амфотерицин В. Он нарушает
проницаемость цитоплазматической мембраны и действует фунгистатически. Резистентность грибков
развивается медленно. Из ЖКТ всасывается плохо его вводят в/в, & полости, субдурально,
ингаляционно, местно. Выводится почками очень медленно (20–40% за неделю). Очень токсичен
(диспептические расстройства, лихорадка, падение АД, нефротоксичность, угнетение кроветворения,
гипокалиемия, нейротоксичность, тромбофлебиты и др.). Применяют только в стационаре под
тщательным контролем. При системных микозах используют также антибиотик микогелтин внутрь и
местно и миконазол — синтетитческий препарат, производное имидазола. Миконазол нарушает
функцию цитоплазматической мембраны грибков. При системных микозах его назначают
парэнтерально, при кандидамикозах и дерматомикозах — местно. Менее токсичен, чем амфотерицин,
но может вызывать тромбофлебиты, тошноту, анемию, аллергию.
Лекция 34
ПРОТИВОТУБЕРКУЛЕЗНЫЕ ЛС. ЛРОТИВОПРОТОЗОЙНЫЕ ЛС.
По этим темам необходимо знать следующие основные вопросы:
* – классификация противотуберкулезных средств;
* – основные принципы применения противотуберкулезных средств;
* – фармакологическая характеристика препаратов группы изониазида;
* – фармакологическая характеристика .препаратов стрептомицина, рифампниина, этамбутола,
применение и ПЭ;
* – резервные противотуберкулезные ЛС, применение и ПЭ;
* – основные принципы химиотерапии туберкулеза;
* – классификация противопротозойных средств;
* – классификация и общая характеристика противомалярийных ЛС, их действие на разные стадии
развитая малярийного плазмодия;
* – фармакологическая характеристика гематошизотропных, гистошизотропных и гамонтотропных
средств;
* – основные принципы применения противомалярийных ЛС;
* – классификация и фармакологическая характеристика противоамебных ЛС;
* – средства для лечения лямблиоза, трихомонодазоза, токсоплазмоза, балантидиаза и леишманиоза,
их МД, применение, ПЭ.
Противотуберкулезные средства
К ним относятся ЛС, избирательно подавляющие рост и размножение микобактерий туберкулеза,
появившиеся в медицинской практике в 40-х годах XX века. В 1944 г, был получен стрептомицин, в
1946 г. для лечения туберкулеза были предложены препараты парааминосалициловой кислоты (ПАСК),
в 1952 г. установлена эффективность производных гидразида изоникотиновой кислоты (ГИНК).
Микобактерми (возбудители туберкулеза и проказы) кислотоустойчивы, плохо поддаются действию
ХТС и вызывают тяжелые, длительно текущие инфекции, требующие продолжительного лечения.
Поэтому противотуберкулезные ЛС должны обладать малой токсичностью при достаточной
эффективности.
По происхождению они делятся на 2 группы: 1) синтетические препараты изониазид, этамбутол,
натрия парааминосалицилат (ПАСК), бепаск, этионамид, протионамид, пиразинамид, тиоацетазон; 2)
антибиотики — стрептомицина сульфат, стрептомицина хлоркальциевый комплекс, рифампицин,
циклосерин, канамицина сульфат, флоримицина сульфат. Синтетические ЛС обладают избирательным
действием на микобактерии, антибиотики имеют широкий спектр противомикробиого действия. Тип
действия преимущественно бактериостатический.
Наиболее сложной проблемой лечения туберкулеза является возникновение устойчивости
микобактерий. Она развивается быстро к антибиотикам группы стрептомицина и рифампицина и
относительно медленно к синтетическим ЛС. Для ее преодоления используют комбинации препаратов.
Другой важной проблемой являются ПЭ. К ним относятся аллергические, токсические реакции и
суперинфекции.
Наиболее
опасными
являются
гепатотоксические,
нефротоксические,
гематотоксические и нейротоксические реакции, появление которых требует отмены препаратов.
Для клиники наиболее удобно делить противотуберкулезные ЛС по эффективности и применению на
3 группы: 1) наиболее эффективные — изониазид, рифампицин; 2) средней эффективности —
этамбутол, стрептомицин, этионамид, пиразинамид, канамицин, циклосерин, флоримицин; 3)
умеренной эффективности — ПАСК, тиоацетазон. По применению их можно подразделить на: 1)
препараты 1-го ряда (основные) — изониазид, этамбутол, рифампицин, стрептомицин и 2) препараты
2-го ряда (резервные) — ПАСК, этионамид, пиразинамид, тиоацетазон, циклосерин, канамицин,
флоримицин. Резервные препараты менее активны и более токсичны. Их назначают при устойчивости
микобактерии к препаратам 1-го ряда или при их непереносимости.
При назначении препаратов быстро снижается интоксикация и улучшается самочувствие. При
острых и свежих формах туберкулеза они более эффективны, чем при вяло текущих, хронических
(напр., фиброзно-кавернозная форма), лучше действуют при туберкулезном поражении покровных
тканей, чем внутренних органов. Действие зависит от концентрации препарата в крови и времени
сохранения оптимальной концентрации. Основное значение имеет пик концентрации. Поэтому
используют прерывистое применение (напр., прием суточной дозы сразу или высоких доз 1–2 раза в
неделю). Используют принцип длительного (курсового), непрерывного и комбинированного лечения в
течение 12–24 месяцев.
Основные препараты (1 ряда). Из производных ГИНК главным является изониазид. Он обладает
высокой активностью и действует только на туберкулезную палочку и палочку проказы. В зависимости
от концентрации оказывает бактериостатическое или бактерицидное действие. МД связан с
нарушением структуры и функции клеточных мембран в результате угнетения синтеза миколевых
кислот, которые участвуют в построении стенки микобактерии, обнаруженных только в них. С этим,
по-видимому, связана высокая избирательность действия производных ГИНК. Устойчивость к
изониазиду развивается значительно медленнее, чем к антибиотикам. Он также задерживает развитие
стрептомициноустойчивых форм бактерий. В кишечнике всасывается хорошо, создавая максимальную
концентрацию в крови через 1–2 ч. Легко проникает через биологические барьеры и равномерно
распределяется в тканях, ликворе и полостях. Скорость инактивации изониазида генетически
обусловлена. У одних больных она происходит медленно, у других быстро. Разница может быть в 2–3
раза. Средние инактиваторы (их большинство) занимают промежуточное положение. У медленных
инактиваторов эффект выражен сильнее и чаще возникают осложнения, чем у средних и быстрых
инактиваторов. Первым дозы надо снижать и удлинять интервалы между приемами, а последним —
увеличивать дозы и укорачивать интервалы. Изониазид применяют при всех формах туберкулеза. ПЭ:
нарушение функций ЦНС (головные боли, головокружение, онемение конечностей, иногда судороги,
усиление приступов эпилепсии), полиневриты, диспептические расстройства, аллергия и др. Считают,
что ПЭ связаны с угнетением образования пиридоксальфосфата из пиридоксина (витамин В6), поэтому
пиридоксин с тиамином (витамин В1) назначают для профилактики ПЭ изониазида и других
производных ГИНК (фтивазид, метазид, салюзид растворимый, ИНГА-17). Они менее активны, чем
изониазид, и их применяют ..лишь при непереносимости последнего.
Этамбутол обладает активностью, несколько уступающей изониазиду. Действует только на
микобактерии туберкулеза. МД связан с угнетением синтеза РНК. Устойчивость развивается медленно.
Всасывается хорошо, максимальная концентрация — через 2–4 ч, продолжительность действия 8 ч.
Применяют при всех формах туберкулеза, чаще в сочетании с другими препаратами. ПЭ: нарушения
зрения (ухудшение цветового восприятия, неврит зрительного нерва), которые проходят после отмены
препарата.
Рифампицин — полусинтетический АБ, действующий на микобактерии и грамположительные
бактерии. По эффективности он не уступает изониазиду. В обычных концентрациях действует
бактериостатически, в более высоких бактерицидно. МД: угнетение синтеза РНК. Всасывается хорошо,
действует 8–12 ч. Легко проникает через барьеры, включая ГЭБ. Применяют при всех формах
туберкулеза. Устойчивость микобактерии развивается быстро, поэтому его надо комбинировать с
другими противотуберкулезными ЛС. ПЭ: нарушения печени, диспепсия, лейкопения, иногда аллергия.
Окрашивает мочу, мокроту и слезную жидкость в красный цвет.
Препараты стрептомицина имеют широкий спектр действия (микобактерии, возбудители чумы,
туляремии, бруцеллеза, кокки, некоторые штаммы протея, синегнойная палочка, возбудители кишечных
инфекций и др.). В первые годы применения стрептомицин был наиболее активным средством лечения
туберкулеза, в настоящее время его относят в препаратам средней эффективности. Основным его
недостатком является быстрое развитие устойчивых форм микобактерии, а также возникновение
стрептомицинозависимых форм, которые в присутствии стрептомицина развиваются быстрее. Из
кишечника практически не всасывается, поэтому вводят в/м 1–2 раза в сутки. Проникает через
плаценту, в полости, но не проходит через ГЭБ. При туберкулезном менингите интралюмбально вводят
только хлоркальциевый комплекс стрептомицина. ПЭ: ототоксичность (поражение вестибулярного,
реже — слухового нервов), миорелаксация и угнетение дыхания, раздражающее действие,
суперинфекции, аллергия. Беременным женщинам и новорожденным противопоказан.
Резервные препараты (2-го ряда). Синтетические средства. К ним относятся этионамид,
пиразинамид, натрия парааминосалицилат, тиоацетазон. Этионамид и пиразинамид действуют на
микобактерии, устойчивые к другим препаратам. Однако устойчивость к ним развивается быстро,
поэтому их следует назначать только в комбинации с другими. В кишечнике всасываются хорошо,
проникают через биологические барьеры, инактивируются в печени и выводятся с мочой. ПЭ:
угнетение печени, диспептические расстройства, ортостатический коллапс, нарушение функций ЦНС,
аллергия. Натрия парааминосалицилат (ПАСК) действует только на туберкулезную палочку. МД
связан с конкурентным антагонизмом с парааминобензойной кислотой (ПАБК), которая необходима
для развития микобактерий. Эффект ПАСК бактериостатический. Устойчивость развивается медленно.
Всасывается хорошо, действует 6 ч. В полости проникает хорошо, через ГЭБ — плохо. Активность
невысокая, поэтому применяют только в сочетании с другими препаратами при всех формах
туберкулеза. ПЭ: диспептические расстройства, иногда угнетение печени, кроветворения, щитовидной
железы, кристаллурия, аллергия. Аналогичными свойствами обладает бепаск. Тиоацетазон действует
на возбудителей туберкулеза и проказы бактериостатически. Устойчивость к нему развивается
медленно. Токсичен (угнетает кроветворение, функции печени, почек).
Антибиотики: циклосерин, канамицин, флоримицин. Циклосерин — АБ широкого спектра
действия. Действует преимущественно бактериостатически. МД связывают с угнетением синтеза
бактериальной стенки. Устойчивость микобактерии развивается медленно. В кишечнике всасывается
хорошо и легко проникает в ткани и ликвор. Токсичен, нередко вызывает судороги, психозы,
возбуждение или депрессию, тремор и т.п. Канамицина сульфат — АБ широкого спектра действия.
Действует бактериостатически и бактерицидно. Устойчивость микобактерий развивается быстро. В
ЖКТ всасывается плохо, поэтому назначают в/м 2 раза в сутки. ПЭ: ототоксичность, нефротоксичность
и др. Флоримицина сульфат оказывает бактериостатический эффект и используется при устойчивости
микобактерии к другим препаратам. По эффективности сходен с канамицином.
При проведении химиотерапии туберкулеза необходимо соблюдать следующие принципы: 1)
своевременное (раннее) начало лечения, не дожидаясь результатов бактериологического анализа; 2)
комбинированное применение препаратов (не менее 2–3); 3) учет формы, фазы, длительности
заболевания, чувствительности и устойчивости возбудителя, переносимости препаратов, наличия
сопутствующих заболеваний; 4) длительный срок химиотерапии (10–12 мес. у впервые выявленных); 5)
регулярность применения препаратов и строгий контроль терапии; 6) индивидуальный выбор схемы
лечения с учетом возраста, сопутствующей патологии, оптимальных доз, ритмов и путей введения; 7)
своевременное выявление ПЭ и устойчивости бактерий.
Противопротозойные средства
Используются для лечения инфекций, вызванных возбудителями из класса простейших (протозоа).
Наиболее распространенными заболеваниями этой группы являются малярия, амебиаз, лямблиоз,
трихомонадоз, токсоплазмоз, балантидиаз, лейшманиоз. По применению эти ЛС делятся на следующие
группы: 1) противомалярийные; 2) противоамебные; 3) противолямблиозные; 4) против трихомонадоза;
5) против балантидиаза; 6) против лейшманиоза.
Противомалярийные средства
Возбудителем малярии является плазмодий, который подразделяется на 4 вида: 2 вида вызывают 3дневную малярию, один — 4-дневную и один — тропическую. Наиболее распространенной является 3дневная малярия. Переносчиком плазмодия (и соотвественно — малярии) является самка комара рода
Анофелес. Половой цикл развития плазмодия происходит в ее теле, где образуются спорозоиты. При
укусе человека они проникают в печень, где начинается бесполый цикл развития плазмодия. Вначале
возникают преэритроцитарные формы, которые в результате деления образуют мерозоиты (первичные
тканевые формы). Они проникают в эритроциты, образуя эритроцитарные формы.При их делении
происходит массовая гибель эритроцитов и возникает приступ малярии, а мерозоиты снова внедряются
в здоровые эритроциты, повторяя цикл шизогонии. Часть мерозоитов превращается в женские и
мужские половые клетки — гамонты. При укусе больного комар вместе с кровью всасывает их,
происходит оплодотворение и начинается цикл полового развития. Часть преэритроцитарных
мерозоитов снова внедряется в клетки печени и образует параэритроцитарные (вторичные тканевые)
формы. Из них снова могут возникать эритроцитарные формы и рецидив малярии.
Таким образом, источником заражения человека малярией является комар, который переносит
возбудителя, приступы малярии обусловлены эритроцитарными формами плазмодия, рецидивы болезни
связаны с вторичными тканевыми формами плазмодия, а распространение малярии — с гамонтами.
Следовательно для успешной борьбы с малярией необходимо воздействовать на все стадии развития
плазмодия в теле человека. В связи с этим противомалярийные ЛС подразделяют на: 1)
гематошизотропные, действующие на эритроцитарные формы (хингамин, галохин, акрихин, хинин); 2)
гистошизотропные, действующие на тканевые формы (хлоридин — на преэритроцитарные, примахин
— на параэритроцитарные); 3) гамонтотропные, действующие на половые формы — гамонты
(примахин, хлоридин, хиноцид).
Гематошизотропные ЛС. Основным является хингамин — производное хинолина. Наиболее
сильно подавляет эритроцитарные формы (мерозоиты). Кроме того, он уничтожает амебы и
используется при амебиазе, обладает иммунодепрессивным и противоаритмическим действием.
Хорошо всасывается в ЖКТ, действует длительно. Эффективен при всех формах малярии. ПЭ
возникают редко (в основном, при лечении коллагенозов большими дозами): диспепсия, дерматиты,
головокружение, нарушение зрения, печени, кроветворения. Устойчивость плазмодия развивается
медленно. Галохин по своим свойствам близок хингамину. Хинин — алкалоид коры хинного дерева,
производное хинолина. Он значительно слабее хингамина и галохина, но эффективен при тропической
малярии, устойчивой к хингамину, а также при множественной устойчивости. Хинин действует быстро,
поэтому его можно вводить в/в для купирования малярийной комы. На матку оказывает
стимулирующее действие. Акрихин — производное акридина, действует при всех формах малярии, но
недостаточно активен. При малярии используют редко; применяют преимущественно при кожном
лейшманиозе, лямблиозе и некоторых гельминтозах. ПЭ: нарушения ЦНС, окрашивание кожи и
слизистых глаз в желтый цвет. В качестве гематошизотропных ЛС можно использовать
сульфаниламиды длительного действия (сульфапиридазин, сульфадиметоксии, сульфален). Действие
развивается медленно, но продолжительно. Они недостаточно эффективны, поэтому их комбинируют с
другими противомалярийными средствами.
Гистошизотропные ЛС применяют для подавления преэритроцитарных (хлоридин) и
параэритроцитарных форм плазмодия (примахин). Хлоридии производное пиримидина, действует
медленно и длительно, поэтому его применяют преимущественно для личной профилактики малярии, а
также при лечении тропической малярии и токсоллазмоза (в комбинации с сульфаниламидами).
Примахин действует как на вторичные (параэритроцитарные) формы, так и на гамонты. Применяют
для предупреждения рецидивов и распространения малярии. ПЭ: диспептические расстройства,
угнетение кроветворения.
Гамонтотропные ЛС. Наиболее эффективно подавляют гамонты хиноцнд и примахин. Они также
угнетают развитие вторичных тканевых форм плазмодия. Применяют для профилактики
распространения и рецидивов малярии.
Противомалярийные ЛС применяют: 1) для лечения малярии; 2) для личной профилактики: 3) для
общественной профилактики. Лечение малярии осуществляется комбинированным курсовым
назначением препаратов (напр., хингамин + примахин). Так как при тропической малярии вторичные
тканевые формы не образуются, ее можно вылечить одним препаратом (напр., хлоридином). При
тяжелом течении малярии с развитием коматозного состояния вводят хинин или хингамин в больших
дозах парэнтерально. Личная профилактика осуществляется приемом хлоридина, который подавляет
преэритроцитарные формы, а также хингамином (для профилактики приступов малярии).
Общественная профилактика включает массовое применение гамонтотропных средств (примахин,
хлоридин, хиноцид).
Противоамебные средства
Амебиаз распространен преимущественно в тропических странах. Чаще всего амебы локализуются в
толстом кишечнике и вызывают амебную дизентерию. Системный амебиаз характеризуется
поражением печени, желчных путей, легких и др. органов. По локализации действия протмвоамебные
ЛС делятся на: 1) эффективные при любой локализации амеб (метронидазол); 2) эффективные при
локализации амеб в просвете кишечника (энтеросептол, хиниофон); 3) эффективные при локализации
амеб в просвете и стенке кишечника (тетрациклины); 4) эффективные при локализации амеб в стенке
кишечника и в печени (эметина гидрохлорид); 5) эффективные при локализации амеб в печени
(хингамин). Основным средством является метронидазол. Однако нередко приходится использовать
сочетания препаратов (напр., эметин + тетрациклин + хиниофон; тетрациклин + энтеросептол +
хингамин). Этим достигается усиление эффекта при одновременном снижении доз отдельных
препаратов и уменьшении ПЭ.
Средства для лечения лямблиоза
Лямблии локализуются преимущественно в 12-перстной кишке и тонком кишечнике, вызывая
дуодениты и энтериты. Основными препаратами для лечения лямблиоза являются метронидазол,
акрихин, аминохинол, фуразолидон. Аминохинол используется не только для лечения лямблиоза, но
и токсоплазмоза, а также при коллагенозах. Переносится хорошо. ПЭ: головная боль, шум в ушах,
диспепсия, аллергия. Об остальных ЛС было сказано выше.
Средства для лечения трихомопадоза
Трихомонады локализуются во влагалище и уретре, вызывая вагиниты и уретриты. Основным
препаратом для их лечения, является метронидазол и его аналоги (тинидазол и др.). Их назначают
внутрь и местно (интравагинально). Они малотоксичны и редко вызывают диспептические явления.
Можно использовать также трихомонацид, нитазол и фуразолидон.
Средства для лечения токсоплазмоза
Токсоплазмы локализуются в лимфатических узлах, кишечнике, матке, легких, ЦНС и др. органах.
Они часто вызывают выкидыши, уродства плода. Для лечения используют хлоридии и
сульфаниламиды. Хлоридин противопоказан в первые 3 месяца беременности. Для профилактики
инфицирования плода токсоплазмами применяют сульфаниламиды.
Средства для лечения балантидиаза
Возбудителем является инфузория, которая локализуется в толстом кишечнике, вызывая острые и
хронические колиты. Для лечения применяют мономицин, хиниофои и тетрациклины, назначаемые
внутрь.
Средства для лечения лейшманиоза
Лейшманиоз существует в двух формах — кожная и висцеральная. При кожном лейшманиозе местно
применяют акрихин в виде примочек, а для резорбтивного действия — мономиции. При этом
необходимо помнить, что он обладает ототоксическим и нефротоксическим действием. При
висцеральном лейшманиозе применяют преимущественно солюсурьмии — препарат пятивалентной
сурьмы, который вводят парэнтерально. МД связан с блокадой сульфгидрильных групп тиоловых
ферментов. ПЭ: тошнота, головные боли, сыпи, иногда агранулоцитоз. Противоядием является унитиол.
Лекция 35
ПРОТИВОГЛИСТНЫЕ СРЕДСТВА. ПРОТИВООПУХОЛЕВЫЕ СРЕДСТВА
Противоглистными ЛС называют препараты, используемые для лечения заболеваний, вызываемых
гельминтами (гельминтозов).
Необходимо знать следующие вопросы:
* – основные виды гельминтов, вызывающие кишечные и тканевые гельминтозы;
* – классификация противоглистных средств по применению;
* – фармакологическая характеристика ЛС, применяемых при кишечных нематодозах;
* -фармакологическая характеристика препаратов, применяемых при кишечных цестодозах;
* – препараты, применяемые для лечения кишечных трематодозов.их МД и ПЭ;
* – ЛС, применяемые для лечения внекишечных гельминтозов, их МД и ПЭ.
В организме человека встречается свыше 150 видов гельминтов. Они подразделяются на круглые
(нематоды), плоские (цестоды) и сосальщики (трематоды). Гельминтозы соответственно называют
нематодозами, цестодозами и трематодозами. Они могут быть кишечными и тканевыми. К кишечным
нематодозам относятся аскаридоз (вызывается аскаридами), энтеробиоз (острицы), трихоцефалез
(власоглав), анкилостомидоз (кривоголовка дуоденальная), стронгилоидоз (угрица кишечная) и др.
Тканевыми немато дозами являются трихинелез, вызываемый трихинами, паразитирующими в мышцах;
драгункулез, вызываемый риштой, локализующейся в подкожной клетчатке; филяриоз, вызываемый
филяриями, паразитирующими в лимфатических узлах и сосудах, и др. Кишечными цестодозами
являются дифилоботриоз (лентец широкий), тениоз (вооруженный, или свинной цепень), тениаринхоз
(невооруженный, или бычий цепень), геминолепидоз (карликовый цепень). К тканевым цестодозам
относятся эхинококкоз (пузырчатая стадия бычьего цепня), цистоцеркоз (пузырчатая стадия свинного
цепня). К трематодозам относятся преимущественно внекищечные гельминтозы. Их вызывают двуустка
печеночная (фасциолез), двуустка кошачья, китайская, ланцетовидная (паразитируют в печени и
легких), различные шистосомы (паразитируют в кровеносных сосудах). Указанные гельминты
обладают различной чувствительностью к препаратам, поэтому для их уничтожения используют
большой арсенал ЛС.
Средства для лечения кишечных нематодозов
К ним относятся левамизол, пиперазин, нафтамон, пирантел, пирвиния памоат, мебендазол, дифезил.
Левамизол является препаратом выбора при аскаридозе. МД связан с парализующим влиянием на
нервно-мышечную систему червей и угнетением метаболизма. Однократный прием препарата
обеспечивает уничтожение паразитов в 90–100% случаев. ПЭ обычно не возникают. Назначения
специальной диэты и слабительных средств не требуется. При анкилостомидозе и строи гилоидозе
действует слабее, чем при аскаридозе. Пиперазина адбпинат наиболее эффективен против аскарид и
остриц. Он парализует мускулатуру гельминтов и стимулирует перистальтику кишечника, что
способствует их изгнанию. Дегельминтация наступает у 90–100% больных. Специальной диэты и
слабительных не требуется. Практически нетоксичен. Нафтамон эффективен против аскарид, остриц,
кривоголовки, власоглава. Парализует мускулатуру червей, оказывает послабляющее действие. По
активности уступает левамизолу и пиперазину. Малотоксичен. Дифезил — производное нафтамона,
наиболее активен против власоглава. Пирантел эффективен при аскаридозе, пирвиния памоат — при
инвазии кишечными угрицами и острицами. Мебендазол (вермокс) действует против многих видов
гельминтов, но наиболее эффективен против власоглава.
Средства для лечения кишечных цестодозов. Используют фенасал, трихлорофен, аминоакрихин,
экстракт мужского папоротника, дезаспидин. Фенасал применяют для лечения цестодозов, вызываемых
лентецом широким, бычьим и карликовым цепнями. При тениозе, вызываемом вооруженным цепнем,
назначать не рекомендуют из-за опасности возникновения цистицеркоза, так как фенасал парализует
червей, снижая их устойчивость к пищеварительным ферментам, которые разрушают их и тем самым
способствуют проникновению зародышей (онкосфер) через стенку кишечника. В результате они
попадают в кровь и разносятся по органам, где из них развиваются цистицерки (пузырчатая стадия
цепня). Фенасал из кишечника всасывается плохо и выводится с каловыми массами. Назначение
слабительных снижает его эффективность. Трихлорофен по МД и спектру антигельминтного действия
сходен с фенасалом. Их часто применяют комбинированно. Аминоакрихин слабее фенасала, обладает
раздражающим действием, поэтому нередко вызывает диспептические расстройства. При инвазии
вооруженным цепнем противопоказан. Экстракт мужского папоротника густой и дезаслидин оказывают
парализующее действие на цестод. При их применении необходимо соблюдать определенные правила.
За 2 дня до приема препаратов исключают жирную пищу, накануне приема дают стакан чая с сухарем
на ночь, утром — очистительную клизму, затем — препарат. Всю дозу экстракта мужского папоротника
в капсулах принимают за 15–30 мин, а через 30–60 мин дают солевое слабительное. Если через 3 ч стул
не появляется, назначают очистительную клизму. Эти правила необходимы для предупреждения
всасывания препарата, обладающего высокой токсичностью. ПЭ: судороги, параличи, атрофия
зрительного нерва, угнетение сердца, коллапс. Они обусловлены резорбтивным действием. Препараты
папоротника всасываются в ЖКТ плохо, но при растворении в жирах всасывание резко возрастает.
Поэтому жиры, включая касторовое масло, должны быть исключены. Противопоказания: заболевания
сердца, печени, почек, воспалительные процессы в ЖКТ.
Средства для лечения кишечного трематодоза
С этой целью обычно используют четыреххлористый этилен. При подготовке к лечению за 2 дня
до начала исключают из диэты жиры, алкоголь, назначают углеводную пищу, а после приема препарата
через 15–30 мин вводят солевое слабительное (магния сульфат или натрия сульфат).
Средства для лечения внекишечных гельминтозов
Препаратом выбора при филяриозах является дитразин, который назначают внутрь независимо от
вокализации филярий. Он часто дает ПЭ: головные боли, слабость, тошнота, рвота. Они быстро
исчезают после лечения. При трихинелозе эффективен мебендазол (вермокс), о котором было сказано
выше. Нередко он проявляет активность при внекишечных цестодозах (эхинококкоз) Наиболее часто
внекишечные гельминтозы вызывают трематоды. При шистосомозах основным препаратом является
антимонила-натрия тартрат (производное сурьмы). Его вводят в/в. Токсичен (нарушения ССС, рвота,
артриты, анафилаксия). Противоядием является унитиол. При поражении печени трематодамн
применяют хлоксил. Эффективен против двуусток. За 2 дня до приема препарата исключают жиры из
пищи и алкоголь. Переносится хорошо, но противопоказан при заболеваниях печени, сердца, при
беременности.
Противоопухолевые средства
Противоопухолевыми (противобластомными) называют ЛС, замедляющие размножение или
вызывающие гибель опухолевых клеток. Лекарственная терапия злокачественных опухолей — одна из
наиболее актуальных проблем медицины. Усиленная ее разработка началась после 1946 г., когда
впервые была показана способность азотистого иприта тормозить рост раковой опухоли.
По этой теме необходимо знать следующие вопросы:
* – классификация противоопухулевых средств;
* – фармакологическая характеристика алкилирующих препаратов;
* – противоопухолевые антиметаболиты, их МД, основные и ПЭ;
* – противоопухолевые антибиотики, МД, применение и ПЭ;
* – противоопухолевые ЛС растительного происхождения, МД, применение, ПЭ,
* – характеристика гормональных ЛС для лечения опухолей;
* – применение ферментных препаратов в лечении новообразований;
* – разные синтетические ЛС и радиактивные изотопы в лечении опухолей;
* – принципы комбинированной химиотерапии злокачественных опухолей.
В большинстве случаев химиотерапия опухолей приводит лишь к ремиссии заболевания. Полного
излечения удается добиться лишь при хорионэпителиоме, остром лимфолейкозе у детей,
лимфогранулематозе, раке яичника, раке кожи без метастазов и при некоторых других видах опухолей.
Общими недостатками противоопухолевых препаратов являются привыкание опухолевых клеток к
ним, низкая избирательность действия и относительно высокая токсичность (угнетение кроветворения,
изъязвление слизистых оболочек ЖКТ, угнетение половой функции, сердца, иммунодепрессивное,
мутагенное и тератогенное действие и др.).
Противоопухолевые ЛС делятся на следующие группы: 1) алкилирующие соединения (допан,
сарколизин, циклофосфан, хлорбутин, тиофосфамид, миэлосан и др.; 2) антиметаболиты (метотрексат,
меркаптопурин, фторурацил, гуанин, фторафур,цитарабин); 3) разные синтетитческие средства
(проспидин, спиразидин, прокарбазин, амсакрин, гемцитабин, дибунол, дикарбазин, митоксантрон,
имифос, цисплатин и др.); 4) антибиотики (оливомицин, рубомицин, дактиномицин, блеомицин,
даунорубицин, доксорубицин, идарубмции, адриамицин, митомицин и др.); 5) ЛС растительного
происхождения (колхамин, виндезин, винорельбин, винбластми, подофилин, тенипозид, этопозмд,
доцетахсел, паклитаксел и др.); 6) гормональные препараты и их антагонисты (эстрогены и
антиэстрогены, гестагены, андрогены и антиандрогены, гонадотропин-рилизинг гормоны,
кортмкостеромды); 7) ферментные препараты (аспарагиназа); 8) ретиноиды (третионнн); 9)
радиоактивные изотопы (изотопы золота, йода).
Адкилирующие соединения. Общеклеточные яды, но а терапевтических дозах больше угнетают
опухолевые клетки, чем здоровые. Известно, что различные факторы канцерогенеза (вирусные РНК,
ионизирующая радиация, химические канцерогены) вызывают мутации в хромосомах, в результате чего
начинается бурный процесс селекции клеток с наиболее выраженной мутабильностыо и повышенной
склонностью к хромосомным перестройкам. Образуются клетки с неудержимой способностью к
делению, принципиальный механизм которого остается таким же, как у здоровых клеток. Поэтому
нуклеиновые кислоты играют решающую роль в процессе размножения клеток опухолей и воздействие
на них может затормозить его. МД алкилирующих веществ связан с тем, что они образуют активный
карбониевый ион, который взаимодействует с ДНК и алкилирует ее. Это нарушает структуру и
стабильность ДНК, что приводит к угнетению деления опухолевых клеток и их гибели. В очень малых
дозах эти вещества оказывают мутагенный эффект, т.е. повреждают гены без остановки деления клеток.
Этим они. напоминают действие ионизирующей радиации, поэтому их называют еще
радиомиметическими. Алкилирующие ЛС эффективны при некоторых истинных опухолях (рак кожи,
яичка, яичников, молочных желез и др.) и при опухолеподобных заболеваниях кроветворного аппарата
(хронические лейкозы, лимфогранулематоз). В основном они задерживают рост опухоли и развитие
метастазов, но в ряде случаев могут вызвать обратное развитие опухоли. Избирательность действия на
опухолевые клетки относительна, но так как они сильнее действуют на быстро делящиеся клетки, то
размножение опухолевых клеток подавляется раньше, чем здоровых. Однако вскоре присоединяется
угнетение деления здоровых клеток в быстрорегенерирующих тканях (кроветворный аппарат, эпителий
ЖКТ, половые клетки). Дозировка препаратов индивидуальна. Длительность терапии определяется
состоянием кроветворения (снижение числа лейкоцитов до 2000). Повторные курсы проводят не
раньше, чем через 1–2 мес.
Алкилирующие препараты подразделяются на следующие группы: а) хлорэтиламины (допан,
сарколизин, циклофосфан, хлорбутин, новоэмбихин и др.); б) этиленимины (тиофосфамид, тиодипин);
в) производные нитрозометилмочевины (гидроксикарбамид, кармустин, ломустин); г) производные
метансульфоновой кислоты (миелосан). Помимо угнетения кроветворения, половой функции эти ЛС
обладают раздражающим действием (диспептические расстройства, флебиты).
Антиметаболиты. Являются антагонистами естественных метаболитов, поэтому вмешиваются в
синтез ДНК и РНК. Это приводит к угнетению деления клеток и их гибели. Действие проявляется на
разных этапах синтеза нуклеиновых кислот и зависит от того, антагонистом какого метаболита является
данный препарат. Напр., метотрексат — антагонист фолиевой кислоты, нарушает образование пуринов
и тимидина. Меркаптопурин и тиогуанин угнетают включение пуринов в полинуклеотиды,
фторурацил, фторафур и цитарабин являются антагонистами пиримидина и нарушают синтез
нуклеотидов, тимидина и их включение в ДНК. Их применяют при лечении лейкозов и истинных
опухолей: метотрексат — при остром лейкозе у детей, меркаптопурин — при лейкозах у детей и
взрослых, оба препарата — при хорионэпителиоме матки, раке молочной железы; фторурацил — при
раке желудка, кишечника, молочной железы. Метотрексат и меркаптопурин назначают внутрь, а
фторурацил — в/в. ПЭ сходны с ПЭ алкилирующих препаратов.
Разные синтетические средства. К ним относятся проспидин, дикарбазин, цисплатин и др.
Проспидин применяют при раке гортани. Он мало угнетает кроветворение, но вызывает
неврологические и диспептические расстройства. Цисплатин является соединением платины, нарушает
структуру ДНК опухолевых клеток. Назначают в/в при раке яичка, яичников, матки, мочевого пузыря,
при плоскоклеточном раке, лимфомах. Токсичен, поэтому используют в сочетаниях с другими
противоопухолевыми ЛС. Аналогичное применение находят другие препараты этой группы.
Аятибиотики. Некоторые АБ наряду с противомикробным действием обладают выраженной
противоопухолевой активностью. В эксперименте они дают высокий эффект, но очень токсичны. МД
связан с угнетением синтеза нуклеиновых кислот, что приводит к цитостатическому эффекту.
Используют при гемобластозах и истинных опухолях. ПЭ проявляются угнетением кроветворения,
иммунодепрессивным действием, нарушением функций ЖКТ, кардиотоксическим эффектом,
выпадением волос и т.п. Дактиномицин применяют при хорионэпителиоме матки, опухоли Вильямса у
детей, лимфогранулематозе. Оливомицин проявляет активность при раке яичника, тератобластоме,
ретикулосаркоме и др. Рубомицин активен при хорионэпителиоме, остром лейкозе, ретикулосаркоме.
Противоопухолевой активностью обладают также блеомицин, карминоиицин и др.
ЛС растительного происхождения. Колхамин — алкалоид безвременника Эффективен при раке
кожи. Применяют в мазях. Вызывает гибель и некроз раковых клеток без повреждения здоровых. При
этом раздражает кожу. Розевин (винбластин), виндезин, винорельбин и винкристин — алкалоиды
барвинка розового, активны при лейкозах и истинных опухолях. Вводят в/в. ПЭ: атаксия, нарушение
нервно-мышечной передачи, невралгия, парэстезия, поражения почек. Подофиллин, тенилозид,
этопозид — препараты из корней подофилла щитовидного. Применяют при раке гортани и мочевого
пузыря. В последние годы стали применять препараты тисса — доцетаксил и паклитаксил.
Гормональные и антигормональные средства. К ним относятся эстрогеиы, гестагены, андрогены и
кортикостероиды. Препараты половых гормонов эффективны при истинных гормонозависимых
опухолях (рак молочной железы, матки, яичников, предстательной железы), кортикостероиды — при
лейкозах. В большинстве случаев эти ЛС дают временный эффект, вызывая ремиссию от 4 мес. до
нескольких лет. Рецидивы, как правило, лечению не поддаются. Они не вызывают гибели опухолевых
клеток, а тормозят их деление и восстанавливают гормональную регуляцию.
Андрогены (тестостерон, метилтестостерон, тестэнат, дростанолон) применяют при раке
молочной железы с сохраненным менструальным циклом или в период менопаузы
продолжительностью не более 5 лет. МД связывают с подавлением синтеза эстрогенов. Основным ПЭ
является вирилизация (мускулинизация) — вторичные половые признаки по мужскому типу.
Антиандрогены (ципростеронацетат, флутамид, бикалутамид, нимутамид) блокируют
клеточные андрогенные рецепторы в опухолях предстательной железы, препятствуя их взаимодействию
с тестостероном, в результате чего прекращается рост опухоли. Эффективность высокая (длительная
ремиссия у большинства больных), переносятся хорошо. Иногда возникают гинекомастия,
гиперчувствительность.
Эстрогеиы (синестрол, диэтилстильбестрол, фосфэстрол, эстрацит и др.) назначают при раке
предстательной железы у мужчин и раке молочной железы у женщин с менопаузой более 5 лет.
Устойчивость опухолевых клеток развивается через 1–2 года. ПЭ: феминизация у мужчин,
диспептические расстройства, геморрагии.
Антиэстрогены (томоксифен, торемифен, анэстразол) конкурентно блокируют эстрогенные
рецепторы в органах-мишенях, препятствуя их взаимодействию с эстрадиолом. Применяют при раке
молочной железы и матки в период после климакса.ПЭ: вагинальные кровотечения, диспептические
расстройства.
При раке матки можно использовать гестагены (прогестерон, медроксинпрогестерон, мегестрол).
Считают, что МД связан с угнетением стимулирующего влияния половых гормонов на опухолевые
клетки. Назначают при аденоме простаты, раке матки и молочной железы.
Аналоги гонадотропин-рилизинг гормона (гозерелин и др.) при длительном применении угнетают
секрецию лютеинизирующего гормона гипофиза, что ведет к снижению синтеза половых гормонов и
подавлению опухолевого роста. Применяют при раке простаты, молочной железы и матки. Обычно
хорошо переносятся.
Основным правилом применения препаратов половых гормонов и антигормонов является назначение
их а дозах, вызывающих значительную перестройку гормонального фона организма.
Кортикостероиды (преднизолон, дексаметазон и др.), а также АКТГ применяют при лейкозах и
других гемобластозах. МД сложен и связан, очевидно, с депрессивным влиянием на синтез
нуклеиновых кислот и белков, что сопровождается угнетением продукции незрелых форменных
элементов крови. Их применяют также а комплексной терапии истинных опухолей.
Ингибиторы биосинтеза кортикостероидов (хлодитан, аминоглютетимид) угнетают секрецию
кортикостероидов. Применяют при болезни Иценко-Кушинга, при опухолях надпочечников,
сопровождающихся повышенной секрецией гормонов. Аминоглютетимид назначают также при раке
молочной железы. Переносятся хорошо, иногда возникают диспептические расстройства и аллергия.
Ферментные препараты. Некоторые ферменты обладают противоопухолевой активностью.
Аспарагиназа разрушает аспарагин, который необходим для синтеза ДНК и РНК. Применяют при
лимфолейкозе.
Радиоактивные изотопы золота, йода подавляют митоз опухолевых клеток и вызывают их гибель.
Вводят в ткань опухоли, в/в и внутрь. Изотопы золота применяют при раке лимфатических желез,
плевры, брюшины и др., изотопы йода — при раке щитовидной железы.
Учитывая быстрое развитие устойчивости опухолевых клеток к препаратам, их целесообразно
комбинировать. Обосновано комбинирование ЛС: 1) обладающих различным МД; 2) действующих на
разные фазы клеточного цикла; 3) оказывающих различное токсическое действие, чтобы избежать
суммации ПЭ; 4) быстро и кратковременно действующих с действующими более медленно и длительно
(для продления ремиссии). Противоопухолевые ЛС действуют сильнее на метастазы, чем на основную
опухоль. Поэтому они не подменяют, а дополняют хирургическое лечение и рентгенотерапию.
Успешная химиотерапия опухолей зависит от правильной тактики. Она проводится в 3 этапа. На 1-м
этапе ставится цель добиться индукции (стимуляции) ремиссии, на 2-м — консолидации ремиссии, на
3-м — продлить ремиссию. С этой целью разработаны различные варианты программы комплексной
терапии. На 1-м этапе проводится интенсивная курсовая химиотерапия с помощью одного из вариантов.
Если после 2-х циклов терапии ремиссия не наступает, следовательно, к этому варианту опухолевые
клетки устойчивы и нужно переходить на новую программу. На 2-м этапе добиваются консолидации
(закрепления) ремиссии, о чем судят по картине крови (уменьшение лейкозных клеток без резко
выраженной лейкопении), 3-й этап служит для максимального подавления опухолевых клеток и
продления ремиссии. Выбор программы химиотерапии зависит от вида опухолевого процесса, возраста
больного, переносимости препаратов и от эффективности проводимого лечения.
Лекция 36
ПРИНЦИПЫ ТЕРАПИИ ОСТРЫХ ОТРАВЛЕНИЯ
Причиной отравлений могут быть любые химические вещества и технические жидкости,
используемые в промышленности, сельском хозяйстве и в быту, а также ЛС. Поэтому их условно делят
на профессиональные, бытовые и лекарственные отравления. В лекции будут рассмотрены
преимущественно те меры помощи, которые оказывают при отравлении лекарственными препаратами.
Однако основные принципы лечения сохраняют свое значение и при других отравлениях.
Из ЛС наиболее часто отравления возникают при использовании снотворных, анальгетиков,
нейролептиков, антисептиков, химиотерапевтических, антихолинэстеразных средств, сердечных
гдикозидов и др. Отравление зависит от вещества, которое его вызвало, от организма и окружающей
среды. Вещество, ставшие причиной отравления, определяет картину отравления и тяжесть. Напр., при
от равлении антихолинэстеразными веществами (фосфорорганические инсектициды) на первый план
выступают симптомы резкого повышения тонуса холинергической системы. При отравлении
алкоголем, снотворными, наркотиками наблюдается глубокое угнетение ЦНС. Быстрота, тяжесть и
некоторые симптомы отравления зависят от организма. Прежде всего имеет значение путь поступления
яда в организм (ЖКТ, дыхательные пути, кожа, слизистые оболочки), который необходимо учитывать
при оказании неотложной помощи. Действие яда зависит от возраста и состояния пострадавшего.
Особенно чувствительны дети и старики, у которых отравления протекают белее тяжело. На действие
яда оказывают влияние также факторы внешней среды (температура, влажность, атмосферное давление,
радиация и т.п.).
Неотложная помощь при отравлениях включает мероприятия общего характера и специфические.
Они преследуют следующие цели: 1) предупреждение дальнейшего всасывания яда в организм; 2)
химическая нейтрализация всосавшегося яда или устранение его действия с помощью антидота; 3)
ускорение выведения яда из организма; 4) нормализация нарушенных функций организма с помощью
ЛС симптоматической терапии. При проведении этих мероприятий большое значение имеет фактор
времени: чем раньше начата терапия, тем больше шансов на благоприятный исход. Порядок
перечисленных мер помощи может меняться в каждом конкретном случае и определяться характером и
тяжестью отравления. Напр., при резком угнетении дыхания решающее значение имеет экстренное
восстановление легочного газообмена. С этого и должны начинаться действия врача.
Предупреждение дальнейшего всасывания яда. Характер мероприятий зависит от пути
поступления яда в организм. Если отравление произошло ингаляционным путем (окись углерода,
окислы азота, аэрозоли инсектицидов, пары бензина и т.п.), пострадавшего надо немедленно удалить из
отравленной атмосферы. При попадании яда на слизистые оболочки и кожу его надо смыть водой. Если
яд попал в желудок, необходимо сделать промывание. Чем раньше начато промывание, тем оно
эффективнее. При необходимости делают повторное промывание, так как труднорастворимые вещества
и таблетки могут задерживаться в желудке несколько часов. Промывание лучше делать через зонд,
чтобы предупредить аспирацию яда и промывных вод. Одновременно с промыванием проводят
нейтрализацию или связывание яда в желудке. Для этой цели используют калия перманганат, танин,
окись магния, активированный уголь, яичные белки, молоко. Калия перманганат окисляет
органические яды, но не реагирует с неорганическими веществами. Его дабавляют к воде при
промывании из расчета 1:5000–1:10000. После промывания его надо удалить из желудка, так как он
оказывает раздражающее действие. Активированный уголь является универсальным адсорбентом.
Его вводят а желудок по 20–30 г в виде водной взвеси. Адсорбированный яд может в кишечнике
отщепиться, поэтому прореагировавший уголь надо удалить. Танин осаждает многие яды, особенно
алкалоиды. Его применяют в виде 0,5% раствора. Поскольку яд может освобождаться, танин надо тоже
удалять. Магния окись — слабая щелочь, поэтому нейтрализует кислоты. Ее назначают из расчета 3
ст. ложки на 2 л воды. Так как магний угнетает ЦНС, после промывания его надо удалить из желудка.
Яичные белки образуют с ядами нерастворимые комплексы и обладают обволакивающими
свойствами. Аналогичным действием обладает молоко, однако при отравлении жирорастворимыми
ядами его применять нельзя. Если промывание желудка произвести невозможно, можно использовать
рвотные средства. Обычно назначают апоморфина гидрохлорид по 0,5–1 мл 0,5% раствора п/к. Рвоту
можно вызвать порошком горчицы (1 чайная ложка на стакан воды) или поваренной солью (2 ст. ложки
на стакан воды). При бессознательном состоянии пострадавшего рвотные средства применять нельзя.
Для удаления яда из кишечника применяют солевые слабительные. Лучше использовать натрия
сульфат, так как магния сульфат может вызвать угнетение ЦНС.
Нейтрализация всосавшегося яда с помощью антидотов. Существуют вещества, способные
нейтрализовать действие ядов путем химического связывания или функционального антагонизма. Их
называют антидотами (противоядия). Действие осуществляется на основе химического или
функционального взаимодействия с ядами. Химическим (конкурентным) взаимодействием обладают
такие антидоты как унитиол, дикаптол, натрия тиосульфат, комплексоны, метгемоглобинообразователи
и деметгемоглобинообразователи. Унитиол и дикаптол благодаря наличию двух сульфгидрильных
групп могут связывать ионы металлов, металлоидов, молекулы сердечных гликозидов. Образовавшиеся
комплексы выводятся с мочой. Угнетение ферментов, содержащих сульфгидрильные группы (тиоловые
ферменты), устраняется. Препараты высокоэффективны при отравлениях соединениями сурьмы,
мышьяка, ртути, золота. Менее эффективны при отравлении препаратами висмута, солями хрома,
кобальта, меди, цинка, никеля, полония, сердечными гликозидами. При отравлении солями свинца,
кадмия, железа, марганца, урана, ванадия и др. они неэффективны. Уиитиол вводят в/м в виде 5%
раствора. Натрия тиосульфат используют при отравлениях соединениями мышьяка, свинца, ртути,
цианидами, с которыми он образует малотоксичные комплексы. Назначают в/в в виде 30% раствора.
Комплексоны образуют клешневидные (хелатные) связи с большинством металлов и радиоактивными
изотопами. Образовавшиеся комплексы малотоксичны и выводятся с мочой. Для ускорения этого
процесса назначают обильное питье и мочегонные. Используют этилендиаминтетраацетат (ЭДТА) в
виде
динатриевой
соли
и
кальцийдинатриевой
соли
—
тетацин-кальций.
Деметгемоглобинообразователи — вещества, способные переводить метгемоглобин в гемоглобин. К
ним относятся метиленовый синий, применяемый в виде “хромосмона” (1% раствор метиленового
синего в 25% растворе глюкозы), и цистамин. Их применяют при отравлениях веществами,
вызывающими образование метгемоглобина (нитриты и нитраты, фенацетин, сульфаниламиды,
левомицетин и др.). В свою очередь вещества, вызывающие образование метгемоглобина
(метгемоглобинообржзователи) амилнитрит, натрия нитрит — используют для нейтрализации
соединений синильной кислоты, так как 3-валентное железо метгемоглобина связывает цианионы и тем
самым предотвращает блокаду дыхательных ферментов. Реактиваторы холинэстеразы (дипироксим,
изонитрозин и др.), взаимодействуя с фосфорорганическими соединениями (хлорофос, дихлофос и
др.), высвобождают фермент ацетилхолинэстеразу и восстанавливают ее активность. Их применяют при
отравлении антихолинэстеразными ядами. При отравлениях широко используют функциональный
антагонизм: напр., взаимодействие холиноблокаторов (атропин) и холинрмиметиков (мускарин,
пилокарпин, антихолинэстеразные вещества), гистамина и антигистаминных ЛС, адреноблокаторов и
адреномиметиков, морфина и налоксона.
Ускорение выведения всосавшегося яда из организма. Лечение отравлений методом
“промывания организма” занимает ведущее положение. Осуществляется введением большого
количества жидкости и быстродействующих диуретиков. Происходит разведение (гемодилюция) яда в
крови и тканях и снижение его концентрации, а назначение осмотических диуретиков или фуросемида
ускоряет его выведение с мочой. Если больной в сознании, назначают обильное питье, если без
сознания — вводят в/в 5% раствор глюкозы или изотонический раствор натрия хлорида. Этот метод
можно использовать только при сохранении выделительной функции почек. Для ускорения выведения
кислых соединений мочу подщелачивают натрия гидрокарбонатом, щелочные соединения быстрее
выводятся с кислой мочой (назначают аммония хлорид). При отравлениях барбитуратами,
сульфаниламидами, салицилатами и особенно ядами, вызывающими гемолиз, применяют заменное
переливание крови и плазмозамещающие растворы (реополиглюкин и др.). При поражении почек
(напр., при отравлении сулемой) используют метод гемодиализа аппаратом искусственной почки.
Эффективным методом детоксикации организма является гемосорбция, осуществляемая с помощью
специальных сорбентов, адсорбирующих яды, находящиеся в крови.
Симптоматическая терапия функциональных нарушений. Направлена на устранение симптомов
отравления и восстановление жизненно важных функций. При нарушениях дыхания показана
интубация, отсасывание содержимого бронхов, искусственная вентиляция легких. При угнетении
дыхательного центра (снотворные, наркотики и др.) можно вводить аналептики (кофеин, кордиамин и
др.). При отравлении морфином для восстановления дыхания применяют его антагонисты (налорфин,
налоксон). Если возникает отек легких, проводится комплексное лечение (см. лекцию 16). Развитие
бронхоспазма является показанием для назначения бронхолитиков (адреномиметики, холиноблокаторы,
эуфиллин). Большое значение имеет борьба с гипоксией. С этой целью, помимо препаратов,
нормализующих дыхание и кровообращение, применяют ингаляцию кислорода. При угнетении
сердечной деятельности используют сердечные гликозиды быстрого действия (строфантин,
коргликон), дофамин, а при нарушениях ритма сердца — антиаритмические ЛС (новокаинамид,
аймалин, этмозин и др.). При острых отравлениях в большинстве случаев снижается тонус сосудов и
АД. Гипотензия приводит к ухудшению кровоснабжения тканей и задержке ядов в организме. Для
борьбы с гипотонией используют вазопрессорные ЛС (мезатон, норадреналин, адреналин, эфедрин).
При отравлениях ядами, возбуждающими ЦНС, нередко возникают судороги, для купирования которых
применяют сибазон, натрия оксибутират, тиопентал-натрий, магния сульфат и др. Аллергические
реакции могут сопровождаться развитием анафилактического шока, который требует проведения
срочных мероприятий: введение адреналина, глюкокортикоидов (преднизолон, гидрокортизон),
бронхолитиков, сердечных гликозидов и др. Одним из частых симптомов тяжелого отравления является
коматозное состояние. Кома обычно возникает при отравлениях ядами, угнетающими ЦНС (алкоголь,
барбитураты, морфин и др.) Лечение проводят с учетом вида комы, ее тяжести и направлено на
восстановление нарушенных функций и метаболизма. При возникновении болевого синдрома
используют наркотические анальгетики, но при этом необходимо учитывать состояние дыхания.
Большое значение придается коррекции водно-электролитного баланса и кислотно-основного состояния
организма.
Таким образом, неотложная помощь при острых отравлениях включает комплекс мероприятий,
выбор и последовательность, которых зависят от характера отравления и состояния пострадавшего.
ПРИЛОЖЕНИЯ
ВОПРОСЫ ДЛЯ ПОДГОТОВКИ К ЭКЗАМЕНУ ПО ФАРМАКОЛОГИИ
1.Сердечные гликозиды. История появления в медицине растений, содержащих сердечные
гликозиды. Виды препаратов. Фармакологические эффекты.
2.МД сердечных гликозидов. Критерии оценки терапевтического действия.
3.Сравнительная характеристика препаратов сердечных гликозидов (активность, всасываемость в
ЖКТ, скорость развития и продолжительность
действия, кумуляция).
4.Клинические проявления интоксикации сердечными гликозидами, их лечение и профилактика.
5.Классификация противоаритмических средств.
6.Сравнительная характеристика противоаритмических средств, у которых преобладает
непосредственное влияние на сердце. Показания к применению.
7.Сравнительная характеристка противоаритмических средств, действующих через вегетативную
иннервацию. Показания к применению.
8.Классификация средств, применяемых при ишемической болезни сердца, основанная на принципах
устранения кислородной недостаточности и по применению.
9.Средства, понижающие потребность миокарда в кислороде и улучшающие его кровоснабжение
(препараты нитроглицерина, антагонисты кальция).
10.Средства, понижающие потребность миокарда в кислороде (бета-адреноблокаторы, амиодарон).
11.Средства, повышающие доставку кислорода к сердцу (коронароактивные).
12.Средства, применяемые при инфаркте миокарда. Принципы лекарственной терапии инфаркта
миокарда.
13.Классификация антигипертензивных средств. Принципы гипотензивной терапии.
14.Гипотензивные средства, понижающие тонус вазомоторных центров. Основные и побочные
эффекты.
15.Механизм гипотензивного действия ганглиоблокаторов. Основные эффекты. Применение.
Побочное действие.
16.Локализация и механизм гипотензивного действия симпатолитиков и альфа-адреноблокаторов.
Побочные эффекты.
17.Механизм гипотензивного действия бета-адреноблокаторов. Основные и побочные эффекты.
Применение в кардиологии.
18.Миотропные
гипотензивные
средства
(периферические
вазодилататоры).
Механизм
гипотензивного действия блокатороа кальциевых каналов. Основные и побочные эффекты.
Применение.
19.Механизм гипотензивного действия средств, влияющих на водно-солевой обмен (диуретиков), их
применение.
20.Механизм гипотензивного действия веществ, влияющих на ренин-ангиотензиновую систему, их
применение.
21.Средства, применяемые для купирования гипертонического криза. 22.Гипертензивные средства.
Показания к применению. Побочное действие.
23.Средства, используемые при недостаточнрсти мозгового кровообращения. Основные группы ЛС и
принципы терапии нарушений мозгового кровообращения.
24.Основные принципы и средства печени мигрени.
25.Противоатеросклеротические средства. Классификация. МД и принципы применения
противоатеросклеротических средств.
26.Классификация средств, влияющих на систему крови. Средства, стимулирующие эритропоэз
(антианемические). МД и применение.
27.Средства, стимулирующие и угнетающие лейкопоэз: МД, применение. 28.Средства,
препятствующие агрегации тромбоцитов: МД, применение.
29.Антикоагулянты прямого действия: МД, показания к назначению, противопоказания, побочные
эффекты.
30.Антикоагулянты непрямого действия: МД, показания и протипоказания, ПЭ.
31.Фибринолитические и антифибринолтические средства. МД, применение.
32.Средства, повышающие свертывание крови (коагулянты): МД, применение, ПЭ.
33.Классификация диуретиков. Локализация и МД мочегонных средств, влияющих на функцию
эпителия почечных канальцев. Их сравнительная характеристика, применение.
34.Производные ксантина и осмотические диуретики: МД, показания к применению.
35.Противоподагричсские средства: МД, показания и противопоказания.
36.Средства, используемые для усиления и ослабления родовой деятельности: МД, основные и
побочные эффекты.
37.Средства, используемые для остановки маточных кровотечений: МД, эффекты.
38.Классификация витаминов, виды витаминотерапии. Препараты витаминов В1, В2, В5, B6. Влияние
на обменные процессы, фармакологические эффекты, применение.
39.Препараты витаминов РР, С, Р. Влияние на обмен веществ. Основные эффекты. Показания к
применению отдельных препаратов.
40.Препараты витамина Д: влияние на обмен кальция и фосфора, Применение, ПЭ.
41.Препараты витаминов А, Е, К: основные эффекты, применение, ПЭ.
42.Гормональные препараты. Классификация, источники получения,
применение.
43.Препараты адренокортикотропного, соматотропного и тиреотропного гормонов передней доли
гипофиза. Показания к их назначению.
44.Препараты гормонов задней доли гипофиза. Показания к назначению.
45.Препараты гормонов щитовидной железы. Основные и побочные эффекты. Показания к
назначению.
46.Антитиреоиднме средства: МД, показания к назначению, ПЭ.
47.Препарат гормона паращитовидной железы: основные эффекты, применение. Значение и
применение кальцитонина.
48.Препараты гормонов поджелудочной железы. МД инсулина, влияние на обмен веществ, основные
эффекты и применение, осложнения при передозировке, их лечение.
49.Синтетические антидиабетические средства. Возможные МД, применение.
50.Гормоны коры надпочечников. Глюкокортикоиды и их синтетические заменители.
Фармакологические эффекты, показания к применению, ПЭ.
51.Минералокортикоиды: влияние на водно-солевой обмен, показания к применению.
52.Женские половые гормоны и их препараты: основные эффекты, показания к назначению.
Контрацептивные средства.
53.Препараты мужских половых гормонов: основные эффекты, применение.
54.Анаболические стероиды: влияние на обмен веществ, применение, ПЭ.
55.Кислоты и щелочи: местное и резорбтивное действие, применение для коррекции кислотноосновного состояния. Острое отравление кислотами и щелочами. принципы лечения.
56.Участне ионов натрия и калия в регуляции функций организма. Применение препаратов катрия и
калия.
57.Роль ионов кальция и магния в регуляции функций организма. Применение препаратов кальция и
магния. Антагонизм между ионами кальция и магния.
58.Принципы коррекции нарушений водно-электролитного баланса. Плазмозамещающие растворы.
Растворы для парэнтерального питания.
59.Основные противоаллергические средства: МД и показания применению.
60.Противогистаминные средства: классификация, МД и показания применению.
61.Иммуностимулирующие (иммуномодулирующие) средства: МД применение.
62.История применения антисептиков (А.П.Нелюбин, И.Земельвейс, Д.Листер). Классификация
антисептических средств. Условия, определяющие противомикробную активность. Основные МД.
63.Галогеносодержащие вещества, окислители, кислоты и щелочи: МД. применение.
64.Соединения металлов: МД, местное и резорбтивное действие, особенности применения отдельных
препаратов. Отравление солями тяжелых металлов. Принципы терапии.
65.Антисептические средства алифатического и ароматического ряда и группы красителей.
Особенности действия и применения.
66.Детергенты, производные нитрофурана и бигуаниды. Их противомикробные свойства и
применение.
67.Классификация
химиотерапевтических средств.
Основные принципы
химиотерапии
инфекционных заболеваний.
68.Сульфаниламидные препараты: МД, классификация, применение, ПЭ.
69.Сульфаниламидные препараты, действующие в просвете кишечника. Показания к назначению.
Комбинированные препараты сульфаниламидов с триметопримом: МД, применение. Сульфаниламиды
для местного применения.
70.Противомикробные средства группы нитрофурана: МД, показания к применению.
71.Противомикробные средства разных групп: механизмы и спектры действия, показания к
применению, ПЭ.
72.История получения антибиотиков (исследования Л.Пастера, И.И.Мечникова, А.Флеминга,
Э.Чейна, З.В.Ермольевой). Классификация антибиотиков по спектру, характеру (типу) и механизму
антимикробного действия. Понятие об основных и резервных антибиотиках.
73.Биосинтетические пенициллины. Спектр и МД. Характеристика препаратов. ПЭ.
74.Полусинтетические пенициллины. Их особенности по сравнению с биосинтетическими
пенициллинами. Характеристика препаратов.
75.Цефалоспорины: спектр и МД, характеристика препаратов.
76.Антибиотики группы эритромицина (макролиды): спектр и МД, характеристика препаратов, ПЭ.
77.Антибиотики группы тетрациклина: спектр и МД, характеристика препаратов, ПЭ,
противопоказания.
78.Антибиотики группы левомицетина: спектр и МД, показания и противопоказания к назначению,
ПЭ.
7 9.Антибиотики группы аминогликозидов: спектр и МД, препараты, ПЭ.
80.Антибиотики группы полимиксина: спектр и МД, применение, ПЭ.
81. Осложнения антибиотикотерапии, меры профилактики и лечения.
82.Противоспирохетозные (противосифилитические) средства: МД отдельных групп препаратов, их
применение, побочное действие.
83.Противотуберкулезные средства: классификация, МД, применение, ПЭ.
84.Противовирусные средства: МД и применение.
85.Противомалярийные средства: направленность действия препаратов на различные формы
плазмодия, принципы лечения, индивидуальной и общественной химиопрофилактики малярии. ПЭ
препаратов.
86.Противоаме6ные средства: особенности действия препаратов на амеб в разных местах
локализации, показания к применению, ПЭ.
87.Средства, применяемые для лечения лямблиоза и трихомонадоза. Сравнительная эффективность
препаратов.
88.Средства, применяемые для лечения токсоплазмоза, балантидиаза, лейшманиоза. Характеристика
препаратов.
89.Противогрибковые средства. Различия в спектре действияи показаниях к применению отдельных
препаратов, ПЭ.
90.Классификация противоглистных средств. Средства, применяемые при кишечных нематодозах.
Характеристика препаратов, ПЭ.
91.Средства, применяемые при кишечных цестодозах. Препараты, применение, ПЭ,
92.Средства, применяемые для лечения внекишечных гельминтозов.
93.Противоопухолевые средства. Классификация. ПЭ препаратов. Характеристика алкилирующих
средств.
94.Характеристика противоопухолевых средств группы антиметаболитов, средств растительного
происхождения. Осложнения при назначении противобластомных средств, их предупреждение и
лечение.
95.Антибиотики с противоопухолевой активностью. Гормональные и ферментные препараты,
применяемые при опухолевых заболеваниях.
96.0сновные принципы терапии острых отравлений фармакологическими веществами. Применение
антидотов, функциональных антагонистов и стимуляторов функций.
97.Лечение отравлений антихолинэстеразными средствами.
Примечание: здесь представлены вопросы по темам 2-й части курса лекций; остальные
экзаменационные вопросы содержатся в 1-й части.
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, КОТОРЫЕ НЕОБХОДИМО УМЕТЬ ВЫПИСАТЬ В РЕЦЕПТАХ
НА ЭКЗАМЕНЕ ПО ФАРМАКОЛОГИИ
Название препарата и его основные Средние терапевтические дозы
Формы выпуска
синонимы
для взрослых и пути введения
Средства, влияющие на системы кровообращения и крови.
Дигитоксин (Digitoxinum)
Внутрь — 0,1 мг, ректально —
Таб. по 0,1 мг, свечи по 0,15
0,15 мг
мг
Дигоксин (Digoxinuni)
Внутрь и в/в — 0,25 мг
Таб. по 0,25 мг, амп. по 1 мл
0,025% раствора
Строфанта К (Strophantinum К)
В/в — 0,25 мг
Амп. по 1 мл 0,05% раствора
Коргликон (Corgliсоnum)
В/в — 0,3 мг
Амп. по 1 мл 0,06 % раствора
Лидокаина гидрохлорид (Lidocaini
В/в — 80 мг, капельно — 2
Амп. по 2 мл 10% раствора и
hydrochloridum)
мг/мин, в/м — 200–400 мг
по 2 и 10 мл 2% раствора
Новокаинамид (Novocainаmidum)
Внутрь, в/м и в/в — 0,25–0,5 г
Таб. по 0,25 и 0,5 г, амп. по 5
мл 10% раствора
Хинидина сульфат (Chinidini sulfas) Внутрь — 0,2–0,4 г
Таб. по 0,1 и 0,2 г
Bepanaмил (Verapamilurn). Изоптин Внутрь — 0,04–0,08 г, в/в –
Таб. по 0,04 и 0,08 г, амп. по 2
0,005–0,01 г
мл 0,25% раствора
Аспаркам (Asparcam)
Внутрь — 1–2 таб., в/в — 10–20 Таб., амп. по 5 и 10 мл
мл
Нитроглицерин (Nitroglycerinum)
Под язык — 0,5–1 таб, 1 капс., 1– Таб. по 0,5 мг, фл. по 5 мл 1%
2 капли 1% спиртового раствора раствора, капс. — 0,5 мг
Сустак (Sustac)
Внутрь — 1 таб.
Таб. по 2,6 мг и 6,4 мг
Нитросорбид (Nitrosorbidum)
Внутрь — 0,005–0,01 г
Таб. по 0,005 и 0,01 г
Но-шпа (No-Sha)
Внутрь — 0,04–0,08 г, в/м и в/в Таб. по 0,04 г, амп. по 2 мл 2%
— 2–4 мл 2% раствора
раствора
Нифедипин (Nifedipine). Фенигидин Внутрь — 0,01–0,02 г
Таб., др. по 0,01 г
(Phenihydinum). Коринфар. Кордафен
Клофелин (Сlорhе1inum). Гемитон, Внутрь — 0,075–0,15мг, п/к, в/м Таб. по 0,075 и 0,15 мг, амп.
и в/в — 0,05–0,1 мг
по 1 мл 0,01% pаствора
Катапрессан, Clonidini
hydrochloridum
Кавинтон (Cavinton). Винпоцетин
Внутрь — 5–10 мг, в/в капельно Таб. по 5 мг, амп. по 2 мл
— 10–20 мг
0,5% раствора
Каптоприл (Captopri1). Калотен
Внутрь — 12,5–50 мг
Таб. по 25, 50 и 100 мг
Дибазол (Dibazolum)
Внутрь — 0,02–0,05 г, в/м и в/в Таб. по 0,02 г, амп. по 1, 2 и 5
— 3–4 мл 1% раствора
мл 1% раствора
Ферковен (Fercovenum)
В/в — 2–5 мл, медленно
Амп. по 5 мл
Ферроплекс (Ferroplex)
Внутрь — 1–2 драже
Драже по 100 в упаковке
Метилурацил (Methyluraciluin)
Внутрь — 0,25–0,5 г
Пор., таб. по 0,5 г, свечи
Гепарин (Heparinum)
В/в — 5000–20000 ЕД
Фл. по 5 мл
Неодикумарин (Neodicumarinum).
Внутрь — 0,05–0,1 г
Таб. по 0,05 и 0,1 г
Пелентан, Ethyl biscoumacetate
Стрептодеказа (Streptodecasum)
В/в — 3000000 ЕД
Фл. по 1–1,5 млн. ЕД
Викасол (Vicasolum)
Внутрь — 0,015 г, в/м — 0.1 г
Таб. по 0,015 г, амп. по 1 мл
1% раствора
Фибриноген (Fibrinogenum)
В/в капелью — 2–4 г
Фл., содержащие 1 и 2 г
Кислота аминокапроновая (Асidum Внутрь — 2–3 г, в/в — 100 мл
Пор., фл. по 100 мл 5%
aminocapronicum)
5% раствора (капельно)
раствора
Меркаптопурин (Mercaptopurinum)
Внутрь — 2–2,5мг/кг
Таб. по 0,05 г
Таб. по 2,5 мг, амп. по 5, 50 и
Метотрексат (Methotrexatum)
Внутрь — 30–50 мг 2 раза в
неделю в/м, в/в — 30 мг 1–2 раза 100 мг
в нед
Мочегонные, маточные средства
Дихлотиазид (Dich1othiazidum).
Внутрь — 0,025–0,05 г
Таб. по 0,025 и 0,1 г
Гипотиазид, Hydroch1orthiazide
Фуросемид (Furosemidum). Лазикс,
Фурантрил и др.
Окситоцин (Oxytocinum),
Синтоцинон
Внутрь, в/м и в/в — 0,02–0,04 г
Таб. по 0,04 г, амп. по 2 мл 1%
раствора
В/м — 0,2–2 ЕД, в/в капелью 4–5 Амп. по 1 мл (5 ЕД)
ЕД в 500 мл 5% раствора
глюкозы
Динопрост (Dinoprost). Энзапрост
В/в капелью — 5 мг в 500 мл 5% Амп. по 1 и 5 мг
раствора глюкозы
Эргометрина малеат (Ergometrini
Внутрь — 0,2–0,4 мг, в/м и в/в — Таб. по 0,2 мг, амп.по 1 мл
mаleas)
0,1–0,2 мг
0,02% раствора
Витаминные и гормональные препараты
Тиамина хлорид (Thiamini chloridum) Внутрь — 0,01 г, в/м — 0,025–0,5 Таб. по 2,5 и 10 мг, амп. по 1
г (1–2 мл 5% раствора)
мл 2,5 и 5% раствора
Кислота никотиновая (Acidum
Внутрь — 0,1 г, в/в — 0,05 г
Пор., таб. по 0,05 г, амп. по 1
nicotinicum). Витамин PP.
мл 1% раствора
Кислота аскорбиновая (Acidum
Внутрь, в/м и в/в — 0,05–0,1 г
Порошок, др., таб. по 0,025–
ascorbinicum). Витамин С
0,05 г, амп. по 1 и 2 мл 5 и
10% раствора
Рибофлавин (Riboflavinum). Витамин Внутрь — 5–10 мг
Пор., таб. по 2, 5 и 10 мг
В2, Beflavin и др.
Внутрь — 20–30 мг, п/к, в/м и в/в Пор., таб. по 2, 5 и 10 мг, амп.
Пиридоксина гидрохлорид
по 1 мл 1 и 5% раствора
(Pyridoxini hydrochloridum). Витамин — 50 мг
В6, Adermin, Hexabion
Рутин (Rutinum). Rutosidum
Внутрь — 20–50 мг
Пор., таб. по 0,02 г
Ретинола ацетат (Retinoli acetas).
Внутрь — 0,01 г (33000 МЕ), до Капс. по 3300, 5000 и 33000
Витамин A
50000 ME
ME, амп. no 1 мл (25, 50 и 100
тыс. ME)
Токоферола ацетат (Tocopheroli
Внутрь и в/м — 50–100 мг (до
Фл. по 10–50 мл и амп. по 1
acetas). Витамин Е
300 мг) в сутки
мл 5, 10 и 30% раствора, капс.
по 0,1 и 0,2 мл,
Эргокальциферол (Ergocalferolum)
Внутрь — 10000–20000 ME
Др. по 500 ME, 0,625, 125 и
Виатмин Д2
0,5% растворы в масле (по 25,
50 и 200 тыс. МЕ в 1 мл), 0,5%
раствор в спирте (200000 ME в
1 мл)
Цианокобаламин
П/к, в/м и в/в — от 0,003 до 0,5 Амп. по 1 мл 0,003, 0,01, 0,02
(Cyanocobalaminum). Витамин В12
мг
и 0,05% раствора
Кортикотропин (Cоrtiсоtгорinum)
В/м — 10–20 ЕД
Фл. по 10–40 ЕД
АКТГ, Actrope, Сortrophin и дp.
Питуитрин для инъекций (Pituitrinum П/к и в/м — 5 ЕД
Амп. по 1 мл (5 ЕД)
pro injectionibus)
Тиреоидин (Thyreoidinum)
Внутрь — 0,05–0,1 г
Порошок, таб. по 0,05 г
Трийодтиронина гидрохлорид
Внутрь — 5–25 мкг (до 100 мкг) Таб. по 20 и 50 мкг
(Triiodthyronini hydrochloridum)
в сутки
Мерказолип (Mercazolilum).
Внутрь — 0.005 г (5мг)
Таб. по 0,005 г
Thiamazole, Mercazole и др.
Инсулин (Insulinum). Actrapid,
П/к, в/м и в/в — 10–50 ЕД
Фл. по 5 и 10мл (40 и 80 ЕД в
Insulpar, Insulin-Antrapid
1 мл)
Преднизолон (Prednisolonum).
Внутрь — 5–10 мг (до 100 мг).
Таб. по 1 и 5 мг, амп. по 25 мг
Codelcortone, Precortalon
в/м и в/в — 30–150 мг (до 400 мг)
Дексаметазон (Dexamethasonum).
Внутрь — 2–3 мг (до 4–6 мг)
Таб. по 0,5 мг
Decacort, Dexacort, Minicort
Внутрь — 2,5–5 мг (под язык),
Таб. по 5 мг, амп. по 1мл 0,5%
Дезоксикортакостерона ацетат
раствора в масле
(Desoxycorticosteroni acetas). ДОКСА, в/м — 5–10 мг в сутки
Desoxycortoni acetas
Синестрол (Synestrolum).
Внутрь и в/м — 0,001 (1 мг)
Hexeswtrolum, Estronal и др.
Тестостерона пропионат (Testosteroni В/м — 0,01–0,025 г
propionas)
Антиаллергические средства
Димедрол (Dimedrolum).
Внутрь — 0,05 г, в/м — 0,01–0,05
Diphenhydramini hydrochloridum
г, в/в капелью — 0,02–0,05 г
Таб. по 0,001, амп. по 1 мл
0,1% и 2 % раствора
Амп. по 1 мл 1% и 5%
раствора в масле
Пор., таб. по 0,02, 0,03 и 0,05
г, амп. по 1 мл 1% раствора,
свечи — 5–20 мг
Таб. по 0,05 и 0,1 г
Диазолин (Diazolinum). Mebhydrolini, Внутрь — 0,05–0,2 г
Napadisylas
Противомикробные и противопаразитарные средства
Фурацилин (Furacilnum). Nitrofural, Наружно — 0,02% раствор,
Пор., таб. по 0,1 г
Nitrofurason и дp.
внутрь — 0,1 г
Бензилпенициллина натриевая соль В/м — 250000–500000 ЕД, в/в — Фл. по 250000, 500000 и
(Benzylpenicillinum-natrium)
1–5 млн. ЕД
1000000 ЕД
Оксациллина натриевая соль
Внутрь, в/м и в/в — 0,25–1 г
Таб., капс. и фл. по 0,25 и 0,5 г
(Oxacillnum-natrium)
Ампициллин (Ampicillinum)
Внутрь — 0,5–1 г
Таб. и капс. по 0,25, 0,5 и 1 г
Эритромицин (Erythromycinum)
Внутрь — 0,1–0,25–0,5 г
Таб. по 0,1 и 0,25 г
Тетрациклин (Tetracyclinum)
Внутрь — 0,25–0,5 г
Таб. по 0,1 и 0,25 г
Левомицетин (Laevomycetinum).
Внутрь — 0,25–0,5 г
Таб. по 0,25 и 0,5 г
Chloramphenicolum и др.
Стрептомицина сульфат
В/м — 0,5–1 г
Фл. по 0,25, 0,5 и 1 г
(Streptomycini sulfas)
Гентамицина сульфат (Gentamycini В/м — 0,2–0,4 мг/кг
Фл. по 0,08 г, амп. по 1 и 2 мл
sulfas)
4% раствора
Цефалексин (Cefalexinum). Цenopeкс, Внутрь — 0,25–0,5 г
Капс. по 0,25 г, таб. по 0,5 г,
Ceflon, Keflin и др.
порошок
Цефазолин (Cephazo1in). Кефзол.
В/м и в/в — 0,5–1 г
Фл. по 0,25, 0,5, 1, 2 и 4 г
Цефамезин, Kefol, Кеzolin и др.
Нистатин (Nystatinum). Mycostatin
Внутрь, ректально,
Таб., свечи по 0,25 и 0,5г.
интравагинально — 0,25–0,5 г
Сульфадимезин (Su1fadimezinum)
Внутрь — 1 г
Пор., таб. по 0,25 и 0,5г
Фталазол (Phthalazolum)
Внутрь — 1–2 г
Пор., таб. по 0,5 г
Бактрим (Bactrim). Бисептол
Внутрь — 1–2 таб.
Таблетки
Фуразолидон (Furasolidonum)
Внутрь — 0,1–0,15 г
Таб. по 0,05 и 0,1 г
Нитроксолин (Nitroxolinum). 5-HOK Внутрь — 0,05–0,1 г
Таб. по 0,05 г
Изониазид (Isoniazidum)
Внутрь — 0,1–0,3 г
Таб. по 0,1 и 0,3 г
Метронидазол (Metronidazolum)
Внутрь — 0,25–0,5 г
Таб. по 0,25 и 0,5 г
Пиперазина адипинат (Piperazini
Внутрь — 1,5–2 г
Таб. по 0,2 и 0,5 г
adipinas)
Левамизол (Levamizolum)
Внутрь — 0,15 г
Таб. по 0,05 и 0,15 г
Фенасал (Phenasalum)
Внутрь — 2–3 г
Таб. по 0,25 г
Унитиол (Unithiolum)
В/м — 1 мл 5% раствора на 10 кг Амп. по 5 мл 5% раствора
массы
Примечание: при выписывании препаратов в рецептах студент должен знать их групповую
принадлежность, основной МД, особенности фармакокинетики и фармакодинамики, показания и
противопоказания для назначения, ПЭ, уметь расчитывать дозы для больных пожилого и старческого
возраста и детей раннего возраста.
СОДЕРЖАНИЕ
Лекция 18. Сердечные гликозиды.
Лекция 19. Противоаритмические средства.
3
9
Лекция 20. Антиангинальные средства.
15
Лекция 21. Антигипертензивные (гипотензивные) средства. Гипертензивные средства.
21
Лекция 22. ЛС, применяемые при недостаточности мозгового кровообращения.
Противоатеросклеротические средства.
29
Лекция 23. ЛС, влияющие на систему крови.
36
Лекция 24. Мочегонные средства. Противоподагрические средства.
44
Лекция 25. ЛС, влияющие на сократительную активность миометрия.
50
Лекция 26. Витаминные препараты.
53
Лекция 27. Гормональные средства.
60
Лекция 28. Гормональные средства (продолжение).
65
Лекция 29. ЛС для регуляции водно-электролитного баланса, кислотно-основного состояния и
парэнтерального питания.
71
Лекция 30. Антигистаминные и другие противоаллергические средства. Иммуномодулирующие
средства.
77
Лекция 31. Дезинфицирующие и антисептические средства. Основные принципы химиотерапии. 81
Лекция 32. Антибиотики.
85
Лекция
33.
Сульфаниламидные
препараты.
Производные
нитрофурана.
Синтетические
противомикробные ЛС разного строения. Противосифилитические средства. Противовирусные ЛС.
Противогрибковые ЛС.
94
Лекция 34. Противотуберкулезные ЛС. Противопротозойные ЛС.
101
Лекция 35. Противоглистные средства. Противоопухолевые средства.
108
Лекция 36. Принципы терапии острых отравлений.
114
Вопросы для подготовки к экзамену по фармакологии.
118
Лекарственные препараты, которые необходимо уметь выписать в рецептах на экзамене по
фармакологии
123
Содержание
127