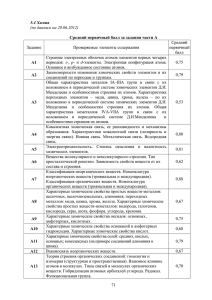
аналитика ЕГЭ 2014 по химии
реклама

Результаты ЕГЭ 2014 Средний тестовый балл Доля участников ЕГЭ, не преодолевших мин. порог Кол-во (доля) 100-балльников край РФ край РФ край РФ 2013 66,75 68,7 1,86 6,3 10 (2,7) 3217 (3,4) 2014 54,8 55,7 10,0 0 (0,0) 482 (0,6) 80.00% 70.00% 60.00% 50.00% 40.00% 30.00% 20.00% 10.00% 0.00% часть 1 часть 2 часть 3 2013 75.21% 56.38% 30.51% 2014 65.04% 37.31% 17.73% 100 90 80 70 60 50 40 30 20 доля выпускников, справившихся с заданием полностью от общего числа выпускников 2013 г. 10 доля выпускников, справившихся с заданием полностью от общего числа выпускников 2014 г. С5 С4 С3 С2 С1 В9 В8 В7 В6 В5 В4 В3 В2 В1 А28 А27 А26 А25 А24 А23 А22 А21 А20 А19 А18 А17 А16 А15 А14 А13 А12 А11 А10 А9 А8 А7 А6 А5 А4 А3 А2 А1 0 А28 А27 А26 А25 А24 А23 А22 А21 А20 А19 А18 А17 А16 А15 А14 А13 А12 А11 А10 А9 А8 А7 А6 А5 А4 А3 А2 А1 90.00 80.00 70.00 60.00 50.00 40.00 30.00 20.00 10.00 0.00 Характерные химические свойства простых веществ (металлов и неметаллов) (А8). Характерные химические свойства оснований в том числе и амфотерных гидроксидов, кислот (А10). Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа (А13). Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола) (А14). Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола (А15). Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды) (А16). Взаимосвязь углеводородов и кислородсодержащих органических соединений (А18). Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия. Природные источники углеводородов, их переработка. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки (А25). 1 • задания, в формулировке которых присутствует отрицание 2 • задания, где необходимо было провести сравнение при выборе правильно ответа 3 • задания на два суждения Какой из перечисленных оксидов реагирует с раствором соляной кислоты, но не реагирует с раствором гидроксида натрия? В отличие от пропана, циклопропан вступает в реакцию… Верны ли следующие суждения о природном газе? А. Основными составляющими природного газа являются метан и ближайшие его гомологи. Б. Природный газ служит сырьём для получения ацетилена B9 B8 28.91 24.88 B7 B6 B5 B4 B3 B2 B1 49.53 50.71 44.08 13.74 40.52 20.14 19.19 26.54 47.87 52.84 17.06 19.43 56.64 47.63 % верно выполненных заданий 19.67 18.72 % частично выполненных заданий Характерные химические свойства простых (металлов и неметаллов) и сложных веществ (оксидов: оснóвных, амфотерных, кислотных, оснований и амфотерных гидроксидов, кислот и солей: средних, кислых, оснóвных; комплексных (на примере соединений алюминия и цинка) (В5), Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений (В6), Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот, сложных эфиров (В8), Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки (В9). Низкая успешность выполнения этих заданий предполагает вывод о несформированности не только знаний выше уже указанных элементов содержания, но и таких умений, как: определять характер среды водных растворов веществ; характеризовать общие химические свойства основных классов неорганических соединений, свойства отдельных представителей этих классов; строение и химические свойства изученных органических соединений; планировать/проводить эксперимент по получению и распознаванию важнейших неорганических и органических соединений, с учетом приобретенных знаний о правилах безопасной работы с веществами в лаборатории и в быту. • задания на соответствие C5 24.88 C4 5.45 C3 9.00 C2 4.98 C1 18.96 21.80 56.16 72.75 40.05 50.95 36.97 44.31 58.06 24.41 31.28 % верно выполненных заданий % частично выполненных заданий % не верно выполненных заданий/ не приступили Обеспечивает проверку знаний и умений: определять степень окисления элементов; определять окислитель и восстановитель; составлять электронный (либо электронно-ионный) баланс и на его основе составлять уравнение окислительно-восстановительной реакции. Затруднения: выбор реакции среды по продуктам реакции и наоборот; составление схемы электронного баланса. Ошибки: определение продуктов реакции, определение степени окисления элементов, определение процессов окисления и восстановления. Используя метод электронного баланса, составьте уравнение реакции Cl2 + I2 + … → HIO3 + … Определите окислитель и восстановитель. Обеспечивает проверку знаний характерных химических свойств неорганических веществ различных классов умений объяснять/характеризовать генетическую связь различных классов неорганических соединений, составлять уравнения реакции с учетом условий их проведения; планировать мысленного эксперимента. Ошибки и затруднения: перевод текста химического эксперимента в химические формулы и уравнения реакций, недостаточность знаний и понимания химических терминов, операций и свойств соединений основных классов неорганических веществ, физических в том числе. Хлорат калия нагрели в присутствии катализатора. Выделившийся бесцветный газ прореагировал с раскалённым железом с образованием железной окалины. Твёрдый остаток растворили в необходимом количестве концентрированной серной кислоты, при этом наблюдали выделение газа с резким запахом. К полученному прозрачному раствору добавили раствор карбоната калия и наблюдали образование бурого осадка и выделение газа. Напишите уравнения четырёх описанных реакций. Обеспечивает проверку целого комплекса знаний по органической химии: глубокого понимания генетической взаимосвязи органических веществ, знания их химических свойств и способов получения, умения учитывать условия проведения реакций, анализировать строение органических веществ. Трудности наличие 3х-4х неизвестных веществ, которые необходимо определить в результате анализа химических превращений, использование структурных формул органических веществ (употребление брутто-формул запрещено) при составлении уравнений соответствующих реакций, окислительно-восстановительные реакции с органическими веществами, электролиз соли органической кислоты. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Х1 Br2, свет 2-бромпропан 2,3-диметилбутан Br2, свет Х2 KOH (спирт) Х3 KMnO4, H2O, 0oC При написании уравнений реакций используйте структурные формулы органических веществ. Х4 Задача комбинированного характера на реакции в водных растворах, включающие оперирование понятиями (массовая доля вещества в растворе/смеси, масса раствор/смеси, масса растворенного вещества, количество вещества); составление уравнений химических реакций (согласно данным условия задачи), необходимых для выполнения стехиометрических расчетов; – выполнение расчетов, необходимых для нахождения ответов на поставленные в условии задачи вопросы; – формулирование логически обоснованного ответа на все поставленные в условии задания вопросы (например, подробное обоснование последовательности действий, результатом которых было установление молекулярной формулы вещества). их использование при расчетах по уравнениям реакции. Основные ошибки: составлении уравнений реакции; использование количественных отношений в химии (количество вещества; молярная масса; молярный объём; массовая доля вещества в растворе/смеси) с учетом стехиометрических соотношений реагирующих веществ, составление плана решения задачи на основе анализа условия задачи, плохое знание условий протекания реакций в растворах и химических свойств неорганических веществ. Определите массовую долю соли в растворе, полученном в результате последовательного растворения в 150 мл воды 10,34 г оксида калия и 6,5 г цинка. Задачи на нахождение молекулярной формулы органического вещества по химической реакции или её схеме, в решении которых лежат последовательные операции: составление схемы химической реакции; определение стехиометрических соотношений реагирующих веществ; вычисления на их основе, приводящие к установлению состава неизвестного вещества Типичными ошибками: вывод общей формулы класса органических веществ; составление уравнения реакции в общем виде; расчет молярной массы вещества. Для полного гидрирования гомолога бензола потребовалось 13,44 л (н.у.) водорода, при этом образовался циклоалкан массой 22,4 г. Запишите уравнение реакции в общем виде. Определите молекулярную формулу гомолога бензола. Считать выход продукта реакции равным 100%.