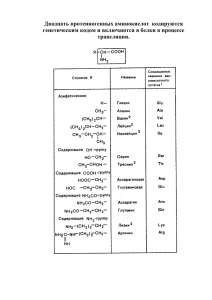
15. Аминокислоты
реклама

Лекция 15 Белки: •Основа костно-мышечных тканей •Иммунная защита организма •Ферменты •Гормоны Природные полимеры, состоящие из остатков a-аминокислот, соединенных амидными связями Классификация аминокислот Заместитель: •Нейтральный •Полярный •Основный •Кислотный •Синтезируемые организмом •Незаменимые 20 аминокислот Алый вальс. Летит из лога Медь прощаний, трав финал. Глина серая, тревога, Церемонность, тишина. Аспидные глуби листопада (Падают в) гигантские аркады. Аланин Валин Лейцин Изолейцин Метионин Пролин Триптофан Фенилаланин Глицин Серин Треонин Цистеин Тирозин Аспарагин и аспарагиновая кислота Глутамин и глутаминовая кислота Лизин Гистидин Аргинин Неполярные алифатические группы Глицин Аланин Валин Лейцин Изолейцин Метионин «Ароматические» группы Фенилаланин Тирозин Триптофан Полярные нейтральные группы Серин Треонин Цистеин Пролин Аспаргин Глутамин Основные группы Лизин Аргинин Гистидин Кислотные группы Аспаргиновая кислота Глутаминовая кислота Способы получения 1. Аминирование a-галогенкарбоновых кислот 2. Аминирование a-галогенкарбоновых кислот по Габриэлю 3. Метод Штреккера-Зелинского Механизм: 4. Синтез на основе малонового эфира Стереохимия аминокислот L-аминокислоты D-аминокислоты L-аланин L-треонин Химические свойства 1. Кислотно-основные свойства биполярный ион (бетаин) Изоэлектрическая точка – значение pH, при котором концентрация биполярного иона максимальна Минимальная растворимость в воде и электропроводность раствора 2. Ацилирование 3. Алкилирование 4. Этерификация 5. Дезаминирование Реакцию используют для количественного определения аминокислот 6. Превращения при нагревании 7. Пептидный синтез 7.1. через хлорангидриды 7.2 карбодиимидный способ