Кафедра детских болезней медицинского факультета РУДН
реклама

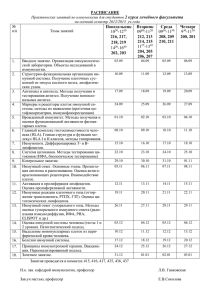
СИСТЕМА HLA И БОЛЕЗНИ Кафедра детских болезней РУДН Профессор Л.Г. Кузьменко ВВЕДЕНИЕ • ХХ век характеризуется интенсивным развитием специализации науки. • Вместе с этим этот век отличался бурным развитием «пограничных» областей науки, что привело к дроблению «классических» дисциплин и формированию новых направлений. • Одним из этих направлений является развитие иммуногенетики. ИММУНОГЕНЕТИКА – СОСТАВНАЯ ЧАСТЬ ГЕНЕТИКИ • Иммуногенетика относительно новая наука. • Начало ее было положено в 1900 г. – с момента открытия Ландштейнером групп крови. • Этим было положено начало учению об изоантигенах тканей. НАПРАВЛЕНИЯ ИММУНОГЕНЕТИКИ ИММУНОГЕНЕТИКА Неинфекционная иммунология Экспериментальная онкология Экспериментальная трансплантология Учение о трансплантационном иммунитете БАЗА ДЛЯ РАЗВИТИЯ ИММУНОГЕНЕТИКИ Основой иммуногенетики является учение о ГЛАВНОМ КОМПЛЕК-СЕ ГИСТОСОВМЕСТИМОСТИ (Major Histocompatibiluty complex - МНС) ГЛАВНЫЙ КОМПЛЕКС ГИСТОСОВМЕСТИМОСТИ Было установлено, что гистосовместимость тканей имеется не только у мышей, но и у собаки, кролика, морской свинки, крысы, обезьян. Широкое распространение гистосовместимости тканей у разных представителей животного мира сформировало понятие о большом (главном) комплексе гистосовместимости. Учение о главном комплексе гистосовместимости стало основным содержанием иммуногенетики, а учение о МНС человека – клинической иммуногенетики Клиническая иммуногенетика основана на прочном фундаменте открытия тканевой совместимости у чловека – системе лейкоцитарных антигенов человека (Human Leukocyte antigen-system – HLA) Антигены МНС выявляются в разных клеточных элементах организма. В наи-большей степени они выражены в мемб-ранах ядросодержащих клеток – лимфоцитах, нейтрофилах, фиксированных клеток органов и тканей. Помимо этого они выявляются в лейкоцитах, тромбоцитах, эри-троцитах. Наиболее изученными являются лейкоцитарные антигены человека, т.е. система HLA. Система HLA – часть МНС. СТРУКТУРА МОЛЕКУЛ HLA Структура молекул HLA включает тяжелую полипептидную цепь с молекулярной массой 39000 – 44000 и легкую цепь. Легкая цепь представ-лена β2микроглобулином с молекулярной массой 12000. Построение молекулы HLA напоминает молекулу IgG. СТРУКТУРА МОЛЕКУЛ HLA Концевая часть полипептидов HLA аналогична Fc- фрагменту иммуноглобу-линов. Полипетдиды HLA погруженны в толщу липидной мембраны и находятся в прочном соединении с ней. Концы тяже-лых и легких полипептидных цепей, кото-рые и обусловливают специфическое ре-агирование с антигенами HLA, обращены наружу. Историческая справка • 1936 год – П. Горер (P. Gorer) открыл локус тканевой совместимости мышей. • В работах G. Snell и P. Gorer изучены гене-тика и серология антигена Р-2. • Установлено, что это комплекс генов, ло-кализующийся уиышей на 17 хромосоме. Отмечен высокий полиморфизм генов этого локуса. • С этого момента иммуногенетика стено-вится самостоятельной В последующем были выделены два гена (Н-2К и Н2D), детерминиро-вавшие образование антигенов в от-вет на которые образуются антитела. Вторая группа Н-2генов детермини-ровала антигены гистосовместимос-ти Н-21, которые, как было установлено, вызывали Т-клеточные реак-ции. Позже к ним были получены антитела. Так заложилось учение о двух классах гистосвместимости. Историческая справка • 40-е годы ХХ века – было выяснено, что антигены тканевой совмести-мости обусловливают процессы отторжения трансплантата и играют важную роль в противоопухолевом иммунитете. Историческая справка • 1958 год – Жан Доссе (J. Dausset) впервые описал антиген лейкоцитов (Мас) и дал его основную иммунологическую и генетическую характеристику. • 1965 год - J. Dausset совместно с Ивани (D. Ivanyi) описал антигенную систему лейко-цитов человека по названием (HuL), кото-рая позже в Международной номенклатуре получила название Human Leukocyte antigen-system – HLA). ЛОКАЛИЗАЦИЯ ГЕНОВ HLA У ЧЕЛОВЕКА • Гены HLA-системы у человека располагается на коротком плече 6 хромосомы. • По протяженности МНС занимает 2 сантиморгана. ___________________________________ Морган – мера расстояния между генами. За единицу генетической длины хромосомы принимается ее отрезок, на котором частота генетического кроссинговера (т.е.обмена идентичными участками между хроматидами гомологичных хромосом в профазе первого мейотического деления) равна 1 %. Сантиморган – 0,01 моргана. Локализация МНС локусов на коротком плече 6-й хромосомы DPB DPA DQB DQA DRB DRA C4 B1 C2 TNF B C A Класс III Класс II Класс I Легенда Локусы I и II классов Широко используемые в научных исследованиях и практике Локусы III класса Находятся в процессе научного исследования НОМЕНКЛАТУРА HLA Согласно номенклатуре ВОЗ (1977 – 1980 гг.) при написании антигенов гистосовместимости после символов HLA через дефис приводится буквенное обозначение сублокуса и порядковый номер аллельного антигена. Например:HLA-А2,HLA-В8, HLA-DRB1-*01 Широкие системы и узкие специфичности HLA А9 А10 А24 А 23 А 25 А 34 В 45 В 55 А 30 В 38 В 17 В 56 В 57 А 31 А 32 А 33 В 16 В 49 В 50 В 22 В 54 А 29 В 21 В 12 В 44 А 26 А 19 В 39 В5 В 51 В 52 В 40 В 58 В 60 В 53 В 15 В 61 В 62 В 63 Учение о главном комплексе гисто-совместимости человека первона-чально (1960 – 1970 гг.) разрабаты-валось исключительно в рамках трансплантологии. Биологическая роль этого комплекса сводилась к созданию трудно преодолимого барьера на пути трансплантации органов и РОЛЬ ГЛАВНОГО КОМПЛЕКСА ГИСТОСОВМЕСТИМОСТИ В ОРГАНИЗМЕ ЧЕЛОВЕКА • • • • К настоящему времени установле-но, что система HLA играет важную роль в трансплантации органов и тканей; регуляции иммунного ответа; межклеточном взаимодействии; противовирусном и противоопухо-левом В последующем, однако, было замечено, что носительство опреде-ленных HLA-антигенов у людей значительно завышено при некоторых болезнях, что свидетельствовало о генетической детерминированности предрасположенности, «запрограм-мированном риске» поражаемости человека той или ИСТОРИЧЕСКАЯ СПРАВКА История клинического направления «HLA и болезни» началась в 1967 г., когда J. Amiel сообщил об отклонениях в фенотипе HLA у больных лимфогранулематозом. Хотя наблюдение J. Amiel в дальнейшем не подтвердилось, оно вызвало интерес к изучению фенотипа HLA у различных групп больных и способствовало развитию указанного РАЗВИТИЕ НАПРАВЛЕНИЯ «HLA и БОЛЕЗНИ» 1972 г. - по инициативе ВОЗ в Ко-пенгагене создается комитет, регис-трирующий все сообщения о взаи-мосвязи между антигенами системы HLA и заболеваниями. 1976 г. – в Париже проводится I Ме-ждународный симпозиум, на котором обсуждались первые итоги этой про-блемы. ПРИНЦИП ВЫЯВЛЕНИЯ БОЛЕЗНИ ПОСРЕДСТВОМ СИСТЕМЫ HLA В последующем сложились основные прин-ципы работы в данной области. В основе сравнения HLA-фенотипов двух групп «больной – здоровый» лежит выявление HLA-антигенов посредством тканевого типирования. Сравнение показателей проводится с помо-щью критериев относительного риска – RR ОСНОВНЫЕ ПРИНЦИПЫ ПОЛОЖИТЕЛЬНЫХ АССОЦИАЦИЙ ДЛЯ ПРОБЛЕМЫ «HLA И БОЛЕЗНИ» • Имеются ассоциации, абсолютно достоверные для всех расовых групп, изученных к настоящему времени (например связи между HLA-В27 и анкилозирующим спондиллитом). • Имеются ассоциации, характерные для определенных этнических групп, связанные с особенностями популяционного распределения HLA-антигенов. ДРУГОЕ НАПРАВЛЕНИЕ ПРОБЛЕМЫ «HLA и БОЛЕЗНИ» • К концу 70-х годов ХХ века было по-казано, что ген, контролирующий си-лу иммунного ответа находится в тесной связи с МНС и картирован у мышей внутри комплекса Н-2 между серологически определямыми локу-сами Н-2К и Н-2D, т.е. в регионе, свя-занным с геном, ГЕН ИММУННОГО ОТВЕТА У ЧЕЛОВЕКА Имеются определенные доказатель-ства, что ген иммунного ответа (IR-ген) у человека находится в тесной связи с HLA-комплексом и, вероятнее всего, располагается в сублокусе DR Проявление функциональной активности IR гена IR-ген – ген силы иммунного ответа Вирусы, бактерии Низкая частота болезней Иммунный ответ IR-ген Высокая предрасположенность Высокая частота болезней Если рассматривать эту схему как от-ражение действительности и реализацию возможностей IR-гена, то ал-лель, способствующий высокому иммунному ответу можно назвать геномпротектором, а аллель, спо-собствующий низкому ответу – ге-ном-провокатором. Аллели гена HLA-А часто несут функ-ции протектора, HLA-В – провока-тора. ИСКЛЮЧЕНИЯ ИЗ ВЫШЕ УКАЗАННОГО ПРАВИЛА • Исключение составляют случаи, при которых наблюдается высокое не-равновесное сцепление генов HLA-А с генами HLA-В. • Генами провокаторами в сублокусе В часто являются следующие группы: крег В7 (В7 – В27), крег В8 (В8 – В14, В18), крег В5 (В5 – В35). При рассмотрении контроля IRгенами антителообразования, высказыва-ется предположение, что в ходе эво-люции происходила селекция IR-ге-нов с высоким типом иммунного ответа, что обеспечивало иммунную защиту против патогенов. Однако можно с достаточным основанием полагать, что высокий тип IRреак-тивности несет повышенный риск развития МАРКЕРЫ БОЛЕЗНЕЙ ОРГАНОВ ДЫХАНИЯ Атопическая бронхиальная астма (БА): м а р к е р ы предрасположенности: HLA-А2, А9, А10, А28; у русских детей – HLA-А1; у детей до 15 лет - HLA-А10 и В7; с наследственной отягощенностью - HLA-А3; тяжелое течение - HLA-В8 и В12; гормонозависимая - HLA-В12 и В35; пыльцевая БА- HLA-В21, В40; п р о т е к т о р ы БА: у русских детей - HLA-А3, А25, В14, В35; гормонозависимая БА - HLA-В5; у казахов - HLA-В27. МАРКЕРЫ ДРУГИХ НЕЭПИДЕМИЧЕСКИХ ЗАБОЛЕВАНИЙ м а р к е р ы инсулинзависимого сахарного диабета: HLA-В8, B15; М а р к е р ы других аутоиммунных заболеваний: HLAВ7; м а р к е р ы системной красной волчанки: HLAВ8; м а р к е р ы ревматической лихорадки: HLA-А9; м а р к е р ы ювенильного ревматоидного артрита: HLAВ10. ДРУГИЕ НЕЭПИДЕМИЧЕСКИЕ ЗАБОЛЕВАНИЯ М а р к е р ы предрасположенности: полипозный риносинусит - HLA-В21, В40; острая пневмония у русских детей - HLA-В7, В27; хронический тонзиллит - HLA-В14; острый пиелонефрит - HLA-А10, В5; острый гломерулонефрит - HLA-А9, В12, В35, В40; мембранозно-пролиферативный гломерулонефрит – HLA-В8, В18; детский липоидный нефроз - HLA-В13; острый лимфоидный лейкоз - HLA-В7, В12, В35, В 40; неблагоприятное течение ОЛЛ - HLA-В22 и В40. ОСТРЫЕ РЕСПИРАТОРНЫЕ ВИРУСНЫЕ ИНФЕКЦИИ маркеры частого возникновения ОРВИ: HLA-А9; русские дети - HLA-А12, А19, В21; дети раннего возраста - HLA-В27; тяжелое течение - HLA-А1, А10; протекторы гриппа - HLA-В8, В40; парагриппа - HLA-В18; частого возникновения ОРВИ - HLA-В13. ВИРУСНЫЕ ГЕПАТИТЫ м а р к е р ы предрасположенности: гепатит А: HLA-А1, А10, В 22; гепатит В: HLA-А9, А10, В5, В8, В16, В18; в таджикской этнической группе - HLAА1, В5; в казахской этнической группе - HLAВ22; хроническое течение гепатита - HLA-А1, В 35; хроническое течение гепатита С - HLA-В8, DR3; гепатит D: HLA-В8; у русских и казахов также HLA-В35; п р о т е к т о р ы: гепатит В: HLA-А9, В13 (в узбекской Другие инфекции М а р к е р ы предрасположенности к пневмококковой инфекции - HLAВ18; Mycoplasma pneumoniaeинфекции - HLA-В18; менингококковая инфекция - HLAВ16; менингококкцемия - HLA-В12; Протекторы менингококковой инфекции - HLAА1, В8; АССОЦИАЦИИ БОЛЕЗНЕЙ С АНТИГЕНАМИ II КЛАССА МНС Маркеры предрасположенности к ауто и м м у н н ы м заболеваниям: DRB1 *01, *03, *04, *08, *09, *10, *17. Маркеры чувствительности к инфекционным заболеваниям DRB1 *11,*12, *13, *14, *15, *16. Взаимодействие системы HLA с системой иммунитета Условные обозначения: АГ – антиген, ПФ- полипептидный фрагмент, Тх1 – Тхелперы 1 типа, Тх2 – Т-хелперы 2 типа, HLA I – молекулы HLA I класса, HLA II – молекулы HLA II класса Фагоцитоз макрофагами АГ и расщепление его на ПФ Связывание ПФ с HLA I Доставка комплекса ПФ + HLA I на поверхность клетки Распознавание (ПФ+ HLA I) Тх1 Лизис клеткимишени Клетки-мишени Связывание ПФ с HLA II Доставка комплекса ПФ + HLA II на поверхность клетки Распознавание (ПФ+ HLA II) Тх2 Синтез антител АНТИГЕНЫ HLA-А У ДЕТЕЙ С ТИМОМЕГАЛИЕЙ АНТИГЕНЫ HLA-В У ДЕТЕЙ С ТИМОМЕГАЛИЕЙ АНТИГЕНЫ HLA-DRB1 У ДЕТЕЙ С ТИМОМЕГАЛИЕЙ ЧАСТОТА ВСТРЕЧАЕМОСТИ АНТИГЕНОВ HLA Патологическое состояние А2 А11 В5 В7 В8 В12 В13 В18 Острый обструктивный бронхит, n = 30 0,57 0,17 0,03 0,27 0,17 0,03 0,23 0,13 Бронхиальная астма, n=7 0,71 0,14 0,14 0,29 0 0,43 0,29 0,29 ОРИ, ассоциирванные с острым стенозирую-щим ларингитом, n =4 0,75 0,25 0 0 0 0,5 0 0,5 Разные заболевания, не сопровождавшиеся синдромом бронхиальной обструкции, 0,68 0,25 0,21 0,07 0,1 0,14 0,18 0,25 ЧАСТОТА ВСТРЕЧАЕМОСТИ АНТИГЕНОВ У ПРЕДСТАВИТЕЛЕЙ РАЗНЫХ ЭТНОСОВ Антигены Русские, n = 42 Другие представители славянской группы n=20 Другая этническая принадлежност ь, n =7 А2 0,69 0,60 0,57 В7 0,24 0,05 0,14 В12 0,19 0,10 0,14 В13 0,17 0,21 0,29 В18 0,21 0,26 0,14 В14 0 0 0 ЧАСТОТА ВЫЯВЛЕНИЯ ГЕТЕРО И ГОМОЗИГОТНЫХ ДЕТЕЙ С ТИМОМЕГАЛИЕЙ В ГРУППАХ ЧАСТО И РЕДКО БОЛЕЮЩИХ ДЕТЕЙ Индикаторы Гетерозиготность Гомозиготность: 1) предрасполож енность к аутоиммунным болезням в т.ч. истинная функциональн ая 2) чувствительно сть к инфекционны м болезням Часто болеющие дети, n = 22 0,273 Редко болеющие дети, n = 16 0,438 0 0,562 0 0 0,312 0,250 0,727 0 0,273 0,454 0 0 Распространенность HLA-антигенов (%) в отдельных популяциях населения Антиге н HLA Москва , n= 150 C-Пб, рус. n = 845 Минск , n= 200 Казахи (АА), n = 105 Корейцы (Кор.) n = 162 А1 23,3 22,2 25,5 22,2 4 А2 49,3 51,6 48,0 39,6 59 А3 24,0 26,9 28,5 19,0 13,3 А9 22,0 27,4 21,0 37,0 34,2 В8 13,3 14,9 10,5 10,0 1 В13 10,0 6,9 11,0 10,5 9 В18 10,0 10,3 18,0 8,9 и.н. В27 7,3 9,9 8,5 8,4 4,7 Частота встречаемости HLA-генов в пуповинной крови Гены HLA Часто встречающиеся Гены HLA Редко встречающиеся А1 0,114 (11,4 %) А69 0,0033 А2 0,288 (28,8 %) А34 0,00035 А3 0,134 (13,4 %) А80 0,00035 А24 0,096 (0,1 %) В47 0,0036 В8 0,067 (0,07 В45 0,002 В13 0,139 (0,14 %) В46 0,002 В18 0,084 (0,08 %) В54 0,0003 В7 0,120 В78 0,0003 %) (0,12 БЛАГОДАРЮ ЗА ВНИМАНИЕ!