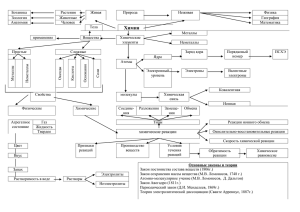
(химические элементы с типично неметаллическими свойствами).
advertisement

Вспомните: • Что такое химический элемент? • Какое вещество называется простым? • Какие основные классы неорганических веществ вы знаете? Памятник Д. И. Менделееву в Санкт-Петербурге В 1829 году Дёберейнер опубликовал найденный им «закон триад»: атомный вес многих элементов близок к среднему арифметическому двух других элементов, близких к исходному по химическим свойствам (стронций, кальций и барий; хлор, бром и йод и др.). Иоганн Вольфганг Дёберейнер Жан Батист Дюма Макс Петтенкофер Первую попытку расположить элементы в порядке возрастания атомных весов предпринял Александр Эмиль Шанкуртуа (1862), который разместил элементы вдоль винтовой линии и отметил частое циклическое повторение химических свойств по вертикали. Однако эта схема не получила конкретного анализа и развития, не указывала точное место элемента в системе. Александр Эмиль Бегуйе де Шанкуртуа «Земная спираль» Шанкуртуа Джон Ньюлендс John Alexander Reina Newlands В 1866 году свой вариант периодической системы предложил химик и музыкант Джон Александр Ньюлендс, модель которого («закон октав») внешне немного напоминала менделеевскую, но была скомпрометирована настойчивыми попытками автора найти в таблице мистическую музыкальную гармонию. Закон октав 1863 – Джон Александер Рейна Ньюлендс. Английский химик. Таблица Мейера 1864 – немецкий ученый Юлиус Лотар Мейер Расположил 44 элемента из известных 62-х в шести столбцах в соответствии с их валентностью по водороду. Однако эта таблица не отражала периодичности свойств. В 1870 г. статья «Природа химических элементов как функция их атомных весов», приведена графическая зависимость атомных объемов от атомных масс (кривая Мейера). Периодическая система химических элементов Д.И.Менделеева Д. И. Менделеев По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». В начале XX века с открытием строения атома было установлено, что периодичность изменения свойств элементов определяется не атомным весом, а зарядом ядра, равным атомному номеру и числу электронов, распределение которых по электронным оболочкам атома элемента определяет его химические свойства. Итогом работы Менделеева в развитии периодического закона является следующий вариант таблицы, который был помещен в 8 издании Основ химии. По свойствам химические элементы классифицируют: • Щелочные металлы (большинство из них растворимо в воде). • Щёлочноземельные металлы (их оксиды — «земли» (по терминологии алхимиков) — сообщают воде щелочную реакцию). • Переходные металлы (переходные элементы) — элементы побочных подгрупп. По свойствам химические элементы классифицируют: • Металлы (группа элементов обладающих характерными металлическими свойствами высокая тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.) • Полуметаллы (металлоиды, амфотерные металлы) — химические элементы, расположенные в периодической системе на границе между металлами и неметаллами.) • Неметаллы (химические элементы с типично неметаллическими свойствами). По свойствам химические элементы классифицируют: • Галогены (химические элементы главной подгруппы VII группы). • Инертные или благородные газы (химические элементы главной подгруппы VIII группы). • Лантаноиды (лантаниды) — семейство из 14 химических элементов III группы 6-го периода периодической таблицы. • Актиноиды (актиниды) — семейство, состоящее из 14 радиоактивных химических элементов III группы 7-го периода периодической системы с атомными номерами 90—103. Лантаноид Классификация атомов 1. По способу застраивания электронной оболочки s- элементы заполняется s-подуровень наружного слоя. Внутренние электронные слои остаются неизменными.Это два первые элемента любого периода p-элементы заполняется р-подуровень наружного слоя Внутренние электронные слои остаются неизменными.Это шесть последних элементов периода (кроме 7-го) d – элементы. Застраивается соседний с наружным уровень. В наружном слое этих элементов на s-подуровне находится чаще 2 реже 1 электрон. Таких элементов по 10 в каждом большом периоде (кроме 7-го) f – элементы. В атомах этих элементов заполняется f-подуровень третьего уровня, считая от внешнего. Сейчас известно 28 таких элементов. Они делятся на два семейства лантаноидов (заполняется 4f-подуровень) и актиноиды (заполняется 5fподуровень). Ответьте на вопросы: • Кто первым попытался систематизировать химические элементы? • Какой ученый составил современную таблицу химических элементов? • О каких основных классах веществ вы узнали на этом уроке? Домашнее задание: • Выучить конспект в тетради. • Подготовить сообщение на тему: «Щелочные металлы. Инертные элементы. Галогены.»