2.4. Электролитические гигрометры. Электролиты – растворы
реклама

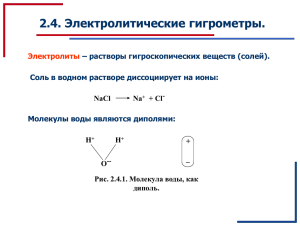
2.4. Электролитические гигрометры. Электролиты – растворы гигроскопических веществ (солей). Соль в водном растворе диссоциирует на ионы: Na+ + Cl- NaCl Молекулы воды являются диполями: H+ H+ O-- + _ Рис. 2.4.1. Молекула воды, как диполь. 2.4. Электролитические гигрометры. Дипольные молекулы воды ориентируются кругом ионов, образуя гидратные (сольватные) оболочки (Рис. 2.4.2). Рис. 2.4.2. Гидратные оболочки иона. В гидратных оболочках молекулы жестко связаны с центральным ионом. Поэтому испарение раствора происходит медленнее, чем испарение воды. Значит, давление насыщения над раствором E* меньше давления насыщения над водой E: E E 2.4. Электролитические гигрометры. Закон Рауля: E E 1 i c E* - давление насыщения над раствором, i – коэффициент Вант-Гоффа, С – концентрация раствора, μ – относительная молекулярная масса воды, μ* – относительная молекулярная масса растворенного вещества. (2.4.1) 2.4. Электролитические гигрометры. E E 1 i c Оставим раствор с электролитом во влажном воздухе (Рис. 2.4.2). Пусть Е* < e. Начинается конденсация воды на раствор. Раствор разбавляется. e E* С E* E* = e e E* Рис. 2.4.2 С Стабильное состояние. E* Теперь предположим Е* > e. Начинается испарение воды с поверхности раствора. Концентрация увеличивается. Единственно стабильное состояние: E* = e. 2.4. Электролитические гигрометры. Значит, если оставить раствор на воздухе, то практически всегда Е* = е. Этим можно воспользоваться для измерения влажности. Электроды Пленка, пропитанная раствором Подложка из пластика Рис. 2.4.3. Датчик влажности (гигристор). 2.4. Электролитические гигрометры. Свяжем сопротивление пленки с влажностью. Пусть: l – длина пленки, b – толщина пленки, d – ширина пленки, – электропроводность раствора. Тогда сопротивление пленки R: R 1 l bd (2.4.2) 2.4. Электролитические гигрометры. Ac(U U ) AcU (2.4.3) A – размерный коэффициент, зависящий от электролита, c – концентрация электролита, U , U – подвижности ионов. Тогда: 1 l R AcU bd (2.4.4) 2.4. Электролитические гигрометры. E E 1 i c R Из закона Рауля: 1 l AcU bd E 1 E 1 f с i i Подставим в (1.4.4): i l R AU (1 f ) bd (2.4.5) 2.4. Электролитические гигрометры. R i l AU (1 f ) bd R Представим это на графике (рис. 2.4.4) 1 0 f Рис. 2.4.4. При увеличении влажности зависимость отличается от той, которая наблюдается при ее уменьшении. Это – гистерезис. 2.4. Электролитические гигрометры. f R f 0 1 f Гистерезис проявляется из-за запаздывания реакции внутренних слоев на изменение влажности. Внутренний слой сохраняет память о предыдущем состоянии раствора. 2.4. Электролитические гигрометры. i l R AU (1 f ) bd Теперь найдем чувствительность гигрометра: i dR l ( S df AU bd S i l 1 1 ( 1 ) ) 2 AU bd 1 f 2 1 f i AU l 1 bd 1 f 2 (2.4.6) При увеличении влажности чувствительность возрастает. 2.4. Электролитические гигрометры. Погрешности электролитического гигрометра. 1. Гистерезис пленки. Способ уменьшения – использование тонких пленок. 2. Разложение раствора электрическим током. Способ уменьшения – использование переменного тока. 2. Температурная погрешность. 2.4. Электролитические гигрометры. Способ уменьшения – компенсационная схема. Схема f i(f,t) Сумматор Схема t Выход i(f) i(t) Рис. 2.4.5. Схема термокомпенсации. Если при изменении t ток со схемы f увеличивается, то ток со схемы t уменьшается на ту же величину. Сумма токов зависит только от влажности.