сульфатированных полисахаридов бурых водорослей
реклама
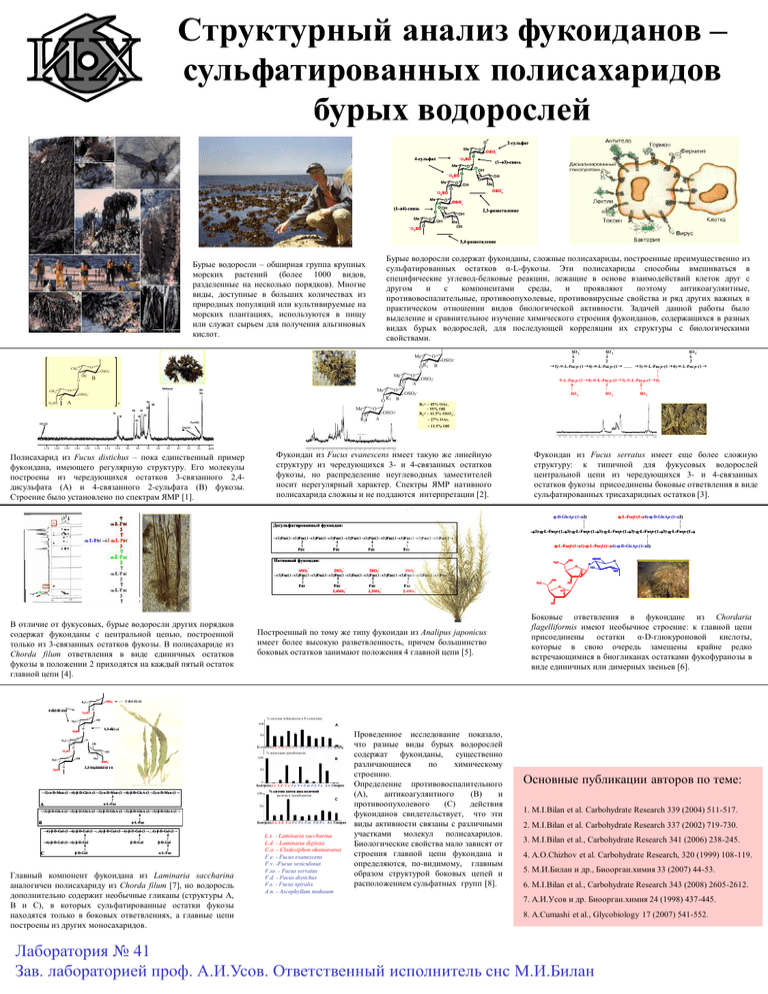
Cтруктурный анализ фукоиданов – сульфатированных полисахаридов бурых водорослей O Me O 2-сульфат OSO 3- - O SO O 3 4-сульфат Me O - O SO O 3 Me O O (13)-связь OH OH O Me OH OSO 3- - O SO O 3 Me O OSO 3- O OH (14)-связь O Me OH O O OH - O SO O 3 2,3-разветвление Me OH 3,4-разветвление Бурые водоросли содержат фукоиданы, сложные полисахариды, построенные преимущественно из сульфатированных остатков α-L-фукозы. Эти полисахариды способны вмешиваться в специфические углевод-белковые реакции, лежащие в основе взаимодействий клеток друг с другом и с компонентами среды, и проявляют поэтому антикоагулянтные, противовоспалительные, противоопухолевые, противовирусные свойства и ряд других важных в практическом отношении видов биологической активности. Задачей данной работы было выделение и сравнительное изучение химического строения фукоиданов, содержащихся в разных видах бурых водорослей, для последующей корреляции их структуры с биологическими свойствами. Бурые водоросли – обширная группа крупных морских растений (более 1000 видов, разделенные на несколько порядков). Многие виды, доступные в больших количествах из природных популяций или культивируемые на морских плантациях, используются в пищу или служат сырьем для получения альгиновых кислот. - O Me O CH3 OH O 5A n O Me 6B 6A OSO3- A 3SO O Me Methanol O O -O OSO3- B O CH3 O R1 R1 O R2 A 1B O Me 2A 2B 4A O 3A R2 Fucf-6C CH3CO 160 150 140 130 120 110 100 90 80 70 60 50 40 30 - B R1= ~ 45% OAc, ~ 55% OH R2= ~ 61.5% OSO3 , OSO3- A ~ 27% OAc, ~ 11.5% OH CH3CO 170 OSO3- OSO3- 3B 5B 4B 1A - SO 3 SO 3 SO 3 2 2 2 3) -a-L-Fuc p-(1 4) -a-L -Fuc p-(1 ........ 3) -a-L-Fuc p-(1 4) -a-L-Fuc p-(1 | | a-L-Fuc p-(1 4) -a-L-Fuc p-(1 3) -a-L-Fuc p-(1 4) 4 2 2 ↑ ↑ ↑ SO 3 SO 3 SO 3 OSO3- B 20 ppm Фукоидан из Fucus evanescens имеет такую же линейную структуру из чередующихся 3- и 4-связанных остатков фукозы, но распределение неуглеводных заместителей носит нерегулярный характер. Спектры ЯМР нативного полисахарида сложны и не поддаются интерпретации [2]. Полисахарид из Fucus distichus – пока единственный пример фукоидана, имеющего регулярную структуру. Его молекулы построены из чередующихся остатков 3-связанного 2,4дисульфата (А) и 4-связанного 2-сульфата (В) фукозы. Строение было установлено по спектрам ЯМР [1]. Десульфатированный фукоидан: 3)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(1 2 4 4 4 ↑ ↑ ↑ ↑ Fuc Fuc Fuc Fuc Фукоидан из Fucus serratus имеет еще более сложную структуру: к типичной для фукусовых водорослей центральной цепи из чередующихся 3- и 4-связанных остатков фукозы присоединены боковые ответвления в виде сульфатированных трисахаридных остатков [3]. a-D-GlcAp-(12) a-L-Fucf-(14)-a-D-GlcAp-(12) | | | | 3)-a-L-Fucp-(13)-a-L-Fucp-(13)-a-L-Fucp-(13)-a-L-Fucp-(13)-a-L-Fucp-(1 | | a-L-Fucf-(12)-a-L-Fucf-(14)-a-D-GlcAp-(12) Нативный фукоидан: H3C - - - HOOC OH O H3C OH O O HO O - 4SO3 2SO3 2SO3 2SO3 3)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(13)Fuc(1 2 4 4 4 ↑ ↑ ↑ ↑ Fuc Fuc Fuc Fuc 2,4SO3 2,3SO3 2,4SO3 OH HO O HO HO В отличие от фукусовых, бурые водоросли других порядков содержат фукоиданы с центральной цепью, построенной только из 3-связанных остатков фукозы. В полисахариде из Chorda filum ответвления в виде единичных остатков фукозы в положении 2 приходятся на каждый пятый остаток главной цепи [4]. O H3C 4-ñóë üô àòû - 2-ñóë üô àò O O3SO O H3C - OSO3- Построенный по тому же типу фукоидан из Analipus japonicus имеет более высокую разветвленность, причем большинство боковых остатков занимают положения 4 главной цепи [5]. % адгезии лейкоцитов к Р-селектину OH 100O A 1,3-ñâÿçü O3SO 50O H 3C O OH - O H3C - O O3SO Контроль L.s. L.d. C.o. F.e. F.v. F.se. F.d. F.s. A.n. WAPS O O3SO OH O OH Боковые ответвления в фукоидане из Chordaria flagelliformis имеют необычное строение: к главной цепи присоединены остатки α-D-глюкуроновой кислоты, которые в свою очередь замещены крайне редко встречающимися в биогликанах остатками фукофуранозы в виде единичных или димерных звеньев [6]. H 3C % агрегации тромбоцитов 100- B OSO3- 2,3-ðàçâåòâë åí è å 50- 21 →2)-α-D-Man-(1→4)-β-D-GlcA-(1→2)-α-D-Man-(1→4)-β-D-GlcA-(1→2)-α-D-Man-(1→ 3 ↑ α-L-Fuc A →3)-β-D-GlcA-(1→3)-β-D-GlcA-(1→3)-β-D-GlcA-(1→3)-β-D-GlcA-(1→3)-β-D-GlcA-(1→ 4 ↑ α-L-Fuc B →6)-β-D-Gal-(1→6)-β-D-Gal-(1→...6)-β-D-Gal-(1→6)-β-D-Gal-(1→…6)-β-D-Gal-(1→ 4 4 4 ↑ ↑ ↑ →6)-β-D-Gal-(1→6)-β-D-Gal β-D-Gal β-D-Gal 4 3 ↑ ↑ β-D-Gal α-L-Fuc C Главный компонент фукоидана из Laminaria saccharina аналогичен полисахариду из Chorda filum [7], но водоросль дополнительно содержит необычные гликаны (структуры А, В и С), в которых сульфатированные остатки фукозы находятся только в боковых ответвлениях, а главные цепи построены из других моносахаридов. 0 Контроль L.s. L.d. C.o. F.e. F.v. F.se. F.d. F.s. A.n. Гепарин 100- % адгезии клеток рака молочной железы к тромбоцитам C 50- Контроль L.s. L.d. C.o. F.e. F.v. F.se. F.d. F.s. A.n. Гепарин L.s. - Laminaria saccharina L.d. - Laminaria digitata C.o. - Cladosiphon okamuranus F.e. - Fucus evanescens F.v. -Fucus vesiculosus F.se. - Fucus serratus F.d. - Fucus distichus F.s. - Fucus spiralis A.n. - Ascophyllum nodosum Проведенное исследование показало, что разные виды бурых водорослей содержат фукоиданы, существенно различающиеся по химическому строению. Определение противовоспалительного (А), антикоагулянтного (В) и противоопухолевого (С) действия фукоиданов свидетельствует, что эти виды активности связаны с различными участками молекул полисахаридов. Биологические свойства мало зависят от строения главной цепи фукоидана и определяются, по-видимому, главным образом структурой боковых цепей и расположением сульфатных групп [8]. Основные публикации авторов по теме: 1. M.I.Bilan et al. Carbohydrate Research 339 (2004) 511-517. 2. M.I.Bilan et al. Carbohydrate Research 337 (2002) 719-730. 3. M.I.Bilan et al., Carbohydrate Research 341 (2006) 238-245. 4. A.O.Chizhov et al. Carbohydrate Research, 320 (1999) 108-119. 5. М.И.Билан и др., Биоорган.химия 33 (2007) 44-53. 6. M.I.Bilan et al., Carbohydrate Research 343 (2008) 2605-2612. 7. А.И.Усов и др. Биоорган.химия 24 (1998) 437-445. 8. A.Cumashi et al., Glycobiology 17 (2007) 541-552. Лаборатория № 41 Зав. лабораторией проф. А.И.Усов. Ответственный исполнитель снс М.И.Билан