Презентация к уроку по теме « Изопроцессы в газах».
реклама

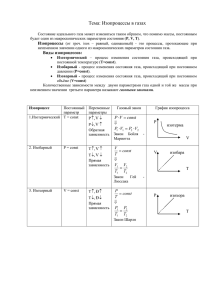
Есть у нас Идеальный газ, И мы запомним сразу Закон, который Клапейрон Открыл для этих газов: Слева в нем – произведение Из объёма и давления, Справа – R на Т стоит, Запиши закона общий вид: m pV = RT M Какой изопроцесс изображён на рисунке? Что вы знаете об этом процессе? Начальное состояние 0 Конечное состояние Т1 С 0 P2 P1 Т2 V1 V2 Q Q С Закон Бойля - Мариотта 1 ~ V р pV = const 1 ~ р V или p1V1 = p2V2 T = const V Роберт Бойль (Великобритания), 1662 г Эдм Мариотт (Франция), 1667 г 0 V P P 0 T 0 T Какой изопроцесс изображён на рисунке? Что вы знаете об этом процессе? Начальное состояние 0 Конечное состояние Т1 С 0 P2 P1 V1 Q V2 Q С Т2 Закон Шарля p ~Т или p = const Т p1 p2 = T1 T2 V = const p Жак Шарль (Франция), 1787 г 0 p T T 0 V 0 V Какой изопроцесс изображён на рисунке? Что вы знаете об этом процессе? Начальное состояние 0 Конечное состояние Т1 С 0 P2 P1 V1 Q Т2 V2 Q С Закон Гей - Люссака V~ Т или V = const Т V1 V2 = T1 T2 p = const Жозеф Луи Гей - Люссак (Франция), 1802 г V V T 0 T 0 P 0 P В одинаковых сосудах при одинаковой температуре находятся водород и углекислый газ. Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки сосуда ? Н2 СО2 ОТВЕТ: М(Н )=2г/моль 2 рV = m M RT М(СО )=44г/моль 2 mRT p= MV Большее давление оказывает водород в 22 раза. 1.Графики каких процессов представлены на участках 1-2; 2-3? 2.Как изменяются P, V и Т на каждом участке? 1 Вариант 2 Вариант Р P 1 2 2 1 3 3 V T 1. Вариант на участке 1-2 P = const; V- увеличивается, T – увеличивается. на участке 2-3 T=const, V – увеличивается, Р – уменьшается. 2. Вариант на участке 1-2 V = const, P- увеличивается, Т – увеличивается. на участке 2-3 T = const, Р – уменьшается V- увеличивается 1. Вариант 2. Вариант Р, Т Р,V Р Р 1 2 2 3 3 1 Т V