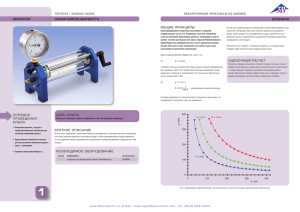
Границы применения закона Бойля
реклама

1 Урок № 7 Тема урока: Изопроцессы в газах. Закон Бойля-Мариотта Цель: установить зависимость между объёмом и давлением газа при постоянной температуре, научиться решать задачи План изучения нового материала 1. Изопроцессы 2. Изотермический процесс 3. Объяснение закона Бойля-Мариотта с точки зрения МКТ 4. Графическое изображение закона 5. Границы применения закона Бойля-Мариотта 6. Решение задач 7. О вреде алкоголя Изучение нового материала 1. Изопроцессы Уравнение состояния идеального газа позволяет описать то, что происходит с газом при любых изменениях всех его параметров. Но много процессов в газах, которые происходят в природе или технике, тогда, когда изменяются два параметра, а третий остаётся неизменным. Процесс – переход системы из одного состояния в другое. Изопроцессы (от греческого «изос» – равный) – это процессы, при которых один из макроскопических параметров – температура, давление, объём при постоянной массе, остаётся неизменным. Газовые законы – количественные зависимости между двумя параметрами газа при неизменном значении третьего параметра. 2. Изотермический процесс Изотермический процесс (от греческого «термо» – тепло) происходит при постоянной температуре. 2 T = const, m = const 𝒑 𝟏 𝑽𝟏 𝑻𝟏 = 𝒑 𝟐 𝑽𝟐 𝑻𝟐 – уравнение состояния, 𝒑𝟏 𝑽𝟏 = 𝒑𝟐 𝑽𝟐 или 𝒑𝟏 𝒑𝟐 = 𝑽𝟐 𝑽𝟏 Закон Бойля-Мариотта pV = const Для данной массы газа произведение давления газа на его объём, постоянно, если температура газа не изменяется. Закон был открыт экспериментально независимо друг от друга в 1662 году английским учёным Р. Бойлем и в 1667 французским учёным Э. Мариоттом. 3. Объяснение закона Бойля-Мариотта с точки зрения МКТ При сжатии газа, при уменьшении объёма, увеличивается его концентрация, возрастает число ударов молекул газа о стенки сосуда, в котором он находится, т. е. давление увеличивается. И, наоборот, при расширении газа давление уменьшается. 4. Графическое изображение закона Графически изотермический процесс изображается в виде изотермы. 3 Рисунок 1,2,3 графики изотерм в осях pV, pT, VT 5. Границы применения закона Бойля-Мариотта Реальный процесс в реальном газе протекает изотермически, если он протекает медленно, т.е. изменением температуры газа за небольшой интервал времени можно пренебречь Пример: Воздух (или инертный газ), находящийся в запечатанном пакете с печеньем расширяется, когда продукт поднят на значительную высоту над уровнем моря (около 2000 м) Рисунок 2 Расширение воздуха в пакете при неизменной температуре 6. Решение задач № 1. Газ сжали изотермически от объёма 8 л до объёма 6 л. Давление при этом возросло на 4 кПа. Каким было начальное давление. Дано: 𝑽𝟏 = 8 л = 8 ∙ 10−3 м3 ; 𝑽𝟐 = 6 л = 6 ∙ 10−3 м3 ; 𝒑𝟐 = 𝒑𝟏 + ∆ 𝒑; ∆ 𝒑 = 4 кПа = 4 ∙ 103 Па 𝒑𝟏 - ? Решение: 𝒑𝟏 𝑽𝟏 = 𝒑𝟐 𝑽𝟐; 𝒑𝟏 𝑽𝟏 = (𝒑𝟏 + ∆ 𝒑) 𝑽𝟐 ; 𝒑𝟏 = 𝒑𝟏 = 4 ∙ 103 Па ∙ 6 ∙ 10−3 м3 8 ∙ 10−3 м3 − 6 ∙ 10−3 м3 ∆ 𝒑 𝑽𝟐 𝑽𝟏 − 𝑽𝟐 = 12 ∙ 103 Па = 12 кПа ; 4 Ответ: 12 кПа № 2. Сплывающий со дна озера пузырёк воздуха вблизи поверхности воды имеет диаметр 2 мм. На какой глубине диаметр пузырька был равен 1,5 мм? Изменение температуры с глубиной не учитывать. Дано: D = 2 мм = 2 ∙ 10−3 м; d = 1, 5 мм = 1, 5 ∙ 10−3 м; 𝑝0 = 105 Па; кг м м ρ = 1000 3; g = 9, 8 2 ≈ 10 2 м с с h-? Решение: Воздух в пузырьке изотермически расширяется. Когда пузырёк находился на глубине h, он испытывал давление 𝒑1 = 𝒑𝟎 + ∆𝒑, где ∆𝒑 = ρgh 𝒑𝟏 𝑽𝟏 = 𝒑𝟎 𝑽𝟐; (𝒑𝟎 + ∆𝒑) 𝑽𝟏 = 𝒑𝟎 𝑽𝟐; (𝒑𝟎 + 𝝆𝒈𝒉) 𝑽𝟏 = 𝒑𝟎 𝑽𝟐 ; h= 𝒑𝟎 (𝑫𝟑 − 𝒅𝟑 ) h= 𝝆𝒈𝒅𝟑 ;h= 𝒑𝟎 (𝑽𝟐 − 𝑽𝟏 ) ; 𝝆𝒈 𝑽𝟏 𝟏 𝟏 𝟔 𝟔 𝑽𝟏 = 𝝅𝒅𝟑 ; 𝑽𝟐 = 𝝅𝑫𝟑 ; 105 Па ((2 ∙ 10−3 м)𝟑 − (1,5 ∙ 10−3 м)𝟑 ) кг м 1000 3 ∙ 10 2 ∙ (1,5 ∙ 10−3 м)𝟑 м с = 14 м Ответ: 14 м № 3. Открытую с двух концов стеклянную вертикальную трубку длиной 50 см наполовину опустили в ртуть. Потом трубку закрыли сверху и вынули. Какова длина столбика ртути, оставшегося в трубке. Атмосферное давление 750 мм рт. ст. Дано: L = 50 см = 50∙ 10−2 м; p = 750 мм рт. ст.; ρ = 1360 l-? Решение: кг м3 ; g = 9, 8 м с2 ≈ 10 м с2 5 Температура не изменяется, воздух в трубке расширяется. 𝒑𝟏 𝑽𝟏 = 𝒑𝟐 𝑽𝟐, где начальное давление 𝒑𝟏 равно атмосферному, 𝒑𝟏 = ρ g Н, где Н = 750 мм рт. ст. = 0,75 м; ρ – плотность ртути, начальный объём жидкости 𝑽𝟏 = 𝑳𝑺 𝟐 ; S – площадь поперечного сечения трубки 𝑽𝟐 = (L – l)S конечный объём ртути в трубке 𝒑𝟐 = 𝒑𝟏 - ∆𝒑; ∆𝒑 = ρ g l; 𝒑𝟐 = 𝒑𝟏 - ρ g l = ρ g Н - ρ g l = ρ g (Н - l) ρgH l= l= 𝐿𝑆 2 𝑯+𝑳 𝟐 = ρ g (Н - l) (L – l) S 𝟏 + √𝑯𝟐 + 𝑳𝟐 𝟐 0,75 м + 50∙ 10−2 м 𝟐 𝟏 + √(0,75 м) 𝟐 + (50 ∙ 10−2 м)𝟐 = 0,174 м 𝟐 Ответ: длина столбика ртути 0,174 м 7. О вреде алкоголя Когда было закончено строительство тоннеля под Темзой в Лондоне, Великобритании, городские власти решили отметить это событие в самом туннеле. Но там, к сожалению, шампанское показалось им лишённое обычной игривости. Но когда они поднялись на поверхность, вино забурлило у них в желудках, стало раздувать жилеты и едва не запенилось из ушей. Одного высокопоставленного чиновника пришлось срочно спускать обратно для рекомпрессии. Объяснить явление. Домашнее задание Задания для самостоятельной работы 1. Прочитать: § 6 [1]; § 42, § 21 п. 1 [3] 2. Ответить на вопросы: 6 а) Что называют изопроцессами? б) Какой процесс называют изотермическим? в) Каким законом описывается изотермический процесс? г) Как формулируют и записывают этот закон? д) Почему уменьшение объёма газа приводит к пропорциональному увеличению его давления, если температура остаётся постоянной? Решить качественные задачи: 3. а) Во время надувания щёк и давление, и объём во рту увеличиваются, а температура остаётся неизменной. Не противоречит ли это закону Бойля-Мариотта? б) Бак с жидкостью, над поверхностью которой находится воздух, герметически закрыт. Почему, если открыть кран, находящийся в нижней части бака, после вытекания некоторого количества жидкости дальнейшее её течение прекратиться? Что надо сделать, чтобы обеспечить свободное вытекание жидкости? 4. Решить задачи: № 1. Во сколько раз изменится давление воздуха в цилиндре, если поршень переместить на 𝟏 𝟑 l влево? вправо? № 2. Во время изотермического сжатия объём газа увеличился на 5 л, а давление увеличилось в 3 раза. Каким был начальный объём газа? № 3. Чтобы подводная лодка всплыла, необходимо с помощью сжатого воздуха вытеснить из балластных цистерн 1 т морской воды. С какой наибольшей глубины может всплыть лодка, имея в запасе 6 баллонов сжатого воздуха объёмом по 30 л? Давление сжатого воздуха 7 МПа.