ПРИМЕНЕНИЕ ГИПОХЛОРИТА НАТРИЯ Дезинфекция питьевой воды
реклама
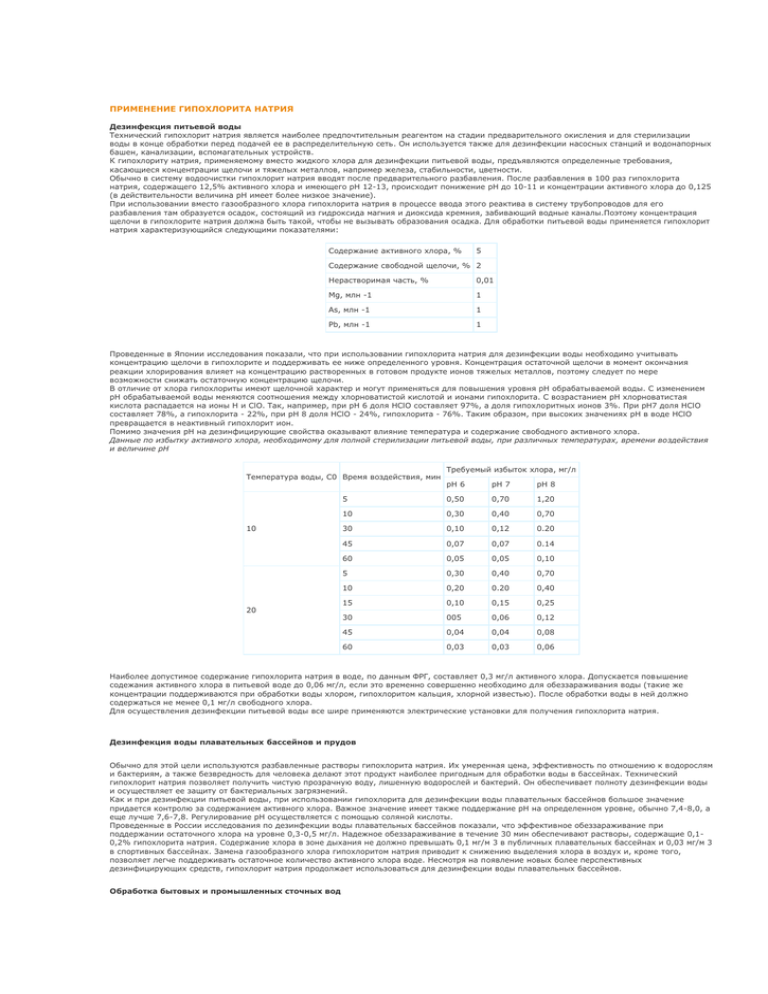
ПРИМЕНЕНИЕ ГИПОХЛОРИТА НАТРИЯ Дезинфекция питьевой воды Технический гипохлорит натрия является наиболее предпочтительным реагентом на стадии предварительного окисления и для стерилизации воды в конце обработки перед подачей ее в распределительную сеть. Он используется также для дезинфекции насосных станций и водонапорных башен, канализации, вспомагательных устройств. К гипохлориту натрия, применяемому вместо жидкого хлора для дезинфекции питьевой воды, предъявляются определенные требования, касающиеся концентрации щелочи и тяжелых металлов, например железа, стабильности, цветности. Обычно в систему водоочистки гипохлорит натрия вводят после предварительного разбавления. После разбавления в 100 раз гипохлорита натрия, содержащего 12,5% активного хлора и имеющего рН 12-13, происходит понижение рН до 10-11 и концентрации активного хлора до 0,125 (в действительности величина рН имеет более низкое значение). При использовании вместо газообразного хлора гипохлорита натрия в процессе ввода этого реактива в систему трубопроводов для его разбавления там образуется осадок, состоящий из гидроксида магния и диоксида кремния, забивающий водные каналы.Поэтому концентрация щелочи в гипохлорите натрия должна быть такой, чтобы не вызывать образования осадка. Для обработки питьевой воды применяется гипохлорит натрия характеризующийся следующими показателями: Содержание активного хлора, % 5 Содержание свободной щелочи, % 2 Нерастворимая часть, % 0,01 Mg, млн -1 1 As, млн -1 1 Pb, млн -1 1 Проведенные в Японии исследования показали, что при использовании гипохлорита натрия для дезинфекции воды необходимо учитывать концентрацию щелочи в гипохлорите и поддерживать ее ниже определенного уровня. Концентрация остаточной щелочи в момент окончания реакции хлорирования влияет на концентрацию растворенных в готовом продукте ионов тяжелых металлов, поэтому следует по мере возможности снижать остаточную концентрацию щелочи. В отличие от хлора гипохлориты имеют щелочной характер и могут применяться для повышения уровня рН обрабатываемой воды. С изменением рН обрабатываемой воды меняются соотношения между хлорноватистой кислотой и ионами гипохлорита. С возрастанием рН хлорноватистая кислота распадается на ионы Н и ClO. Так, например, при рН 6 доля HСlO составляет 97%, а доля гипохлоритных ионов 3%. При рН7 доля HСlO составляет 78%, а гипохлорита - 22%, при рН 8 доля HСlO - 24%, гипохлорита - 76%. Таким образом, при высоких значениях рН в воде HСlO превращается в неактивный гипохлорит ион. Помимо значения рН на дезинфицирующие свойства оказывают влияние температура и содержание свободного активного хлора. Данные по избытку активного хлора, необходимому для полной стерилизации питьевой воды, при различных температурах, времени воздействия и величине рН Температура воды, С0 Время воздействия, мин 10 20 Требуемый избыток хлора, мг/л pН 6 рН 7 рН 8 5 0,50 0,70 1,20 10 0,30 0,40 0,70 30 0,10 0,12 0.20 45 0,07 0,07 0.14 60 0,05 0,05 0,10 5 0,30 0,40 0,70 10 0,20 0.20 0,40 15 0,10 0,15 0,25 30 005 0,06 0,12 45 0,04 0,04 0,08 60 0,03 0,03 0,06 Наиболее допустимое содержание гипохлорита натрия в воде, по данным ФРГ, составляет 0,3 мг/л активного хлора. Допускается повышение содежания активного хлора в питьевой воде до 0,06 мг/л, если это временно совершенно необходимо для обеззараживания воды (такие же концентрации поддерживаются при обработки воды хлором, гипохлоритом кальция, хлорной известью). После обработки воды в ней должно содержаться не менее 0,1 мг/л свободного хлора. Для осуществления дезинфекции питьевой воды все шире применяются электрические установки для получения гипохлорита натрия. Дезинфекция воды плавательных бассейнов и прудов Обычно для этой цели используются разбавленные растворы гипохлорита натрия. Их умеренная цена, эффективность по отношению к водорослям и бактериям, а также безвредность для человека делают этот продукт наиболее пригодным для обработки воды в бассейнах. Технический гипохлорит натрия позволяет получить чистую прозрачную воду, лишенную водорослей и бактерий. Он обеспечивает полноту дезинфекции воды и осуществляет ее защиту от бактериальных загрязнений. Как и при дезинфекции питьевой воды, при использовании гипохлорита для дезинфекции воды плавательных бассейнов большое значение придается контролю за содержанием активного хлора. Важное значение имеет также поддержание рН на определенном уровне, обычно 7,4-8,0, а еще лучше 7,6-7,8. Регулирование рН осуществляется с помощью соляной кислоты. Проведенные в России исследования по дезинфекции воды плавательных бассейнов показали, что эффективное обеззараживание при поддержании остаточного хлора на уровне 0,3-0,5 мг/л. Надежное обеззараживание в течение 30 мин обеспечивают растворы, содержащие 0,10,2% гипохлорита натрия. Содержание хлора в зоне дыхания не должно превышать 0,1 мг/м 3 в публичных плавательных бассейнах и 0,03 мг/м 3 в спортивных бассейнах. Замена газообразного хлора гипохлоритом натрия приводит к снижению выделения хлора в воздух и, кроме того, позволяет легче поддерживать остаточное количество активного хлора воде. Несмотря на появление новых более перспективных дезинфицирующих средств, гипохлорит натрия продолжает использоваться для дезинфекции воды плавательных бассейнов. Обработка бытовых и промышленных сточных вод Гипохлорит натрия применяется для обработки бытовых и промышленных вод, для разрушения животных и растительных микроорганизмов, устранения запахов (особенно образующихся из серосодержащих веществ), обезвреживания промышленных стоков, например, от цианистых соединений. Он может быть использован для обработки воды, содержащей аммоний. Процесс осуществляют при температуре выше 70 0 С в щелочной среде с добавлением CaCl2 или СаСО3 для разложения соединений аммиака. Для очистки от фенолов (содержание 0,42-14,94 мг/л) используют 9% раствор гипохлорита натрия в количестве 0,2-8,6 мг/л. Степень очистки достигает 99,99%. При обработке гипохлоритом воды, содержащей фенолы, происходит образование фенолоксифенолов. В ходе обработки вод, содержащих гуминовые вещества, последние превращаются в хлороформы, дихлоруксусную кислоту, трихлоруксусную кислоту, хлоральдегиды и некоторые другие вещества, концентрация которых в воде значительно ниже. Известны данные об использовании гипохлорита натрия для удаления ртути из сточных вод. Использование гипохлорита натрия в пищевой промышленности В начале восьмидесятых годов институт биологии и ее применения к проблемам питания в Дижоне (Франция) провел изучение дезинфицирующих средств, используемых в пищевой промышленности. Гипохлорит натрия был оценен среди этих продуктов по первому классу как наиболее пригодный для этих целей и наиболее экономичный. Он показал высокую эффективность в отношении почти всех растительных клеток, спор и бактерий. По этой причине гипохлорит натрия находит широкое применение в пищевой промышленности для дезинфекции с целью уничтожения ракообразных и моллюсков; для различных промывок; для борьбы против бактериофагов в сыроваренной промышленности; для дезинфекции резервуаров, загонов для скота. Гипохлорит натрия относится к числу средств используемых в пивоваренной промышленности. Обычно применяют раствор, содержащий 30-40 мг/л активного хлора. Гипохлорит натрия является отличным антимикробным агентом. В частности в США его применяют для обработки зерна. Использование гипохлорита натрия в молочной промышленности На предприятиях молочной промышленности основное назначение дезинфицирующих мероприятий - предупреждение микробного инфицирования молочных продуктов. Гипохлорит натрия является достаточно эффективным средством, используемым для этой цели. В России применяют для этих целей гипохлорит натрия марки А. Он содержит 170 г/л активного хлора и 40-60 г/л щелочи. Бактерицидное действие гипохлорита натрия проявляется при 20-25 0 С и экспозиции 3-5 минут.Для снижения корозирующего действия гипохлорита был предложен препарат ГИПОХЛОР. Его получают смешением гипохлорита натрия, каустической соды и метасиликата натрия. Коррозирующее действие этого препарата на металлические поверхности в 10-15 раз меньше, чем обычного гипохлорита натрия. В молочной промышленности традиционные средства дезинфекции начинают вытесняться новыми препаратами, обладающими одновременно и моющими и дезинфицирующими свойствами. Наиболее перспективными из них являются натриевая и калиевая соли трихлоризоциануровой кислоты. Использование гипохлорита в рыбоводстве Гипохлорит натрия в виде разбавленных растворов уничтожает все виды патогенных агентов и используется для дезинфекции водоемов с твердым дном и берегами. Кроме того он используется при дезинфекции рыболовных сетей, сачков и баков из пластика для хранения рыбы. Использование гипохлорита в здравоохранении В комплексе профилактических мероприятий, направленных на ограничение больничных инфекции, важную роль играет дезинфекция. Для этой цели может быть использован гипохлорит натрия. В частности, в ПНР для этих целей используют гипохлорит натрия производства Тарновского азотного предприятия, с содержанием активного хлора не менее 55. Гипохлорит натрия оказывает дезинфицирующее действие на граммположительные и грамм-отрицательные бактерии, туберкулезные палочки, споры бактерий, болезнетворные грибки и вирусы. Имеются сведения (Россия) использования растворов гипохлорита натрия (0,03-0,05%) для лечения гнойных абцессов, гнойных гайморитов, розовых угрей и трофических язв как наружное средство и средство для инъекций. Другие области применения Гипохлорит входит в составы синтетических моющих средств, используемых в бытовой химии, в составы дезинфицирующей пасты с отбеливающим эффектом, дезинфицирующих средств с окислительными, хлорирующими и бактерицидными свойствами. В настоящее время за рубежом и в России наметилась тенденция развития использования гипохлорита натрия для дезинфекции небольших объемов воды с применением электролитического метода его получения. Этот метод находит все большую популярность во всем мире. Хотя гипохлорит натрия продолжает использоваться в пищевой, молочной промышленности, но он все более вытесняется другими видами средств, обладающими сочетанием моющих и дезинфицирующих свойств. Все чаще его вводят в составы таких средств. Количественная оценка эффективности химических бактерицидов и их квалификация Здесь использованы следующие количественные показатели: 1. Относительная гермицидная активность препарата по сравнению с эталоном (за эталон брали активность хлорамина) А = С1 / С0 где С1 - концентрация препарата, вызывающая 100% гибель микроорганизмов за определенное время (как правило - 5, 15 и 30 мин); С0 - концентрация хлорамина вызывающая 100% гибель тех же организмов за тот же период времени. В таблице 1 представлена относительная активность некоторых препаратов. № Химическая группа препарата Действующее начало, % РекоменНазначение Относительдуемые (спектр антимик- ная дезинфициконцентрации % робного действия) рующая активность по препарату 1. ХЛОРАКТИВ НЫЕ СОЕДИНЕНИЯ Активный хлор 1. Хлорамин 26-28 0,05-5,0 Бактерии, вирусы, 1,0 грибы 2. Хлорная известь 26-35 0,2-10,0 Бактерии, вирусы, 0,5 грибы, споры 3. Нейтральный гипохлорит кальция 50-60 0,15-0,9 Бактерии, вирусы, 5,5 грибы, споры 4. Гипохлорит кальция технический 30-40 0,1-7,0 Бактерии, вирусы, 0,7 грибы, споры 17 1,0 Бактерии, вирусы, 50,0 грибы 0,5-0,9 0,125-0,5 Бактерии, вирусы, 10,0 грибы Na (K) соль 7. дихлоризоциануровой кислоты 52 0,1-0,3 Бактерии, вирусы, 16,6 грибы 8. Хлорцин 11-15 0,5-1,0 Бактерии, вирусы 5,0 9. Препарат ДП-2 40 0,1-0,5 Бактерии, вирусы, 10,0 грибы, споры 10. Сульфохлора тин 15,6 0.1-2,5 Бактерии, вирусы 2,0 2. ПЕРЕКИСНЫЕ СОЕДИНЕНИЯ Перекись водорода 11. Пергидроль 30 2,0-6,0 Бактерии, вирусы, 0,8 споры 12. Грилен 20 0,25-6,0 Бактерии, вирусы, 0,8 грибы, споры 13. Дезоксон Надуксусная кислота 1,0-2,0 Бактерии, вирусы 2,5 14. Амфолан Смесь хлоргидратов 0,5-2,0 полиаминов 30,0 Бактерии 2,5 15. Ниртан Алкилтриметил аммоний хлорид С14-С16 1,5-3,0 Бактерии 1,7 16. Гибитан Поли гексаметилен гуадин глюконат 20,0 2,5 Бактерии 10,0 17. Полисепт Поли гексаметилен гуанидин гидрохлорид 20,0 1,0 Бактерии 5,0 Гипохлорит натрия, 5. получаемый химическим путем 6. Гипохлорит натрия, получаемый электрохимическим путем 3. ПАВ 4. ПРОЧИЕ 2. Коэффициент различия (К0) - величина отражающая спектральную активность препарата, его универсальность или специфичность. Активность каждого из препаратов исследовали по отношению к 6-ти видам тест-микроорганизмов, которые моделируют возбудителей соответственно кишечных инфекций бактериальной этимологии (E Coli),капельных инфекций бактериальной этимологии (Saureus), респираторных вирусных инфекций (вир. гриппа), энтеровирусных инфекций (вир. Полиомиелита), дерматомикозов (Candida albicans), а также по отношению к споровозбудителям (Bac. cereus). Коэффициент различия (К) исчисляли как отношение максимальной концентрации и минимальной концентрации, вызывающей гибель одного из видов микроорганизмов, представленых в спектре. При этом "К1" включает неспорообразующие микроорганизмы, а "К2" - весь спектр. Приведенные данные позволяют выбрать тип дезинфектанта, время контакта, необходимую концентрацию для дезинфекции данного объекта. Аналоги гипохлорита натрия Среди аналоговгипохлорита натрия первое место по масштабам применения занимают другие хлорактивные соединения. Среди них гипохлорит кальция. Твердый гипохлорит кальция выпускается в виде порошка, таблеток и гранул. Препараты гипохлорита кальция отличаются высоким содержанием активного хлора, хорошей стабильностью, высокой растворимостью в воде и малой гигроскопичностью. Производство продукта в гранулированном виде способствует широкому применению продукта для дезинфекции посуды и оборудования в пищевой промышленности, в прачечной, в бытовой химии. Следующим аналогом является хлорная известь. В настоящее время хлорная известь потеряла свое значение одного из основных средств дезинфекции. Это произошло вследствие развития электролитических методов получения хлора и гипохлорита. А также производства гипохлорита кальция с повышенным по сравнению с хлорной известью содержанием хлора. В качестве одного из аналогов гипохлорита используется диоксид хлора. В литературе практически не приводятся данные по производству и потреблению диоксида хлора. Это происходит вследствии того, что диоксид хлора должен обязательно получаться на месте потребления. Диоксид хлора хорошо растворяется в воде не реагируя с ней при этом. Диоксид хлора имеет более сильное дезинфицирующее воздействие, чем хлор. Является сильным бактерицидом, спорицидом и вирицидом. Прекрасно уничтожает запахи и привкусы. Не взаимодействует с аммиаком. Дезинфицирующая способность не зависит от рН. Не требует специальных хранилищ. Сохраняет высокое остаточное содержание в воде. Говоря об аналогах гиппохлорита натрия следует упомянуть о других дезинфектантах, применяемых для обработки питьевой воды. Это: Перманганат калия. Удобен для дезинфекции трубопроводов, так как не требует специального сложного оборудования. Не дает побочных эффектов, но редко применяется самостоятельно. Йод. Не взаимодействует с аммиаком или аналогичными веществами. Однако его высокая стоимость, ограниченность наличия, технологические трудности затрудняют его широкое применение. Хлорид брома. Близок по своим дезинфицирующим свойствам к хлору, однако образует токсичные бромированные соединения. Серебро. Требуется очень небольшое количество для уничтожения большинства организмов. Не придает воде вкуса, для человека не токсичен, в работе полностью безопасен. Применяется ограниченно из-за высокой стоимости. Указанные выше дезинфектанты не всегда позволяют достичь нужных результатов, поскольку существует целый ряд микроорганизмов, стойких к указанным средствам дезинфекции. Поэтому в ряде областей, в частности в медицине, в сельском хозяйстве, в различных отраслях пищевой промышленности, в текстильной, а также при дезинфекции воды, применяются различные органические дезинфицирующие средства, отличающиеся высокой биоцидной активностью, стабильностью, более низкой токсичностью и не образующие при биоразложении токсичных продуктов. Действие органических дезинфектантов основано на их окислительной способности. К дезинфицирующим средствам относятся прежде всего: фенольные соединения; альдегиды, кислоты, спирты; хлоризоцианураты; хлорциануровые кислоты. Фенольные соединения применяются в основном в медицине в качестве дезинфектантов. Среди фенольных соединений можно назвать такие, как алкилфенолы, галоидфенолы, бифенолы, алкилбензилгалогенофенолы, бензилфенолы и др. Для указанных целей, а также в рыбной промышленности для дезинфекции средств ухода за рыбой порименяют различные альдегиды: формальдегид, глутароальдегид, адинальдегид, оксальдегид, малональдегид, муравьиный альдегид. Их используютсамостоятельно или в смеси со спиртами. Альдегиды как дезинфектанты отличаются от фенольных соединений тем, что они не дают запаха, безвредны для кожи, не активны по отношению к конструкционным материалам. Разрушение микроорганизмов является одним из основных свойств, присущих большинству кислот. Некоторые из них рассматриваются как антисептики, дезинфектанты и антибиотики. К ним можно отнести такие кислоты, как соляная, уксусная, надуксусная, трихлоруксусная, фосфоноуксусная, борная, лимонная, надмуравьиная, основной областью применения которых является медицина. В больницах для дезинфекции воздуха помещений, инструментов, влажной уборки поверхностей, а также в молочной промышленности широко применяют такие спирты, как метанол, этанол, пропанол, изопропанол, йодистый спирт и др., обладающие высоким бактерицидным, антисептическим свойствами при минимальном времени контакта. Для дезинфекции воды в плавательных бассейнах и водоемах, чистки туалетов, а также для дезинфекции в молочной промышленности широкое применение нашли хлоризоцианураты, а также моно-, ди-, трихлоризоциануровая кислоты. Так в США для дезинфекции воды в плавательных бассейнах, где ранее применяли только гипохлориты, в настоящее время доля хлоризоциануратов составляет 40-46% от общего количества дезинфицирующих средств, используемых в этой области. Для дезинфекции воды предложены различные композиции на основе хлоризоциануратов или хлоризоциануровых кислот. Например для дезинфекции воды предложены композиции, , состоящие из трихлорциануровой кислоты, бикарбоната щелочного металла и воды или дихлоризоцианурата, талька кислоты и воды. Для чистки туалетов предложена композиция, состоящая из ди- или трихлорциануровой кислоты или хлоризоциануратов и хлорида и сульфата натрия. Для очистки опорожненых водоемов с влажным дном и берегами предлагается использовать цианамид кальция. Очень часто в сельском хозяйстве, в различных отраслях пищевой промышленности, в медицине процессы дезинфекции сопровождают процессы мойки и чистки. Поэтому в настоящее время наблюдается тенденция использования препаратов, обладающих одновременно моющими и дезинфицирующими свойствами. Уже в течение многих лет такие препараты поставляют фирмы США, Японии и Западной Европы. Эти препараты обладают высокими моющими и биоцидными свойствами; адгезионными показателями, устойчивостью в жесткой воде, хорошо растворяются в воде. Они обладают высокой стабильностью в течение не менее одного года, хорошими свойствами в период биоразложения. Они не токсичны для людей и животных, не оказывают раздражающего действия на нашу слизистую оболочку, не вызывают коррозии металлических поверхностей различных емкостей и аппаратуры. К моюще-дезинфицирующим веществам можно отнести четвертичные аммониевые и пиридиновые соединения, различные поверхностно активные вещества (ПАВ), органические хлорамины, йодоформы или композиции на их основе. Самое широкое применение из них находят четвертичные аммониевые соединения или композиции на их основе. В различных отраслях пищевой промышленности и в медицине применяются следующие моюще-дезинфицирующие средства на основе четвертичныхаммониевых и пиридиновых соединений: хлорид диизобутилфеноксиэтоксиэтилдиметиллауриламмония или бензоиламмония; хлорид или бромид лаурилметилбензиламмония; хлорид или бромид метилпиридина; сульфат лаурилпиридина; хлорид или бромид лаурилпиридина. В медицине и в пищевой промышленности, особенно в консервной, применяют соединения гидатоина, такие, как хлориды или бромиды.N,N диметил - N- додециламмония; N, - диметил - N - бензиламмония; N,N - диметил - N - этилдодециламмония и др. Для дезинфекции и мойки оборудования и трубопроводов при производстве пищевых продуктов и напитков нашли применение такие четвертичные аммониевые основания, как диоктилдиметиламмониевые или додецилдиметиламониевые. В качестве моюще-дезинфицирующих средств применяют некоторые катионные и амфотерные ПАВ. Однако амфотерные ПАВ очень дорогостоящи и характеризуются низкой антибиологической активностью. Их целесообразно применять в тех случаях, когда нельзя использоватьсильнокислые и щелочные моюще-дезинфицирующие растворы. Органические хлорамины используют как и отбеливающее средство или в качестве компонентов различных композиций. Хлорамины не так быстро выделяют хлор, как гипохлорид кальция, вследствие они более эффективны в течение длительного времени. Коррозионная активность их значительно ниже, чем гипохлорита. С экономической точки зрения они менее выгодны, чем гипохлорит, поскольку они дороже. Для дезинфекции питьевой воды используют такие хлорамины, как п-толуоулсульфохлорамин; бензосульфохлорамин. А также 3 - хлор 4,4 -диметил 2 оксамедион. Он стабильнее в водном растворе, чем дихлорантин и гипохлорит натрия, и требует более длительного времени контакта. Среди комплексных органических соединений йода наибольшее практическое применение нашли его соединения с ПАВ, получившие название йодофоров, которые достаточно широко применяют в сельском хозяйстве. Йодофоры очень эффективны в борьбе с болезнетворными бактериями, вирусами, спорами, грибками, дрожжами и др. В последние годы в России разработан и изучен ряд новых дезинфицирующих средств на основе хлорактивных соединений и ПАВ, обладающие полифункциональными свойствами, хлорцин, дезам, ДП - 2, дезбел характеризуются дезинфицирующим и моющим действием; бентахлор, гексахлор и хлорцин наряду с этими свойствами обладают чистящим действием. Преимуществом средств на основе ПАВ - нитрана и амфоланана - является отсутствие коррозирующего действия. Разрешены промышленный выпуск и применение хлорцина, дезама, ДП-2, бентахлора, гексахлора, дезбела, аморолана и ниртана. Приведенный анализ дезинфектантов был бы не полным если мы не коснулись перекиси водорода и ее производных. Недостаток перекиси водорода - быстрая разлагаемость в присутствии белка и крови. Этих недостатков лишены ее производные - надкислоты, которые являются эффективными спорцидами. Однако коррозионная активность этих материалов сдерживает широту их использования. Перекись водорода в сочетании с катамином АБ (созданный на базе поличетвертичного аммония) позволила получить препарат, по своей активности превышающий отдельно взятые перекись водорода и катамин АБ. Произошло это за счет способности катамина АБ нарушать проницаемость мембраны клеток и тем самым потенцировать дезинфекционную активность перекиси водорода. Спектральная активность дезинфицирующих средств № Химическая группа, препарат Кишечные инфекции бакт. этиологии Капельные РеспираЭнтероСпорообра- К1 инфекции торные Дерматовирусные зующие бакт. вирусные микозы инфекции возбудители этиологии инфекции К2 1. ХЛОР АКТИВНЫЕ СОЕДИНЕНИЯ 1. Хлорная известь 0,2-1,0 0,2-10,0 0,5 1,0-3,0 10,0 10,0-20,0 10 / 0,2 = 50 20 / 0,2 = 100 2. Нейтральный гипохлорит кальция 0,5-0,6 0,15-0,5 0,15-0,3 0,6-0,9 0,3 1,0-7,5 0,9 / 0,15 = 6 7,5 / 0,15 = 50 3. Гипохлорит кальция технический 0,1-7,0 0,1-7,0 0,5 1,0-7,0 1,5 3,5-8,0 7,0 / 0,1 = 70 8,0 / 0,1 = 804. Гипохлорит натрия, получаемый электрическим 0,125-0,25 0,125-0,5 0,125-0,25 0,5 0,3-0,5 не активен 0,5 / 0,125 = 4 ----- 5. Хлорамин 0,05-3,0 0,005-5,0 0,5 1,0-3,0 5,0 не активен 5 / 0,05 = 100 ----- Na (K) соль 6. дихлоризоциануровой кислоты 0,1-0,2 0,1-0,5 0,1 0,1-0,3 0,5 2-5,0 0,5 / 0,1 = 5 5 / 0,1 = 50 7. Хлорцин 0,5-2,0 0,5-2,0 1,0 2,0-5,0 2,0-5,0 7,5 5 / 0,5 = 10 7,5 / 0,5 = 15 8. Препарат ДП-2 0,1-0,2 0,1-1,0 0,5 0,1-0,5 0,3-0,5 3,0-7,5 1 / 0,1 = 10 7,5 / 0,1 = 75 9. Сульфохлорантин 0,1-0,2 0,1-2,5 0,1 0,1-0,2 1,0 не активен 2,5 / 0,1 = 25 ----- 10. Пергидроль (Перекись водорода) 3,0 3,0 2,0 3,0-4,0 2,0-4,0 3,0-6,0 4,0 / 2,0 = 2 6,0 / 2,0 =3 11. Дезоксон (надуксусная кислота) 1,0-2,0 1,0-2,0 2,0 1,0-2,0 1,0-2,0 20,0 2,0 / 1,0 = 2 20,0 / 1,0 = 20 12. Грилен (Н2О + ЧАС) 0,25-2,5 1,0-2,0 2,0-3,0 1,0 3,0-6,0 3,0 / 0,25 = 12 6,0 / 0,25 = 24 2. ПЕРЕКИСНЫЕ СОЕДИНЕНИЯ 0,25-2,5 3. ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА 13. Амфолан 0,5-2,0 0,5-2,0 не активен 2,0 / 0,5 = 4 ----- 14. Ниртан 1,5-3,0 1,5-3,0 не активен 3,0 / 1,5 = 2 ----- 15. Гибитан 0,5 0,5 не активен 0,5 / 0,5 = 1 ----- 16. Полисепт 1,0 1,0 не активен 1,0 / 1,0 = 1 ----- 4. ПРОЧИЕ Дезинфекционные свойства хлора и гипохлорита натрия При растворении хлора в воде идут две параллельные реакции: Cl2 + H2O = H+ + Cl- + HСlO HСlO = H- + ClOДезинфектантами в данном случае являются хлор и хлорноватистая кислота. При увеличении рН 6 увеличивается концентрация ионов ClO, которые не имеют дезинфекционной способности и, соответственно уменьшаются бактерицидные свойства раствора. В случае гипохлорита натрия идут следующие реакции: NaClO + H2O = NaOH + HСlO Дезинфектантом в данном случае является только хлорноватистая кислота. При разборе микробиологического механизма дезинфекции, обращают на себя внимание следующие два сообщения: 1. 2. Отмечено образование ассоциатов микроорганизмов, в которые проникновение хлора затруднено, вследствие чего дезинфекция как процесс, увеличивается во времени. При взаимодействии гипохлорита натрия с Ecoli 1257 (палочка Кока) и streptococcus feссalis, добавочное действие электрического поля и УФ излучения позволяет увеличить дезинфицирующий эффект в 100 и даже 1000 раз. Предполагают, что при воздействии указанных физических агентов происходит изменение цитоплазматической мембраны, что делает клетку более уязвимой. Оставл сделанные выводы в компетенции авторов статей, следует отметить, что разрушение микроорганизмов происходит при их непосредственном контакте с дезинфектантами, такими как Cl2 и HСlO и начинается с разрушения цитоплазматической мембраны, окружающей клетку. Аналоги гипохлорита кальция Аналогами гипохлорита кальция, способными образовывать устойчивые соединения в сухом состоянии являются: гипохлорит натрия, гипохлорит Li (LiClO) и хлорная известь. KClO существует только в растворах. Гипохлориты других щелочных металлов не образуют стойких солей и не имеют практического применения. Сравнительное исследование хлора и гипохлорита натрия как окислителей и дезинфектантов при подготовке питьевой воды. Использование жидкого хлора не обеспечивает достаточную безопасность и культуру производства.В процессе хлорирования образуются токсичные, канцерогенные и мутагенные летучие галогеносодержащие соединения. В качестве альтернативы жидкому хлору был использован гипохлорит натрия. Исследование производилось на р.Томь. Технический гипохлорит натрия (ТУ 6-01-29-93) изготавливался на производственном объединении "Химпром" г Кемерово. Гипохлорит натрия содержал 120-160 г/дм 3 активного хлора и 40-90 г/дм 3 щелочи. В течение года проводили гигиенические исследования. По бактерицидному эффекту гипохлорит натрия не уступает жидкому хлору. Содержание в воде хлороформа, тетрахлорметана и бромдихлорметана снизилось по сравнению с использованием жидкого хлора на 15, 14 и 12% соответственно. Токсичность воды с учетом содержания всех примесей и их совместного токсического действия уменьшалась на 10-13% в зависимости от сезона. Замена жидкого хлора гипохлоритом целесообразна при условии равноценных результатов обработки воды (эффективность коагуляции, показатели качества питьевой воды) а также с учетом последствий хлорирования для механизмов и конструкций. После проведения соответствующих исследований доказано, что при любом содержании твердой фазы в природной воде коагуляция как для хлора так и для гипохлорита происходит идентично. При использовании жидкого хлора скорость коррозии в 4-20 раз выше, чем при использовании гипохлорита. Использование оного позволяет продлить срок использования трубопроводов сверхнормативный в 2-6 раза. Анализ полученных данных показал, что тип дезинфектанта практически не влияет на нормируемые ГОСТ 287-89. Концентрация галогенносодержащих соединений снижена (в зависимости от сезона) на 15-36,5% при использовании в качестве дезинфектанта гипохлорита натрия. РАСТВОРЫ ГИПОХЛОРИТА НАТРИЯ: основные свойства и использование при обработке воды Гипохлорит натрия - NaClO, получают хлорированием водного раствора сухого натра (NaOH) или электроидом раствора сухого натрия (NaCl). Молекулярная масса NaClO (по международным атомным массам 1971 г.) - 74,44. Промышленностью выпускается в виде водных растворов различной концентрации. Водные растворы гипохлорита натрия (ГХН) стали использоваться для дезинфекции с самого зарождения хлорной промышленности. Благодаря высокой антибактериальной активности и широкому спектру действия на различные микроорганизмы, это дезинфицирующее средство находит применение во многих направлениях человеческой деятельности, в том числе и при обработке воды. Дезинфицирующее действие ГХН основано на том, что при растворении в воде он точно так же, как хлор при растворении в воде, образует хлорноватистую кислоту, которая оказывает непосредственное окисляющее и дезинфицирующее действие. NaClO+H2O-NaOH+HСlO Реакция является равновесной, и образование хлорноватистой кислоты зависит от величины рН и температуры воды. В РФ состав и свойства ГХН, выпускаемого промышленностью, или получаемого непосредственно у потребителя в электрохимических установках, должен соответствовать требованиям, предъявляемым в (3,4). Основные характеристики растворов ГХН, регламентируемые этими документами, приведены в таб.1. Таблица 1. Основные физико-химические показатели растворов гипохлорита натрия, выпускаемых в РФ (3, 4) Норма для марок Наименование показателя По (3) Марка А По (4) Марка Б Марка А Марка Б Марка В Марка Г Марка Э 1.Внешний вид Жидкость Жидкость зеленовато-желтого зеленовато-желтого цвета цвета Бесцветная жидкость 2.Коэффициент светопропускания, %, не менее 20 20 Не регламентируется Не регламентируется 3.Массовая концентрация активного хлора, г/дм3, не менее 190 170 120 120 190 120 7 4.Массовая концентрация щелочи в пересчете на NaOH, 10-20 г/дм3 40-60 40 90 10-20 20-40 1 5.Массовая концентрация железа, г/дм3, не более 0,06 Не регламентируется 0,02 Не регламентируется Примечания: 1. 2. Для растворов по (3) допускается потеря активного хлора по истечении 10 суток со дня отгрузки не более 30% первоначального содержания и изменение окраски до красновато-коричневого цвета. Для растворов по (4) допускается потеря активного хлора по истечении 10 суток со дня отгрузки для марок А и Б не более 30% первоначального содержания, для марок В и Г - не более 20%, для Марки Э - не более 15%. В соответствии с (3-5) растворы гипохлорита натрия различных марок применяют: раствор марки А по (3) - в химической промышленности, для обеззараживания питьевой воды и воды плавательных бассейнов, для дезинфекции и отбелки; раствор марки Б по (3) - в витаминной промышленности, как окислитель для отбеливания ткани; раствор марки А по (4) - для обеззараживания природных и сточных вод в хозяйственно-питьевом водоснабжении, дезинфекции воды рыбохозяйственных водоемов, дезинфекции в пищевой промышленности, получения отбеливающих средств; раствор марки Б по (4) - для дезинфекции территорий, загрязненных фекальными сбросами, пищевыми и бытовыми отходами; обеззараживании сточных вод; раствор марки В, Г по (4) - для дезинфекции воды рыбохозяйственных водоемов; раствор марки Э по (4) - для дезинфекции аналогично марка А по (4), а также дезинфекции в медико-санитарных учреждениях, предприятиях общественного питания, объектах ГО и др., а также обеззараживание питьевой воды, стоков и отбеливания. Необходимо отметить, что для изготовления растворов гипохлорита натрия марок АБ по (3) и растворов марки А по (4) не допускается применение абгазного хлора от хлорпотребляющих органических и неорганических производств, а также едкого натра, полученного ртутными методами. Растворы марки Б по (4) получают из абгазного хлора стадии снижения производства хлора органических и неорганических производств и диафрагменного или ртутного едкого натра. Растворы марок В и Г по (4) получают из абгазного хлора стадии снижения производства хлора и диафрагменного едкого натра с добавлением стабилизирующей добавки - цитраля сорта "Парфюмерный" по (6). Растворы марки Э по (4) получают электролизом раствора поваренной соли. Требования безопасности и охраны окружающей среды при работе с растворами гипохлорита натрия Растворы гипохлорита натрия по (3) и марок А, Б, В, и Т по (4) являются сильными окислителями, при попадании на кожу могут вызвать ожоги, а при попадании в глаза - слепоту. Раствор гипохлорита натрия марки Э по (4) оказывает умеренно раздражающее действие на кожные покровы и слизистые оболочки. Кумулятивными,. кожно-резорбтивными свойствами и сенсибилизирующим действием не обладает; по уровню токсичности этот раствор относится к малоопасным веществам 4го класса опасности по (7). При нагревании выше 35оС гипохлорит натрия разлагается с образованием хлоратов и выделением хлора и кислорода. ПДК хлора в воздухе рабочей зоны 1 мг/м3 ; в воздухе населенных мест 0,1 мг/м3 максимальная разовая и 0,03 мг/м3 среднесуточная (7). Гипохлорит натрия негорюч и невзрывоопасен. Однако гипохлорит натрия по (3) и марок А, Б, В, и Г по (4) в контакте с органическими горючими веществами (опилки, ветошь и др.) в процессе высыхания может вызвать их самовозгорание. При попадании на окрашенные предметы гипохлорит натрия всех марок может вызвать их обесцвечивание. Помещение для производства и применения гипохлорита натрия по (3) и марок А, Б, В и Г по (4) должны быть оборудованы принудительной приточно-вытяжной вентиляцией. Оборудование должно быть герметичным. Индивидуальная защита персонала должна осуществляться с применением специальной одежды в соответствии с (8) и индивидуальных средств защиты: противогазов марки Б или БКФ по (9), перчаток резиновых и очков защитных по (10). При попадании раствора гипохлорита натрия на кожные покровы необходимо обмыть их обильной струей воды в течение 10-12 мин., при попадании брызг продукта в глаза следует немедленно промыть их обильным количеством воды и направить пострадавшего к врачу. Разлитый продукт по (3) и марок А, Б, В, и Г по (4) необходимо смыть большим количеством воды. При проливе гипохлорита натрия марки Э (4) необходимо собрать его при помощи тряпки или смыть водой и протереть. Ткань промыть водой. Сточные воды, содержащие гипохлорит натрия, должны направляться на станцию нейтрализации. Гипохлорит натрия в полиэтиленовых и стеклянных емкостях должен храниться в неотапливаемых вентилируемых складских помещениях. Гипохлорит натрия не допускается хранить с органическими продуктами, горючими материалами и кислотами. Использование растворов гипохлорита натрия при обработке воды Многолетн практика использования растворов гипохлорита натрия для обработки воды, как в нашей стране, так и за рубежом показывает, что эти реагенты могут использоваться в широком диапазоне: Для обработки природных и сточных вод в системе хозяйственно-питьевого водоснабжения, для дезинфекции воды в плавательных бассейнах и водоемах различного назначения, при обработке бытовых и промышленных сточных вод и др. В связи с тем, что этой проблеме посвящены многие тома публикаций, ниже рассматриваются сведения, приведенные в обзорных материалах (1, 11, 12). Использованиерастворов ГХН для обработки питьевой воды Использование растворов гипохлорита натрия предпочтительно на стадии предварительного окисления и для стерилизации воды перед подачей ее в распределительную сеть. Обычно в систему водоочистки растворы ГХН вводят после разбавления примерно в 100 раз. При этом, помимо снижения концентрации активного хлора, снижается также величина рН (с 12-13 до 10-11), что способствует повышению дезинфицирующей способности раствора. Помимо значения рН на дезинфицирующие свойства раствора оказывают температура и содержание свободного активного хлора. В табл. 2 приведены данные по избытку свободного активного хлора, необходимому для полной стерилизации при различных температурах, времени воздействия и величине рН питьевой воды. При обработке питьевой воды остаточное содержание активного хлора допускается в пределах 0,3-0,5 мг/дм 3 . При этом доза активного хлора, вносимая в воду, может быть значительно выше и зависит от хлорпоглощаемости воды (табл. 3). Таблица 2. Данные по избытку активного хлора, необходимые для полной стерилизации питьевой воды, при различных температурных, времени воздействия и величине рН (1) Требуемый избыток Температура Время воздействия, хлора, мг/дм 3 воды, оС мин. 10 20 РН 6 рН 7 рН 8 5 0,50 0,70 0,120 10 0,30 0,40 0,70 30 0,10 0,12 0,20 45 0,07 0,07 0,14 60 0,05 0,05 0,10 5 0,30 0,40 0,70 10 0,20 0,20 0,40 15 0,10 0,15 0,25 30 0,05 0,06 0,12 45 0,04 0,04 0,08 60 0,03 0,03 0,06 Таблица 3. Некоторые данные об использовании гипохлорита натрия при обработке воды (11) Технологический процесс Величина активного хлора, Регистрируемое остаточное вносимого в воду, содержание активного хлора, мг/дм 3 мг/дм 3 1 2 3 1.Обеззараживание питьевой воды и очистка промышленных стоков 1.1.Хлорирование питьевой воды 3-10 0,3-0,5 1.2.Дезинфекция трубопроводов, резервуаров чистой воды, баков водонапорных башен 75-100 0,3-0,5 1.3.Обезвреживание бытовых 5-10 сточных и шахтных вод. 1.4.Обеззараживание циансодержащих стоков. 50*10 3-100*10 3 2.Борьба с болезнями рыб 3.Железнодорожный и морской транспорт. 3.1.Обезвреживание воды на железных дорогах. 5 3.2.Обезвреживание сточных вод на железных 10 дорогах. 3.3.Хлорирование воды в грузовых танках судов. 15 1,5 (не менее) 4.Система бытового обслуживания населения. 4.1.Дезинфекция емкостей питьевой воды. 750-1000 4.2.Обеззараживание воды в плавательных бассейнах 3-10 0,3-0,5 Использование растворов ГХН для обработки воды плавательных бассейнов Использование растворов ГХН для дезинфекции воды плавательных бассейнов и прудов позволяет получать чистую прозрачную воду, лишенную водорослей и бактерий. При обработке бассейнов растворами ГХН необходимо тщательно контролировать содержание активного хлора в воде. Важное значение имеет также поддержание РН на определенном уровне, обычно 7,4-8,0, а еще лучше 7,6-7,8.Регулирование рН осуществляется введением специальных добавок, например, соляной кислоты. Как и в случае обработки питьевой воды, содержание остаточного хлора в воде плавательных бассейнов должно находиться на уровне 0,3-0,5 мг/дм 3 . Надежное обеззараживание в течение 30 мин. Обеспечивают растворы, содержащие 0,1-0,2% гипохлорита натрия. При этом содержание активного хлора в зоне дыхания не должно превышать 0,1 мг/м 3 в публичных плавательных бассейнах и 0,031 мг/м 3 в спортивных бассейнах. Следует отметить, что замена газообразного хлора гипохлоритом натрия приводит к снижению выделения хлора в воздух и, кроме того, позволяет легче поддерживать остаточное количество хлора в воде. Использование растворов ГХН для обработки сточных вод Гипохлорит натрия широко применяется для обработки бытовых и промышленных сточных вод для разрушения животных и растительных микроорганизмов; устранения запахов (особенно образующихся из серосодержащих веществ); обезвреживания промышленных стоков, в том числе содержащих цианистые соединения. Он может быть использован также для обработки воды, содержащей аммоний, фенолы и гуминовые вещества. В последнем случае могут образовываться хлороформ, дихлор - и трихлоруксусная кислоты, хлоральгураты и некоторые другие вещества, концентрация которых в воде значительно ниже. Гипохлорит натрия также используется для обезвреживания промышленных стоков от цианистых соединений; для удаления сточных вод ртути, а также для обработки охлаждающей конденсаторной воды на электростанциях (в последнем случае используется мало концентрированный гипохлорит натрия марки Э по (1). Некоторые данные о необходимом содержании активного хлора в воде, при использовании для ее обработки растворов гипохлорита натрия приведены в табл. 3. Конкретная доза раствора ГХН при обработке воды определяется исходя из данных этой таблицы и свойств применяемого раствора (см. табл.1). Раствор гипохлорита натрия используется также и во многих других отраслях народного хозяйства, но эти случаи применения в данном обзоре не рассматриваются. ОПРЕДЕЛЕНИЕ ОСНОВНЫХ ХАРАКТЕРИСТИК РАСТВОРОВ ГИПОХЛОРИТА НАТРИЯ Исследованию подвергались три образца растворов гипохлорита натрия. Образец №1 - импортный раствор ГХН представленный для испытания фирмой "ДиЭл Проспектен".Изготовитель - фирма "Bayer" (Германия).Ориентировочный срок изготовления: июнь-июль 2001 года. Образец №2 - раствор марки А по (3) из партии, изготовленной ОАО "Синтез" по технологии компании "ДиЭл Проспектен" 5 сентября 2001 года. Образец №3 - раствор, полученный хлорированием промышленного раствора едкого натра, по содержанию активного хлора превышающий марку А по (4). Изготовлен в период между 5 и 8 сентября 2001 года. 2.1.Определение исходного состава растворов гипохлорита натрия. В соответствии с (3) определялись следующие основные характеристики сравниваемых растворов: внешний вид; коэффициент светопропускаемости, %; массовая концентрация активного хлора, г/дм 3 ; массовая концентрация щелочи в пересчете на NaOH, г/дм 3 ; массовая концентрация железа, г/дм 3 ; Для более полной характеристики исследуемых растворов ГХН дополнительно определялись: массовая концентрация хлоридов натрия, г/дм 3 ; показатель концентрации водородных ионов (рН); массовая концентрация хлората натрия "NaClO3", г/дм 3 ; Результаты определения основных показателей качества исследованных растворов приведены в табл.4. 2.2.Определение скорости разложения растворов ГХН Определение скорости разложения гипохлоритных растворов определялась двумя способами: 1. 2. При комнатной температуре (для образцов №1 и 2). При этом одна проба каждого образца ГХН хранилась в естественных условиях (днем - на свету), а вторая проба - постоянно в темноте. При температуре 55 о С (скорости испытания). В этом случае длительность испытания 7 час. Соответствует длительности хранения в темноте равной 1 году. Результаты определения скорости разложения растворов ГХН при комнатной температуре приведены в табл.5. Данные о скорости разложения растворов ГХН всех трех образцов при температуре 55 оС приведены в табл.6. К сожалению, испытания образца №3 были прекращены преждевременно (отключение электроэнергии из-за аварии на электрораспределительной подстанции).Однако полученные данные позволили рассчитать процент раствора ГХН №3 за период испытаний 3часа, то есть, около 4месяцев хранения при комнатной температуре (данные приведены в табл. 4 в скобках). Таблица 5. Экспериментальные данные о скорости разложения гипохлорита натрия при комнатной температуреТаблица 5. Экспериментальные данные о скорости разложения гипохлорита натрия при комнатной температуре Образец №1 Дата анализов Образец №2 Хранение на свету Хранение в темноте Хранение на свету Хранение в темноте Содержание Содержание Содержание Содержание Процент разложения, % Процент разложения, % Процент разложения, % Процент разложения, % АХ, г/ дм3 От исход- От предыного дущего АХ, г/ дм3 От исход- От предыного дущего 120,0 АХ, г/ дм3 От исход- От предыного дущего 186,0 АХ, г/ дм3 От исход- От предыного дущего 07.09.01г. 120,0 11.09. 117,1 2,42 2,42 117,1 2,42 2,42 172,9 7,04 7,04 186,0 176,0 5,38 5,38 14.09. 112,1 6,58 4,27 115,1 4,08 1,71 169,0 9,14 2,25 169,0 9,14 3,98 19.09. 110,0 8,33 1,87 112,0 6,66 2,69 159,7 14,14 5,50 163,0 12,36 3,55 22.09. 107,3 10,58 2,45 112,0 6,66 0 157,0 15,59 1,69 160,0 13,98 1,84 Таблица 6. Данные о скорости разложения гипохлорита натрия при температуре 55 о С Продолжительность испытаний Содержание АХ, г/дм 3 Исходное После испытаний Процент разложения, % Образец №1 3 120,0 115,3 3,92 Образец №2 3 186,0 163,0 12,36 Образец №3 2 159,0 154,5 2,83 (4,24) Примечание: В скобках указана величина разложения в пересчете на длительность испытаний в 3 часа. Оценка исходного качества импортного раствора ГХН Оценка исходного содержания активного хлора (АХ) и хлорида натрия в импортном растворе ГХН производилась из следующих соображений: 1. 2. По данным заказчика партия гипохлорита натрия поступила из-за рубежа в конце июля с.г. Учитывая, что какое-то, может быть и небольшое время, продукт находился на складе изготовителя и транспортировался, то по состоянию на время измерений 05.09.01г.) общее время его хранения и транспортировки было примерно равно 60 суткам. По результатам двухнедельных испытаний на стабильность, приведенным в табл., было принято,что потеря активного хлора за эти 60 суток составляла в среднем 120-109,65 = 0,69 г/дм 3 в сутки. 15 3. (среднее значение для случаев хранения на свету и в темноте). Из этих соображений было рассчитано первоначальное содержание активного хлора в импортном продукте, равное 120+0,69*60=161,4 г/дм 3 Принимая, что разложение гипохлорита натрия происходит, в основном, по реакции 2NaClO -2NaCl+O2 можно оценить исходное содержание в исходном растворе ГХН хлорида натрия из следующих соображений.На 1г-моль NaClO (74,5) при его разложении образуется 1г-моль хлорида натрия (58,5). Таким образом коэффициент пересчета составляет 0,785. Отсюда исходное содержание хлорида натрия в продукте составляет 179-0,785*0,69*74,5/51,5*60=179-47=132 г/дм 3 Полученные величины близки к значениям активного хлора и хлорида натрия в растворе гипохлорита натрия, изготовленном на ОАО "Скоропусковский опытный завод" (см.табл. 4). ОБСУЖДЕНИЕ ПОЛУЧЕННЫХ РЕЗУЛЬТАТОВ Сравнение качества исследованных растворов ГХН Прежде всего обращает на себя внимание резкое различие между образцами растворов №1 и №2 по внешнему виду. Светложелтый импортный продукт соответственно имеет высокий коэффициент светопропускаемости (98%), а продукт производства ОАО "Синтез", представляющий собой слабопрозрачную жидкость темнокрасного цвета, имеет коэффициент светопропускаемости 31%. Как следует из данных, приведенных в табл.4, это напрямую связано с содержанием в растворах железа. По данным (2) предельно допускаемое содержание железа в растворах ГХН не должно превышать 0,005 мг/дм 3 .Поэтому раствор производства ОАО "Синтез", хотя он по этому показателю соответствует требованиям действующего нормативного документа (см. Табл. 1), далее отстает от требований, предъявляемых к гипохлориту натрия как к химическому продукту, имеющему высокие служебные свойства. Раствор гипохлорита натрия производства ОАО СОЗ (образец№3) по данному показателю близок к импортному: цвет - светложелтый, коэффициент светопропускания - 88%. Содержание железа в этом растворе составляет 0,0047 мг/дм 3 , что соответствует требованиям, приведенным в (г). Присутствие в растворе ГХН железа снижает его стабильность. Об этом в частности, свидетельствуют данные о скоростях разложения исследованных растворов ГХН, приведенных в табл. 5 и 6.Их значения для образцов №1 и 3 значительно ниже, чем для образца №2, но очень близки между собой. Из этого можно сделать однозначный вывод о том, что требования к растворам ГХН по (3) значительно уступают требованиям к служебным свойствам растворов, требуемых промышленность и основаны на возможностях технологий, принятых на предприятиях - изготовителях бывшего СССР и находившихся, как известно, на низком уровне. Исходное содержание активного хлора в образцах растворов ГХН №1 и 3 меньше чем в образце №2. При этом содержание в них хлорида натрия соответствует стехиометрическому. В то же время в образце №2, в котором содержание активного хлора примерно в 1,16 раза больше, чем в образцах №1 и 3, содержание хлорида натрия в 1,21 раза выше стехиометрического соотношения (177 г/ дм 3 вместо 146 г/ дм 3), что дополнительно свидетельствует о низком уровне культуры производства, в частности, отсутствии контроля за уровнем температуры технологического процесса. Таким образом, можно сделать вывод, что гипохлорит натрия, изготовленный на СОЗ по технологии компании "ДиЭл Проспектен" (образец №3) практически аналогичен импортному продукту _ гипохлориту натрия фирмы "Bayer" (Германия). Более того, несмотря на отсутствие специальных консервирующих добавок гипохлорит натрия (образец №3) является более стабильным, чем немецкий и срок его гарантированного хранения превосходит немецкий на два - три месяца. Исследовательская группа ГОСНИИ "Хлорпроект"
