На правах рукописи Щукин Иван Александрович 14.00.13 – «Нервные болезни»
реклама

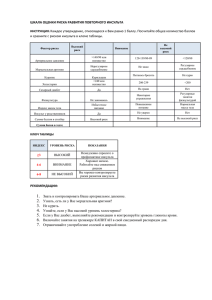
На правах рукописи Щукин Иван Александрович «КЛИНИКО-ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ И ДИФФЕРЕНЦИРОВАННАЯ ТЕРАПИЯ ГЕМОРРАГИЧЕСКОГО ИНСУЛЬТА» 14.00.13 – «Нервные болезни» Автореферат диссертации на соискание ученой степени кандидата медицинских наук Москва - 2007 Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию» Научный руководитель: Доктор медицинских наук, профессор М.Ю. Мартынов Официальные оппоненты: Доктор медицинских наук, профессор С.А. Румянцева Доктор медицинских наук, профессор М.Ю. Максимова Ведущее учреждение: Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского. Защита состоится «29» мая 2007 года в 14.00 часов на заседании диссертационного совета К 208.072.01 при Российском государственном медицинском университете (117997, г. Москва, ул. Островитянова, д.1). С диссертацией можно ознакомиться в библиотеке Российского государственного медицинского университета по адресу 117 997, г. Москва, ул. Островитянова, д.1 Автореферат разослан «19» апреля 2007 года. Учёный секретарь диссертационного совета Кандидат медицинских наук, доцент Л.В. Губский Актуальность проблемы. Частота геморрагических инсультов (ГИ) составляет 15-25%, и смертность в течение первого года после заболевания достигает 50-55 % [Е.И. Гусев, В.И. Скворцова, 2001]. В каскаде событий, происходящих после выхода крови из разорвавшегося сосуда, большую роль играет превращение оксигемоглобина в деокси- и метгемоглобин и гемосидерин. Эти процессы активируют перекисное окисление липидов, приводят к гибели нейронов в культуре, способствуют развитию сосудистого спазма, запуску процессов апоптоза [Xi G, 2002]. Кроме этого, определенное значение в патофизиологическом каскаде при ГИ может иметь локальное снижение мозгового кровотока и перифокальная ишемия [Carhuapoma, 2000, Huang, 2002]. Также, в зоне, окружающей гематому, возможно развитие воспалительной реакции [Xi G, 2002]. Существует два подхода к лечению геморрагического инсульта – хирургический и консервативный [А.Н. Коновалов, Ф.А. Сербиненко, 1973, В.В. Крылов 1995, Broderick, 1999]. В последние годы в экспериментальных и клинических исследованиях при геморрагическом инсульте повышенное внимание уделяется изучению эффективности антиоксидантных и хелаторных препаратов. Показана эффективность этамзилата Na (дицинона), обладающего выраженной антиоксидантной активностью [Е.И. Гусев, 1993]. Большое внимание уделяется фактору VIIа, назначение которого обеспечивает локальный гемостаз [Hedner, 1998, Mayer, 2003]. В эксперименте установлено, что применение клометиазола и ганаксолона обеспечивает нейропротективный эффект при ГИ через их способность связываться с GABA рецепторами [Wahlgren, 2000, Nakamura, 2003]. Препаратом, уменьшающим выработку свободных радикалов, высвобождение цитохрома С и активацию каспазы, является тауроурсодеоксихолиевая кислота, введение которой при экспериментальном ГИ способствует более благоприятному течению заболевания [Lyden, 1999, Rodrigues, 2003]. 2 Одним их эффективных природных препаратов, обладающим антиоксидантным и хелаторными свойствами, является отечественный препарат Гистохром, относящийся к хиноидным пигментам, содержащимся в панцирях и иглах морских ежей [Л.В. Богуславская, 1985]. Гистохром сдерживает образование продуктов перекисного окисления липидов, улучшает клинические и биохимические показатели при тромболитической коронарной реперфузии у больных острым инфарктом миокарда [Г.Б. Еляков, 1999]. Гистохром применяется при лечении заболеваний, связанных с кровоизлияниями в стекловидное тело и сетчатку. Его введение, особенно на ранних стадиях кровоизлияния, способствует более быстрому разжижению и разрыхлению сгустка крови [Е.А. Егоров, 1999, М.Р. Гусева, 2003]. Таким образом, исследования последних лет показывают, что при геморрагическом инсульте актуальным является дальнейшее изучение патофизиологических механизмов повреждения головного мозга и разработка новых методов дифференцированной консервативной терапии. Цель исследования: В экспериментальных и в клинических условиях изучить патофизиологические механизмы повреждения головного мозга при геморрагическом инсульте и разработать способы их дифференцированной коррекции. Задачи исследования: 1. Изучить динамику перифокального отёка, состояние микроциркуляторного русла, выраженность перифокальной ишемии и воспалительной реакции при экспериментальном геморрагическом инсульте. 2. Изучить влияние препарата Гистохром на динамику перифокального отёка, состояние микроциркуляторного русла, выраженность перифокальной ишемии и воспалительной реакции при экспериментальном геморрагическом инсульте. 3. У больных с геморрагическим инсультом на разных временных этапах заболевания уточнить значение сочетанного анализа шкалы ком Глазго, 3 Скандинавской шкалы инсульта, объема гематомы, отека и внутрижелудочкового кровоизлияния, выраженности смещения срединных структур головного мозга для прогнозирования исхода заболевания и степени функционального восстановления по шкале Бартель. 4. У больных с геморрагическим инсультом изучить состояние спонтанной и индуцированной на адреналин агрегации тромбоцитов, размеров агрегатов и скорости агрегации, а также уровень фибриногена. 5. У больных с геморрагическим инсультом изучить влияние препарата Гистохром на выраженность и динамику неврологических нарушений, оцениваемую по шкале ком Глазго и по Скандинавской шкале инсульта, на степень функционального восстановления по шкале Бартель и на показатели реологических свойств крови и сопоставить эти результаты с результатами, полученными в контрольной группе. Научная новизна: Впервые в нашей стране проведено моделирование геморрагического инсульта у лабораторных животных с последующей оценкой неврологических и поведенческих нарушений, проведением высокопольного МРТ и гистологического исследования на разных сроках экспериментального геморрагического инсульта. Показано, что при экспериментальном геморрагическом инсульте происходит ряд последовательных патофизиологических изменений, включающих развитие в перифокальной области гематомы отёка, микроциркуляторных нарушений, ишемии и воспалительной реакции. Впервые исследовано влияние антиоксидантного и хелаторного препарата Гистохром на течение экспериментального геморрагического инсульта и показано его положительное действие на регресс неврологических и поведенческих нарушений, на динамику перифокального отёка головного мозга, нарушений микроциркуляции, выраженность ишемических изменений и воспалительной реакции (по данным высокопольного МРТ и гистологического исследования). 4 Показана важность сочетанной оценки в динамике таких клинических и нейровизуализационных параметров, как сумма баллов по шкале ком Глазго и по Скандинавской шкале инсульта, объёма гематомы, отека и внутрижелудочкового кровоизлияния и выраженности смещения срединных структур головного мозга для прогнозирования исхода заболевания и степени функционального восстановления. У больных с геморрагическим инсультом изучены спонтанная и индуцированная на адреналин агрегация тромбоцитов, скорость агрегации, размер тромбоцитарных агрегатов и уровень фибриногена. Установлено, что при геморрагическом инсульте имеются выраженные нарушения тромбоцитарного звена гемостаза: у большинства (≈⅔) больных отмечается повышение спонтанной и индуцированной агрегации тромбоцитов на адреналин, скорости агрегации и увеличения размеров тромбоцитарных агрегатов и уровня фибриногена. Впервые изучено влияние препарата Гистохром на течение геморрагического инсульта в клинических условиях и показано, что его назначение способствует более быстрому регрессу неврологической, в первую очередь общемозговой и менингеальной, симптоматики. Выявлено, что Гистохром снижает спонтанную и индуцированную на адреналин агрегацию тромбоцитов, размеры тромбоцитарных агрегатов и скорость агрегации, уровень фибриногена. Научно-практическая значимость работы: Моделирование геморрагического инсульта у лабораторных животных позволяет изучать различные этапы патофизиологического каскада при этом заболевании, а также эффективность и безопасность назначения лекарственных препаратов. У больных с геморрагическим инсультом сочетанный анализ в динамике тяжести состояния по шкале ком Глазго, выраженности неврологических симптомов по Скандинавской шкале инсульта, объёма гематомы и внутрижелудочкового кровоизлияния и выраженности смещения срединных струк- 5 тур головного мозга позволяет прогнозировать исход заболевания и степень функционального восстановления и, соответственно, оптимизировать терапию и реабилитационные мероприятия. Лечение больных с геморрагическим инсультом должно включать назначение антиоксидантных и хелаторных препаратов, так как препараты этих групп, влияя на определенные этапы патофизиологического каскада, способствуют более быстрому регрессу общемозговой, менингеальной и очаговой неврологической симптоматики. Изучение спонтанной и индуцированной агрегации у больных с геморрагическим инсультом выявило выраженные нарушения тромбоцитарного звена гемостаза, в связи с чем при развитии геморрагического инсульта необходимо в динамике исследовать систему тромбоцитарного гемостаза и назначать препараты, влияющие на реологические свойства крови. Основные положения, выносимые на защиту: 1. При геморрагическом инсульте наблюдаются сложные патофизиологические процессы, включающие развитие перифокального отёка, микроциркуляторные нарушения, ишемические изменения и воспалительную реакцию. Эти изменения максимально выражены по периферии гематомы, однако в отдельных случаях могут наблюдаться и в отдалённых от очага участках головного мозга. 2. Анализ цереброспинальной жидкости методом ВЭЖХ при экспериментальном геморрагическом инсульте выявляет наличие в ней Гистохрома и продуктов его метаболизма, что указывает на его способность проникать через ГЭБ. По данным высокопольного МРТ и гистологического исследования введение Гистохрома сопровождается более быстрым уменьшением перифокального отёка, нарушений микроциркуляции, выраженности ишемии и воспалительной реакции, что проявляется опережающим по сравнению с контрольными животными уменьшением неврологических симптомов и поведенческих нарушений. 6 3. У больных с геморрагическим инсультом сочетанный анализ в динамике тяжести состояния по шкале ком Глазго, выраженности неврологической симптоматики по Скандинавской шкале инсульта, объёмов гематомы, отека и внутрижелудочкового кровоизлияния, а также выраженности смещения срединных структур головного мозга позволяет прогнозировать исход заболевания и степень функционального восстановления. 4. При геморрагическом инсульте ≈ у ⅔ больных наблюдается повышение спонтанной и индуцированной (на адреналин) агрегации тромбоцитов, скорости агрегации, увеличение размера тромбоцитарных агрегатов и уровня фибриногена. Наиболее выраженные изменения выявлены у больных, поступавших в крайне тяжелом состоянии. 5. У больных с геморрагическим инсультом Гистохром при внутривенном введении быстро проникает через ГЭБ и обнаруживается в неизмененном виде и в виде метаболитов в цереброспинальной жидкости. Назначение его благоприятно влияет на динамику заболевания, при этом положительный эффект препарата в первую очередь проявляется опережающим, по сравнению с контрольной группой, уменьшением общемозговой и менингеальной симптоматики. Наиболее эффективно применение Гистохрома у больных, поступающих в тяжелом состоянии. Назначение Гистохрома сопровождается улучшением реологических свойств крови. После введения Гистохрома у больных отмечается снижение спонтанной и индуцированной агрегации тромбоцитов на адреналин, скорости агрегации, размера тромбоцитарных агрегатов и уровня фибриногена. Апробация работы и внедрение в практику. Основные положения диссертации представлены и обсуждены на совместной научно-практической конференции сотрудников кафедры неврологии и нейрохирургии лечебного факультета, лаборатории по изучению нарушений мозгового кровообращения Российского государственного университета, 12 и 13 неврологических отделений и 10 отделения реанимации и интенсивной терапии ГКБ № 1 им. Н.И. Пирогова от 20 июня 2006 года. 7 Полученные данные внедрены в работу 12 и 13 неврологических отделений и 10 отделения реанимации и интенсивной терапии ГКБ № 1. Публикации. По теме диссертации опубликовано 5 печатных работ. Структура и объём диссертации: Диссертация изложена на 161 страницах машинописи, включает 5 глав: обзор литературы, описание материалов и методов, 3 главы, отражающие результаты собственных исследований, заключение, выводы, практические рекомендации и библиографический указатель, содержащий 266 источников (35 отечественных и 231 зарубежных). Диссертация содержит 2 диаграммы, 21 таблицу, 9 рисунков. Методы и материалы. Экспериментальная часть исследования. Экспериментальная часть работы выполнена на 48 крысах – самцах линии Wistar в возрасте 3-6 месяцев. Все животные были разделены на две группы: основную, получавшую Гистохром, и контрольную. В каждой группе было выделено 8 подгрупп, в зависимости от времени последнего МРТ исследования и вывода животного из эксперимента. Животным моделировался геморрагический инсульт по методике Rosenberg, 1991 г. Общий объём гематомы в пересчёте на клинические условия составлял ≈ 40 - 50 мл, и по локализации они соответствовали кровоизлияниям, которые возникают при разрыве лентикуло-стриарных артерий. Гистохром вводился внутрибрюшинно в дозе 0,7 мг/кг. Первая доза вводилась через 30 минут после создания гематомы, далее с промежутком в 1012 часов. Контрольной группе внутрибрюшинно вводился 0,9% раствор NaCl в эквивалентной дозе в те же временные интервалы. Всем животным дважды было выполнено МРТ исследование: сразу после создания гематомы и, в зависимости от группы, через 6, 12, 24, 48 и 72 часа, затем 7 суток, 14 суток и 21 сутки. МРТ исследование проведено на томогра- 8 фе для экспериментальных исследований «PharmaScan US 70/16» (Bruker, Германия) с магнитным полем 7,0 Тесла и частотой 300 MHz. Обнаружение Гистохрома в цереброспинальной жидкости (ЦСЖ) проводили методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на хроматографе Agilent Technologies 1100 (Германия) с колонкой ZORBAX Eclipse XDB-C8 (США) при температуре 30º С. До и после операции производилась оценка неврологических изменений по шкале Menzes и поведенческих нарушений - латентного периода задержки животного в светлой камере (тест пассивного избегания). Оценка по шкале Menzes проводилась за сутки до операции и затем после операции через 6, 12, 24, 48 и 72 часа, на 7, 14 и 21 сутки. Латентный период задержки начинал оцениваться через 24 часа после создания гематомы. После последнего МРТ исследования подопытное животное усыплялось хлороформом с последующим введением параформальдегида (4% раствор). Зафиксированный головной мозг разрезался вдоль канала, по которому вводилась кровь. Анализировались образцы ткани из пораженного и здорового полушарий. На срезах толщиной 5 мкм, окрашенных толлуидиновым синим по Нисслю и гемотоксилин-эозином, оценивали структуру гематомы, отек, изменения нейронов и глиальных клеток, нейтрофильную, лимфоцитарную и макрофагальную реакции. Степень выраженности признака оценивалась по балльной шкале («-» - отсутствие признака, «++++» - максимальная степень). Клиническая часть исследования. Клиническая часть исследования включала 64 пациента, у которых было диагностирован геморрагический инсульт, подтвержденный КТ. У всех больных причиной кровоизлияния была артериальная гипертензия. Тридцать больных составили основную группу, получавшую в составе основной терапии препарат Гистохром, и 34 - контрольную. Неврологическое обследование проводилось на 1, 2, 3, 7, 14, 21 дни заболевания и перед выпиской больного из стационара. Изучение тяжести состояния больных и прогнозирование исхода заболевания проводилось на осно- 9 вании шкалы ком Глазго (ШКГ) на 1 и 3 сутки заболевания. Все пациенты, в зависимости от количества баллов по ШКГ, были разделены на 3 группы: 1 группа – 3-6 баллов, 2 – 7-12 баллов, 3 – 13-15 баллов. Выраженность неврологической симптоматики оценивалась по Скандинавской шкале инсульта (СШИ) 4 раза: на 1, 3, 7 и 30 сутки заболевания. По Скандинавской шкале инсульта все пациенты были разделены на три группы: меньше 34 баллов, 35-44 балла и 45-58 баллов. Степень функционального исхода определялась по шкале Бартель на 30 сутки заболевания. Все пациенты были разделены на две группы: группа с благоприятным исходом (шкала Бартель - 61-100 баллов) и группа с неблагоприятным исходом (шкала Бартель < 60 баллов и летальные исходы). Исследование реологических свойств крови проводилось на агрегометре «Биола» Россия. Изучались спонтанная и индуцированная адреналином агрегация, размер тромбоцитарных агрегатов и скорость агрегации. Определялся также уровень фибриногена (весовой метод Рутберга). Исследование всех вышеуказанных параметров проводилось перед первым введением Гистохрома в основной группе или физиологического раствора в контрольной группе и через один час после окончания введения. Обнаружение Гистохрома в ЦСЖ у больных проводили также как в экспериментальном разделе исследования. Компьютерная томография выполнялась на томографе ”HiSpeed CT/e Dual” фирмы General Electric, США. При проведении КТ толщина среза и шаг томографа составляли 5 - 10 мм. Объём гематомы, объём отёка и внутрижелудочкового кровоизлияния (ВЖК) вычисляли по специальной программе, поставляемой с компьютерным томографом. Также измерялось смещение срединных структур головного мозга на уровне тела III желудочка. Всем больным с геморрагическим инсультом проводилась терапия, включавшая назначение противоотёчных, сосудистых, антибактериальных и симптоматических препаратов. Проводилась коррекция дыхательных, гемодинамических и водно-электролитных нарушений. Кроме этого, в основной 10 группе ежедневно на протяжении 5-ти дней назначался препарат Гистохром. Введение препарата осуществлялось согласно схеме, разработанной Российским научно-производственным кардиологическим комплексом МЗ и СР РФ, по 5,0 мл 1% раствора внутривенно на 100,0 мл физиологического раствора. Первое введение проводилось струйно медленно, последующие – капельно, с частотой 60 капель в минуту. В контрольной группе ежедневно на протяжении 5 дней на фоне основной терапии внутривенно вводился физиологический раствор 0,9% - 100,0 мл. Анализ результатов проводился методом компьютерной обработки с использованием пакета статистических программ STATISTICA 6.0, SPSS 6,1. Динамику объёма гематомы и перифокального отёка рассчитывали при помощи программного обеспечения томографа ParaVision 3.0.1. Сравнение распределения исследуемого признака между группами проводилось с применением таблиц 2×2, 2×n и расчетом χ2, корректированного по Йетсу. Описательная статистика применялась для вычисления среднего значения исследуемых показателей и их среднеквадратичных отклонений. Различия между показателями считались достоверными при вероятности ошибки менее 5%. Результаты исследования. Экспериментальная часть. При проведении ВЭЖХ цереброспинальной жидкости, взятой у животных 6 и 12 часовых групп, был обнаружен гистохром. Его идентифицировали по времени удерживания (11,12 минуты), совпадающем со временем удерживания стандартного образца, а также по присутствию на хроматограмме пика со временем удерживания 6,64 минуты, характерного для продукта окисления гистохрома (рисунок 1). 11 Рисунок 1. ВЭЖХ цереброспинальной жидкости крысы № 2 (1,5 часа после введения второй дозы Гистохрома) При анализе неврологической симптоматики через 6 и 12 часов после развития гематомы у животных обеих групп отмечались одинаково выраженные нарушения: крысы были адинамичны, более чем у 25% из них наблюдалась тенденция к спонтанному вращению в противоположную сторону (4 балла по шкале Menzes). В 50,0% наблюдений в основной группе и в 44,5% наблюдений в контрольной группе отмечалось движение в противоположную очагу сторону при удержании крысы за хвост (3 балла). При осмотре через 24 часа в основной группе отмечено дальнейшее уменьшение симптомов, в то время как у контрольных животных неврологические нарушения были прежними. Сумма баллов в группе с Гистохромом составила 1,61±0,51, а в контрольной - 1,99±0,49 (t=2,29, p=0,003). Аналогичная динамика симптомов отмечена и через 48 часов. При следующем осмотре (через 72 часа) в основной группе симптомы были представлены тонической флексией передней противоположной лапы при подъёме за хвост (1 балл). В контрольной группе неврологические нарушения стали достоверно меньше, чем через 48 часов (t=3,56, p=0,004), однако различия между группами сохранялись (t=3,72, p=0,001). Эти различия продолжали сохраняться и через неделю после заболевания (t=2,8, p=0,013). В дальнейшем, в обеих группах неврологические симптомы продолжали уменьшаться и к 14-м суткам исчезли. 12 Латентный период начинали анализировать через 24 часа после заболевания, и задержка у животных контрольной группы в этой временной точке составила более 1 минуты (69±8 сек), в то время как в группе с Гистохромом задержка была меньше - 61±6 сек (t=3,51, p=0,001). При обследовании через 48 часов после операции в обеих группах выявлено уменьшение латентного периода по сравнению с осмотром через 24 часа (р<0,007), однако различия между группами сохранялись (t=2,46, p=0,02). Через 72 часа у животных основной и контрольной групп отмечено дальнейшее укорочение латентного периода (р<0,015), при этом различия между группами исчезли. К 7 и 14 суткам латентный период существенно сократился, приблизившись к норме. При проведении МРТ и морфологического исследования в первые часы после кровоизлияния в узкой зоне (0,2-0,5 мм), окружающей гематому, выявлялся околоклеточный и периваскулярный отек (рисунок 2). Через 12-24 часа явления отека продолжали нарастать, распространяясь на расстояние до 1-2 мм от геморрагического очага. Отек мозга сопровождался рядом последовательных морфологических изменений со стороны сосудистой стенки и микроциркуляторного русла (таблица 1). Первоначально отмечался спазм артериол с эффектом запустевших сосудов. На 2-3 дни после кровоизлияния это состояние сменялось паретическим расширением капилляров, артериол и венул. В просвете сосудов в этот период выявлялись скопления форменных элементов крови, а перикапиллярные пространства были расширены. В областях, перифокальных от кровоизлияния, наблюдались реактивные изменения эндотелия и экссудация жидкой части крови через некротизированные стенки сосуда. На этой стадии часто можно было наблюдать краевое стояние лейкоцитов, формирующих под Рисунок 2 МРТ через 6 часов после развития геморрагического инсульта. 13 эндотелием длинные ряды. Расширенные периваскулярные пространства, заполненные плазмой, свидетельствовали о значительно повышенной проницаемости сосудистой стенки. Вследствие повышенной проницаемости стенок сосудов в окружающих их пространствах часто наблюдались вторичные диапедезные кровоизлияния. Одновременно с отеком с первых часов заболевания обнаруживались дистрофические изменения нейронов и глиальных клеток (таблица 1), достигавшие максимального значения на узких участках, окружавших геморрагический очаг. В этих областях наблюдались зоны обширного Таблица 1. Динамика морфологических изменений в головном мозге крыс. Группа Изменения Вторичные Изменения Реакция Инфильтрация микроциркуляции очаги нейронов глии нейтрофилами 1 2 1 6 часов +/++ + 12 часов ++/+++ ++ + 24 часов ++ +++ 48 часов ++ 72 часов 7 суток 2 1 2 1 2 1 2 ++++ ++++ ++ +++ + - ++ +++ ++++ +++ ++++ ++ + + + +++ ++++ +++ +++ ++ + +++ -/+ + ++ ++ +++ +++ +/++ +++ +/++ +/++ - - ++ ++++ ++ ++++ + ++ + ++ - - +/++ +++ ++ ++ + + 14 14 суток + ++ - - + ++ + ++ - + Где: 1 – основная группа, 2 – контрольная группа аутолиза, представленные бесструктурной, слабо-базофильной тканью, содержащей лишь единичные глиальные элементы. Кроме этих изменений, в областях, расположенных перифокально от гематомы, выявлялось значительное количество нейронов с признаками ишемического повреждения пикноз и вакуолизация цитоплазмы. В отдельных случаях ишемические изменения наблюдались на значительном удалении от кровоизлияния - в коре, гиппокампе, структурах среднего мозга. Эти изменения, однако, носили временный характер и не приводили к гибели клеток. В астроцитах и олигодендроцитах в течение первых трех суток обнаруживались явления дегенеративного характера, а, начиная с 7 дня, в глиальных клетках активизировались процессы пролиферации (таблица 1). Впоследствии восстановительные процессы с участием глиальных клеток приводили к формированию капсулы вокруг очага кровоизлияния. С момента кровоизлияния в периферических участках гематомы формировались очаговые скопления лейкоцитов с преобладанием среди них сегментоядерных клеток (таблица 1). К 48-72 часам нейтрофильная инфильтрация достигала максимальной степени выраженности. Очаговые скопления нейтрофилов располагались в виде ограничительного вала по краю гематомы и были наиболее выражены в ишемизированных областях. Лимфоцитарная инфильтрация начинала развиваться через 3-4 дня после кровоизлияния и достигала максимальных значений к 7-10 дням. При анализе влияния Гистохрома на выраженность отека при геморрагическом инсульте отмечена разная динамика его изменения между группами (p=0,049). После 48 часов перифокальный отек более быстро (р=0,0021 для тенденции) уменьшался в основной группе и практически полностью исчезал к 7 суткам. У животных, получавших Гистохром, были более ярко выражены признаки воспалительной реакции с развитием нейтрофильной инфильтрации (таблица 1). В тоже время, ее выраженность не достигала той степени 15 интенсивности, которая отмечалась в контрольной группе. В этот же период времени аналогичные изменения отмечались со стороны микроциркуляторного русла (таблица 1). Затем, начиная с 24-48 часов и вплоть до конца наблюдения, на фоне более активных восстановительных процессов заметно быстрее протекали явления стабилизации микроциркуляторных нарушений, и уменьшение выраженности изменений со стороны артериол значительно опережало контрольную группу (таблица 1). Это сопровождалось менее выраженным повреждением нейрональных и глиальных элементов, ускорением процессов организации очага, особенно со 2-го дня заболевания (таблица 1). Таким образом, экспериментальное исследование показало, что геморрагический инсульт - это сложный каскад патофизиологических реакций с определённой временной последовательностью, включающий развитие отека, нарушений микроциркуляции, ишемических и дегенеративных изменений нейронов и глии и воспалительной реакции. Гистохром проникает через ГЭБ и обнаруживается в ЦСЖ уже через 1,5 часа после внутрибрюшинного введения. По данным МРТ и гистологического исследования введение Гистохрома сопровождается более быстрым уменьшением перифокального отёка и нарушений микроциркуляции, меньшим повреждением нейронов и глиальных элементов, что проявляется опережающим по сравнению с контрольной группой уменьшением очаговых симптомов и поведенческих нарушений. Клиническая часть исследования. Среди обследованных мужчин было 36 (56,2%), женщин - 28 (43,8%). Средний возраст составил 60,1±10,3 лет (женщины - 58,9±11,1, мужчины 61,1±9,7). В основной группе средний возраст был 58,1±11,6 лет (мужчины 57,4±9,4, женщины - 60,3±10,7). В контрольной группе - 61,7±8,9 лет (мужчины - 61,7±11,1, женщины - 59,8±10,7). Среди всех обследованных превалировали наблюдения с полушарной локализацией кровоизлияний – 96,9%. В правом полушарии ГИ локализовался в 40,6% случаев (26 больных), в левом – в 54,5% (35 наблюдений), в одном случае гематомы были в обоих полуша- 16 риях. Прорыв крови в желудочки мозга отмечался в 42,2% наблюдений (27 больных). Локализация гематом между группами не различалась. Ранее было показано, что важным фактором, позволяющим достоверно прогнозировать исход мозгового инсульта, является тяжесть состояния больного, оцененная в первые сутки заболевания по шкале ком Глазго [Flemming, 1999, Phan, 2000]. В настоящем исследовании установлено, что оценка тяжести состояния по шкале ком Глазго в более поздние сроки заболевания также является важной для прогнозирования исхода заболевания и степени инвалидизации. Различия между группами с удовлетворительным и неудовлетворительным восстановлением по шкале Бартель, оцененные по шкале ком Глазго на 3 сутки заболевания, были достоверны (р=0,000). Кроме этого, в выполненном исследовании также показана важность оценки выраженности неврологических симптомов по Скандинавской шкале инсульта на протяжении всей 1-ой недели заболевания. В основной и контрольной группах установлена обратная корреляция между суммой баллов по СШИ на 1, 3 и 7 сутки болезни и степенью инвалидизации по шкале Бартель (r>0,83, р<0,001). При анализе нейровизуализационных данных установлено, что наиболее значимыми факторами, влияющими на исход заболевания, были объём гематомы, перифокального отёка и внутрижелудочкового кровоизлияния (ВЖК), а также выраженность смещения срединных структур головного мозга (таблица 2). В основной и контрольной группах отмечена высокая достоверность различий в объемах кровоизлияний между больными с хорошим и с неудовлетворительным восстановлением (р=0,000). В основной группе у больных с хорошим восстановлением объём гематомы составлял 16,7±12,8 см³, а у пациентов с выраженной инвалидизацией - 40,5±14,1 см³. Объем гематомы в обеих группах был прямо связан с вероятностью неблагоприятного исхода заболевания (r>0,81, p=0,000), а также с суммой баллов по ШКГ в 1 и 3 сутки (r>0,75, р<0,000) и по СШИ в 1, 3, 7 и 30 сутки заболевания (r>0,83, р<0,001). Таблица 2 17 Факторы, влияющие на исход заболевания. Шкала Бартель 61-100 Основная Контрольгруппа ная группа 16,7±12,8 12,1±8,0 Шкала Бартель <60 Основная Контрольгруппа ная группа 40,5±14,1 35,5±17,6 0,000 V отёка 19,1±12,5 19,2±16.7 36,1±19,9 36,1±17,2 0,007 V ВЖК Прорыв крови в желудочки (%) Смещение (%) 0,9±0,6 1,05±0,8 7,6±2,55 6,86±2,01 0,003 4 4 9 10 0,004 3 4 10 12 0,000 V гематомы р Объём перифокального отёка также прямо коррелировал с тяжестью состояния по шкале ком Глазго на 1 и 3 сутки заболевания (r>0,49, р<0,01) и с выраженностью неврологической симптоматики по СШИ в 1, 3 и 7 сутки (r>0,53, р<0,01). Также установлена связь между объемом отека и степенью инвалидизации по шкале Бартель (r=0,54, р<0,01). Важным прогностическим фактором было смещение срединных структур головного мозга. В основной группе смещение срединных структур у пациентов с неудовлетворительным восстановлением отмечено в 10 наблюдениях, а у пациентов с хорошим восстановлением - в 3 наблюдениях (χ2=13,1, р=0,000). Аналогичные результаты получены в контрольной группе: 12 и 4 пациента соответственно (χ2=11,76, р=0,000). Кроме того, в обеих группах у больных с неудовлетворительным восстановлением достоверно чаще наблюдался прорыв крови в желудочки мозга (χ2>6,99, р<0,004). Объём внутрижелудочкового кровоизлияния был важным прогностическим фактором. В обеих группах отмечена высокая достоверность различий (р<0,003) в объемах ВЖК между больными с хорошим и с неудовлетворительным восстановлением (таблица 2). Выявлена прямая корреляция между объёмом ВЖК и степенью инвалидизации по шкале Бартель (r=0,65, р=0,000). В обеих группах установлена прямая корреляция между объёмом ВЖК и тяжестью состояния по ШКГ на 1 и 3 сутки заболевания (r>0,62, 18 р=0,000). Кроме того, у больных с большими по объёму ВЖК выявлена корреляция с суммой баллов по СШИ на 1, 3, 7 и 30 сутки (r>0,46, р=0,000). При анализе летальных исходов было отмечено, что все умершие больные поступили в крайне тяжелом состоянии. Объем гематом составлял 35-65 см3, объём отёка достигал 80 см³. У всех отмечался прорыв крови в желудочки мозга и объём ВЖК достигал 30 см³. Сумма баллов по шкале ком Глазго была меньше 8. Аналогичные результаты были получены Broderick J.P., 1993: летальность в группе пациентов с объемом гематомы больше 60 мл в сочетании с суммой баллов по шкале ком Глазго меньше 8 достигала 91%. При исследовании реологических свойств крови у больных обеих групп отмечены разнонаправленные изменения спонтанной и индуцированной на адреналин агрегации тромбоцитов, скорости агрегации и размеров агрегатов (таблица 3). Спонтанная агрегация превышала нормативные значения у 12,8% больных, а значения индуцированной агрегации на адреналин были повышены у 51,6% пациентов и снижены у 8,2% обследованных. Наиболее значительные изменения отмечались в подгруппе больных, поступавших в крайне тяжелом состоянии (спонтанная агрегация - 0,32±0,27, индуцированная агрегация - 67,08±28,92, скорость агрегации - 68,85±31,17, размер агрегатов - 8,7±1,7). У больных этой подгруппы интенсивность агрегации тромбоцитов на адреналин коррелировала с объемом отёка и ВЖК (r>0,22, р<0,081). Также отмечена корреляция между выраженностью неврологических симптомов по СШИ на 1 и 3 сутки заболевания и индуцированной агрегацией тромбоцитов (r>0,26, р<0,03). Таблица 3 Показатели агрегации тромбоцитов и уровень фибриногена у больных с геморрагическим инсультом Min – Max. Med ± SD Норма Спонтанная 0,0 - 1,8 0,68±0,57 <1,35 агрегация Индуцированная 31,3 – 104,0 65,57±17,31 45-55 агрегация Скорость 25,8 – 100,0 60,78±18,37 35-55 19 агрегации Размер агрегатов Фибриноген 5,2 - 11,6 7,41±1,36 4,5-6,5 3,2 – 4,9 4,28±0,48 3,5-4,5 Таким образом, для прогнозирования исхода геморрагического инсульта и степени функциональной инвалидизации по шкале Бартель целесообразно сочетано анализировать тяжесть состояния больных по шкале ком Глазго не только на 1, но и на 3 сутки заболевания и выраженность неврологических симптомов по Скандинавской шкале инсульта на 1, 3 и 7 сутки заболевания. Изучение реологических свойств крови показывает, что при геморрагическом инсульте более чем у ½ больных отмечается активация тромбоцитарного звена гемостаза с повышением индуцированной на адреналин агрегации тромбоцитов, скорости агрегации и размеров тромбоцитарных агрегатов, в то время как спонтанная агрегация в большинстве наблюдений остается в пределах нормы. Выраженность нарушений агрегации в определенной степени связана с объемом кровоизлияния и наличием крови в желудочках, а также с тяжестью состояния больного. Все пациенты основной группы получали Гистохром. Во время лечения побочных эффектов не было. Для установления факта проникновения Гистохрома через ГЭБ у одного больного двукратно методом ВЭЖХ было исследовано содержание препарата в ЦСЖ. Гистохром в концентрации 0,0085 и 0,0065 мкг/мл и его метаболиты были обнаружены в обоих образцах. До введения препарата достоверной разницы по данным клинического и нейровизуализационного обследования и состоянию реологических свойств крови между пациентами основной и контрольной группы отмечено не было. На фоне введения Гистохрома отмечалась более быстрая динамика уменьшения неврологических симптомов, оцениваемых по СШИ. Уже к третьим суткам в основной группе этот показатель был достоверно выше - 2,7 баллов, чем в контроле - 0,8 баллов (р=0,000) (рисунок 3). К 7 суткам прирост сум- 20 марного клинического балла в основной группе пациентов также был достоверно больРисунок 3 Рисунок 4 прирост суммарного клинического балла в подгруппе больных, поступавших в тяжелом состоянии прирост суммарного клинического балла в основной и контрольной группах 12,511,7 10 5 5,9 2,7 20 осн.гр. 4,1 баллы баллы 15 контр.гр. 0,8 0 3 7 сутки 10,73 10 4,74 1,07 0 30 3 15,55 12,71 осн. гр. 5,28 7 сутки контр. гр. 30 ше по сравнению с контрольной группой (5,9 и 4,1 баллов, соответственно, р=0,000). Наибольшие различия в динамике прироста суммы баллов по СШИ были у больных, поступивших в тяжелом состоянии (рисунок 4). Это связано с тем, что в основной группе (в подгруппе больных, поступавших в тяжелом состоянии) к 3 и 7 суткам значительно уменьшилось количество больных с общемозговой и менингеальной симптоматикой. У больных в состоянии средней тяжести достоверных различий между группами в динамике прироста суммарного клинического балла не было. Отсутствие различий было связано с тем, что все пациенты поступали в сознании, общемозговая и менингеальная симптоматика была выражена незначительно. Таблица 4 Агрегация тромбоцитов и уровень фибриногена до и после введения Гистохрома. До введения После введения Гистохрома Гистохрома Спонтанная агрегация Индуцированная агрегация Норма t р 0,55±0,52 0,16±0,29 < 1,35 6,76 0,000 60,93±19,28 54,26±19,63 45-55 6,28 0,000 21 Скорость агрегации Размер агрегатов Фибриноген 62,38±21,51 55,47±23,12 35-55 3,91 0,001 7,45±1,66 4,40±0,47 6,13±1,70 4,32±0,40 4,5-6,5 3,5-4,5 4,58 3,82 0,000 0,001 При изучении влияния Гистохрома на реологические свойства крови установлено, что после однократного внутривенного введения препарата отмечено достоверное снижение спонтанной и индуцированной агрегации тромбоцитов и уровня фибриногена (таблица 4). При анализе с учетом тяжести больных установлено, что в подгруппе больных, поступавших в крайне тяжелом состоянии, после введения Гистохрома отмечено достоверное снижение спонтанной агрегации, индуцированной агрегации тромбоцитов на адреналин и размеров агрегатов. Показатели спонтанной агрегации, количества тромбоцитов и фибриногена достоверно не изменились. У больных в тяжелом состоянии и в состоянии средней тяжести после введения препарата отмечено достоверное снижение спонтанной и индуцированной агрегации тромбоцитов. Кроме этого, в отличие от больных, поступавших в крайне тяжелом состоянии, в этих подгруппах отмечалось уменьшение скорости агрегации. Также, у больных средней тяжести после введения Гистохрома отмечено достоверное снижение уровня фибриногена. Таким образом, клиническая часть исследования показывает, что особенностью течения геморрагического инсульта при назначении Гистохрома является более быстрая по сравнению с контрольной группой динамика уменьшения общемозговых и менингеальных симптомов. Эти различия наиболее выражены у тяжелых больных. Назначение Гистохрома приводит к достоверному снижению спонтанной и индуцированной на адреналин агрегации тромбоцитов, скорости агрегации и размера агрегатов, уровня фибриногена и наиболее выражено у больных, поступающих в состоянии средней тяжести и в тяжелом состоянии. 22 Выводы 1. При геморрагическом инсульте наблюдаются сложные патофизиологические процессы, включающие развитие перифокального отёка, микроциркуляторные нарушения, ишемические изменения и воспалительную реакцию. Эти изменения имеют определенную временную последовательность и максимально выражены по периферии гематомы, однако в отдельных случаях указанные выше изменения преходящего характера могут наблюдаться и в отдалённых участках головного мозга. 2. Отёк при экспериментальном геморрагическом инсульте по данным высокопольного МРТ (7,0 Тесла) и гистологического исследования выявляется уже через 6 часов после кровоизлияния, достигает своего максимума через 12-24 часа и начинает уменьшаться к 2 суткам. С 3-4 суток отмечается повторное нарастание отёка, что вероятно связано с развитием воспалительной реакции вследствие инфильтрации перифокальной зоны активированными нейтрофилами, гемолиза эритроцитов и усилением окислительного стресса. 3. Микроциркуляторные нарушения при геморрагическом инсульте в первые 12-24 часа характеризуются спазмом артериол с последующим (через 48-72 часа) паретическим расширением капилляров, артериол и венул. В области, окружающей гематому, выявляются изменения эндотелия и некротизация стенок сосудов, что сопровождается значительным повышением сосудистой проницаемости и развитием вторичных диапедезных кровоизлияний, которые наиболее часто развиваются на 2-3 сутки заболевания. 4. При экспериментальном геморрагическом инсульте в области, окружающей гематому, выявляются признаки ишемического повреждения нейронов и глии. Эти изменения могут носить необратимый характер и наблюдаются уже через 6-12 часов после кровоизлияния, достигая максимальной выраженности к 2-3 суткам. Кроме того, преходящие ишемические повреждения нейронов и глии могут развиваться в областях мозга, удалённых от кровоизлияния. 23 5. При экспериментальном геморрагическом инсульте в зоне, окружающей гематому, развивается воспалительная реакция. Скопления сегментоядерных клеток в периферических участках гематомы отмечаются уже с первых часов кровоизлияния, а к 48-72 часам наблюдается выраженная нейтрофильная инфильтрация. Наиболее значительные скопления нейтрофилов выявляются в зонах с ишемическим повреждением мозговой ткани. Лимфоцитарная инфильтрация достигает максимума через 7-10 дней. 6. При экспериментальном геморрагическом инсульте Гистохром проникает через гематоэнцефалический барьер и обнаруживается в цереброспинальной жидкости. Применение Гистохрома при экспериментальном геморрагическом инсульте сопровождается опережающим по сравнению с контрольными животными уменьшением неврологических симптомов и поведенческих нарушений, что обусловлено более быстрым регрессом перифокального отёка, менее выраженными микроциркуляторными нарушениями и ишемическим повреждением мозга. 7. У больных с геморрагическим инсультом сочетанный анализ в динамике тяжести состояния по шкале ком Глазго, выраженности неврологических симптомов по Скандинавской шкале инсульта, объёмов гематомы, перифокального отека и внутрижелудочкового кровоизлияния и выраженности смещения срединных структур головного мозга позволяет прогнозировать исход заболевания и степень функционального восстановления по шкале Бартель и оптимизировать терапию и реабилитационные мероприятия. 8. При геморрагическом инсульте отмечаются изменения спонтанной и индуцированной на адреналин агрегации тромбоцитов и уровня фибриногена. У более чем ½ больных наблюдается повышение индуцированной (на адреналин) агрегации тромбоцитов, скорости агрегации, увеличение размера тромбоцитарных агрегатов. В остальных случаях индуцированная на адреналин агрегация не изменена или снижена. Спонтанная агрегация в большинстве случаев остается в пределах нормы. Наиболее выраженные изменения выявляются у больных, поступавших в крайне тяжелом состоянии. Отмечена 24 корреляционная связь между объёмом внутрижелудочкового кровоизлияния, объёмом отёка и агрегацией тромбоцитов на адреналин. 9. У больных с геморрагическим инсультом Гистохром после внутривенного введения проникает через гематоэнцефалический барьер и обнаруживается в цереброспинальной жидкости в неизмененном виде и виде продуктов его метаболизма. Назначение Гистохрома больным с геморрагическим инсультом благоприятно влияет на динамику заболевания, при этом положительный эффект препарата в первую очередь обусловлен опережающим по сравнению с контрольной группой уменьшением общемозговой и менингеальной симптоматики. У больных, получавших Гистохром, прирост суммарного клинического балла по Скандинавской шкале инсульта был достоверно выше на 3 и 7 сутки заболевания по сравнению с контрольной группой. Наиболее выраженный эффект Гистохрома наблюдался у больных, поступавших в тяжелом состоянии. 10. Назначение Гистохрома сопровождается улучшением реологиче- ских свойств крови. После однократного внутривенного введения гистохрома у больных отмечалось достоверное снижение спонтанной и индуцированной на адреналин агрегации тромбоцитов, скорости агрегации и размера тромбоцитарных агрегатов, а также уровня фибриногена. Практические рекомендации 1. У больных с геморрагическим инсультом для прогнозирования течения и исхода заболевания целесообразно в динамике сочетано оценивать тяжесть состояния по шкале ком Глазго, по СШИ, объёмы гематомы, отека и внутрижелудочкового кровоизлияния и выраженность смещения срединных структур головного мозга. 2. У больных с геморрагическим инсультом для коррекции гемореологических нарушений и профилактики ишемических осложнений необходимо в динамике исследовать спонтанную и индуцированную агрегацию тромбоци- 25 тов и включать в комплексное лечение препараты, нормализующие реологические свойства крови. 3. В дифференцированной терапии геморрагического инсульта рекомендуется использовать препарат Гистохром, обладающий антиоксидантными и хелаторными свойствами, а также влияющий на реологические свойства крови, особенно у больных, поступающих в тяжелом состоянии. По материалам диссертации опубликованы печатные работы: 1. В.А. Стоник, Е.И. Гусев, М.Ю. Мартынов, М.Р. Гусева, И.А. Щукин, И.Г. Агафонова. Поиск препаратов для лечения геморрагического инсульта: применение МРТ для оценки эффективности гистохрома. Доклады Российской Академии наук 2005, том 405, с. 421-424. 2. М.Ю. Мартынов, И.А. Щукин, А.А. Никонова, И.Е. Сердюк. Терапия хронической сосудистой мозговой недостаточности. Справочник поликлинического врача. 2006, № 8, с. 71-76. 3. Е.В. Коплик, И.А. Щукин, И.Н. Боравков, М.Ю. Мартынов. Влияние острого эмоционального стресса на течение экспериментального геморрагического инсульта. Материалы 9 Всероссийского съезда неврологов. 2006 г с. 424. 4. Е.В. Коплик, И.А. Щукин, И.Н. Боравков, М.Ю. Мартынов. Течение экспериментального геморрагического инсульта на фоне предшествующего эмоционального стресса. Материалы Российского медицинского форума 2006, с. 78.