Химия - ЛСМ
реклама
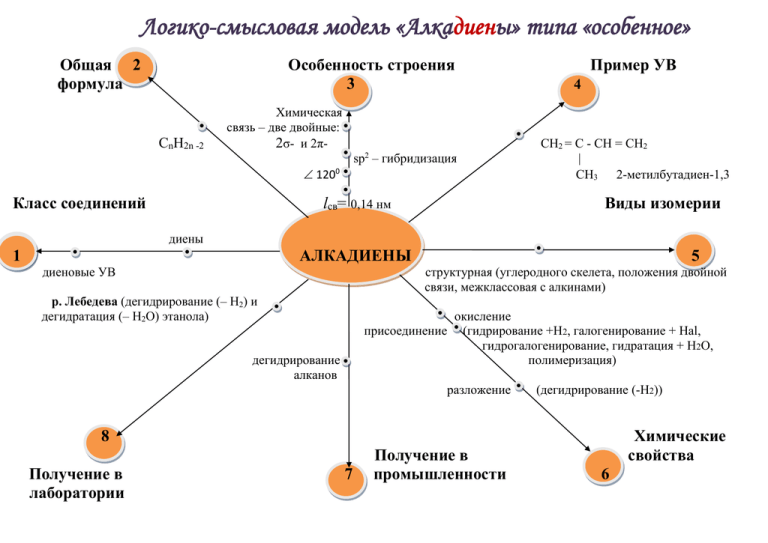
Логико-смысловая модель «Алкадиены» типа «особенное» Общая 2 формула Особенность строения 3 CnH2n -2 Химическая связь – две двойные: 2σ- и 2πsp – гибридизация 2 120 0 Класс соединений Пример УВ 4 СН2 = С - СН = СН2 | СН3 2-метилбутадиен-1,3 Виды изомерии lсв= 0,14 нм диены 1 АЛКАДИЕНЫ диеновые УВ 5 структурная (углеродного скелета, положения двойной связи, межклассовая с алкинами) р. Лебедева (дегидрирование (– Н2) и дегидратация (– Н2О) этанола) окисление присоединение (гидрирование +Н2, галогенирование + Hal, гидрогалогенирование, гидратация + Н2О, полимеризация) дегидрирование алканов разложение (дегидрирование (-Н2)) Химические свойства 8 Получение в лаборатории 7 Получение в промышленности 6 Логико-смысловая модель «Алканы» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 Химическая связь - одинарная σ СН3 – СН – СН - СН2 - СН3 | | CnH2n +2 sp – гибридизация 3 109028 Класс соединений СН3 С2Н5 2-метил-3-этилпентан Виды изомерии lсв= 0,154 нм предельные насыщенные АЛКАНЫ 1 алифатические парафины структурная: углеродного скелета гидрирование непредельных УВ гидролиз карбида алюминия окисление (полное - горение; неполное - каталитическое) из природного сырья замещение (галогенирование, нитрование, сульфирование) разложение (крекинг, дегидрирование) декарбоксилирование (р. Дюма) р. Вюрца с Na 5 из синтез-газа изомеризация (кат. AlCl3) Химические свойства 8 Получение в лаборатории 7 Получение в промышленности 6 Логико-смысловая модель «Алкены» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 Химическая связь – двойная: σ и π СН3 – С = СН - СН3 | CnH2n sp – гибридизация 2 1200 Класс соединений СН3 2-метилбутен-2 lсв= 0,134 нм Виды изомерии непредельные этиленовые пространственная (геометрическая) АЛКЕНЫ 1 ациклические 5 структурная (углеродного скелета, положения двойной связи, межклассовая с циклоалканами) дегидратация спиртов окисление (полное - горение; неполное – KMnO4 обесцв.) присоединение (гидрирование +Н2, галогенирование + Hal, гидрогалогенирование, гидратация + Н2О, полимеризация) дегидрогалогенирование галогеналканов крекинг (NaOH спиртовой) алканов дегалогенирование дегидрирование дигалогеналканов (Mg, Zn) алканов разложение (крекинг, дегидрирование (-Н2)) гидрирование алкинов 8 Получение в лаборатории 7 Получение в промышленности 6 Химические свойства Логико-смысловая модель «Алкины» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 Химическая связь – тройная:1σ и 2π CnH2n-2 sp – гибридизация 1800 Класс соединений СН3 – СН - С ≡ СН | СН3 3-метилбутен-1 lсв= 0,120 нм Виды изомерии непредельные ацетиленовые АЛКИНЫ 1 ациклические 5 структурная (углеродного скелета, положения тройной связи, межклассовая с алкадиенами) окисление (полное - горение; неполное – KMnO4 обесцв.) присоединение (гидрирование +Н2, галогенирование + Hal, гидрогалогенирование, гидратация + Н2О р. Кучерова, полимеризация) дегидрогалогенирование дигалогеналканов (NaOH спиртовой) дегидрирование алканов гидролиз карбида кальция (СаС2) замещение на краю цепи (Ag2О, NH3 . H2O) Химические свойства 8 Получение в лаборатории 7 Получение в промышленности 6 Логико-смысловая модель «Ароматические УВ» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 Химическая связь – σ и π, бензольное кольцо бензол CnH2n - 6 sp – гибридизация 2 1200 Класс соединений Виды изомерии lсв= 0,14 нм АРЕНЫ циклические ароматические УВ 1 структурная: углеродного скелета, боковой цепи сплавление солей бензойной кислоты со щелочами (декарбоксилирование) 5 окисление – горение присоединение (гидрирование, галогенирование) алкилирование по Фриделю-Крафтсу реакция Вюрца-Фиттига переработка нефти и газа тримеризация ацетилена замещение (галогенирование, нитрование, сульфирование, алкилирование (CH3Cl)) дегидрирование циклоалканов 8 Получение в лаборатории дегидроциклизация алканов 7 Получение в промышленности Химические 6 свойства Логико-смысловая модель «Спирты» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 R(ОH)2 химическая связь - одинарная σ R(OH)3 две или несколько ОН-гидроксогрупп окончание -ДИОЛ -ТРИОЛ С2Н4(ОН)2 этандиол (этиленгликоль)-яд! С3Н5(ОН)3 пропантриол (глицерин) Класс соединений Виды изомерии СПИРТЫ 1 предельные многоатомные 5 структурная: углеродного скелета, положения ОН-группы окисление глицерин: гидролиз жиров замещение (с щелочными металлами, с гидроксидом меди (II) при комнатной t) р. этерификации Получение 7 6 Химические свойства Логико-смысловая модель «Спирты» типа «особенное» Общая 2 формула Особенность строения 3 CnH2n + 1ОН CnH2n+2О R-OH Пример УВ 4 химическая связь - одинарная σ окончание -ОЛ ОН-гидроксогруппа (межмолекулярная водородная связь) СН3ОН метанол (метиловый) – ЯД! С2Н5ОН этанол (этиловый) Класс соединений Виды изомерии СПИРТЫ 1 предельные одноатомные гидратация алкенов гидролиз галогеналканов гидрирование альдегидов и кетонов метанол из синтез-газа этанол – брожение углеводов Получение 7 5 структурная: углеродного скелета, положения ОН-группы, межклассовая с простыми эфирами окисление (полное – горение, неполное – каталитическое) замещение (Н – кислотные свойства: активный металл, реакция этерификации с кислотами; ОН – гидрогалогенирование) отщепление (дегидрирование, дегидратация: внутримолекулярная, межмолекулярная) 6 Химические свойства Логико-смысловая модель «Фенолы» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 Ar - ОH химическая связь – σ и π Ar - (OH)2 одна или несколько ОН-гидроксогрупп окончание - ОЛ C6H5OH фенол Класс соединений Виды изомерии 1 ФЕНОЛЫ предельные многоатомные из каменноугольной смолы (фенолят + кислота) гидролиз хлорбензола сплавление солей аренсульфокислот со щелочами кумольный способ (окисление изопропилбензола) Получение 7 5 изомерия боковой цепи, положения заместителей в бензольном кольце кислотные свойства по ОН-группе (диссоциация индикатор, с металлами, щелочами, солями) по бензольному кольцу замещение галогенирование, нитрование, сульфирование) присоединение (гидрирование) поликонденсация (с метаналем с образованием фенолформальдегидной смолы) 6 Химические свойства Логико-смысловая модель «Циклоалканы» типа «особенное» Общая 2 формула Особенность строения 3 Пример УВ 4 Химическая связь - одинарная σ замкнутый цикл СН2 / \ CH2 – CH – CH3 метилциклопропан CnH2n sp – гибридизация 3 Класс соединений Виды изомерии насыщенные УВ 1 ЦИКЛОАЛКАНЫ алициклические структурная: углеродного скелета, межклассовая с алкенами 5 карбоциклические окисление (полное: горение) из ароматических (дегидрирование) из дигалогенпроизводных (взаимодействие с Na, Zn) замещение (С5 и т.д.) присоединение (С3 и С4) из нефти разложение изомеризация Химические свойства 8 Получение в лаборатории 7 Получение в промышленности 6