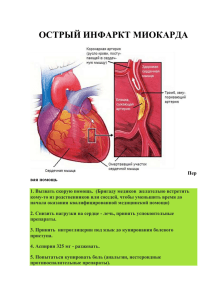
Основные побочные эффекты метотрексата
реклама

Цитостатические иммунодепрессивные препараты ЦИТОСТАТИЧЕСКИЕ ИММУНОДЕПРЕССИВНЫЕ ПРЕПАРАТЫ Цитостатические иммунодепрессанты (ЦИ) – группа препаратов, обладающая угнетающим влиянием на различные пролиферирующие клетки (цитостатическое действие), в том числе иммунокомпетентные (иммуносупрессивное действие). Иммуносупрессивное действие цитостатических препаратов стало основой их применения в ревматологии при аутоиммунных и иммунокомплексных заболеваниях. Универсальность цитостатического действия обеспечивает также неспецифический противовоспалительный эффект ЦИ. Этот эффект связан торможением пролиферации нелимфоидных клеток (моноциты, макрофаги, нейтрофилы, фибробласты) в очаге воспаления и воздействием на пролиферативную фазу воспаления. В ревматологии используются алкилирующие соединения (циклофосфамид, хлорамбуцил), нарушающие функционирование нуклеиновых кислот и белков путем алкилирования – введения в молекулу нестойких углеводородных остатков; и антиметаболиты (метотрексат, азатиоприн), являющиеся структурными аналогами естественных метаболитов (фолиевой кислоты – метотрексат и пуриновых оснований – азатиоприн). Все чаще при ревматических заболеваниях примененяется селективный иммунодепрессант циклоспорин А (ЦА), избирательно угнетающий активность Т-лимфоцитов, не относящийся к классу ЦИ. В основе лечения системных заболеваний соединительной ткани лежит противовоспалительная и иммуносупрессивная терапия часто с сочетанным применением ГКС и цитостатических иммунодепрессантов. Основаниями для сочетанного применения этих классов препаратов являются следующие соображения – ГКС и цитостатики имеют разные точки приложения при подавлении иммунного воспаления: ГКС преимущественно подавляют Th1, а цитостатики Th2 иммунные реакции и, таким образом, действуют на разные звенья патогенеза воспаления, кроме того, комбинированное 233 Цитостатические иммунодепрессивные препараты применение ГКС и цитостатиков позволяет снизить дозы того и другого препарата и уменьшить вероятность побочных эффектов. Показаниями для назначения ЦИ являются: тяжелое течение ревматического заболевания, сопряженное с неблагоприятным прогнозом (при условии потенциальной обратимости поражений), неэффективность стандартного лечения (в частности стероидорезистентность), стероидозависимость и побочные эффекты терапии ГКС, вызывающие необходимость снизить дозу или отменить ГКС. Особое место среди показаний занимают поражение ЦНС, легких и почек, прогрессирование которых не удается купировать монотерапией ГКС. Поражение почек особенно опасно при быстропрогрессирующем течении нефрита, развитии нефротического синдрома (при СКВ, системных васкулитах, ревматоидном артрите и др.) в связи с опасностью осложнений (нефротический криз, гематологический криз, развитие ДВС-синдрома, почечной недостаточности). При лечении ревматоидного артрита в качестве базисного препарата первого ряда назначается метотрексат. ЦИ чаще назначают в сочетании с ГКС, что позволяет уменьшить дозы обоих классов препаратов. Ограничивают применение ЦИ развитие осложнений, в основном связанных с универсальностью цитостатического действия (действует на все быстро пролиферирующие клетки), и, прежде всего, на клетки кроветворных органов, клетки репродуктивной системы, эпителий кишечника. Наиболее серьезными осложнениями алкилирующих ЦИ является угнетение костного мозга, токсическое действие на репродуктивную систему и развитие инфекций (бактериальных, грибковых, вирусных, в том числе и оппортунистических), может активизировать скрыто протекающие инфекции. Антиметаболиты вызывают депрессию костного мозга в меньшей степени, менее всего – метотрексат. Алкилирующие ЦИ действуют на репродуктивную функцию и мужчин и женщин, но в разной степени. Циклофосфамид менее токсичен у мужчин, чем хлорамбуцил, у женщин можно применять хлорамбуцил, так как яичники менее чувствительны к его действию. Побочные эффекты хлорамбуцила такие же, что и у циклофосфамида, за исключением действия на мочевой пузырь, но выраженность их меньше и они реже развиваются. Однако в 234 Цитостатические иммунодепрессивные препараты связи с более высоким риском онкологических заболеваний и гонадотоксичностью хроламбуцил применяется реже. Комбинированное применение ЦИ с ГКС уменьшает угнетающее влияние на костный мозг, но повышают восприимчивость к инфекциям. В ревматологии используются небольшие дозы ЦИ, которые реже вызывают выраженные побочные эффекты. Циклоспорин А не вызывает побочных эффектов, свойственных алкилирующим цитостатикам и антиметаболитам в связи со способностью избирательно угнетать функции Тлимфоцитов. Циклоспорин А не угнетает костный мозг, не способствует развитию инфекций, не угнетает функцию репродуктивных органов, обладает минимальной тератогенностью и онкогенностью. Однако его применение ограничивают развитие нефропатии (часто бессимптомной), связанной с вазоконстрикцией приносящих артериол клубочка и снижением почечного кровотока и артериальной гипертензии (часто бессимптомной). Несмотря на высокую клиническую эффективность ЦИ, возможность токсических эффектов делает необходимой серьезную оценку благоприятных и неблагоприятных последствий применения ЦИ. Угроза развития побочных эффектов и осложнений терапии ЦИ требует тщательного базового обследования больного для выявления предикторов риска побочных эффектов и осложнений терапии, а также определения исходного состояния органов и систем, вовлеченных в круг токсического действия ЦИ и для дальнейшего мониторирования их состояния и раннего выявления признаков токсического влияния препаратов. Как правило, угроза развития побочных эффектов или осложнений требует коррекции дозы или отмены препарата (временной или окончательной). Для преодоления токсического действия иммуносупрессивных препаратов имеются следующие направления: поиск нетоксичных или низкотоксичных иммуносупрессантов, поиск и синтез иммунотропных веществ с селективным действием (в этой связи особые надежды возлагаются на циклоспорин А) или усовершенствование методов применения имеющихся иммуносупрессивных препаратов с целью максимального повышения эффективности 235 Цитостатические иммунодепрессивные препараты и снижения побочных эффектов. Оба направления активно разрабатывается в настоящее время. Одним из методов, позволяющих уменьшить токсические эффекты циклофосфамида при сохранении его эффективности, явилось прерывистое в/в болюсное введение больших доз циклофосфамида 15-20 мг/кг (или меньших 0,5-2,5 мг/кг) в виде «пульсов» аналогично пульс-терапии ГКС. В зависимости от показаний такие «пульсы» проводятся ежемесячно или 1 раз в 3 месяца, иногда 1 раз в неделю. Доза циклофосфамида в «пульсах» также меняется в зависимости от показаний. Такой способ введения циклофосфамида превосходит по эффективности и безопасности пероральный прием, обеспечивает более быстрый клинический эффект, ассоциирован с уменьшением частоты осложнений со стороны мочевого пузыря и репродуктивных органов. Кроме того, пульс-терапия циклофосфамидом позволяет назначать его длительное время, в отличие от перорального приема, при котором курс лечения не должен превышать 12 недель в связи с высоким риском осложнений Boumpas D.T. et al., (1993). Поэтому Cameron J.S. (1999) рекомендует при волчаночном нефрите индукцию ремиссии проводить «пульсами» циклофосфамида, а для поддержания ремиссии использовать менее токсичный азатиприн. При проведении пульс-терапии циклофосфамидом лейкопения обычно возникает на 7-14 сутки после начала лечения. Для контроля лейкопении общий анализ крови в фазе индукции иммуносупрессии следует проводить через день. Дозу препарата регулируют таким образом, чтобы уровень лейкоцитов был не ниже 2 г/л. Через 3 недели уровень лейкоцитов обычно нормализуется. При ежедневном приеме циклофосфамида общий анализ крови следует проводить 1 раз в 2 недели, поддерживая количество лейкоцитов на уровне 3 г/л. Внутривенное введение циклофосфамида эффективно при СКВ (волчаночном нефрите, васкулите, поражении ЦНС, тромбоцитопении и легочных поражениях); в случае прогрессирующего интерстициального легочного фиброза при ССД и воспалительных миопатиях; при генерализованных формах узелкового полиартериита с быстропрогрессирующим поражением почек или неблагоприятным прогнозом. Ежедневно циклофосфамид назначается при тяжелом течении РА в случае 236 Цитостатические иммунодепрессивные препараты неэффективности других препаратов или наличии васкулита; при гранулематозе Вегенера с тяжелым поражением жизненно важных органов; при микроскопическом полиангиите; Для уменьшения токсических реакций при применении циклоспорина А необходимо проводить следующие мероприятия: не назначать дозу более 5 мг/кг в сутки, во время лечения контролировать концентрацию сывороточного креатинина, и не допускать ее повышения более 30% от исходного; во время лечения циклоспорином А не назначать потенциально нефротоксичные препараты и препараты, влияющие на его биодоступность. О клинической эффективности ЦИ судят по регрессу клинических проявлений болезни, уменьшению активности процесса, торможению прогрессирования заболевания (особенно поражения почек, легких и ЦНС), отсутствию обострений, прекращению стероидозависимости. Циклофосфамид (циклофосфан, эндоксан, цитоксан) Циклофосфамид (Ц) относится к алкилирующим цитостатикам. Механизм действия Ц связан с нарушением функций ДНК и РНК, путем алкилирования (введение в молекулы нестойких углеводородных остатков), что блокирует деление клеток, а при значительной степени алкилирования приводит к ее гибели. Алкилирующие цитостатики действуют не только на активно делящиеся клетки, но и на клетки, находящиеся в покое. Однако преимущественное влияние они оказывают все же на пролифилирующие клетки. При применении в ревматологии в основном – на иммуннокомпетентные клетки. Наиболее чувствительны к действию Ц лимфоциты, преимущественно В-лимфоциты. Действие Ц приводит к Т- и В-лимфопении с преимущественной элиминацией В-лимфоцитов; подавлению антигенстимулированной бласттрансформации лимфоцитов; торможению синтеза антител и гипогаммаглобулинемии; подавлению функциональной активности В-лимфоцитов in vitro. В конечном счете, подавляются гуморальные и клеточные иммунные реакции. 237 Цитостатические иммунодепрессивные препараты Ц хорошо абсорбируется из ЖКТ, биодоступность его при этом составляет 75%. При в/в введении биодоступность составляет 90%. Связавается с белками плазмы на 12-14%. Метаболизируется в печени, подвергаясь окислению (в основном под действием цитохрома Р-450) и превращаясь в активные метаболиты фосфорамид и акролеин. Эти метаболиты и определяют цитостатические и иммуннодепрессивные качества Ц. Максимальная концентрация метаболитов после в/в введения достигается через 2-3 часа, но быстро уменьшается в течение первых суток. Концентрация Ц и активных метаболитов в тканях после перорального приема не отличается от таковой после в/в введения. Период полувыведения при в/в введении составляет 5-7 часов; Ц выводится почками и с желчью. При выведении с мочой до 60% Ц выводится в виде метаболитов, что определяет один из основных побочных эффектов Ц – развитие геморрагического цистита; до 25% Ц выводится в неизменном виде. Показания при ревматических заболеваниях: системная красная волчанка, системные васкулиты, ревматоидный артрит, системная склеродермия, полимиозит/дематомиозит, синдром Шегрена; Противопоказания: Гиперчувствительность Гипоплазии костного мозга Гемоцитопении Сопутствующая инфекция Выраженная кахексия Терминальные стадии онкологических заболеваний Беременность Лактация Назначать с осторожностью при тяжелых заболеваниях печени, почек, тяжелых заболеваниях органов кровообращения. Способ применения: При лечении диффузных заболеваний соединительной ткани (системных васкулитов, СКВ и др.) начальная суточная доза обычно составляет 1-2,5 мг/кг в сутки, внутрь. В составе комбинированной терапии назначается внутривенно в дозе 10-15 мг/кг или 1-1,5 г/м² поверхности тела. При введении в виде «пульсов» применяют дозы до 10-15 мг/кг. Кратность и доза введений зависит от тяжести проявлений и 238 Цитостатические иммунодепрессивные препараты прогноза заболевания. При поддерживающей терапии используются меньшие дозы 200-400 мг/нед. Побочные эффекты Ц дозозависимы, и при дозах, используемых в ревматологии, встречаются реже и выражены меньше, они часто исчезают при уменьшении дозы Ц. Для эффективного контроля за наиболее опасными токсическими эффектами Ц необходимо проведение соответствующих мероприятий. Динамическое исследование общего анализа крови позволит предотвратить клинически значимые гемоцитопении и контролировать иммуносупрессию; исследование общего анализа мочи – осложнения со стороны мочевого пузыря. Для профилактики цистита применяются методы, направленные на уменьшение времени контакта токсических метаболитов со стенкой мочевого пузыря, уменьшение их концентрации, усиление выведения и связывание токсических метаболитов. Основные побочные эффекты циклофосфамида Система органов Проявления Система Гемоцитопении: кроветворе лейкопения, ния нейтропения, тромбоцитопения, Тяжелое угнетение функции костного мозга встречается редко; Возможно учащение интеркуррентных инфекций на фоне цитопений (в том числе грибковые инфекции и опоясывающий лишай); Система Хронический цистит мочевыде- (выявляется у 50% при ления ежедневном приеме, особенно опасно развитие геморрагического цистита*, рака мочевого пузыря**; Мониторинг, профилактика Информирование пациента о возможных побочных реакциях и их симптомах; В начале лечения: общий анализ крови количество тромбоцитов и общий анализ мочи; трансаминазы; креатинин; В динамике: регулярное наблюдение за больным; Общий анализ крови и общий анализ мочи в период индукции ремиссии (или при увеличении дозы) через день, в период поддерживающей терапии – 1 раз в неделю; При длительном лечении – 1 раз в 12 месяца; Для предупреждения геморрагического цистита рекомендуется: однократный прием всей дозы утром с большим к-вом жидкости; обильное питье (2-3 л/сут); частое опорожнение мочевого пузыря; 239 Цитостатические иммунодепрессивные препараты Система органов Репродукт ивная система ЖКТ Кожа Прочие Проявления Мониторинг, профилактика Дисменорея; Реже бесплодие у женщин и азооспермия у мужчин; Тошнота, рвота, диарея, анорексия, токсический гепатит, реже холестатический гепатит, гипертрансфераземия; Реже стоматит; Реакции в виде кожной сыпи (уртикарная, пятнисто-папулезная) реже алопеция; Более высокий риск онкологических заболеваний (особенно лейкозов и лимфом), возможно развитие опухолей через длительное время после прекращения лечения**; Осалгии, миалгии; Головная боль; При пульс-терапии Ц использование уромитексан (месна)*** по 240 мг/м² поверхности тела до введения Ц, через 4 и 8 часов после введения; При признаках геморрагического цистита (гематурия) провести цистоскопию, временно отменить препарат или снизить дозу; При лейкопении ниже 3 г/л и/или нейтропении ниже 1,5 г/л или тромбоцитопении ниже 100 г/л Ц отменить; Пациентам детородного возраста рекомендовать надежную контрацепцию; *причина – один из активных метаболитов акролеин; **случаи переходно-клеточного рака регистрируются через 17 лет после отмены Ц, в этой связи некоторые авторы рекомендуют осуществлять наблюдение за больными, получавшими Ц в течение всей жизни, в частности, проводить общий и цитологический анализ мочи каждые 3-6 месяцев после прекращения лечения Ц (Radis C.D. et al., 1995; Talar-Williams C. Et al., 1996) ***связывает акролеин в мочевом пузыре; 240 Цитостатические иммунодепрессивные препараты Азатиоприн (имуран) Аналог гипоксантина, относится к группе антиметаболитов, действует цитостатически. В организме трансформируется в собственно атиметаболит 6-меркаптопурин, который, встраиваясь в молекулы ДНК и РНК вместо 6-тиогуанина (естественного метаболита), нарушает их репликацию. Антиметаболитное действие А развивает преимущественно в фазу синтеза (S-фаза) клеточного цикла. Мишенью для А являются активно делящиеся клетки. При использовании в ревматологии, А тормозит пролиферацию иммунокомпетентных клеток, в первую очередь в макрофагов и лимфоцитов (в большей степени Т-лимфоцитов, опосредованно В-лимфоцитов), при длительном применении угнетает синтез антител. Возможно, в реализации клинического эффекта при ревматических заболеваниях имеет значение и другие механизмы действия, в частности - противовоспалительный. А хорошо абсорбируется в ЖКТ. В крови связывается с белками на 30%. Метаболизируется в печени с образованием активного антиметаболита 6-меркаптопурина. Период полувыведения 6-меркаптопурина составляет 0,7-3 часа. А выводится почками, в основном в виде метаболита. Показания в ревматологии: ревматоидный артрит, системная красная волчанка, системные васкулиты. При одновременном назначении с аллопуринолом необходимо уменьшить дозу А на 25%. Аллопуринол, угнетая активность ксантиноксидазы, способствует повышению концентрации 6-меркаптопурина и увеличивает вероятность развития побочных реакций. Способ применения: начинают с суточной дозы 2-2,5 мг/кг, чаще всего 150 мг/сут 2-4 приема. Максимальная суточная доза 300 мг/сут. Первые признаки клинического эффекта регистрируются на 4-й – 6-й неделе лечения. При сохранении клинического эффекта и хорошей переносимости в течение 3-4 месяцев, дозу А можно снизить до поддерживающей: 100-75-5025 мг/сут. Если поддерживающие дозы недостаточны для поддержания ремиссии, их рекомендуется вновь увеличить. При отсутствии эффекта в течение 3 месяцев А следует отменить. 241 Цитостатические иммунодепрессивные препараты Побочные эффекты такие же, как и у всех цитостатиков. Становятся причиной отмены препарата у 20-30% больных. Большинство побочных эффектов дозозависимы и купируются после отмены препарата. Противопоказания: гиперчувствительность, беременность (однако, имеются данные об отсутствии патологии у ребенка и матери при применении А в первом триместре беременности). Осторожность требуется при назначении больным с заболеваниями печени и больным с почечной недостаточностью. Основные побочные эффекты азатиоприна Система органов Система кроветворения Кожа Др. аллергические реакции ЖКТ Репродук тивная система Прочие Проявления Мониторинг Гемоцитопении (в той или иной степени наблюдаются у 50% больных): лейкопения, тромбоцитопения, анемия (возможны с мегалобластным типом эритропоэза, гемолитическая); Тяжелое угнетение функции костного мозга встречается редко; Возможно учащение интеркуррентных инфекций на фоне цитопений (в том числе грибковые инфекции и опоясывающий лишай); Аллергические реакции в виде кожной сыпи, реже алопеция; Лекарственная лихорадка, артериальная гипотония, артралгии, миалгии; Информирование пациента о возможных побочных реакциях и их симптомах; В начале лечения: общий анализ крови количество тромбоцитов и общий анализ мочи; трансаминазы; креатинин; В динамике: регулярное наблюдение за больным; Общий анализ крови и общий анализ мочи 1 раз в неделю (или при увеличении дозы), при длительном лечении – 1 раз в 1-2 месяца При лейкопении ниже 4 г/л и/или нейтропении ниже 2 г/л или тромбоцитопении ниже 150 г/л Ц отменить; Тошнота, рвота, гастралгии, диарея, анорексия, холестатический гепатит, гипертрансфераземия; Реже стоматит; Дисменорея; В единичных случаях развитие острой почечной недостаточности, острых заболеваний легких, менингиты; Более высокий риск онкологических заболеваний;* *при применении после трансплантации органов частота лимфопролиферативных заболеваний выше, при использовании в ревматологии онкогенный риск точно не установлен; 242 Цитостатические иммунодепрессивные препараты Эффективность А при РА доказана в контролируемых исследованиях. Его клинический эффект сопоставим с эффектом основных базисных препаратов, в первую очередь метотрексата и солей золота. По лечебному действию азатиоприн подобен метотрексату, но выраженность положительного эффекта при его применении меньше, а переносимость хуже. Метотрексат (М). По структуре подобен фолиевой кислоте. Относится к классу антиметаболитов (вещества, приводящие к повреждению и гибели соответствующих клеток, благодаря конкуренции с естественными метаболитами). Являясь антагонистом фолиевой кислоты, свое цитостатическое действие М развивает в фазу синтеза клеточного цикла (S-фаза), приводя к угнетению дигидрофолатредуктазы и нарушая синтез пуриновых нуклеотидов и, соответственно, синтез ДНК. Токсические эффекты М также связаны с его антифолатным действием. В настоящее время эффект М при РА объясняют не столько иммунносупрессивным сколько противовоспалительным действием. В клетке М подвергается полиглютаминированию с образованием биологически активных метаболитов. Установлено, что эти метаболиты, в отличие от М, реализуют свое действие не только посредством ингибирования дигидрофолатредуктазы, но и других «фолатзависимых» ферментов. Глютаминированные производные ингибируют ряд ферментов, в частности тимидилатсинтетазу и 5-амио-имидазол4-карбоксамидорибонуклеотид (АИКАР). Этим объясняется эффективность малых доз М, недостаточных для полного подавления дигидрофолатредуктазы. Накопление АИКАР в клетке приводит к высвобождению аденозина, проявляющего антивоспалительную активность. Таким образом, М в малых дозах можно рассматривать не как антипролиферативный (иммуносупрессивный), а как противовоспалительный препарат. М назначается внутрь и парентерально. М быстро всасывается из пищеварительного тракта примерно на 50%. Максимальная концентрация в крови после перорального приема определяется через 1 час. 50% М связываются с белками крови. Метаболизируется в печени, частично – флорой кишечника, при этом подвергается полиглютамилированию с образованием фармакологически активных метаболитов. В 243 Цитостатические иммунодепрессивные препараты тканях М распределяется неравномерно. Его концентрация в синовиальной оболочке и кости приблизительно в 10 раз больше, чем в плазме. При экссудативном перикардите, плеврите или асците М долго сохраняет свою концентрацию в полостях и оттуда постепенно проникает в кровь. В тканях почек М обнаруживается в течение нескольких недель, в тканях печени – несколько месяцев. При пероральном приеме период полувыведения составляет 9-10 часов, при в/м введении – около 3 часов и при в/в введении – около 24 часов. 50-80% М выделяются с мочой в неизменном виде. Около 10% выводятся с желчью с последующей реабсорбцией в кишечнике. Показания для применения М в ревматологии: ревматоидный артрит (препарат первого выбора БТ); болезнь Стилла у взрослых; ювенильный артрит; полимиозит/дерматомиозит; синдром Шегрена; серонегативные спондилоартропатии; псориатический артрит; системная красная волчанка; системные васкулиты; системная склеродермия; Противопоказания для назначения М: гиперчувствительность, беременность, лактация, выраженные гемоцитопении, лейкоз с геморрагическим синдромом, выраженная почечная недостаточность (скорость клубочковой фильтрации менее 50 мл/мин), выраженная печеночная недостаточность, алкогольный гепатит, вирусные гепатиты В и С, инфекционные заболевания (особенно ветряная оспа, в том числе недавно перенесенная, опясывающий лишай), иммунодефицит (в том числе СПИД), язвенная болезнь желудка и двенадцатиперстной кишки, язвенный колит. М следует применять с осторожностью у пожилых больных, при обезвоживании, язвенном колите, пептических язвах, подагре или наличии уратных камней, умеренных почечной или печеночной недостаточности, при плеврите, асците, при умеренной супрессии кроветворения, после проводившейся ранее химиотерапии или лучевой терапии. 244 Цитостатические иммунодепрессивные препараты Способ применения: М для уменьшения побочных эффектов назначают после еды (всасывание М при этом уменьшается, особенно при употреблении молочной пищи). М назначается 3 раза через 12 часов 1 раз в неделю в дозе 7,5-20 мг/нед. Такой режим приема объясняется тем, что в период между первым и третьим приемом большинство иммунокомпетентных клеток входят в фазу синтеза. Эффект терапии М наступает через 3-5 недель. При лечении РА вначале уменьшаются артралгии, утренняя скованность, лихорадка, слабость. Затем отмечается уменьшение экссудативных явлений в суставах, лабораторных показателей воспалительной активности, висцеральных проявлений РА. Длительное (в течение лет) применение М приводит к уменьшению прогрессирования эрозий (у некоторых больных даже их регресс). Обычно лечение начинают с 7,5 мг/нед. (у пожилых больных 5 мг/нед.), при неэффективности через 2 месяца дозу М увеличивают на 2,5 мг/нед. каждые 1,5-2 месяца до дозы 15-20 мг/нед. (при этом возможно нарастание побочных реакций). Оценку токсичности проводят через неделю после приема препарата или повышения дозы. При раннем выявлении большинство побочных реакций обратимо. В случае выявления побочных реакций следует уменьшить дозу М или отменить его в зависимости от клинической значимости побочного эффекта. При лечении псориатического артрита обычно эффективна доза 7,5 мг/сут. Имеются сообщения об использовании М для внутрисуставного введения. Назначение метотрексата при других ревматических заболеваниях осуществляется по принципам, изложенным выше. Основные побочные эффекты метотрексата, мониторинг, профилактика*, лечение Побочный Мониторинг, Лечение эффект профилактика Анорексия, тошнота, рвота, гастралгии Диарея Стоматит, язвы ротовой полости Информирование пациента о Уменьшить дозу или возможных побочных реакциях отменить М (временно или и их симптомах; полностью) Информирование пациента о Отменить М из-за высокого возможных побочных реакциях риска развития геморрагичес и их симптомах; кого энтерита и перфорации Информирование пациента о Отменить М возможных побочных реакциях Назначить фолиевую и их симптомах; кислоту в дозе 5-50 мг/сут 245 Цитостатические иммунодепрессивные препараты Побочный эффект Мониторинг, профилактика Головная боль, головокружения Повышение трансаминаз, гепатит, цирроз печени Информирование пациента о возможных побочных реакциях и их симптомах; Анамнез: алкоголизм, контакт с гепатотоксичными веществами, сахарный диабет, избыточный вес, пожилой возраст, гепатит в анамнезе, положительные маркеры ВГ В и С, персистирующая гипераспартаттрансфераземия (более 50%, при определении в течение года) гипоальбуминемия, псориаз повышают гепатотоксичность М, перед назначением рекомендуется выполнить биопсию печени; При исходном нормальном уровне трансаминаз – контроль каждые 3 месяца. Исследовать уровень альбумина каждые 6 недель. Хроническая гепатотоксичность развивается через 2 года приема или достижении кумулятивной дозы 1,5 г Общий анализ крови вначале лечения через день, в течение первого месяца раз в 5 дней, затем раз в неделю; при достижении стойкого улучшения - ежемесячно Общий анализ крови, тромбоциты вначале лечения через день, в течение первого месяца раз в 5 дней, затем раз в неделю; при достижении стойкого улучшения - ежемесячно Информирование пациента о возможных побочных реакциях и их симптомах; Информирование пациента о возможных побочных реакциях и их симптомах; Лейкопения** Тромбоцитопе ния**, анемия** Вторичные инфекции Кожные аллергические реакции, фотосенсибилизация, депигментация 246 Лечение Уменьшить дозу или отменить М (временно или полностью) Отменить М при двукратном повышении активности трансаминаз или ЩФ; При необъяснимой гипоальбуминемии М отменить; Отменить М при лейкопении менее 4 г/л или нейтропении менее 2 г/л Назначить фолиевую кислоту в дозе 5-50 мг/сут Отменить М при тромбоцитопении менее 150 г/л Назначить фолиевую кислоту в дозе 5-50 мг/сут Временная отмена Цитостатические иммунодепрессивные препараты Побочный эффект Мониторинг, профилактика Алопеция Информирование пациента о возможных побочных реакциях и их симптомах; Пневмонит (бронхиолит) – регистрируется редко; интерстициаль ный легочной фиброз (единичные сообщения) Нефротоксичность Лечение Рентгенография грудной клетки до Отмена М. начала лечения. Побочные эффекты со Вызванная М легочная стороны легких могут возникать при токсичность может любой дозе М, даже при дозе 7,5 быть не полностью мг/нед. О вероятности легочных обратимой осложнений следует думать при Для лечения появлении на фоне лечения М любых применить легочных симп-томов. Следует соответствующие дозы исключить другие причины легочной ГКС симптоматики, прежде всего инфекции. У больных группы риска (больные с почечной недостаточностью) не применять либо не превышать дозу 5 мг/нед. Больным со снижением скорости клубочковой фильтрации ниже 50 мл/мин назначение М противопоказано. Пожилым больным, принимающим НПВП, назначать М в дозе не более 5мг/нед. Больным с нормальной функцией почек исследовать креатинин 2 раза в году. * частоту многих побочных эффектов (связанных с дефицитом фолатов: стоматит, гемоцитопении) можно уменьшить при назначении фолиевой кислоты в дозе 5-50 мг/сут (или фолината кальция – может использоваться как антидот при токсических реакциях на М); усиление токсического действия М возможно при одновременном приеме с НПВП (снижается выделение метотрексата почками); Не рекомендуется сочетать высокие дозы М с приемом НПВП, если необходим прием НПВП, назначать препараты короткого действия; ** для предупреждения гемоцитопений не назначать одновременно с М лекарственные средства с антифолатным действием (триметоприм/сульфаметоксазол); Дозы М, используемые в ревматологии гораздо меньше, чем дозы, используемые с цитотоксическими целями, поэтому побочные эффекты при его применении встречаются реже, а выраженность их меньше. По соотношению эффективность / токсичность М превосходит другие базисные препараты. Не рекомендуется применение доз более 25 мг/нед. Если при применении М его эффективность недостаточна, возможно его комбинированное назначение с другим «базисным» препаратом. 247 Цитостатические иммунодепрессивные препараты Хлорамбуцил (хлорбутин, лейкеран) Алкилирующий цитостатический препарат, оказывающий свое действие без биотрансформации в печени (в отличие от циклофосфамида, который в печени трансформируется в активные метаболиты, определяющие его фармакологическую активность). Прямое влияние Х на ДНК приводит к нарушению репликации и трансляции ДНК и к гибели клетки. В терапевтических концентрациях больше действует на лимфоидную ткань, чем на гранулоциты, тромбоциты, эритроциты. Х полностью абсорбируется из ЖКТ, связывается с белками крови на 99%, метоболизируется в печени с образованием фармакологически активного метаболита – фенилуксусного иприта. Период полувыведения - 1,5 часа, фенилуксусного иприта – 2,5 часа. Показания в ревматологии: Ревматоидный артрит; Системная красная волчанка; Системные васкулиты; Полимиозит/дерматомиозит; Болезнь Бехчета; Противопоказания: Гиперчувствительность к хлорамбуцилу и другим алкилирующим препаратам; Назначать с осторожностью при: Предшествующих лучевой и цитостатической терапии (назначать не ранее, чем через 1,5-2 месяца после окончания предшествующей терапии); Тяжелой патологии печени и почек (нарушение метаболизма Х в печени и усиление токсичности; усиление миелосупрессии при почечной недостаточности); Острой патологии ЖКТ; Гипоплазии костного мозга, гемоцитопении; Беременность, лактация; Сопутствующая инфекция; Выраженная кахексия; Терминальные стадии онкологических заболеваний; Способ применения: Обычно назначается 15-20 мг/сут. 248 Цитостатические иммунодепрессивные препараты Основные побочные эффекты хлорамбуцила Система органов ЖКТ Аллергические реакции Система мочевыделения Система кроветворения Репродуктивная система Прочие Проявления Тошнота, рвота, диарея, анорексия, токсический гепатит, холестатический гепатит, гипертрансфераземия; Язвенный стоматит; Кожная сыпь, мультиформная эритема, синдром СтивенсаДжонсона, синдром Лайелла; лихорадка; Гиперурикемия и гиперурикемическая нефропатия; Асептический цистит; Гемоцитопении (обратимы при своевременном прекращении лечения): лейкопения, нейтропения, лимфопения; тромбоцитопения, снижение уровня гемоглобина; Возможно учащение интеркуррентных инфекций на фоне цитопений (в том числе грибковые инфекции и опоясывающий лишай); Дисменорея, аменорея; Азооспермия; Более высокий риск онкологических заболеваний, зависит от длительности приема и суммарной дозы (особенно острый миелолейкоз). Мониторинг, профилактика Информирование пациента о возможных побочных реакциях и их симптомах; В начале лечения: общий анализ крови количество тромбоцитов и общий анализ мочи; трансаминазы; креатинин, уровень мочевой кислоты; В динамике: регулярное наблюдение за больным; Общий анализ крови и общий анализ мочи в период индукции ремиссии 1 раз в неделю (или при увеличении дозы), в период поддерживающей терапии – 1 раз в 1-2 недели. При длительном лечении – 1 раз в 1-2 месяца. При лейкопении ниже 4 г/л и/или нейтропении ниже 2 г/л или тромбоцитопении ниже 150 г/л Х отменить; При развитии тяжелых аллергических реакций Х отменить; Для предупреждения гиперурикемии рекомендуется обильное питье, при гиперурикемии – препараты, влияющие на рН мочи, аллопуринол; Пациентам детородного возраста рекомендовать надежную контрацепцию; 249 Цитостатические иммунодепрессивные препараты Циклоспорин А (сандиммун, циклоспорин, имуспорин, неорал*) Циклический полипептид, выделенный из грибков Tolypocladium inflatum и Cylindrocarpon lucididum. Циклоспорин А (ЦА) отличается от цитостатических иммунодепрессантов тем, что иммунодепрессивное действие у ЦА не сочетается цитотоксической активностью. ЦА не влияет на метаболизм клеток, не угнетает костный мозг и не влияет на функции фагоцитов. Тем самым не вызывает характерных для цитостатических иммунодепрессантов осложнений: гемоцитопений, инфекций, увеличения риска канцерогенеза. Механизм действия ЦА до конца не выяснен. Его связывают с избирательным торможением функций Тлимфоцитов. ЦА связывается с цитоплазматическим рецепторным белком 17 Kda циклофилон, образующийся комплекс циклоспорин-циклофилин конкурентно связывается и ингибирует кальциневрин, что приводит к подавлению транскрипции «ранних» генов цитокинов, прежде всего ИЛ-2 и ИФН, а также ИЛ-3, ИЛ-4, ИЛ-6, СD40L, ГМ-КСФ, ФНО- и угнетению Т-клеточных иммунных реакций, которые участвуют в реализации острого и хронического воспаления при РА. Некоторые авторы считают, что ЦА блокирует действие простагландина Е2 и ИЛ-1, ИЛ-3, которые ответственны за деструкцию костной ткани при РА. По воздействию на цитокины ЦА подобен ГКС и эта особенность ЦА способствует их синергизму. Именно селективная иммуносупрессивная активность ЦА делает его перспективным для применения в ревматологии. Показания в ревматологии: ревматоидный артрит (тяжелое течение, резистентное к лечению другими препаратами БТ, при плохой переносимости стандартных базисных препаратов или наличии противопоказаний к их применению). Противопоказания: Гиперчувствительность (в том числе к полиоксиэтилированному касторовому маслу); Тяжелое нарушение функции почек; Артериальная гипертензия; Злокачественные новообразования; Назначать с осторожностью одновременно с лекарственными средствами, увеличивающими токсичность (особенно нефротоксичность) ЦА. 250 Цитостатические иммунодепрессивные препараты Способ применения: Внутрь по 75-500 мг/сут; Внутривенно капельно по 150-350 мг/сут. При лечении СКВ ЦА эффективен при волчаночном нефрите (показан при нефротическом синдроме, связанным с мембранозным волчаночным нефритом), тромбоцитопении или панцитопении. При волчаночном нефрите способствует трансформации нефротического синдрома в мочевой. В настоящее время имеются доказательные данные о достаточной эффективности и хорошей переносимости терапии ЦА. Переносимость терапии ЦА при назначении суточных доз ниже 3 мг/кг, достаточно высокая, однако и при таких дозировках регистрируются побочные эффекты. *Неорал микроэмульсионная форма ЦА для приема внутрь в обычных для ЦА дозах, но с более полным и быстрым всасыванием и большей биодоступностью, максимальная концентрация в крови при его применении выше и достигается быстрее, фармакокинетика неорала более предсказуема; Основные побочные эффекты циклоспорина А Система органов Проявления Органы Артериальная кровообраще гипертензия (часто ния бессимптомная) встречается в 2050% случаев; Мониторинг, профилактика, лечение В начале лечения: установить исходный уровень АД, контроль АД каждые 2 недели в первые 3 месяца лечения, затем – каждые 4 недели; При развитии артериальной гипертензии – антигипертензивная терапия, которая как правило хорошо контролирует АД (препараты выбора дигидроперидиновые производные, не влияющие на фармакокмнетику ЦА); У больных, страдающих артериальной гипертензией этот побочный эффект регистрируется чаще; Артериальное давление нормализуется после снижения дозы, отмены ЦА и под влиянием антигипертензивной терапии. 251 Цитостатические иммунодепрессивные препараты Система органов Проявления Почки (нефротоксичность зависит от дозы)* Нефропатия, часто бессимптомная (иногда с морфологическими изменениями в клубочках и канальцах: интерстициальный фиброз с атрофией канальцев и повреждением артериол); Гематурия; Аллергические реакции Кожная сыпь; развитие анафилаксии вплоть до шока (реакция на полиоксиэтилированное касторовое масло, входящее в состав р-ра для инфузий); Нервная система и органы чувств Головная боль; Головокружения; Эпилептический синдром; Парестезии; Гиперестезии; Миастения/миопати я; Энцефалопатия; Нарушение зрения; Нарушение сознания; 252 Мониторинг, профилактика, лечение В начале лечения: до лечения установить исходный уровень креатинина по результатам не менее чем двух измерений; Общий анализ мочи; В процессе лечения исследовать уровень креатинина каждые 2 недели в первые 3 месяца лечения, затем – каждые 4 недели; При повышении уровня креатинина, более чем на 30%, суточную дозу ЦА снизить на 1 мг/кг**; Исследовать уровень креатинина через месяц; При сохранении уровня креатинина на 30% выше исходного – прекратить лечение ЦА; при возвращении к исходному значению, или увеличении не более 10% от базового уровня – продолжить лечение уменьшенной дозой. В большинстве случаев после отмены ЦА функция почек восстанавливается, как правило, обратимы и морфологические изменения. У части больных стойкие морфологические изменения сохраняются. Тщательный аллергологический анамнез; Методика в/в инфузии: концентрат развести в соотношении 1:20-1:100 физиологическим р-ром хлорида натрия или 5% р-ра декстрозы и вводить в течение 2-6 часов; Мониторинг симптомов анафилаксии во время инфузии; Информирование пациента о возможных побочных реакциях и их симптомах; Регулярное наблюдение за больным; Цитостатические иммунодепрессивные препараты Система органов Проявления ЖКТ Тошнота, рвота, диарея, анорексия, токсический гепатит; Обмен веществ Гиперлипидемия; Гиперкалиемия; Гипомагниемия; Гиперплазия десен с их кровоточивостью; Увеличение массы тела; Дисменорея/аменорея; Прочие Мониторинг, профилактика, лечение Информирование пациента о возможных побочных реакциях и их симптомах; Регулярное наблюдение за больным; *основным фактором риска считают применение высоких доз препарата, малые дозы ЦА (2,5-3 мг/кг в сутки) практически не вызывают угнетения функции почек и обладают хорошей клинической эффективностью, однако при лечении ЦА целесообразно контролировать концентрацию ЦА в крови, токсические реакции минимальны при концентрации ЦА в крови менее 500 мг/мл; ** во время лечения ЦА повышение уровня креатинина менее чем на 30% от базового ассоциировано с минимальным риском необратимого поражения почек, дозу ЦА нужно снижать до достижения уровня креатинина не выше, чем 30% от базового; 253