Химия - Schools.by
реклама

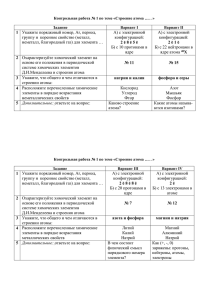
Олимпиадные задания по химия 7 класс Часть А. Тест. 1.Химический символ N соответствует элементу: а)натрий б)неон в)накель г)азот 2.В каком случае речь идет о химическом явлении? а)измельчение сахара в пудру б)плавление железного лома в)почернение на воздухе изделий из серебра г)сжижжение воздуха для получения кислорода. 3.Укажите химическую формулу сульфида алюминия: а)AlS б)Al2S в)AlS3 г) Al2 S3. 4.Из приведенных реакций выберите реакцию(-и) замещения: 1)NaCl + AgNO3 = AgCl + NaNO3 2) AgNO3 + Fe = Fe(NO3) + 2Ag 3)Cu(OH)2 + 2HCl = CuCl2 + 2H2O 4)CuO + H2 = Cu + H2O а) 2 б) 4 в) 2,4 г) 3,4. 5.Укажите количество вещества хлорида кальция массой 1,11г : а) 0,15 моль б) 0,10 моль в) 0,015 моль г) 0,01 моль. 6.В каком из оксидов массовая доля кислорода наибольшая? а) N2O5 б) N2O3 в) P2O5 г) P2O3. 7.Основным компонентом воздуха (по объему) является: а) кислород б) азот в) оксид углерода (IV) г) инертные газы. 8.Выберите способы очистки воды от растворимых примесей: 1) отстаивание а) 1,2 б) 2,3 2) перегонка в) 3,4 3) фильтрование 4) вымораживание г) 2,4 9.С соляной кислотой реагируют: а) Na2SO4 б) H2SiO3 в) LiOH г) CO2 10.Дана смесь веществ: песок, вода, соль, бумажные опилки. Опишите последовательность выделения всех компонентов этой смеси. Олимпиадные задания Химия 9 класс Часть А. Тест. 1.Только названия веществ написаны в ряду: а) иней, вода, цинк; б) стекло, медь, магний; в) вода, кремний, алюминий; г) дерево, целлюлоза, сталь. 2.Химическая формула соединения кальция с азотом (III): а) CaN б) Ca2N3 в) Ca3N г) Ca3N2. 3.Укажите уравнения реакции замещения: 1)CaCO3 = CaO + CO2 2)Mg + H2SO4 = MgSO4 + H2 3)HCl + NaOH = NaCl + H2O 4)3ZnO + 2Al = Al2O3 + 3Zn. а) 1,3 б) 2,4 в) 1,4 г) 3,4 4.В ряду N ⟶ O ⟶ F ⟶ Ne радиус атома: а) увеличивается б) увеличивается, а затем уменьшается в) уменьшается г) уменьшается, а затем увеличивается. 5.Сколько протонов в ядре атома с электронной конфигурацией …3S2 а) 4 б) 11 в) 12 г) 20. 6.Какие реакции ионного обмена протекают до конца: 1) HCl + AgNO3 = AgCl + HNO3 2)NaCl + KOH = KCl + NaOH 3) BaCl2 + H2SO4 = BaSO4 + 2HCl 4) HNO3 + KCl = HCl + KNO3 а) 2 б) 1,3 в) 1,2,3 г) 3,4 7.Укажите аллотропные модификации углерода 1) алмаз 2) графит 3) карбид 4) карбин а) 1,4 б) 2,3 в) 1,2,4 г) 3,4. 8.Из перечисленных веществ укажите число кислотных оксидов: N2O5, CO2, Cr2O3, Mn2O7, CaO, ZnO, Cl2O5 а) 5 б) 3 в) 1 г) 4. 9.В трех одинаковых сосудах содержится Н2, О2, СО2. Наибольшее число молекул содержится в сосуде: а) с водородом б) с кислородом в) с оксидом углерода (IV) г) количество молекул одинаковое. 10.В следующей схеме Mg ⟶ A ⟶ Mg(OH)2 ⟶ MgCl2 буквой «А» зашифровано: а) MgO б) MgSO4 в) H2O г) O2. Олимпиадные задания 10 класс Тест А А1. Нуклиды, имеющие, одинаковый атомный номер, но различное массовое число, называют: 1) 2) 3) 4) изотопами; аллотропными модификациями; молекулами; ионам. А2. Охарактеризуйте ковалентную связь: а) образуется при связывании атомов неметаллов; б) возникает при образовании общих электронных пар; в) общие электронные пары смещены к более электроотрицательному элементу; г) бывает полярной и неполярной: 1) 2) 3) 4) а, б, в; а, б, в, г; б, в; а, б, г. А3. Одновременно в водном растворе в значительных количествах способны находиться ионы: 1) 2) 3) 4) Na+, H+, NO3-, S2-; Na+, F-, Cl-, H+; H+, Cl-, NO3-, Ba2+; Cu2+, NO3-, OH-, K+. A4. Гидроксид металла состава Ме(ОН)2 является продуктом реакции, схема которой: 1) 2) 3) 4) Ca+H2O; Li2O+H2O; KHCO3 + KOH; CaCO3 + H2O; А5. Атомы всех неметаллов в основном состоянии: 1) 2) 3) 4) Содержит неспаренные электроны; На внешнем электронном слое содержит более трех электронов; Имеют меньше энегргии, чем в возбужденном состоянии; Имеют меньший радиус, чем соответствующие катионы. А6. Укажите формулы соответственно веществ X, Y и Z для цепочки превращений CuCl2 ___x___ Cu ___y___ CuSo4 ___z___ CuS: 1) 2) 3) 4) Na, H2SO4 (конц.), K2S; Zn, H2SO4 (разб.), Na2S; Fe, H2SO4 (конц), H2S; K, H2SO4 (конц.), K2S. Тест В В1. Рассчитайте объем 12,04*10 молекул фтора. В2. При восстановлении оксида металла Ме2О3 массой 160 г получили металл и воду массой 54 г. Укажите относительную атомную массу данного металла. В3. Сколько 4%-го раствора азотной кислоты (в граммах) можно приготовить из 400 г 15%-го ее раствора. В4. Газы, полученные при термическом разложении 27,25 г смеси нитратов натрия и меди (2), пропустили через 115,2 мл воды. При этом 1,12 л газа (н.у.) не поглотилось. Определите массовую долю нитрата в исходной смеси Олимпиадные задания 11 класс 1. Первым металлом, который человек научился выплавлять, был: а) олово; б) железо; в) медь; г) золото. 2. Смель глины и воды можно разделить методом: а) выпаривания; б) фильтрования; в) отстаивания; г) перегонки. 3. Неверным относительно воздуха является утверждение: а) массовая доля азота равна 78%; б) содержит примерно пятую часть кислорода; в) основной компонент – азот; г) содержит аргон. 4. Три атома входят в состав формульной еденицы: а) воды; б) мела; в) соды; г) кварца. 5. В образце сульфата алюминия массой 3,42 г содержатся атомы кислорода химическим количеством: а) 120 моль; б) 1,92 моль; в) 0,01 моль; г) 0,12 моль. 6. В каком случае речь идет о кремнии, как о простом веществе: а) кварц содержит кремний; б) из кремния изготавливают интегральные схемы; в) в природе широко распрастранены соединения кремния; г) радиус кремния отличается от радиуса углерода. 7. Укажите пару веществ, в одинаковой массе которых содержится одинаковое число атомов водорода: а) Cu(OH)2 и H2SO4; б) H2SO4 и H2CO3; в) H3PO и H3PO4; г) H2SO4 и H2O. 8. С какими веществами реагирует калий-оксид? а) Cu(OH)2; б) H2SO4; в) H2O; г) K2SO4. 9. В растворах каких веществ фенолфталеин малиновый? а) кислот; б) воде; в) щелочей; г) солей. 10. С какими веществами реагирует серная кислота? а) Li; б) CaO; в) HCl; г)Au. Задача 1. При нагревании 1,225 г вещества получены О2 и 0,745 г КСl. Установите формулу вещества, приведите необходимые расчеты. Задача 2. Цинк массой 13 г сплавили с серой массой 3,2 г без доступа кислорода. Продукт реакции растворили в избытке раствора соляной кислоты. Определите химической количество и объем выделившихся газов. Задача 3. Составьте цепочку превращений: Металл – основной оксид – основание – соль Укажите тип химической реакции в каждом превращении.