Арцукевич И.М. ПРЕДСКАЗАНИЕ ЭФФЕКТИВНОГО
реклама

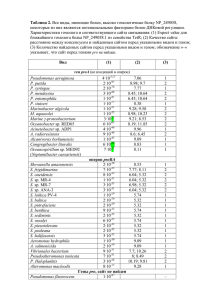
УДК 579.222 И.М. Арцукевич, О.Б. Цехан ПРЕДСКАЗАНИЕ ЭФФЕКТИВНОГО МИКРОСООБЩЕСТВА ДЛЯ БИОДЕГРАДАЦИИ МЕТАНОЛА И ФОРМАЛЬДЕГИДА В СТОЧНЫХ ВОДАХ Предлагается новый прогностический метод формирования микробиологического сообщества для биодеградации загрязнений. Этот подход основывается на знании кинетических скоростей индивидуальных этапов и на идентификации узких ветвей биохимической трансформации химических загрязнителей. Для того чтобы предотвратить аккумуляцию промежуточных метаболитов, предложено использовать совместно две культуры микроорганизмов, дополняющих друг друга с точки зрения оптимального течения деградации токсических веществ. Их использование предотвращает аккумулирование промежуточных соединений. Математическая модель, выстроенная на примере биодеградации двух часто сопутствующих друг другу токсических соединений – метанола и формальдегида – с использованием микроорганизмов: бактерии Pseudomonas putida и культуры дрожжей Candida boidinii, подтверждает эффективность предложенного подхода. Ключевые микроорганизмы слова: Pseudomonas putida, Candida boidinii, сточные воды, формальдегид, метанол, Разработанный и запатентованный нами способ очистки сточных вод, образующихся в процессе синтеза карбамидных смол на предприятиях по производству древесностружечных плит, позволяет эффективно, с низкой энергоемкостью очистить сточные воды от формальдегида и метанола [1]. После двухэтапной обработки стоков концентрации формальдегида и метанола в кубовом остатке удовлетворяют условиям сброса его в городской коллектор. Однако в ряде случаев существуют требования более высокой очистки сточных вод, причем, в виду низких остаточных концентраций метанола и формальдегида ее рационально проводить микробиологическим способом [2]. Особенно это актуально в отношении формальдегида, т.к. известна его канцерогенная активность в отношении микробных клеток и клеток животных [3]. Существует группа метилотрофных дрожжей, к которым относится культура Candida boidinii, использующих в качестве источника углерода и энергии метанол. Общая схема выглядит следующим образом: CH3OH → HCOH → HCOOH → CO2 +H2O При этом первый этап протекает согласно механизму: CH3OH + О2 → HCOH + H2О2 Основываясь на полученных нами данных по деградации метанола и далее формальдегида культурой Candida boidinii, в том числе и в иммобилизованном состоянии [4], нами был сделан вывод, что процесс превращения метанола в углекислый газ и воду имеет узкое звено. Накопление промежуточного продукта – муравьиной кислоты – тормозит весь процесс в целом. Схематически это можно представить следующим образом: CH3OH → HCOH ───> HCOOH → CO2 +H2O Этот факт является препятствием широкомасштабного использования монокультуры Candida boidinii для очистки сточных вод, предложенного Подгорским [5]. В то же время в природе существуют метилотрофы, использующие в качестве единственного источника углерода и энергии не метанол, а формальдегид – Pseudomonas putida. Они широко распространены в различных водоемах и представляют собой грамотрицательные палочкообразные бактерии, катализирующие превращение НСОН в метанол и муравьиную кислоту, используя крайне высоко активный фермент формальдегиддисмутазу [6]. Формальдегид при мягких условиях рН в окислительно- 2 восстановительной реакции превращается в метанол и муравьиную кислоту, которые в дальнейшем метаболизируются до углекислого газа и воды: 2НСОН +Н2О → CH3OH + HCOOH→ CO2 +H2O Сотрудники университета г.Барселоны провели исследование по механизму биодеградации формальдегида культурой бактерии Pseudomonas putida F61 (коллекции микроорганизмов г.Абердин, Шотландия). Изучалась кинетика исчезновения и образования метаболитов CH3OH и HCOOH. Полученные результаты, а особенно высокая скорость дисмутазной реакции, позволили им высказать предположение о возможности использования этой культуры для очистки от формальдегида формальдегидсодержащих сточных вод [7]. Биохимическая трансформация поллютантов чистыми микробиологическими культурами в лабораторных условиях описана достаточно подробно. Однако в реальных условиях окружающей среды метаболизм загрязнителей реализуется, как правило, микробиологическими сообществами. Такая биологическая целесообразность участия групп микроорганизмов в биодеградации загрязнителей – увеличение эффективности процесса в целом. Из данных, представленных графически в цитируемой статье, мы рассчитали среднюю скорость исчезновения метаболитов. Эти данные, как и результаты, полученные нами с культурой Candida boidinii KD 1(из коллекции Тартуского университета, Эстония), суммированы в табл.1. Таблица 1. Средняя скорость исчезновения метаболитов, рассчитанная из данных, представленных в [7]. Культура Реакция Candida boidinii CH3OH → НСОН Средняя скорость мг/мин. на 1г клеток 1.15 Candida boidinii НСОН → HCOOH 0.3 Pseudomonas putida НСОН → 0.5CH3OH + 0.5HCOOH 166.7 Pseudomonas putida CH3OH-исчезновение 0.5 Pseudomonas putida HCOOH-исчезновение 4.2 Принимая во внимание очень высокую начальную скорость биодеградации формальдегида, действительно, очень заманчиво применить культуру Pseudomonas putida для очистки формальдегидсодержащих сточных вод. С другой стороны, однако, относительно низкая скорость исчезновения метанола, образующегося из формальдегида, может ингибировать весь процесс биодеградации. В этой связи мы предложили использовать две культуры – Candida boidinii и Pseudomonas putida – совместно для очистки сточных вод, содержащих или формальдегид или смесь формальдегида с метанолом. Последний вариант соответствует случаю стоков трех белорусских предприятий (ОАО «Мостодрев», ЗАО «Пинскдрев», ОАО «Мозырьдрев») [8]. Имея общие метаболиты, эти культуры, возможно, могут крайне гармонично дополнять друг друга. При очень высокой скорости деградации НСОН Pseudomonas putida – эта скорость низкая у Candida boidinii. В то же время, более высокая скорость деградации метанола Candida boidinii и – низкая скорость этого процесса у Pseudomonas putida. На основе величин скоростей индивидуальных реакций сконструирована логическая схема, отображающая преимущественную циркуляцию метаболитов (рисунок1): 2 3 Н2О Н2О Рисунок 1. Преимущественная циркуляция метаболитов в присутствии двух видов микроорганизмов: Pseudomonas putida и Candida boidinii Нами построена математическая модель, помогающая выработать стратегию «разгрузки», преодоления «узких мест», возникающих при биодеградации смеси двух токсических веществ, часто сопутствующих друг другу в сточных водах: формальдегида и метанола. В результате анализа построенных математических моделей установлено, что поглощение этих соединений и их дальнейшая утилизация в присутствии обоих линий происходит гораздо быстрее, чем если в системе присутствует только одна культура Pseudomonas putida. Сравним динамику процесса биодеградации формальдегида и метанола в присутствии одной культуры Pseudomonas putida и в присутствии обоих линий. Для сравнения скоростей деградации метаболитов в двух указанных условиях построим математические модели процессов в виде дифференциальных уравнений 1-го порядка. Будем использовать следующие обозначения: f – формальдегид; me – метанол; С f (t ) – концентрация формальдегида в стоках в момент времени t ; Сme (t ) – концентрация метанола в стоках в момент времени t ; f С me – концентрация формальдегида, полученного из метанола; С me f – концентрация метанола, полученного из формальдегида; T f me – время превращения единицы формальдегида в метанол культурой Pseudomonas putida; Tme f – время превращения единицы метанола в формальдегид культурой Candida boidinii; Tme – время деградации единицы метанола культурой Pseudomonas putida. Основываясь на значениях величин средних скоростей реакций (таблица 1), мы сделали следующие предположения: 1. в стоках присутствуют и метанол и формальдегид; 2. T f me << Tme f ; 3. T f me << Tme ; 4. Tme f < Tme ; 5. при использовании двух культур метаболиты циркулируют согласно схеме (рисунок 1); 6. время исчезновения муравьиной кислоты в среде не принимается во внимание, так как эта стадия не ограничивает весь процесс. I. Рассмотрим процесс деградации формальдегида и метанола культурой Pseudomonas putida. Структурную схему этого процесса можно представить в виде (рисунок 2): 3 4 НСОН 0.5 CH3OH + 0.5HCOOH Pseudomonas putida ↓ Pseudomonas putida Pseudomonas putida исчезновение из среды CH3OH Рисунок 2. Схема утилизации формальдегида культурой Pseudomonas putida. В соответствии с этой схемой, с учетом предположения 6, упрощенно процесс деградации формальдегида и метанола можно рассматривать в виде двух последовательных стадий элементарных реакций, в результате которых с течением времени изменяются концентрации метаболитов: В соответствии с этой схемой с учетом предположения 6 упрощенно процесс деградации формальдегида и метанола можно рассматривать в виде двух последовательных стадий элементарных реакций, в результате которых с течением времени изменяются концентрации метаболитов: T f me Tme me С f (t ) Сme (t ) 0.5C f (t ) Cme (t ) В силу предположения 3 будем считать процесс 1-ой стадии исчезновение мгновенным, поэтому me C me f (0) 0.5C f (0) . На второй стадии скорость изменения концентрации метанола C f (t ) можно описать дифференциальным уравнением C me d me f (t ) C f (t ) . dt Tme Для получения уравнения кинетической кривой проинтегрируем полученное уравнение. t dC me f (t ) me 0 C f (t ) t dt ; 0 Tme Отсюда: me ln C me f (t ) ln C f (0) ln C me f (t ) C me f (0) t ; Tme t . Tme В итоге с учетом C me f (0) 0.5C f (0) получаем функцию, отражающую процесс изменения концентрации метанола, полученного из формальдегида C me f (t ) 0.5C f (0)e t Tme . (Ia) Аналогично для метанола имеем Cme (t ) Cme (0)e t Tme . (Ib) Заметим, что экспоненциальная зависимость концентрации от времени (как в Ia, Ib) характерна для большинства химических реакций. II. Пусть теперь в процессе деградации участвуют два типа бактерий – Candida boidinii и Pseudomonas putida. Этот процесс упрощенно можно представить как серию большого количества 4 5 элементарных циклов. Структурная схема одного цикла процесса, протекающего за время Tme , имеет вид (рисунок 3): НСОН putida Pseudomona s 0.5 CH3OH + 0.5HCOOH ↓ Candida boidinii CH3OH один цикл boidinii Candida НСОН … Рисунок 3. Схема утилизации формальдегида культурами Pseudomonas putida и Candida boidinii. На первом этапе цикла пренебрегаем «медленным» процессом преобразования формальдегида в метанол культурой Candida boidinii. На втором этапе учитываем, что процесс преобразования формальдегида в метанол тормозится в связи с ингибированием продуктом реакции – метанолом. Поэтому относительно второго этапа цикла считаем, что временно происходит только накопление формальдегида. Заметим, что в результате каждого такого цикла концентрация формальдегида уменьшается как минимум вдвое. Динамика изменения концентрации формальдегида и метанола в результате указанных циклов отражается схемой (для сокращения записей зависимость функций от t не отражается): T T me f f me me С f ( t ) Сme ( t ) 0.5C f Cme 1-ый цикл 0.5C f T T f me f me f Cme 0.25C me 0 . 5 C me f 2-ой цикл T f me f me 0.25C f 0.5Cme 0.125 C f 0.25Cme ... 3-ий цикл Процесс, изображенный на схеме, понимаем следующим образом. Пусть имеется смесь одной единицы формальдегида и одной единицы метанола. Очень быстро (считаем, мгновенно) под действием Pseudomonas putida 1 единица формальдегида преобразуется в 0.5 единиц метанола, при этом 1 единица метанола не изменилась. Затем, под действием Candida boidinii происходит преобразование метанола в формальдегид (со средней скоростью T 1 me f ). При этом, так же, как и ранее, имеем уравнение кинетической кривой для концентрации метанола, полученного из формальдегида, на временном промежутке 0, Tme f 1 C me f (t ) 2 C f (0) e t Tme f , Откуда далее, согласно структурной схеме, на момент времени Tme f начала второго цикла Tme f , 2Tme f имеем 5 6 C me f (Tme f 2 ) 2 C f (0) e 1 t 1 Tme f C 2 (0) e f t Tme f . (2) t Tme f Далее, с учетом полученного начального условия (2), для второго цикла получаем уравнение кинетической кривой C me f (t ) 2 2 C f (0) e t Tme f , и на момент времени 2Tme f начала третьего цикла 2Tme f ,3Tme f имеем C me f (2Tme f 3 ) 2 C f (0) e 2 t 1 Tme f C 2 f (0) e t Tme f . t 2Tme f Обобщая полученные выше представления, получаем для t Tme f ; 2Tme f ; .......NTme f дискретных моментов времени уравнение динамики концентрации метанола, полученного из формальдегида C me f (t ) t 1 Tme f C 2 f (0) e t Tme f . (3a) Рассуждая аналогично, получаем уравнение динамики метанола Cme (t ) t T 2 me f t C (0) e Tme f me , t Tme f ; 2Tme f ; .......NTme f . (3b) Для сравнения качества деградации сравним концентрации метанола, полученного из формальдегида, по двум описанным схемам, например, на момент Tme f . Согласно данным таблицы 1 при 0.5 Tme f 1 1 1 , Tme с учетом 0.647405 e 1.15 2e 0.18394 имеем из (Ia) и (3a) 1.15 0.5 C me f (Tme f 1 ) 2 C f (0) e Tme f Tme 2 1 > C me f (Tme f ) 2 C f (0) e . Из (Ia) и (3a) легко видеть, что с течением времени разница между левой и правой частью последнего неравенства еще увеличивается. Это доказывает, что при использовании двух культур для обеззараживания стоков концентрация в среде метанола и формальдегида, действительно, уменьшается быстрее, чем при использовании одной культуры. Аналогичное неравенство получаем, также из (Iб) и (3б). Таким образом, математическая модель подтверждает большую эффективность микробиологического сообщества в разрушении токсических метаболитов НСОН- и CH3OHсодержащих сточных вод, чем при использовании одной культуры. СПИСОК ЛИТЕРАТУРЫ 6 7 1. Способ очистки сточных вод, содержащих формальдегид и метанол: пат.3278, C02F1/58, C02F1/04/ И.М. Арцукевич, Д.А. Опарин, И.Э Гуляй, И.И. Степуро, Л.Я. Пикуль; заявитель Институт биохимии НАН Беларуси. – №119, заявл. 29.01.93; опубл.30.03.2000 // Афiцыйны бюл. / Нац. цэнтр iнтэлектуал. уласнасцi. – 2000. – № 1. – С.152. 2. Способ микробиологической очистки сточных вод от метанола: пат.963960, С02F3/34/ М.Б. Цинберг, В.А. Швец, Б.М. Гальперин, А.Д. Денис, П.И. Гвоздяк, О.М. Севастьянов, В.Д. Шугорев и А.М. Эскин; заявитель Волго-Уральский научно-исследовательский и проектный институт по добыче и переработке сероводородсосержащих газов и Институт коллоидной химии воды АН Украины. - №2972030; заявл. 08.08.80; опубл. 07.10.82 // Открытия. Изобретения. – 1982. – №37. – С. 75. 3. Перечень веществ, продуктов, производственных процессов, бытовых и природных факторов, канцерогенных для человека: ГН 1.1.725-98:.утв. Постановлением Главного государственного санитарного врача Российской Федерации от 23 декабря 1998 г., № 32:текст по состоянию на 5 марта 2004 г. : ГН 1.2.1841-04. – Режим доступа: http://www.zodchii.ws/normdocs/info-335.html. – Дата доступа: 21.05.2012. 4. Artsukevich, I. Ostrovsky Ju. Methanol utilization using immobilized cells of methylotrophic yeast Candida boidinii: abstract / I.Artsukevich, Ju. Ostrovsky // 5-th European Congress. – Denmark, 1990. – P.266. 5. Podgorsky, V. The effect of medium mineralization on yeast growth and methanol consumption / V. Podgorsky, V.Ivanov, T. Kachur // Biotechnologija.– 1987. – №3. – Р. 481-483. 6. Kato, N. The Dismutation of Aldehydes by a Bacterial Enzymy / K.Shirakawa, H.Kobayashi, C.Sakazawa // Agric. Biol. Chem. – 1983. – №47 (1) .– Р. 39-46. 7. Adorer, N. Mechanism of formaldehyde biodegradation / N.Adorer, C. Casas, C. De Mas, C.Sola // Appl microb biotechnol. – 1990. – № 33.– Р. 217-220. 8.Арцукевич, И.М. Очистка сточных вод от метанола и формальдегида / И.М. Арцукевич, И.Э. Гуляй, В.В. Опекунов // Веснік ГрДУ імя Янкі Купалы. Сер. 5. Эканоміка. Сацыялогія. Біялогія.–2012 .– № 2(131) .– C.142-148. 7 8 УДК 579.222 Предлагается новый прогностический метод формирования микробиологического сообщества для биодеградации загрязнений. Этот подход основывается на знании кинетических скоростей индивидуальных этапов и на идентификации узких ветвей биохимической трансформации химических загрязнителей. Для того чтобы предотвратить аккумуляцию промежуточных метаболитов, предложено использовать совместно две культуры микроорганизмов, дополняющих друг друга с точки зрения оптимального течения деградации токсических веществ. Их использование предотвращает аккумулирование промежуточных соединений. Математическая модель, выстроенная на примере биодеградации двух часто сопутствующих друг другу токсических соединений – метанола и формальдегида – с использованием микроорганизмов: бактерии Pseudomonas putida и культуры дрожжей Candida boidinii, подтверждает эффективность предложенного подхода. Ключевые микроорганизмы слова: Pseudomonas putida, Candida boidinii, сточные воды, формальдегид, метанол, I.M.Artsukevich, V.B.Tsekhan PREDICTION OF THE EFFECTIVE MICROCOMMUNITY FOR BIODEGRADATION OF METHANOL AND FORMALDEHYDE FROM WASTEWATER We suggest a new prognostic approach of formation microbial community for pollution biodegradation. This approach based on the understanding of kinetic rates individual steps and identification of the narrow branches in biochemical transformation of chemical polluters. To prevent the accumulation of intermediate metabolite, we suggest to use two culture microorganisms which compliment each other. The above prevents the accumulation of intermediate metabolites. The mathematical model built on the example of biodegradation of the two tocsins – methanol and formaldehyde, usins Pseudomonas putida and Candida boidinii proves the efficacy of the suggested method. Key words: Pseudomonas putida, Candida boidinii, waste water, methanol, formaldehyde, microorganisms 8 9 Арцукевич Ирина Моисеевна, канд. биол. наук, доц. каф. строительного материаловедения УО «ГрГУ им.Я.Купалы». Гродно. Ул.Курчатова, 1-а. Тел 8029 889 73 59 МТС, e-mail: [email protected] Арцукевiч Iрына Маiсееуна, канд. бiял. навук, дацэнт каф. будайнiчага матэрыялазнаустства УА «ГрДУ iм.Я.Купалы. Гродна, вул.Курчатага, 1-а. тэл. 8029 889 73 59 МТС, e-mail: [email protected] Artsukevich Iryna Moiseevna PhD, associate professor of the constructional material science department of Yanka Kupala State University of Grodno, Kurchatov Str.,1-a Цехан Ольга Борисовна канд.физ-мат.наук, доцент, зам. декана факультета экономики и управления ГрГУ им. Я.Купалы, Гродно, ул.Горького, 95, к.402, 48–72–43 (сл.) Vel 16–314–48, [email protected] Tsekhan Volha PhD, senior lecture, Deputy of dean of Faculty of economics and management Yanka Kupala State University of Grodno Цэхан Вольга Барысаўна Арцукевич Ирина Моисеевна, канд. биол. наук, доц. каф. строительного материаловедения УО «ГрГУ им.Я.Купалы». Гродно. Ул.Курчатова, 1-а. Тел 8029 889 73 59 МТС, e-mail: [email protected] Арцукевiч Iрына Маiсееуна, канд. бiял. навук, дацэнт каф. будайнiчага матэрыялазнаустства УА «ГрДУ iм.Я.Купалы. Гродна, вул.Курчатага, 1-а. тэл. 8029 889 73 59 МТС, e-mail: [email protected] Artsukevich Iryna Moiseevna PhD, associate professor of the constructional material science department of Yanka Kupala State University of Grodno, Kurchatov Str.,1-a Цехан Ольга Борисовна канд.физ-мат.наук, доцент, зам. декана факультета экономики и управления ГрГУ им. Я.Купалы, Гродно, ул.Горького, 95, к.402, 48–72–43 (сл.) Vel 16–314–48, [email protected] Tsekhan Volha PhD, senior lecture, Deputy of dean of Faculty of economics and management Yanka Kupala State University of Grodno Цэхан Вольга Барысаўна 9 10 10