Календарно-тематическое планирование по химии 8 класс ( 70 часов, 2...
реклама
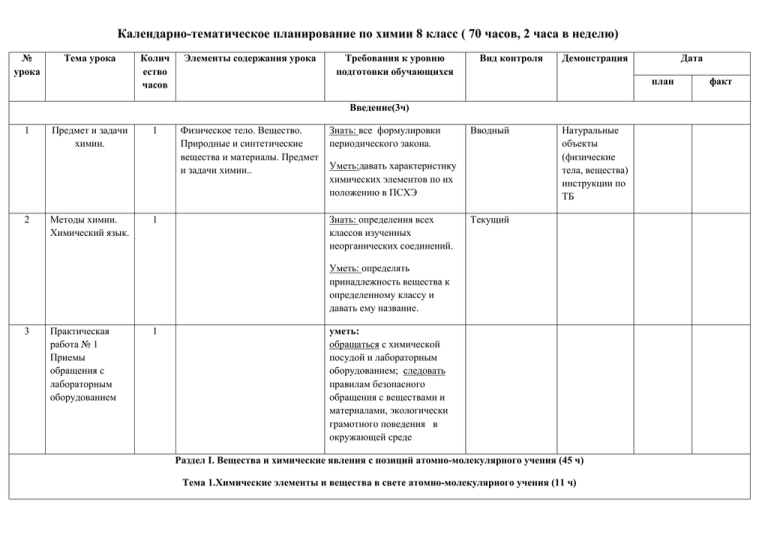
Календарно-тематическое планирование по химии 8 класс ( 70 часов, 2 часа в неделю) № урока Тема урока Колич ество часов Элементы содержания урока Требования к уровню подготовки обучающихся Вид контроля Демонстрация план Введение(3ч) 1 2 Предмет и задачи химии. Методы химии. Химический язык. 1 1 Физическое тело. Вещество. Природные и синтетические вещества и материалы. Предмет и задачи химии.. Знать: все формулировки периодического закона. Вводный Уметь:давать характеристику химических элементов по их положению в ПСХЭ Знать: определения всех классов изученных неорганических соединений. Натуральные объекты (физические тела, вещества) инструкции по ТБ Текущий Уметь: определять принадлежность вещества к определенному классу и давать ему название. 3 Практическая работа № 1 Приемы обращения с лабораторным оборудованием 1 Дата уметь: обращаться с химической посудой и лабораторным оборудованием; следовать правилам безопасного обращения с веществами и материалами, экологически грамотного поведения в окружающей среде Раздел I. Вещества и химические явления с позиций атомно-молекулярного учения (45 ч) Тема 1.Химические элементы и вещества в свете атомно-молекулярного учения (11 ч) факт Понятие «вещество» в физике и химии. Физические и химические явления. 1 Атомы, молекулы, химические элементы . Формы существования элементов в природе. 1 6 Состав веществ. Простые и сложные вещества. Закон постоянства состава веществ. 1 Химическое соединение. Простое вещество. Сложное вещество. Простые вещества: металлы и неметаллы. 7 Атомномолекулярное учение. 1 Молекула. Атом. 4 5 Вещество. Физические и химические явления. Признаки химических реакций. Обратимые и необратимые изменения. Текущий Физические и химические явления. Изучение свойств веществ: серы, железа, сахара, поваренной соли, воды Текущий Модели атомов и молекул. распознавать простые и сложные вещества; Текущий Коллекция металлов и неметаллов Знать основные положения атомно-молекулярного учения. Текущий Возгонка йода. Расширение воды при нагревании. Опыты по диффузии уметь: объяснять отличие физических явлений от химических; - называть признаки химических реакций; Молекула. Атом. Химический элемент. Изотоп. знать/понимать: - знаки химических элементов; - понятия: химический элемент, атом, молекула Относительная атомная молекулярная масса. Массовая доля элемента в соединении. 1 Масса атома. Атомная единица массы. Относительная атомная масса. Эталон. Знать относительные атомные массы элементов. 9 Решение задач 1 Относительная молекулярная масса. Истинная масса молекул. Массовая доля элемента. Уметь: производить расчеты по химическим формулам индивидуальный 10 Периодическая система химических элементов Д.И. Менделеева 1 Периодический закон. Система. Период. Группа. Главная и побочная подгруппы. Порядковый номер элемента. Знать - Периодический закон Д.И.Менделеева; Текущий Набор слайдов, таблиц «Периодическ ий закон и строение атома» 11,12 Валентность химических элементов 2 Валентность: постоянная, переменная Правило четностинечетности. Высшая валентность. Низшая валентность. определять валентность химических элементов в б составлять формулы бинарных соединений по валентности;инарных соединениях; Текущий Таблица «Валентность химических элементов» 13 Количество вещества моль. Молярная масса. 1 Количество вещества. Моль. Постоянная Авогадро. Знать и понимать понятие количество вещества. Моль Текущий 14 Решение задач. Расчеты по химическим формулам 1 8 Текущий вычислять относительную молекулярную массу веществ - изменение свойств элементов в периодах и группах П.С тематический Тема 2. Химические реакции. Закон сохранения массы и энергии. (7ч) Сущность химических реакций и признаки их протекания. Тепловой эффект реакции. 1 Закон сохранения массы и энергии 1 17 Уравнения химических реакций. 1 18 Решение задач: расчеты по химическим уравнениям. 1 15 16 Химическая реакция. Признаки протекания реакции. Экзотермические и эндотермические реакции. Тепловой эффект. Термохимическая реакция. уметь: Закон сохранения массы при химических реакциях. Взаимопревращение видов энергии. знать/понимать: Коэффициент. Индекс. составлять уравнения химических реакций различных типов (расставлять коэффициенты в уравнениях х.р.) Опыты, иллюстрирую щие превращения различных видов энергии друг в друга - называть признаки и условия осуществления химических реакций Текущий законы сохранения массы и энергии. Текущий Опыты, иллюстрирую щие закон сохранения массы вещества 19 Типы химических реакций 1 20 Обобщение знаний по темам 1-3 1 21 Контрольная работа № 1 1 Реакции соединения, разложения, обмена, замещения. определять типы химических реакций; Типы химических реакций: разложение малахита, взаимодействи е железа с раствором сульфата меди (II); нагревание медной проволоки;вза имодействие серной кислоты с нитратом бария; итоговый Тема 3. Методы химии (2ч) 22 Методы, связанные с изучением веществ. 1 Описание. Наблюдение. Эксперимент. Индикатор. Анализ. Синтез. 23 Химический язык. Химические термины. Понятие об индикаторах. 1 Индикаторы: фенолфталеин, метиловый оранжевый, лакмус Знать основные методы изучения химии. Текущий Тема 4Вещества в окружающей нас природе и технике (6ч) Чистые вещества и смеси. 1 25 Практическая работа № 2 Очистка веществ. 1 26 Растворы. Практическая работа № 3 Растворимость веществ. 1 Раствор. Растворимость. Ненасыщенный, насыщенный, пересыщенный растворы. Кривые растворимости. 27 Способы выражения концентрации растворов 1 Процентная концентрация. Массовая доля. Молярная концентрация. 28 Решение задач на растворы. 1 24 Чистое вещество. Гомогенные и гетерогенные смеси. Разделение смесей. Примеси. Идентификация. Перегонка. Хромотография. Знать: вводный отличие чистых веществ от смесей. Знать: основные способы очистки веществ Текущий Текущий Разделение смесей различными методами отстаивание, фильтрование, с помощью делительной воронки, методом хроматографии дистилляция. 29 Практическая работа № 4 Приготовление раствора заданной концентрации. уметь: 1 - вычислять массу воды и веществ в растворах с определенной массовой долей растворенного вещества Тема 5. Понятие о газах. Воздух. Кислород. Горение. (8ч) 30 Законы ГейЛюссака и Авогадро. 1 Законы Гей-Люссака и Авогадро 31 Решение задач. Расчеты на основании газовых законов. 1 32 Воздух-смесь газов. 1 Состав воздуха. Инертные газы. 33 Кислород химический элемент и простое вещество. Получение кислорода. 1 Химический элемент. Простое вещество. Термическое разложение. Катализатор. Каталитическая реакция. - вычислять объемы газов по известному количеству вещества одного из вступивших в реакцию или получающихся веществ. Текущий Уметь рассчитывать относительную плотность газов Текущий Знать состав воздуха Текущий 34 Практическая работа № 5 Получение кислорода и изучение его свойств. 1 следовать правилам получения и собирания кислорода; распознавать опытным путем кислород 35 Химические свойства и применение кислорода. 1 36 Обобщение знаний по темам 4,5 1 Текущий 37 Контрольная работа № 2 1 итоговый Оксиды. Окисление. Сжигание в атмосфере кислорода серы, угля, красного фосфора, железа; Опыты, подтверждающ ие состав воздуха; Опыты по воспламенени ю и горению Тема 6. Основные классы неорганических соединений (11ч) 38 Оксиды и их классификация. Понятие об амфотерности. 1 Кислотные, основные, амфотерные оксиды. Гидроксиды. знать/понимать:формулы химических веществ Рассмотрение образцов оксидов 39 Основаниягидроксиды основных оксидов. 1 Щелочи. Нерастворимые основания. Гидроксогруппы. знать/понимать:формулы химических веществ Текущий Рассмотрение образцов основании 40 Кислоты. 1 Кислоты. Кислотный остаток. знать/понимать:формулы химических веществ Текущий Рассмотрение образцов кислот 41 Соли: состав и номенклатура. 1 Соли. Формулы солей. знать/понимать:формулы химических веществ Текущий 42 Химические свойства оксидов. 1 Хим. Свойства оксидов. З знать химические свойства к оксидов Текущий 43 Получение и химические свойства оснований. 1 Хим. Свойства оснований. Амфотерность. З знать химические свойства к оснований Текущий 44 Химические свойства кислот. 1 Хим. Свойства кислот З знать химические свойства к кислот Текущий 45 Химический свойства солей. 1 Хим. Свойства солей. З знать химические свойства к солей Текущий 46 Обобщение знаний по теме «Генетическая связь между классами неорганических соединений» 1 генетическая связь неорганических соединений определять принадлежность неорганических веществ к определенному классу. Текущий Опыты, иллюстрирую щие существование генетической связи между соединениями фосфора, углерода, натрия, кальция. 47 Практическая работа № 6 Исследование свойств кислот, оксидов, оснований. 1 48 Контрольная работа № 3 1 определять принадлежность неорганических веществ к определенному классу. итоговый Раздел II Химические элементы, вещества и химические реакции в свете электронной теории (21 ч) Тема 7. Строение атома (4ч) 49 Состав и важнейшие характеристики атома. 1 Протон, нейтрон, электрон. Ядро атома. Заряд атома. Порядковый номер. Химический элемент. уметь: объяснять физический смысл порядкового номера химического элемента, номера группы и периода Текущий 50 Изотопы. Химический элемент. 1 Изотопы. Радиоизотопы. знать изотопы. Химические элементы Текущий 51,52 Строение электронных оболочек атомов. 2 Электронное облако. Атомная орбиталь. Орбитальные характеристики электрона. Спаренные и неспаренные электроны. составлять схемы строения атомов первых 20 элементов П.С. Д.И.Менделеева Текущий Тема 8. Периодический закон и Периодическая система элементов Д.И. Менделеева.(3ч) 53 Свойства химических элементов и их периодические изменения. 1 Порядковый номер. Электронное строение атомов. Химическое соединение. Формулы соединений. Свойства химических элементов и их периодические изменения. - объяснять сходство и различие в строении атомов химических элементов; 54 Периодический закон и Периодическая система элементов Д.И. Менделеева в свете теории строения атома. 1 Заряд ядра. Формулировка периодического закона. Физический смысл периодического закона. Причина периодичности свойств элементов. - описывать свойства высших оксидов химических элементов (№ 1-20), Текущий 55 Характеристика химических элементов по положению в периодической системе. 1 Большие и малые периоды. Группы и подгруппы элементов. уметь: объяснять физический смысл порядкового номера химического элемента, номера группы и периода Текущий Тема 9. Строение вещества. (4 ч) 56 Валентные состояния и химические связи атомов элементов. 1 Химические связи. Валентность. Валентные электроны. Возбужденное состояние атома. объяснять закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп. 57 Ковалентная связь и её виды. 1 Общая электронная пара. Ковалентная связь. определять тип химической связи между атомами в простых веществах и типичных соединениях. Текущий 58 Понятие об ионной связи. Степень окисления Ионы.. Ионная связь и ее свойства. Условность типов химической связи. Степень окисления. Определение числа и знака степени окисления элементов в соединении. определять тип химической связи между атомами в простых веществах и типичных соединениях. Текущий 59 Кристаллическое состояние вещества. Кристалл. Элементарная ячейка кристалла. Кристаллическая решетка. Типы кристаллических решеток. Знать кристаллические Текущий состояния веществ. Кристаллические решетки. Модели кристаллическ их решеток веществ с ионным, атомным и молекулярным строением Тема 10. Химические реакции в свете электронной теории. (4ч) Реакции, протекающие с изменением и без изменения степени окисления. Окислительновосстановительны е реакции. 1 61 Расстановка коэффициентов методом электронного баланса 1 Уметь определять окислитель и восстановитель, выполнять баланс электронов, расставлять коэффициенты МЭБ Текущий 62 Обобщение знаний по темам 6-10. 1 Знать сущность и классификацию химических реакций в свете электронной теории Текущий 63 Контрольная работа № 4 1 60 Окисление. Восстановление. Окислитель. Восстановитель. Окислительновосстановительные реакции. Окислительновосстановительные реакции. Классификация реакций. уметь:-определять степень окисления элементов в соединениях; Примеры ОВР различных типов: горение веществ, взаимодействи е металлов с галогенами, серой, растворами солей, кислот итоговый Тема 11. Водород – рождающий воду и энергию. (2ч) 64 65 Водород., физикохимические свойства. Получение и применение водорода. 1 Практическая работа № 7 Получение водорода и исследование его свойств. 1 Водород. Способы получения водорода. распознавать водород опытным путем; Газообразный водород. Жидкий водород. Твердый водород. - называть и характеризовать свойства водорода и воды. Текущий уметь следовать правилам получения и собирания водорода. Тема 12. Галогены (5 ч) 66 Галогены – химические элементы и простые вещества. 1 Электронное строение атомов галогенов. Степени окисления. уметь:называть и характеризовать свойства галогенов, хлороводорода, соляной кислоты 67 Физикохимические свойства галогенов. 1 Изменение свойств галогенов в группе. Галогены- окислители. уметь: называть и характеризовать свойства галогенов Текущий 68 Хлороводород. Соляная кислота. Хлориды. 1 уметь: называть и характеризовать свойства хлороводорода, соляной кислоты Текущий Получение водорода в лаборатории Горение водорода Восстановлени е меди из оксида в токе водорода 69 Практическая работа № 8 Получение соляной кислоты и опыты с ней. 70 Обобщение знаний по темам 10,11. Зачет-игра. итоговый