№ Тема урока Кол-во Знания и умения
реклама
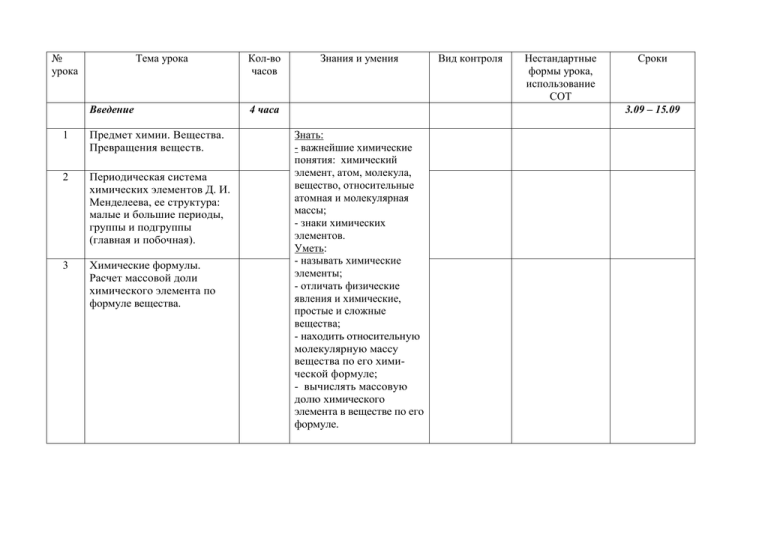
№ урока Тема урока Введение 1 Предмет химии. Вещества. Превращения веществ. 2 Периодическая система химических элементов Д. И. Менделеева, ее структура: малые и большие периоды, группы и подгруппы (главная и побочная). 3 Химические формулы. Расчет массовой доли химического элемента по формуле вещества. Кол-во часов Знания и умения 4 часа Вид контроля Нестандартные формы урока, использование СОТ Сроки 3.09 – 15.09 Знать: - важнейшие химические понятия: химический элемент, атом, молекула, вещество, относительные атомная и молекулярная массы; - знаки химических элементов. Уметь: - называть химические элементы; - отличать физические явления и химические, простые и сложные вещества; - находить относительную молекулярную массу вещества по его химической формуле; - вычислять массовую долю химического элемента в веществе по его формуле. 4 Тема 1. Атомы химических элементов Основные сведения о строении атомов. 5 Изменение числа нейтронов в ядре атома — образование изотопов. Строение электронных оболочек атомов. 6 Изменение числа электронов на внешнем электронном уровне атомов химических элементов. Понятие об ионной связи. 7 Взаимодействие атомов химических элементовнеметаллов между собой. Ковалентная неполярная и полярная химическая связь. 6 часов 17.09-27.10 Знать: - важнейшие химические понятия: ион, химическая связь, валентность, электроотрицательность; - основной законы химии – периодический закон. Уметь: - объяснять физический смысл атомного (порядкового) номера химического элемента, номеров группы и периода, к которым элемент принадлежит в периодической системе Д. И. Менделеева; - объяснять закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп; - определять тип химической связи в соединениях, валентность элемента в соединениях; - составлять схемы строения атомов первых 20 элементов периодической системы Д. И. Менделеева. 8 Взаимодействие атомов химических элементовметаллов между собой. Понятие о металлической связи. 9 Контрольная работа № 1 по теме «Атомы химических элементов». Тема 2. Простые вещества 10 Простые вещества — металлы и неметаллы. Аллотропия. 11 Количество вещества. Моль. Молярная масса. Молярный объем газообразных веществ. 12 Решение задач. Расчеты с использованием понятий «количество вещества», «молярная масса», «молярный объем газов», «постоянная Авогадро». 13 Контрольная работа №2 по теме «Простые вещества» Контрольная работа № 1 4 часа 29.10-17.11 Знать: химические понятия: моль, молярная масса, молярный объем. Уметь: - находить молярную массу вещества; - вычислять количество вещества, объем или массу по количеству вещества, относительную плотность газа. Контрольная работа №2 Тема 3. Соединения химических элементов 14 Степень окисления. Бинарные соединения – оксиды и летучие водородные соединения. 15 Основания, их состав и названия. Кислоты, их состав и названия. 16 Соли, их состав и названия. 17 Типы кристаллических решеток. Закон постоянства состава. 18 Чистые вещества и смеси. Массовая и объемная доли компонента смеси. Расчеты, связанные с использованием понятия «доля». 19 Контрольная работа № 3 «Соединения химических элементов». 6 часов 26.11-12.01.08 Знать закон постоянства состава вещества. Уметь: - называть соединения изученных классов; - определять состав веществ по их формулам, степень окисления элемента в соединениях, принадлежность веществ к определенному классу соединений; - составлять формулы неорганических соединений изученных классов; - вычислять массовую и объемную доли компонентов смеси веществ; - вычислять массовую долю вещества в растворе по известной массе растворенного вещества и массе растворителя; - вычислять массы растворяемого вещества и растворителя, необходимые для приготовления определенной массы раствора с известной массовой долей растворенного вещества. Химический диктант Контрольная работа № 3 Тема 4. Изменения, происходящие с веществами 20 Физические и химические явления. 21 Закон сохранения массы веществ. Химические уравнения. Типы химических реакций. 22 Расчеты по химическим уравнениям. Решение задач на нахождение количества вещества, массы или объема продукта реакции по количеству вещества, массе или объему исходного вещества. Расчеты с использованием понятия «доля», когда исходное вещество дано в виде раствора с заданной массовой долей растворенного вещества или содержит определенную долю примесей. 23 Контрольная работа № 4 «Изменения, происходящие с веществами». 4 часа 14.01-6.02 Знать: важнейшие химические понятия: химическая реакция, классификация реакций; основной закон химии: закон сохранения массы веществ. Уметь: - уравнивать химические уравнения, опираясь на знание закона сохранение масс веществ; - определять типы химических реакций; - вычислять по химическим уравнениям массы или количества вещества по известной массе или количеству вещества одного из вступающих в реакцию веществ или продуктов реакции; - вычислять массы (количества вещества, объема) продукта реакции, если известна масса исходного Контрольная вещества, содержащего работа № 4 определенную долю примесей; - вычислять массы (количества вещества, объема) продукта реакции, если известна масса раствора и массовая доля растворенного вещества. Тема 5. Растворение. Растворы. Свойства растворов электролитов. 24 Растворение как физикохимический процесс. Растворимость веществ в воде. Электролитической диссоциации. 25 Основные положения теории электролитической диссоциации. 26 Ионные уравнения реакций. Условия протекания реакции обмена между электролитами до конца в свете ионных представлений. Кислоты, их классификация и свойства в свете теории электролитической диссоциации. Основания, их классификация и свойства в свете теории электролитической диссоциации. Оксиды, их классификация и свойства. 27 28 29 30 Соли, их классификация и свойства в свете теории электролитической диссоциации. 11 часов 21.02-3.05 Знать: важнейшие химические понятия: - электролит и неэлектролит; - электролитическая диссоциация; - окислитель и восстановитель; - окисление и восстановление; - классификацию неорганических веществ. Уметь: - называть соединения изученных классов; - объяснять сущность электролитической диссоциации, реакций ионного обмена; - характеризовать химические свойства основных классов неорганических веществ; - определять возможность протекания реакций ионного обмена; - составлять уравнения химических реакций; - уравнивать окислительновосстановительные реакции методом электронного баланса. Тест «Кислоты» Тест «Основания» Тест «Оксиды» 31 Генетическая связь между классами неорганических веществ. 32 Окислительновосстановительные реакции. 33 Составление уравнений окислительновосстановительных реакций методом электронного баланса. 34 Контрольная работа № 5 по теме «Растворение. Растворы. Свойства растворов электролитов». Тест «Соли» Контрольная работа № 5