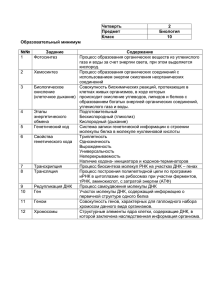
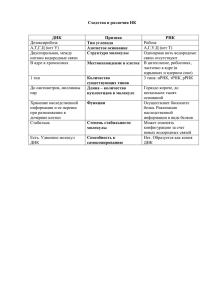
Белки-молекулярные машины
реклама

Белки-молекулярные машины A. F0F1-ATPase B. Flagella motor C/D.Kinesin/Dynein transport along microtubules E. Muscle contraction F. RNA polymerase Масштаб энергий EATP = 80 pN*nm kBT = 4 pN*nm Тепловое движение существенно для работы мол. машин. Science 317, 333 (2007) Флагеллярный аппарат бактерий Escherichia coli использует тонкие длинные нити называемые флагеллами (flagella) для передвижения вращением. Флагелла вращается против ч.с., создавая момент силы (103 pN*nm, 250 kT) заставляющий вращаться бактерию по ч.с. с частотой около 100 Hz. Флагеллярный аппарат Грам-отрицательных бактерий. Экспериментальное наблюдение работы мол. машин (single molecule experiments) F1-ATPase– нанопропеллер. Последовательность фотографий флуоресцирующей актиновой метки (133-ms интервал), ковалентно связанной с ротором ( -субъединица), демонстрирует вращательное движение производимое F1-ATPase мотором. Связанный с поверхностью кинезиновые моторы продвигающие микротубулиновый перевозчик, с которым связаны молекулы ДНК (их перемещение по открытым полиуретановым каналам регистрируется с помощью флуоресценции). Скорость микротрубочки 1 mm/s, (перемещения актиновых филамент может достигать скорости 10 mm/s). M.G. L. van den Heuvel and C. DekkerScience 317, 333 (2007) Миозиновый шаговый двигатель. Actin molecule Spontaneous nucleation and elongation 10 10 106 102 10 1 B P Myosin-V walking on an actin filament Pointed ADP ADP ATP ADP ADP Barbed ADP ADP+Pi Science 326, 1208 (2009) ADP ADP +Pi Сокращение мускулов «Шаги» миозина V по актиновым филаментам Миозины представляют из себя разнообразное семейство белков состоящее из 18 классов, из которых мускульный миозин II изучен наиболее тщательно. Небольшие структурные изменения в каталитическом домене при гидролизе АТФ усиливаются лѐгкой цепью и приводят к «шаговому» движению связывающего домена лѐгкой цепи другого мономера миозина. Миозин V может передвигаться в одиночку и тем самым удобен для исследования. J.E. Molloy and C. Veigel Myosin Motors Walk the Walk, Science 300, 2045 (2003) A.Yildiz, et al. Myosin V Walks Hand-Over-Hand: Single Fluorophore Imaging with 1.5-nm Localization, Science 300, 2061 (2003) Траектория трѐх молекул миозина. «Зависание» вызвано освобождением молекулы АДФ. Траектория миозина криволинейная, так что миозин делает полный оборот вокруг актинового филамента при продвижении на 2 m. Различные способы «шагания» молекулы миозина V вдоль актинового филамента. Был разработан метод флуоресцентной визуализации с точностью локализации положения на плоскости отдельной флуоресцентной метки 1.5 nm в субсекундном временном диапазоне и фотостабильностью на протяжении нескольких минут. Упрощѐнная схема актомиозинового цикла. V.Ovchinnikov, B.L. Trout and M.Karplus Mechanical Coupling in Myosin V: A Simulation Study, J. Mol. Biol. (2010) 395, 815–833 F0F1-ATPase структура (подшипник) (вращ. вал) (рычаг) Central rotor Stator ab2 ab2c10-15 Junge W., Sielaff H., Engelbrecht S., Nature 459, 364 (2009) c10-15 3 F0F1-ATPase схема работы ( )3 формирует 6 нуклеотид связывающих центра, 3 катал. и 3 некаталитических. MgATP связывается с отрицательной кооперативностью: KD ~ 1 nM, 1 M, 30 M. Средний M = 56 pNnm. При таком моменте вся энергия гидролиза АТФ превращается в механ. энергию, т.е. F1 работает без проскальзывания. F0 мотор способен переносить 6500 протонов в секунду через мембрану при потенциале 100 mV с высокой специфичностью (107). F0F1 мотор имеет разное передаточное число для разных организмов в зависимости от числа субъединиц c. Для хлоропластов Протон:АТФ = 4 (теорет. знач. 4,7, поскольку у них 14 мономеров в с-кольце). Junge W., Sielaff H., Engelbrecht S., Nature 459, 364 (2009) F0F1-ATPase –наблюдение вращения, измерение момента силы Junge W., Sielaff H., Engelbrecht S., Nature 459, 364 (2009) Полимерная везикула, содержащая бактериородопсин и F0F1-ATPase синтезирует АТФ используя протонный градиент, создаваемый бактериородопсином под действием света. H. J. Choi, C. D. Montemagno, Nano Lett. 5, 2538 (2005). Структурная ДНК нанотехнология Возможность сборки нанообъектов точно располагая их компоненты друг относительно друга во множестве экземпляров является одной из основных целей нанотехнологии и науки о материалах; В природе эта цель достигается за счѐт сборки биомолекул молекул под действием нековалентных взаимодействий; Молекулы ДНК являются наиболее выдающимися представителями самособирающихся компонентов. Две одиночные цепи ДНК под действием водородных связей, -стэкинга, электростатического и гидрофобного взаимодействий образуют двойную спираль, подчиняясь правилу комплементарности оснований; Это свойство молекулы ДНК может быть использовано для сборки нанообъектов, использующих двойные спирали ДНКв качестве элементов «строительных конструкций», позволяющих точно позиционировать компоненты в структуре проектируемой системы. P.W.K. Rothemund, Nature 440, 297 (2006). Бактериальная ДНК использовалась для построения оригами на плоскости (японское искусство формирования фигур из бумаги). ДНК-Конструкции N. Seeman предложил использовать 4way DNA Holliday junctions с “липкими” концами для формирования регулярных поверхностных структур из молекул ДНК. 1D->2D ДНК плитка Черепица (плитка) Плоская решѐтка Вязанка двойных Спиралей ДНК (нанотрубки) Aldae F.A., Palmer A.L., Sleiman H.F. Assembling materials with DNA as guide, Science 321, 1795 (2008) Метод построения двумерных слоѐв из ДНК. a. Схематический вид двойных ДНК перехлѐстов. Миотический DX (MDX), пара гомологичных хромосом,перехлѐстывается для обмена генетической информацией(HJ означает Holliday junctions). Структура аналога (ADX), используемого как плитка при построении двумерных ДНК матриц, состоит из 2х комплементарных красных нитей, 2х синих связывающих нитей и центральной зелѐной связывающей нити. b. Два типа ADX молекул A и B*. B* содержит дополнительный ДНК домен исходящий из центра и выступающий почти перпендикулярно плоскости DX молекулы. c. Комплементарные концы ADX молекул представлены различными геометрическими фигурами указывающими на их соответствие при самосборке. Размер одной плитки 4x16 nm и они соединяются т.о., что выступы B* расположены на расстоянии 32 nm друг от друга. d. B* выступы видны как «полоски» на ДНК «плитке» в атомном силовом микроскопе. Nadrian C. Seeman, DNA in a material world Nature 421, 427 (2003) Paul W. K. Rothemund Folding DNA to create nanoscale shapes and patterns Nature 440, 297(2006). Sanderson K., Nature 464, 158 (2010) Синтезируемые молекулы ДНК не превышают 150 пар оснований. Более длинные молекулы ДНК можно взять из вирусов (7000 нуклеотидов). Зная последовательность ДНК, можно предложить набор коротких нуклеотидов (200 штук по 16 оснований), которые служили в качестве «скобок» (staples) зафиксировав укладку молекулы ДНК. Смешав эти «кнопки» с вирусной ДНК в буфере, нагрев и охладив полученную смесь, одноцепочечная молекула ДНК свяжется должным образом со «скобками», формирую планируемые узоры («смайлики»). Возможные приложения: Нанолинейка (fluorescent dye labeled staples); Искуственный лист (попытка сборки белков фотосистемы II на заготовке из ДНК оригами); Доставка лекарств (активная молекула + ДНК «ящик» + белки вирусной оболочки); Подложка для наноэлектронных устройств; «Скульптуры» из ДНК T. H. LaBean Nature 459,331 (2009) Метод проектирования и сборки 3D наноструктур из ДНК. a. Трубочки заготовки выстраиваются в гексагональную решѐтку. b. Часть секций удаляется из трубочек, так же как скульптор вырубает скульптуру из камня. Оставшиеся трубочки будут ДНК дуплексами в окончательной структуре. ДНК структура проектируется протяжкой одноцепочечной молекулы ДНК (M13 вирус) через каждую трубочку в заготовке, после чего комплементарная цепь проектируется таким образом, чтобы связаться с вирусной ДНК в заготовке. Сотни коротких участков ДНК подбираются таким образом, чтобы образовать «скрепки» между соседними трубочками заготовки, удерживая структуру в целом. После синтеза «скрепки» смешиваются с ДНК в растворе и при определѐнных условиях смесь сворачивается в искомую структуру. Douglas S.M. et. al. Self-assembly of DNA into nanoscale three-dimensional shapes. Nature 459, 414 (2009) Ящик из ДНК с открывающейся крышкой Andersen E.S., et al. Self-assembly of a nanoscale DNA box with a controllable lid, Nature 459, 73 (2009) Cy5 Cy3 Размер ящика 42*36*36 nm3, был сформирован с помощью одноцепочечной M13 ДНК и (220+59) «скрепок» придавших форму ящика. Размер внутренней полости позволяет поместить туда рибосому или полиовирус.