Название группы: _____Эхо химии________ Участники: ______Туранцева Оксана, Смелая Алевтина, Иванчик Эльвира_____________
advertisement
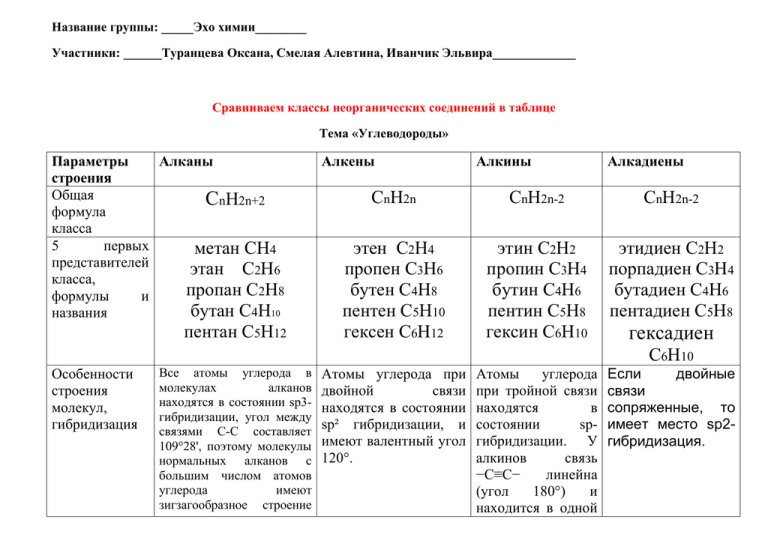
Название группы: _____Эхо химии________ Участники: ______Туранцева Оксана, Смелая Алевтина, Иванчик Эльвира_____________ Сравниваем классы неорганических соединений в таблице Тема «Углеводороды» Параметры Алканы строения Общая CnH2n+2 формула класса 5 первых метан СH4 представителей этан С2Н6 класса, пропан С2Н8 формулы и бутан С4Н10 названия пентан С5Н12 Алкены Алкины Алкадиены СnH2n СnH2n-2 СnH2n-2 этен С2Н4 пропен С3Н6 бутен С4Н8 пентен С5Н10 гексен С6Н12 этин С2Н2 пропин С3Н4 бутин С4Н6 пентин С5Н8 гексин С6Н10 этидиен С2Н2 порпадиен С3Н4 бутадиен С4Н6 пентадиен С5Н8 гексадиен С6Н10 Особенности строения молекул, гибридизация Все атомы углерода в молекулах алканов находятся в состоянии sр3гибридизации, угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение Атомы углерода при двойной связи находятся в состоянии sp² гибридизации, и имеют валентный угол 120°. Атомы углерода при тройной связи находятся в состоянии spгибридизации. У алкинов связь −С≡С− линейна (угол 180°) и находится в одной Если двойные связи сопряженные, то имеет место sp2гибридизация. (зигзаг). Длина связи С-С в предельных углеводородах равна 0,154 нм (1нм=1*109м). Физические свойства, как изменяются в классе Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи При нормальных условиях неразветвлённые алканы с CH4 до C4H10 — газы; с C5H12 до C13H28 — жидкости; после C14H30 — твёрдые тела. Температуры плавления и кипения алкенов (упрощенно) увеличиваются с молекулярной массой и длиной главной углеродной цепи. При нормальных условиях алкены с C2H4 до C4H8 — газы; с C5H10 до C17H34 — жидкости, после C18H36 — твёрдые тела. Алкены плоскости. Атомы углерода связаны одной σ- и двумя π-связями, максимальная электронная плотность которых расположена в двух взаимно перпендикулярных плоскостях. Длина тройной связи примерно 0,121 нм, энергия связи 836 кДж/моль. Алкины по своим физическим свойствам напоминают соответствующие алкены. Низшие (до С4) — газы без цвета и запаха, имеющие более высокие температуры кипения, чем аналоги в алкенах. Алкины плохо Бутадиен — газ (tкип -4,5°С), изопрен — жидкость, кипящая при 34°С, диметилбутадиен — жидкость, кипящая при 70°C. Изопрен и другие диеновые углеводороды способны полимеризоваться в каучук. Натуральный Особенности химических свойств (4-5 самых основных) Температуры плавления и кипения понижаются от менее разветвленных к более разветвленным. Так, например, при 20 °C н-пентан — жидкость, а неопентан — газ. газообразные алканы горят бесцветным или бледно-голубым пламенем с выделением большого количества тепла. не растворяются в воде, но хорошо растворяются в органических растворителях. растворимы в воде, лучше — в органических растворителях. каучук в очищенном состоянии является полимером с общей формулой (С5Н8)n и получается из млечного сока некоторых тропических растений. Каучук хорошо растворим в бензоле, бензине, сероуглероде. Горение, нитрование, Галогенирование, гидрогалогенирование, гидроборирование, гидратация, алкилирование. Образование алкинидов, реакции нуклеофильного замещения алкинидов, галогенирование, гидратация. Реакция электрофильного присоединения(АЕ), полимеризация диеновых углеводородов, получение бутадиена из этилового спирта в присутствии катализатора. Изомерия углеродного скелета, изомерия крекинг, галогенирование, сульфохлорирование (реакция Рида), изомеризация Существует ли Изомерия изомерия, углеводородной цепи. какие виды Под влиянием Алкенам свойственна Алкинам изомерия различных свойственна типов. Если алкан изомерия катализаторов при нагревании углеводороды нормального строения подвергаются изомеризации перестройке углеродного скелета с образованием алканов разветвленного строения. С4Н10 имеет 2 изомера, то алкену с тем же числом углеродных атомов формулы С4Н8 соответствует уже 6 изомерных соединений (4 алкена и 2 циклоалкана). Такое многообразие изомеров объясняется тем, что наряду со структурной изомерией углеродного скелета для алкенов характерны, вопервых, другие разновидности структурной изомерии - изомерия положения кратной связи и межклассовая изомерия. Во-вторых, в ряду алкенов проявляется пространственная изомерия, связанная с различным углеродного положения двойных скелета (начиная с связей, цис-трансC5H8), изомерия изомерия. положения тройной связи (начиная с C4H6) и межклассовая изомерия с алкадиенами. положением заместителей относительно двойной связи, вокруг которой невозможно внутримолекулярное вращение. Самые важные Нефть,бутан,природный Этилен, пропилен, Этин,пропин,бутин Бутадиен, для человека газ,пропан. бутилен. порпадиен. представители данного класса органических соединений Вопросы, на которые необходимо ответить! 1) Почему углеводороды так называются? _______Углеводороды состоят из атомов водорода и углерода.__________________________________________________________________________________________ __________________________________________________________________________________________________ ____________________________________________________________ 2) В чем основная разница предельных и непредельных углеводородов? _____ Предельные углеводороды - это углеводороды, атомы углерода в которых соединены в прямые или разветвленные цепочки без кратных (двойных или тройных) связей. 3) А непредельные - это углеводороды либо имеющие кратные связи, либо замкнутые в кольцо, либо и то и другое вместе.____________________________________________________________________________________________ __________________________________________________________________________________________________ ____________________________________________________________ МОЖНО ПОЛЬЗОВАТЬСЯ ИНТЕРНЕТ-ИСТОЧНИКАМИ, НО ОБЯЗАТЕЛЬНО УКАЗАТЬ ИХ АДРЕСА В ДОКУМЕНТЕ! Вариант отправляем по электронной почте karpuhinamv@mail.ru c названием Задание 1. Группы «Название» Источники: учебник Химия 10 класс. Базовый уровень. Габриелян О. С; http://ru.wikipedia.org/ http://www.gazpromschool.ru http://www.chemel.ru/


