численное моделирование работы системы вентиляции в
реклама

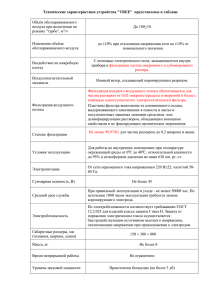
ЧИСЛЕННОЕ МОДЕЛИРОВАНИЕ РАБОТЫ СИСТЕМЫ ВЕНТИЛЯЦИИ В ОПЕРАЦИОННОЙ С. Третьяков/S. Tretyakov Как известно, в настоящее время требования к чистоте воздуха в операционных достаточно высоки, что связано с необходимостью превентивного предотвращения послеоперационного сепсиса. Согласно исследованиям 1998 г., проведенным зарубежом [1], стоимость последующего лечения сепсиса составляет 2850 долл. на один случай инфицирования. Более того, данная сумма даже близко не учитывает моральные и физические страдания, которые испытывает пациент в данном случае. Источниками инфекции в операционной являются микроорганизмы, которые паразитируют на коже человека и не приносят ему существенного вреда без попадания в открытую рану. Их перенос в пространстве операционной осуществляется засчет отшелушивания частиц кожи хирургического персонала, а также открытых частей кожи пациента. Размеры частиц кожи составляют приблизительно 20 микрон и они легко проходят через хлопковую униформу персонала с размерами пор в 80-100 микрон. Таким образом, воздушная среда операционной должна соответстующим образом отфильтровываться для сохранения концентрации частицпереносчиков в пределах, установленных законодательством. Как правило, вентиляционная система, установленная в операционной, является системой рециркулятивного типа, т.е. отобранный в помещении воздух возвращается туда же после очистки на высокоэффективных фильтрах. Существует два варианта размещения фильтра – напольный и потолочный. В соответствии с многочисленными исследованиями, потолочное размещение более оправдано с эпидемиологической точки зрения, т.к. свежеотфильтрованный воздух поступает сразу на хирургическую рану, привнося минимальное количество паразитоносителей. В данном случае очень критическим является возникновение направленной вверх тепловой конвекции со стороны персонала, которая привносит частицы-переносчики в чистый потока от фильтра. Применение фильтрующей системы зависит от типа операционной – в обычных операционных используется т.н. воздушная система высокой эффективности очистки по частицам (high efficiency particulate air - HEPA). Для помешений трансплантологии и сходных «высокочистых» операционных используются системы ультрачистой вентиляции (ultra clean ventillation - UCV), с более высокой эффективностю очистки и, соответственно, стоимостью. Rafat Al-Waked [2] в своей работе модельно рассмотрел возможность использования системы типа HEPA, в противовес использованию UCV, для поддеражания высокочистой среды в операционной. В статье рассмотрен перенос частиц-носителей по операционной и особое внимание уделяется концентрации частиц в районе операционной раны. План операционной, рассмотренной в работе, представлен на Рис.1, она включает в себя: 1) трехмерное пространство операционной, заполненное воздухом (168 м3) 2) оборудование, в т.ч. энерговыделяющее: операционный стол, анестезирующий аппарат (э.в.), столы и стены, хирургическая 3) 4) 5) 6) лампа/surgical light (э.в.), лампы всеобщего освещения/theatre lights (э.в.). в модели эти элементы представлены граничными условиями типа «стенка», причем граничные отмеченные индексом э.в. дополнены условием постоянности теплового потока с поверхности. Персонал. Граничное условие типа «стенка», причем персонал испускает частицы-носители, углекислый газ при дыхании и тепловой поток. Пациент. Граничное условие типа «стенка» с выделением тепла и углекислого газа (ниже, чем персонал, т.к. в состоянии наркоза). Хирургическая рана – «ловушка» для частиц (скорость частицы искуственно становится нулевой при попадании в рану) Заборные решетки/return air grill – граничное условие типа «выход» Потолочная фильтрующая система/HEPA filters – граничное условие типа «вход», воздух не содержит частицы-носители. Рисунок 1. Схематичное представление модели Моделирование процесса осуществлялось в среде CFD-ACE с использованием стандартной модели турбулентности типа «к-эпсилон». Перенос частиц-носителей моделировался в Лагранжевой постановке, основанной на решении формулировки второго закона Ньютона отдельно для каждой частицы, с учетом суммарной силы, действующей на частицу от всех механизмов: гравитации, архимедовой силы, силы лобового сопротивления потоку. Учет тепловых аспектов процесса достигался путем решения уравнения энергии для системы, при этом особое внимание уделялось возникновению конвективных токов воздуха и частиц-переносчиков. Перенос углекислого газа моделировался на основании стандартной модели для диффузии газа. Более детально о модели и результатах моделирования можно узнать, связавшись с автором или в работе [2]. В данной работе рассмотрены 4 основных системы вентилирования помещения, приведенные в Таблице. Более того, каждая из систем была рассмотрена со следующиъ точек зрения: • работы в диапазоне скоростей потока воздуха, • обеспечения комфортной температуры в помещении, • распространения углекислого газа, • скорости потока в районе хирургической раны, • нескольких типов хирургических ламп, т.к. конвекционные контртоки на пути воздуха из фильтра обусловленны ее энергонапряженностью, • использование занавески вокруг фильтра, предназначенной для фокусировки потока на стол, • различные комбинации по заборным решеткам. № опции 1 2 3 4 Тип UCV UCV HEPA* HEPA* Площадь фильтра, м2 5,76 9 5,4 8,36 Скорость после фильтра, м/с 0,38 0,33 0,47 0,63 Стоимость системы, тыс. долл. 120,8 146,1 88,49 105,1 * - система типа НЕРА набрана из четырех фильтров, расположенных по контуру над операционным столом Рисунок 2. Слева – векторы скорости потока воздуха, справа – контуры температуры По результатам моделирования, приведенным на Рис. 2 для опции № 3 оказалось, что энергонапряженное оборудование вызвает тепловую конвекцию воздуха, образуя циркуляторные течения, способствующие загрязнению хирургической раны. Таким образом, одной из основных рекомендаций исследователей было использование минимальной по размерам и энерговыделению хирургической лампы. Более того, оказалось, что первые три опции из приведенных в Таблице удовлетворяют нормативам по содержанию частиц в помещениях особой чистоты (не обычных операционных). Опиця №4, в которой из-за большой площади фильтрующей поверхности был увеличен центральный зазор между плитами фильтров, не является удовлетворительной. Причиной этому послужило неоднородное поле потока на входе в помещение, которое увеличивает количество вортексных структур в помещении, равномерно распределяя частицы-носители по объему. Таким образом, наиболее экономически оправданным является использование относительно недорогой конфигурации НЕРА-системы, уровень очистки в которой достигает величин для более эффективных UCV. Некоторые дополнительные заключения, сделанные при анализе результатов моделирования: 1) использование направляющей воздух занавески неоправданно, т.к. приводит к интенсификации конвекции от персонала и лампы, образуя контр-токи на пути чистого воздуха. 2) расположение заборных решеток существенно не влияет на распределение частиц-носителей в помещении. 3) различные размеры заборных решеток также существенно не влияют на распределение частиц-носителей. 4) минимизация энерговыделения в помещении – один из важнейших факторов к снижению концентрации частиц в районе раны. 5) увеличение скорости на фильтрах оправданно лишь до определенной величины, после чего наблюдается интенсивный перенос носителей к ране. Более того, высокая скорость воздуха у раны способствует ее высыханию. Ссылки: 1. Martone W.J. et al (1998). Incidence and Nature of Endemic and Epidemic Nosocomial Infections. Chapter 30 In-hospital infection. 4 th. Edition Philadelphia. 2. R. Al-Waked. Effect of ventilation strategies of infection control innside operating theatres. Engineering Applications of Computational Fluid Mechanics, v.4, n.1, pp.1-16 (2010). Автор благодарит д-ра К.В. Чау, заместителя редактора Engineering Applications of Computational Fluid Mechanics за разрешение использовать статью [2] и рисунки из журнала для написания данного обзора. The author kindly acknowledge Dr. K.W. Chau, Associate Editor of Engineering Applications of Computational Fluid Mechanics, for the permission to use paper [2] and figures from the Journal when writing the current review.