Вариант № 1
реклама
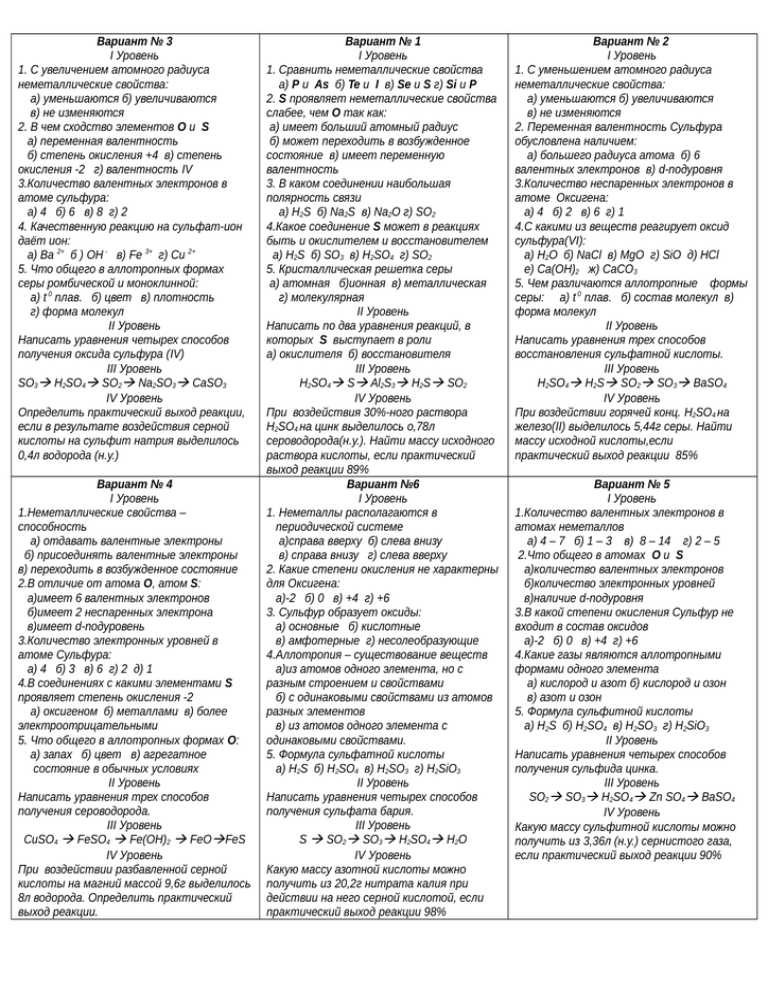
Вариант № 3 I Уровень 1. С увеличением атомного радиуса неметаллические свойства: а) уменьшаются б) увеличиваются в) не изменяются 2. В чем сходство элементов O и S а) переменная валентность б) степень окисления +4 в) степень окисления -2 г) валентность IV 3.Количество валентных электронов в атоме сульфура: а) 4 б) 6 в) 8 г) 2 4. Качественную реакцию на сульфат-ион даёт ион: а) Ba 2+ б ) OH - в) Fe 3+ г) Cu 2+ 5. Что общего в аллотропных формах серы ромбической и моноклинной: а) t 0 плав. б) цвет в) плотность г) форма молекул II Уровень Написать уравнения четырех способов получения оксида сульфура (IV) III Уровень SO3 H2SO4 SO2 Na2SO3 CaSO3 IV Уровень Определить практический выход реакции, если в результате воздействия серной кислоты на сульфит натрия выделилось 0,4л водорода (н.у.) Вариант № 4 I Уровень 1.Неметаллические свойства – способность а) отдавать валентные электроны б) присоединять валентные электроны в) переходить в возбужденное состояние 2.В отличие от атома O, атом S: а)имеет 6 валентных электронов б)имеет 2 неспаренных электрона в)имеет d-подуровень 3.Количество электронных уровней в атоме Сульфура: а) 4 б) 3 в) 6 г) 2 д) 1 4.В соединениях с какими элементами S проявляет степень окисления -2 а) оксигеном б) металлами в) более электроотрицательными 5. Что общего в аллотропных формах O: а) запах б) цвет в) агрегатное состояние в обычных условиях II Уровень Написать уравнения трех способов получения сероводорода. III Уровень CuSO4 FeSO4 Fe(OH)2 FeOFeS IV Уровень При воздействии разбавленной серной кислоты на магний массой 9,6г выделилось 8л водорода. Определить практический выход реакции. Вариант № 1 I Уровень 1. Сравнить неметаллические свойства а) P и As б) Te и I в) Se и S г) Si и P 2. S проявляет неметаллические свойства слабее, чем O так как: а) имеет больший атомный радиус б) может переходить в возбужденное состояние в) имеет переменную валентность 3. В каком соединении наибольшая полярность связи а) H2S б) Na2S в) Na2O г) SO2 4.Какое соединение S может в реакциях быть и окислителем и восстановителем а) H2S б) SO3 в) H2SO4 г) SO2 5. Кристаллическая решетка серы а) атомная б)ионная в) металлическая г) молекулярная II Уровень Написать по два уравнения реакций, в которых S выступает в роли а) окислителя б) восстановителя III Уровень H2SO4 S Al2S3 H2S SO2 IV Уровень При воздействия 30%-ного раствора H2SO4 на цинк выделилось о,78л сероводорода(н.у.). Найти массу исходного раствора кислоты, если практический выход реакции 89% Вариант №6 I Уровень 1. Неметаллы располагаются в периодической системе а)справа вверху б) слева внизу в) справа внизу г) слева вверху 2. Какие степени окисления не характерны для Оксигена: а)-2 б) 0 в) +4 г) +6 3. Сульфур образует оксиды: а) основные б) кислотные в) амфотерные г) несолеобразующие 4.Аллотропия – существование веществ а)из атомов одного элемента, но с разным строением и свойствами б) с одинаковыми свойствами из атомов разных элементов в) из атомов одного элемента с одинаковыми свойствами. 5. Формула сульфатной кислоты а) H2S б) H2SO4 в) H2SO3 г) H2SiO3 II Уровень Написать уравнения четырех способов получения сульфата бария. III Уровень S SO2 SO3 H2SO4 H2O IV Уровень Какую массу азотной кислоты можно получить из 20,2г нитрата калия при действии на него серной кислотой, если практический выход реакции 98% Вариант № 2 I Уровень 1. С уменьшением атомного радиуса неметаллические свойства: а) уменьшаются б) увеличиваются в) не изменяются 2. Переменная валентность Сульфура обусловлена наличием: а) большего радиуса атома б) 6 валентных электронов в) d-подуровня 3.Количество неспаренных электронов в атоме Оксигена: а) 4 б) 2 в) 6 г) 1 4.С какими из веществ реагирует оксид сульфура(VI): а) H2O б) NaCl в) MgO г) SiO д) HCl е) Ca(OH)2 ж) CaCO3 5. Чем различаются аллотропные формы серы: а) t 0 плав. б) состав молекул в) форма молекул II Уровень Написать уравнения трех способов восстановления сульфатной кислоты. III Уровень H2SO4 H2S SO2 SO3 BaSO4 IV Уровень При воздействии горячей конц. H2SO4 на железо(II) выделилось 5,44г серы. Найти массу исходной кислоты,если практический выход реакции 85% Вариант № 5 I Уровень 1.Количество валентных электронов в атомах неметаллов а) 4 – 7 б) 1 – 3 в) 8 – 14 г) 2 – 5 2.Что общего в атомах O и S а)количество валентных электронов б)количество электронных уровней в)наличие d-подуровня 3.В какой степени окисления Сульфур не входит в состав оксидов а)-2 б) 0 в) +4 г) +6 4.Какие газы являются аллотропными формами одного элемента а) кислород и азот б) кислород и озон в) азот и озон 5. Формула сульфитной кислоты а) H2S б) H2SO4 в) H2SO3 г) H2SiO3 II Уровень Написать уравнения четырех способов получения сульфида цинка. III Уровень SO2 SO3 H2SO4 Zn SO4 BaSO4 IV Уровень Какую массу сульфитной кислоты можно получить из 3,36л (н.у.) сернистого газа, если практический выход реакции 90%
