Пример решение по разделу структурная
реклама
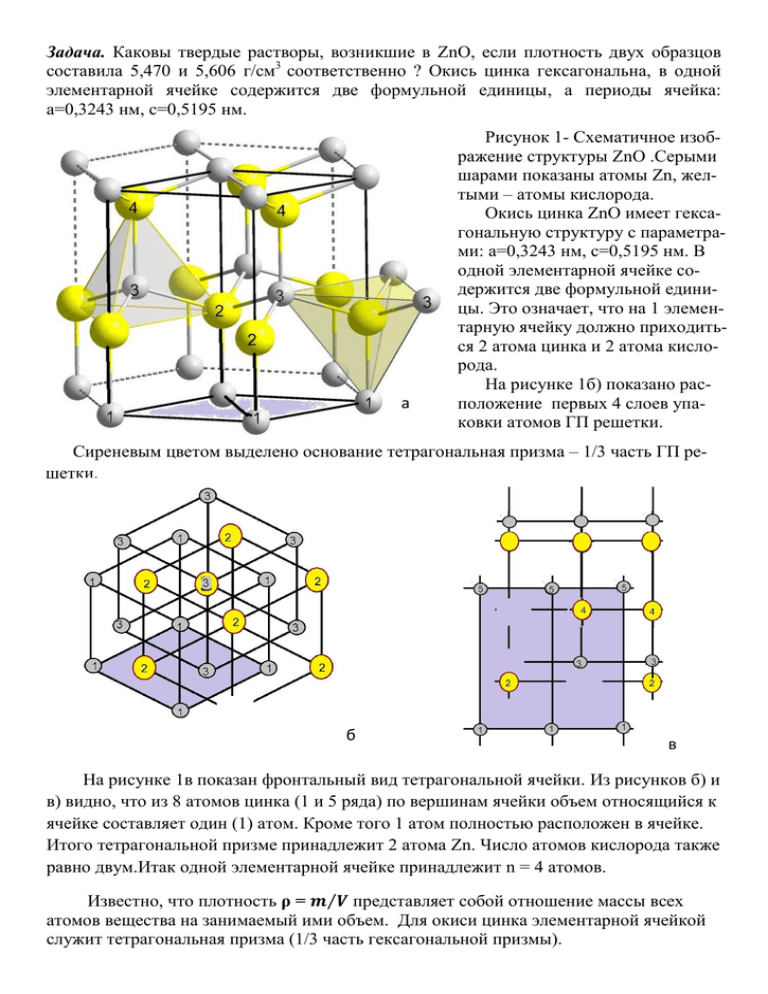
Задача. Каковы твердые растворы, возникшие в ZnO, если плотность двух образцов составила 5,470 и 5,606 г/см3 соответственно ? Окись цинка гексагональна, в одной элементарной ячейке содержится две формульной единицы, а периоды ячейка: а=0,3243 нм, с=0,5195 нм. a Рисунок 1- Схематичное изображение структуры ZnO .Серыми шарами показаны атомы Zn, желтыми – атомы кислорода. Окись цинка ZnO имеет гексагональную структуру с параметрами: а=0,3243 нм, с=0,5195 нм. В одной элементарной ячейке содержится две формульной единицы. Это означает, что на 1 элементарную ячейку должно приходиться 2 атома цинка и 2 атома кислорода. На рисунке 1б) показано расположение первых 4 слоев упаковки атомов ГП решетки. Сиреневым цветом выделено основание тетрагональная призма – 1/3 часть ГП решетки. б в На рисунке 1в показан фронтальный вид тетрагональной ячейки. Из рисунков б) и в) видно, что из 8 атомов цинка (1 и 5 ряда) по вершинам ячейки объем относящийся к ячейке составляет один (1) атом. Кроме того 1 атом полностью расположен в ячейке. Итого тетрагональной призме принадлежит 2 атома Zn. Число атомов кислорода также равно двум.Итак одной элементарной ячейке принадлежит n = 4 атомов. Известно, что плотность ρ = 𝒎⁄𝑽 представляет собой отношение массы всех атомов вещества на занимаемый ими объем. Для окиси цинка элементарной ячейкой служит тетрагональная призма (1/3 часть гексагональной призмы). Объем тетрагонально призмы равен V = S*h, 1 где S – площадь основания, S = d1*d2; 2 h - высота призмы, 0,5195 нм . d1 = a = 0,3243 нм; d2 = а√3 = 0,3243 нм *1,732=0,5617 нм. V= 0,5195 * 0,5* 0,3243*0,5617 = 0,0473*10-21 см3 Отсюда общее число атомов N в 1см3 ZnO будет равно: N = n/V = 84,54*1021 атомов Атомный вес Zn равен 65,37 единиц; атомный вес кислорода равен 16 единицам. 1 Атомная единица массы равна 1.66 * 10-24 граммов. Так как в 1 элементарной ячейке число атомов цинка равно числу атомов кислорода, то число атомов каждого из них равно N/2. Отсюда плотность ZnO при случае идеальной решетке равна ρ= (N⁄2)∗AZn ·1.66∗10−24 +(N⁄2)∗Ao ∗1.66∗10−24 1 = 5,710 г/см3 Так как плотность двух образов ZnO по условию задачи равны 5,470 и 5,606 г/см3 это означает, что концентрация цинка в окиси цинка не соответствует идеальной структуре. Таким образом, не все места отведенные цинку в решетке окиси цинка заполнены цинком и он образует твердый раствор вычитания или твердый раствор замещения. Далее задачу на практике можно решать разными способами. Какой путь решения Вы предложили бы?