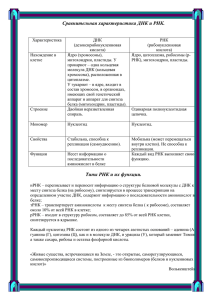
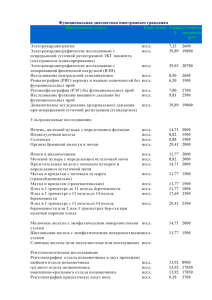
Гущин А.Е. - Стандартизованная аналитическая технология
реклама

ПРОЕКТ Гущин А.Е., Рыжих П.Г., Анисимова Н.С., Творогова М.Г., Шипулин Г.А. ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, г.Москва Иванов А.М., Криворучко А.Б. Военно- медицинская академия, г.Санкт-Петербург Савичева А.М., ФБГУ НИИАГ им. Д.О.Отта СЗО РАМН, г. Санкт-Петербург Федеральный закон от 21.11.2011. №323ФЗ «Об основах здоровья граждан Российской Федерации» Сравнимые результаты исследований, полученные в разных лабораториях. Получение наиболее достоверной лабораторной информации, эффективное использование которой в процессе клинической диагностики и мониторинга проводимого лечения пациентов предполагает оптимальные результаты оказания медицинской помощи при наблюдаемых формах патологии. Сифилис Гонококковая инфекция Хламидийная инфекция Урогенитальный трихомониаз Урогенитальные заболевания, вызванные Mycoplasma genitalium Генитальный герпес Папилломавирусная инфекция Бактериальный вагиноз Урогенитальный кандидоз Клинические рекомендации разработаны специалистами : Дерматовенерологами Гинекологами Урологами КР-2012 – впервые носят междисциплинарный характер Диагноз заболевания устанавливается только на основе результатов лабораторных исследований Инфекция КР-2010 КР-2012 Сифилис Микроскопия, ПИФ, РМП, РПГА, ИФААТ, РИФ, РИБТ, ИБ Микроскопия, ПИФ, МБМ *, РМП, ИФА, РПГА, РИФ, ИБ, РИБТ Гонорея (N.gonorrhoeae) Микроскопия, Культ.иссл. Микроскопия, Культ.иссл., МБМ Хламидиоз (C.trachomatis ) Культ.иссл., МАНК, ПИФ, ИФА (±) МБМ, Культ.иссл. М. genitalium МАНК МБМ Трихомониаз (T.vaginalis) Микроскопия, Культ.иссл. Микроскопия, МБМ, Культ.иссл. Кандидоз Микроскопия, Культ.иссл. Микроскопия, Культ.иссл. МБМ (+вид.дифф) Бактериальный вагиноз кр. Амсель, микроскопия кр.Амсель, кр.Ньюджент, МБМ (Gv, Av., Mh, U) Генитальный герпес ПЦР, ДНК-гибр., Вирус.иссл., ПИФ, РНИФ, ИФААТ,РСК, РПГА МБМ, ИФААТ, Аног.бородавки ПЦР (+генотип), цитология МБМ (+генотип), цитология МБМ* - Молекулярно-биологические методы исследования, направленные на обнаружения специфических фрагментов ДНК и /или РНК с использованием тест-систем, разрешенных к медицинскому применению в РФ. Впервые вводят в разряд рекомендуемых методов диагностики всех ИППП молекулярно-биологические методы Но не определяют порядка проведения и требований к выполнению исследований Патогенные микроорганизмы и цель лечебных мероприятий – полная элиминации возбудителя Сходные симптомы и клинические проявления инфекции, но разные протоколы лечения Общий биотоп для локализации инфекции и общий материал для исследования Одинаковые факторы риска инфицирования и пути передачи Общие положения Требования к описанию стандартизованных технологий и стандартизованных оперативных процедур клинических лабораторных исследований 1. Цель исследования Установление единых требований к выполнению исследования по выявлению НК (ДНК и/или РНК) возбудителей ИППП NCMT с применением молекулярнобиологических методов в клиникодиагностических лабораториях 2. Требования к обеспечению выполнения технологии 2.1. Требования к специалистам и вспомогательному персоналу 2.2. Требования к обеспечению безопасности труда медицинского персонала 2.3. Материальные ресурсы, необходимые для выполнения технологии: приборы, средства измерения, лабораторное оборудование 2.4. Реактивы 2.5. Прочий расходуемый материал Зона приема, регистрации, разбора и первичной обработки материала Зона выделения нуклеиновых кислот из образцов биологического материала Зона приготовления реакционных смесей для проведения амплификации НК Зона проведения реакции амплификации НК Для проведения исследования могут быть использованы только наборы реагентов, зарегистрированные на территории РФ в установленном порядке Врачи клинической лабораторной диагностики, врачи-бактериологи, врачивирусологи, врачиэпидемиологи, биологи, прошедшие специализацию и периодическое повышение квалификации в установленном порядке. Указанные специалисты должны иметь удостоверение о краткосрочном повышении квалификации на лицензированных курсах «ПЦРдиагностика инфекционных заболеваний» или аналогичных. Противоэпидемический режим работы лаборатории при работе с микроорганизмами III-IV групп патогенности – СП 1.3.2322-08, Действия и работа персонала: соблюдение общих правил работы в молекулярно-биологических лабораториях (МУ 1.3.2569-09), стандартов по формированию и поддержанию безопасности рабочей среды в медицинских лабораториях при манипуляциях с пробами пациентов, химическими реактивами и другими объектами потенциальной опасности для здоровья людей (ГОСТ Р 52905-2007). Сбор, временное хранение, обеззараживание и транспортировка потенциально опасных отходов, загрязненных остатками биологического материала, образующихся в процессе выполнения технологии (СанПиН 2.1.7.2790-10). 3. Характеристика методик выполнения технологии 3.1. Взятие образцов биологического материала 3.2. Идентификация образца (направление) 3.3. Приемлемость образца 3.4. Описание хода выполнения данной стандартизованной технологии (СОП) 3.5. Описание стандартизованных оперативных процедур (принцип метода, этапы, линейность, чувствительность и специфичность, калибраторы) 4. Регистрация результатов Вид биологического материала Возбудитель Соскобное отделяемое слизистых N.gonorrhoeae, C.trachomatis, оболочек урогенитального тракта M.genitalium, T.vaginalis (влагалища, цервикального канала, уретры) Соскобное отделяемое слизистой N.gonorrhoeae, C.trachomatis ротоглотки Отделяемое конъюнктивы глаз N.gonorrhoeae, C.trachomatis Моча первая порция (для мужчин) N.gonorrhoeae, C.trachomatis, M.genitalium, T.vaginalis Секрет предстательной железы N.gonorrhoeae, C.trachomatis, M.genitalium, T.vaginalis Процедура получения Транспортировка Хранение фамилия и инициалы (код) пациента, возраст или дата рождения, пол, у женщин, день менструального цикла или срок беременности (недель), дата и время получения образца, вид биологического материала (например, моча, вагинальное отделяемое и др.) предварительный клинический диагноз, фамилия и инициалы врача, назначившего исследование. Выделение и очистка НК возбудителей ИППП-NCMT Проведение реакции амплификации и детекции продуктов Анализ и обработка результатов с выдачей лабораторного заключения Все этапы технологии должны выполняться в строгом соответствии с инструкцией к наборам реагентов. Метод выявления ДНК NCMT – полимеразная цепная реакция (ПЦР) с электрофоретической детекцией продуктов с гибридизационно-флуоресцентной детекцией «по конечной точке» с гибридизацционно-флуоресцентной детекцией в режиме реального времени Метод выявления РНК NCMT – реакция транскрипционной амплификации NASBA (Nucleic acid sequence-based amplification) с гибридизацционно-флуоресцентной детекцией в режиме реального времени 1.Внутренний контрольный образец (ВКО), рекомбинантный препарат ДНК или РНК в зависимости от типа аналита и методики. ВКО с известной концентрацией добавляется в каждую пробу на этапе выделения НК и в результате проходит через все этапы анализа одновременно с изучаемым биологическим образцом. ВКО служит контролем эффективности выделения, амплификации и детекции. 2.Отрицательный контрольный образец (ОКО) – образец, заведомо не содержащий искомый возбудитель. Служит для контроля возможной контаминации во время экстракции НК и при приготовлении амплификационных смесей. При тестировании более 10 клинических образцов рекомендуется параллельно тестировать не меньше двух ОКО. 3. Отрицательный контроль амплификации (К– ), образец, заведомо не содержащий нуклеиновых кислот искомого возбудителя, который служит для контроля возможной контаминации реактивов или оборудования продуктами амплификации предыдущих исследований. 4. Положительный контрольный образец (К+), образец, содержащий фрагмент генома исследуемого возбудителя, который служит для контроля качества реактивов, работы прибора, условий амплификации. Результаты исследования образцов биологического материала проводятся с учетом результатов исследования контрольных образцов Аналитическая чувствительность отражает минимальное количество аналита (ДНК или РНК) в мл образца, которое может быть обнаружено тестом в 100% случаев. Аналитическая чувствительность тестов, предназначенных для выявления возбудителей ИППП, как патогенных микроорганизмов, должна обеспечивать их выявление при наличии в биологическом материале в концентрации 103 геномных эквивалентов в мл и меньше. Аналитическая специфичность - способность теста определять данный конкретный аналит (напр., ДНК или РНК C.trachomatis) в окружении других аналогичных аналитов (например, ДНК или РНК других микроорганизмов, человека и др.). Аналитическая специфичность тестов, предназначенных для выявления ДНК или РНК возбудителей ИППП (N.gonorrhoeae, C.trachomatis, M.genitalium, T.vaginalis), до лжна составлять 100%. При использовании качественных методов для выявления ДНК или РНК возбудителей ИППП – NCMT представляется как: ДНК или РНК возбудителя «Обнаружена» ДНК или РНК возбудителя «Не обнаружена» 5. Обеспечение качества выполнения технологии 5.1. Внутрилабораторный контроль качества 6. Трудозатраты на выполнение технологии 5.2. Ведение регистрации контрольных мероприятий 5.3. Контроль качества материалов и оборудования 5.4. Внутрилабораторный контроль качества исследований 5.5. Внешняя оценка качества 5.6. Непрерывное образование специалистов Федеральный закон от 4 мая 2011 г. N 99-ФЗ "О лицензировании отдельных видов деятельности". Приказ Министерства здравоохранения и медицинской промышленности РФ № 8 от 19 января 1995 г «О развитии и совершенствовании деятельности лабораторий клинической микробиологии (бактериологии) лечебно-профилактических учреждений». Приказ Минздрава РФ № 380 25.12.1997 г. «О состоянии и мерах по совершенствованию лабораторного обеспечения диагностики и лечения пациентов в учреждениях здравоохранения Российской Федерации». Приказ Министерства здравоохранения и социального развития Российской Федерации (Минздравсоцразвития России) от 23 июля 2010 г. N 541н "Об утверждении Единого квалификационного справочника должностей руководителей, специалистов и служащих, раздел "Квалификационные характеристики должностей работников в сфере здравоохранения". ПРИКАЗ МЗ РФ от 20.12.2012 № 1183н «Об утверждении номенклатуры должностей медицинских работников и фармацевтических работников» ГОСТ Р 52905-2007 «Требования безопасности». ГОСТ Р 53079.1-2008 «Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть 1. Правила описания методов исследования». ГОСТ Р ИСО 15189-2009 «Лаборатории медицинские. Частные требования к качеству и компетентности». СП 1.3.2322-08 «Безопасность работы с микроорганизмами III-IV групп патогенности (опасности) и возбудителями паразитарных заболеваний». СанПиН 2.1.7.2790-10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами». МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Клинические рекомендации Российского общества дерматовенерологов и косметологов. Москва, 2012.– 112 с. [email protected] с пометкой: для САТ-NCMT