На правах рукописи КАРПЕЧЕНКО НАТАЛЬЯ ЮРЬЕВНА ДНК
advertisement

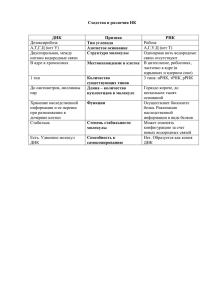
На правах рукописи КАРПЕЧЕНКО НАТАЛЬЯ ЮРЬЕВНА ДНК-ДНК ВЗАИМОДЕЙСТВИЯ В ОБЛАСТИ МИКРОСАТЕЛЛИТНЫХ ПОВТОРОВ КАК ФАКТОР ГЕНЕТИЧЕСКОЙ НЕСТАБИЛЬНОСТИ, ВОВЛЕЧЕННЫЙ В ПРОЦЕСС КАНЦЕРОГЕНЕЗА Онкология - 14.01.12 АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук Москва – 2014 Работа выполнена в Федеральном государственном бюджетном учреждении «Российский онкологический научный центр имени Н.Н. Блохина» Российской Академии Медицинских Наук Научный руководитель: Якубовская Марианна Геннадиевна – доктор медицинских наук, заведующий отделом химического канцерогенеза Научно-исследовательского института Канцерогенеза федерального государственного бюджетного учреждения «Российский онкологический научный центр имени Н.Н. Блохина» Российской Академии Медицинских Наук Официальные оппоненты: Журков Вячеслав Серафимович – доктор медицинских наук, ведущий научный сотрудник лаборатории генетического мониторинга федерального государственного бюджетного учреждения «Научно-исследовательский института экологии и гигиены окружающей среды имени А.Н. Сысина» Минздрава России Петренко Анатолий Анатольевич – кандидат биологических наук, молекулярный биолог лаборатории молекулярной патологии медицинского центра «Геномед» Ведущая организация: Государственное бюджетное образовательное учреждении высшего профессионального образования «Российской национальный исследовательский медицинский университет имени Н.И. Пирогова» Минздрава России Защита состоится «__» ___________ 2014 года в __:__ часов на заседании диссертационного совета Д 001.017.01 в Федеральном государственном бюджетном учреждении «Российский онкологический научный центр имени Н.Н. Блохина» Российской Академии Медицинских Наук по адресу: 115478, Москва, Каширское шоссе, дом 24 С диссертацией можно ознакомиться в библиотеке Федерального государственного бюджетного учреждения «Российский онкологический научный центр имени Н.Н. Блохина» Российской Академии Медицинских Наук по адресу: 115478, Москва, Каширское шоссе, дом 24 и на сайте www.ronc.ru Автореферат разослан «__» ___________2014 года Ученый секретарь диссертационного совета, профессор, доктор медицинских наук Ю.В. Шишкин 3 ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ Актуальность исследования Соматическая гомологичная рекомбинация (ГР) – один из ключевых механизмов поддержания стабильности генома клетки, обеспечивающий репарацию двунитевых разрывов ДНК. Дефекты данной репарационной системы повышают вероятность злокачественной трансформации клетки при действии генотоксических факторов и обнаруживаются в опухолевых клетках в виде хромосомных аберраций. Лежащее в основе ГР копирование генетической информации с гомологичной молекулы ДНК в ряде случаев сопровождается потерей гетерозиготности, что, в свою очередь, приводит к манифестации рецессивных мутаций, одному из наиболее распространенных процессов при канцерогенезе. Этот механизм лежит в основе патогенеза наследственной ретинобластомы и опухолей при синдроме Ли-Фраумени. Многочисленные данные свидетельствуют о неравномерном распределении по геному рекомбинационных событий. «Горячими» точками рекомбинации являются микросателлитные последовательности ДНК, наиболее распространенная из которых – poly(CA/TG). Механизмы, лежащие в основе влияния микросателлитных повторов на частоту ГР до настоящего времени остаются практически неизученными. Одним из возможных объяснений подобного влияния служит наличие конформационных особенностей в области микросателлитных повторов, влияющих на стадии инициации и (или) терминации ГР. Понимание механизмов влияния (CA/TG)n-повторов необходимо для выявления локусов с наибольшей предрасположенностью к потере гетерозиготности, что раскроет возможности для формирования групп риска и позволит более точно определять прогноз заболевания. Таким образом, изучение закономерностей ДНК-ДНК взаимодействий в области микросателлитных повторов является актуальной задачей современной молекулярной биологии и экспериментальной онкологии. Цели и задачи исследования Целью данного исследования являлось изучение важных для инициации и терминации ГР структурно-функциональных особенностей микросателлитных (CA/TG)nлокусов. Для достижения этой цели были поставлены следующие задачи: 1) оптимизация метода визуализации ДНК с использованием флуоресцентного красителя SYBR Gold (SG) по протоколу предокрашивания; 2) анализ влияния poly(CA/TG) на процесс миграции точки перекреста структур Холлидея; 3) изучение закономерностей 4 взаимодействия (инвазии) олигонуклеотидов d(СА)10 и d(GT)10 с гомологичным участком плазмидной ДНК, а также геномной ДНК олигонуклеотидной инвазии микросателлитные локусы: в другие, (CT/GA)n, человека; 4) анализ возможности также широко (AT/TA)n, распространенные, (CAG/GTC)n, (СТТ/GAA)n, (CGG/GCC)n, (GGT/CCA)n и (GGGT/CCCA)n. Научная новизна В настоящем исследовании впервые проведено изучение закономерностей ранее показанного в лаборатории М.Г. Якубовской встраивания олигонуклеотидов d(CA) 10 и d(TG)10 во внутреннюю комплементарную последовательность дуплексной ДНК. Установлено, что структурные особенности (CA/TG)n-повтора, лежащие в основе образования комплекса олигонуклеотид-ДНК, формируются in vivo и остаются стабильными на протяжении экстракции ДНК. Показано, что интенсивность инвазии одноцепочечных фрагментов последовательность d(CA)10 и сверхспирализованной микросателлитного d(GT)10 в (CA/TG)n-повторяющуюся плазмидной локуса ДНК зависит от следующим (CA/TG)31 = (CA/TG)94 > (CA/TG)10 > (CA/TG)15 = (CA/TG)25. длины образом: При изучении влияния мольного соотношения дуплекс/олигонуклеотид на интенсивность взаимодействия (CA/TG)n-локуса плазмидной ДНК с комплементарными одноцепочечными фрагментами, обнаружено повышение интенсивности инвазии олигонуклеотидов с увеличением соотношения от 1/10 до 1/1, при достижения которого, дальнейшего возрастания интенсивности встраивания не происходит. Установлено, что интенсивность взаимодействия микросателлитных локусов (CA/TG)31 с одноцепочечными фрагментами d(CA)10 и d(GT)10, не изменяется при использовании ряда солевых буферных растворов, однако снижается в безсолевых условиях. Кроме того, анализ возможности олигонуклеотидного встраивания в другие микросателлитные последовательности показал, что среди (GA/TC)n-, (TA/AT)n-, (CAG/GTC)n-, (CGG/GCC)n-, (CTT/GAA)n-, (GGT/CCA)n- и (GGGT/CCCA)n-повторов, такой способностью обладают только длинные (CTT/GAA)n-локусы, сверхспирализации формирующие неканоническую H-форму в ДНК. условиях В отрицательной рамках изучения функционирования (CA/TG)n-повторов в качестве точек терминиции ГР с помощью электронной микроскопии установлено, что гетерология между микросателлитными локусами (CA/TG)n в шесть повторяющихся единиц ингибирует миграцию ветвей 5 структуры Холлидея, промежуточного продукта рекомбинационного процесса, чего не наблюдается в случае полной гомологии. Кроме того, при проведении данного исследования предложен новый подход в использовании для визуализации ДНК флуоресцентного красителя SYBR Gold (SG), основанный на отсутствии влияния последнего на электрофоретическую подвижность ДНК при низких соотношениях SG / ДНК. Оптимизированный метод окрашивания нуклеиновых кислот позволяет более рационально использовать этот дорогостоящий краситель. Научно-практическая значимость исследования Настоящая работа посвящена изучению актуальной проблемы, касающейся молекулярных механизмов канцерогенеза. В данном оригинальном исследовании продемонстрированы закономерности взаимодействия дуплексной ДНК с одноцепоченым фрагментом в области микросателлитных повторов, объясняющие их функционирование в качестве «горячих» точек соматической ГР. Полученные данные о взаимодействии микросателлитных одноцепочечной ДНК, влиянии локусов на этот (CA/TG)n процесс c длины комплементарной повторяющейся последовательности и мольного соотношения дуплекс / олигонуклеотид, а также о способности гетерологии в области (CA/TG)n-повтора ингибировать миграцию ветвей структуры Холлидея расширяют представление о молекулярных механизмах рекомбинационной репарации и причинах генетической нестабильности. Результаты исследования важны для сравнительной оценки вероятности соматической ГР по различным повторяющимся последовательностям, что в перспективе должно позволить выявлять предрасположенность к потере гетерозиготности по определенным локусам и, соответственно, определять риск развития онкологического заболевания и способствовать составлению более точного прогноза его течения. Кроме того, оптимизированный в ходе данной работы протокол использования флуоресцентного красителя ДНК SYBR Gold расширяет возможности его применения в молекулярнобиологических исследованиях, позволяя в целом ряде случаев избежать использования мутагенных и токсичных соединений. Методы исследования Работа выполнена с использованием классических молекулярно-биологических методов исследования (полимеразная цепная реакция, культивирование бактериальных 6 клеток, выделение и очистка ДНК из клеток и тканей, молекулярное клонирование, электрофоретическое разделение ДНК в агарозном геле), электронной микроскопии и статистической обработки полученных данных. Кроме того, в настоящей работе для изучения ДНК-ДНК взаимодействий, наряду с введением радиоактивной метки, применен более современный подход, основанный на использовании флуоресцентномеченных олигонуклеотидов и флуоресцентного красителя последнего поколения SYBR Gold. Положения, выносимые на защиту В структуре микросателлитных (CA/TG)n-локусов in vivo возникают 1. конформационные особенности, обуславливающие возможность их спонтанного взаимодействия с одноцепочечными фрагментами d(CA)10 и d(GT)10. Среди других микросателлитных локусов способностью к спонтанному 2. взаимодействию с гомологичной одноцепочечной ДНК обладают только длинные (CTT/GAA)n-повторы, формирующие в условиях отрицательной сверхспирализации неканоническую H-форму ДНК. Интенсивность взаимодействия d(CA)10 и d(GT)10 с (CA/TG)n-локусом 3. дуплексной ДНК зависит от длины повтора, соотношения дуплекс / олигонуклеотид и солевых условий. Обладающие полной гомологией (СА/TG)n-микросателлитные локусы не 4. влияют на миграцию ветвей структуры Холлидея, промежуточного продукта гомологичной рекомбинации, в то время как гетерология в области повторяющейся последовательности ингибирует данный процесс, что может способствовать ее ферментативному разрешению в этих участках генома. 5. Оптимизированный в ходе данной работы протокол визуализации ДНК с помощью флуоресцентного красителя последнего поколения SYBR Gold позволяет сократить финансовые и временные затраты на этапе пробоподготовки ДНК и избежать использования токсичных и мутагенных соединений. Апробация результатов Результаты работы были представлены 28 сентября 2012 года на совместной научной конференции лабораторий отдела химического канцерогенеза, лабораторий отдела трансформирующих генов опухолей, лаборатории онкогеномики и лаборатории молекулярной эндокринологии НИИ Канцерогенеза ФГБУ «РОНЦ им. Н.Н. Блохина» 7 РАМН. Основные положения диссертации представлены на 4 международных научных конференциях. По теме диссертации опубликовано 8 печатных работ. Структура и объем диссертационной работы Диссертация изложена на 131 страницах машинописного текста и содержит следующие разделы: введение, обзор литературы, экспериментальную часть, включающую изложение и обсуждение результатов, заключение, выводы и список цитируемой литературы. Материал иллюстрирован 25 рисунками и 9 таблицами. Библиографический указатель включает 197 цитированных работ. СОДЕРЖАНИЕ РАБОТЫ 1. SYBR Оптимизация метода визуализации ДНК с помощью флуоресцентного красителя SYBR Gold по протоколу предокрашивания Gold (SG) - наиболее чувствительный флуоресцентный краситель нуклеиновых кислот, важным достоинством которого является возможность его применения для препаративного электрофореза с использованием ДНК в последующих экспериментах, что представляется актуальным при изучении ДНК-ДНК взаимодействий. В виду влияния SG на электрофоретическую подвижность ДНК фирмой-производителем рекомендовано применение процедуры постокрашивания, однако такой подход требует большого количества этого дорогостоящего красителя и характеризуется невысоким качеством получаемых электрофореграмм. Таким образом, первоочередной задачей настоящего исследования являлась оптимизация протокола предокрашивания с SG при проведении агарозного гель-электрофореза. При описании различных флуоресцентных красителей ДНК определяющей характеристикой принято считать соотношение краситель / ДНК (отношение количества молекул красителя к числу пар оснований ДНК). Поскольку молярная концентрация SG, в поставляемых фирмой «Invitrogen» (США), растворах не раскрывается, в настоящем исследовании для определения этого параметра использовался коэффициент экстинкции минимально возможный для данной группы соединений (50000 М-1) как это делали другие авторы (Cosa et al., 2001). Таким образом, на основании выполненных спектрофотометрических измерений, концентрация SG в поставляемом фирмой растворе (10000-кратный) должна составляет порядка 1,3 х 10-2 М. Это значение и используется в дальнейшем для расчета соотношений краситель / ДНК в анализируемых растворах. 8 1.1. Определение стабильности комплекса SG - ДНК при проведении агарозного гель-электрофореза Одним из важнейших критериев возможности использования красителя для предокрашивания является стабильность образуемого им с ДНК комплекса в условиях проведения электрофореза. Устойчивость комплекса SG - ДНК в настоящей работе определялась на основании измерения скорости его движения в агарозном геле, а также по изменению интенсивности флуоресценции данного комплекса с течением времени. В результате серии экспериментов было показано, что скорость движения комплекса SG ДНК оставалась постоянной, по крайней мере, на протяжении 3-х часов проведения электрофореза и составляла 5,26 ± 0,04 мм/час при соотношении краситель / ДНК 1/25 и 4,86 ± 0,04 мм/час при соотношении 2/5. Полученные данные свидетельствуют о высокой стабильности комплекса SG - ДНК, поскольку вымывание красителя неизбежно привело бы к изменению скорости движения молекул ДНК (рис. 1). Кроме того, сравнение электрофореграмм, полученных после 1, 2 и 3 часов проведения электрофореза не выявило уменьшения интенсивности свечения полос геля, содержащих исследуемый комплекс. Соотношения SG/ДНК: 1 - 1/25; 2 – 2/5; М – маркер молекулярной массы λ/BstEII (1000 нг). Внизу указано время в минутах от начала эксперимента. Рисунок 1 - Электрофореграммы ДНК, окрашенной SYBR Gold, при проведении электрофореза в течение различных интервалов времени Выявление несвязавшегося с ДНК SG в растворах при различных количественных соотношениях краситель / ДНК В рамках оптимизации метода предокрашивания с SG необходимо было оценить 1.2. количество красителя, способного провзаимодействовать с ДНК. Выявление несвязавшегося с ДНК SG осуществлялось двумя способами. В первом случае - путем измерения спектров поглощения растворов, полученных после удаления из них уже сформировавшихся комплексов SG - ДНК, что достигалось методом центрифугирования на колонках Microcon YM-30 («Millipore», США). В результате было показано, что, свободный краситель обнаруживается в фильтратах образцов, где изначально 9 соотношение краситель / ДНК составляло 8/1 и 4/1. Их оптическая плотность равна 0,43 и 0,40 соответственно. В то же время, оптическая плотность фильтрата, где первоначальное соотношение краситель / ДНК было 4/5, оказалась всего 0,0034, что составляет менее 1% исходной концентрации (рис. 2А). А. Спектры поглощения фильтратов растворов: 1 – 3 мкл стокового раствора SG в 400 мкл ТЕбуфера1; 2 – тот же раствор с добавлением 3 мкг геномной ДНК; 3 – тот же раствор с добавлением 6 мкг геномной ДНК; 4 – тот же раствор с добавлением 30 мкг геномной ДНК. Б. Электрофореграммы ДНК: 1-4 – 500 нг ПЦР-продукта размером 464 п.о.2, окрашенного фильтратом, полученным после удаления уже сформированного комплекса SG - ПЦР-продукт 1129 п.о. (500 нг); 5-8 – ранее образовавшийся комплекс SG - ПЦР-продукт 1129 п.о.; 1,5 - 2,5 нл; 2,6 - 25 нл; 3,7 - 50 нл; 4,8 - 250 нл стокового раствора красителя. Рисунок 2 - Определение несвязавшегося с ДНК SYBR Gold в растворах после удаления комплекса краситель - ДНК Во-втором случае, несвязавшийся с ДНК SG выявлялся в фильтрате путем повторного окрашивания вновь добавленного фрагмента ДНК. Электрофореграмма, представленная на рисунке 2Б, свидетельствует о том, что окрашивание вновь добавленной ДНК в фильтратах образцов не происходит, если соотношение краситель / ДНК в образце до фильтрации не превышает 4/5. Суммируя все полученные данные, можно сделать вывод, что в растворах ДНК с низкими значениями соотношения 1 2 TE-буфер: 10 мM Tрис-HCl, 1 мM ЭДТА, pH 7.6 п.о. – пары оснований 10 SG/ ДНК практически весь краситель должен находиться в комплексе с нуклеиновой кислотой. Зависимость электрофоретической подвижности окрашенной ДНК от соотношения SG/ ДНК Для выявления характера влияния SG на скорость ДНК в агарозном геле, проведено 1.3. сравнение электрофоретической подвижности ДНК, окрашенной до проведения электрофореза и после него. Для этого в ходе эксперимента были приготовлены серии проб объемом по 10 мкл каждая, содержащие различное количество очищенного ПЦРпродукта размером 1129 п.о. (пар оснований) и SG в количестве эквивалентном его содержанию в 5 нл стокового раствора. Сравнение электрофореграмм показало, что снижения электрофоретической подвижности не наблюдалось в пробах, где соотношение краситель/ДНК было меньше или равно 1/25 (рис. 3). А. Электрофореграмма ДНК (предокрашивание). Б. Электрофореграмма ДНК (постокрашивание). Количество ПЦР-продукта в образцах: 1 - 2000 нг, 2 – 1000 нг, 3 – 500 нг, 4 – 250 нг, 5 – 100 нг, 6 – 50 нг, 7 – 20 нг. М – 1000 нг маркера молекулярной массы λ/BstEII. Рисунок 3 - Визуализация ДНК с использованием SYBR Gold по протоколам пред- и постокрашивания Для более полного представления о характере влияния SG на подвижность окрашенной им ДНК проанализирована электрофоретическая подвижность фракций ДНК, содержащих 1000, 100 и 10 нг ПЦР-продукта размером 1129 п.о. при трех значениях соотношения краситель/ДНК (1/50; 1/25 и 2/5). На электрофореграмме представлены данные об отсутствии влияния SG на подвижность ДНК при соблюдении соотношения краситель/ДНК 1/50 и 1/25 (рис. 4). При соотношении же краситель/ДНК равном 2/5 уменьшение электрофоретической подвижности наблюдается во всех пробах, причем, снижение электрофоретической подвижности возрастает с увеличением количества ДНК в пробе (рис. 4, дорожки 7-9). 11 М – маркер молекулярной массы λ/BstEII, 1000 нг. Количество ПЦР-продукта длиной 1129 п.о.: 1,4,7 - 1000 нг; 2,5,8 - 100 нг; 3,6,9 - 10 нг. Соотношения краситель/ДНК 1-3 - 1/50; 4-6 - 1/25; 7-9 - 2/5. Рисунок 4 - Электрофоретическая подвижность ДНК в зависимости от соотношения SG/ДНК Таким образом, полученные данные свидетельствуют об отсутствии изменений подвижности ДНК при образовании комплексов с SG, если соотношение краситель/ДНК не превышает 1/25, что позволяет использовать данный высокоэффективный краситель по протоколу предокрашивания для образцов с известным количеством ДНК. 2. Изучение структурно-функциональных особенностей (СА/TG)n-повторов, важных для процессов инициации и терминации гомологичной рекомбинации Poly(CA/TG) – один из наиболее распространенных микросателлитных повторов млекопитающих, включая человека. Многочисленные данные свидетельствуют об их функционировании в качестве «горячих» точек рекомбинации (Wahls, 1998; Majewski et al., 2000). Однако, механизм влияния (CA/TG)n-повторов на этот процесс остается неизвестным. Вероятнее всего он связаны со структурными особенностями данной последовательности ДНК. В настоящей работе продолжено, ранее начатое в лаборатории М.Г. Якубовской, изучение этих особенностей с точки зрения процессов инициации и терминации ГР. 2.1. Анализ влияния poly(CA/TG) на процесс миграции точки перекреста структур Холлидея Изучение влияния СА-микросателлитов на процесс «миграции ветвления» структур Холлидея осуществлялось с помощью модельной системы, основанной на образовании симметричных крестообразных структур ДНК в высококонцентрированных водных растворах гомологичных линейных дуплексов (Yakubovskaya et al., 2001). Полученные, таким образом, популяции структур Холлидея визуализировались с помощью электронной микроскопии и подразделялись на три группы исходя из расположения 12 точки перекреста (рис. 5) с последующим проведением статистической обработки полученных данных. А. Схема строения дуплексной ДНК, образующей анализируемые структуры Холлидея. Б. Электронная микрофотография контрольной фракции дуплексной ДНК. В. Электронная микрофоторгафия структур Холлидея. Цифрами I, II и III обозначена локализация точек перекреста структур Холлидея, лежащая в основе их распределения по группам. Увеличение в 10000 раз. Рисунок 5 - Формирование структур Холлидея линейными фрагментами ДНК 13 Анализ локализации точки перекреста в популяциях структур Холлидея, образованных ПЦР-продуктами. Статистический анализ показал, что в популяции структур Холлидея, образованных фрагментами неповторяющейся последовательности, максимальное число крестообразных структур принадлежит I группе. Во фракции же структур Холлидея, образованных дуплексами, содержащими (CA/TG)31-повтор, максимальное число структур принадлежит II группе с локализацией точек перекреста в районе повтора (таблица 1). Таблица 1 - Локализация точки перекреста в популяциях структур Холлидея, образованных ПЦР-продуктами Структуры Холлидея Содержащие (СА/TG)31-повтор, % Рэндомная последовательность, % 38,4 ± 5,8* 49,1 ± 3,71* 52,27 ± 4,94** 38,2 ± 2,52** 9,3 ± 3,75 12,1 ± 3,07 I – структуры Холлидея с локализацией точки перекреста ветвей в области 1248 п.о. II – структуры Холлидея с локализацией точки перекреста ветвей в области 248496 п.о. III – структуры Холлидея с локализацией точки перекреста ветвей в области 496745 п.о. *, ** - различия статистически значимы (р<0,01) Анализ локализации точки перекреста в популяциях структур Холлидея, образованных фрагментами плазмидной ДНК. Статистический анализ полученных данных показал, что как во фракциях структур Холлидея, образованных (CA/TG) 31содержащими фрагментами плазмиды, так и плазмидными фрагментами, содержащими повторов, большинство структур принадлежит I группе (таблица 2). не 14 Таблица 2 - Локализация точки перекреста в популяциях структур Холлидея, образованных фрагментами плазмидной ДНК Содержащие (СА/TG)31повтор, % Рэндомная последовательность, % 58,7 ± 12,27 60,7 ± 9,51 24,03 ± 7,87 23,4 ± 8,45 13,5 ± 8,2 15,9 ± 7,68 Структуры Холлидея I – структуры Холлидея с локализацией точки перекреста ветвей в области 1150 п.о. II – структуры Холлидея с локализацией точки перекреста ветвей в области 150300 п.о. III – структуры Холлидея с локализацией точки перекреста в области 300450 п.о. Анализ локализации точки перекреста в популяциях структур Холлидея, образованных фрагментами плазмидной ДНК, несущими разное число (СА/TG)nповторов. Анализ данных электронной микроскопии показал, что локализация точки перекреста в области повторяющейся последовательности встречается достоверно чаще в популяции структур Холлидея, имеющих (CA/TG)25/31-гетерологию, по сравнению со структурами, образованными полностью гомологичными дуплексами (таблица 3). Таблица 3 - Локализация точки перекреста в популяциях структур Холлидея, образованных фрагментами плазмидной ДНК, несущими (СА/TG)n-повторы с разным числом повторяющихся единиц Структуры Холлидея I – структуры Холлидея с локализацией точки перекреста ветвей в области 1150 п.о. II – структуры Холлидея с локализацией точки перекреста ветвей в области 150300 п.о. III – структуры Холлидея с локализацией точки перекреста ветвей в области 300450 п.о. Содержащие (СА/TG)31/25-повтор, % Содержащие (СА/TG)25-повтор, % 53,8 ± 2,3* 66 ± 5,42* 34,76 ± 3,92** 20,5 ± 5,65** 8,55 ± 2,27 13,5 ± 4,74 *, ** - различия статистически значимы (р<0,01) Таким образом, по результатам исследования можно сделать вывод, о том, что гетерология в области (CA/TG)n-локуса ингибирует миграцию ветвей структуры 15 Холлидея, промежуточного продукта гомологичной рекомбинации, и, тем самым, может способствовать ее ферментативному разрешению в этих участках генома. 2.2. Особенности олигонуклеотидной инвазии во внутреннюю комплементарную последовательность дуплексной ДНК Ранее продемонстрирован феномен инвазии олигонуклеотидов d(CA)10 и d(TG)10 в линейную и кольцевую молекулы ДНК, содержащие (CA/TG)31-последовательность (Гасанова и др., 2010). При этом в случае неповторяющейся последовательности подобное взаимодействие обнаружено не было. Полученные данные свидетельствуют о существовании конформационных особенностей в области (CA/TG)n-повтора, по всей видимости, лежащие в основе синаптической стадии ГР. Соответственно, представляло интерес дальнейшее изучение этого феномена. 2.2.1. Оптимизация метода визуализации ДНК-ДНК взаимодействий с помощью флуоресцентно меченных олигонуклеотидов Во всех предыдущих исследованиях, касающихся ДНК-ДНК взаимодействий для визуализации олигонуклеотидной инвазии в дуплексную ДНК олигонуклеотиды, содержащие на 5'-конце радиоактивный фосфор использовались 32 Р. В настоящей работе оптимизирован более современный подход, основанный на введении в состав олигонуклеотида флуоресцентной метки. В ходе оптимизации были выбраны два флуоресцентных красителя: карбоксифлуоресцеин (FAM) и тетраметилкарбоксиродамин (TAMRA), а в качестве модели - ранее изученное В.К. Гасановой встраивание олигонуклеотида в комплементарный концевой участок линейного дуплекса случайной последовательности (Гасанова и др., 2005). В результате было показано, что расположение флуоресцентного красителя на 3'-конце, как в случае FAM, так и TAMRA, препятствует встраиванию олигонуклеотида в комплементарный ему концевой участок ПЦР-продукта (рис. 6). Таким образом, в ряде последующих экспериментов по изучению олигонуклеотидной инвазии использовались олигонуклеотиды, несущие TAMRA на 5'конце (далее обозначенные как 5'T), так как, в отличие от FAM, данный краситель был менее подвержен фотовыцветанию. 16 I – электрофореграмма, II –скан геля3, III - олигонуклеотиды, меченные флуоресцентным красителем. М – маркер молекулярной массы λ/BstEII (1000 нг). ПЦР-продукт (800 нг) инкубировался4 со следующими олигонуклеотидами: 1 - 3'-метка- PUC19-VSP-S, 2 - 5'-меткаPUC19-VSP-S, 3 - Ki-ras-3'-метка, 4 - Ki-ras-5'-метка; олигонуклеотиды 1,2 – комплементарны концевому участку линейного дуплекса, 3,4 - не комплементарны концевому участку линейного дуплекса. Рисунок 6 - Визуализация инвазии в линейный концевой участок ПЦР-продукта олигонуклеотидов, меченных флуоресцентными красителями TAMRA (A) или FAM (Б) 2.2.2. Инвазия олигонуклеотидов d(CA)10 и d(TG)10 в эукариотическую ДНК Ранее исследования по изучению закономерностей олигонуклеотидной инвази выполнялись с использованием прокариотической (плазмидной) ДНК. В настоящей работе в рамках дальнейшего исследования особенностей встраивания олигонуклеотидов d(CA)10 и d(TG)10 во внутренний комплементарный участок дуплексной ДНК проведен анализ возможности инвазии d(CA)10 и d(TG)10 в ДНК эукариот. В качестве объекта исследования была выбрана геномная ДНК, выделенная из нормальной и опухолевой тканей молочной железы и обработанная эндонуклеазами рестрикции HindIII или EcoRI («СибЭнзим», Россия). В результате эксперимента встраивание в геномную ДНК показано для олигонуклеотида 5′T-d(TG)10 (рис. 7, дорожки 3,5,7), в то время как инвазии 5′T-d(CA)10 обнаружено не было (рис. 7, дорожки 2,4,6). 3 Получен с помощью лазерного сканера гелей высокого разрешения Typhoon (GE Healthcare, Германия). 4 Здесь и далее инкубация проводилась в буфере, содержащем 6 мM Трис-HCl, 1 мM ЭДТА, 300 мM NaCl (pH 7.5), при 37°С в течение суток. 17 Электрофореграмма (вверху) и скан геля (внизу) геля: М – маркер молекулярной массы λ/BstEII (1000 нг); геномная ДНК (2000 нг) инкубировалась: 1 – без олигонуклеотида; 2, 4, 6 – с 5′Td(CA)10; 3, 5, 7 – с 5′T-d(TG)10. Количество олигонуклеотида - 17 пмоль на пробу. Рисунок 7 - Инвазия олигонуклеотидов 5′T-dCA10 и 5′T-dTG10 в эукариотическую геномную ДНК, обработанную эндонуклеазами рестрикции HindIII (А) и EcoRI (Б) 2.2.3. Олигонуклеотидная инвазия в ди-, три- и тетрануклеотидные последовательности Для того чтобы понять, является ли олигонуклеотидная инвазия свойством всех микросателлиных последовательностей, или она характерна только для poly(CA/TG), проанализирована возможность подобного взаимодействия в области ди-, три- и тетрануклеотидных повторов. В ходе первого эксперимента оценивалась возможность олигонуклеотдного встраивания в геномную ДНК, полученную из опухолевой и нормальной тканей молочной железы. При этом, были выбраны следующие олигонуклеотиды: 5′T-d(CT)10, 5′T-d(GA)10, 5′T-d(AT)10, 5′T-d(CCA)7, 5′T-d(GGT)7, 5′Td(CCCA)5 и 5′T-d(GGGT)5. В результате эксперимента встраивания ни одного из вышеуказанных олигонуклеотидов в геномную ДНК обнаружено не было, в то время как инвазия 5′T-d(GT)10 выявлялась на обычном уровне (рис. 8). Электрофореграмма (вверху) и скан геля (внизу) геля: М – маркер молекулярной массы λ/BstEII (1000 нг); геномная ДНК (2000 нг) инкубировалась: 1 - с олигонуклеотидом случайной последовательности 5′T-Ki-ras, 2 – 5′T-d(GA)10, 3 – 5′T-d(CT)10, 4 – 5′T-d(AT)10, 5 – 5′T-d(CCA)7, 6 – 5′T-d(GGT)7, 7 – 5′T-d(CCCA)5, 8 – 5′T-d(GGGT)5, 9 – 5′T-d(GT)10. Количество олигонуклеотида – 17 пмоль на пробу. Рисунок 8 - Инвазия олигонуклеотидов различных повторяющихся последовательностей в эукариотическую геномную ДНК 18 Для второго эксперимента использовались плазмиды, содержащие следующие последовательности: (CAG/GTC)80, (CGG/GCC)40, (CTT/GAA)20 и (CTT/GAA)114. Данные плазмиды инкубировались с радиоактивно меченными олигонуклеотидами (далее обозначенные как d(X)*), комплементарными повторяющейся последовательности дуплексной ДНК. В результате было показано, что формирование комплекса происходит лишь в случае совместной инкубации d(GAA)7* с плазмидой, содержащей (CTT/GAA)114повтор. Полученный результат хорошо согласуется с литературными данными о способности длинных (CTT/GAA)n-последовательностей образовывать неканоническую H-форму ДНК, при которой (CTT)-нить остается свободной и доступной для взаимодействия. I Электрофореграмма, II авторадиограмма комплекса, III авторадиограмма олигонуклеотидов. М - маркер молекулярной массы λ/BstEII (1000 нг). Плазмиды содержат следующие повторы: 1,2 – (CAG)80; 3,4 – (CGG)40; 5,6 – (CTT)20; 7,8 – (CTT)114. Радиоактивно меченные олигонуклеотиды: 1 – d(CAG)7*; 2 – d(CTG)7*; 3 – d(GCC)7*; 4 – d(CGG)7*; 5,7 – d(CTT)7*; 6,8 – d(GAA)7*. Рисунок 9 - Олигонуклеотидная инвазия в плазмиды, содержащие тринуклеотидные повторы 2.2.4. Анализ возможности олигонуклеотидной инвазии в (CA/TG)nпоследовательность дуплексной ДНК после удаления ранее сформированного комплекса Для того чтобы понять являются ли структурные особенности (CA/TG)n-повтора, лежащие в основе олигонуклеотидной инвазии, его динамической характеристикой или они формируются только в условиях in vivo проведено исследование, в рамках которого, изучалась возможность повторного образование межмолекулярных комплексов после удаления из раствора уже сформированных (рис. 10). В результате было показано, что повторного образования комплекса ДНК-олигонуклеотид ни в случае d(CA)10*, ни в случае d(TG)10* не происходит (рис. 10Б, дорожки 3,4,7,8). Полученные данные свидетельствуют о том, что структурные особенности (CA/TG)n-последовательности, 19 обуславливающие возможность олигонуклеотидной инвазии, возникают в клетке и остаются стабильными на протяжении процесса выделения ДНК. А. Схема проведения эксперимента. Б. Электрофореграмма (вверху) и авторадиограмма (внизу) геля. М – маркер молекулярной массы λ/BstEII (1000 нг). 1-6 – линеаризованная плазмида pE105, 7-10 - плазмида pE10. Инкубация дуплексной ДНК с радиоактивно меченным олигонуклеотидом d(CA)10*: 1, 3, 5, 7, 9; инкубация дуплексной ДНК с радиоактивно меченным олигонуклеотидом d(TG)10*: 2, 4, 6, 8, 10. Первая инкубация дуплексной ДНК со следующими биотинилированными олигонуклеотидами: ki-ras-biotin-5' – 1, 2; d(CA)10-biotin-5' – 3, 7; d(TG)10-biotin-5' – 4, 8; без олигонуклеотидов – 5, 6, 9, 10. Рисунок 10 - Анализ встраивания олигонуклеотидов dCA10* и dTG10* в дуплексную ДНК, содержащую (CA/TG)31-повтор, после удаления ранее сформированного комплекса 5 Плазмида pE10 является производной плазмиды PUC19, содержащей (CA/TG)31-повтор. 20 2.2.4. Встраивание олигонуклеотидов d(CA)10 и d(TG)10 в дуплексную ДНК с разной длиной (CA/TG)n-повтора Проведен анализ влияния длины (CA/TG)n-повтора дуплексной ДНК на процесс олигонуклеотидной инвазии. С этой целью предварительно была получена коллекция плазмид, производных PUC19, содержащих разное число повторов, а именно: (CA/TG) 10, (CA/TG)15, (CA/TG)25, (CA/TG)31 и (CA/TG)94. В результате анализа показано, что инвазия 5′T-d(CA)10 или 5′T-d(TG)10 олигонуклеотидов происходит в комплементарную повторяющуюся последовательность плазмидной ДНК при любой длине poly(CA/TG), но с разной интенсивностью. А именно, наблюдается резкое снижение интенсивности флуоресценции в случае плазмид, содержащих (CA/TG)15- и (CA/TG)25-повторы (рис. 11, дорожки 3,4), по сравнению с теми, которые несли (CA/TG)10, (CA/TG)31 и (CA/TG)94 (рис. 11, дорожки 2, 5, 6). I – электрофореграмма, II – скан геля, III – скан олигонуклеотидов, меченных TAMRA по 5'концу. А. Инкубация плазмид с 5′T-d(TG)10. Б. Инкубация плазмид с 5′T-d(CA)10. Количество повторов в плазмидах: 1 – без повторов, 2 - (CA/TG)10, 3 - (CA/TG)15, 4 - (CA/TG)25, 5 - (CA/TG)31, 6 - (CA/TG)94. М – маркер молекулярной массы λ/BstEII (1000 нг). Рисунок 11 - Инвазия 5′T-d(CA)10 и 5′T-d(TG)10 олигонуклеотидов в плазмиды, содержащие разное число (CA/TG)n-повторов 2.2.5. Зависимость интенсивности инвазии олигонуклеотидов d(CA)10 и d(TG)10 в плазмиду, содержащую (CA/TG)31-повтор, от мольного соотношения плазмида / олигонуклеотид В рамках изучения особенностей встраивания олигонуклеотидов d(CA)10 и d(TG)10 в комплементарную повторяющуюся последовательность дуплексной ДНК, проведен анализ влияния ДНК / олигонуклеотид. на этот процесс мольного В ходе проведения исследования соотношения плазмидная показано, что количество 21 олигонуклеотидов, встроившихся в дуплекс, возрастает с повышение соотношения дуплекс / олигонуклеотид от 1/10 до 1/1, после достижения которого происходит выход на плато без дальнейшего повышения интенсивности встраивания (рис. 12). I – электрофореграмма, II –скан геля, III - олигонуклеотиды, меченные TAMRA по 5'-концу. Мольное соотношение плазмида/олигонуклеотид: 1,6 – 1/50; 2,7 – 1/20; 3, 8 – 1/1; 4, 9 – 5/1; 5, 10 – 10/1. Плазмида инкубировалась с 5′T-d(CA)10: 1-5 и 5′T-d(TG)10: 6-10. Рисунок 12 - Интенсивности инвазии олигонуклеотидов 5′T-d(CA)10 и 5′T-d(TG)10 в плазмиду, содержащую (CA/TG)31-повтор, от мольного соотношения плазмида/олигонуклеотид 2.2.6. Олигонуклеотидная инвазия в разных солевых условиях Принимая во внимания, что одним из возможных объяснений олигонуклеотидной инвазии в области CA-микросателлитов является способность данной повторяющейся последовательностью формировать неканонические формы ДНК, образование которых сильно зависит от условий микроокружения, проведено сравнение интенсивности встраивания dCA10 и dTG10 при различных солевых условиях. В результате этого исследования было показано, что интенсивность олигонуклеотидной инвазии остается практически постоянной при использовании ряда солевых растворов, однако снижается в бессолевых условиях (рис. 13). 22 А. 30-кратный мольный избыток 5′T-d(CA)10 по отношению к плазмиде (вверху – элктрофореграмма, внизу – скан геля). Б. Эквимолярное количество 5′T-d(CA)10 по отношению к плазмиде (вверху – элктрофореграмма, внизу – скан геля). М – 1000 нг маркера молекулярного веса λ/BstEII. К – плазмида UC-CA31, инкубированная без олигонуклеотида в TES-буфере. Условия инкубации: 1 – dd, 2 - TE-буфер, 3 - TES-буфер, 4 - TSM-буфер, 5 – PBS, 6 - G-буфер6. Рисунок 13 - Инвазия олигонуклеотида 5′T-d(CA)10 в плазмиду, содержащую (CA/TG)31повтор в разных солевых условиях ВЫВОД 1. Микросателлитные спонтанному взаимодействию локусы с (CA/TG)n обладают одноцепочечной ДНК способностью d(GT)10, что к было продемонстрировано на сверхспирализованной, релаксированной и линеаризованной плазмидной ДНК, а также геномной ДНК человека. 2. Среди других микросателлитных локусов, а именно, (GA/TC)n, (TA/AT)n, (CAG/GTC)n, (CGG/GCC)n, (CTT/GAA)n, (GGT/CCA)n и (GGGT/CCCA)n, способностью к спонтанному взаимодействию с гомологичной одноцепочечной ДНК обладают только длинные (CTT/GAA)n-повторы, формирующие в условиях отрицательной сверхспирализации неканоническую H-форму ДНК. 3. Топологические особенности ДНК в области микросателлитных локусов (CA/TG)n, определяющие их способность к взаимодействию с одноцепочечными фрагментами d(CA)10 и d(GT)10, формируются in vivo. 4. При изучении влияния длины повторяющегося локуса (CA/TG)n, находящегося в составе сверхспирализованной плазмидной ДНК, на особенности встраивания в дуплекс одноцепочечных фрагментов d(СА)10 и d(GT)10 было установлено, 6 TE-буфер (10 мM Tрис-HCl, 1 мM ЭДТА, pH 7.6), TES-буфер (6 мM Трис-HCl, 1 мM ЭДТА, 300 мM NaCl, pH 7.5), TSM-буфер (6 мM Трис-HCl, 300 мM NaCl, 6 мM MgCl2, pH 7.8), PBS (137 мМ NaCl, 2,7 мM KCl, 10 мM Na2HPO4, 1,76 мM KH2PO4, pH 7.4), G-буфер (20 мM HEPES, 140 мM NaCl, 50 мM KCl, pH 7.3). 23 что интенсивность ДНК-ДНК взаимодействия убывает в ряду: (CA/TG)31 = (CA/TG)94 > (CA/TG)10 > (CA/TG)15 = (CA/TG)25. Интенсивность 5. взаимодействия сверхспирализованной плазмидной микросателлитных локусов (CA/TG)31 ДНК с комплементарными одноцепочечными фрагментами зависит от их мольного соотношения и возрастает с повышением соотношения дуплекс / олигонуклеотид от 1/10 до 1/1, после достижения которого, выходит на плато. Интенсивность взаимодействия микросателлитных локусов (CA/TG)31 с 6. одноцепочечными фрагментами d(CA)10 и d(GT)10, не изменяется при использовании ряда солевых буферных растворов, однако снижается в беcсолевых условиях. Обладающие полной гомологией (СА/TG)n-микросателлитные локусы не 7. влияют на миграцию ветвей структуры Холлидея, промежуточного продукта гомологичной рекомбинации, в то время как гетерология в области повторяющейся последовательности ингибирует данный процесс, что может способствовать ее ферментативному разрешению в этих участках генома. 8. Флуоресцентный краситель нуклеиновых кислот SYBR Gold не влияет на электрофоретическую подвижность ДНК при его низких соотношениях с биополимером, что позволило оптимизировать протокол визуализации ДНК и сократить финансовые и временные затраты на этапе пробоподготовки ДНК и избежать использования токсичных и мутагенных соединений при проведении исследования. СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ 1. Gasanova, V. Homology-mediated oligonucleotide invasion into the repetitive region of linear and supercoiled DNA / V. Gasanova, N. Karpechenko, G. Belitsky, C. Gaillard, F. Strauss, N. Dolinnaya, M. Yakubovskaya // FASEB, Biological consequence of alternatively structured DNA, Abstractbook – 2010. – p. 39. 2. Karpechenko, N. Peculiarities of SYBR Gold-DNA interaction which are important for nucleic acid visualization / N. Karpechenko, E. Lesovaya, V. Gasanova, A. Ivanov, K. Kirsanov, G. Belitsky, M. Yakubovskaya // The Biophysical Society 55th Annual Meeting Abstractbook – 2011. – p. 213. 3. Gasanova, V. Invasion of d(CA)10- and d(TG)10-oligonucleotides into (CA/TG)31- repetitive region of linearized and supercoiled plasmid / V. Gasanova, N. Karpechenko, C. 24 Gaillard, F. Strauss, G. Belitsky, N. Dolinnaya, M. Yakubovskaya // Recombination. Keystone Symposia on Molecular Cell Biology, Abstractbook – 2011. – p. 25. 4. Karpechenko, N. CA-microsatellite instability as a factor of branch migration impeding in Holliday junctions / N. Karpechenko, V. Gasanova, N. Dolinnaya, V. Popenko, M. Yakubovskaya // Cancer Research. – 2012. - № 8(Suppl.) – doi:1538-7445.AM2012-2112. 5. Карпеченко, Н.Ю. Визуализация ДНК при гель-электрофорезе флуоресцентным красителем sybr gold по протоколу предокрашивания / Н.Ю. Карпеченко, В.К. Гасанова, Н.В. Ряднинская, Е.А. Лесовая, К.И. Кирсанов, Г.А. Белицкий, М.Г. Якубовская // Вопросы биологической, медицинской и фармацевтической химии. - 2012. - №10. - С. 6973. 6. Карпеченко, Н.Ю. Влияние CA-микросателлитов на гомологичную рекомбинацию / Н.Ю. Карпеченко, В.К. Гасанова, В.И. Попенко, М.Г. Якубовская // Технологии живых систем. – 2013 – № 9. – С. 33-39. 7. Шалгинских, Н.А. Эпигенетические механизмы регуляции экспрессии генов в химическом канцерогенезе / Н.А. Шалгинских, Н.Ю. Карпеченко, А.М. Оглоблина, Е.А. Лесовая, К.И. Кирсанов, Д.С. Набережнов, Г.А. Белицкий, М.Г. Якубовская // Вопросы биологической, медицинской и фармацевтической химии. - 2014. - №3. - С. 46-68. 8. Карпеченко, Н.Ю. Спонтанная олигонуклеотидная инвазия в (CA/TG)n-повторы как основа их функционирования в качестве «горячих» точек рекомбинации / Н.Ю. Карпеченко, В.К. Гасанова, Н.Г. Долинная, Д.С. Набережнов, М.Г. Якубовская // Вопросы биологической, медицинской и фармацевтической химии. – 2014 – № 4. – С. 30-35.